обмен аминокислот.ppt
- Количество слайдов: 42

КАТАБОЛИЗМ АМИНОКИСЛОТ q. Трансаминирование q. Дезаминирование q. Цикл мочевинообразования q. Деградация аминокислот

Неполярные аминокислоты
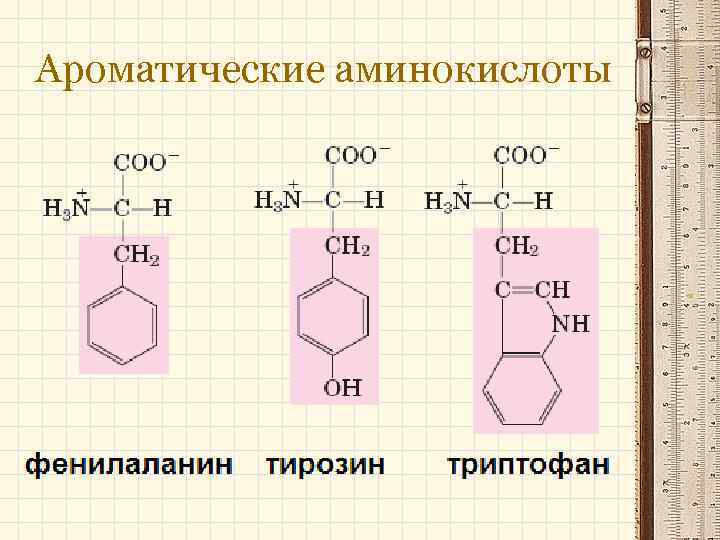
Ароматические аминокислоты
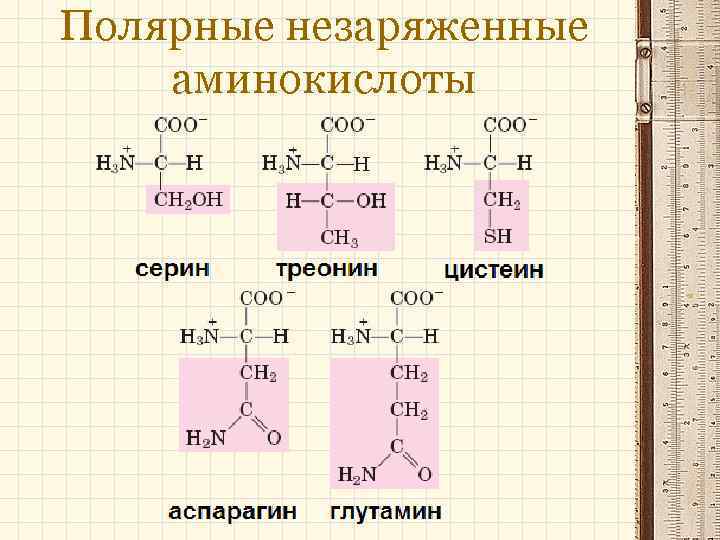
Полярные незаряженные аминокислоты
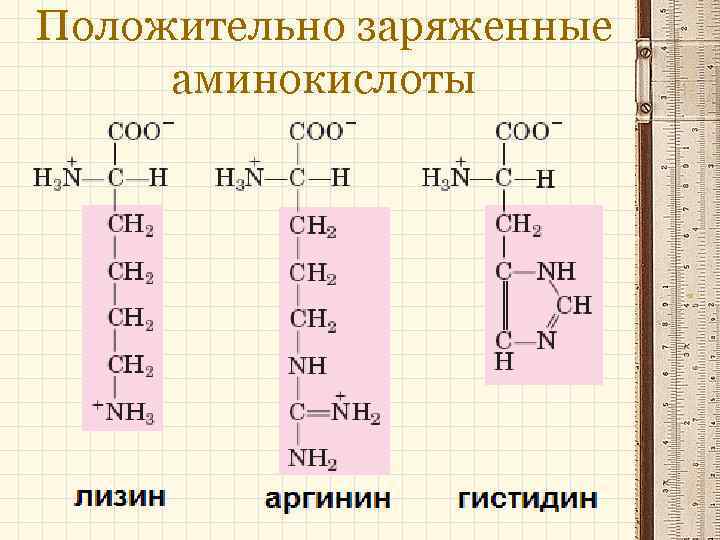
Положительно заряженные аминокислоты
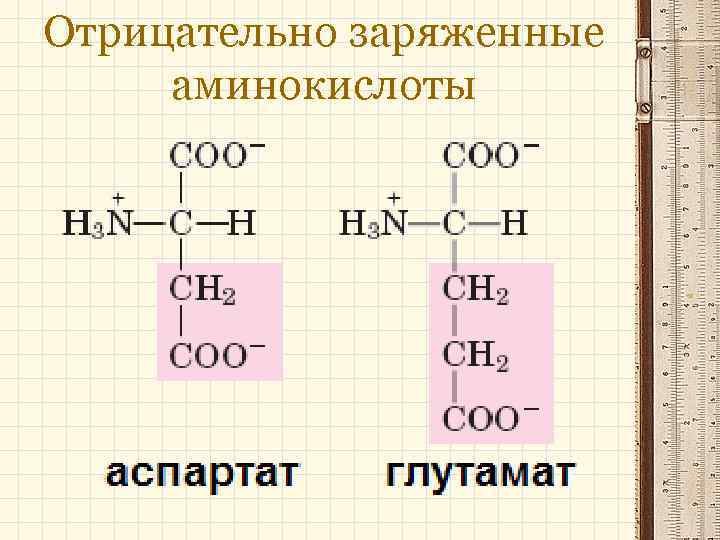
Отрицательно заряженные аминокислоты
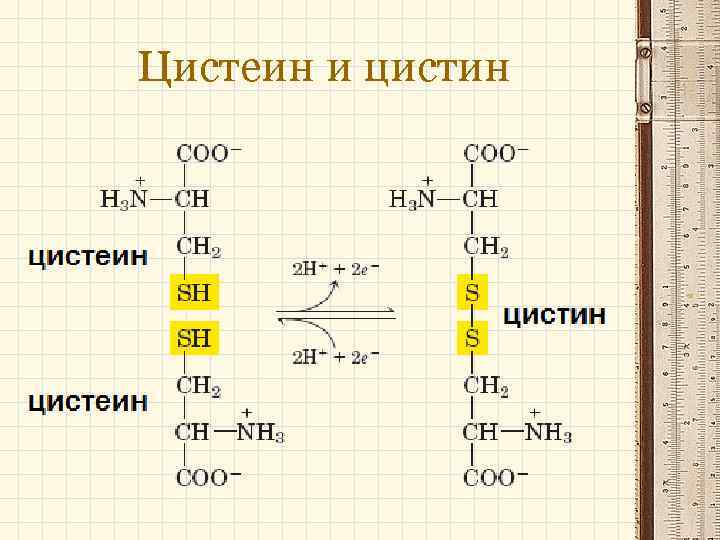
Цистеин и цистин
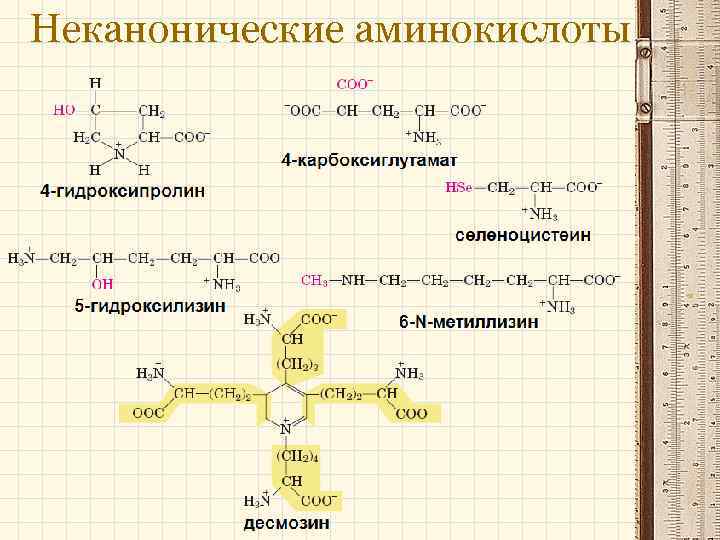
Неканонические аминокислоты
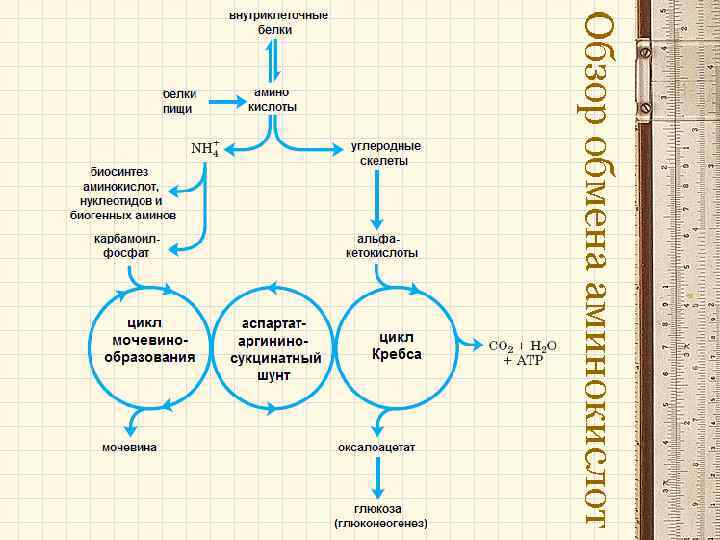
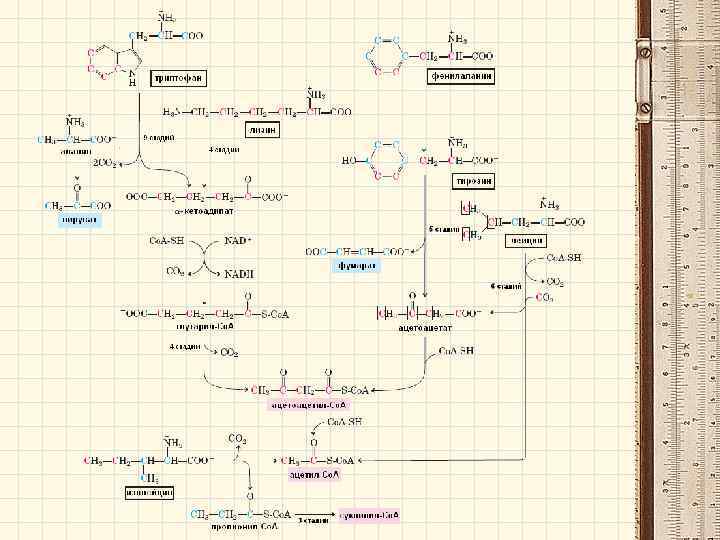
Обзор обмена аминокислот
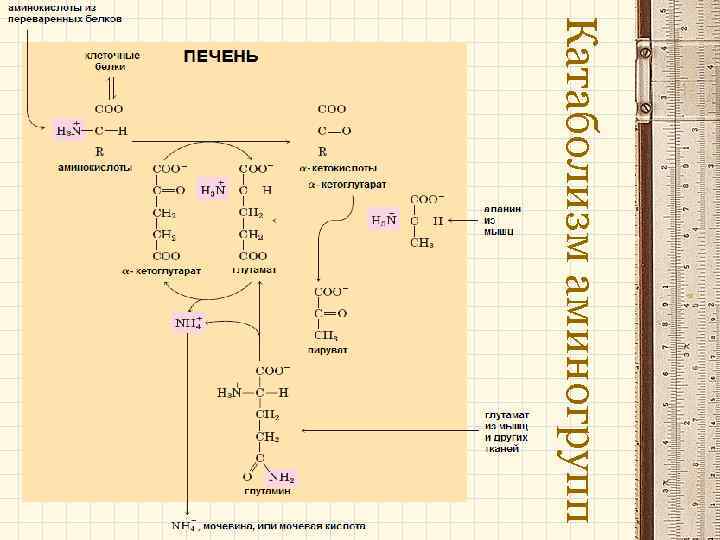
Катаболизм аминогрупп
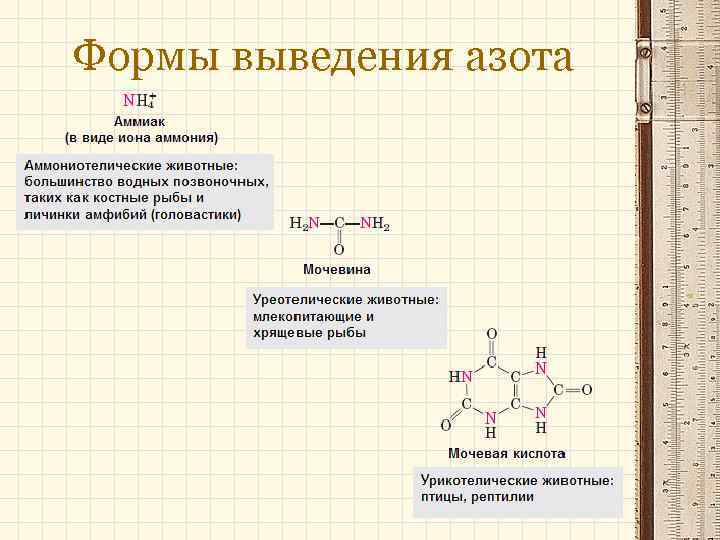
Формы выведения азота
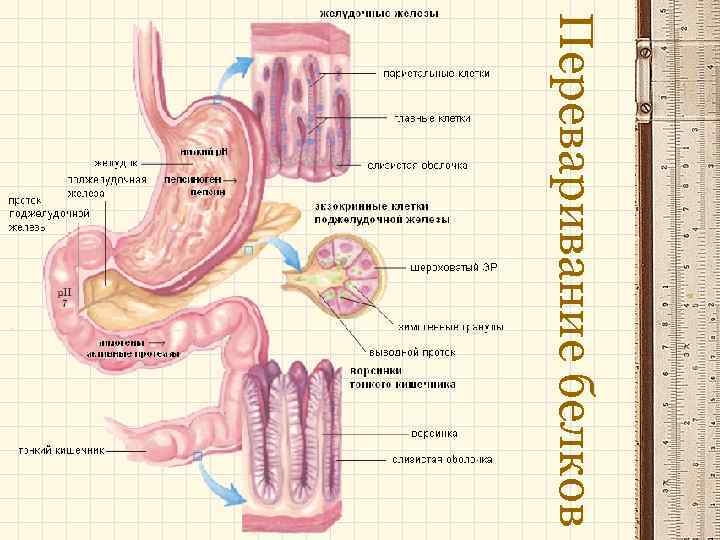
Переваривание белков
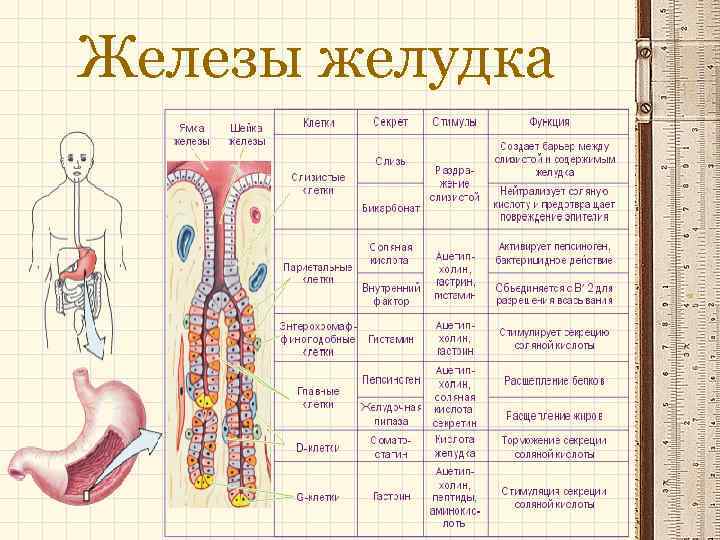
Железы желудка
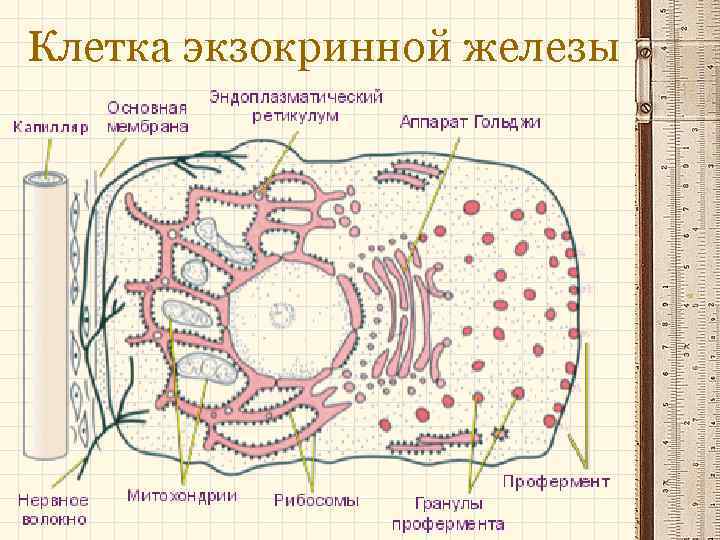
Клетка экзокринной железы
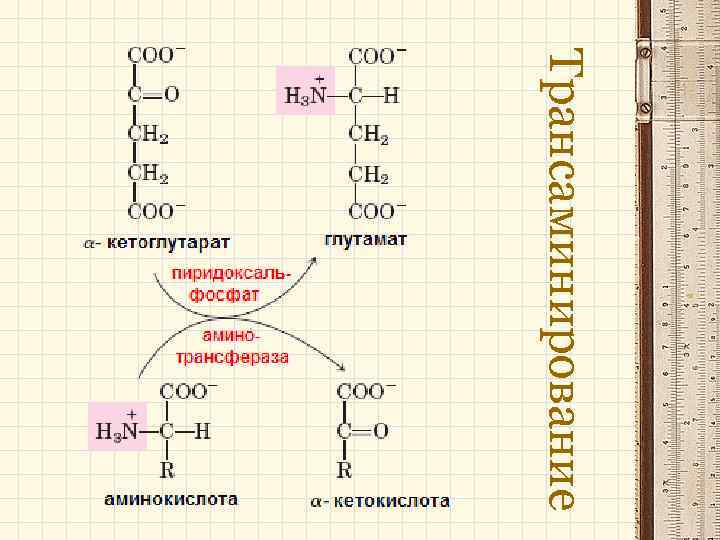
Трансаминирование
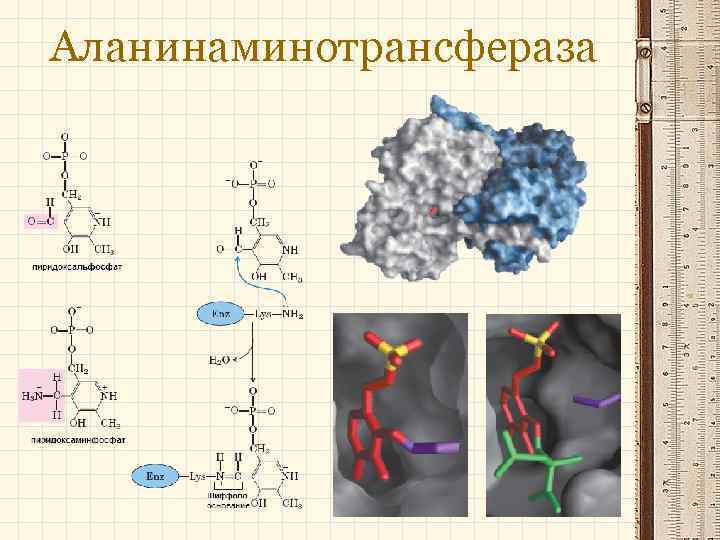
Аланинаминотрансфераза
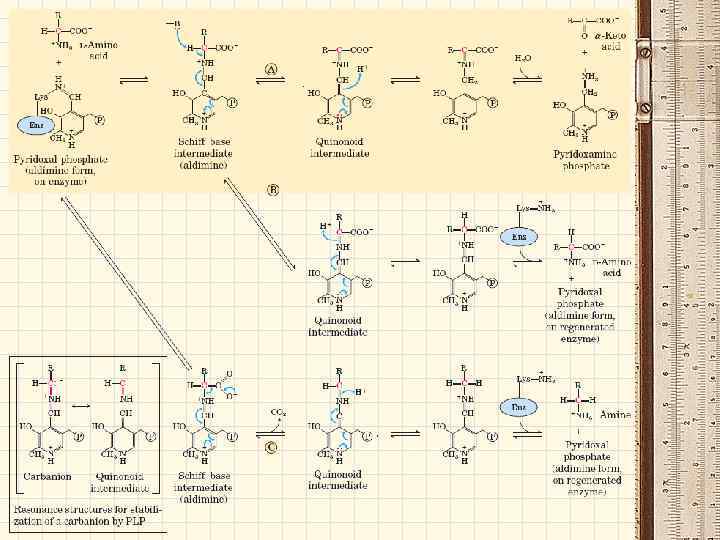
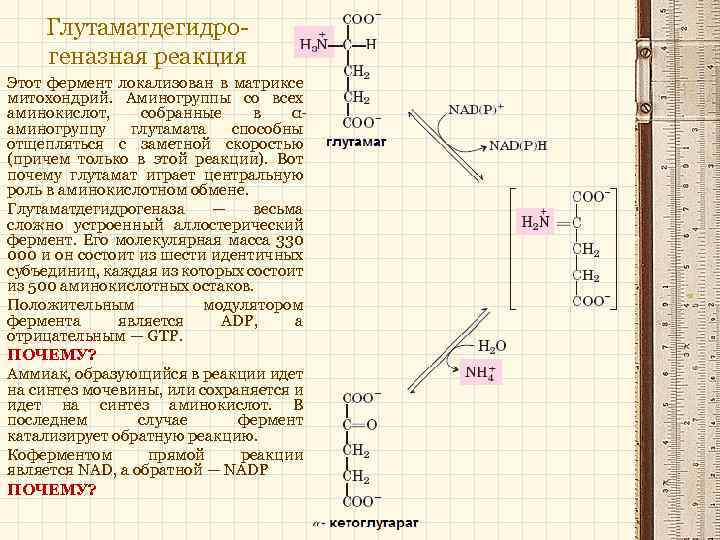
Глутаматдегидрогеназная реакция Этот фермент локализован в матриксе митохондрий. Аминогруппы со всех аминокислот, собранные в αаминогруппу глутамата способны отщепляться с заметной скоростью (причем только в этой реакции). Вот почему глутамат играет центральную роль в аминокислотном обмене. Глутаматдегидрогеназа — весьма сложно устроенный аллостерический фермент. Его молекулярная масса 330 000 и он состоит из шести идентичных субъединиц, каждая из которых состоит из 500 аминокислотных остаков. Положительным модулятором фермента является ADР, а отрицательным — GTP. ПОЧЕМУ? Аммиак, образующийся в реакции идет на синтез мочевины, или сохраняется и идет на синтез аминокислот. В последнем случае фермент катализирует обратную реакцию. Коферментом прямой реакции является NAD, а обратной — NADP ПОЧЕМУ?

Транспорт аммиака с помощью глутамина Образующийся токсичный аммиак должен быть немедленно превращен в нетоксичный метаболит. Происходит это во всех тканях в глутаминсинтетазной реакции. Эта реакция превращения глутамата в глутамин через промежуточный продукт — γ-глутамилфосфат. Образующийся глутамин представляет собой нейтральное нетоксичное соединение, способное легко проъодить через клеточные мембраны; этим он отличается от глутамата, не отличающегося такой способностью, поскольку он несет суммарный отрицательный заряд. У уреотелических животных глутамин доставляется с кровью в основном в печень (в меньшем количестве в кишечник и почки), где происходит глутаминазная реакция с высвобождением аммиака, идущего на синтез мочевины. Глутамин — это та форма, в которой, главным образом, и транспортируется аммиак: в крови людей его содержание во много крат превышает содержание других аминокислот.
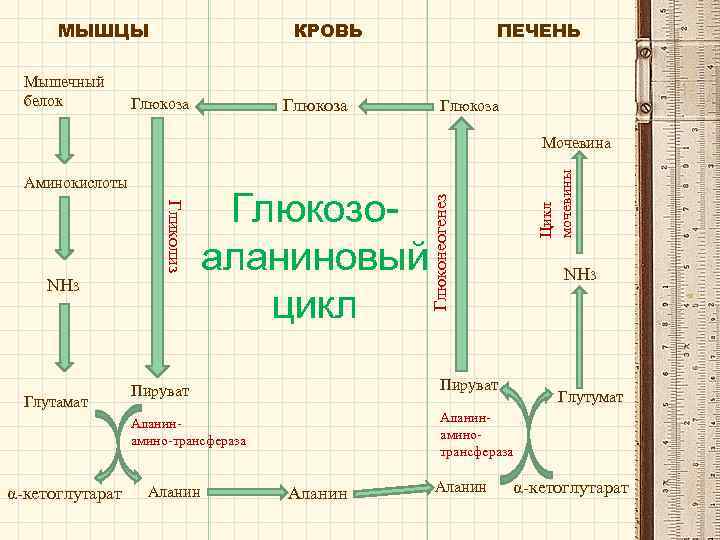
МЫШЦЫ Мышечный белок КРОВЬ Глюкоза ПЕЧЕНЬ Глюкоза Гликолиз NH 3 Глюкозоаланиновый цикл Глюконеогенез Аминокислоты Цикл мочевины Мочевина NH 3 α-кетоглутарат Пируват Аланинамино-трансфераза Глутамат Пируват Аланинаминотрансфераза Аланин Глутумат α-кетоглутарат
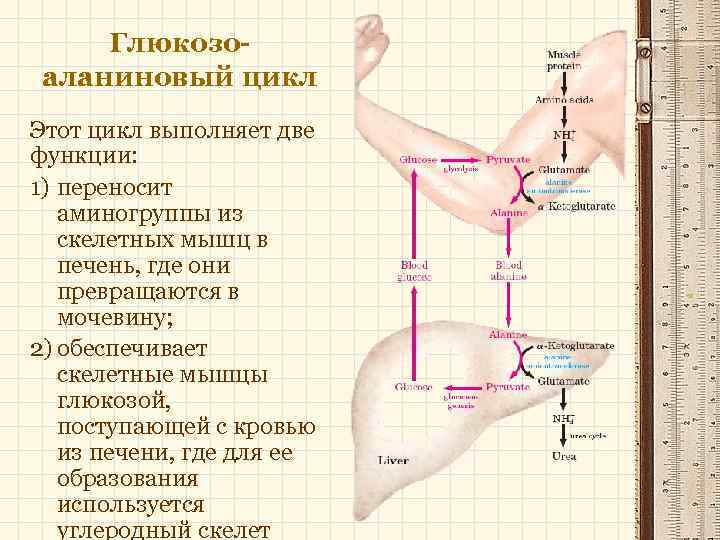
Глюкозоаланиновый цикл Этот цикл выполняет две функции: 1) переносит аминогруппы из скелетных мышц в печень, где они превращаются в мочевину; 2) обеспечивает скелетные мышцы глюкозой, поступающей с кровью из печени, где для ее образования используется углеродный скелет
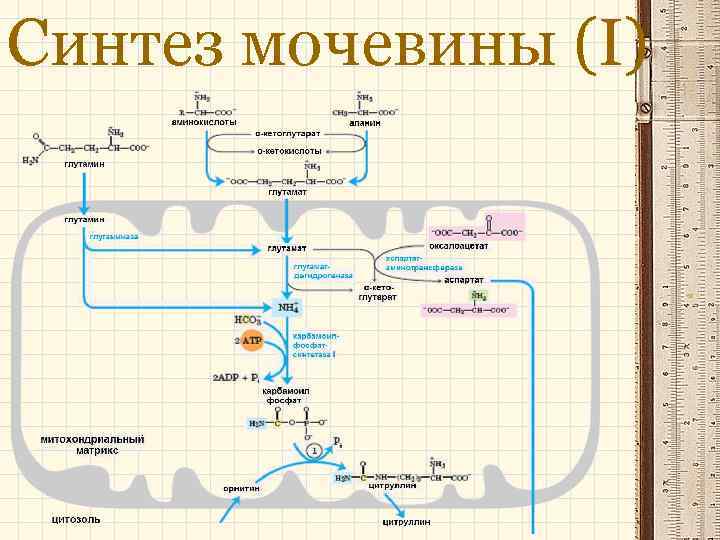
Синтез мочевины (І)
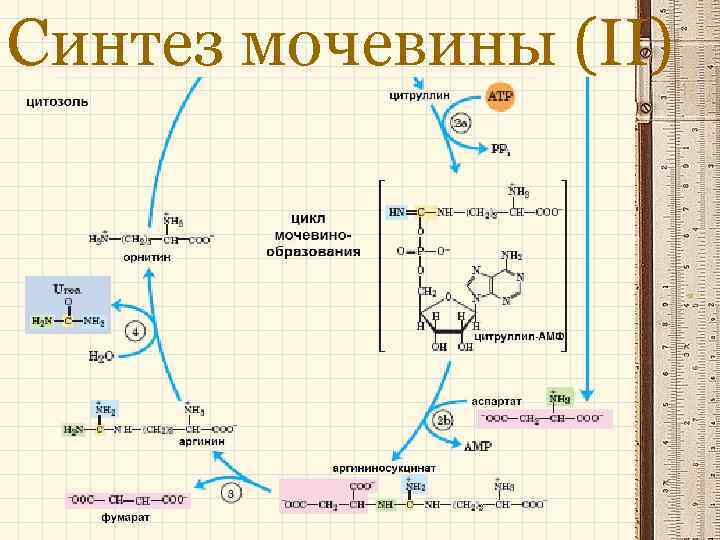
Синтез мочевины (ІІ)
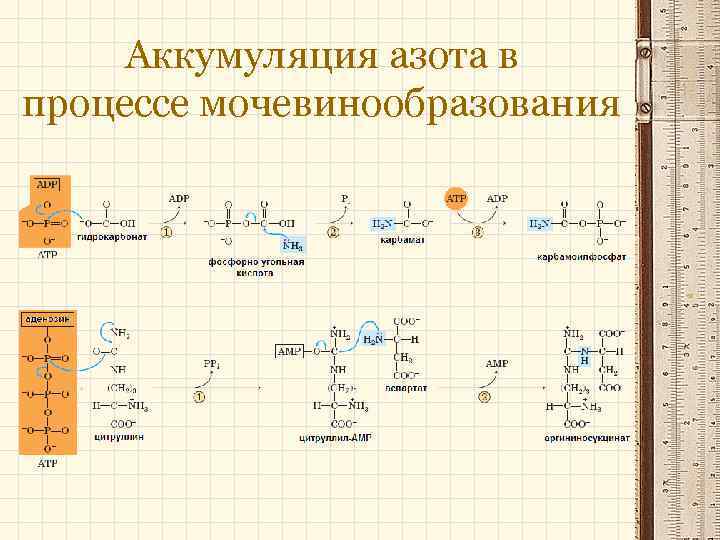
Аккумуляция азота в процессе мочевинообразования
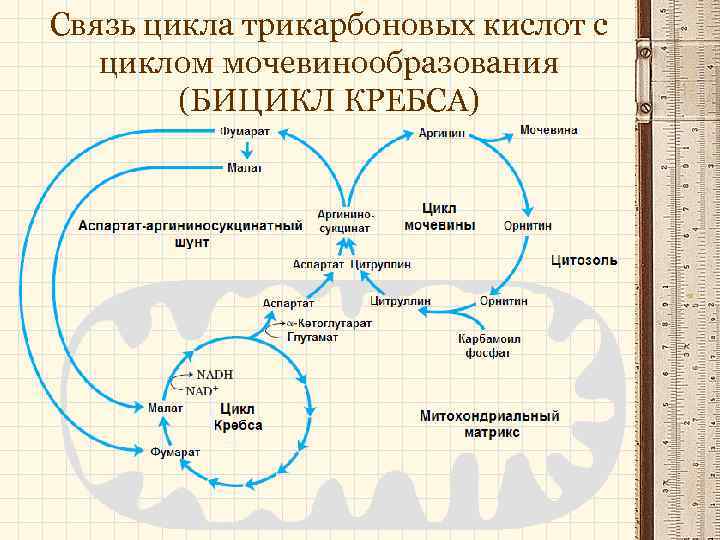
Связь цикла трикарбоновых кислот с циклом мочевинообразования (БИЦИКЛ КРЕБСА)

Регуляция синтеза мочевины Первый фермент цикла мочевинообразования — карбамоил фосфат синтетаза І — аллостерически регулируется Nацетилглутаматом, который синтезируется из ацетил- Cо. A и глутамата N-ацетилглутамат синтазой. У растений и микроорганизмов этот фермент катализирует первый шаг синтеза аргинина dе novo, но у млекопитающих N-ацетилглутамат синтаза в печени выполняет исключительно регуляторную функцию. Концентрация N-ацетилглутамата определяется глутаматом и ацетил-Co. A, а также аргинином — активатором ацетилглутамат синтазы, и, поэтому, активатором цикла мочевины).
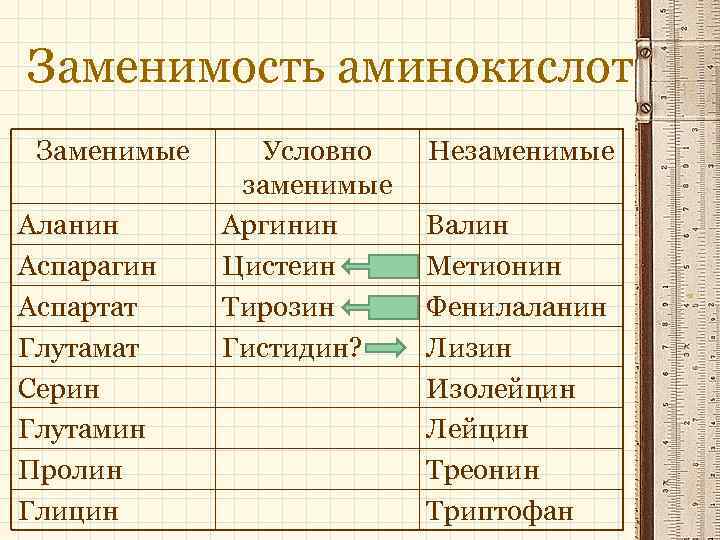
Заменимость аминокислот Заменимые Аланин Аспарагин Аспартат Глутамат Серин Глутамин Пролин Глицин Условно заменимые Аргинин Цистеин Тирозин Гистидин? Незаменимые Валин Метионин Фенилаланин Лизин Изолейцин Лейцин Треонин Триптофан
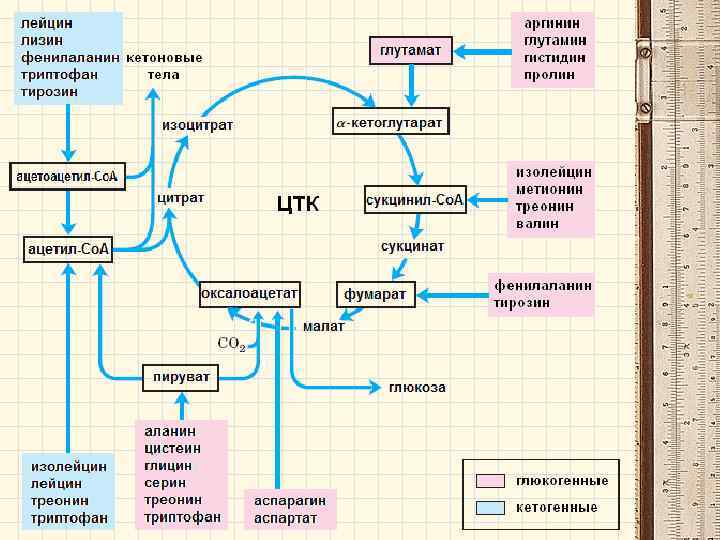
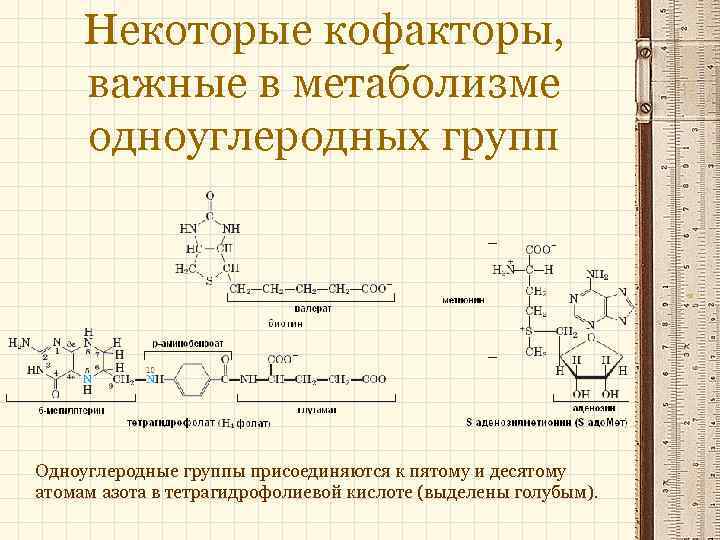
Некоторые кофакторы, важные в метаболизме одноуглеродных групп Одноуглеродные группы присоединяются к пятому и десятому атомам азота в тетрагидрофолиевой кислоте (выделены голубым).
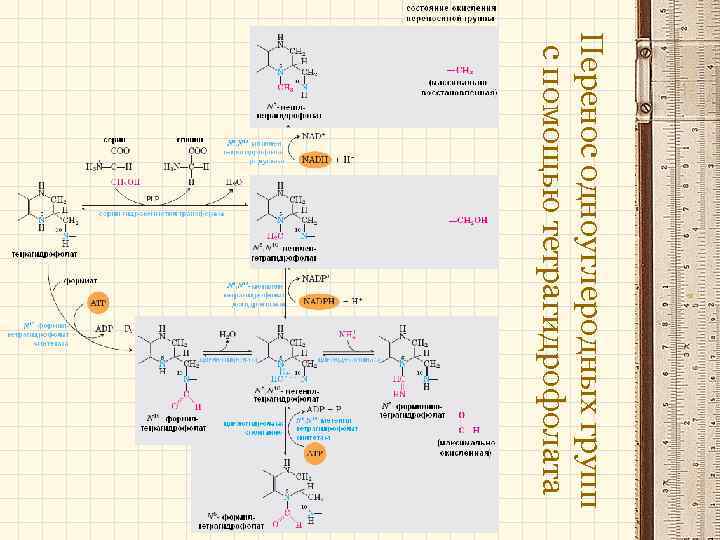
Перенос одноуглеродных групп с помощью тетрагидрофолата
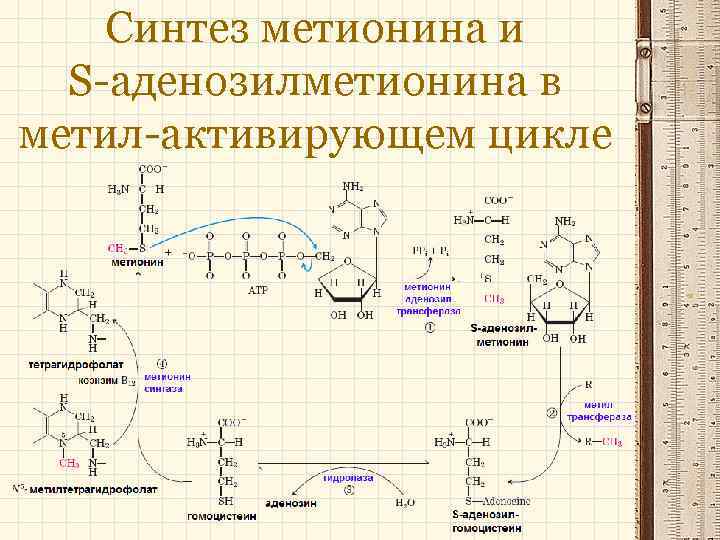
Синтез метионина и S-аденозилметионина в метил-активирующем цикле
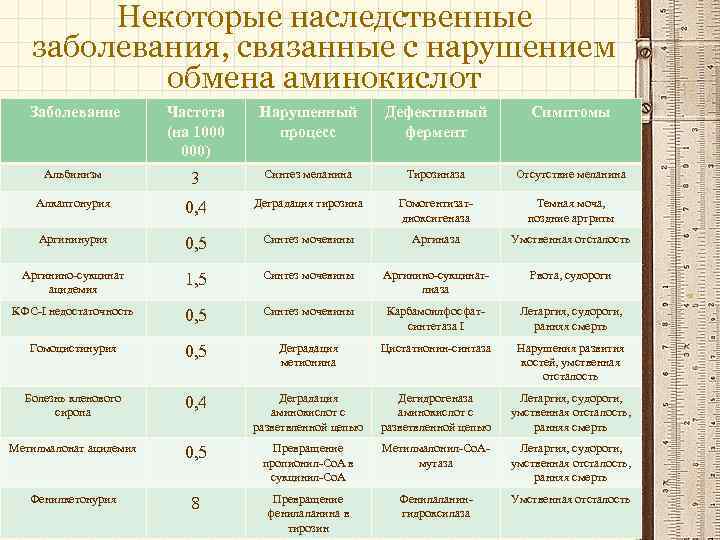
Некоторые наследственные заболевания, связанные с нарушением обмена аминокислот Заболевание Частота (на 1000 000) Нарушенный процесс Дефективный фермент Симптомы Альбинизм 3 Синтез меланина Тирозиназа Отсутствие меланина Алкаптонурия 0, 4 Деградация тирозина Гомогентизатдиоксигеназа Темная моча, поздние артриты Аргининурия 0, 5 Синтез мочевины Аргиназа Умственная отсталость Аргинино-сукцинат ацидемия 1, 5 Синтез мочевины Аргинино-сукцинатлиаза Рвота, судороги КФС-І недостаточность 0, 5 Синтез мочевины Карбамоилфосфатсинтетаза І Летаргия, судороги, ранняя смерть Гомоцистинурия 0, 5 Деградация метионина Цистатионин-синтаза Нарушения развития костей, умственная отсталость Болезнь кленового сиропа 0, 4 Деградация аминокислот с разветвленной цепью Дегидрогеназа аминокислот с разветвленной цепью Летаргия, судороги, умственная отсталость, ранняя смерть Метилмалонат ацидемия 0, 5 Превращение пропионил-Со. А в сукцинил-Со. А Метилмалонил-Со. Амутаза Летаргия, судороги, умственная отсталость, ранняя смерть Фенилкетонурия 8 Превращение фенилаланина в тирозин Фенилаланингидроксилаза Умственная отсталость
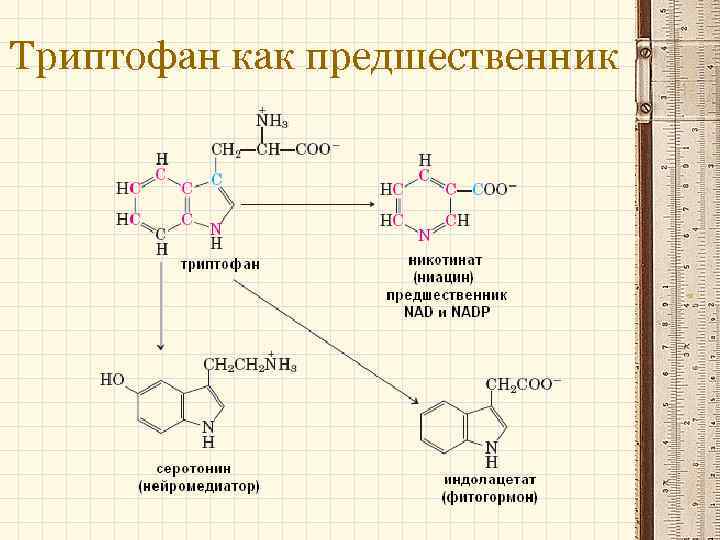
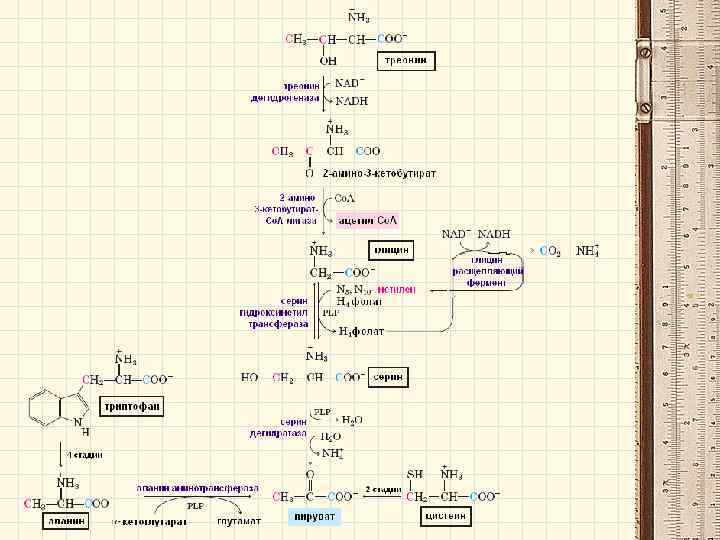
Триптофан как предшественник
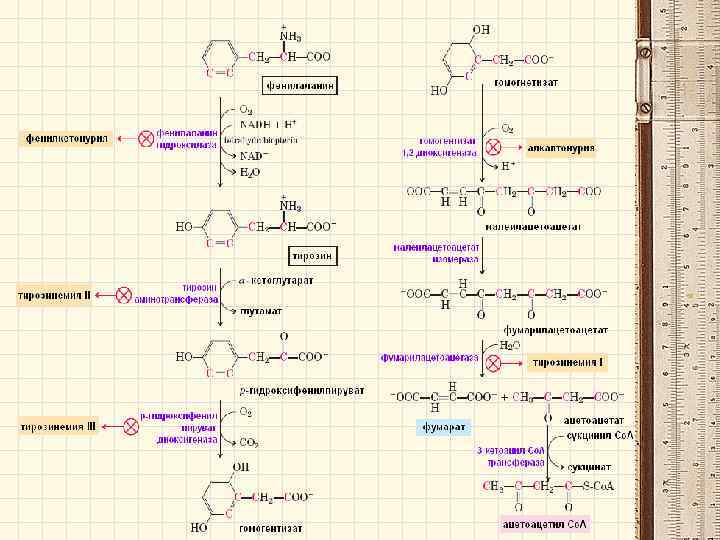
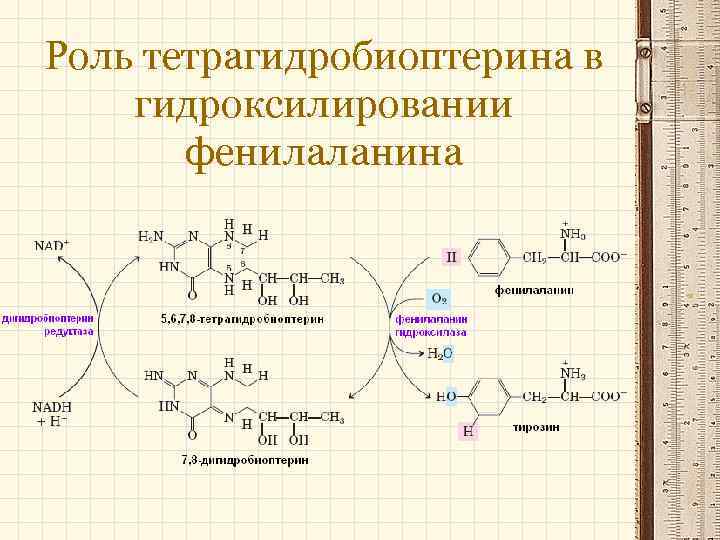
Роль тетрагидробиоптерина в гидроксилировании фенилаланина
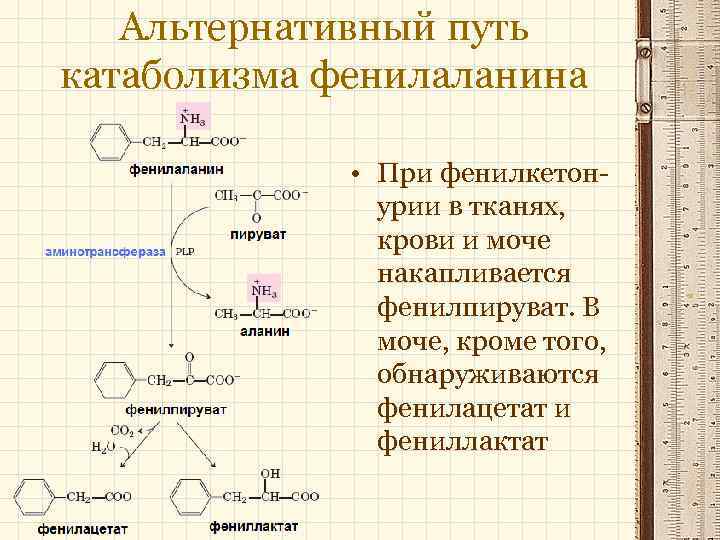
Альтернативный путь катаболизма фенилаланина • При фенилкетонурии в тканях, крови и моче накапливается фенилпируват. В моче, кроме того, обнаруживаются фенилацетат и фениллактат
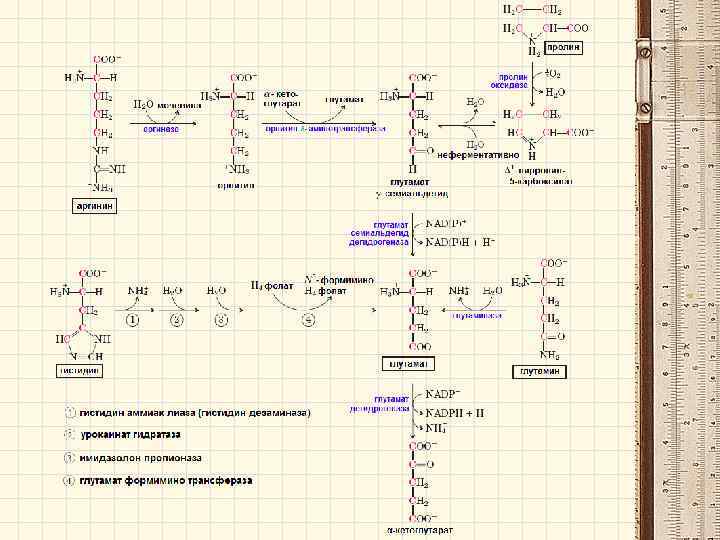
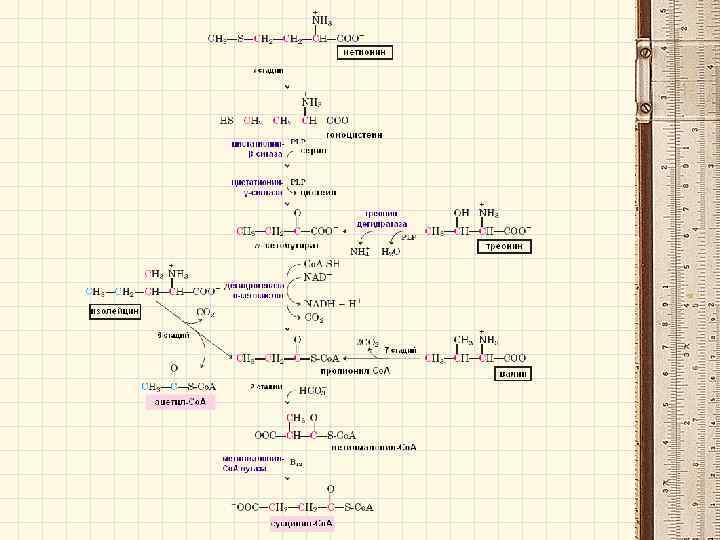
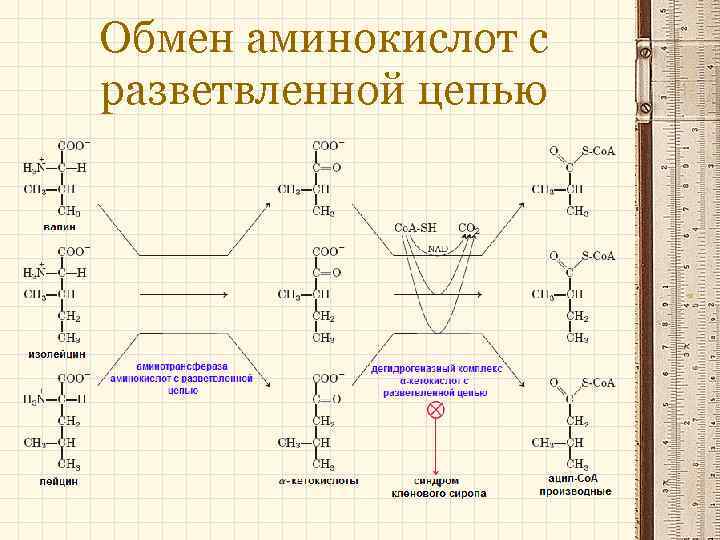
Обмен аминокислот с разветвленной цепью
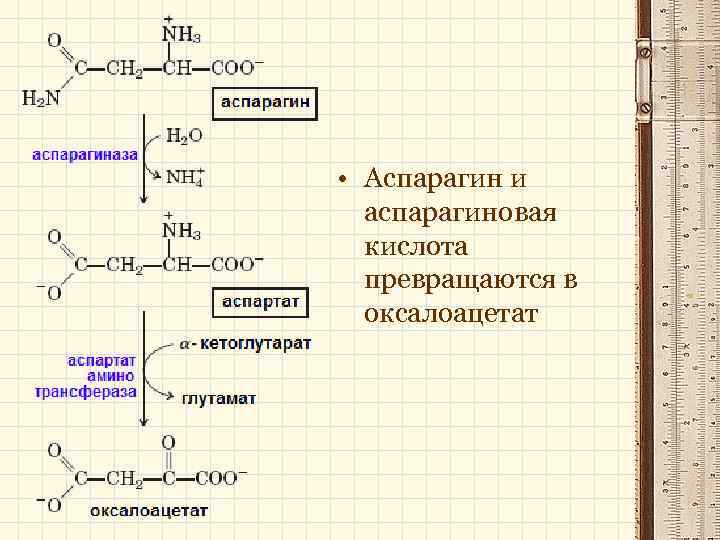
• Аспарагин и аспарагиновая кислота превращаются в оксалоацетат
обмен аминокислот.ppt