d43479cc9f96112088135e7fe1c087cc.ppt
- Количество слайдов: 24
 Картирование ДНК. Программа Геном Человека. Геномная дактилоскопия.
Картирование ДНК. Программа Геном Человека. Геномная дактилоскопия.
 Картирование генов – определение положения данного гена на какой-либо хромосоме относительно других генов. Используют три основные группы методов картирования генов : ►физическое (определение с помощью рестрикционных карт, электронной микроскопии и некоторых вариантов электрофореза межгенных расстояний – в нуклеотидах), ►генетическое (определение частот рекомбинаций между генами, в частности, в семейном анализе и др. ), ►цитогенетическое (гибридизации in situ, получение монохромосомных клеточных гибридов, делеционный метод и др. )
Картирование генов – определение положения данного гена на какой-либо хромосоме относительно других генов. Используют три основные группы методов картирования генов : ►физическое (определение с помощью рестрикционных карт, электронной микроскопии и некоторых вариантов электрофореза межгенных расстояний – в нуклеотидах), ►генетическое (определение частот рекомбинаций между генами, в частности, в семейном анализе и др. ), ►цитогенетическое (гибридизации in situ, получение монохромосомных клеточных гибридов, делеционный метод и др. )
 Геном человека Геном - вся совокупность генетического материала l 23 пары хромосом и мт. ДНК l все гены и межгенные участки l ~ 3 млрд пар нуклеотидов
Геном человека Геном - вся совокупность генетического материала l 23 пары хромосом и мт. ДНК l все гены и межгенные участки l ~ 3 млрд пар нуклеотидов
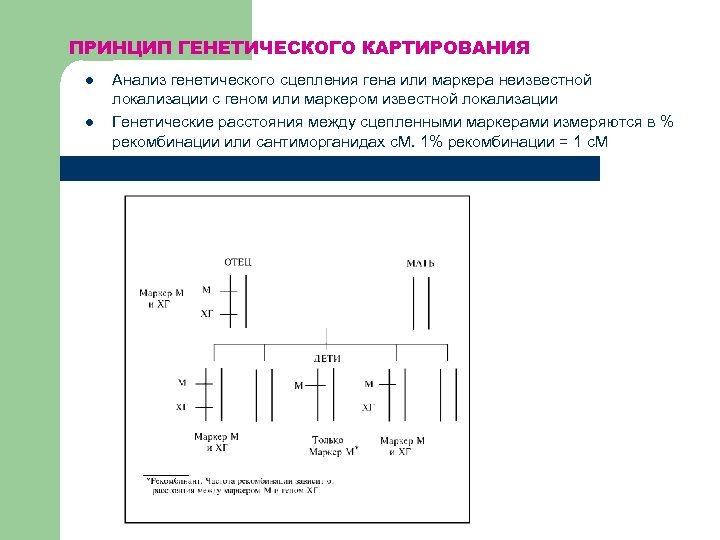 ПРИНЦИП ГЕНЕТИЧЕСКОГО КАРТИРОВАНИЯ l l Анализ генетического сцепления гена или маркера неизвестной локализации с геном или маркером известной локализации Генетические расстояния между сцепленными маркерами измеряются в % рекомбинации или сантиморганидах c. М. 1% рекомбинации = 1 с. М
ПРИНЦИП ГЕНЕТИЧЕСКОГО КАРТИРОВАНИЯ l l Анализ генетического сцепления гена или маркера неизвестной локализации с геном или маркером известной локализации Генетические расстояния между сцепленными маркерами измеряются в % рекомбинации или сантиморганидах c. М. 1% рекомбинации = 1 с. М
 Программа ГЕНОМ ЧЕЛОВЕКА l Проект по расшифровке генома человека The Human Genome Project, HGP Международный научноисследовательский проект, главной целью которого было определить последовательность нуклеотидов, которые составляют ДНК и идентифицировать 20, 000 -25, 000 генов в человеческом геноме. Проект начался в 1990 году, под руководством Джеймса Уотсона под эгидой Национальной организации здравоохранения США
Программа ГЕНОМ ЧЕЛОВЕКА l Проект по расшифровке генома человека The Human Genome Project, HGP Международный научноисследовательский проект, главной целью которого было определить последовательность нуклеотидов, которые составляют ДНК и идентифицировать 20, 000 -25, 000 генов в человеческом геноме. Проект начался в 1990 году, под руководством Джеймса Уотсона под эгидой Национальной организации здравоохранения США
 Цель проекта заключается в выяснении последовательности оснований во всех молекулах ДНК в клетках человека. Одновременно должна быть установлена локализация всех генов, что помогло бы выяснить причины наследственных заболеваний и этим открыть пути к их лечению. l Чтобы последовательно приближаться к решению проблемы картирования генов человека, было сформулировано пять основных целей: 1) завершить составление детальной генетической карты, на которой были бы помечены гены, отстоящие друг от друга на расстоянии, не превышающем в среднем 2 млн оснований (1 млн оснований принято называть 1 мегабаза, сокращенно Мб, от англ. слова base - основание); 2) составить физические карты каждой хромосомы (разрешение 0, 1 Мб); 3) получить карту всего генома в виде охарактеризованных по отдельности клонов (5 тыс. оснований в клоне, или 5 килобаз, Кб); 4) завершить к 2004 году полное секвенирование ДНК (разрешение 1 основание) и 5) нанести на полностью завершенную секвенсовую карту все гены человека (к 2005 году). Ожидалось, что, когда все указанные цели будут достигнуты, исследователи определят все функции генов и разработают методы биологического и медицинского применения полученных данных.
Цель проекта заключается в выяснении последовательности оснований во всех молекулах ДНК в клетках человека. Одновременно должна быть установлена локализация всех генов, что помогло бы выяснить причины наследственных заболеваний и этим открыть пути к их лечению. l Чтобы последовательно приближаться к решению проблемы картирования генов человека, было сформулировано пять основных целей: 1) завершить составление детальной генетической карты, на которой были бы помечены гены, отстоящие друг от друга на расстоянии, не превышающем в среднем 2 млн оснований (1 млн оснований принято называть 1 мегабаза, сокращенно Мб, от англ. слова base - основание); 2) составить физические карты каждой хромосомы (разрешение 0, 1 Мб); 3) получить карту всего генома в виде охарактеризованных по отдельности клонов (5 тыс. оснований в клоне, или 5 килобаз, Кб); 4) завершить к 2004 году полное секвенирование ДНК (разрешение 1 основание) и 5) нанести на полностью завершенную секвенсовую карту все гены человека (к 2005 году). Ожидалось, что, когда все указанные цели будут достигнуты, исследователи определят все функции генов и разработают методы биологического и медицинского применения полученных данных.
 РЕЗУЛЬТАТЫ: l l Расшифрованные геномы. 1995 г. - бактерия Hemophilus influenza; . 1996 г. - клетка дрожжей (6 тыс. генов, 12, 5 Мб); 1998 г. - круглый червь Caenorhabditis elegans (19 тыс. генов, 97 Мб).
РЕЗУЛЬТАТЫ: l l Расшифрованные геномы. 1995 г. - бактерия Hemophilus influenza; . 1996 г. - клетка дрожжей (6 тыс. генов, 12, 5 Мб); 1998 г. - круглый червь Caenorhabditis elegans (19 тыс. генов, 97 Мб).
 РЕЗУЛЬТАТЫ: l Изученные гены человека. За 1995 г. длина участков ДНК человека с установленной последовательностью оснований увеличилась почти в 10 раз. Но хотя прогресс был налицо, результат за год составил менее 0, 001% от того, что предстояло сделать. Но уже к июлю 1998 г. было расшифровано почти 9% генома, а затем каждый месяц появлялись новые значительные результаты. Изучив большое число копий генов в виде с. ДНК и сопоставив их последовательности с участками хромосомной ДНК, к ноябрю 1998 г. расшифровали 30 261 ген (примерно половина генома).
РЕЗУЛЬТАТЫ: l Изученные гены человека. За 1995 г. длина участков ДНК человека с установленной последовательностью оснований увеличилась почти в 10 раз. Но хотя прогресс был налицо, результат за год составил менее 0, 001% от того, что предстояло сделать. Но уже к июлю 1998 г. было расшифровано почти 9% генома, а затем каждый месяц появлялись новые значительные результаты. Изучив большое число копий генов в виде с. ДНК и сопоставив их последовательности с участками хромосомной ДНК, к ноябрю 1998 г. расшифровали 30 261 ген (примерно половина генома).
 ГЕНОМНАЯ ДАКТИЛОСКОПИЯ l Представляет собой метод, используемый в судебно-медицинской экспертизе для идентификации лиц на основе уникальности последовательностей ДНК индивидуума. Метод был открыт в 1984 году британским генетиком Алеком Джеффризом (Alec John Jeffreys).
ГЕНОМНАЯ ДАКТИЛОСКОПИЯ l Представляет собой метод, используемый в судебно-медицинской экспертизе для идентификации лиц на основе уникальности последовательностей ДНК индивидуума. Метод был открыт в 1984 году британским генетиком Алеком Джеффризом (Alec John Jeffreys).
 Повреждения генов и наследственные болезни. Из 10 тыс. известных заболеваний человека около 3 тыс. наследственные болезни. Они необязательно наследуются (передаются потомкам). Просто вызваны они нарушениями наследственного аппарата, то есть генов (в том числе в соматических клетках, а не только в половых). Выявление молекулярных причин "поломки" генов важнейший результат проекта. Число изученных болезнетворных генов быстро растет, и через 3 -4 года мы познаем все 3 тыс. генов, ответственных за те или иные патологии. Это поможет разобраться в генетических программах развития и функционирования человеческого организма, в частности, понять причины рака и старения. Знание молекулярных основ заболеваний поможет их ранней диагностике, а значит, и более успешному лечению. Адресное снабжение лекарствами пораженных клеток, замена больных генов здоровыми, управление обменом веществ и многие другие мечты фантастов на наших глазах превращаются в реальные методы современной медицины.
Повреждения генов и наследственные болезни. Из 10 тыс. известных заболеваний человека около 3 тыс. наследственные болезни. Они необязательно наследуются (передаются потомкам). Просто вызваны они нарушениями наследственного аппарата, то есть генов (в том числе в соматических клетках, а не только в половых). Выявление молекулярных причин "поломки" генов важнейший результат проекта. Число изученных болезнетворных генов быстро растет, и через 3 -4 года мы познаем все 3 тыс. генов, ответственных за те или иные патологии. Это поможет разобраться в генетических программах развития и функционирования человеческого организма, в частности, понять причины рака и старения. Знание молекулярных основ заболеваний поможет их ранней диагностике, а значит, и более успешному лечению. Адресное снабжение лекарствами пораженных клеток, замена больных генов здоровыми, управление обменом веществ и многие другие мечты фантастов на наших глазах превращаются в реальные методы современной медицины.
 Общие принципы геномной дактилоскопии l Методы молекулярной генетики, несмотря на свою сложность, нашли широкое применение в судебно-медицинских исследования. Объясняется это их высочайшей точностью и возможностью работать с минимальным количеством образца. Наиболее востребованным из таких современных методов является геномная дактилоскопия. Ее задача сводится к получению индивидуальных генетических профилей исследуемых лиц для их дальнейшего сравнения. l l На первом этапе необходимо получить очищенную ДНК из доступных исследователю образцов. А их спектр довольно широк: это может быть и кровь, и волосы, и жевательная резинка, и окурок сигареты, т. е. практически любые объекты, с которыми контактировал человек. Далее необходимо оценить количество полученной ДНК, это делают с помощью метода ПЦР в реальном времени, который кроме количества позволяет определить пригодность образца для использования в полимеразной цепной реакции. На следующей стадии проводят специфичную амплификацию (наработку необходимого количества копий) вариабельных участков генома – STR-локусов, которые отличаются у разных людей только количеством единиц повтора, т. е. длиной последовательности. ПЦР проводят с праймеров, несущих флюоресцентную метку, что позволяет легко детектировать продукты амплификации. Заключительным этапом является электрофоретический анализ, который позволяет определить генотипы тестируемых лиц по длине продуктов амплификации STR-локусов. Полученные генетические профили анализируют и в зависимости от задач исследования делают вывод о наличии биологического родства или принадлежности образцов тому или иному человека.
Общие принципы геномной дактилоскопии l Методы молекулярной генетики, несмотря на свою сложность, нашли широкое применение в судебно-медицинских исследования. Объясняется это их высочайшей точностью и возможностью работать с минимальным количеством образца. Наиболее востребованным из таких современных методов является геномная дактилоскопия. Ее задача сводится к получению индивидуальных генетических профилей исследуемых лиц для их дальнейшего сравнения. l l На первом этапе необходимо получить очищенную ДНК из доступных исследователю образцов. А их спектр довольно широк: это может быть и кровь, и волосы, и жевательная резинка, и окурок сигареты, т. е. практически любые объекты, с которыми контактировал человек. Далее необходимо оценить количество полученной ДНК, это делают с помощью метода ПЦР в реальном времени, который кроме количества позволяет определить пригодность образца для использования в полимеразной цепной реакции. На следующей стадии проводят специфичную амплификацию (наработку необходимого количества копий) вариабельных участков генома – STR-локусов, которые отличаются у разных людей только количеством единиц повтора, т. е. длиной последовательности. ПЦР проводят с праймеров, несущих флюоресцентную метку, что позволяет легко детектировать продукты амплификации. Заключительным этапом является электрофоретический анализ, который позволяет определить генотипы тестируемых лиц по длине продуктов амплификации STR-локусов. Полученные генетические профили анализируют и в зависимости от задач исследования делают вывод о наличии биологического родства или принадлежности образцов тому или иному человека.
 l «Геномный оттиск» ДНК человека В качестве гибридизационной пробы для анализа рестриктазного гидролизата суммарной геномной ДНК человека использовался радиоактивный меченный молекулярный зонд 33. 15 Джеффриса.
l «Геномный оттиск» ДНК человека В качестве гибридизационной пробы для анализа рестриктазного гидролизата суммарной геномной ДНК человека использовался радиоактивный меченный молекулярный зонд 33. 15 Джеффриса.
 Молекулярно-генетический идентификационный анализ позволяет исследовать особые участки ДНК, строго специфичные для каждого индивидуума, и получить, таким образом, уникальный генетический «паспорт» или «удостоверение личности» человека, которое нельзя ни скрыть, ни изменить, ни подделать. Индивидуализирующие признаки, определяемые на уровне ДНК, характеризуются почти абсолютной устойчивостью, то есть сохраняются в организме человека неизменными всю его жизнь и неизменными отображаются в его биологических следах. Поэтому идентификационная значимость генетических признаков чрезвычайно высока.
Молекулярно-генетический идентификационный анализ позволяет исследовать особые участки ДНК, строго специфичные для каждого индивидуума, и получить, таким образом, уникальный генетический «паспорт» или «удостоверение личности» человека, которое нельзя ни скрыть, ни изменить, ни подделать. Индивидуализирующие признаки, определяемые на уровне ДНК, характеризуются почти абсолютной устойчивостью, то есть сохраняются в организме человека неизменными всю его жизнь и неизменными отображаются в его биологических следах. Поэтому идентификационная значимость генетических признаков чрезвычайно высока.
 Технологии молекулярно-генетической индивидуализации: l В судебно-экспертной практике базовыми молекулярно-генетическими технологиями признаны: анализ полиморфизма (вариабельности) длины рестриктазных фрагментов ДНК, анализ полиморфизма длины амплифицированных фрагментов ДНК и анализ полиморфизма нуклеотидных последовательностей (сайт-полиморфизма) ДНК.
Технологии молекулярно-генетической индивидуализации: l В судебно-экспертной практике базовыми молекулярно-генетическими технологиями признаны: анализ полиморфизма (вариабельности) длины рестриктазных фрагментов ДНК, анализ полиморфизма длины амплифицированных фрагментов ДНК и анализ полиморфизма нуклеотидных последовательностей (сайт-полиморфизма) ДНК.
 Анализ полиморфизма длины рестриктазных фрагментов ДНК
Анализ полиморфизма длины рестриктазных фрагментов ДНК
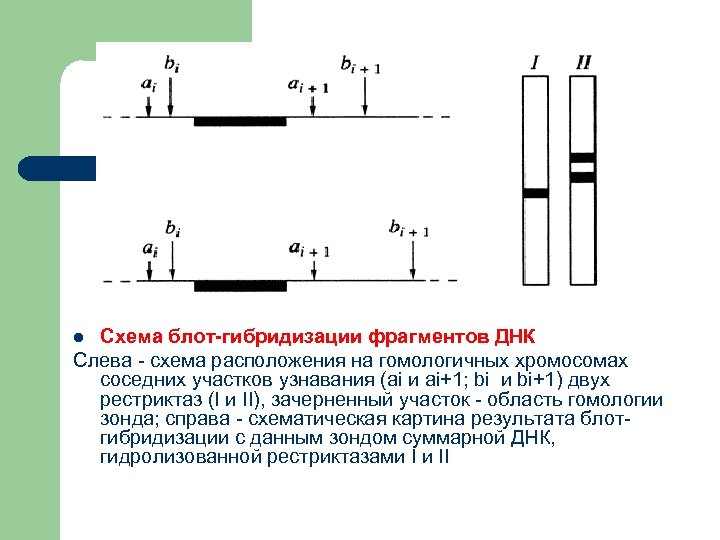 Схема блот-гибридизации фрагментов ДНК Слева - схема расположения на гомологичных хромосомах соседних участков узнавания (ai и ai+1; bi и bi+1) двух рестриктаз (I и II), зачерненный участок - область гомологии зонда; справа - схематическая картина результата блотгибридизации с данным зондом суммарной ДНК, гидролизованной рестриктазами I и II l
Схема блот-гибридизации фрагментов ДНК Слева - схема расположения на гомологичных хромосомах соседних участков узнавания (ai и ai+1; bi и bi+1) двух рестриктаз (I и II), зачерненный участок - область гомологии зонда; справа - схематическая картина результата блотгибридизации с данным зондом суммарной ДНК, гидролизованной рестриктазами I и II l
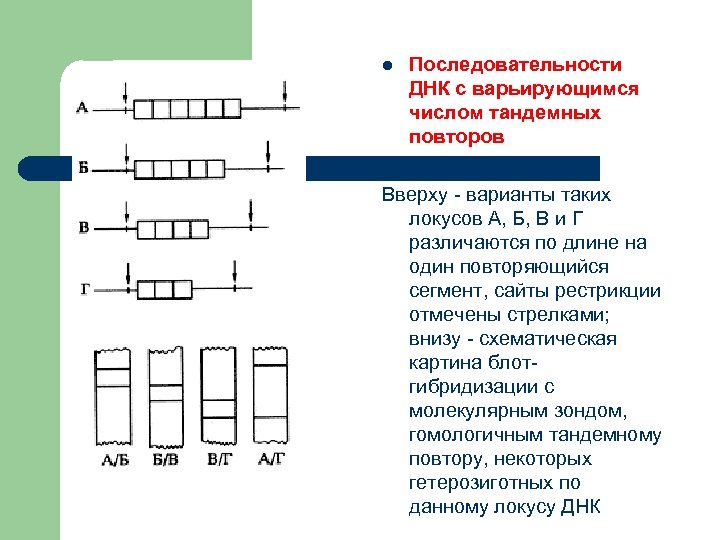 l Последовательности ДНК с варьирующимся числом тандемных повторов Вверху - варианты таких локусов А, Б, В и Г различаются по длине на один повторяющийся сегмент, сайты рестрикции отмечены стрелками; внизу - схематическая картина блотгибридизации с молекулярным зондом, гомологичным тандемному повтору, некоторых гетерозиготных по данному локусу ДНК
l Последовательности ДНК с варьирующимся числом тандемных повторов Вверху - варианты таких локусов А, Б, В и Г различаются по длине на один повторяющийся сегмент, сайты рестрикции отмечены стрелками; внизу - схематическая картина блотгибридизации с молекулярным зондом, гомологичным тандемному повтору, некоторых гетерозиготных по данному локусу ДНК
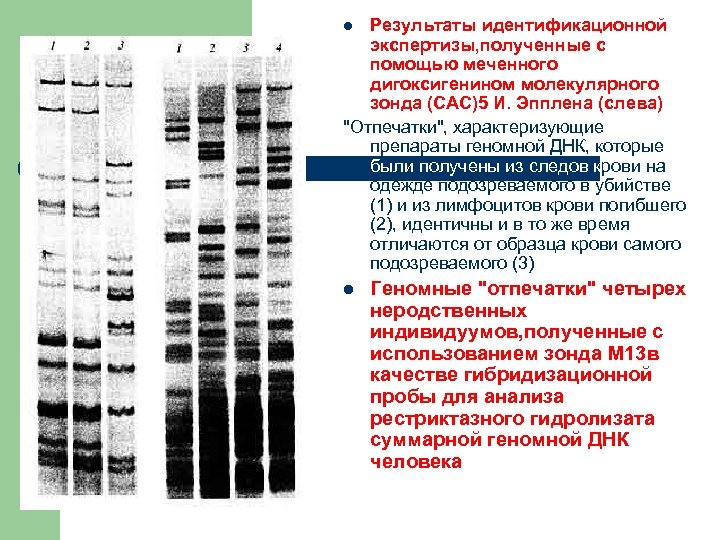 Результаты идентификационной экспертизы, полученные с помощью меченного дигоксигенином молекулярного зонда (САС)5 И. Эпплена (слева) "Отпечатки", характеризующие препараты геномной ДНК, которые были получены из следов крови на одежде подозреваемого в убийстве (1) и из лимфоцитов крови погибшего (2), идентичны и в то же время отличаются от образца крови самого подозреваемого (3) l l Геномные "отпечатки" четырех неродственных индивидуумов, полученные с использованием зонда М 13 в качестве гибридизационной пробы для анализа рестриктазного гидролизата суммарной геномной ДНК человека
Результаты идентификационной экспертизы, полученные с помощью меченного дигоксигенином молекулярного зонда (САС)5 И. Эпплена (слева) "Отпечатки", характеризующие препараты геномной ДНК, которые были получены из следов крови на одежде подозреваемого в убийстве (1) и из лимфоцитов крови погибшего (2), идентичны и в то же время отличаются от образца крови самого подозреваемого (3) l l Геномные "отпечатки" четырех неродственных индивидуумов, полученные с использованием зонда М 13 в качестве гибридизационной пробы для анализа рестриктазного гидролизата суммарной геномной ДНК человека
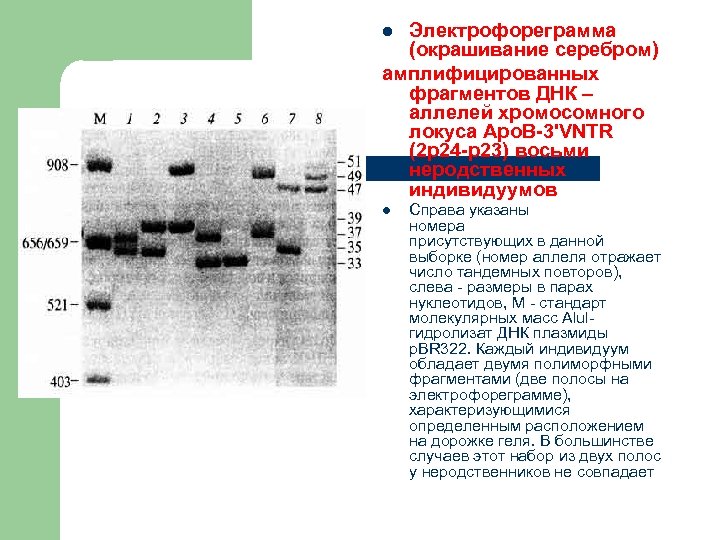 Электрофореграмма (окрашивание серебром) амплифицированных фрагментов ДНК – аллелей хромосомного локуса Apo. B-3'VNTR (2 р24 -р23) восьми неродственных индивидуумов l l Справа указаны номерааллельных вариантов, присутствующих в данной выборке (номер аллеля отражает число тандемных повторов), слева - размеры в парах нуклеотидов, М - стандарт молекулярных масс Alulгидролизат ДНК плазмиды p. BR 322. Каждый индивидуум обладает двумя полиморфными фрагментами (две полосы на электрофореграмме), характеризующимися определенным расположением на дорожке геля. В большинстве случаев этот набор из двух полос у неродственников не совпадает
Электрофореграмма (окрашивание серебром) амплифицированных фрагментов ДНК – аллелей хромосомного локуса Apo. B-3'VNTR (2 р24 -р23) восьми неродственных индивидуумов l l Справа указаны номерааллельных вариантов, присутствующих в данной выборке (номер аллеля отражает число тандемных повторов), слева - размеры в парах нуклеотидов, М - стандарт молекулярных масс Alulгидролизат ДНК плазмиды p. BR 322. Каждый индивидуум обладает двумя полиморфными фрагментами (две полосы на электрофореграмме), характеризующимися определенным расположением на дорожке геля. В большинстве случаев этот набор из двух полос у неродственников не совпадает
 l Анализ полиморфизма нуклеотидных последовательностей ДНК
l Анализ полиморфизма нуклеотидных последовательностей ДНК
 Карта митохондриального генома человека Отмечены гены, локализованные на митохондриальной ДНК, и сайты инициации транскрипции (РL и PH) и репликации (OL и OH), соответственно, легкой и тяжелой цепей митохондриальной ДНК
Карта митохондриального генома человека Отмечены гены, локализованные на митохондриальной ДНК, и сайты инициации транскрипции (РL и PH) и репликации (OL и OH), соответственно, легкой и тяжелой цепей митохондриальной ДНК
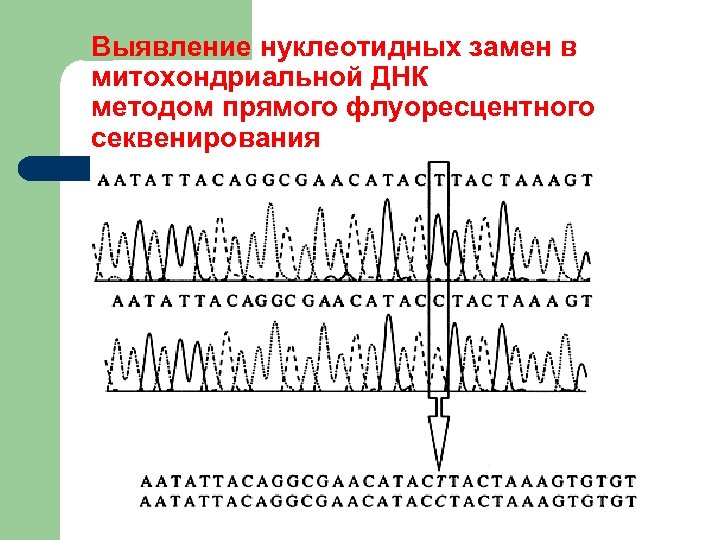 Выявление нуклеотидных замен в митохондриальной ДНК методом прямого флуоресцентного секвенирования
Выявление нуклеотидных замен в митохондриальной ДНК методом прямого флуоресцентного секвенирования
 Возникшая на базе новейших достижений академической биологической науки, технология генетической индивидуализации поначалу лишь обозначила перспективы, указала новые возможные пути решения целого ряда специальных задач в медицинской генетике, генеалогических исследованиях и близнецовом анализе, эпидемиологии, селекции, популяционной и эволюционной генетике, и, наконец, судебной биологии и криминалистике Очевидно, что реализация этих возможностей неизбежно потребовала дальнейшей углубленной разработки, модификации и адаптирования метода в русле каждого конкретного направления. Что касается судебномедицинских аспектов генетической идентификации, то здесь экспертный идентификационный анализ продолжает свое развитие уже не только как область молекулярногенетических исследований, но и как элемент комплексного криминалистического знания, направленного на расследование и раскрытие преступлений.
Возникшая на базе новейших достижений академической биологической науки, технология генетической индивидуализации поначалу лишь обозначила перспективы, указала новые возможные пути решения целого ряда специальных задач в медицинской генетике, генеалогических исследованиях и близнецовом анализе, эпидемиологии, селекции, популяционной и эволюционной генетике, и, наконец, судебной биологии и криминалистике Очевидно, что реализация этих возможностей неизбежно потребовала дальнейшей углубленной разработки, модификации и адаптирования метода в русле каждого конкретного направления. Что касается судебномедицинских аспектов генетической идентификации, то здесь экспертный идентификационный анализ продолжает свое развитие уже не только как область молекулярногенетических исследований, но и как элемент комплексного криминалистического знания, направленного на расследование и раскрытие преступлений.
 Спасибо за внимание.
Спасибо за внимание.


