17 карбоновые кислоты.ppt
- Количество слайдов: 56
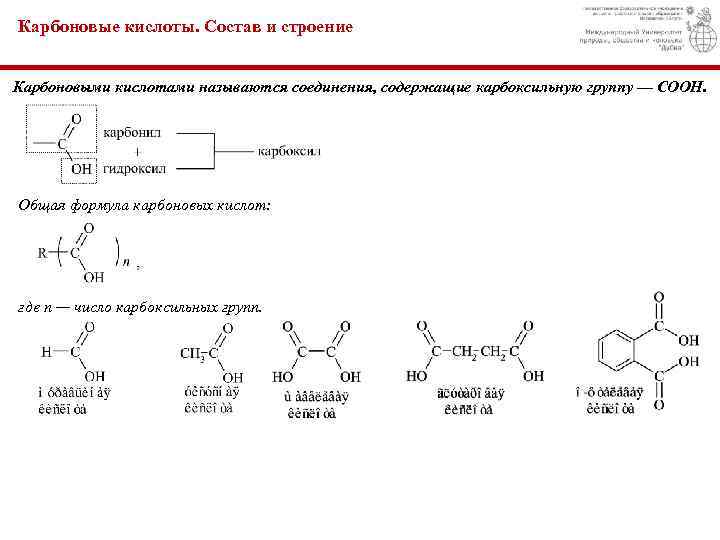
Карбоновые кислоты. Состав и строение Карбоновыми кислотами называются соединения, содержащие карбоксильную группу — СООН. Общая формула карбоновых кислот: где n — число карбоксильных групп.
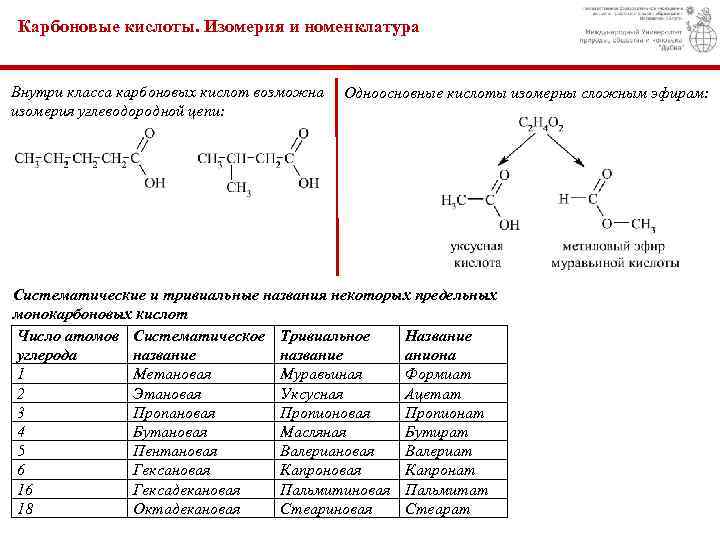
Карбоновые кислоты. Изомерия и номенклатура Внутри класса карбоновых кислот возможна изомерия углеводородной цепи: Одноосновные кислоты изомерны сложным эфирам: Систематические и тривиальные названия некоторых предельных монокарбоновых кислот Число атомов Систематическое Тривиальное Название углерода название аниона 1 Метановая Муравьиная Формиат 2 Этановая Уксусная Ацетат 3 Пропановая Пропионат 4 Бутановая Масляная Бутират 5 Пентановая Валериат 6 Гексановая Капронат 16 Гексадекановая Пальмитиновая Пальмитат 18 Октадекановая Стеариновая Стеарат
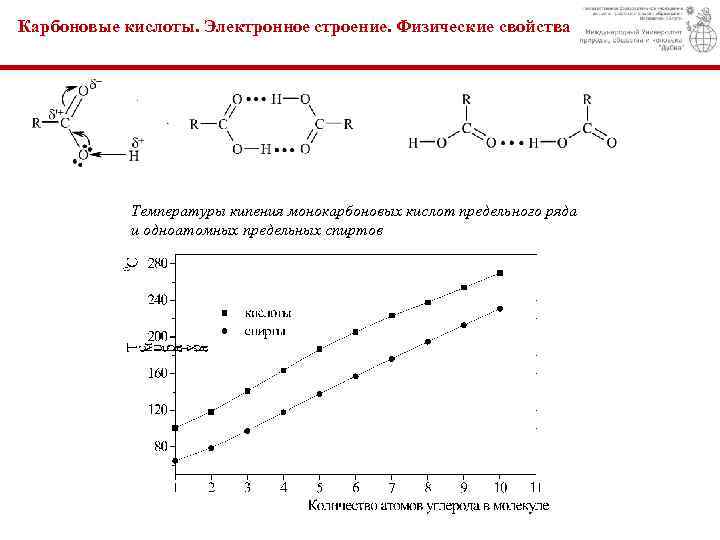
Карбоновые кислоты. Электронное строение. Физические свойства Температуры кипения монокарбоновых кислот предельного ряда и одноатомных предельных спиртов
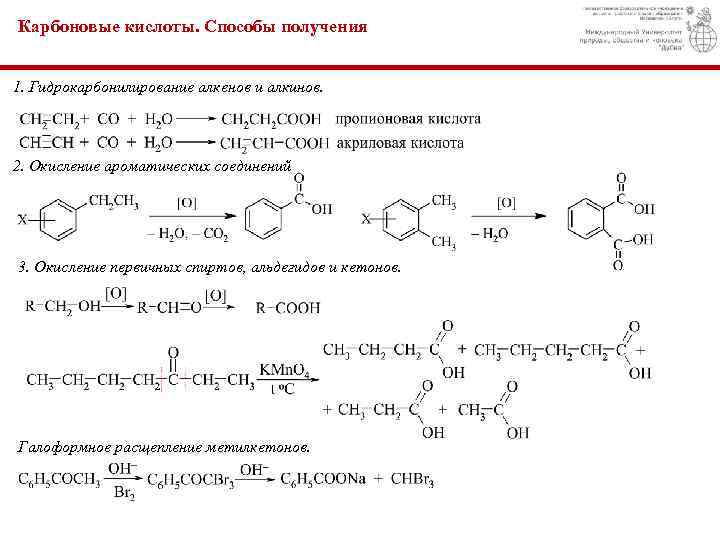
Карбоновые кислоты. Способы получения 1. Гидрокарбонилирование алкенов и алкинов. 2. Окисление ароматических соединений 3. Окисление первичных спиртов, альдегидов и кетонов. Галоформное расщепление метилкетонов.
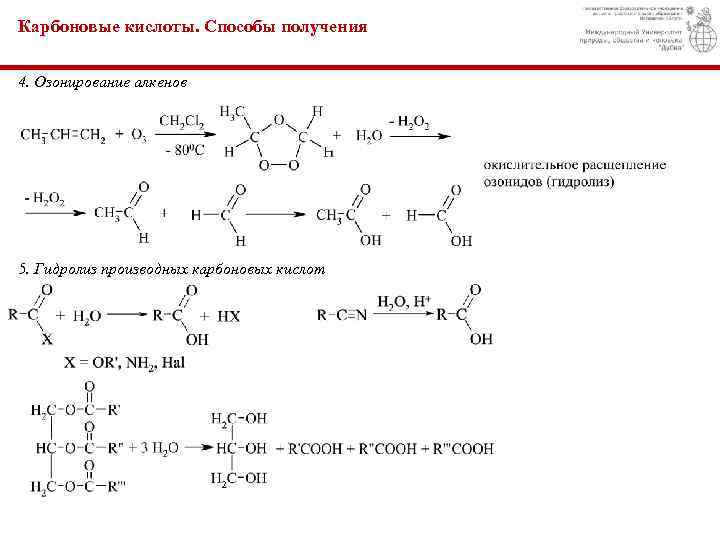
Карбоновые кислоты. Способы получения 4. Озонирование алкенов 5. Гидролиз производных карбоновых кислот

Карбоновые кислоты. Способы получения 6. Карбоксилирование реактивов Гриньяра 7. Специфические способы получения муравьиной и уксусной кислот. 7. 1. Муравьиная кислота 7. 2. Уксусная кислота
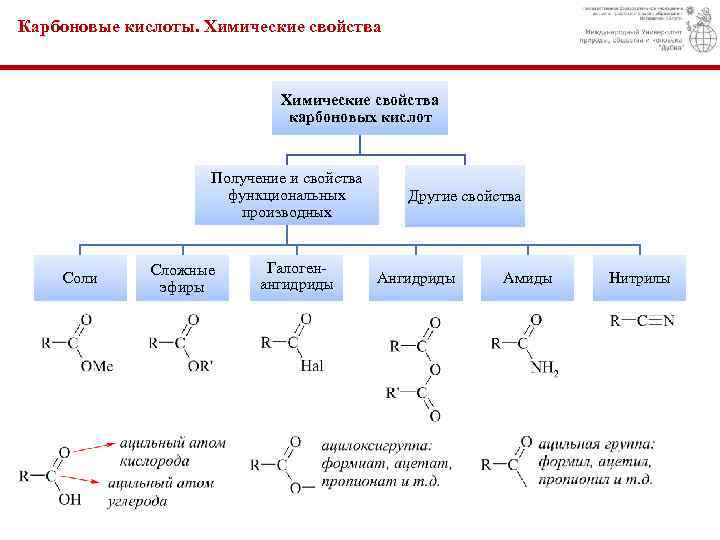
Карбоновые кислоты. Химические свойства карбоновых кислот Получение и свойства функциональных производных Соли Сложные эфиры Галогенангидриды Другие свойства Ангидриды Амиды Нитрилы

Соли карбоновых кислот. 1. Диссоциация. ЭД заместители снижают кислотность, ЭА – повышают. 2. Образование солей. Для карбоновых кислот характерны все реакции кислот, приводящие к образованию солей: — взаимодействие с активными металлами; — взаимодействие с основными оксидами; — взаимодействие со щелочами; — взаимодействие с аммиаком и гидратом окиси аммония; — взаимодействие с солями более слабых кислот (например, с карбонатами).

Сложные эфиры — это соединения, которые образуются в результате взаимодействия карбоновых или кислородсодержащих неорганических кислот со спиртами.
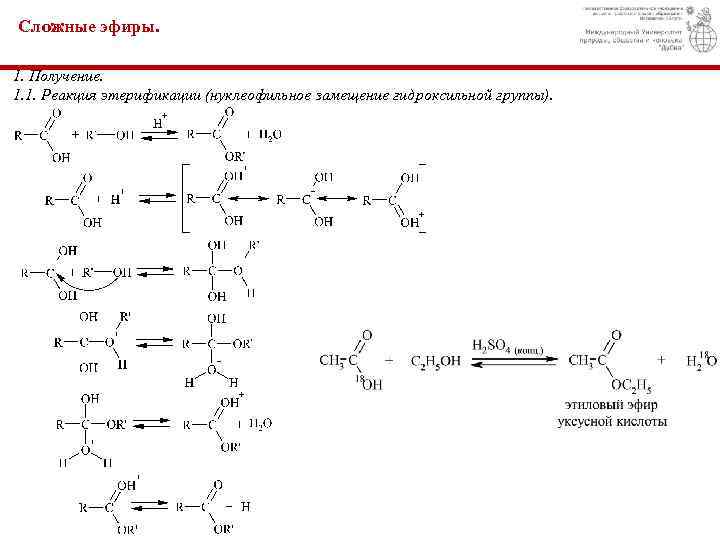
Сложные эфиры. 1. Получение. 1. 1. Реакция этерификации (нуклеофильное замещение гидроксильной группы).

Сложные эфиры. 1. 2. Взаимодействие ангидридов со спиртами и фенолами 1. 3. Взаимодействие галогенангидридов со спиртами и фенолами 1. 4. Присоединение спиртов и фенолов к кетенам. 2. Свойства. 2. 1. Гидролиз.

Сложные эфиры. 2. 2. Переэтерификация. 2. 3. Взаимодействие с реактивом Гриньяра. – низкая температура 2. 4. Восстановление: – алюмогидридом лития; – натрием в этаноле (по Буво-Блану)

Жиры — смесь сложных эфиров, образованных глицерином и высшими карбоновым кислотами (ВКК). Поэтому со структурной точки зрения жиры представляют собой триглицериды карбоновых кислот. C 15 H 31 COOH — пальмитиновая, C 17 H 35 COOH — стеариновая, C 17 H 33 COOH — олеиновая, C 17 H 31 COOH — линолевая, C 17 H 29 COOH — линоленовая. Техническая классификация жиров Тип Твердые Смешанные Жидкие (масла) Особенности строения Содержат остатки насыщенных ВКК Содержат остатки насыщенных и ненасыщенных ВКК Содержат остатки ненасыщенных ВКК Происхождение Животные Исключения Рыбий жир (жидкий) Животные Растения Кокосовое масло (твердое)

Жиры

Жиры Гидролиз. Присоединение водорода.

Жиры Присоединение галогенов. Реакции окисления и полимеризации. Функции жиров в живых организмах: • энергетическая; • запасная; • защитная.
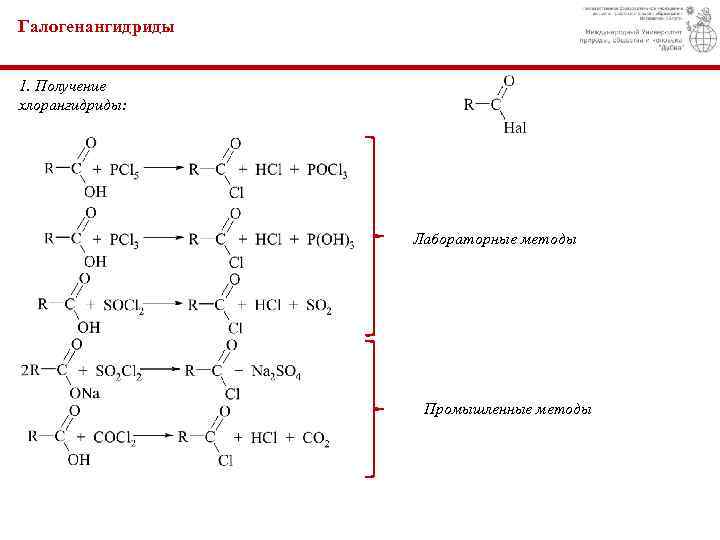
Галогенангидриды 1. Получение хлорангидриды: Лабораторные методы Промышленные методы
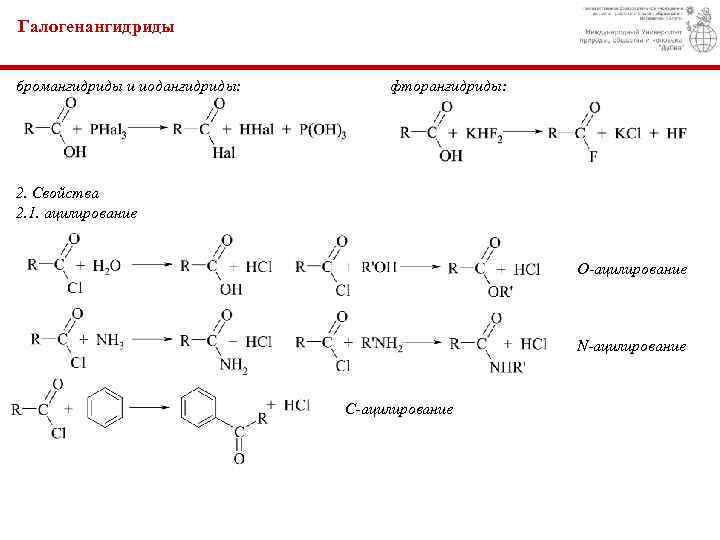
Галогенангидриды бромангидриды и иодангидриды: фторангидриды: 2. Свойства 2. 1. ацилирование О-ацилирование N-ацилирование C-ацилирование
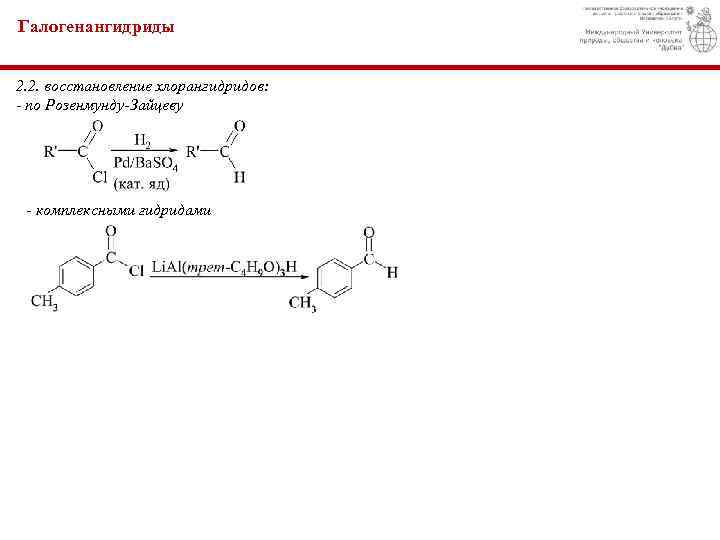
Галогенангидриды 2. 2. восстановление хлорангидридов: - по Розенмунду-Зайцеву - комплексными гидридами
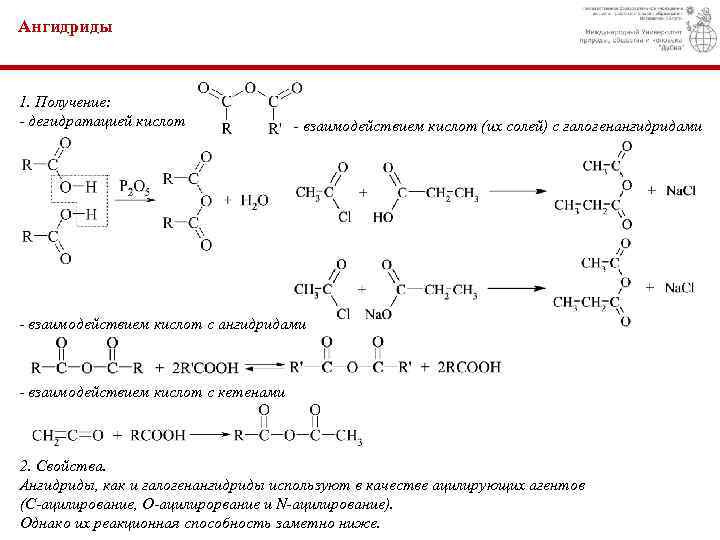
Ангидриды 1. Получение: - дегидратацией кислот - взаимодействием кислот (их солей) с галогенангидридами - взаимодействием кислот с кетенами 2. Свойства. Ангидриды, как и галогенангидриды используют в качестве ацилирующих агентов (С-ацилирование, O-ацилирорвание и N-ацилирование). Однако их реакционная способность заметно ниже.
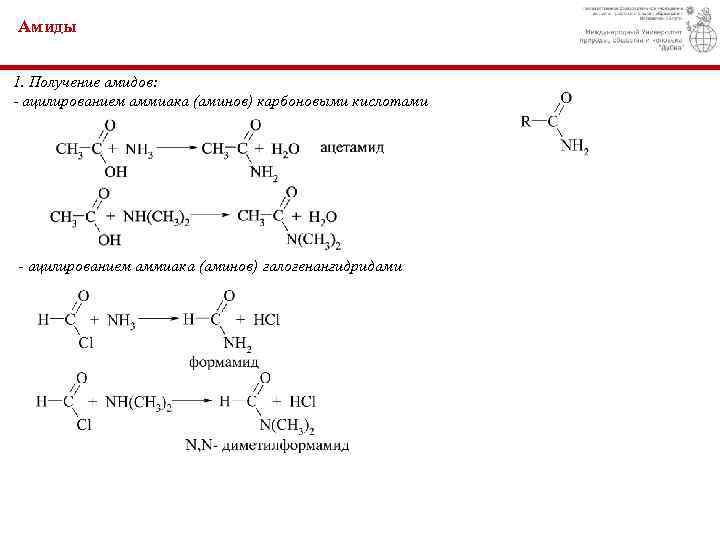
Амиды 1. Получение амидов: - ацилированием аммиака (аминов) карбоновыми кислотами - ацилированием аммиака (аминов) галогенангидридами
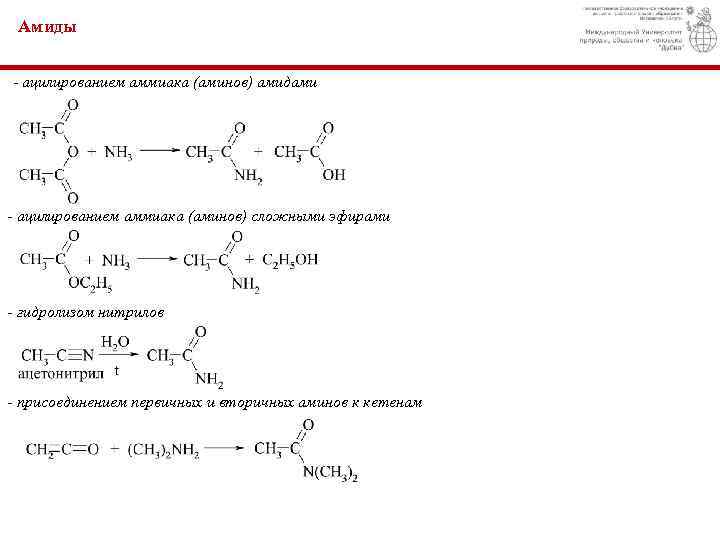
Амиды - ацилированием аммиака (аминов) амидами - ацилированием аммиака (аминов) сложными эфирами - гидролизом нитрилов - присоединением первичных и вторичных аминов к кетенам

Амиды 2. Свойства амидов: - дегидратация под действием водоотнимающих средств - гидролиз - реакция (перегруппировка) Гофмана - восстановление

Нитрилы 1. Получение нитрилов: - дегидратация амидов под действием водоотнимающих средств - аммонолиз карбоновых кислот - дегидратация оксимов альдегидов - из галогеналканов и солей синильной кислоты - из аминов с промежуточным образованием солей диазония
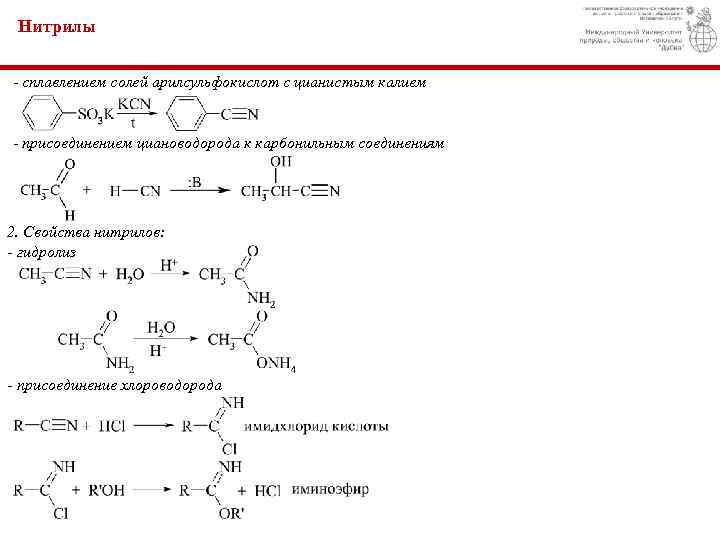
Нитрилы - сплавлением солей арилсульфокислот с цианистым калием - присоединением циановодорода к карбонильным соединениям 2. Свойства нитрилов: - гидролиз - присоединение хлороводорода
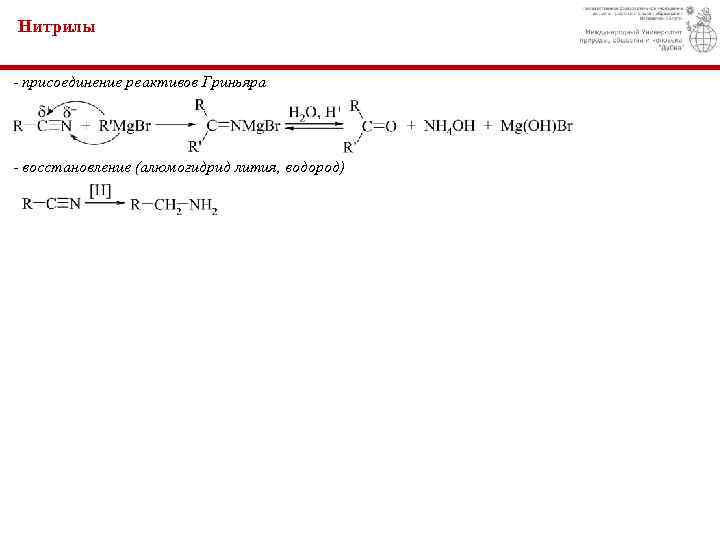
Нитрилы - присоединение реактивов Гриньяра - восстановление (алюмогидрид лития, водород)
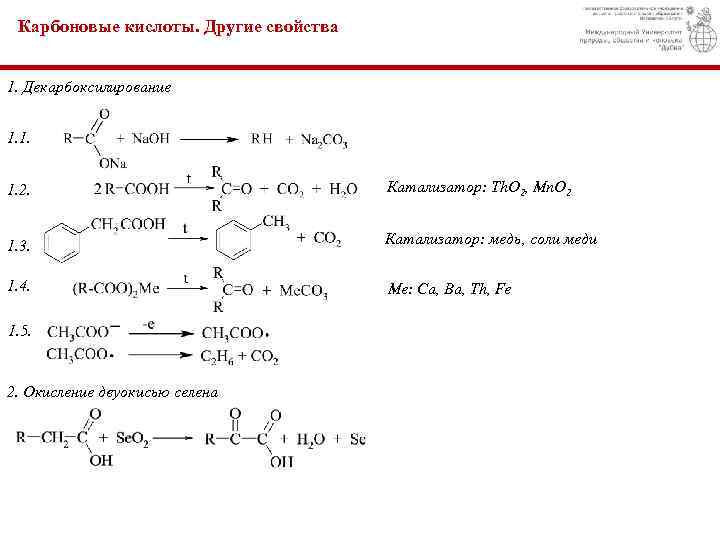
Карбоновые кислоты. Другие свойства 1. Декарбоксилирование 1. 1. 1. 2. Катализатор: Th. O 2, Mn. O 2 1. 3. Катализатор: медь, соли меди 1. 4. Me: Ca, Ba, Th, Fe 1. 5. 2. Окисление двуокисью селена

Карбоновые кислоты. Другие свойства 3. Реакции карбоновых кислот и их производных, протекающие с участием енолят-анионов: 3. 1. Сложноэфирная конденсация Кляйзена
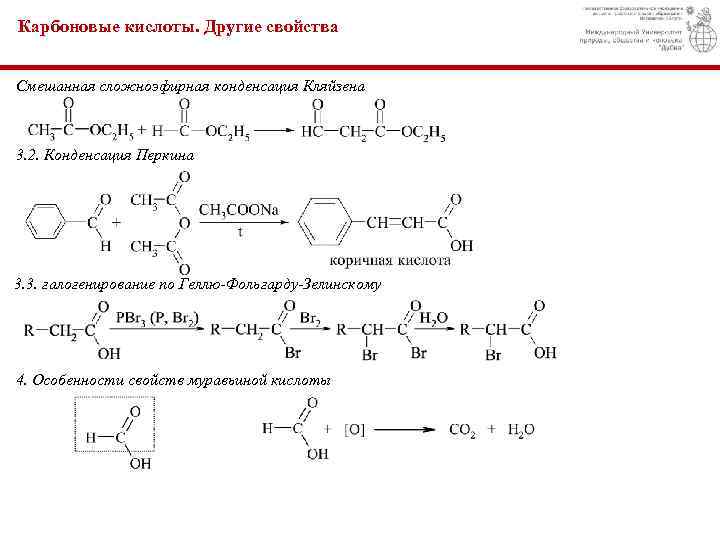
Карбоновые кислоты. Другие свойства Смешанная сложноэфирная конденсация Кляйзена 3. 2. Конденсация Перкина 3. 3. галогенирование по Геллю-Фольгарду-Зелинскому 4. Особенности свойств муравьиной кислоты
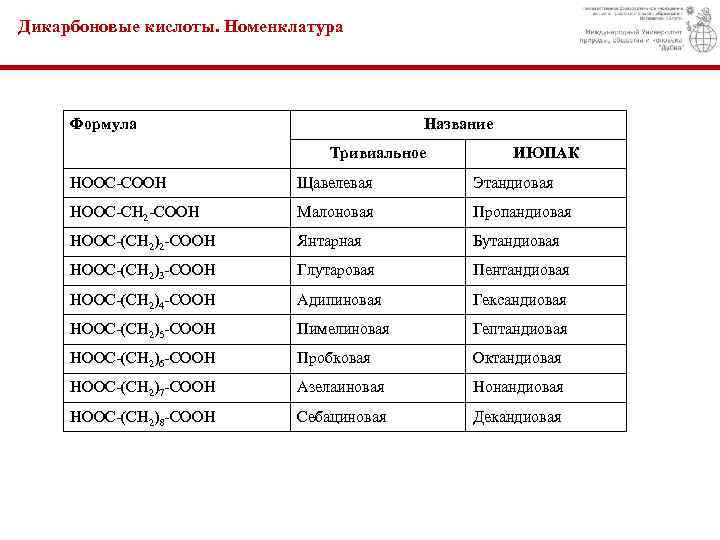
Дикарбоновые кислоты. Номенклатура Формула Название Тривиальное ИЮПАК HOOC-COOH Щавелевая Этандиовая HOOC-CH 2 -COOH Малоновая Пропандиовая HOOC-(CH 2)2 -COOH Янтарная Бутандиовая HOOC-(CH 2)3 -COOH Глутаровая Пентандиовая HOOC-(CH 2)4 -COOH Адипиновая Гександиовая HOOC-(CH 2)5 -COOH Пимелиновая Гептандиовая HOOC-(CH 2)6 -COOH Пробковая Октандиовая HOOC-(CH 2)7 -COOH Азелаиновая Нонандиовая HOOC-(CH 2)8 -COOH Себациновая Декандиовая
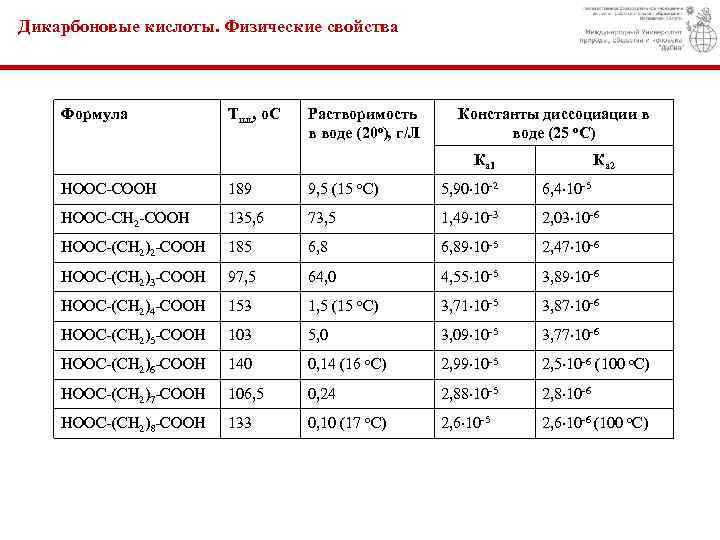
Дикарбоновые кислоты. Физические свойства Формула Тпл. , о. С Растворимость в воде (20 о), г/Л Константы диссоциации в воде (25 о. С) Ка 1 Ка 2 HOOC-COOH 189 9, 5 (15 о. С) 5, 90 10 -2 6, 4 10 -5 HOOC-CH 2 -COOH 135, 6 73, 5 1, 49 10 -3 2, 03 10 -6 HOOC-(CH 2)2 -COOH 185 6, 89 10 -5 2, 47 10 -6 HOOC-(CH 2)3 -COOH 97, 5 64, 0 4, 55 10 -5 3, 89 10 -6 HOOC-(CH 2)4 -COOH 153 1, 5 (15 о. С) 3, 71 10 -5 3, 87 10 -6 HOOC-(CH 2)5 -COOH 103 5, 0 3, 09 10 -5 3, 77 10 -6 HOOC-(CH 2)6 -COOH 140 0, 14 (16 о. С) 2, 99 10 -5 2, 5 10 -6 (100 о. С) HOOC-(CH 2)7 -COOH 106, 5 0, 24 2, 88 10 -5 2, 8 10 -6 HOOC-(CH 2)8 -COOH 133 0, 10 (17 о. С) 2, 6 10 -5 2, 6 10 -6 (100 о. С)
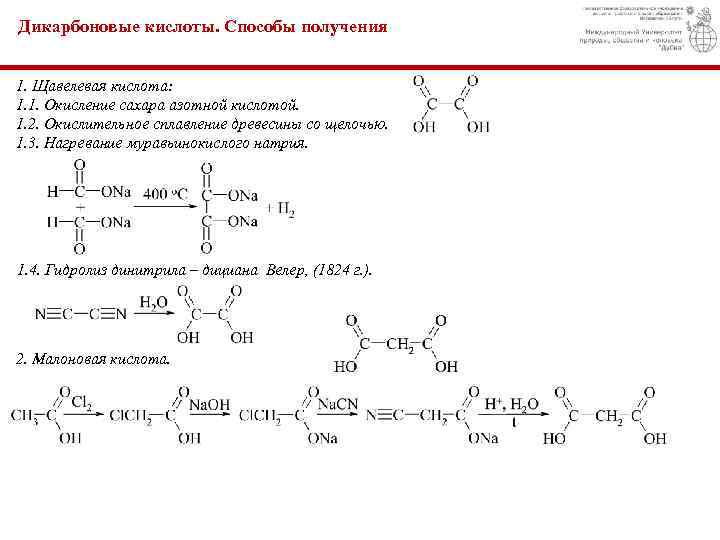
Дикарбоновые кислоты. Способы получения 1. Щавелевая кислота: 1. 1. Окисление сахара азотной кислотой. 1. 2. Окислительное сплавление древесины со щелочью. 1. 3. Нагревание муравьинокислого натрия. 1. 4. Гидролиз динитрила – дициана Велер, (1824 г. ). 2. Малоновая кислота.
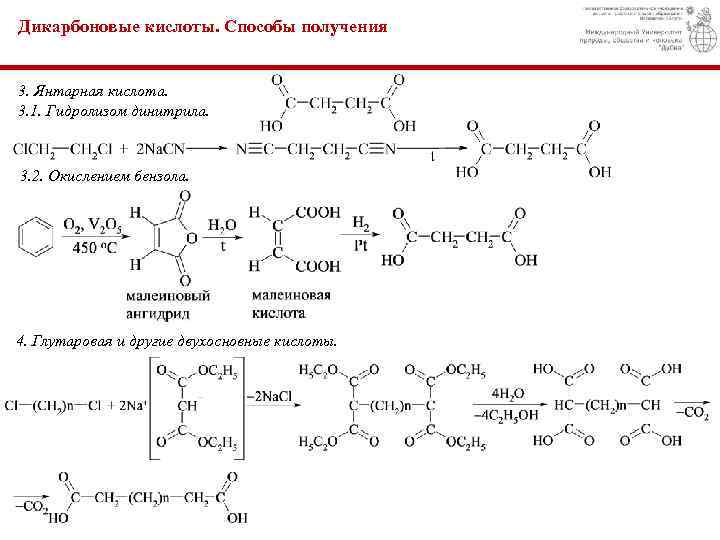
Дикарбоновые кислоты. Способы получения 3. Янтарная кислота. 3. 1. Гидролизом динитрила. 3. 2. Окислением бензола. 4. Глутаровая и другие двухосновные кислоты.
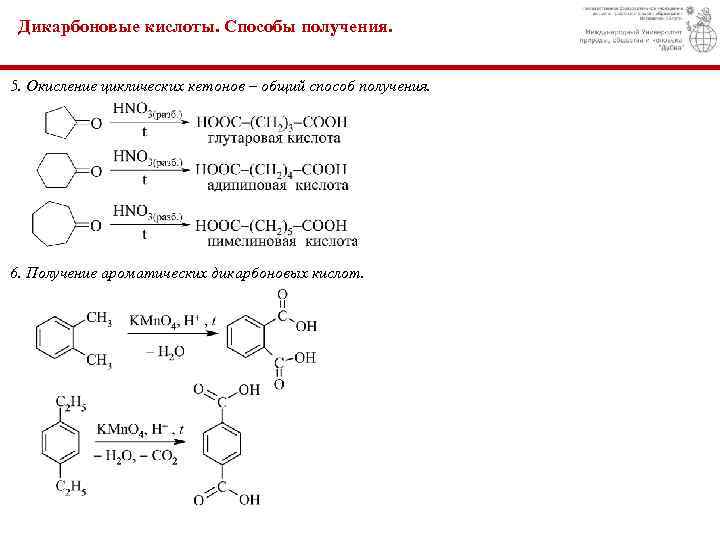
Дикарбоновые кислоты. Способы получения. 5. Окисление циклических кетонов – общий способ получения. 6. Получение ароматических дикарбоновых кислот.

Дикарбоновые кислоты. Химические свойства. 1. Щавелевая кислота. Не образует ангидрида. 1. 1. Декарбоксилирование. 1. 2. Разложение серной кислотой. 1. 3. Окисление. 2. Малоновая кислота. 2. 1. Декарбоксилирование. 2. 2. Дегидратация.
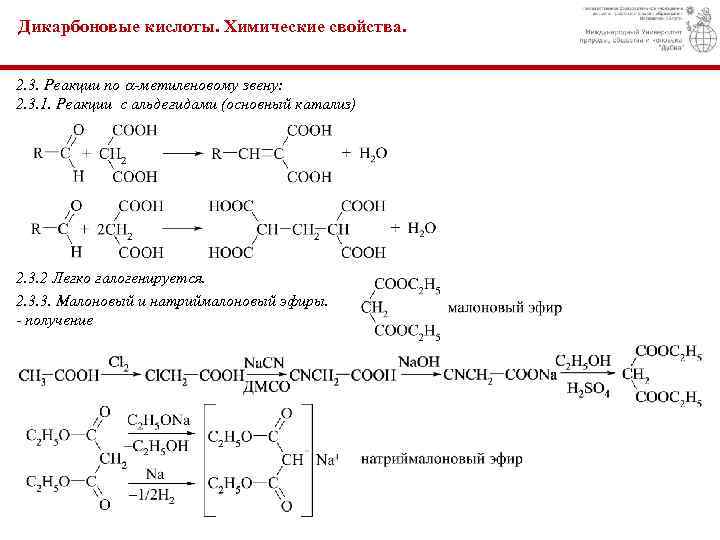
Дикарбоновые кислоты. Химические свойства. 2. 3. Реакции по -метиленовому звену: 2. 3. 1. Реакции с альдегидами (основный катализ) 2. 3. 2 Легко галогенируется. 2. 3. 3. Малоновый и натриймалоновый эфиры. - получение
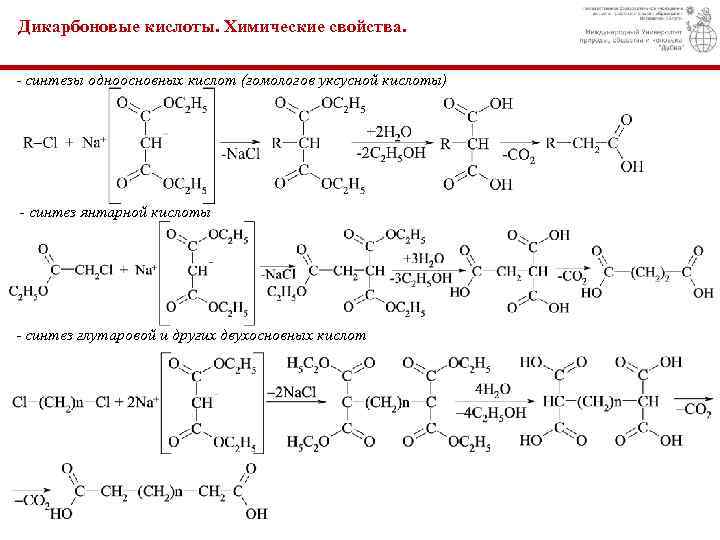
Дикарбоновые кислоты. Химические свойства. - синтезы одноосновных кислот (гомологов уксусной кислоты) - синтез янтарной кислоты - синтез глутаровой и других двухосновных кислот
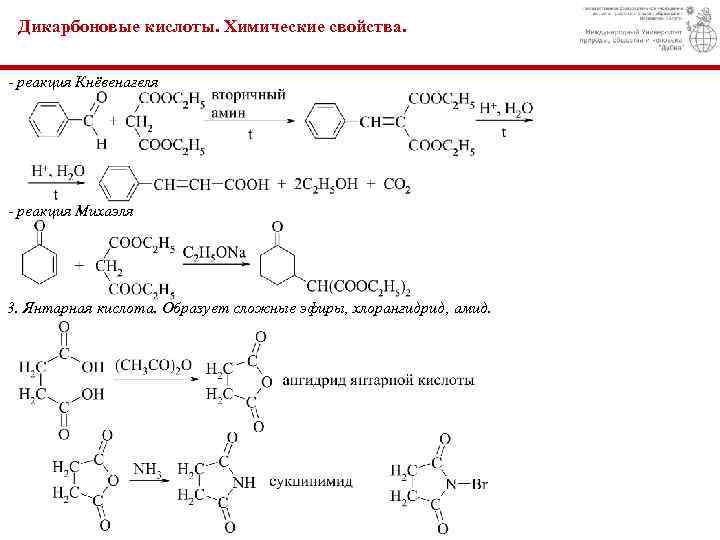
Дикарбоновые кислоты. Химические свойства. - реакция Кнёвенагеля - реакция Михаэля 3. Янтарная кислота. Образует сложные эфиры, хлорангидрид, амид.
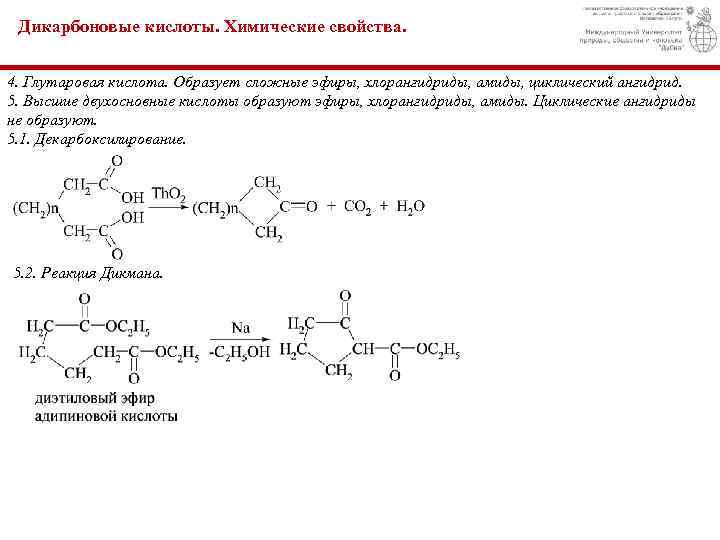
Дикарбоновые кислоты. Химические свойства. 4. Глутаровая кислота. Образует сложные эфиры, хлорангидриды, амиды, циклический ангидрид. 5. Высшие двухосновные кислоты образуют эфиры, хлорангидриды, амиды. Циклические ангидриды не образуют. 5. 1. Декарбоксилирование. 5. 2. Реакция Дикмана.
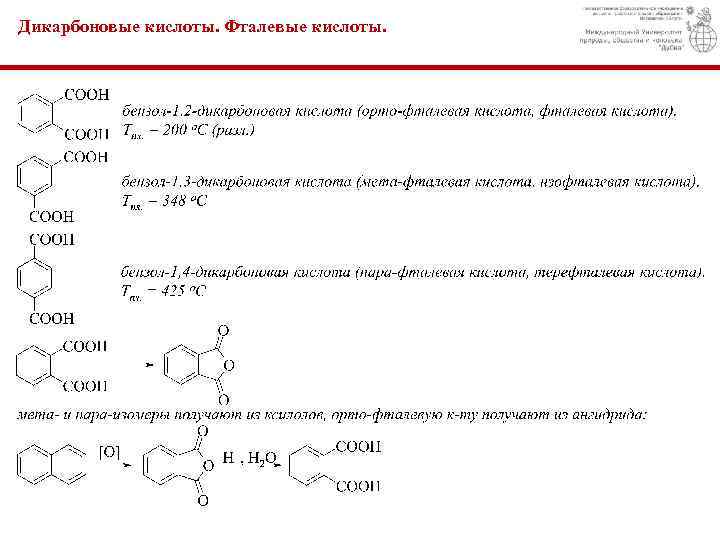
Дикарбоновые кислоты. Фталевые кислоты.
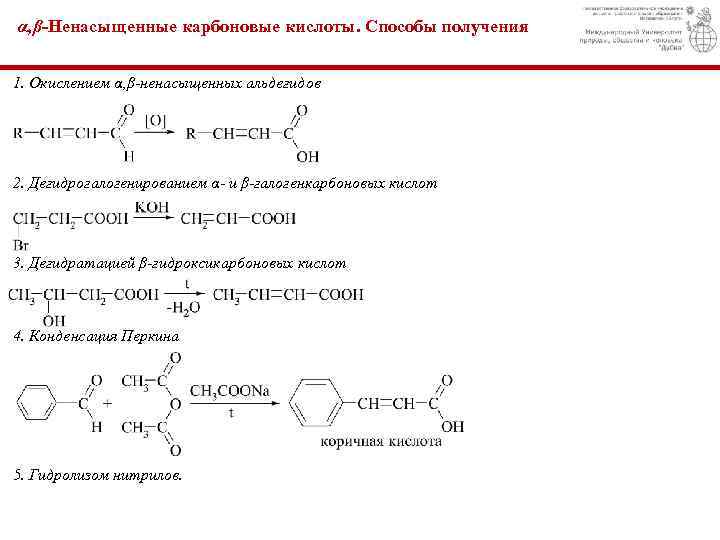
α, β-Ненасыщенные карбоновые кислоты. Способы получения 1. Окислением α, β-ненасыщенных альдегидов 2. Дегидрогалогенированием α- и β-галогенкарбоновых кислот 3. Дегидратацией β-гидроксикарбоновых кислот 4. Конденсация Перкина 5. Гидролизом нитрилов.

α, β-Ненасыщенные карбоновые кислоты. Свойства 1. Кислотность Соединение p. Ka СH 3 CH 2 COOH 4, 87 < CH 2 CHCOOH 4, 26 < 2. Присоединение 2. 1. 1, 2 -Присоединение - галогенирование - диеновый синтез - восстановление (водород, амальгама натрия) < < CHCCOOH 1, 84
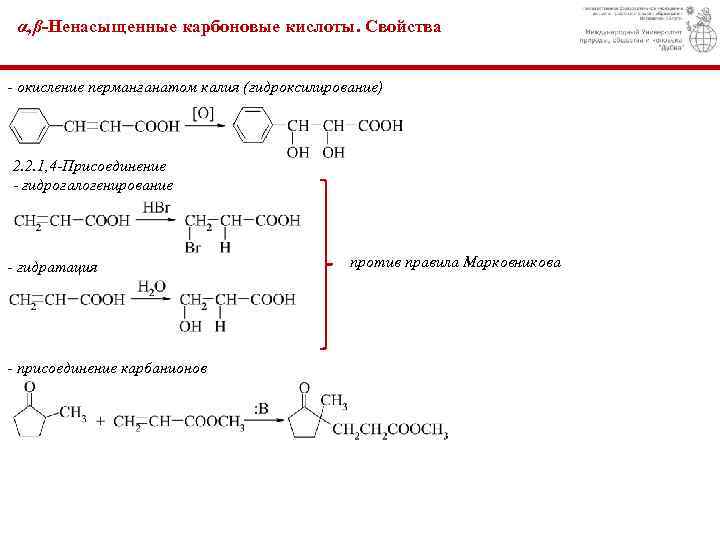
α, β-Ненасыщенные карбоновые кислоты. Свойства - окисление перманганатом калия (гидроксилирование) 2. 2. 1, 4 -Присоединение - гидрогалогенирование - гидратация - присоединение карбанионов против правила Марковникова

α, β-Ненасыщенные карбоновые кислоты. Малеиновая и фумаровая кислоты формулы Тпл. , о. С химические свойства 290 135 (анг. ) d 20 1, 635 1, 590 Ка 1 9, 3· 10 -4 2, 9· 10 -5 Ка 2 получение 130 Ткип. , о. С физические свойства 295 (возг. ) 1, 7· 10 -2 2, 6· 10 -7

Галогензамещенные карбоновые кислоты. Получение: 1. Прямым галогенированием при облучении светом или в присутствии перекисных катализаторов (моно-, ди- и трихлоуксусные кислоты). Галогенирование кислот с более длинными радикалами происходит в различные положения. 2. α-Галогензамещенные кислоты получают галогенированием по Геллю-Фольгарду-Зелинскому 3. Получение монохлоруксусной кислоты: - гидролиз трихлорэтилена - окисление этиленхлоргидрина 4. Получение трихлоруксусной кислоты:
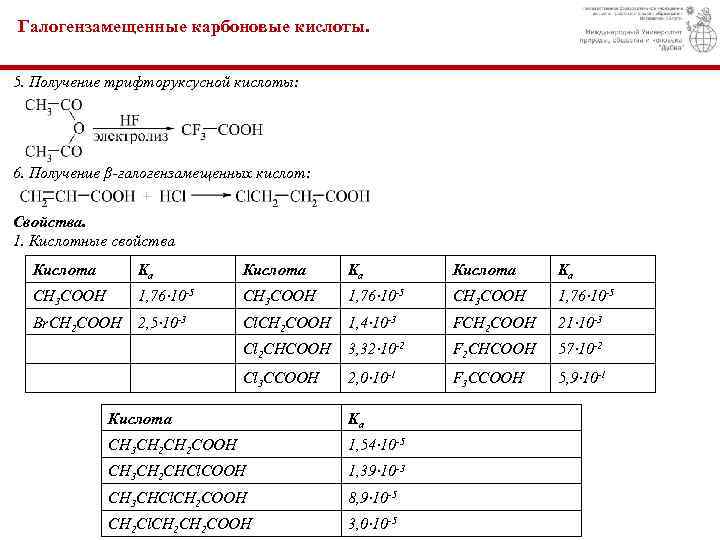
Галогензамещенные карбоновые кислоты. 5. Получение трифторуксусной кислоты: 6. Получение β-галогензамещенных кислот: Свойства. 1. Кислотные свойства Кислота Ka CH 3 COOH 1, 76· 10 -5 Br. CH 2 COOH 2, 5· 10 -3 Cl. CH 2 COOH 1, 4· 10 -3 FCH 2 COOH 21· 10 -3 Cl 2 CHCOOH 3, 32· 10 -2 F 2 CHCOOH 57· 10 -2 Cl 3 CCOOH 2, 0· 10 -1 F 3 CCOOH 5, 9· 10 -1 Кислота Ka CH 3 CH 2 COOH 1, 54· 10 -5 CH 3 CH 2 CHCl. COOH 1, 39· 10 -3 CH 3 CHCl. CH 2 COOH 8, 9· 10 -5 CH 2 Cl. CH 2 COOH 3, 0· 10 -5

Галогензамещенные карбоновые кислоты. 2. Реакции электрофильного замещения Реакции с сильными нуклеофилами сопровождаются обращением конфигурации, со слабыми – нет.

Оксикислоты. Угольная кислота и ее производные Фосген. Ткип. = 8, 3 о. С, медленно гидролизуется водой, быстро – щелочами:

Оксикислоты. Угольная кислота и ее производные Эфиры угольной кислоты. Сернистые производные угольной кислоты. Сероуглерод – CS 2. Ткип. =46 о. С. Крайне огнеопасен. Получают прямым взаимодействием угля и серы. Применение:
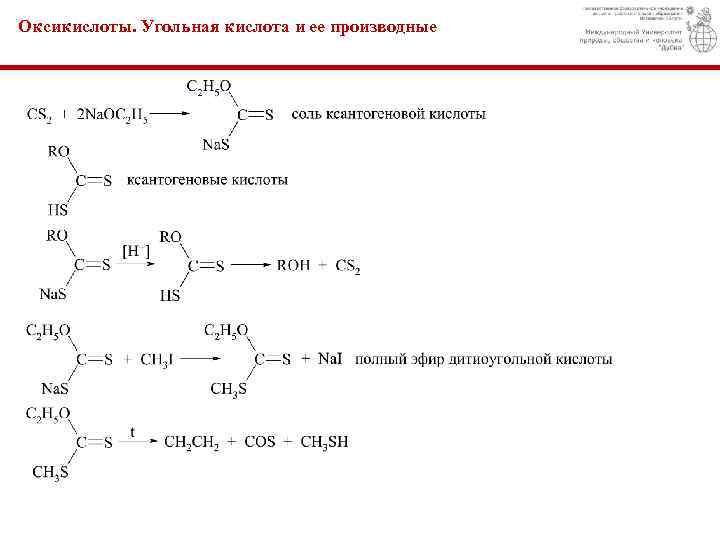
Оксикислоты. Угольная кислота и ее производные

Оксикислоты. Угольная кислота и ее производные Азотистые производные угольной кислоты. Промышленный способ Синтез по Велеру, 1828 г. Нуклеофильность - алкилирование - ацилирование
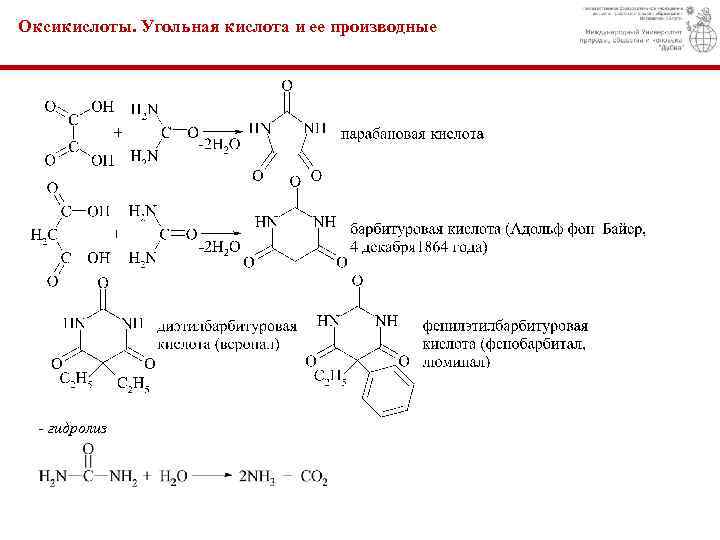
Оксикислоты. Угольная кислота и ее производные - гидролиз

Оксикислоты. Угольная кислота и ее производные Электрофильность: - образование уретанов - образование алкилмочевин - образование семикарбазида

Оксикислоты. Угольная кислота и ее производные Нитрилы угольной кислоты. Циановая кислота

Оксикислоты. Получение: -оксикислот
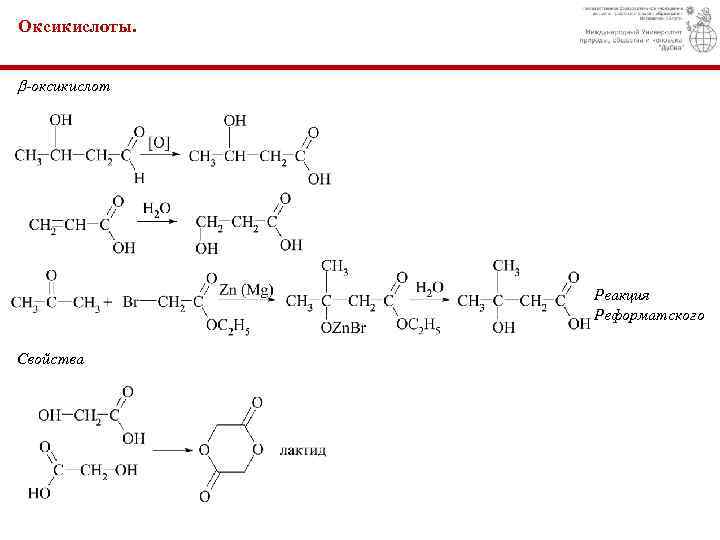
Оксикислоты. -оксикислот Реакция Реформатского Свойства
17 карбоновые кислоты.ppt