Карбоновые кислоты.pptx
- Количество слайдов: 13

Карбоновые кислоты. Презентацию подготовила Кузнецова Татьяна, ИЭУи. П СФУ, гр. ЭБ 13 -01 Б

Функциональная группа Группа атомов: карбоксильная –C O OH группа ( карбоксил)

По количеству карбоксильных групп различают: Одноосновные : RCOOH, н. р. Уксусная кислота CH₃-C O OH Двухосновные: н. р. Щавелевая кислота и янтарная O=C-C=O O=C-CH₂-C=O OH OH Многоосновные: н. р. Лимонная кислота OH HOOC-CH₂-COOH
![Получение Окислением первичных спиртов и альдегидов: [O] R-CH₂-OH R-C=O [O] R-C=O OH H OH Получение Окислением первичных спиртов и альдегидов: [O] R-CH₂-OH R-C=O [O] R-C=O OH H OH](https://present5.com/presentation/1/-57810837_243543402.pdf-img/-57810837_243543402.pdf-4.jpg)
Получение Окислением первичных спиртов и альдегидов: [O] R-CH₂-OH R-C=O [O] R-C=O OH H OH Ароматические карб. кислоты образуются окислением гомологов бензола: CH₃ [O] COOH

Гидролизом различных производных карбоновых кислот: н. р. гидролиз сложного эфира O CH₃-C-O-C₂H₅ + H₂O H⁺ CH₃-COOH + C₂H₅OH

Физические свойства предельных одноосновных кислот. Если содержат до 4 -х атомов углерода: жидкие с характерным резким запахом. От 4 -х до 9 -ти : вязкие маслянистые жидкости с неприятным запахом. Более 9 -ти: твёрдые вещества, не растворимы в воде. Температура кипения увеличивается с ростом относительной молекулярной массы. Растворимость снижается с увеличением числа атомов в углеводородном радикале.

Химические свойства Диссоциация: CH₃-COOH CH₃-COOˉ + H⁺ Взаимодействие с металлами (до водорода): 2 CH₃-COOH + Fe (CH₃-COO)₂Fe + H₂ Взаимодействие с основными оксидами: 2 R-COOH + Ca. O (R-CОО)₂Ca + H₂O

Взаимодействие с гидроксидами металлов : R-COOH + Na. OH R-COONa + H₂O 2 R-COOH + Ca(OH)₂ (R-COO)₂Ca + 2 H₂O Взаимодействие с солями более слабых кислот: CH₃COOH + C₁₇H₃₅COONa CH₃COONa + C₁₇H₃₅COOH 2 CH₃COOH + K₂CO₃ 2 CH₃COOK + H₂O + CO₂
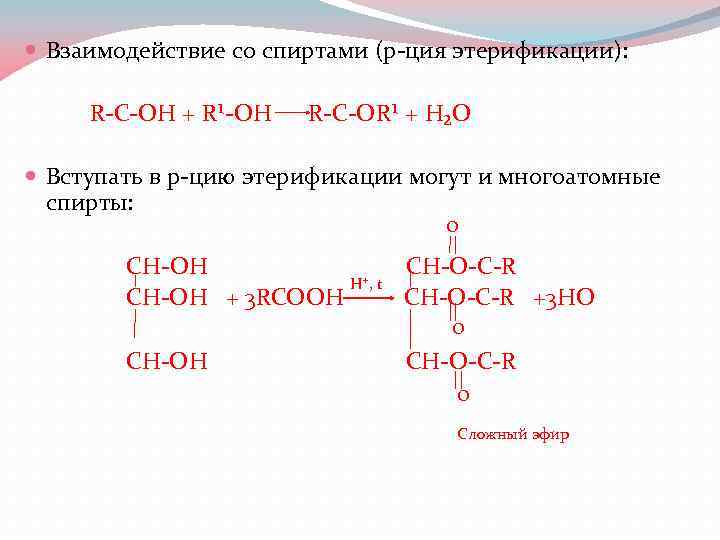
Взаимодействие со спиртами (р-ция этерификации): R-C-OH + R¹-OH R-C-OR¹ + H₂O Вступать в р-цию этерификации могут и многоатомные спирты: O CH-OH CH-O-C-R H⁺, t CH-OH + 3 RCOOH CH-O-C-R +3 HO O CH-OH CH-O-C-R O Сложный эфир

Реакции присоединения по кратной связи: катализатор Cn. H 2 n-1 COOH + H CH₂=CH-COOH + Br₂ Cn. H 2 n+1 COOH CH₂Br-CHBr-COOH Реакции замещения (с галогенами): CH₃-COOH + Cl₂ P(красный) CH₂Cl-COOH + HCl

Где встречаются карбоновые кислоты Муравьиная (метановая) кислота HCOOH – жалящая жидкость, выделяемая муравьями. Уксусная (этановая) кислота CH₃COOH– продукт окисления этанола на воздухе. Щавелевая (этандионовая) кислота HOOC-COOHеё соли встречаются во многих растениях, например в щавеле и кислице.

Применение Муравьиная кислота: пищевая, кожевенная, фармацевтическая промышленность; медицина; окрашивание тканей и бумаги. Уксусная кислота: пищевая промышленность; кожевенная, лакокрасочная промышленность; получение гербицидов. Соли пальмитиновой и стеариновой кислот: обладают моющим действием. Соли олеиновой кислоты: широкое применение в технике. Щавелевая кислота: полировка металлов; деревообрабатывающая и кожевенная промышленность.

Использован материал учебника по химии О. С. Габриеляна, Ф. Н. Маскаева, С. Ю. Пономарева, В. И. Тетерина. 7 -е издание. Москва, 2006 г. Спасибо за внимание!
Карбоновые кислоты.pptx