Карбоновые кислоты.ppt
- Количество слайдов: 21

КАРБОНОВЫЕ КИСЛОТЫ Электронный дидактический материал информационного типа Составитель: Сабирзянова А. З. , преподаватель биохимии © ГАОУ СПР «Казанский медицинский колледж» Выход
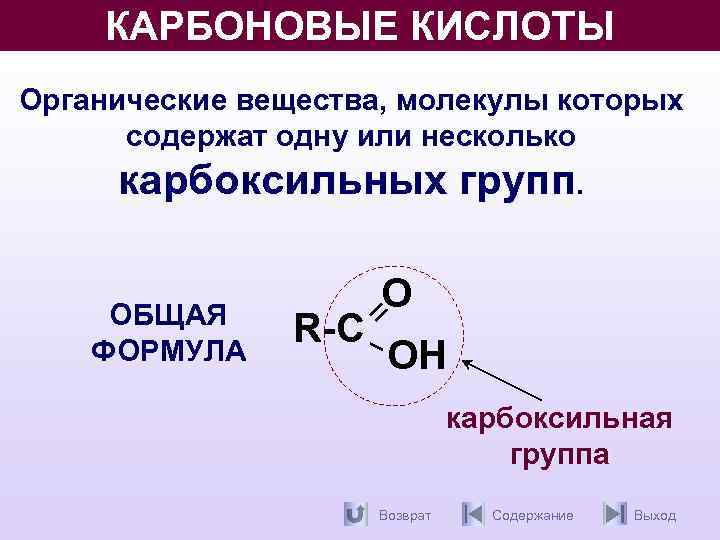
КАРБОНОВЫЕ КИСЛОТЫ Органические вещества, молекулы которых содержат одну или несколько карбоксильных групп. ОБЩАЯ ФОРМУЛА R-С О ОН карбоксильная группа Возврат Содержание Выход
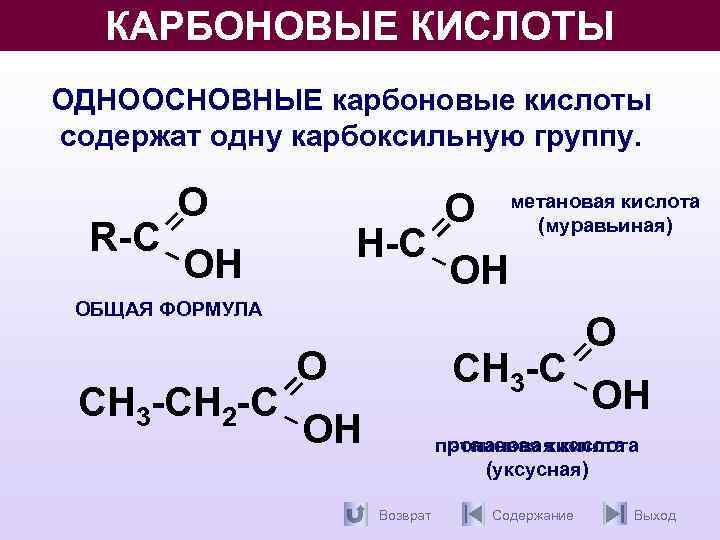
КАРБОНОВЫЕ КИСЛОТЫ ОДНООСНОВНЫЕ карбоновые кислоты содержат одну карбоксильную группу. R-С О Н-С ОН О метановая кислота (муравьиная) ОН ОБЩАЯ ФОРМУЛА СН 3 -СН 2 -С О СН 3 -С ОН О ОН пропановая кислота этановая кислота (уксусная) Возврат Содержание Выход
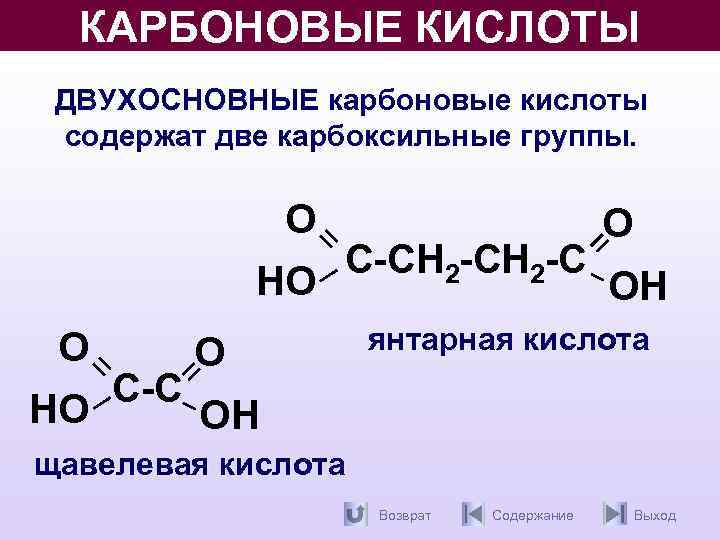
КАРБОНОВЫЕ КИСЛОТЫ ДВУХОСНОВНЫЕ карбоновые кислоты содержат две карбоксильные группы. О НО С-СН 2 -С О О ОН янтарная кислота ОН щавелевая кислота Возврат Содержание Выход
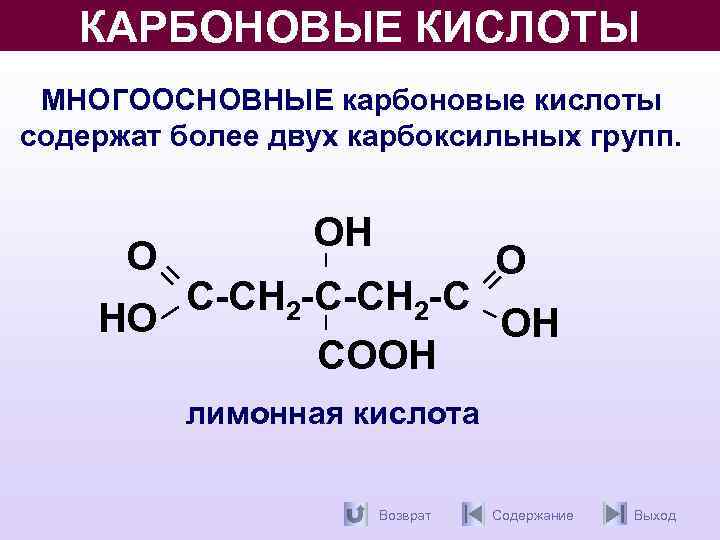
КАРБОНОВЫЕ КИСЛОТЫ МНОГООСНОВНЫЕ карбоновые кислоты содержат более двух карбоксильных групп. О ОН О С-СН 2 -С НО ОН СООН лимонная кислота Возврат Содержание Выход
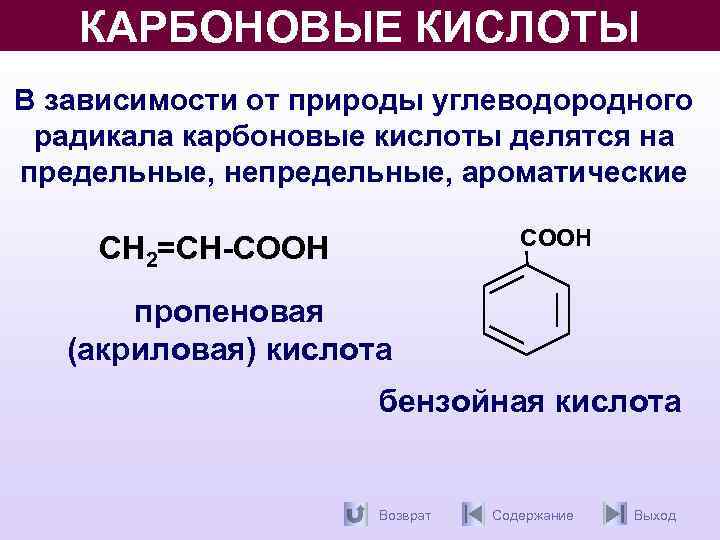
КАРБОНОВЫЕ КИСЛОТЫ В зависимости от природы углеводородного радикала карбоновые кислоты делятся на предельные, непредельные, ароматические CООН СН 2=СН-СООН пропеновая (акриловая) кислота бензойная кислота Возврат Содержание Выход
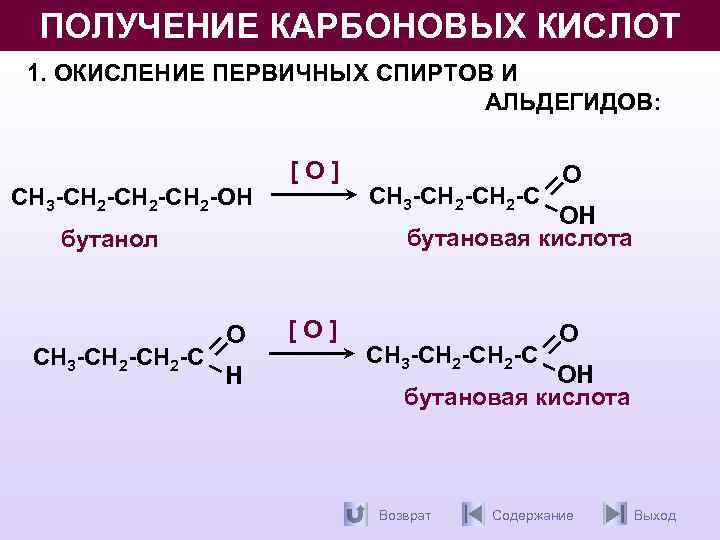
ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ 1. ОКИСЛЕНИЕ ПЕРВИЧНЫХ СПИРТОВ И АЛЬДЕГИДОВ: СН 3 -СН 2 -СН 2 -ОН [O] ОН бутановая кислота бутанол СН 3 -СН 2 -С О Н СН 3 -СН 2 -С О [O] СН 3 -СН 2 -С О ОН бутановая кислота Возврат Содержание Выход
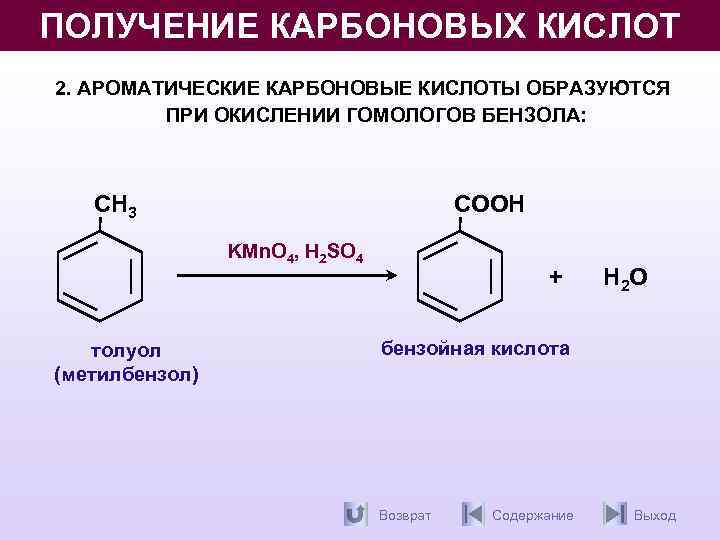
ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ 2. АРОМАТИЧЕСКИЕ КАРБОНОВЫЕ КИСЛОТЫ ОБРАЗУЮТСЯ ПРИ ОКИСЛЕНИИ ГОМОЛОГОВ БЕНЗОЛА: CH 3 CООН KMn. O 4, H 2 SO 4 толуол (метилбензол) + H 2 О бензойная кислота Возврат Содержание Выход
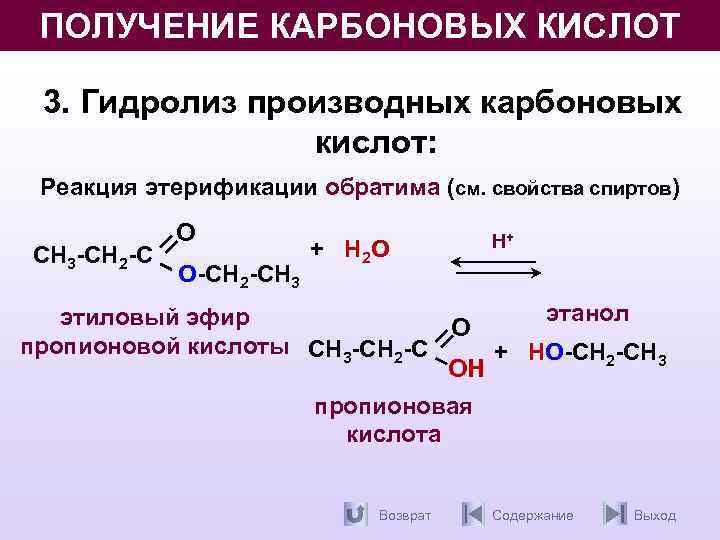
ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ 3. Гидролиз производных карбоновых кислот: Реакция этерификации обратима (см. свойства спиртов) СН 3 -СН 2 -С О О-СН 2 -СН 3 + Н 2 O Н+ этанол этиловый эфир О пропионовой кислоты СН 3 -СН 2 -С + НО-СН 2 -СН 3 ОН пропионовая кислота Возврат Содержание Выход
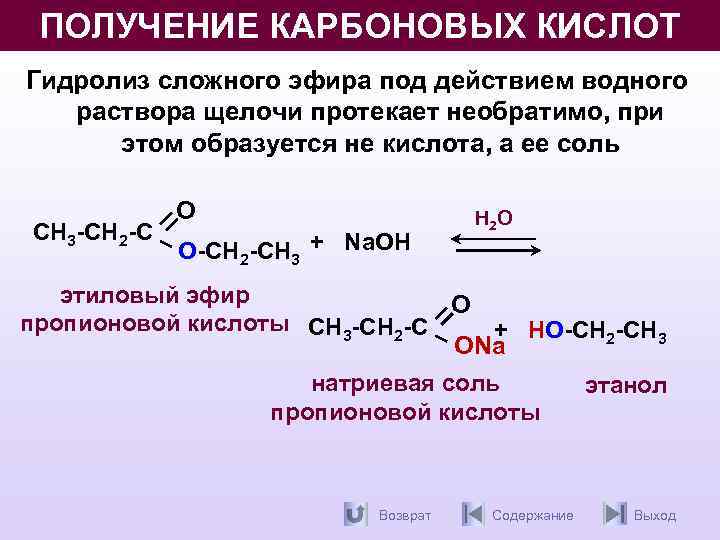
ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ Гидролиз сложного эфира под действием водного раствора щелочи протекает необратимо, при этом образуется не кислота, а ее соль СН 3 -СН 2 -С О О-СН 2 -СН 3 + Na. OH H 2 O этиловый эфир О пропионовой кислоты СН 3 -СН 2 -С + НО-СН 2 -СН 3 ОNa натриевая соль этанол пропионовой кислоты Возврат Содержание Выход
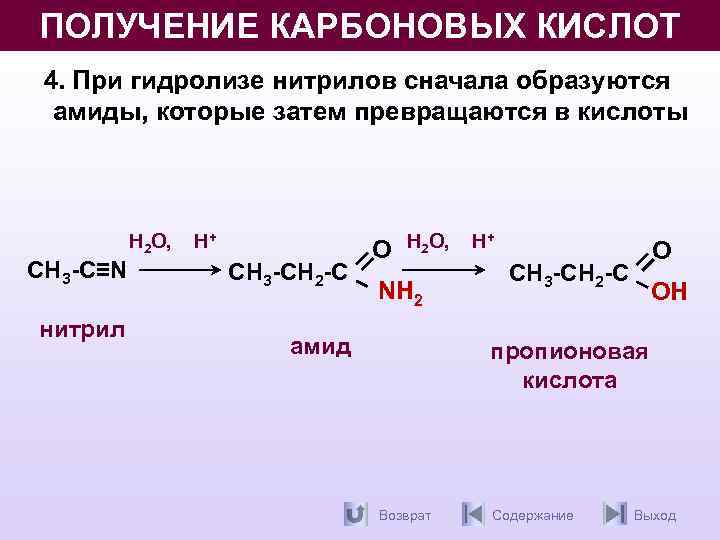
ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ 4. При гидролизе нитрилов сначала образуются амиды, которые затем превращаются в кислоты H 2 O , СН 3 -C≡N нитрил Н+ СН 3 -СН 2 -С О H 2 O , NH 2 амид Н+ О СН 3 -СН 2 -С ОН пропионовая кислота Возврат Содержание Выход

ХИМИЧЕСКИЕ СВОЙСТВА КАРБОНОВЫХ КИСЛОТ 1. ВЗАИМОДЕЙСТВИЕ С МЕТАЛЛАМИ Железо восстанавливает водород из уксусной кислоты 2 СН 3 -СООН + Fe этановая кислота (СН 3 -СОО)2 Fe + H 2 ацетат железа 2. ВЗАИМОДЕЙСТВИЕ С ОСНОВНЫМИ ОКСИДАМИ 2 R-СООН + Ca. O карбоновая кислота (R-СОО)2 Ca + H 2 O соль карбоновой кислоты Возврат Содержание Выход

ХИМИЧЕСКИЕ СВОЙСТВА КАРБОНОВЫХ КИСЛОТ 3. ВЗАИМОДЕЙСТВИЕ С ГИДРОКСИДАМИ МЕТАЛЛОВ (реакция нейтрализации) 2 R-СООН + Ca(OН)2 карбоновая кислота R-СООН + Na. OН карбоновая кислота (R-СОО)2 Ca + 2 H 2 O соль карбоновой кислоты R-СООNa + H 2 O соль карбоновой кислоты Возврат Содержание Выход
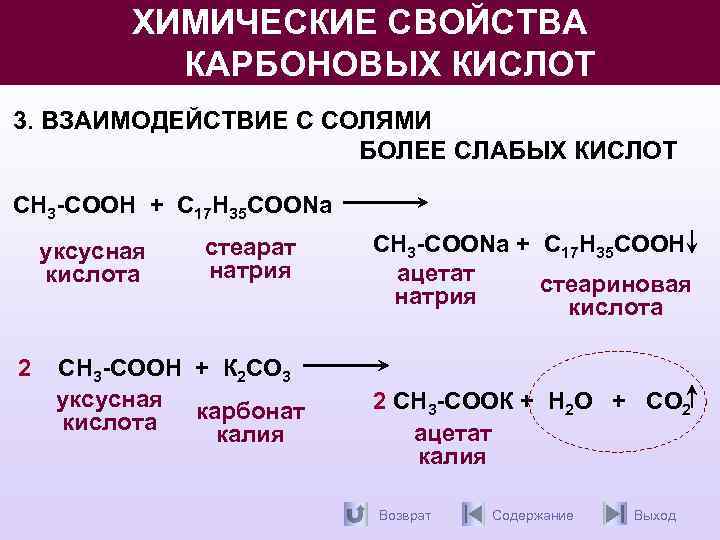
ХИМИЧЕСКИЕ СВОЙСТВА КАРБОНОВЫХ КИСЛОТ 3. ВЗАИМОДЕЙСТВИЕ С СОЛЯМИ БОЛЕЕ СЛАБЫХ КИСЛОТ СН 3 -СООН + С 17 Н 35 СООNa уксусная кислота 2 стеарат натрия СН 3 -СООН + К 2 СО 3 уксусная карбонат кислота калия СН 3 -СООNa + С 17 Н 35 СООН ацетат стеариновая натрия кислота 2 СН 3 -СООК + Н 2 О + СО 2 ацетат калия Возврат Содержание Выход
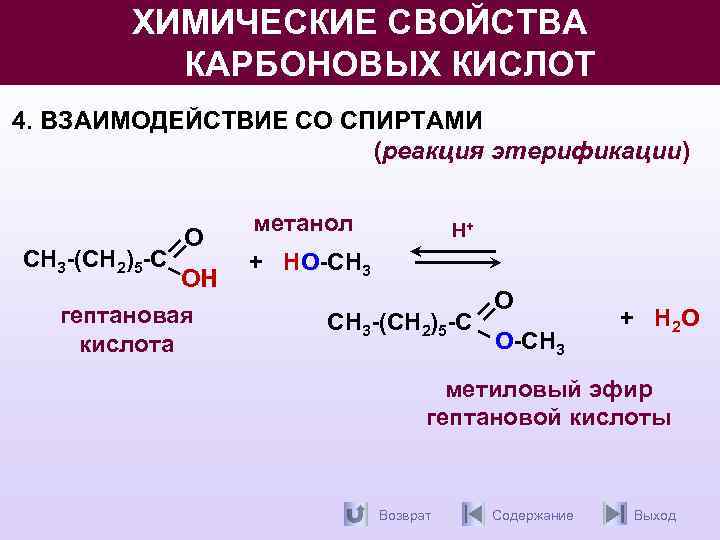
ХИМИЧЕСКИЕ СВОЙСТВА КАРБОНОВЫХ КИСЛОТ 4. ВЗАИМОДЕЙСТВИЕ СО СПИРТАМИ (реакция этерификации) СН 3 -(СН 2)5 -С О ОН гептановая кислота метанол Н+ + НО-СН 3 -(СН 2)5 -С О О-СН 3 + Н 2 O метиловый эфир гептановой кислоты Возврат Содержание Выход
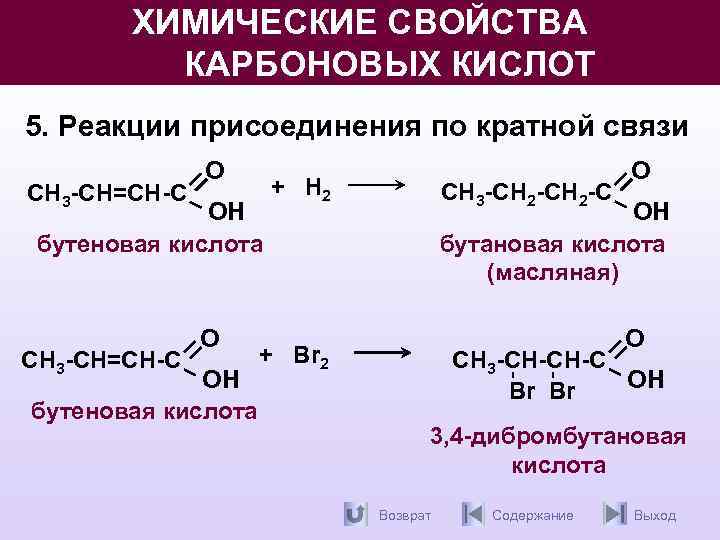
ХИМИЧЕСКИЕ СВОЙСТВА КАРБОНОВЫХ КИСЛОТ 5. Реакции присоединения по кратной связи СН 3 -СН=СН-С О OН бутеновая кислота + H 2 СН 3 -СН 2 -С О OН бутановая кислота (масляная) О + Br 2 СН 3 -СН-СН-С OН Br Br 3, 4 -дибромбутановая кислота Возврат Содержание Выход

ХИМИЧЕСКИЕ СВОЙСТВА КАРБОНОВЫХ КИСЛОТ 6. Реакции замещения α СН 3 -СН 2 -С О Р (красный) + Br 2 OН пропановая кислота α О + СН 3 -СН-С OН Br α СН 3 -СН-С + НCl OН Br α-бромпропановая кислота 2 -бромпропановая кислота Р (красный) Br 2 2 -бромпропановая кислота О α О СН 3 -С-С Br 2 OН 2, 2 -дибромпропановая кислота Возврат Содержание Выход

ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ Муравьиная кислота применяется в кислота медицине, пчеловодстве, в органическом синтезе, при получении растворителей и консервантов; в качестве сильного восстановителя. Впервые была выделена в XVII веке из красных лесных муравьев. Содержится также в соке жгучей крапивы. Безводная муравьиная кислота – бесцветная жидкость с острым запахом и жгучим вкусом, вызывающая ожоги на коже. Применяется в текстильной промышленности в качестве протравы при крашении тканей, для дубления кож, а также для различных синтезов. Возврат Содержание Выход

ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ Уксусная кислота применяется в кислота пищевой и химической промышленности (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров). В домашнем хозяйстве как вкусовое и консервирующее вещество. Широко распространена в природе – содержится в выделениях животных (моче, желчи, испражнениях), в растениях (в зеленых листьях). Образуется при брожении, гниении, скисании вина, пива, содержится в кислом молоке и сыре. Возврат Содержание Выход

ЛИЕТРАТУРА 1. «Химия» / ред. О. С. Габриеляна – М. : Изд. центр «Академия» – Учебник для профессий и специальностей естественнонаучного профиля – 2011. – 384 с. 2. «Химия 10 класс» / О. С. Габриелян, Ф. Н. Маскаев, С. Ю. Пономарев, В. И. Теренин – М. : Дрофа – Учебник – профильный уровень – 2011. – 318 с. 3. «Химия в тестах, задачах и упражнениях» / О. С. Габриелян, Г. Г. Лысова – М. : Изд. центр «Академия» – учебное пособие для студентов сред. проф. образования – 2012. – 224 с. Возврат Содержание Выход
Конец работы. Вы действительно хотите закончить работу с информационным материалом темы «Карбоновые кислоты» ? Да Нет
Карбоновые кислоты.ppt