КАРБОНИЛ 2.ppt
- Количество слайдов: 94
КАРБОНИЛЬНЫЕ СОЕДИНЕНИЯ АЛЬДЕГИДЫ И КЕТОНЫ
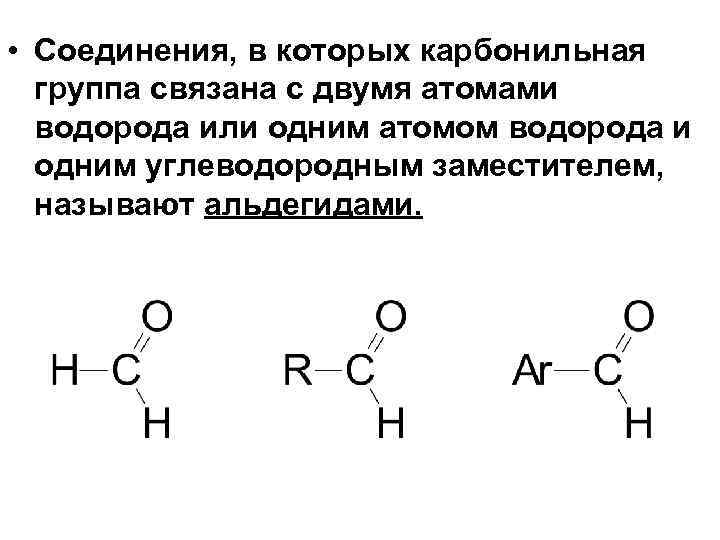
• Соединения, в которых карбонильная группа связана с двумя атомами водорода или одним атомом водорода и одним углеводородным заместителем, называют альдегидами.

Соединения, в которых карбонильная группа связана с двумя углеводородными заместителями, одинаковыми или различными, называют кетонами. Углеводородные заместители могут быть алифатическими, алициклическими (насыщенными или ненасыщенными) или ароматическими.

Номенклатура • К названию углеводорода, соответствующего главной цепи, прибавляют суффикс –аль для альдегидов или суффикс –он для кетонов.
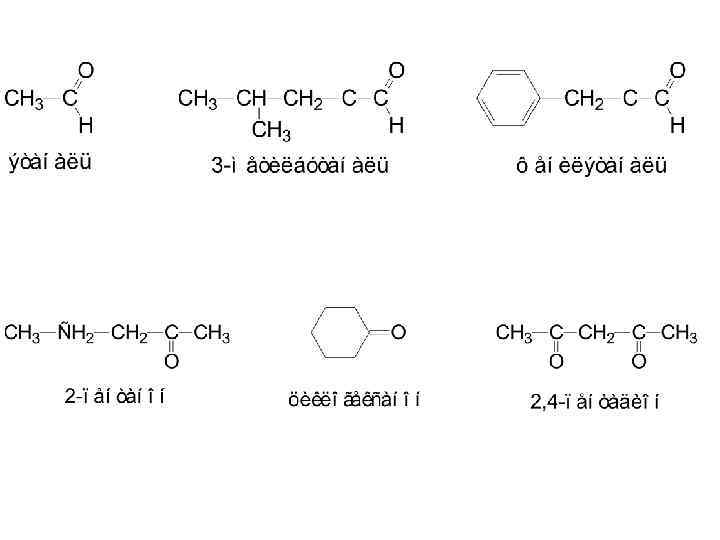
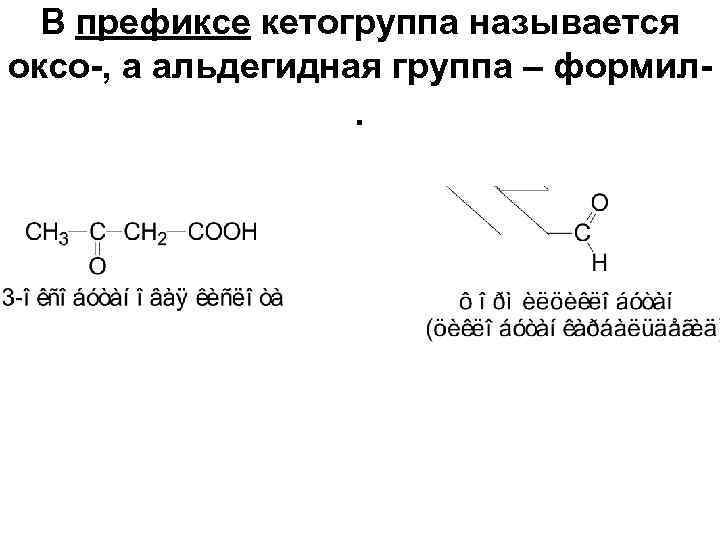
В префиксе кетогруппа называется оксо-, а альдегидная группа – формил- .
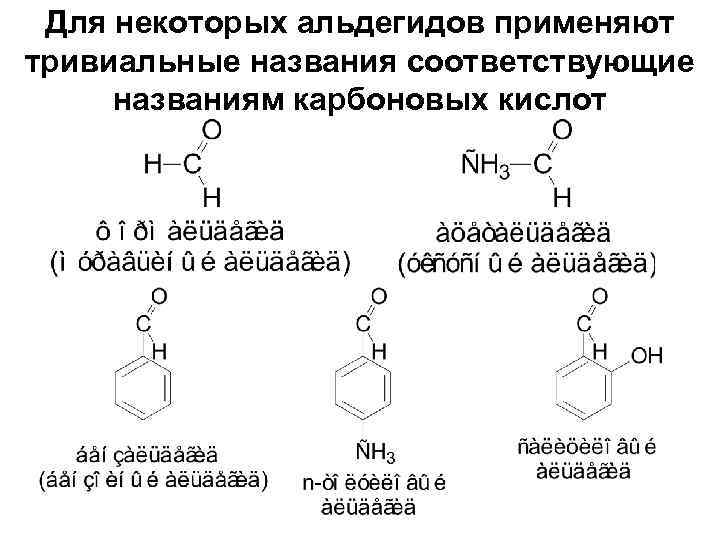
Для некоторых альдегидов применяют тривиальные названия соответствующие названиям карбоновых кислот
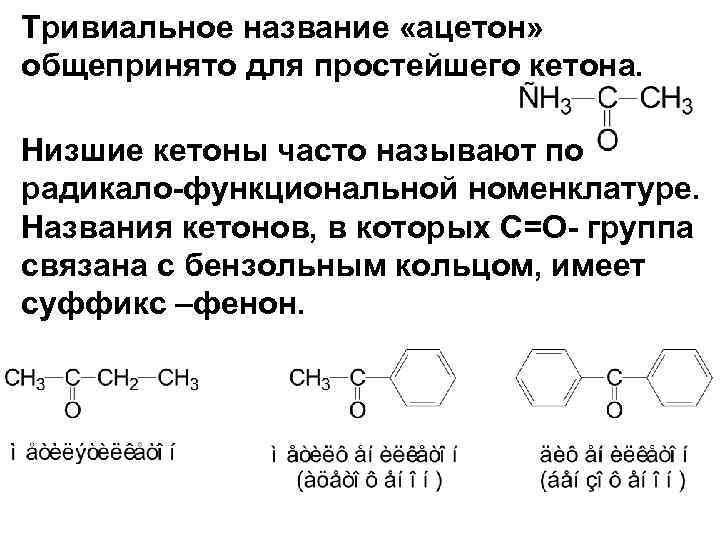
Тривиальное название «ацетон» общепринято для простейшего кетона. Низшие кетоны часто называют по радикало-функциональной номенклатуре. Названия кетонов, в которых С=O- группа связана с бензольным кольцом, имеет суффикс –фенон.
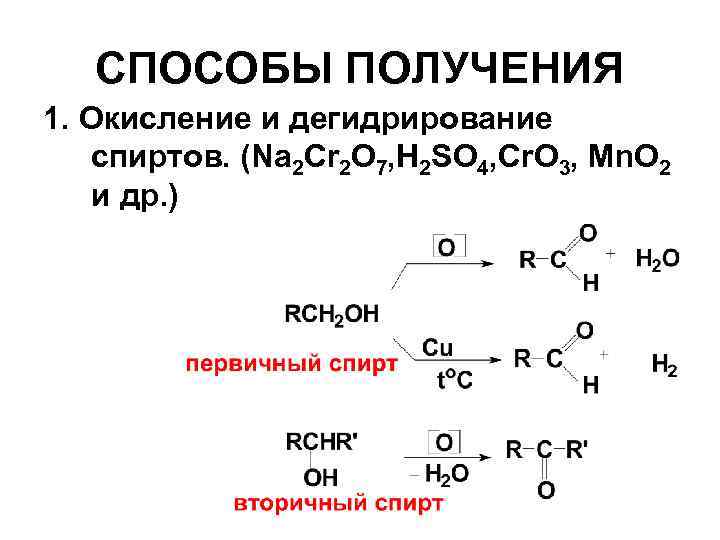
СПОСОБЫ ПОЛУЧЕНИЯ 1. Окисление и дегидрирование спиртов. (Na 2 Cr 2 O 7, H 2 SO 4, Cr. O 3, Мn. O 2 и др. )
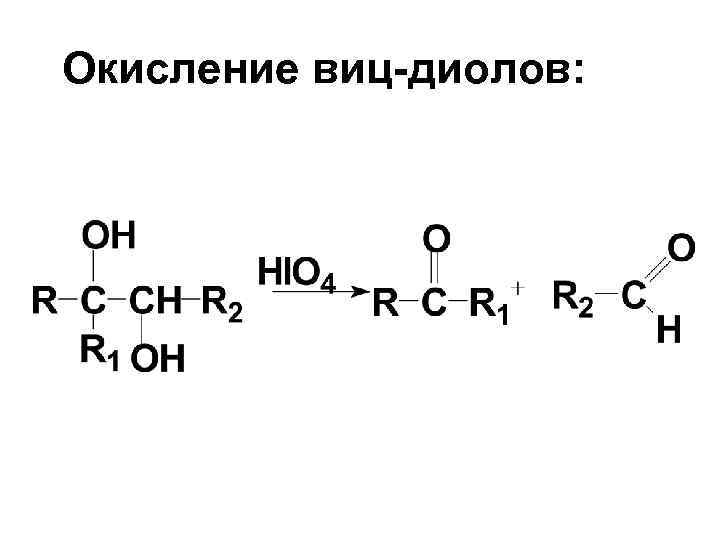
Окисление виц-диолов:
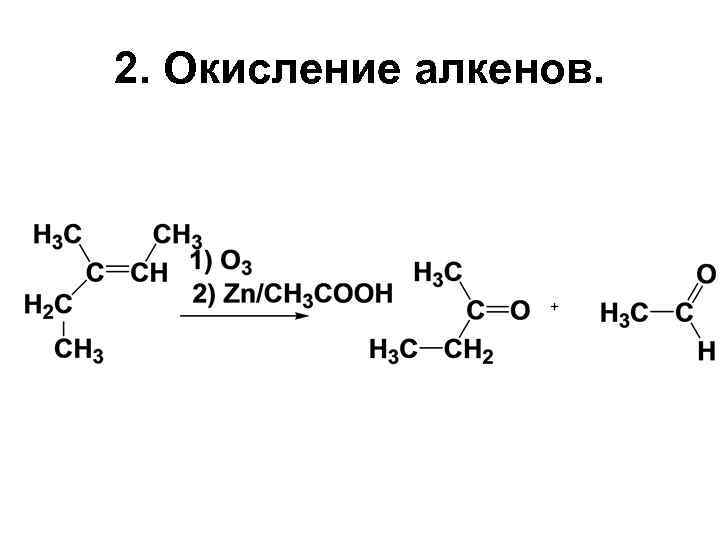
2. Окисление алкенов.

При окислении в присутствии солей Pd углеродная цепь не разрушается:
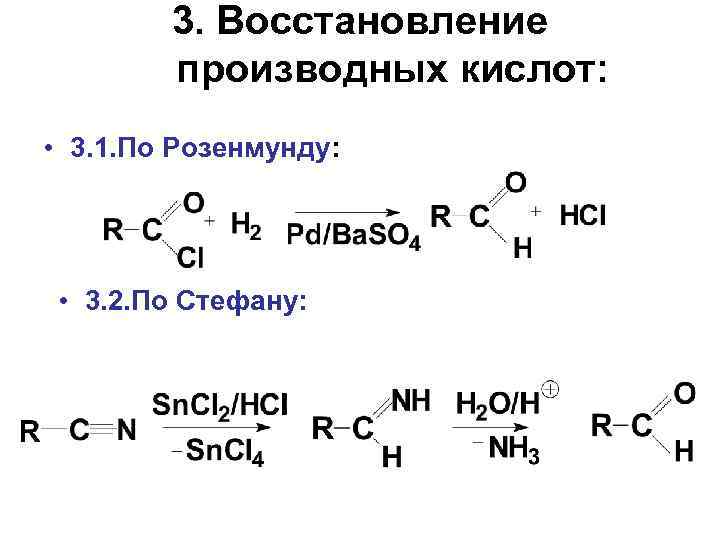
3. Восстановление производных кислот: • 3. 1. По Розенмунду: • 3. 2. По Стефану:
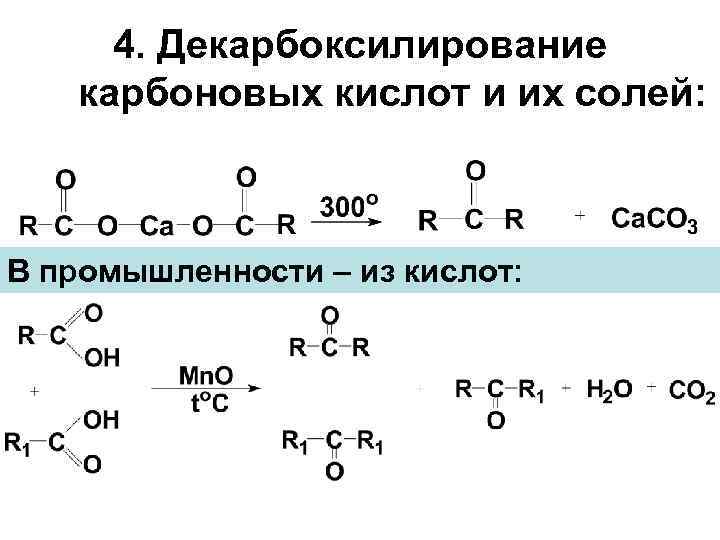
4. Декарбоксилирование карбоновых кислот и их солей: В промышленности – из кислот:
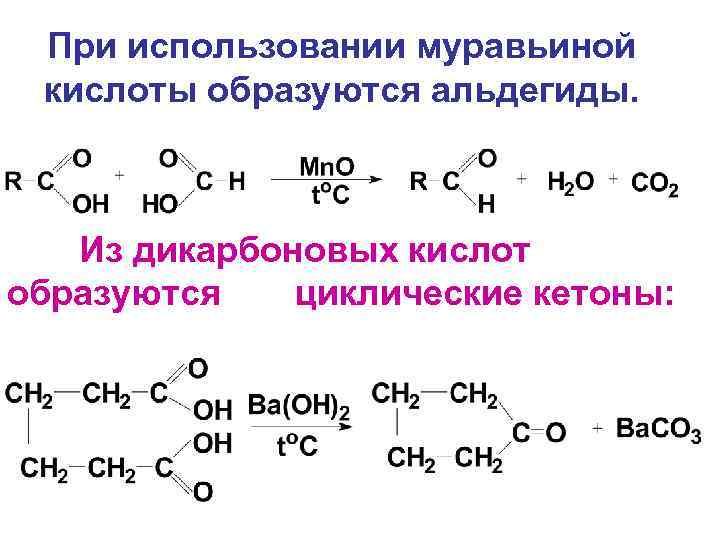
При использовании муравьиной кислоты образуются альдегиды. Из дикарбоновых кислот образуются циклические кетоны:
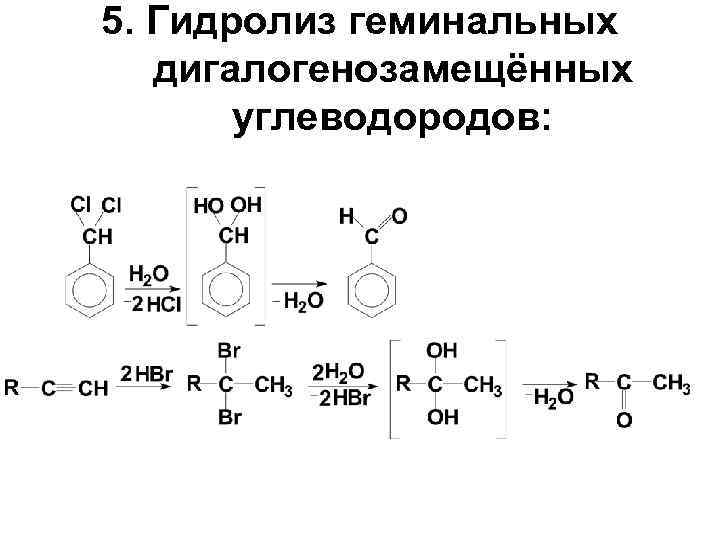
5. Гидролиз геминальных дигалогенозамещённых углеводородов:


6. Гидратация по Кучерову:

7. Оксосинтез:

8. Cинтез ароматических альдегидов и кетонов: • 8. 1. Окисление боковой цепи аренов.

8. 2. Ацилирование по Фриделю. Крафтсу:
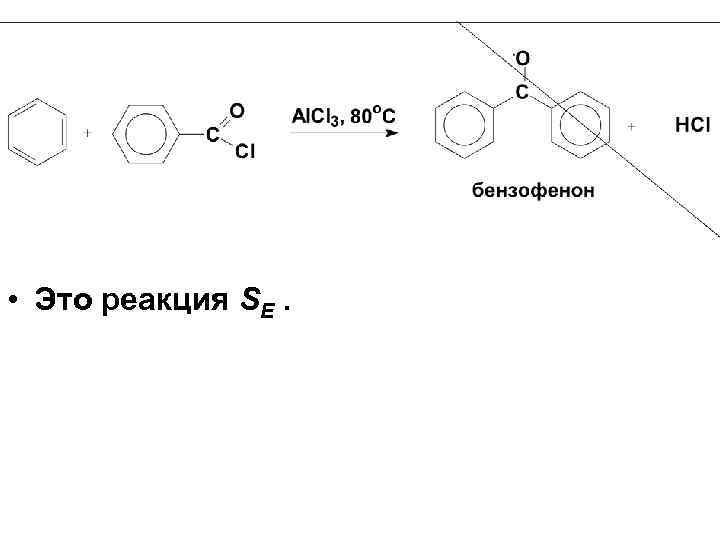
• Это реакция SE.
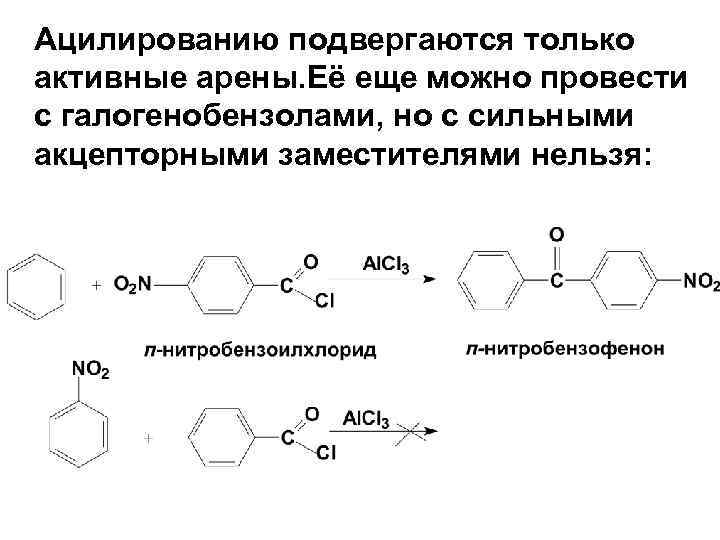
Ацилированию подвергаются только активные арены. Её еще можно провести с галогенобензолами, но с сильными акцепторными заместителями нельзя:
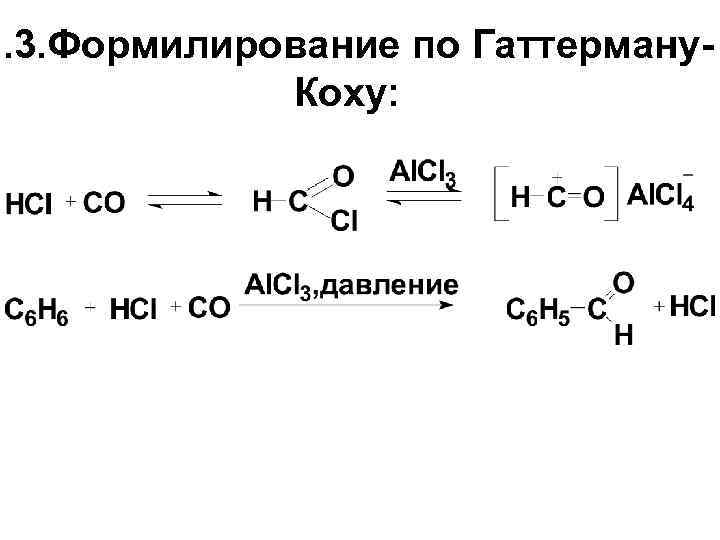
8. 3. Формилирование по Гаттерману. Коху:

8. 4. Формилирование по Реймару-Тиману:

8. 5. Пергруппировка Фриса:

ФИЗИЧЕСКИЕ СВОЙСТВА • Низшие алифатические альдегиды и кетоны кроме газообразного формальдегида, являются подвижными жидкостями. • Первые представители (формальдегид, ацетон) растроримы в воде за счет образования с ней водородных связей. С увеличением R растворимость снижается, ароматические плохо растворимы. • Альдегиды и кетоны имеют более низкие Т. кип. , чем спирты и кислоты, так как не образуют ассоциатов.
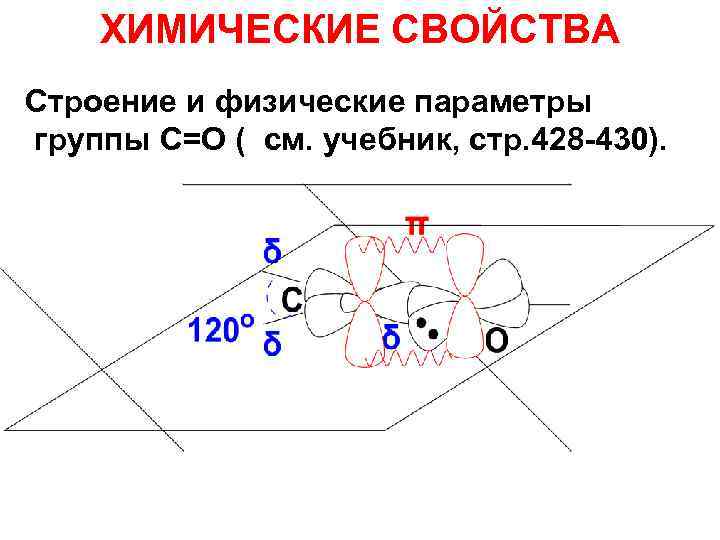
ХИМИЧЕСКИЕ СВОЙСТВА Строение и физические параметры группы С=О ( см. учебник, стр. 428 -430).

Отличие С=О связи от С=С связи • Отличие С=О связи от С=С связи – её высокая полярность. • Е связи С=О>Е связи С=С, • длина связи меньше (0, 121 нм<134 нм). • Colby/ketone.

Реакционная способность обусловлена:

• Электрофильный центр участвует в реакциях нуклеофильного присоединения (AN); • Основный центр участвует в кислотном катализе в реакциях присоединения, а также процессах енолизации; • α- СН-кислотный центр – при его участии протекают многие реакции, в частности реакции конденсации. • Связь С-Н в альдегидной группе разрывается при окислении. • Ненасыщенные и ароматические карбонильные соединения реагируют по С=С и Ar-ядру.

1. Реакции нуклеофильного присоединения. Идут по одной из двух схем:

• Большинство реакций AN обратимы. • Электронодонорные заместители в R повышают реакционную способность карбонильных соединений, электронодонорные снижают её. Кетоны менее реакционноспособны, чем альдегиды, так как электронодонорное влияние двух R сильнее. • Из-за +М эффекта бензольного кольца ароматические альдегиды и кетоны менее реакционноспособны, чем алифатические.
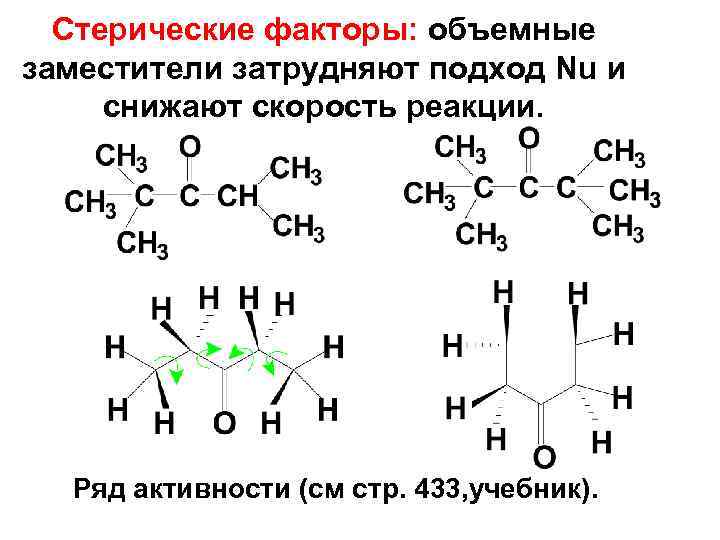
Стерические факторы: объемные заместители затрудняют подход Nu и снижают скорость реакции. Ряд активности (см стр. 433, учебник).

Природа нуклеофила определяет выбор условий реакции. • Сильные нуклеофилы реагируют без Kt, для слабых необходима активация субстрата или реагента. Если активируют реагент, то реакцию осуществляют в условиях основного Kt, если субстрат – в условиях кислотного Kt.

1. 1. Реакции AN с О-содержащими нуклеофилами. • 1. 1. 1. Реакция с Н 2 О. Гидратированы в водном р-ре при 25 о. С Формальдегид – 100%; Ацетальдегид – 51%; Пропаналь – 46%; Ацетон – нет.

1. 1. 2. Реакция со спиртами. Полуацетали не выделяют из-за их неустойчивости.

Исключение – циклические полуацетали из γ- и δ-гидроксиальдегидов

Полуацетали далее превращаются в ацетали в реакции со второй молекулой спирта: • В кислой среде ацетали подвергаются гидролизу, в щелочной – устойчивы. Поэтому образование ацеталей – метод защиты карбонильной группы.

Кетоны менее активны в реакциях со спиртами, но с 1, 2 -диолами образуют циклические кетали: • Образование циклических ацеталей используется для защиты1, 2 - и 1, 3 - диольных фрагментов в химии углеводов.

1. 2. Реакции AN с серодсодержащими нуклеофилами. Реакция с гидросульфитом натрия. Образование гидросульфитных производных (α-гидроксисульфонатов Na). Под действием кислот или соды бисульфитное производное разлагается с выделением исходного карбонильного соединения. Реакция используется для выявления альдегидов и метилкетонов, а также для очистки альдегидов.

1. 3. Реакции AN с азотсодержащими нуклеофилами. • Нуклеофилы:
Для активации субстрата используют Kt :

1. 3. 1. Реакция с аммиаком и аминами. • Реакция приводит к иминам, которые неустойчивы и полимеризуются:

Восстановительное аминирование: • С аминами образуются N-замещенные имины, которые являются более стабильными, чем продукты с аммиаком.

• Соединения, содержащие хотя бы одну Ar -заместитель обладают большей устойчивостью – их называют основания Шиффа. • Гидролиз замещенных иминов в кислой среде приводит к регенерации исходных альдегида и амина.

1. 3. 2. Реакция с гидразинами. • Образуются гидразоны:
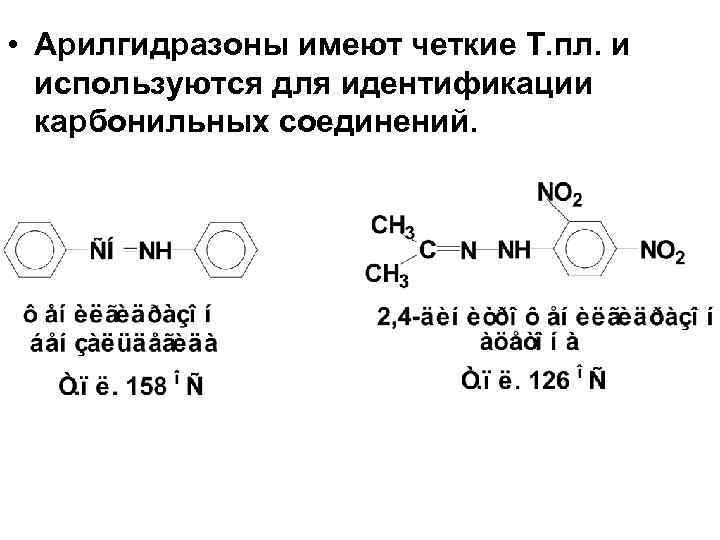
• Арилгидразоны имеют четкие Т. пл. и используются для идентификации карбонильных соединений.

Восстановление по Кижнеру. Вольфу:
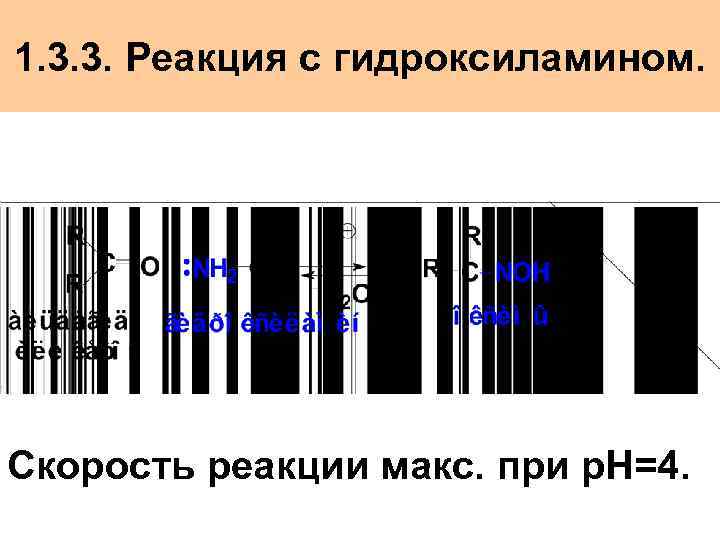
1. 3. 3. Реакция с гидроксиламином. Скорость реакции макс. при р. Н=4.
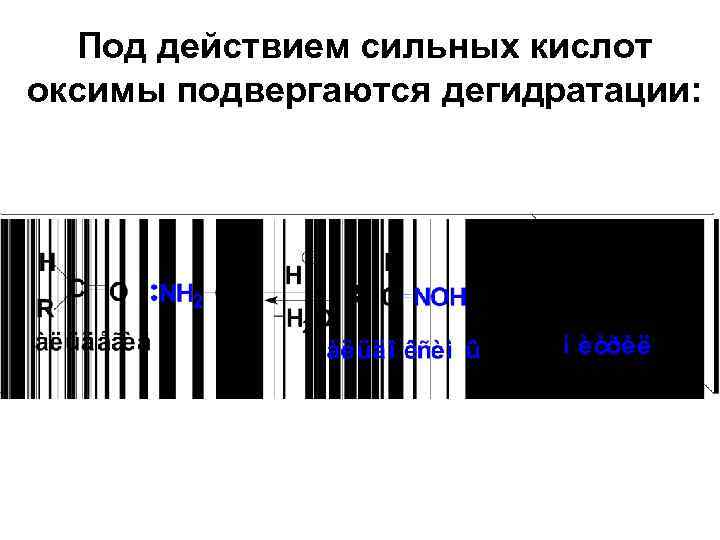
Под действием сильных кислот оксимы подвергаются дегидратации:

Под действием сильных кислот оксимы кетонов претерпевают перегруппировку в амиды кислот (перегруппировку Бекмана): стр. 440 -441, учебник.

Перегруппировка Бекмана используется в промышленности:

1. 4. Реакции AN с углеродсодержащими нуклеофилами. 1. 4. 1. Реакция с HCN. Приводит к образованию гидроксинитрилов и позволяет удлинить углеродную цепь на один атом:

Реакция используется для получения гидроксикарбоновых кислот:

1. 4. 2. Реакция с магнийорганическими соединениями.


2. Реакции конденсации. • К этим реакциям относят реакции присоединении или замещения атома кислорода карбонильной группы с образованием новой С-С связи. В реакциях участвуют карбонильные субстраты и С-Н кислоты, в качестве которых могут выступать и карбонильные соединения:

Карбонильная компонента: альдегиды и кетоны жирного и алифатического ряда. Метиленовая компонента: обладающие С-Н кислотностью альдегиды, кетоны, сложные эфиры, ангидриды кислот, нитросоединения и др. Карбонильные соединения как С-Н кислоты. Стр. 442 -444, учебник.
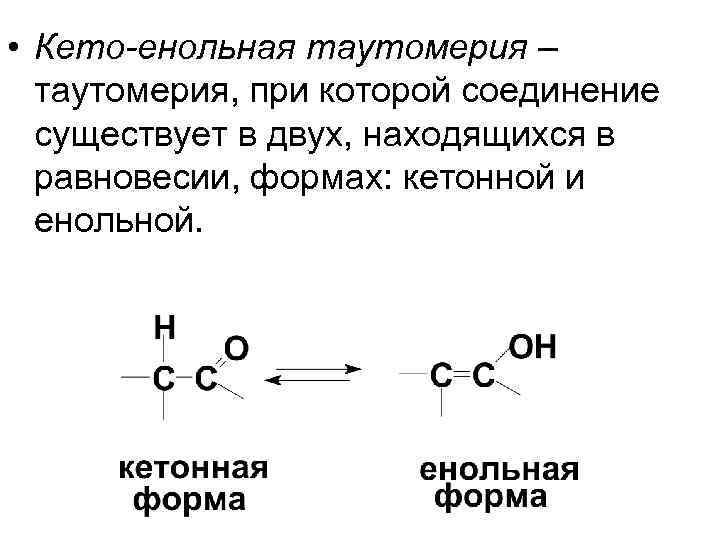
• Кето-енольная таутомерия – таутомерия, при которой соединение существует в двух, находящихся в равновесии, формах: кетонной и енольной.
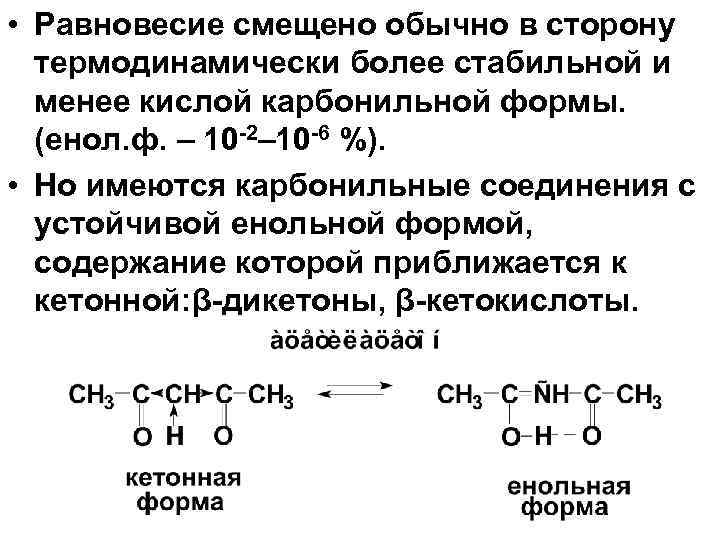
• Равновесие смещено обычно в сторону термодинамически более стабильной и менее кислой карбонильной формы. (енол. ф. – 10 -2– 10 -6 %). • Но имеются карбонильные соединения с устойчивой енольной формой, содержание которой приближается к кетонной: β-дикетоны, β-кетокислоты.

• Енолизация облегчается в присутствии оснований и лимитируется стадией образования карбоаниона: Альдольная конденсация – обратимая реакция, обратный процесс называется альдольным расщеплением (ретроальдольной реакцией).

2. 1. Альдольная и кротоновая конденсации. • Альдольная конденсация. Реакция протекает при действии на альдегиды или кетоны разбавленных щелочей. При этом одна молекула альдегида представляет собой карбонильную компоненту, а другая – метиленовую
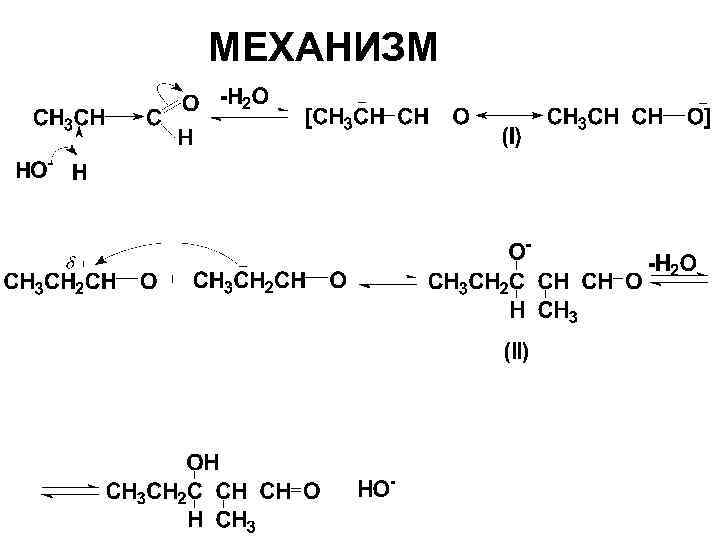
МЕХАНИЗМ

Возможен и кислотный катализ енолизации:
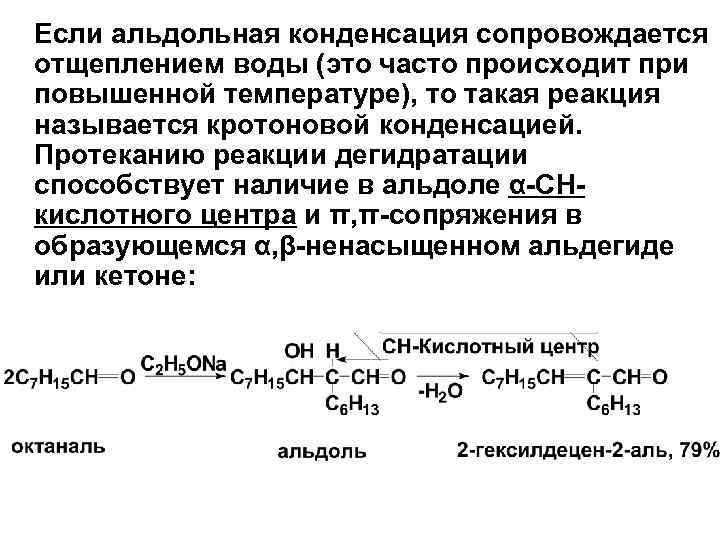
Если альдольная конденсация сопровождается отщеплением воды (это часто происходит при повышенной температуре), то такая реакция называется кротоновой конденсацией. Протеканию реакции дегидратации способствует наличие в альдоле α-СНкислотного центра и π, π-сопряжения в образующемся α, β-ненасыщенном альдегиде или кетоне:

• Реакции альдольной или кротоновой конденсации часто проводятся в смешанном варианте, когда карбонильная и метиленовая компоненты – разные соединения. Карбонильная компонента должна иметь высокую реакционную способность в реакциях нуклеофильного присоединения. Метиленовая компонента должна обладать достатоно высокой СН-кислотностью.
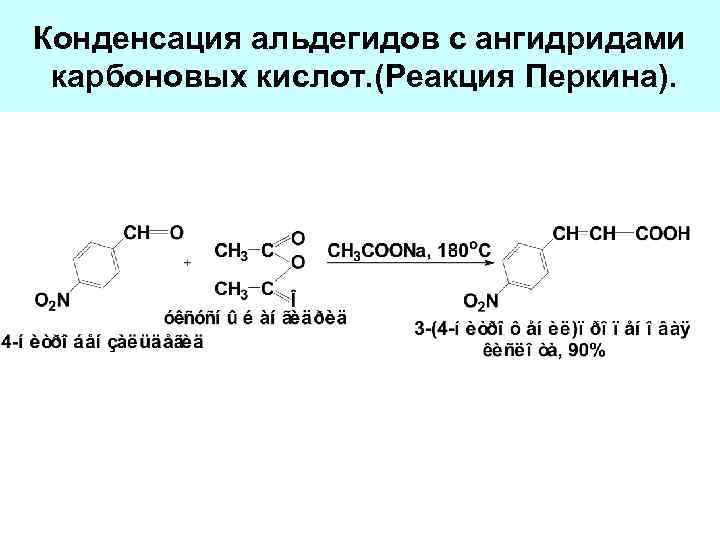
Конденсация альдегидов с ангидридами карбоновых кислот. (Реакция Перкина).

Механизм:
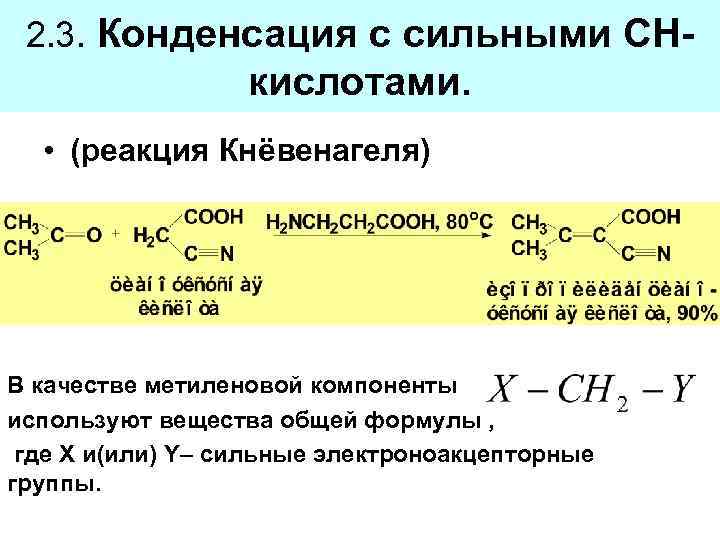
2. 3. Конденсация с сильными СН- кислотами. • (реакция Кнёвенагеля) В качестве метиленовой компоненты используют вещества общей формулы , где X и(или) Y– сильные электроноакцепторные группы.
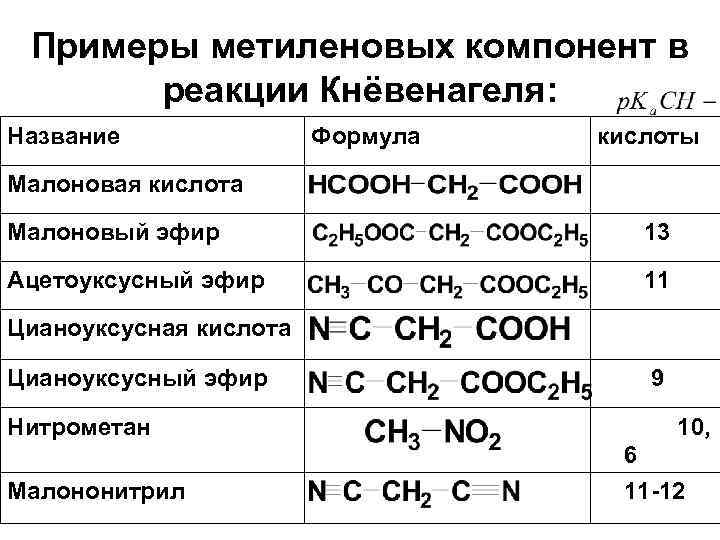
Примеры метиленовых компонент в реакции Кнёвенагеля: Название Формула кислоты Малоновая кислота Малоновый эфир 13 Ацетоуксусный эфир 11 Цианоуксусная кислота Цианоуксусный эфир Нитрометан Малононитрил 9 10, 6 11 -12
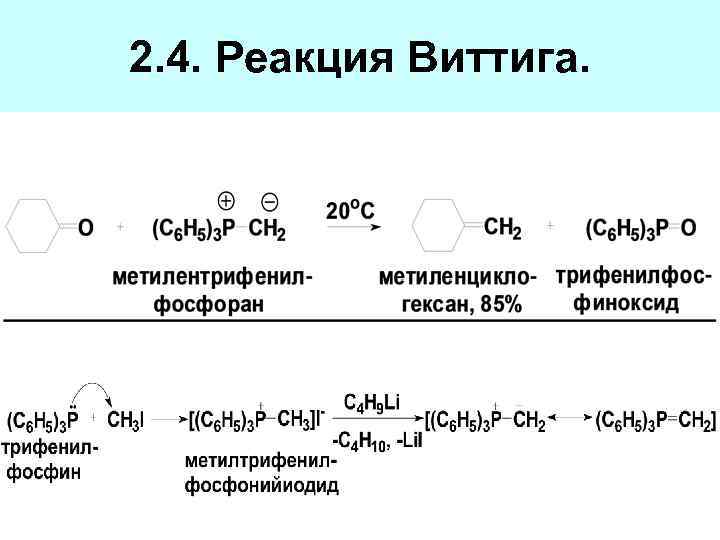
2. 4. Реакция Виттига.

Механизм реакции Виттига:

3. Реакции окисления и восстановления. 3. 1. Диспропорционирование. Реакция Канниццаро:
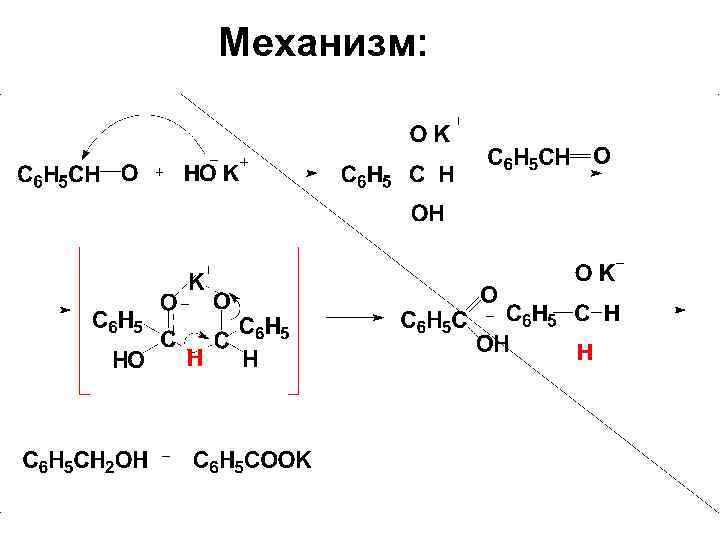
Механизм:
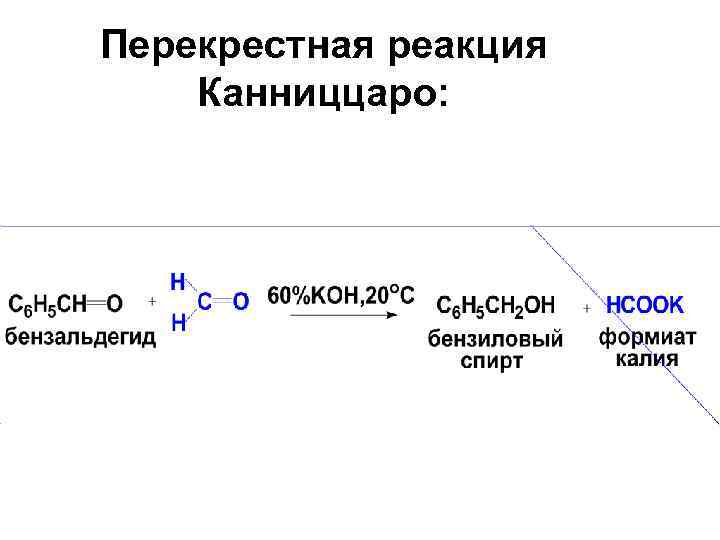
Перекрестная реакция Канниццаро:

3. 2. Реакция Тищенко: • Этому превращению подвергаются альдегиды, имеющие С-Н кислотный атом углерода.

3. 3. Восстановление комплексными гидридами металлов: • алюмогидрид лития Li. Al. H 4, • борогидрид натрия Na. BH 4.

Механизм:
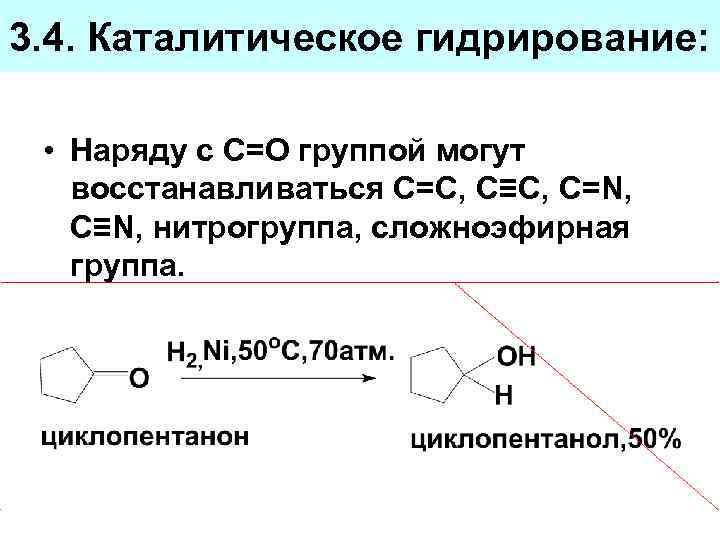
3. 4. Каталитическое гидрирование: • Наряду с С=О группой могут восстанавливаться С=С, C≡C, C=N, C≡N, нитрогруппа, сложноэфирная группа.

3. 5. Восстановление по Клеменсену.

3. 6. Восстановление по Кижнеру. Вольфу.
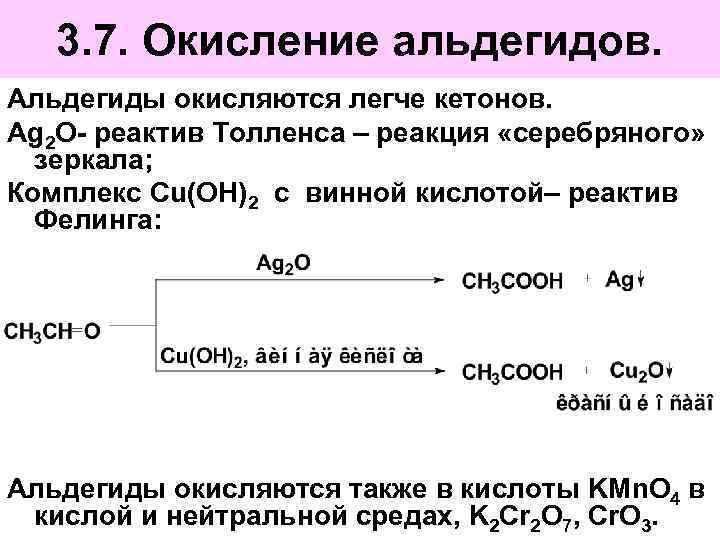
3. 7. Окисление альдегидов. Альдегиды окисляются легче кетонов. Ag 2 O- реактив Толленса – реакция «серебряного» зеркала; Комплекс Cu(OH)2 с винной кислотой– реактив Фелинга: Альдегиды окисляются также в кислоты KMn. O 4 в кислой и нейтральной средах, K 2 Cr 2 O 7, Сr. O 3.

• Кетоны окисляются в зависимости от окислителя в соединения разных классов, их окисление сопровождается в основном разрывом углеродного скелета. • Кетоны окисляются пероксидными соединениями в сложные эфиры. Реакция Байера-Виллигера:
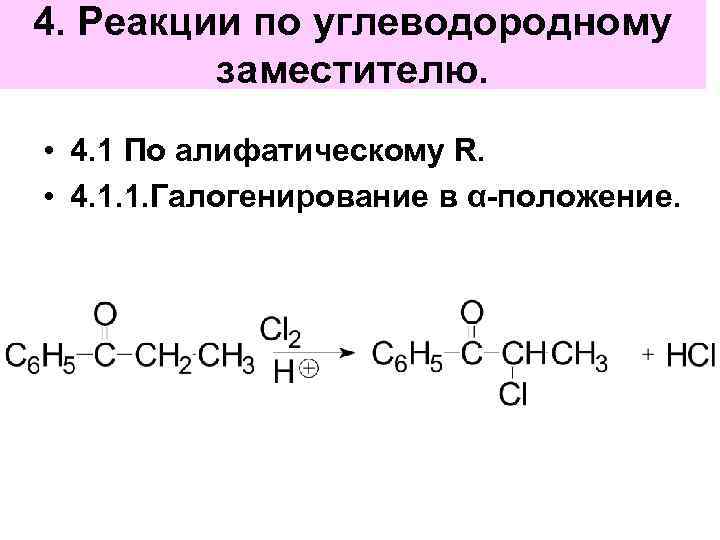
4. Реакции по углеводородному заместителю. • 4. 1 По алифатическому R. • 4. 1. 1. Галогенирование в α-положение.
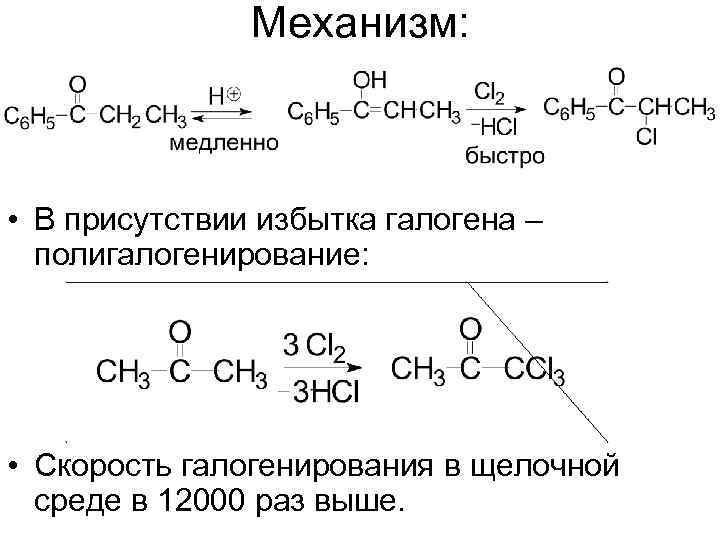
Механизм: • В присутствии избытка галогена – полигалогенирование: • Скорость галогенирования в щелочной среде в 12000 раз выше.
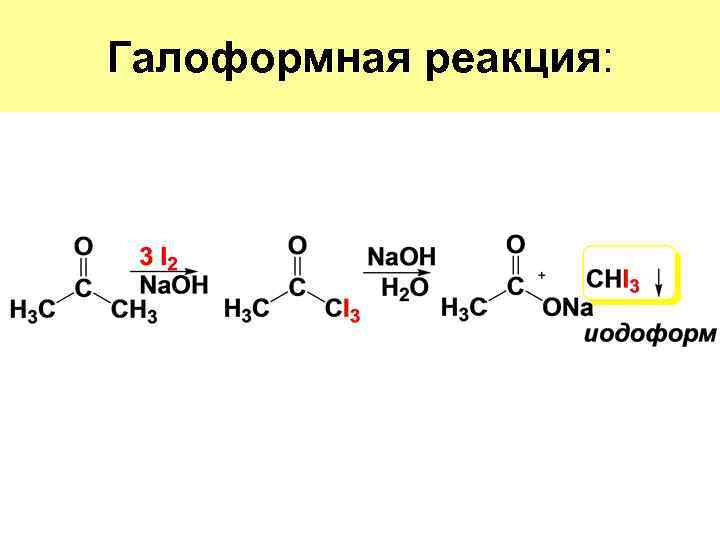
Галоформная реакция:

• 4. 1. 2. Карбонильная группа оказывает сильное влияние на кратные связи, если они оказываются в α, β-положениях. (Учебник, стр. 456 -457). • Colby/Enones.
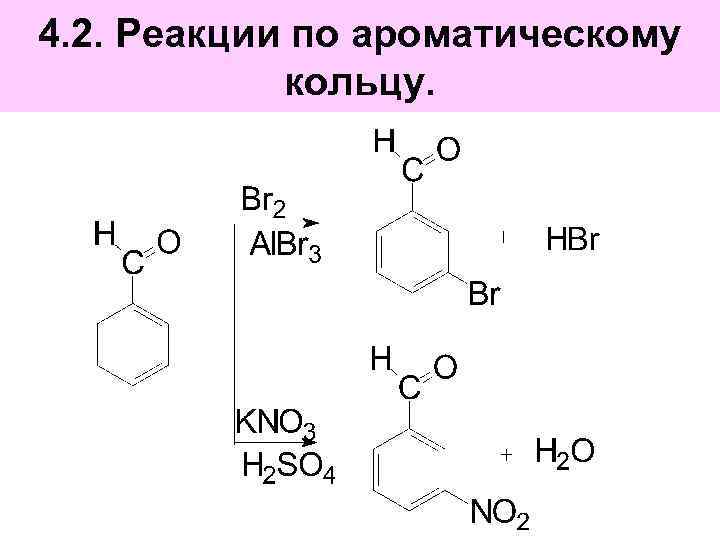
4. 2. Реакции по ароматическому кольцу.
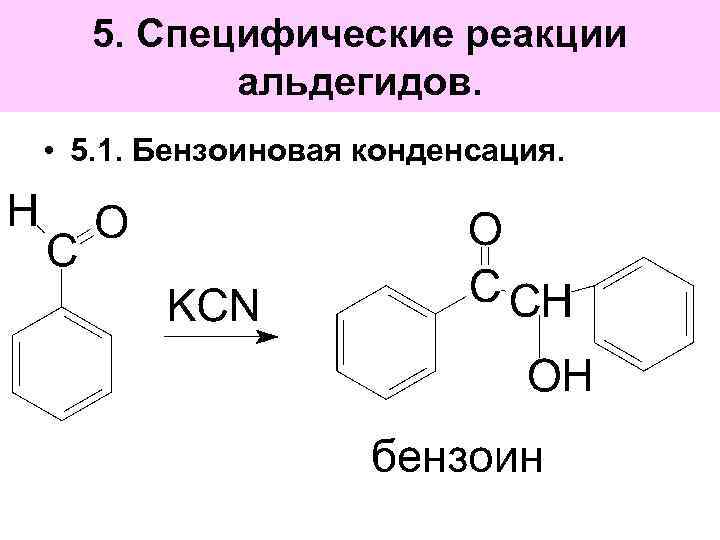
5. Специфические реакции альдегидов. • 5. 1. Бензоиновая конденсация.

Механизм бензоиновой конденсации:
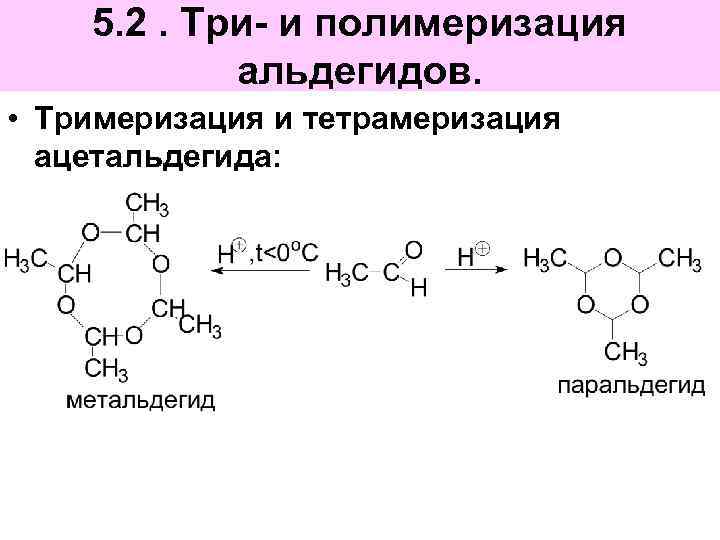
5. 2. Три- и полимеризация альдегидов. • Тримеризация и тетрамеризация ацетальдегида:
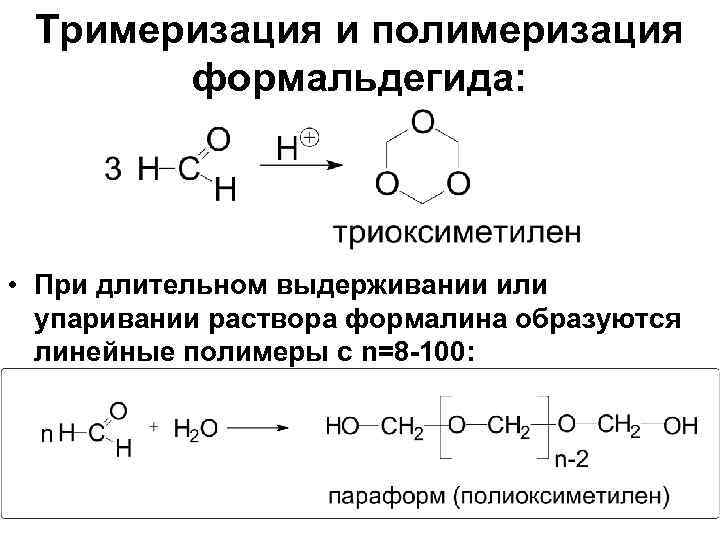
Тримеризация и полимеризация формальдегида: • При длительном выдерживании или упаривании раствора формалина образуются линейные полимеры с n=8 -100:
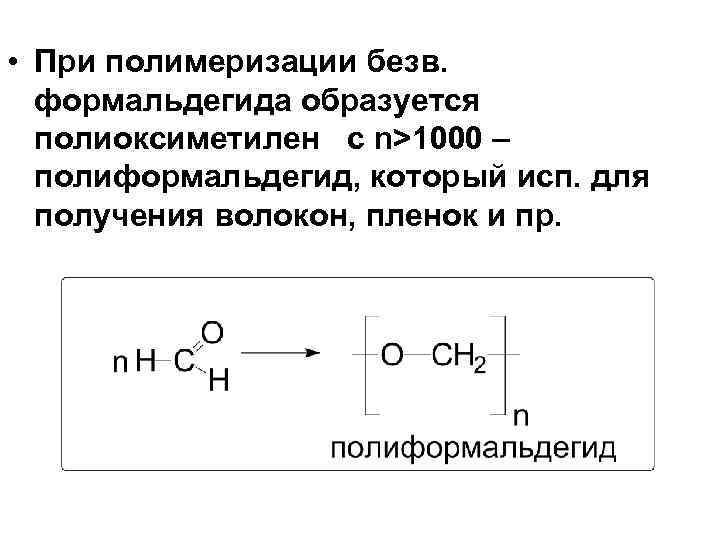
• При полимеризации безв. формальдегида образуется полиоксиметилен с n>1000 – полиформальдегид, который исп. для получения волокон, пленок и пр.
КАРБОНИЛ 2.ppt