
Карбон Вуглець

Знаходження в природі С 0, 14% Карбонатні гірські породи (99%С) Ст. ок. +4 Са. СО 3 – кальцит у вигляді вапняку, мармуру, крейди. Mg. CO 3 – магезит Са. СО 3·Mg. CO 3 – доломіт Fe. СО 3·Mg. CO 3, Zn. CO 3 – важкі шпати Cu 2 CO 3(OH)2 ((Cu. OH)2 CO 3) – малахіт Na 2 CO 3 – сода


Нафта(Сх. Ну), газ(СН 4, С 2 Н 6), вугілля, торф, сланці в біосфері(0, 01%) 200000 млрд. т. в атмосфері(≈ 0, 03% СО 2) 2000 млрд. т. у вільному стані зустрічається у вигляді графіта та алмаза Добування СН 4 + О 2 → С + 2 Н 2 О СН 4 С + 2 Н 2 сажа

С 2 s 22 p 2 С* 2 s 12 p 3 вал. = 2 вал. = 4 Ступінь окиснення С С С -4. . 0. . . +4 С С Утворює ланцюги, цикли С

Алотропні модифікації карбону Графіт має високу тепло- та електропровідність (як метали) ρ= 2, 1÷ 2, 3 г/см 3 tпл. = 4492 о. С(10 МПа) tсубл. = 3800 о. С(за звичайного тиску)
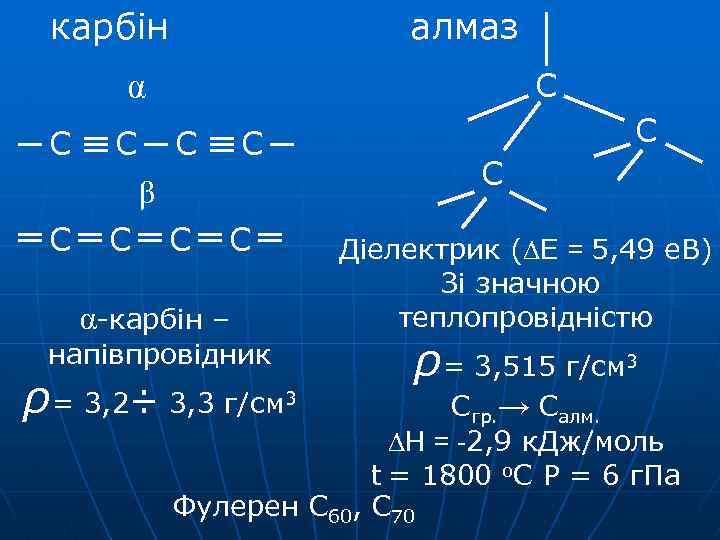
карбін алмаз С α С С β С С α-карбін – напівпровідник ρ= 3, 2÷ 3, 3 г/см 3 С С Діелектрик (∆Е = 5, 49 е. В) Зі значною теплопровідністю ρ= 3, 515 г/см 3 Сгр. → Салм. ∆Н = -2, 9 к. Дж/моль t = 1800 о. С Р = 6 г. Па Фулерен С 60, С 70

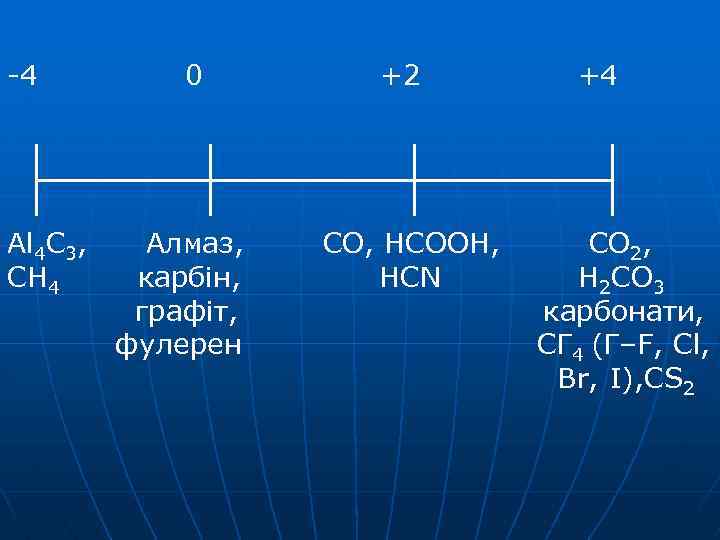
-4 Al 4 C 3, CH 4 0 Алмаз, карбін, графіт, фулерен +2 СО, НСОOH, HCN +4 СО 2, Н 2 СО 3 карбонати, СГ 4 (Г–F, Cl, Br, I), CS 2

C доволі інертний, тому що сполуки є полімерами і щоб розірвати зв’язки потрібні значні затрати енергії Ме + С → Ме. С карбіди 0 0 -4 2 Н 2 + С СН 4 +4 С + О 2 → СО 2 C + 2 S → СS 2 2 C + N 2 → С 2 N 2 диціан С + 2 F 2 → СF 4 (тільки з F 2) 3 С + 4 НNO 3(к. ) 3 СО 2 + 4 NO + 2 H 2 O

КАРБІДИ МЕТАЛІВ s- i p- Ме d - Me Ca+2 C→Ca. C 2 Fe 3 C(цементит), WC, W 2 C, Ti. C, Cr 3 C 2, Mo. C, >20000 Ca. O+3 C Ca. C 2+CO металевий зв’язок, проводять 4 Al + 3 C → Al 4 C 3 електричний струм, малоактивні, з водою 2 Be + C → Be 2 C не взаємодіють, тугоплавкі. Ca. C 2+2 H 2 O→Ca(OH)2+C 2 H 2↑ Ca. C 2 – ацетиленід Al 4 C 3+12 H 2 O→ 4 Al(OH)3+3 CH 4 Al 4 C 3 - метанід
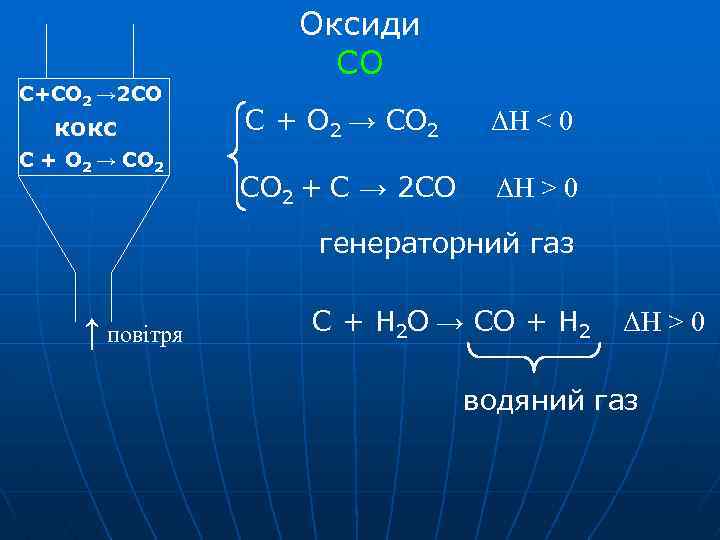
С+CО 2 → 2 СО кокс С + О 2 → СО 2 Оксиди СО С + О 2 → СО 2 ΔН < 0 СО 2 + С → 2 СО ΔН > 0 генераторний газ ↑ повітря С + H 2 О → СО + H 2 ΔН > 0 водяний газ
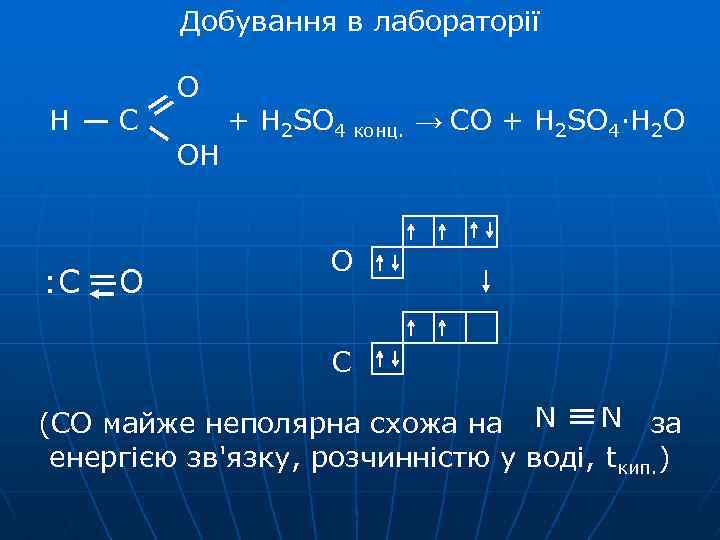
Добування в лабораторії Н С О ОН : С О + H 2 SO 4 конц. → CO + H 2 SO 4·H 2 O O C N за (СО майже неполярна схожа на N енергією зв'язку, розчинністю у воді, tкип. )
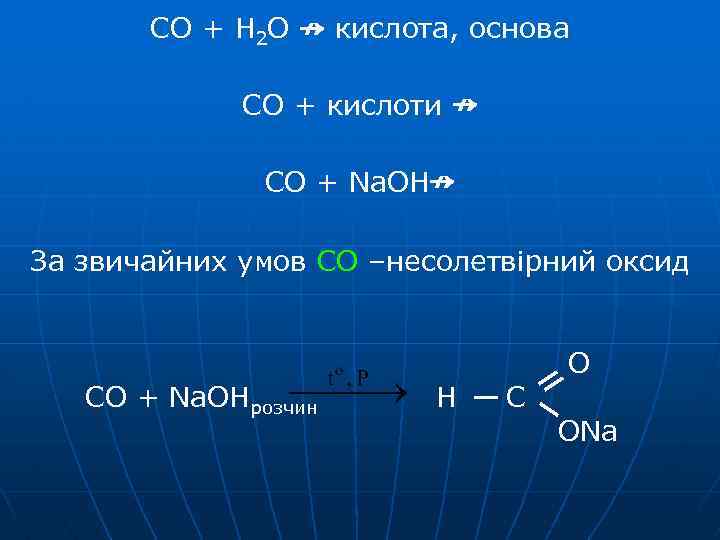
CO + H 2 O ↛ кислота, основа CO + кислоти ↛ CO + Na. OH↛ За звичайних умов СО –несолетвірний оксид CO + Na. OHрозчин Н С О ОNa

+2 CO – типовий відновник +2 +4 СО + О 2 → СО 2 ΔН < 0 СО + Сl 2 → COCl 2 (фосген) 3 CO + Fe 2 O 3 → 2 Fe + 3 CO 2 CO + H 2 O CO 2↑ + H 2↑

4 CO +Ni ⇆ Ni(CO)4 карбоніл 5 CO + Fe Fe(CO)5 СО – донор електронів Розкладом карбонілів отримують метали високої чистоти CO + NH 3 H 2 O + HCN ціановоднева) кислота

СО 2 в промисловості Ca. CO 3 Ca. O + CO 2 в лабораторії: Ca. CO 3 + 2 HCl → Ca. Cl 2 + CO 2↑ + H 2 O O π σ C π σ O молекула неполярна CO 2 – безбарвний газ, важчий за повітря “сухий лід” tсубл. = -78, 48 о. С

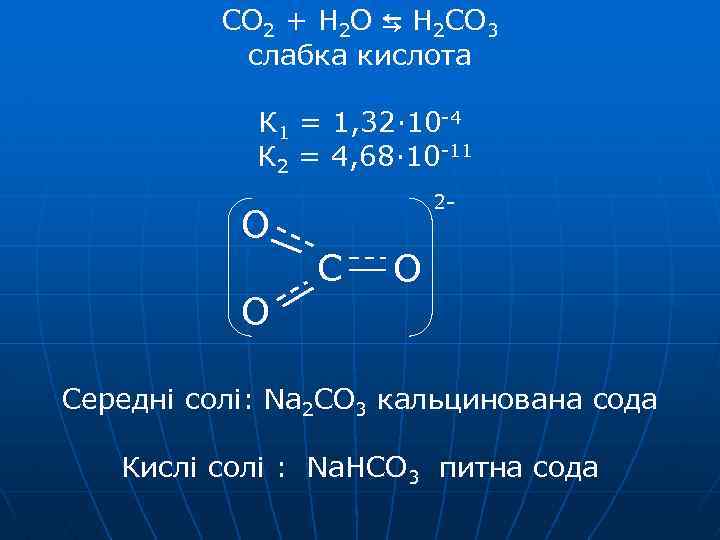
CO 2 + H 2 O ⇆ H 2 CO 3 слабка кислота К 1 = 1, 32· 10 -4 К 2 = 4, 68· 10 -11 О О 2 - С О Середні солі: Na 2 CO 3 кальцинована cода Кислі солі : Na. HCO 3 питна сода

Розчинними є лише карбонати лужних металів(крім Li 2 CO 3) та амонію. Розчинні солі у водних розчинах гідролізують Ca. Cl 2 + Na 2 CO 3 → Ca. CO 3↓ + 2 Na. Cl 2+ 2 - Ca + CO 3 → Ca. CO 3↓ 2 Cu. Cl 2 + 2 Na 2 CO 3 + Н 2 О → (Cu. ОН)2 CO 3↓ +CO 2↑ +4 Na. Cl 2+ 2 - 2 Cu + 2 CO 3 + Н 2 О → (Cu. ОН)2 CO 3↓ +CO 2↑ Cr 2(CO 3)3 Al 2(CO 3)3 не існують
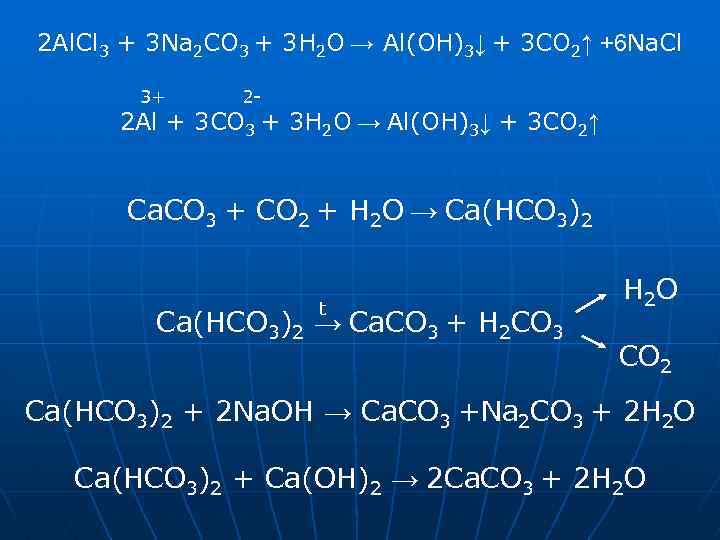
2 Al. Cl 3 + 3 Na 2 CO 3 + 3 Н 2 О → Al(ОН)3↓ + 3 CO 2↑ +6 Na. Cl 3+ 2 - 2 Al + 3 CO 3 + 3 Н 2 О → Al(ОН)3↓ + 3 CO 2↑ Ca. CO 3 + CO 2 + Н 2 О → Ca(HCO 3)2 t Ca(HCO 3)2 → Ca. CO 3 + H 2 СO 3 Н 2 О СO 2 Ca(HCO 3)2 + 2 Na. OH → Ca. CO 3 +Na 2 CO 3 + 2 Н 2 О Ca(HCO 3)2 + Ca(OH)2 → 2 Ca. CO 3 + 2 Н 2 О

+4 CO 2 – найвищий ступінь окиснення, але окисні властивості виражені дуже слабо +4 0 Mg + CO 2 → 2 Mg. O + C +4 +2 C + CO 2 → 2 CO CO 2 – застосовують у вогнегасниках


Сполуки з сульфуром СН 4 + 4 S → CS 2 + H 2 S C + 2 S → CS 2 сірковуглець Добрий розчинник для жирів, олій, восків, смол, каучуків, а також для сірки, фосфору, йоду, тощо, у воді він розчиняється погано, зі спиртом змішується у будь-яких співвідношеннях. Його застосовують як розчинник, та екстрагент, а також для боротьби зі шкідниками, але основну масу сірковуглецю витрачають для одержання віскозного шовку. Отруйний, вогненебезпечний.

CS 2 – безбарвна рідина, tкип. = 46, 2 о. С молекула лінійна, неполярна CS 2 – кислотний сульфід CS 2 + Na 2 S → Na 2 CS 3 кислота тіокарбонат основа CO 2 + Na 2 О → Na 2 CО 3 Na 2 CS 3 + 2 HCl карбонат H 2 CS 3 + 2 Na. Cl тіовугільна кислота К 1 = 2· 10 -3

H 2 CS 3 → H 2 S + CS 2 найстійкіша із тіокислот H 2 CS 3 + 2 H 2 O → CO 2 + 3 H 2 S(повільно) CS 2 + 2 H 2 O CO 2 + H 2 S CS 2 – тіоангідрид CS 2 – сильний відновник -2 +4 CS 2 + 3 O 2 → CO 2 + 2 SO 2 -2 0 CS 2 + Cl 2 → S + CCl 4

СПОЛУКИ З ГАЛОГЕНАМИ Фреони СF 4 (tкип. = -128 о. С) та СF 2 Сl 2 вони мають значну теплоту випаровування за низької температури кипіння і застосовуються як робочі речовини холодильних машин. Їх використовують також у виробництві дезодорантів СCl 4 - безбарвна рідина, застосовують як дуже добрий розчинник органічних речовин, його негорючість іноді використовують для гасіння пожеж
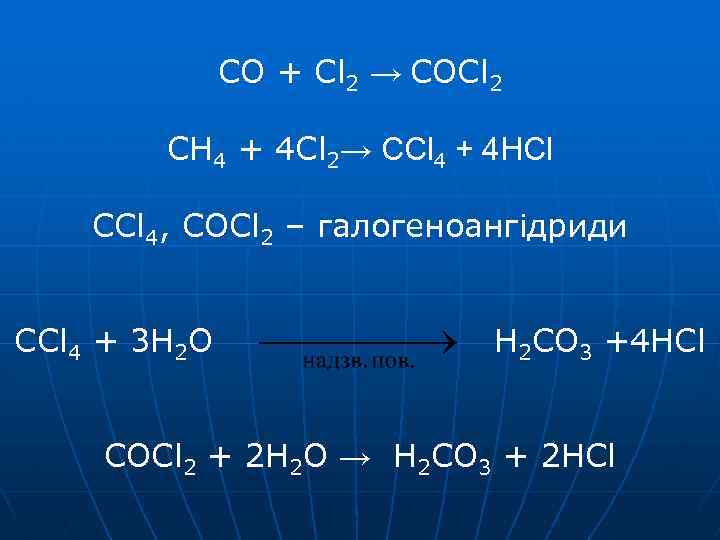
CO + Cl 2 → COCl 2 CH 4 + 4 Cl 2→ CCl 4 + 4 HCl CCl 4, COCl 2 – галогеноангідриди CCl 4 + 3 H 2 O H 2 CO 3 +4 HCl COCl 2 + 2 H 2 O → H 2 CO 3 + 2 HCl

СПОЛУКИ З НІТРОГЕНОМ C 2 N 2 2 Ag. CN 2 Ag + C 2 N 2 Cu. SO 4 + 4 KCN → 2 Cu. CN↓ + C 2 N 2 + 2 K 2 SO 4 Диціан – надзвичайно отруйний газ tкип. = -21 OС
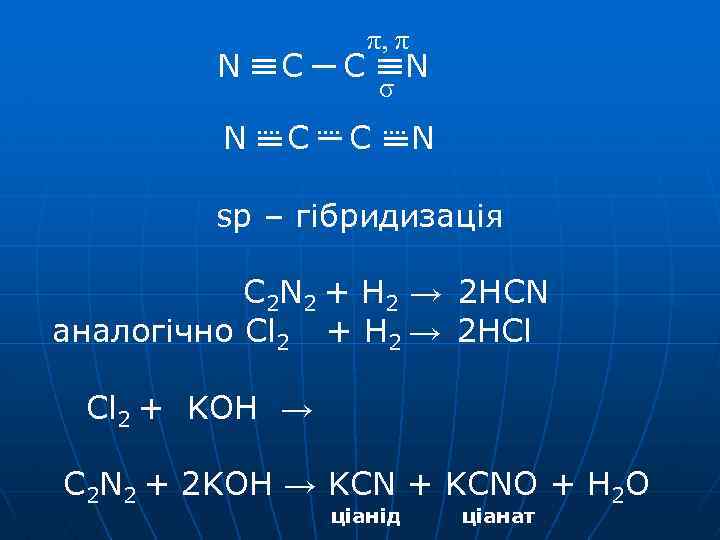
π, π N С С σ N N sp – гібридизація C 2 N 2 + H 2 → 2 HCN аналогічно Cl 2 + H 2 → 2 HCl Cl 2 + KOH → C 2 N 2 + 2 KOH → KCN + KCNO + H 2 O ціанід ціанат
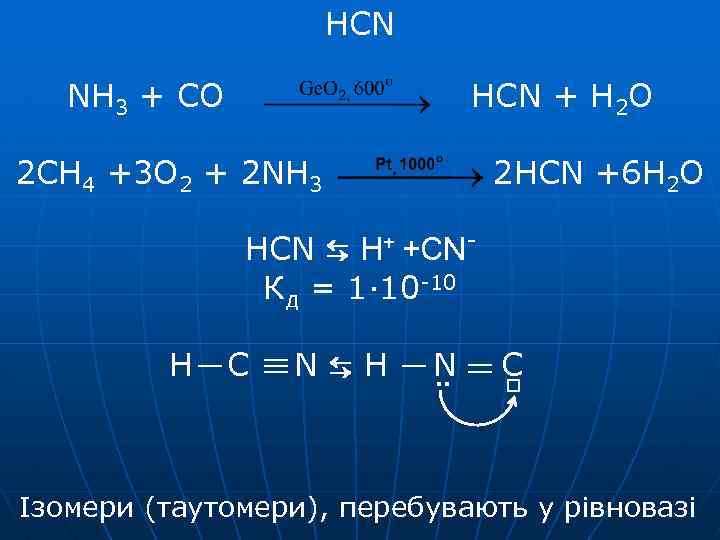
HCN NH 3 + CO HCN + H 2 O 2 CH 4 +3 O 2 + 2 NH 3 2 HCN +6 H 2 O HCN ⇆ H+ +CNКд = 1· 10 -10 H C N⇆H N ¨ C □ Ізомери (таутомери), перебувають у рівновазі

Промислові способи добування солей: K 2 CO 3 + C + 2 NH 3 2 Na. NH 2 + 2 C 2 KCN + 3 H 2 O 2 Na. CN + 3 H 2 O CN- - ліганд сильного поля Fe. Cl 2 + 6 KCN → K 4[Fe(CN)6] + 2 KCl

CN- - має відновні властивості 2 KCN + O 2 → 2 KCNO HOCN Кд≈10 -4 H О C ціанова N⇆H N C ізоціанова О⇆ H О N ¨ C □ “гримуча”

HNСO + H 2 O → CO 2 + NH 3 + HNСO → CO(NH 2)2 NH 4 OCN → CO(NH 2)2 ціанат амонію Ag. ONC, Hg(ONC)2 – фульмінати Hg(ONC)2 - “гримуча ртуть” використовується як детонатор KCN + S KSCN тіоціанат (роданід) калію

H S C N⇆H N C S НSCN - сильна кислота(К=0, 14), тому роданіди лужних металів не гідролізують [Со(NH 3)5 NCS]2+ [Со(NH 3)5 SCN]2+ ізомерія зв'язку Fe. Cl 3 + 6 KSCN → K 3[Fe(SCN)6] + 3 KCl Hg(SCN)2 – тіоціанат Hg 2 Hg(SCN)2 Hg. S + CS 2 + C 3 N 4