Карбоновые кислоты.ppt
- Количество слайдов: 34



Карбо новые кисло ты — класс органических соединений, молекулы которого содержат одну или несколько функциональных карбоксильных групп -COOH. Кислые свойства объясняются тем, что данная группа может сравнительно легко отщеплять протон. За редкими исключениями карбоновые кислоты являются слабыми. Например, у уксусной кислоты CH 3 COOH константа кислотности равна 1, 75· 10 -5. Ди- и трикарбоновые кислоты более сильные, чем монокарбоновые.

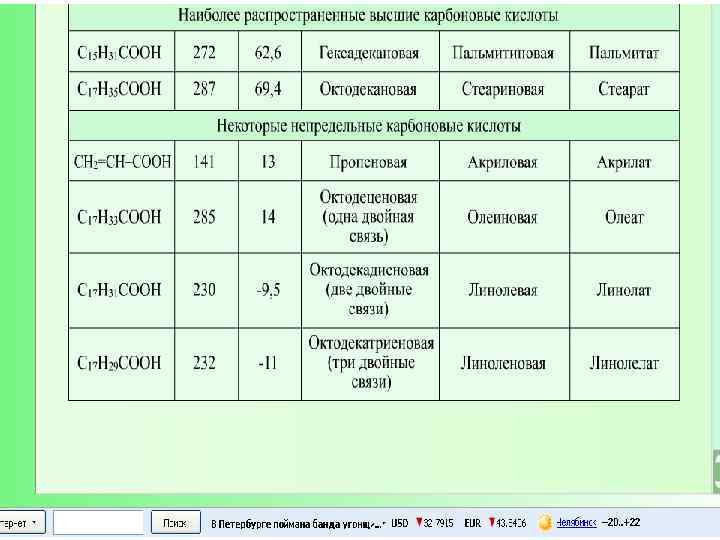
Тривиальные названия муравьиная кислота, (HCOOH ) пропионовая кислота(CH 3 CH 2 COOH ), валериановая кислота(С 4 Н 9 COOH ), пальмитиновая кислота(С 15 Н 31–СООН ), стеариновая кислота(CH 3(CH 2)16 COOH ), щавелевая кислота(C 2 O 4 H 2 СООН ), малоновая кислота(C 3 O 4 H 4 СООН), янтарная кислота(НООС(СН 2)2 СООН ), адипиновая кислота(НООС(СН 2)4 СООН ), лимонная кислота(C 6 H 8 O 7 СООН), яблочная кислота(НООССН(ОН)СН 2 СООН ), D- винная кислота. (2 С 4 Н 6 О 6*2 Н 2 О) уксусная кислота(CH 3 COOH ), масляная кислота(CH 3 CH 2 COOH ), капроновая кислота(С 5 Н 11 COOH), олеиновая кислота(СН(СН 2)7 СООН ),
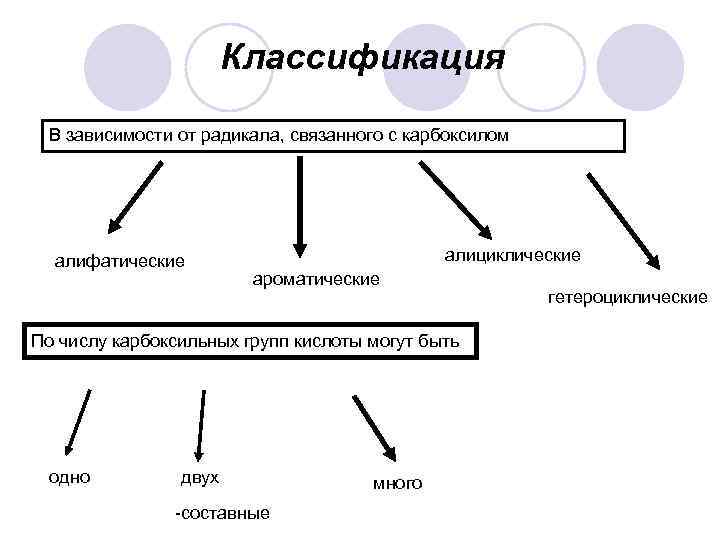
Классификация В зависимости от радикала, связанного с карбоксилом алифатические алициклические ароматические По числу карбоксильных групп кислоты могут быть одно двух -составные много гетероциклические
Низшие карбоновые кислоты — жидкости с острым запахом, хорошо растворимые в воде. С повышением относительной молекулярной массы растворимость кислот в воде уменьшается, а температура кипения повышается. Высшие кислоты, начиная с пеларгоновой (н-нонановой) СН 3 -(СН 2)7 -СООН, — твердые вещества, без запаха, нерастворимые в воде.
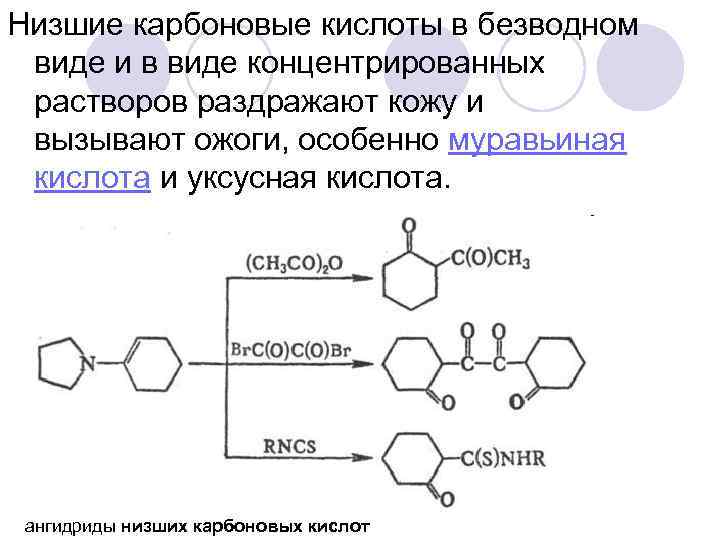
Низшие карбоновые кислоты в безводном виде и в виде концентрированных растворов раздражают кожу и вызывают ожоги, особенно муравьиная кислота и уксусная кислота. ангидриды низших карбоновых кислот


Наиболее важные химические свойства, характерные для большинства карбоновых кислот: 1) Карбоновые кислоты при реакции с металлами или их осно вными гидроксидами дают соли соответствующих металлов: 2 CH 3 COOH + Mg = (CH 3 COO)2 Mg + H 2 Уксусная кислота магний CH 3 COOH + Уксусная кислота Сахароза или средняя соль водород Na. OH = CH 3 COONa + H 2 O гидроксид ацетат натрия вода

Также карбоновые кислоты могут вытеснять более слабую кислоту из её соли, например: CH 3 COOH + Na. HCO 3 = CH 3 COONa + H 2 CO 3 (потом H 2 CO 3 разлагается на углекислый газ и воду)

2) Карбоновые кислоты в присутствии кислого катализатора реагируют со спиртами, образуя сложные эфиры (реакция этерификации): CH 3 COOH + СН 3 СН 2 ОН = Уксусная кислота этанол CH 3 COOCH 2 СН 3 + H 2 O Карбоновая кислота вода

3) При нагревании аммонийных солей карбоновых кислот образуются их амиды: CH 3 COONH 4 = CH 3 CONH 2 + H 2 O ацетат аммония Ацетамид вода

Под действием SOCl 2(Тионилхлорида ) карбоновые кислоты превращаются в соответствующие хлорангидриды. CH 3 COOH + SOCl 2 = CH 3 COCl + HCl +SO 2 Хлороводород УКСУСНАЯ КИСЛОТА Тионилхлорид Ацетилхлорид Диоксид серы

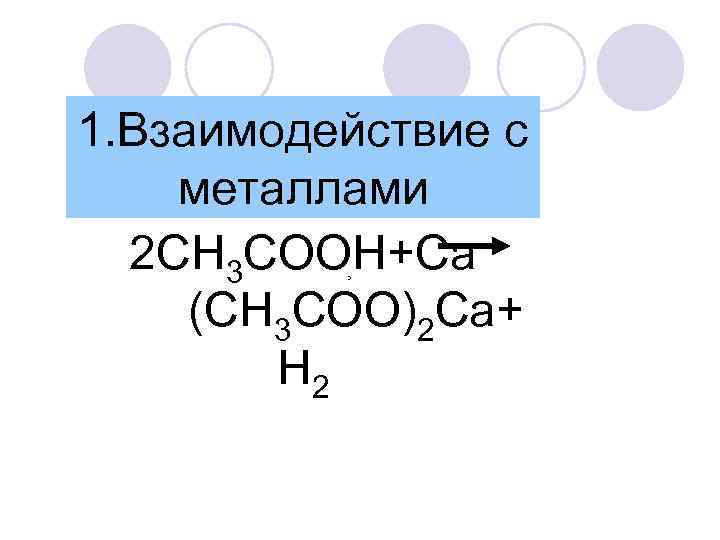
1. Взаимодействие с металлами 2 CH 3 COOH+Ca (CH 3 COO)2 Ca+ H 2
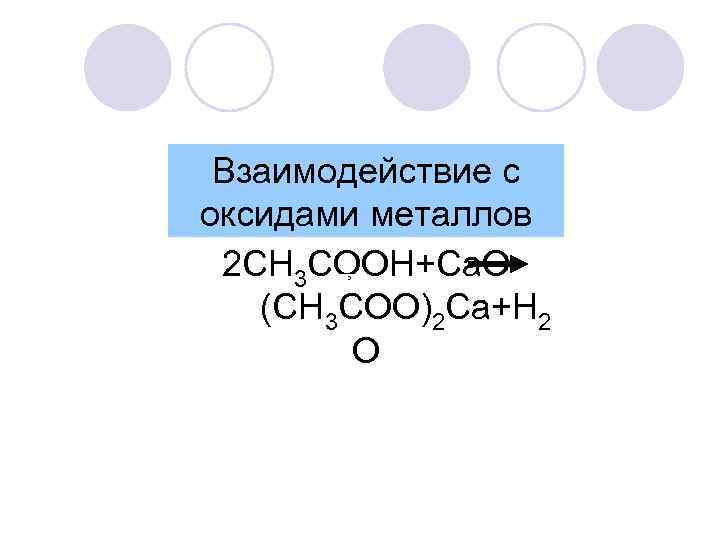
Взаимодействие с оксидами металлов 2 CH 3 COOH+Ca. O (CH 3 COO)2 Ca+H 2 O
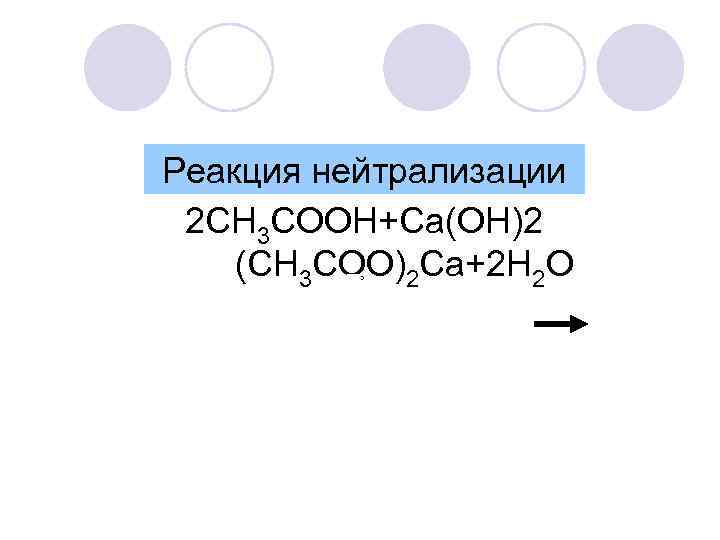
Реакция нейтрализации 2 CH 3 COOH+Ca(OH)2 (CH 3 COO)2 Ca+2 H 2 O
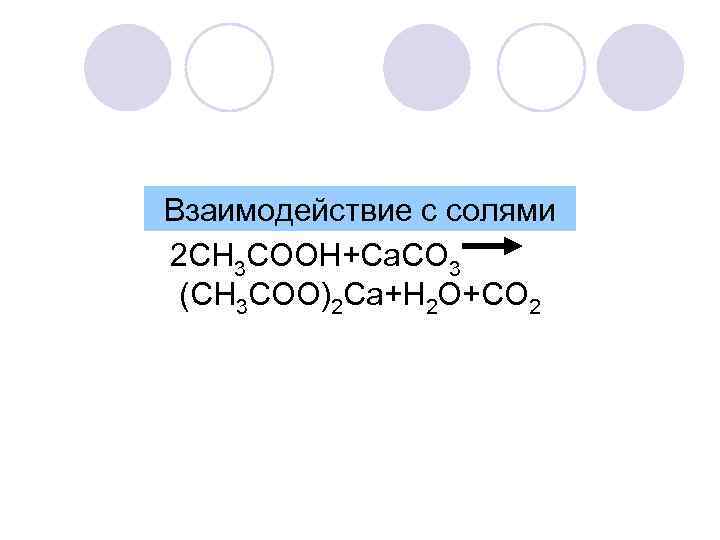
Взаимодействие с солями 2 CH 3 COOH+Ca. CO 3 (CH 3 COO)2 Ca+H 2 O+CO 2
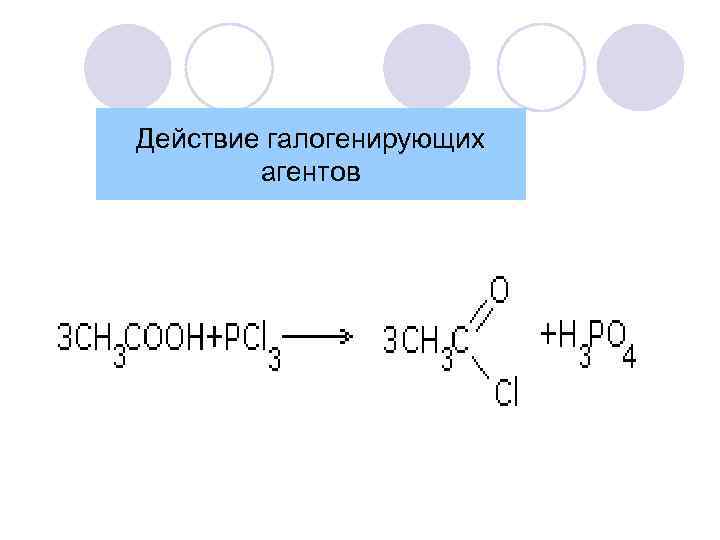
Действие галогенирующих агентов
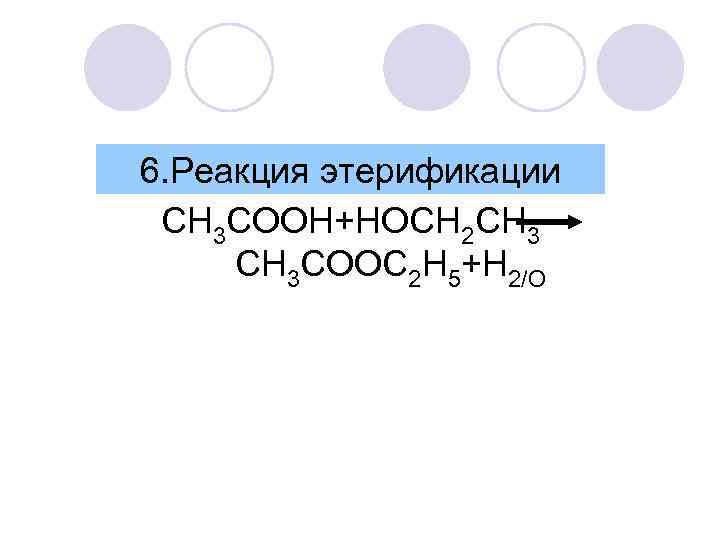
6. Реакция этерификации CH 3 COOH+HOСH 2 CH 3 CH 3 COOC 2 H 5+H 2/O

Галогенирование кислот CH 3 COOH+Br 2 CH 2 Br. COOH
Окисление спиртов. Окисление Альдегидов.

широко распространены в природе в свободном состоянии и в виде производных (главным образом сложных эфиров). Так, в летучем масле герани содержится пеларгоновая кислота, в лимонах - лимонная. В состав животных и растительных жиров и масел входят глицериды высших нормальных К. к. жирного ряда, из которых преобладают пальмитиновая кислота, стеариновая кислота и олеиновая кислота.


К. к. , их производные, а также многочисленные соединения, содержащие наряду с карбоксильной иные функциональные группы (например, аминокислоты, оксикислоты и др. ), имеют большое биологическое значение и находят разнообразное практическое применение.

Муравьиную и уксусную кислоты, например, применяют при крашении и печатании тканей;

уксусную кислоту и уксусный ангидрид — в производстве ацетилцеллюлозы.

Аминокислоты входят в состав белков. В медицине используют салициловую кислоту, nаминосалициловую кислоту (ПАСК) и др.

Высшие жирные К. к. широко применяют как сырьё для производства мыла, лаков и красок,

поверхностно-активных веществ, как эмульгаторы в производстве каучуков, как пластификаторы в производстве резин и др.

Адипиновая кислота — один из исходных продуктов в производстве полиамидного волокна (найлона), терефталевая — в производстве полиэфирного волокна (лавсана, терилена), полимерный нитрил акриловой кислоты (орлон) применяют как синтетическое волокно, близкое по свойствам к натуральной шерсти.

Полимеры и сополимеры эфиров метакриловой кислоты используют как органическое стекло.
Карбоновые кислоты.ppt