Заняття7.ppt
- Количество слайдов: 26

КАРБАНІОНИ. МЕТАЛООРГАНІЧНІ СПОЛУКИ (ТРИЛОГІЯ. ЧАСТИНА 2) Сучасні методи органічного синтезу

Способи добування МОС Металювання (Н М) ØПряме металювання Ø Металювання за участі солей металів ØДепротонування за участі основ (зокрема МОС) Переметалювання (М’ М) ØПереметалювання за участі металів ØПереметалювання за участі солей металів ØПереметалювання за участі металоорганічних сполук Обмін галогену та інших груп на метал (Х М) ØВідновлення металом Ø Відновлення за участі солей аніон-радикалів ØОбмін галогену за участі металоорганічних сполук Реакції приєднання до кратних зв’язків ØВідновлення металом 2 ØПриєднання гідридів (псевдо)металів ØПриєднання металоорганічних сполук

Переметалювання (М’ М) Переметалювання за участі металів ØКласичний метод, має велике історичне значення ØM 2 лівіше в ряду активностей металів за М 1 (суттєва різниця) ØM 2 – переважно лужні та лужноземельні метали, M 1 – Sn, Hg ØРеакція досить повільна ØНа практиці використовується рідко 3

Переметалювання (М’ М) Переметалювання за участі солей металів ØНайзагальніший метод добування сполук малоактивних металів та неметалів ØM 2 правіше в ряду активностей металів за М 1 (найчастіше Li, Mg) ØУ випадку М 1 – Li, Mg реакція швидка ØХ – зазвичай галогени, трифлат, алкоксиди ØДуже часто RM 2 генеруються та використовуються in situ ØНеметали: проблеми утворення сумішей продуктів при частковому заміщенні 4
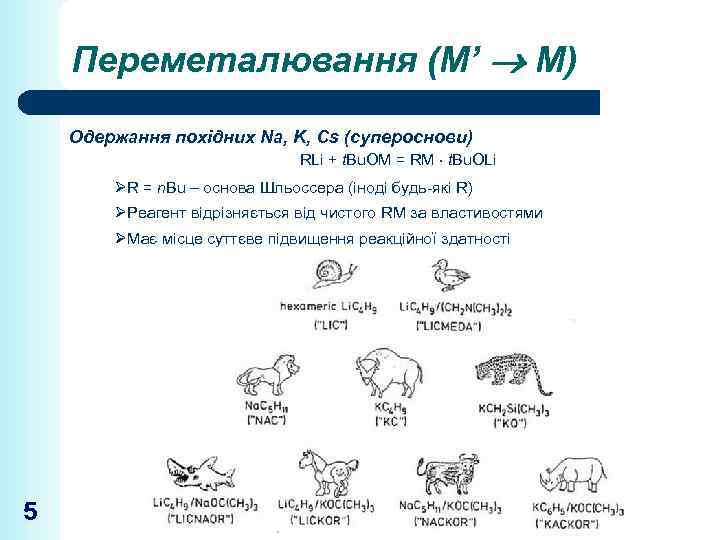
Переметалювання (М’ М) Одержання похідних Na, K, Cs (супероснови) RLi + t. Bu. OM = RM t. Bu. OLi ØR = n. Bu – основа Шльоссера (іноді будь-які R) ØРеагент відрізняється від чистого RM за властивостями ØМає місце суттєве підвищення реакційної здатності 5

Переметалювання (М’ М) Одержання похідних Zn, Cd, Hg RLi + MCl 2 = RMCl + Li. Cl 2 RLi + MCl 2 = R 2 M + 2 Li. Cl (також магній) Ø Zn: часто одержують in situ, іноді за реакцією RX + Mg + Zn. Cl 2 (ультразвук) комплекси R 2 Zn – Mg. X 2 відрізняються за активністю від чистих R 2 Zn надлишок RLi: утворення три- та тетраалкілцинкатів Ø Cd: зазвичай одержують R 2 Cd термічно нестійкі – одержують in situ отруйні – майже повністю витіснені купратами Ø Hg: крім Li, Mg, також B (первинний алкіл, алкеніл) термічно та гідролітично стійкі дуже отруйні – історія, доказ утворення нестійких МОС, “цікаві досліди” 6
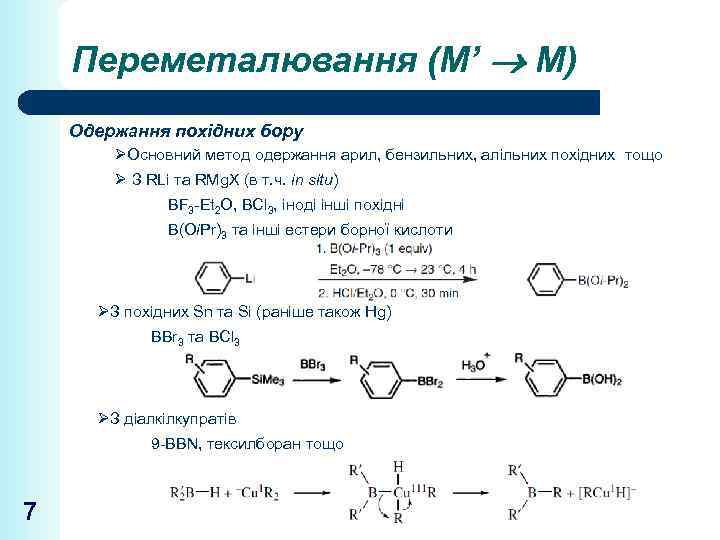
Переметалювання (М’ М) Одержання похідних бору ØОсновний метод одержання арил, бензильних, алільних похідних тощо Ø З RLi та RMg. X (в т. ч. in situ) BF 3 -Et 2 O, BCl 3, іноді інші похідні B(Oi. Pr)3 та інші естери борної кислоти ØЗ похідних Sn та Si (раніше також Hg) BBr 3 та BCl 3 ØЗ діалкілкупратів 9 -BBN, тексилборан тощо 7
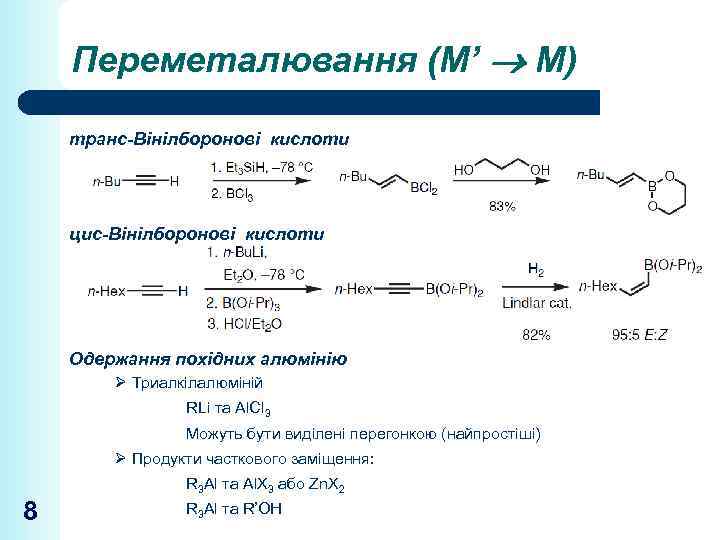
Переметалювання (М’ М) транс-Вінілборонові кислоти цис-Вінілборонові кислоти Одержання похідних алюмінію Ø Триалкілалюміній RLi та Al. Cl 3 Можуть бути виділені перегонкою (найпростіші) Ø Продукти часткового заміщення: R 3 Al та Al. X 3 або Zn. X 2 8 R 3 Al та R’OH
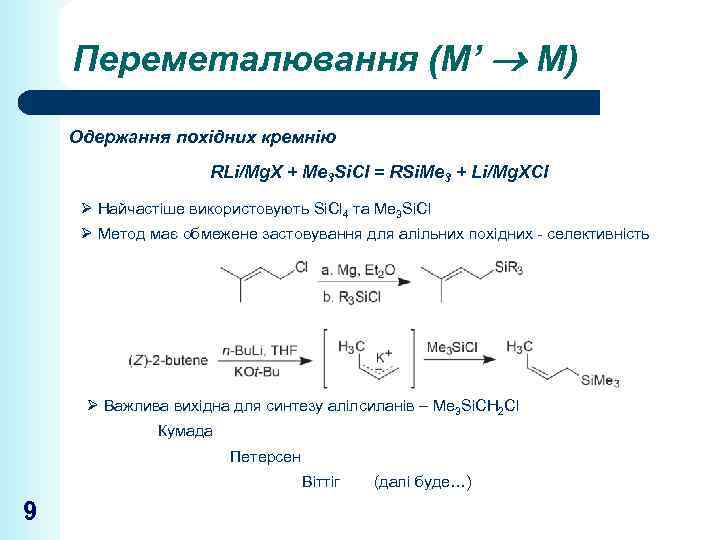
Переметалювання (М’ М) Одержання похідних кремнію RLi/Mg. X + Me 3 Si. Cl = RSi. Me 3 + Li/Mg. XCl Ø Найчастіше використовують Si. Cl 4 та Me 3 Si. Cl Ø Метод має обмежене застовування для алільних похідних - селективність Ø Важлива вихідна для синтезу алілсиланів – Me 3 Si. CH 2 Cl Кумада Петерсен Віттіг 9 (далі буде…)
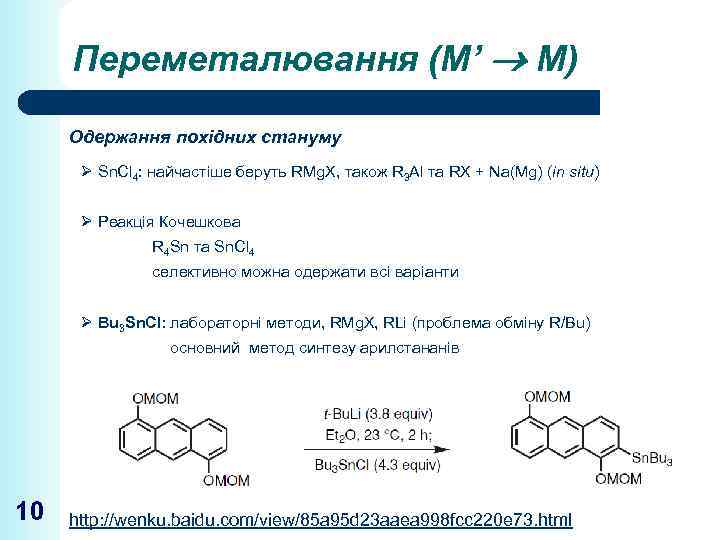
Переметалювання (М’ М) Одержання похідних стануму Ø Sn. Cl 4: найчастіше беруть RMg. X, також R 3 Al та RX + Na(Mg) (in situ) Ø Реакція Кочешкова R 4 Sn та Sn. Cl 4 селективно можна одержати всі варіанти Ø Bu 3 Sn. Cl: лабораторні методи, RMg. X, RLi (проблема обміну R/Bu) основний метод синтезу арилстананів 10 http: //wenku. baidu. com/view/85 a 95 d 23 aaea 998 fcc 220 e 73. html

Переметалювання (М’ М) Переметалювання за участі металоорганічних сполук ØБільш активний метал зв’язується з менш активним карбаніоном Ø Метод синтезу деяких типів сполук Li, Mg, рідше Zn Ø Реакція дуже швидка (Li, Mg) (швидше обміну галогену на метал) ØЗбереження конфігурації ØПеревага: у продукті відсутні електрофільні RX, які є при обміні галогену 11
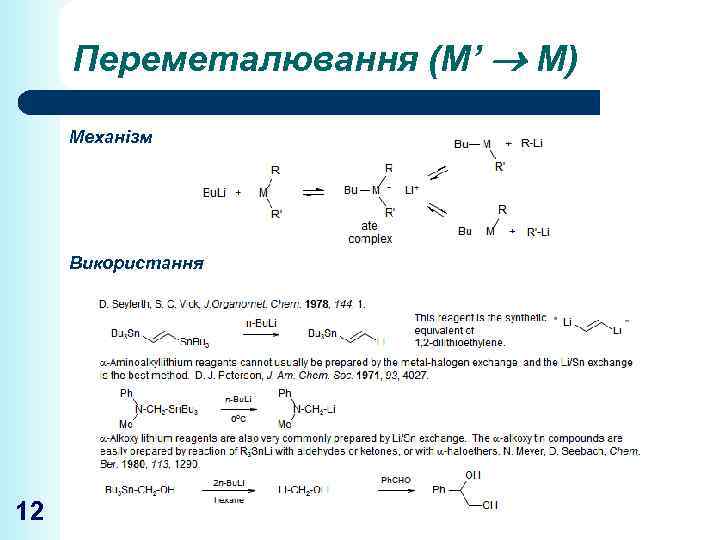
Переметалювання (М’ М) Механізм Використання 12

Обмін галогену на метал (Х М) Відновлення металом: “прямий” синтез МОС ØОсновний метод добування у промисловості ØКрім класичних Li та Mg, добувають Zn, Si (кат. С-Cu, 250 -550 С) ØУ сучасній лабораторній практиці широко застосовують лише для Mg (багато Mg, Li доступні комерційно – середня вартість) ØРеакція гетерогенна та повільна, перебіг сильно залежить від активності поверхні металу ØРеакція прискорюється ультразвуком ØРеакційна здатність: F << Cl < Br < I; іноді використовують SR чи OR ØВ цьому ж ряду збільшується швидкість реакції Вюрца 13
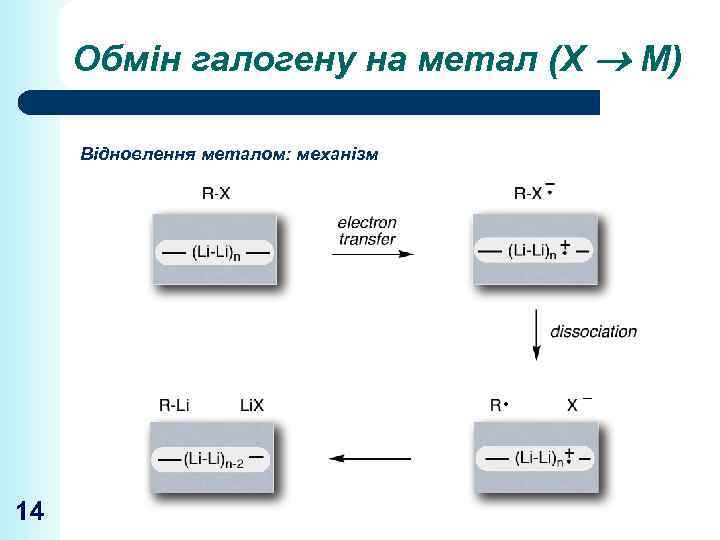
Обмін галогену на метал (Х М) Відновлення металом: механізм 14

Обмін галогену на метал (Х М) Відновлення металом: одержання похідних літію ØRX: найкращі результати з хлоридами, іноді бромідами (Me. I) ØБензил, аліл: етери та тіоетери ØЛітій: невеликий надлишок, активація натрієм (0. 5 -2%) ØОбов’язкова атмосфера аргону ØРозчинники: вуглеводні. Для Me. Li та Ph. Li – Et 2 O (Чому? ) ØОсновний промисловий метод. Світове виробництво ~1800 тон за рік (в основному n. Bu. Li ) ØБагато доступних комерційно як розчини у вуглеводнях. Наприклад, n. Bu. Li в гексані: 1. 6 M, 2. 5 M, 10 М. Жовтуваті розчини, при тривалому зберіганні – білий осад Li. H. Зберігання: 4 С 15

Обмін галогену на метал (Х М) Відновлення металом: одержання похідних магнію ØRX: хлориди, броміди. Арилхлориди майже не реагують (в Et 2 O). ØМагній: стехіометрично. Магнієва стружка, також магнієвий пил, магній Ріке ØЄ індукційний період. Часто потрібна активація: йод, Br. CH 2 Br, Me. I, Hg. Cl 2 Ø“Grignard grade Mg”: 1 -2% Na/K ØАтмосфера аргону не обов’язкова ØРозчинники: етер, ТГФ (для вініл – тільки ТГФ, реагенти Нормана) Чому ТГФ працює з малоактивними галогенідами? ØОсновний промисловий метод ØКомерційно доступні розчини в ТГФ, також Et 2 O, THF-toluene (до ~3 M) ØЗберігання: 15– 30 С (Чому? ) 16

Обмін галогену на метал (Х М) Відновлення металом: одержання похідних цинку ØRX: йодиди, алкілброміди. При наявності стабілізації – хлориди та естери сульфокислот. Тим не менш, переважно активні галогеніди ØЦинк: звичайний порошковий, цинк-мідь, цинк-срібло, цинк Ріке, активація ультразвуком Ø Розчинник: етери, вуглеводні–ДМФ, ГМФТА тощо Ø Допустимі функціональні групи: ROOC, ROOCC=C, ROOCC C, RCOC=C, RNHCO, RC C, NC, ROOCNH, RCONH, (RCO)2 N, Hal, RCOO, Ph. S, Ph. O 2 S, Ph. COS, (RO)2 OP, Me 3 Si, n-Bu 3 Sn, (RO)2 B Відстань до галогену: 2– 6 атомів, можуть бути С=С зв’язки у положенні 3 і вище 17
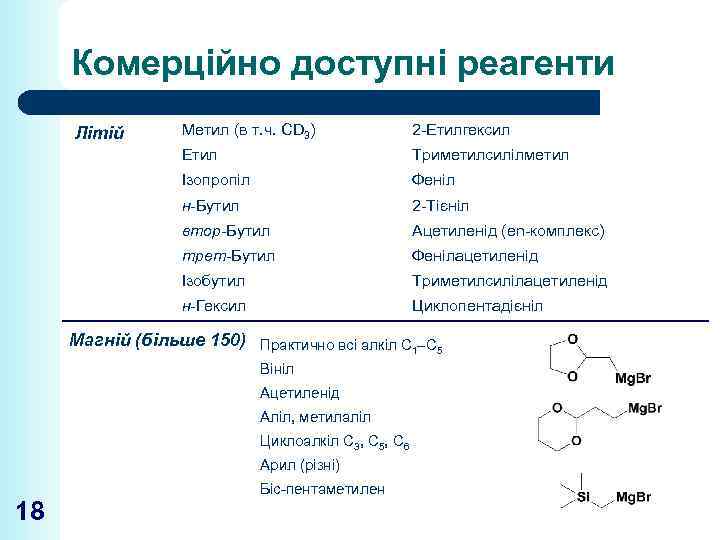
Комерційно доступні реагенти Метил (в т. ч. CD 3) 2 -Етилгексил Етил Триметилсилілметил Ізопропіл Феніл н-Бутил 2 -Тієніл втор-Бутил Ацетиленід (en-комплекс) трет-Бутил Фенілацетиленід Ізобутил Триметилсилілацетиленід н-Гексил Літій Циклопентадієніл Магній (більше 150) Практично всі алкіл С 1–С 5 Вініл Ацетиленід Аліл, метилаліл Циклоалкіл С 3, С 5, С 6 Арил (різні) 18 Біс-пентаметилен

Обмін галогену на метал (Х М) Відновлення за участі солей аніон-радикалів ØRX: галогеніди, тіоетери (дуже ефективні). ØАніон-радикали: нафталенід літію, Li. DBB, LDMAN. Можуть бути генеровані in situ, каталітично ØРеакція гомогенна, а тому швидша та селективніша за “прямий” синтез 19 ØПереметалювання з Mg. Br 2 – магнійорганічні сполуки

Обмін галогену на метал (Х М) Обмін галогену за участі металоорганічних сполук: Li ØУмови: Bu. Li (n-, t-), – 100 to – 78 C, pentane-ether або. THF Øn-Bu. Li: 1 еквівалент; t-Bu. Li: 2 еквіваленти (Чому? ) ØРеакційна здатність: I > Br >> Cl (майже не реагують) ØРеакція дуже швидка, швидша за реакції приєднання. Швидкість може бути більшою за швидкість переносу протону ØРеакція оборотня ØСубстрати: арил, вініл (менш реакційноздатні), циклопропіл. Алкіл – за наявності внутрішнього електрофілу або з t-Bu. Li ØВінільні та циклопропільні субстрати: збереження конфігурації 20
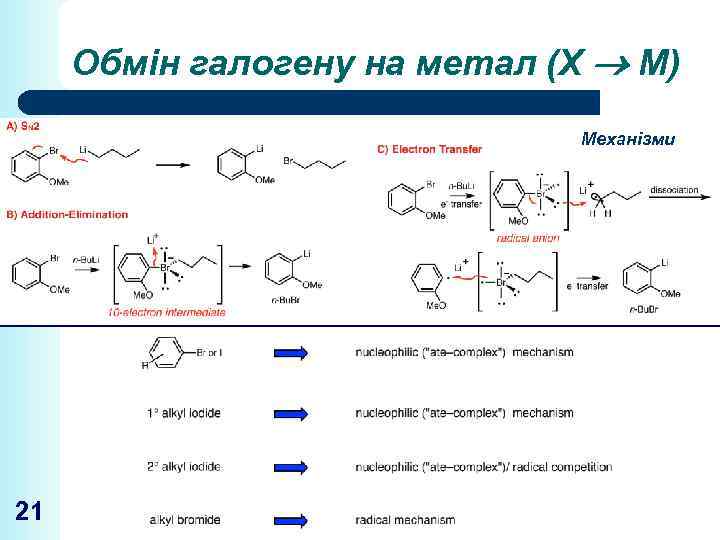
Обмін галогену на метал (Х М) Механізми 21
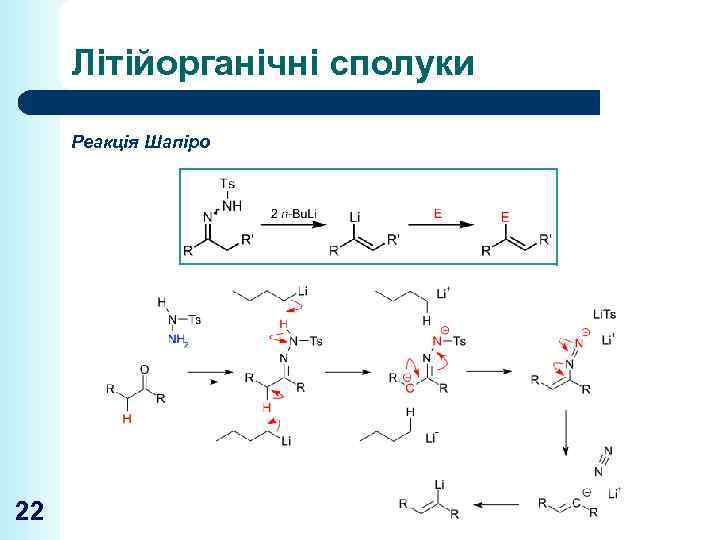
Літійорганічні сполуки Реакція Шапіро 22

Обмін галогену на метал (Х М) Обмін галогену за участі металоорганічних сполук: Mg Øi-Pr. Mg. Cl/Br, – 40 to 25 C, THF are the most common conditions. ØMagnesium-halogen exchange reactions typically employ one equivalent of -Pr. Mg. Cl/Br. ØAlkyliodides are more reactive than the corresponding bromides. Alkylchlorides are essentially inert. ØOnly highly reactive electrophiles (aldehydes/ketones) react at significant rates below 0 °C. This allows for the preparation of organomagnesium reagents containing cyano, nitro, ester, benzylic chloride, secondary tosylate, tertiary amide, imine, amidine, aromatic amino (deprotonated), heteroaromatics functional groups. ØThe rate of magnesium-halogen exchange is accelerated by electron-withdrawing and ortho-chelating groups. ØVinyl iodides are also suitable substrates for magnesium-halogen exchange. Higher temperatures and longer reactions times are required, which limits the functional group tolerance of this method. Ø More reactive combinations (как раз для винильных): i-Pr. Mg. Cl/Br + Li. Cl 2 n-Bu. Li + i-Pr. Mg. Cl/Br 23 Цинк: поширений реагент – діетилцинк i
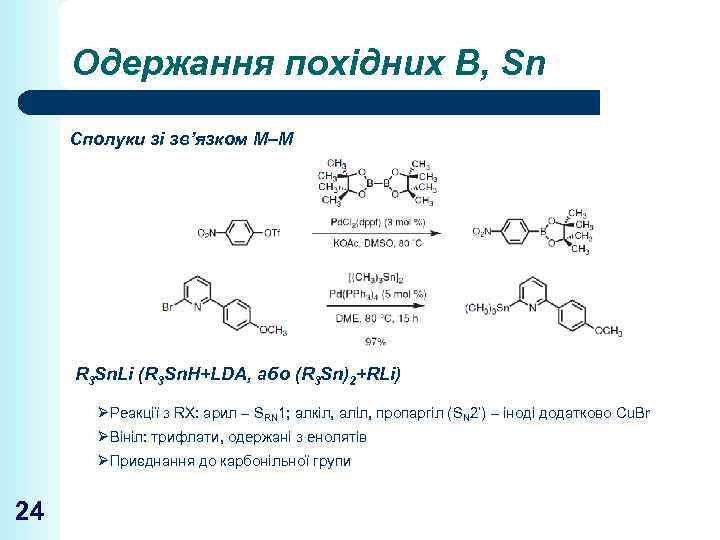
Одержання похідних B, Sn Сполуки зі зв’язком М–М R 3 Sn. Li (R 3 Sn. H+LDA, або (R 3 Sn)2+RLi) ØРеакції з RX: арил – SRN 1; алкіл, аліл, пропаргіл (SN 2’) – іноді додатково Сu. Br ØВініл: трифлати, одержані з енолятів ØПриєднання до карбонільної групи 24

TO BE CONTINUED… 25
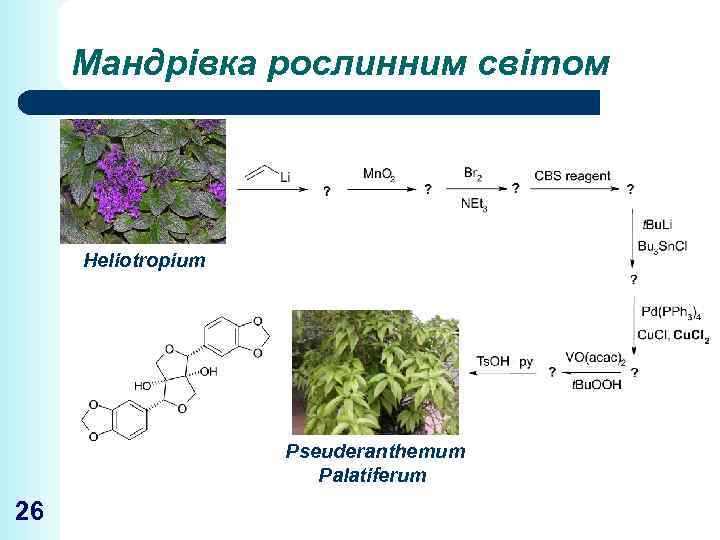
Мандрівка рослинним світом Heliotropium Pseuderanthemum Palatiferum 26
Заняття7.ppt