Канцерогенез....ppt
- Количество слайдов: 37

Канцерогенез студентка 1 курса магистратуры ИТЭБ Коробейникова М. О. l. Москва, 2014

Канцерогене з (лат. cancerogenesis; cancer — рак + др. -греч. γένεσις — зарождение, развитие) — сложный патофизиологический процесс зарождения и развития опухоли. (син. онкогенез).
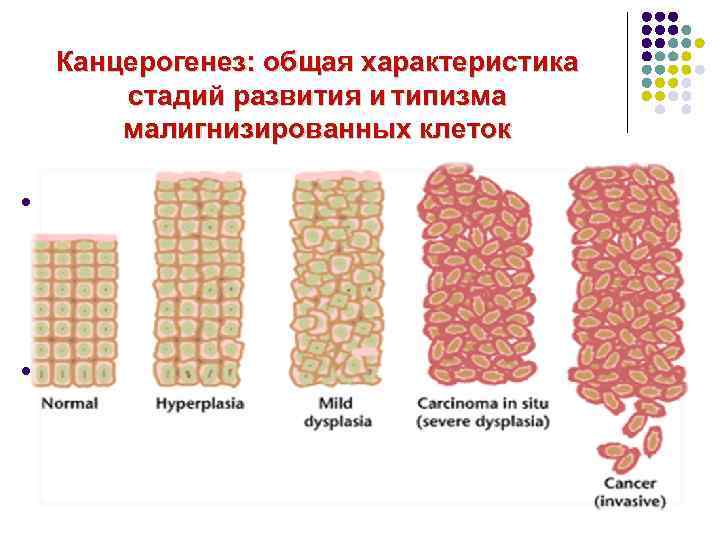
Канцерогенез: общая характеристика стадий развития и типизма малигнизированных клеток l Канцерогенез – это многоступенчатый процесс накопления изменений в геноме клеток, приводящий к появлению «асоциальных клеток» , характеризующихся морфологическим, функциональным, биохимическим атипизмом, автономным ростом, «ускользанием» клеток от гуморальных и нервных влияний. l Касаясь стадий канцерогенеза, необходимо отметить ряд последовательных этапов развития неоплазии, в частности, стадию инициации, стадию размножения опухолевых клеток, или промоции, стадию опухолевой прогрессии
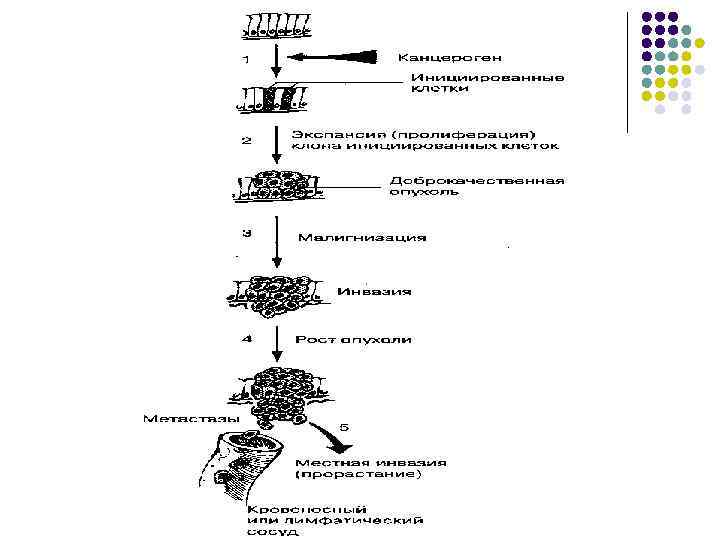
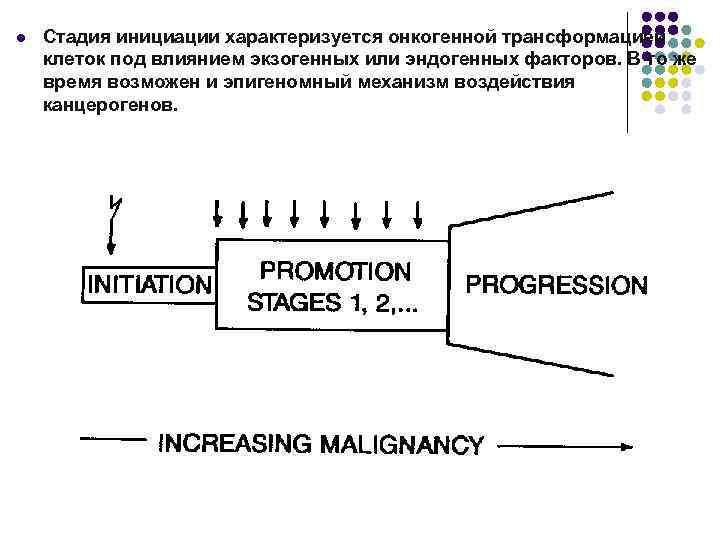
l Стадия инициации характеризуется онкогенной трансформацией клеток под влиянием экзогенных или эндогенных факторов. В то же время возможен и эпигеномный механизм воздействия канцерогенов.

l Как известно, многие химические канцерогены, а также воздействие физических и биологических факторов на организм могут вызывать мутации ДНК, провоцирующие экспрессию протоонкогенов или депрессию (утрату) антионкогенов. l При эпигеномном характере действия канцерогенов экспрессия онкогенов возникает в связи с нарушением регуляции клеточного роста без повреждения самого генетического материала. При эпигенетическом коканцерогенном эффекте патогенных факторов возникает инактивация белков – продуктов антионкогенов- или активация пострецепторных ростовых факторов. Такое воздействие, как правило, не вызывает развития опухоли, но усиливает ростовые эффекты других факторов, способствуя пролиферации мутантных клеток и формированию неоплазии. l Неоплазия - иначе неоплазма, бластома новообразование ткани, опухоль.

Эффект канцерогенов-мутагенов называется инициирующим, а коканцерогенов – активирующим. Прямой генотоксический эффект канцерогенов возникает в процессе: lалкилирования, lделеции, lтранслокации, lамплификации генов. Если мутация затрагивает гены, регулирующие клеточное размножение, клетка становится инициированной, то есть потенциально способной к неограниченному делению, но требующей для фенотипического проявления этого свойства дополнительных воздействий.

l l l Существует множество химических соединений, так называемых промоторов, хроническое воздействие которых на инициированные клетки приводит к развитию второй стадии канцерогенеза – промоции, то есть интенсивному размножению малигнизированных клеток и формированию опухоли. В механизмах развития промоции важная роль отводится нарушениям взаимодействия онкогенов и антионкогенов. Активация протоонкогенов может происходить в результате точковых мутаций в самом протоонкогене, транслокации протоонкогена или его амплификации. В патогенезе неоплазии, в частности, стадии промоции, важная роль отводится ограничению синтеза белковсупрессоров пролиферации, в связи с подавлением активности генов р53, p. Rb, индукторов апоптоза, ДНКрепарирующих ферментов, а также гиперэкспрессии Myc, Ras. Заключительной фазой канцерогенеза является стадия опухолевой прогрессии.

Автономия злокачественных клеток обеспечивается за счет нескольких процессов: l 1) секреции малигнизированной клеткой митогенов, вызывающих аутокринную стимуляцию пролиферации клеток, в частности, фактора роста опухоли, тромбоцитарного фактора и фактора роста опухоли; l 2) количественных и качественных изменений рецепторов к факторам роста; l 3) нарушения передачи сигнала к клеточному росту на пострецепторном уровне; l 4) экспрессии онкогенами транскрипционных факторов. Многостадийность канцерогенеза предполагает возникновение последовательных мутаций в значительном количестве доминантных или рецессивных онкогенов или развитие коканцерогенного (синканцерогенного) эффекта под влиянием различных инициирующих факторов – канцерогенов физической, химической, биологической природы.
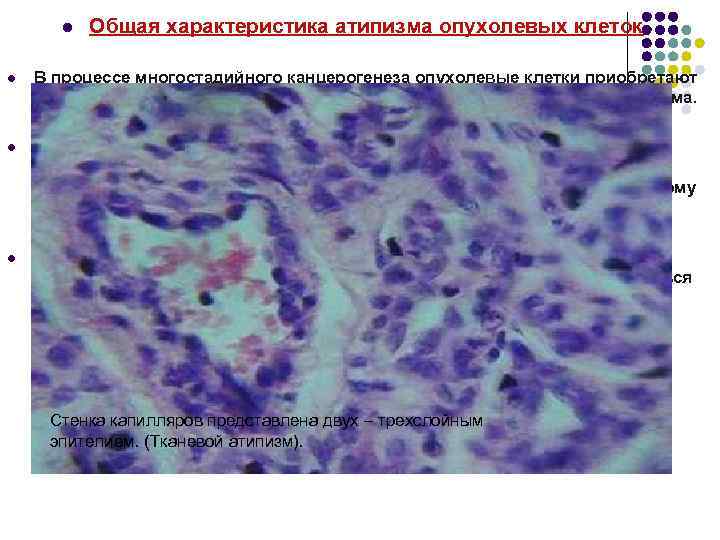
l Общая характеристика атипизма опухолевых клеток l В процессе многостадийного канцерогенеза опухолевые клетки приобретают признаки морфологического, функционального и метаболического атипизма. l Тканевой атипизм опухолевых клеток проявляется в снижении их адгезивных способностей вследствие необратимого фосфорилирования белков цитоскелета; при этом нарушается фиксация клеток к межклеточному веществу. l Атипизм в культуре тканей проявляется отсутствием контактного торможения роста, ослаблением адгезивности, способностью размножаться в полужидкой среде. Стенка капилляров представлена двух – трехслойным эпителием. (Тканевой атипизм).

К морфологическим особенностям опухолевых клеток необходимо отнести: lнарушение структуры и функции цитоплазматических, l митохондриальных, lлизосомальных мембран, lуменьшение количества мембранных рецепторов и изменения их структуры, l появление новых рецепторов, lв связи с чем возникает ослабление, усиление или извращение нервных и гуморальных влияний на трансформированные клетки. Характерными признаками клеточного атипизма являются геномные и хромосомные мутации в виде полиплоидии, ануэплоидии, делеции, дупликации, транслокации, инверсии. Генные мутации при канцерогенезе столь же стереотипны и могут носить характер мягких и жестких мутаций.

l Биохимический атипизм раковых клеток проявляется снижением антиоксидантного потенциала, наличием в митохондриях аномальной кольцевой или одноцепочечной ДНК. l Для опухолевых клеток характерна чрезмерная активация пентозного цикла окисления глюкозы – основного поставщика рибозо-5 -фосфата, необходимого для синтеза нуклеиновых кислот. l Опухолевые клетки потенциально бессмертны (феномен иммортализации) в связи с высокой активностью теломеразы – фермента, восстанавливающего исходную длину теломер после удвоения ДНК, а также в связи с подавлением апоптоза малигнизированных клеток.

Инвазия тканей и метастазирование Инвазия и метастазирование - кардинальные признаки злокачественной опухоли. Они являются основной причиной гибели больных раком. Способность злокачественной опухоли к метастазированию основана на: инфильтрирующем росте с инвазией в лимфатические и кровеносные сосуды, слабой связи между опухолевыми клетками, на благоприятной биохимической ситуации в тканях для приживления ракового эмбола.

Каскад метастазирования включает в себя четыре стадии: 1. Отделение опухолевых клеток от основного опухолевого узла и внедрение в экстрацеллюлярный матрикс (ЭЦМ). Инвазия ткани. 2. Проникновение опухолевых клеток в просвет сосудов (пермеация) и агрегация с другими метастазирующими опухолевыми клетками. Распространение клеток по лимфатическим и кровеносным сосудам (раковая эмболия). 3. Фиксация опухолевых клеток на интиме сосудов капиллярного типа с образованием тромба. 4. Переход из кровеносных и лимфатичесих сосудов в прилегающую ткань. Приживление и размножение клеток (экстраваскулярная пролиферация), индукция ангиогенеза. Формировние метастаза (вторичного опухолевого узла).
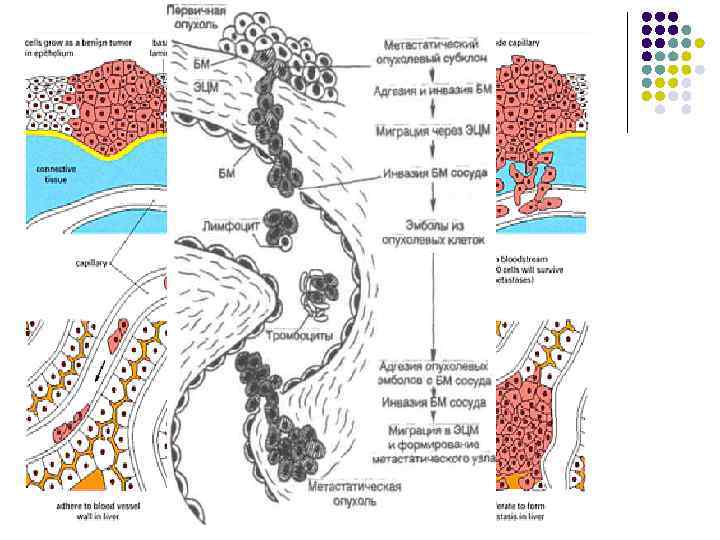

Факторами, облегчающими метастазирование, являются: экспрессия опухолевыми клетками на их мембране адгезивных молекул, способствующих метастазированию; секреция протеаз; торможение антипротеазных активностей молекул ЭЦМ, окружающего опухоль. Итак, на каждом из этапов опухолевой прогрессии опухоль приобретает и необратимо закрепляет за собой новые фенотипические черты, позволяющие ей наращивать собственную массу, давать метастазы и уходить от контролирующих и сдерживающих ее рост возможностей организма
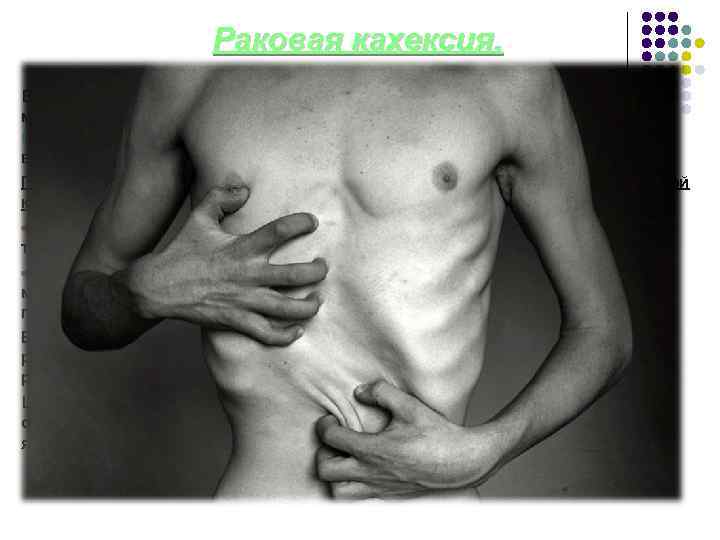
Раковая кахексия. Больные раком страдают от резчайшего исхудания за счет уменьшения массы жировой и мышечной ткани. Такое состояние называется раковой кахексией или общим истощением, и обычно оно сопровождается выраженной слабостью, анорексией (отказом от еды) и анемией. Причины раковой кахексии неоднозначны, и она отличается от алиментарной кахексии, которая может быть вызвана длительным голоданием. При голодании сначала в весе теряет жировая, а лишь затем мышечная ткань. При раке происходит параллельное уменьшение массы жировой и мышечной ткани. Установлено, что основной обмен при раке, в отличие от голодания, повышен. В настоящее время имеются четкие доказательства того, что кахексия при раке является результатом действия на организм определѐнных растворимых факторов - цитокинов. Цитокины продуцируются как самой опухолью, так и клетками организма в ответ на опухоль. Важнейшим цитокином, вызывающим раковую кахексию является фактор некроза опухолей α(ФНО-α). Его синоним - кахектин.

Дополнительными факторами, определяющими раковую кахексию, являются резкие изменения вкусовых ощущений и нарушение регуляции аппетита у больных раком. Эта проблема, очевидно, связана с влиянием медиаторов ответа фазы на центры, регулирующие аппетит, а также с нарушениями жирового метаболизма. Получение в чистом виде и расшифровка химической структуры цитокинов, ответственных за возникновение и прогрессирование раковой кахексии, будет способствовать разработке адекватных методов лечения раковой кахексии. Теории канцерогенеза и общие механизмы опухолевой трансформации клетки. На сегодняшний день существует четыре теории происхождения рака или теории канцерогенеза: ü вирусная, üтеория химического канцерогенеза, üлучевого канцерогенеза, üнаследственная теория.

Мишенями для действия всех канцерогенных агентов или онкогенных 3. Гены, регулирующие апоптоз. Могут быть как доминантными, так и факторовтаким генам относят: мутированный протоонкоген bcl-2, рецессивными. К являются следующие варианты в норме ослабляющий апоптоз и пособствующий увеличению клеточной генов: популяции, мутированный протоонкоген bax, в норме способствующий 1. Гены, усиливающие рост. Это так называемые протоонкогены апоптозу, нормальный ген р-53, который участвует в синтезероста продукта нормальные гены, необходимые для обеспечения обновления и онкогена bax, и через него в те периоды, когда он в этом нуждается. Под клеточной массы организма тоже усиливающий апоптоз. Нарушение баланса активности этих трех генов: bcl-2, bax и р-53, влиянием различных мутаций протоонкогены могут превращаться в онкогены. влияющих на ход апоптоза является важнейшим фактом, сдвигающим Протоонкогены - доминантные гены, поэтому для клональной опухолевой апоптоз в сторону его ослабления и обеспечивающим опухолевым пролиферации достаточно возникновение одного мутировавшего клеткам их «бессмертность» . В дополнение к этим классам генов, протоонкогена. участвующих в онкогенезе, или туморосупрессирующие репарации ДНК. 2. Гены, тормозящие рост, необходимо назвать гены, являющиеся Нарушения в системе этих генов вызывают нестабильность генома, что рецессивными. Злокачественная опухоль возникает только в случае предрасполагаетутраты обоих такихмутациям, которые дают начало генам инактивации или клетки к генным генов. К туморосупрессирующим опухолевому процессу. относят Rb-ген. Утеря обоих аллелей этого гена приводит к злокачественному заболеванию глаза - ретинобластоме (опухоли из ретинобластов - незрелых клеток, предшественников ретиноцитов). Наследственный дефект обоих аллелей Rb-гена - явление чрезвычайно редкое, если же дефектным является один аллель, то приобретенная мутация второго аллеля с высокой вероятностью может привести к возникновению ретинобластомы, поскольку в этом случае уже утеряно «генное прикрытие» здоровым аллелем.
Вирусный канцерогенез. Вирусно-генетическая теория возникновения опухолей, предложенная еще в 40 -х годах Л. И. Зильбером, получила за прошедшие годы многочисленные подтверждения. Вирусы не являются единственной причиной рака, они играют большую роль в этиологии злокачественных заболеваний как у человека, так и у животных. В этом принимают участие различные ДНК- и РНКсодержащие вирусы. Опухоли, у которых вирусы идентифицированы в качестве этиологических факторов, обнаружены у многих видов млекопитающих и птиц. Они способны вызывать трансформацию Рак считается «чумой XXI-го века» . клеток in vitro и индуцировать опухоли in vivo. В составе этих вирусов идентифицированы либо специальные гены ( онкогены ), продукты которых непосредственно контролируют трансформированный фенотип зараженных клеток, либо гены, продукты которых индуцируют экспрессию других генов, участвующих в контроле пролиферации клеток. Оба типа вирусов представляют собой прекрасную модель для изучения изменений в биологическом поведении клеток в результате взаимодействия различных типов генов. Вирусный канцерогенез имеет ряд существенных особенностей, связанных с привнесением в клетку собственной генетической информации. В случае онкогенных ретровирусов можно утверждать, что они выступают либо в качестве агентов, активирующих клеточные протоонкогены (слабоонкогенные вирусы ) , либо несут трансформирующие последовательности, ведущие свое происхождение от тех же клеточных протоонкогенов. Причем имеющиеся мутационные различия в кодирующей последовательности вирусного онкогена и клеточного протоонкогена играют существенную роль в повышении его трансформирующей активности.

Классификация онковирусов. Все онковирусы делятся на ДНК и РНК-содержащие вирусы. l. ДНК-содержащие вирусы животных, такие как аденовирусы, могут вызывать опухоли только в лабораторных условиях. Другие вирусы, например, бычий вирус папилломы, вызывают как злокачественные, так и доброкачественные опухоли у их природных хозяев. l. ДНК-содержащие вирусы человека, участвующие в формировании рака человека, можно расклассифицировать на 4 группы: 1. вирусы, вызывающие папилломы (папилломавирусы), 2. вирус Эпстейн-Барра (EBV), 3. вирус гепатита В (HBV), 4. вирус герпеса, вызывающий саркому Капоши (KSHV).
Краткая характеристика отдельных ДНК-содержащих онковирусов Вирус папилломы человека Вирус Эпстейн-Барра Вирус гепатита В

РНК-содержащие онкогенные вирусы (онкорнавирусы). Известен только один РНК-содержащий вирус (ретровирус), вызывающий злокачественную опухоль у людей, а именно: острый Т-клеточный лейкоз у взрослых. В Японии и на Карибских островах заболевание носит эндемический характер, спорадические случаи этого заболевания обнаружены во всех районах мира. Подобно вирусу иммунодефицита человека (HTLV-3), HTLV-1 имеет тропизм к С 04+клеткам. Они являются главной клеточной мишенью для опухолевой трансформации. Этот вид лейкоза развивается приблизительно в 1% случаев у инфицированных лиц после длительного латентного периода (от 20 до 30 лет). Помимо лимфолейкоза, HTLV-1 выявлен при тропическом спастическом парапарезе, а также при некоторых формах увеита и артрита, встречающихся в районах эндемии.

Химический канцерогенез. Стадии химического канцерогенеза. Общепринято считать, что химический канцерогенез протекает в две стадии: инициации и промоции. Инициация является результатом непосредственного контакта обязательного канцерогена с клеткой, который ведет к мутациям и стойкому необратимому изменению клеточного генома. Следующая стадия химического канцерогенеза-стадия промоции. Промоторы или «толкачи» - это химические вещества, обладающие ростовыми свойствами и способствующие пролиферации инициированных клеток. Являясь сильными митогенами, промоторы способствуют возникновению дополнительных мутаций в активно пролиферирующих клетках. По этой причине хроническое воспаление, сопровождающееся гибелью клеток и одновременным их усиленным новообразованием, является фактором риска в плане возникновения опухолевого процесса.

Характеристика химических канцерогенов и инициация канцерогенеза. По своему происхождению химические вещества, вызывающие канцерогенез, могут быть природными и синтетическими, а также экзогенными и эндогенными. Последние, как правило, выполняют роль промоторов. Полициклические ароматические углеводороды - наиболее сильные канцерогены. К ним относятся 3, 4 - бензпирен, обнаруженный впервые как продукт перегонки каменного угля. Он и послужил причинным фактором описанного Персивалем Поттом рака мошонки у трубочистов, поскольку содержался в саже, которая попадала в складки мошонки мальчиков, занимавшихся в детстве чисткой каминных дымоходов. Рак возникал у них гораздо позже, много лет спустя, когда мальчики-трубочисты достигали зрелого возраста. Полициклические углеводороды содержатся в отходах табака и, в первую очередь, повинны в возникновении рака легких и мочевого пузыря у курильщиков.
Ароматические амины и азокрасители. Вещества этой природы Ароматические амины и азокрасители. обладают Органотропизмо. Бета-нафтиламин связан с возникновением рака мочевого пузыря у людей. Некоторые азокрасители, используемые для окраски пищевых продуктов (маргарина), такие, как азобензол масляный желтый, способны вызвать рак печени. В настоящее время во многих государствах применение их в пищевой промышленности запрещено. Канцерогены, встречающиеся в природе. Среди известных нам Канцерогены, встречающиеся в природе. химических канцерогенов, вырабатываемых растениями и микрорганизмами, потенциальным печеночным канцерогеном является афлотоксин В 1, продуцируемый некоторыми штаммами грибка Аспергилус флавус (желтая плесень). Афлатоксин содержится в земляных орехах. Из других потенциальных канцерогенов следует назвать следующие: ü асбест; ü винилхлорид; üмышьяк; ü хром и никель.

Промоторы химического канцерогенеза. Концепция двустадийного канцерогенеза была предложена Беренблюмом в 1940 году, а ее обоснованию послужили экспериментальные и жизненные наблюдения.
Лучевой канцерогенез. Любые формы лучевой энергии, такие как ультрафиолетовая часть солнечного спектра, ионизирующее излучение в форме α, β- или γ-частиц, рентгеновское излучение, действие протонов или нейтронов обладает способностью опухолевой трансформации всех видов клеток «in vitro» , а также вызывают опухоли у человека и подопытных животных. Прослеживается связь между УФО и раком кожи, описаны профессиональные раки у врачейрентгенологов и лиц, занятых в атомной промышленности.

Онкобелки и их свойства. Механизмы трансформации нормального генома клетки в его онкопрототип ведут к синтезу такой трансформированной клеткой онкобелков, являющиеся продуктами онкогенов. Синтез онкобелков является последним звеном в цепи генетических событий. Именно онкобелки выполняют роль ростовых факторов. В физиологических условиях клеточная пролиферация включает в себя следующие фазы или события: включает в себя ü связывание фактора роста с его специфическим рецептором, ü временную и ограниченную активацию рецепторов фактора роста, üпередачу полученных цитоплазмой сигналов группой вторичных мессенджеров на ядро, ü активацию ядерных белков ü вход и продвижение клетки по пути митотического цикла.

В соответствие с их функциями онкобелки могут играть следующие роли: фактор роста, рецепторы факторов роста, мембранные G-белки, вовлекаемых в передачу ростовых сигналов с клеточной мембраны на цитоплазму, вторичные мессенджеровы, ДНК-связывающие белки.

Роль цитотоксических лимфоцитов в противоопухолевом иммунитете Защитные противоопухолевые механизмы организма включают в себя клеточные и гуморальные реакции иммунитета. Наиболее важную роль в иммунном противостоянии опухоли играют реакции клеточного типа с участием цитотоксических лимфоцитов - CD 4+. Специфические цитотоксические лимфоциты особенно эффективны в борьбе против опухолей, вызываемых вирусами (лимфомы Беркитта, папилломы). Иммунологическая специфичность Т-клеток направлена как против тумороспецифических, так и против туморосвязанных антигенов. В настоящее время Т-лимоциты, инфильтрирующие опухоль, используются при иммунотерапии некоторых видов рака.

Роль цитотоксических лимфоцитов в противоопухолевом иммунитете Защитные противоопухолевые механизмы организма включают в себя клеточные и гуморальные реакции иммунитета. Специфические цитотоксические лимфоциты особенно эффективны в борьбе против опухолей, вызываемых вирусами (лимфомы Беркитта, папилломы). Иммунологическая специфичность Т-клеток направлена как против тумороспецифических, так и против туморосвязанных антигенов. В настоящее время Т-лимоциты, инфильтрирующие опухоль, используются при иммунотерапии некоторых видов рака. Наибольшая эффективность этих клеток в борьбе со злокачественными опухолями объясняется тем, что на опухолевых клетках снижена экспрессия молекул HLA и по этой причине они избегают клеточного распознавания CD 8+ сенсибилизированными лимфоцитами.

Антитело-зависимая клеточная цитотоксичность - иммунологический феномен, позволяющий распознавать ассоциированный с клеткой (встроенный в клетку) антиген благодаря прикреплению к нему антител с помощью их Fab-фрагмента. Fcфрагмент при этом остается незанятым и после активации его различными факторами клетка, как правило, гибнет.

Выделяют три варианта гибели опухолевой клетки, атакованной антителами: 1. Комплемент-зависимый лизис. 2. Активация фагоцитов и включение в борьбу с опухолевыми клетками. 3. Активация нашивных киллеров. Уничтожение опухолевых клеток осуществляют лимфотоксины, обладающие выраженным цитопатогенным эффектом. Среди них наиболее активным является ФНО-β. Он так и называется - лимфотоксин.
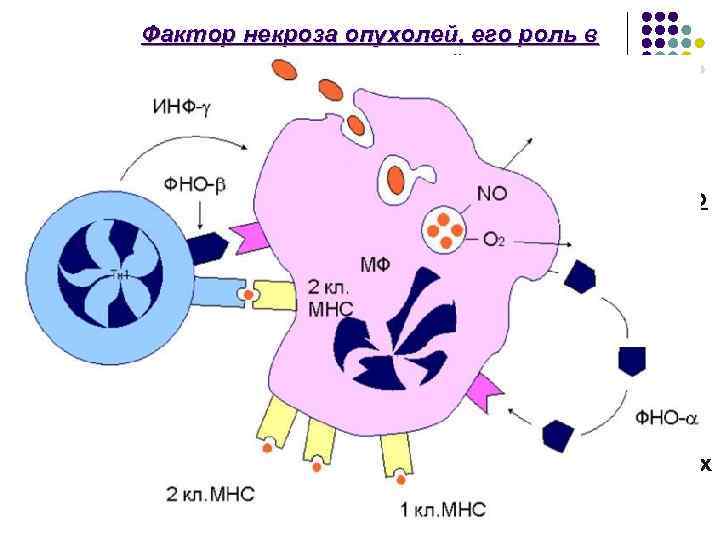
Фактор некроза опухолей, его роль в противоопухолевой защите. Фактор некроза опухолей в двух его формах: ФНО-α и ФНО-β. Различают следующие механизмы противоопухолевого эффекта ФНО: 1. Вызывает геморрагический некроз опухоли. 2. Играет важную роль в активации феноменов иммунологической защиты. 3. Способствует распознаванию опухолевых клеток клетками иммунной системы. 4. Тормозит репарацию ДНК поврежденных опухолевых клеток.

l l Список литературы ПАТОЛОГИЯ ОПУХОЛЕВОГО РОСТА. КАНЦЕРОГЕНЕЗ. Методическое пособие для студентов. Под ред. проф. О. Д. Мишнѐва, проф. Г. В. Порядина. - М. РГМУ, 2002, 41 с. l Г. А. Белицкий Химический канцерогенез l http: //www. rae. ru/monographs/178 -5587 l http: //humbio. ru/humbio/01122001/cancsv/00041 de 8. htm l http: //humbio. ru/humbio/01122001/vir-can/00018753. htm

Спасибо за внимание!
Канцерогенез....ppt