03f6d32f371ba00ba8c79539e2ecc7bd.ppt
- Количество слайдов: 79

KAN İLE BULAŞAN ENFEKSİYONLARDA TARAMA TESTLERİNDE NAT MI? ELISA MI? NAT VE ELISA MI? Başkan: Tartışmacılar: Dr Ramazan Uluhan Dr Yasemin Heper Dr N Banu Pelit
TRANSFÜZYON HAYAT KURTARIR !!! …. . AMA

Transfüzyon ile bulaşan etkenlerin bazıları § Virüsler § HBV, HCV, HDV, HAV, HGV, HIV I-II, HTLV I-II, TTV, EBV, CMV, Parvovirus B 19, HHV 6, HHV 8, Batı Bil Ensefalit Virüsü § Bakteriler § Bruselloz, Salmonelloz, Yersinyoz, Sifiliz, rekurren ateş, Lyme hastalığı, Q ateşi, Kayalık Dağlar benekli ateşi, § Staphylococcus epidermidis ve diğer KNS, Bacillus spp, Streptococcus spp, Staphylococcus aureus, Corynebacterium spp, Enterococcus spp, Proprionibacterium acnes, Micrococcus spp, Clostridium perfringes, Escherichia coli, Enterobacter spp, Serratia spp, Klebsiella spp, Pseudomonas spp, Yersinia enterocolitica, Acinetobacter spp, Burkholderia cepacia, § Parazitler § Sıtma, Toksoplazmoz, Kala Azar, Chagas hastalığı, Filariazis, Babezyoz § Mantarlar § Aspergillus, Penicillium, Candida § Prionlar § Varyant Creutzfeld Jacobs Hastalığı

Bulaşı önlemek için neler yapılıyor? § Bağışçı seçimi § Mikrobiyolojik tarama testleri § Bakteriyel bulaşın önlenmesi ve saptanmasına yönelik uygulamalar § Patojen inaktivasyon teknikleri

Mikrobiyolojik tarama testleri Hangi etkenleri - Hangi testlerle tarayalım § § § Uluslararası normlar Epidemiyolojik veriler Hastalığın önemi, tedavi edilebilirliği Rutinde kullanılabilecek test mevcut mu Maliyet-etkinlik değerlendirmeleri

Tarama testlerine rağmen neden enfeksiyon bulaşır? § Pencere dönemi !!! § Tarama testlerin duyarlılığı § Mutant suşlar § Testin yakalayamadığı serotipler § Bağışçıda immün supresyon § Laboratuvar hataları….

Tarama Testleri § En yüksek duyarlılıkta olan testler seçilir § Prevalans düşük pozitif prediktif değer de düşük § Tekrarlayan reaktivite bakılır § Doğrulama yapılır § Pozitif – Negatif kararı verilir § Bağışçıya bildirimde önemli

Transfüzyon Reaksiyonları § Bakteriyel kontaminasyon 1: 2000 § TRALI 1: 100 000 § Sepsis 1: 140 000 § Akut hemolitik reaksiyon 1: 600 000 § Viral bulaş riski 1: 1 000

Tarama Testleri

HBs. Ag § HBs. Ag pozitifliği § § § % 1 - 4, 5 § TKMTD anketi % 4. 33 (2003) %1. 99 (2006) İmmünodiffüzyon (I. kuşak) Karşıt elektroforez (II. kuşak) RIA ve ELISA (III. kuşak) Enfeksiyon sonrası kanda saptanma 1 -12 hafta Duyarlılık sınırı 0. 06 -1. 5 ng/ml § Kan bankalarında en az 0. 5 ng/ml olmalı Doğrulama: nötralizasyon § veya diğer hepatit belirteçleri

Anti-HCV § Anti-HCV pozitifliği § TKMTD anketi % 0. 3 – 1, 8 % 0. 5 (2003) %0. 45 (2006) § Antikor yanıtının ortaya çıkması 12 hafta – 6 ay § II. kuşak ELİSA kitleri ile 6 -7 haftada III. kuşak ELİSA kitleri ile 5 -6 haftada § III. kuşak kitlerde kor, NS 3, NS 4, NS 5 antijenleri § Kor proteinine karşı geliştirilmiş anti-HCV Ig. M antikor testlerinin fazla değeri yoktur § Doğrulama RIBA, HCV-RNA

Anti-HIV § TKMTD anketi % 0. 2 (2003) - % 0. 12 (2006) § Doğrulananlar % 3. 5 § HIV enfeksiyonunda antikorların saptanması: 6 -8 hafta § Kitlerde Anti-HIV I + anti-HIV II birlikte § p 24 antijeni 2 -3 hafta § İndirekt ELISA (II. kuşak) Çift antijen sandviç yöntemi (III. kuşak) § Hem Ig. M hem de Ig. G türü antikorlar § Seropozitiflik 3 haftada saptanabilmektedir § Doğrulama: Western Blott, HIV-RIBA, PCR

Aklımızda bulunsun § Ülkemizdeki kan bankalarının tümü § Uygun yöntem kullanıyor mu? § Yöntemi uygun kullanıyor mu? § Algoritma doğru mu? § Kalite kontrol? ?

Diğer testler § ALT § Neopterin § Anti-HBc § HCV core Ag Aklımızda bulunsun: Bu testleri uygulayabilir miyiz? ?

Neopterin § § § IFN-gamma ile aktive olmuş monosit/makrofajlardan salınır T helper tip 1 lenfosit aktivasyon göstergesi Viral, hücre içi bakteri ve parazit enfeksiyonları, ayrıca inflamatuar hastalıklar, malignensiler, bazı nörolojik ve kardiyak hastalıklarda artar Serokonversiyon öncesi artar Avusturya’da kan bankalarında kullanılıyor § %3. 2 donör kaybı § Türkiye’de bağışçılarda yüksek bulunma oranı %5 § 2760 gönüllü donörde 141 § 57’si ileri tetkiki kabul etmiş, 16 tanesinde çeşitli hastalıklar kanıtlanmış Fişenk Bİ, Us D, Özcebe İO, Hasçelik G, Scand J Infect Dis, 2005

ALT § HCV, HBV, CMV … § PT-NANBH’lerin %40’ı ALT değeri 45 IU/L üzeri kanlarla gelişiyor, normal ALT düzeyi olan kanlar verildiğinde bunların %23 -31’i önlenebiliyor ABD, 1981 § Tarama test duyarlılıklarındaki artış § Nonspesifik § Bağışçı kaybı: %1, 6 -4, 6 § Normal değer? ? Standardizasyon sorun. § 40 IU/L üzeri: 1973 - %2, 8, 1982 - %3, 1, 1986 - %4, 6

Anti-HBc § HCV ve HIV için de dolaylı belirteç § Ciddi donör kaybı § UÜTF donörlerinde %18 pozitif § Anti-HBc titresine göre ? § Titre yüksek ise HBV-DNA pozitifliği fazla (Eşik değer? ) § ALT ile birlikte ? § Anti-HBs ile birlikte ? Anti-HBs titresine göre ? § Anti-HBs titresi yüksek ise, HBV-DNA negatif (Eşik değer? ) § Testler hangi sırada ? § Ek zaman, emek, maliyet, karmaşa… HBV prevalansının düşük olduğu ülkeler için uygun.

HCV core Ag testleri § Ortho Clinical Diagnosis § 1. kuşak: Kalitatif, mikroplate EIA, serbest HCV Ag § 2. kuşak: Kantitatif, Anti-HCV+HCV Ag kompleksi § Eiken Chemical § Otomatize § Abbot Laboratories § Mikropartikül kemoluminesan, HCV Ag § HCV Ag ve anti-HCV’yi birlikte saptayan kombine test
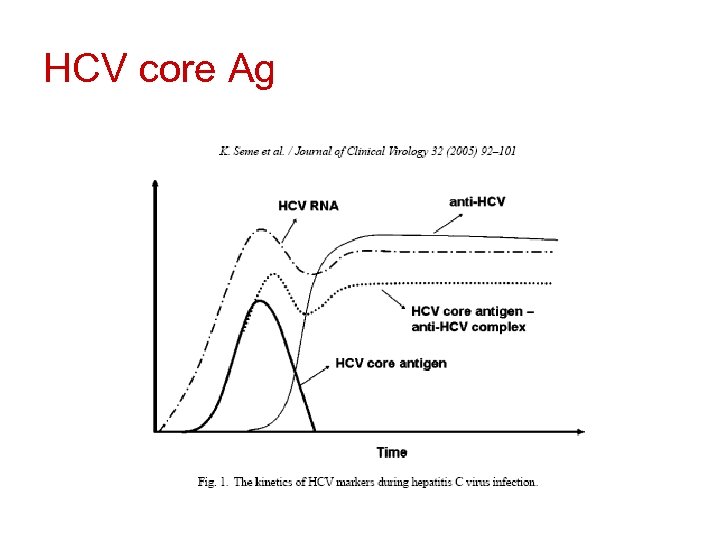
HCV core Ag

Donör popülasyonlarında yapılan 12 çalışmadan çıkan sonuçlar (314 880 bağışçı, 11 olgu yakalanmış): § 3. kuşak anti-HCV testlerinden 40 -50 gün önce saptayabiliyor § Klinik duyarlılığı NAT’a yakın § Ortalama fark 1 -5 gün § Genel olarak duyarlılığı NAT’a göre %94 -97 § Düşük risk grubunda özgüllüğü %99, 5 -99, 9 § HCV genotipleri arasında fark yok § 2. kuşak testler daha duyarlı Seme K et al, J Clin Virol, 2005

Olanakları sınırlı kan bankalarında örnekler havuzlanarak çalışılabilir mi? § 110 tane 6 örnekli havuzda, NAT’a göre § Duyarlılık %80 -82 (%95 CI: 66, 3 - 91, 4) § Özgüllük ≥%98 (%95 CI: 89, 4 -100) Sarov B et al, Transfus Med, 2007 § Serokonversiyon panelleri ile yapılan havuzlama çalışmalarında benzer sonuçlar Beer N et al, Transfusion 2006

DSÖ Önerisi: § HCV için ELISA veya basit / hızlı testler kullanılabilir § Doğrulama testleri § Line/Strip immunoassay testleri • RIBA HCV 3. 0 SIA (Chiron) • Inno-LIA HCV antibody III (Immunogenetics) § NAT § HCV core Ag saptayan yeni ELISA’lar anti-HCV testlere ek olarak kullanılabilir. Kısıtlı olanaklara sahip ülkelerde bağışçı taramasında anti-HCV’ye ek olarak NAT yerine kullanılmaları uygundur.

Çözüm arayışları § Test duyarlılıklarında artış § Pozitif prediktif değer? § Doğrulama testleri § Dolaylı testler (surrogate testler) § ALT, neopterin… § Ek testler § Anti-HBc, p 24, HCV core Ag… § NAT
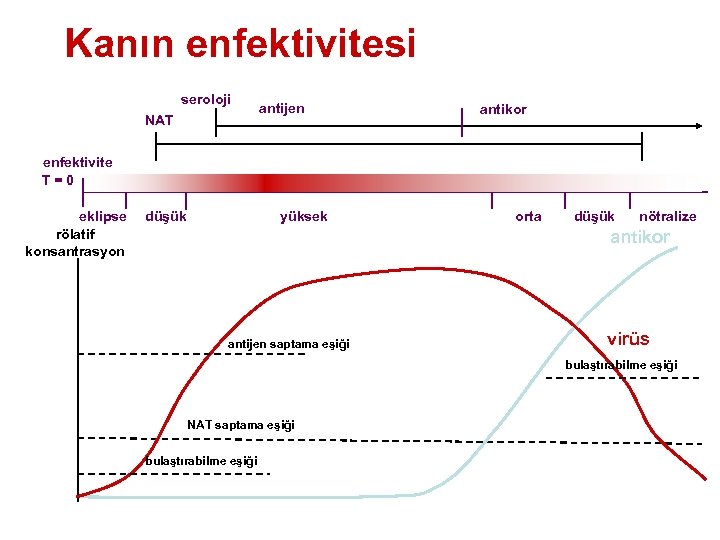
Kanın enfektivitesi seroloji NAT antijen antikor enfektivite T = 0 eklipse rölatif konsantrasyon düşük yüksek orta düşük nötralize antikor antijen saptama eşiği virüs bulaştırabilme eşiği NAT saptama eşiği bulaştırabilme eşiği
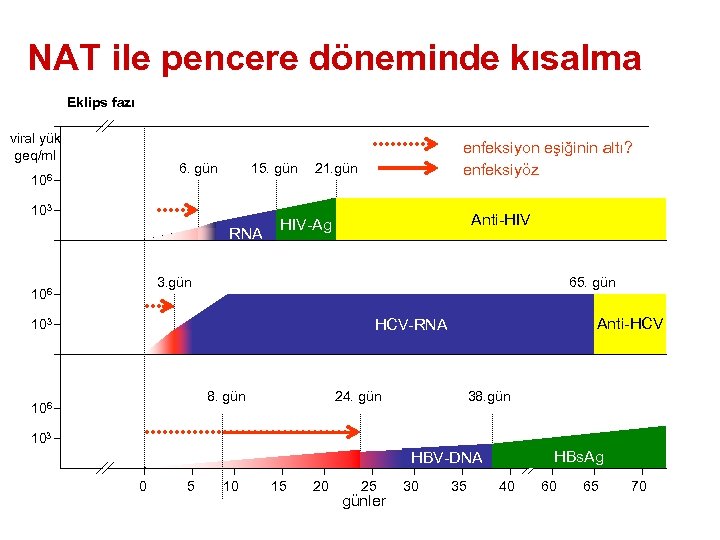
NAT ile pencere döneminde kısalma Eklips fazı viral yük geq/ml 6. gün 106 15. gün 103 RNA enfeksiyon eşiğinin altı? enfeksiyöz 21. gün Anti-HIV HIV-Ag 3. gün 106 65. gün Anti-HCV HCV-RNA 103 8. gün 106 24. gün 38. gün 103 HBs. Ag HBV-DNA 0 5 10 15 20 25 günler 30 35 40 60 65 70

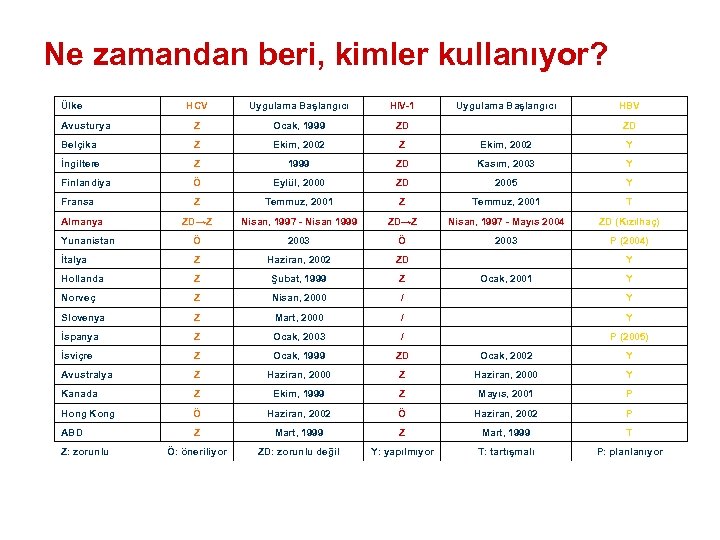
Ne zamandan beri, kimler kullanıyor? Ülke HCV Uygulama Başlangıcı HIV-1 Uygulama Başlangıcı HBV Avusturya Z Ocak, 1999 ZD ZD Belçika Z Ekim, 2002 Y İngiltere Z 1999 ZD Kasım, 2003 Y Finlandiya Ö Eylül, 2000 ZD 2005 Y Fransa Z Temmuz, 2001 T ZD→Z Nisan, 1997 - Nisan 1999 ZD→Z Nisan, 1997 - Mayıs 2004 ZD (Kızılhaç) Yunanistan Ö 2003 P (2004) İtalya Z Haziran, 2002 ZD Y Hollanda Z Şubat, 1999 Z Ocak, 2001 Y Norveç Z Nisan, 2000 / Y Slovenya Z Mart, 2000 / Y İspanya Z Ocak, 2003 / P (2005) İsviçre Z Ocak, 1999 ZD Ocak, 2002 Y Avustralya Z Haziran, 2000 Y Kanada Z Ekim, 1999 Z Mayıs, 2001 P Hong Kong Ö Haziran, 2002 P ABD Z Mart, 1999 T Ö: öneriliyor ZD: zorunlu değil Y: yapılmıyor T: tartışmalı P: planlanıyor Almanya Z: zorunlu
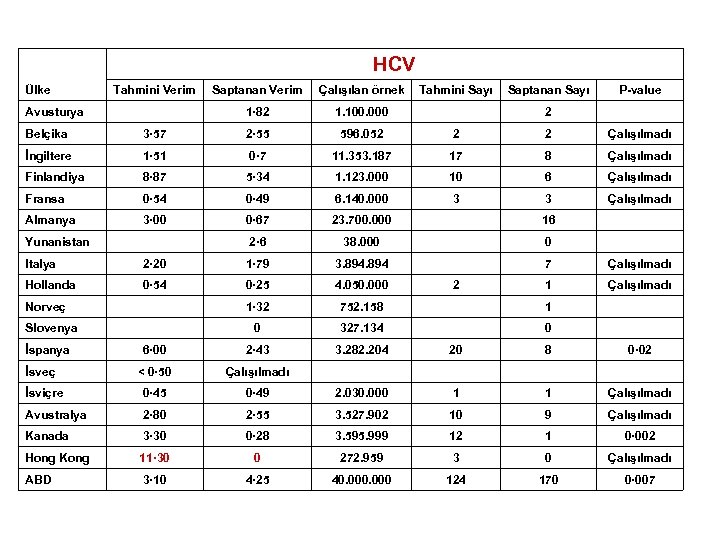
HCV Tahmini Verim Saptanan Verim Çalışılan örnek Tahmini Sayı Saptanan Sayı P-value 1· 82 1. 100. 000 2 Belçika 3· 57 2· 55 596. 052 2 2 Çalışılmadı İngiltere 1· 51 0· 7 11. 353. 187 17 8 Çalışılmadı Finlandiya 8· 87 5· 34 1. 123. 000 10 6 Çalışılmadı Fransa 0· 54 0· 49 6. 140. 000 3 3 Çalışılmadı Almanya 3· 00 0· 67 23. 700. 000 16 2· 6 38. 000 0 Italya 2· 20 1· 79 3. 894 7 Çalışılmadı Hollanda 0· 54 0· 25 4. 050. 000 2 1 Çalışılmadı Norveç 1· 32 752. 158 1 Slovenya 0 327. 134 0 6· 00 2· 43 3. 282. 204 20 8 0· 02 < 0· 50 Çalışılmadı İsviçre 0· 45 0· 49 2. 030. 000 1 1 Çalışılmadı Avustralya 2· 80 2· 55 3. 527. 902 10 9 Çalışılmadı Kanada 3· 30 0· 28 3. 595. 999 12 1 0· 002 Hong Kong 11· 30 0 272. 959 3 0 Çalışılmadı ABD 3· 10 4· 25 40. 000 124 170 0· 007 Ülke Avusturya Yunanistan İspanya İsveç
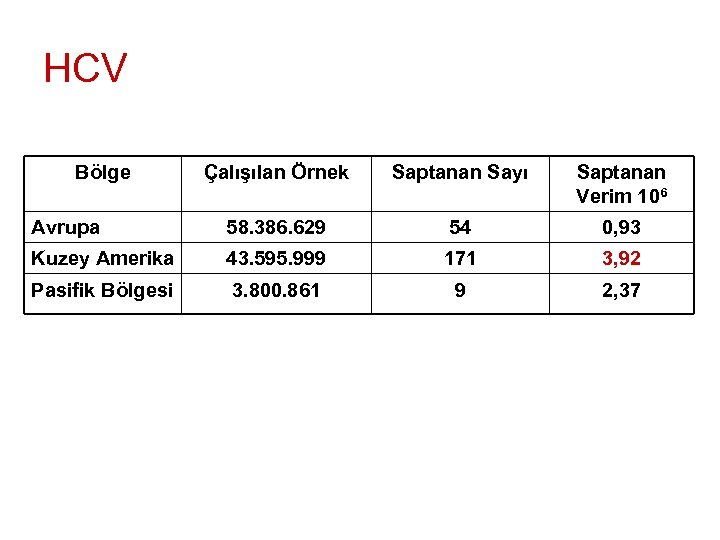
HCV Bölge Çalışılan Örnek Saptanan Sayı Saptanan Verim 106 Avrupa 58. 386. 629 54 0, 93 Kuzey Amerika 43. 595. 999 171 3, 92 Pasifik Bölgesi 3. 800. 861 9 2, 37
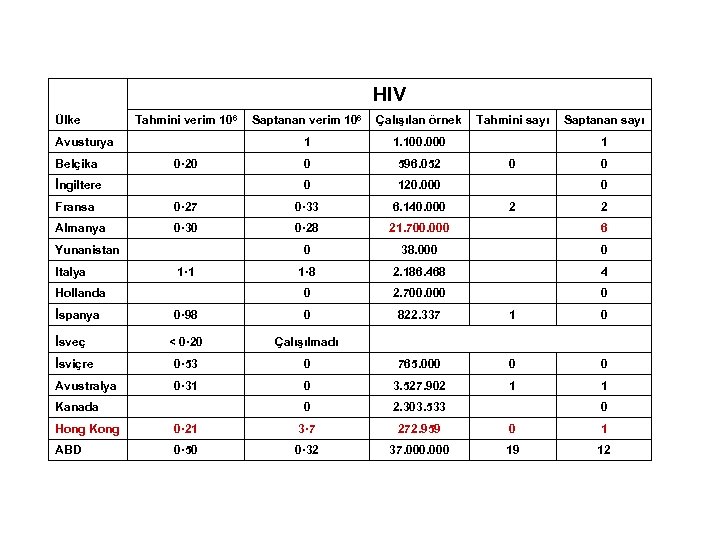
HIV Tahmini verim 106 Saptanan verim 106 Çalışılan örnek Tahmini sayı Saptanan sayı 1 1. 100. 000 1 Belçika 0· 20 0 596. 052 0 0 İngiltere 0 120. 000 0 Fransa 0· 27 0· 33 6. 140. 000 2 2 Almanya 0· 30 0· 28 21. 700. 000 6 0 38. 000 0 1· 1 1· 8 2. 186. 468 4 Hollanda 0 2. 700. 000 0 İspanya 0· 98 0 822. 337 1 0 < 0· 20 Çalışılmadı İsviçre 0· 53 0 765. 000 0 0 Avustralya 0· 31 0 3. 527. 902 1 1 0 2. 303. 533 0 Hong Kong 0· 21 3· 7 272. 959 0 1 ABD 0· 50 0· 32 37. 000 19 12 Ülke Avusturya Yunanistan Italya İsveç Kanada
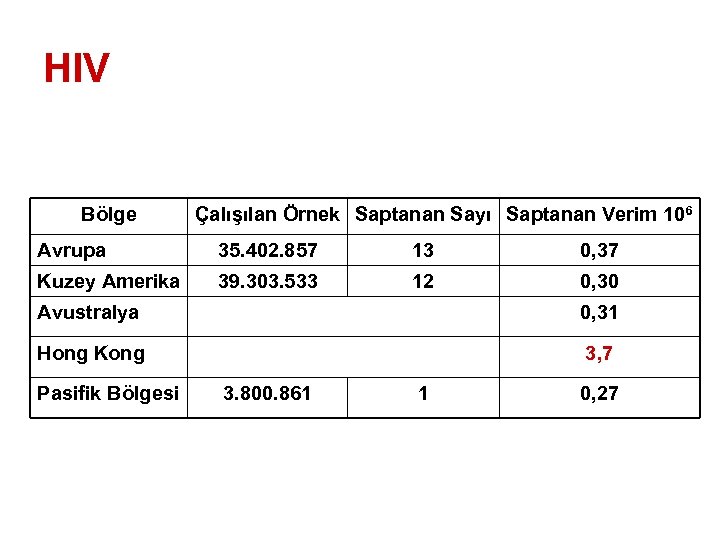
HIV Bölge Çalışılan Örnek Saptanan Sayı Saptanan Verim 106 Avrupa 35. 402. 857 13 0, 37 Kuzey Amerika 39. 303. 533 12 0, 30 Avustralya 0, 31 Hong Kong 3, 7 Pasifik Bölgesi 3. 800. 861 1 0, 27
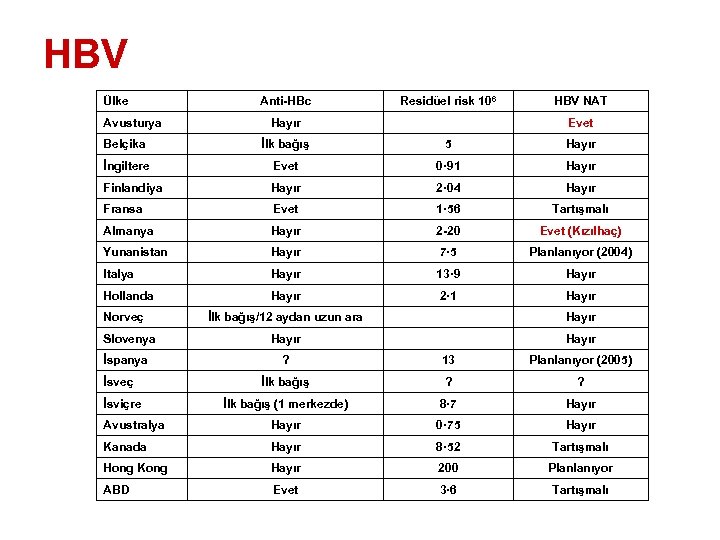
HBV Ülke Anti-HBc Residüel risk 106 HBV NAT Hayır Evet Belçika İlk bağış 5 Hayır İngiltere Evet 0· 91 Hayır Finlandiya Hayır 2· 04 Hayır Fransa Evet 1· 56 Tartışmalı Almanya Hayır 2 -20 Evet (Kızılhaç) Yunanistan Hayır 7· 5 Planlanıyor (2004) Italya Hayır 13· 9 Hayır Hollanda Hayır 2· 1 Hayır İlk bağış/12 aydan uzun ara Hayır ? 13 Planlanıyor (2005) İlk bağış ? ? İlk bağış (1 merkezde) 8· 7 Hayır Avustralya Hayır 0· 75 Hayır Kanada Hayır 8· 52 Tartışmalı Hong Kong Hayır 200 Planlanıyor ABD Evet 3· 6 Tartışmalı Avusturya Norveç Slovenya İspanya İsveç İsviçre

?
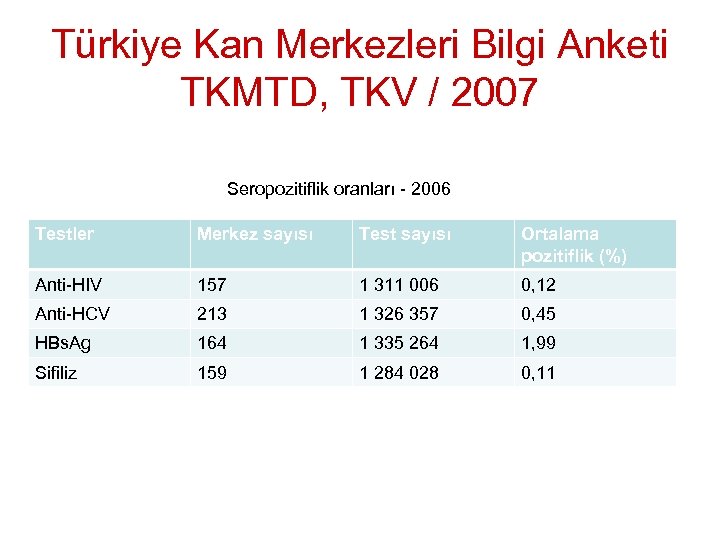
Türkiye Kan Merkezleri Bilgi Anketi TKMTD, TKV / 2007 Seropozitiflik oranları - 2006 Testler Merkez sayısı Test sayısı Ortalama pozitiflik (%) Anti-HIV 157 1 311 006 0, 12 Anti-HCV 213 1 326 357 0, 45 HBs. Ag 164 1 335 264 1, 99 Sifiliz 159 1 284 028 0, 11

NAT screning of HBV in blood donors Kemahlı S, Solaz NN, Bozdayı M, Cin S Transfus Clin Biol, 8(S 1): 18 s, 2001 ISBT VIIth European Congress, Paris § 7372 bağışçı § HBs. Ag, anti-HBc Ig. G+Ig. M, anti-HCV, anti-HIV • Mikropartikül ELISA, Abbot Axsym, Chicago, USA § NAT 8 örnekli havuzlarda çalışılmış (in-hause) § NAT duyarlılık 100 genom/ml

NAT screning of HBV in blood donors Kemahlı S, Solaz NN, Bozdayı M, Cin S Transfus Clin Biol, 8(S 1): 18 s, 2001 ISBT VIIth European Congress, Paris § 7372 bağışçı § HBs. Ag (+) %2 (n=149) § Anti-HBc Ig. G-Ig. M (+) %10, 8 (n=789) § İzole anti-HBc(+) %3, 1 (n=232) § İzole anti-HBc(+), HBV-DNA(+) %0, 03 (n=2) § Ayrıca 2 örnekte anti-HBc ve anti-HBs birlikte pozitif § Seroloji ile atlanan HBV: 1 / 3686
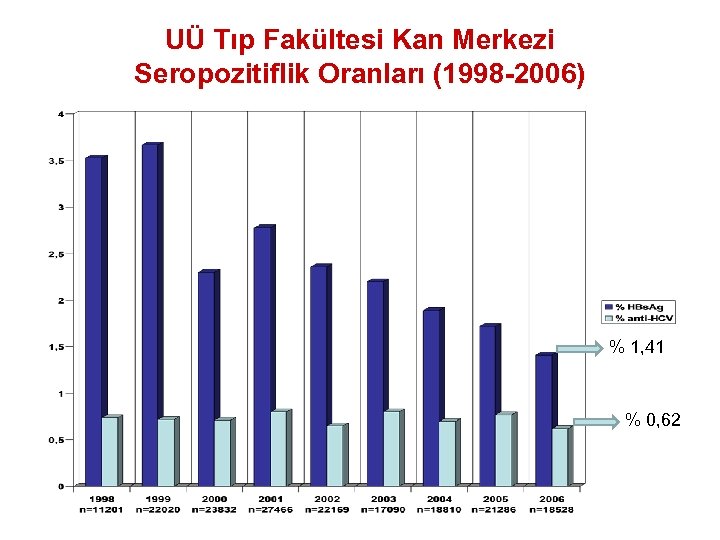
UÜ Tıp Fakültesi Kan Merkezi Seropozitiflik Oranları (1998 -2006) % 1, 41 % 0, 62

İzole anti-HBc Ig. G+Ig. M pozitif donörlerde Real-Time PCR ile HBV-DNA araştırılması (Uludağ Üniversitesi) Bal H, Heper Y, Kumaş T, Mıstık R, Töre O II. Ulusal Kan Merkezleri ve Transfüzyon Tıbbı Kongresi, 2008 § 9282 HBs. Ag negatif bağışçı § Anti-HBc Ig. G+Ig. M pozitif bulunanlarda anti-HBs § Ortho Clinical Diagnostics, Vitros, Brazil § İzole Anti-HBc pozitif örneklerde PCR (Real-time) § Örnekler tek çalışılmış, havuzlama yapılmamıştır. • Otomatik ekstarktör: Presicion System Science Co. Ltd. , Magtration Maga. Zorb DNA Common Kit 200, Japan • PCR kiti: QIAGEN, Artus 3000, Germany • PCR cihazı: Corbett Research, Rotor-Gene 2000/3000, Australia

İzole anti-HBc Ig. G+Ig. M pozitif donörlerde Real-Time PCR ile HBV-DNA araştırılması (Uludağ Üniversitesi) Bal H, Heper Y, Kumaş T, Mıstık R, Töre O II. Ulusal Kan Merkezleri ve Transfüzyon Tıbbı Kongresi, 2008 § 9282 HBs. Ag negatif bağışçı § 1679 Anti-HBc pozitif (%18) § 218 izole anti-HBc pozitif (% 2, 7) § 1 HBV-DNA pozitif (%0. 012) Çalışma dışı kalan serumlar nedeniyle 1 / 8333

Sağlıklı Kan Bağışçılarında Hepatit B Virus DNA’sının Araştırılması (S. B. Ankara Eğitim ve Araştırma Hastanesi) Karakoç AE, Berkem R, Beyaz E II. Ulusal Kan merkezleri ve Transfüzyon Tıbbı Kongresi, 2008 § 4484 HBs. Ag negatif bağışçı § 187 havuz (186’sı 24’lük, bir tanesi 20 örnekli havuz) § PCR: Robogene Hepatitis B Virus Quantification Kit, Al Roboscreen Gmb. H, Leipzig, Almanya) § Üç havuz reaktif, ikisi tekrarlayan reaktif § Tekrarlayan reaktif iki havuzdan birinde tek, diğerinde iki § § § örnekte reaktif sonuç Bu örnekler tekrar çalışıldığında biri negatif, ikisi reaktif İki reaktif örnek ELISA ile negatif ve bu iki örneğin bağışçılarından alınan yeni örnekler de negatif Pozitif sonuç yok, PCR’da hatalı pozitiflik %0. 04

Anti-HCV negatif donörlerde Real-Time PCR ile HCV-RNA araştırılması Kabaş M, Heper Y, Mıstık R, Töre O § 2592 anti-HCV negatif donör § 24’lük 108 havuz § Bir havuzda pozitiflik § 24 örnek tek çalışıldığında tümü negatif
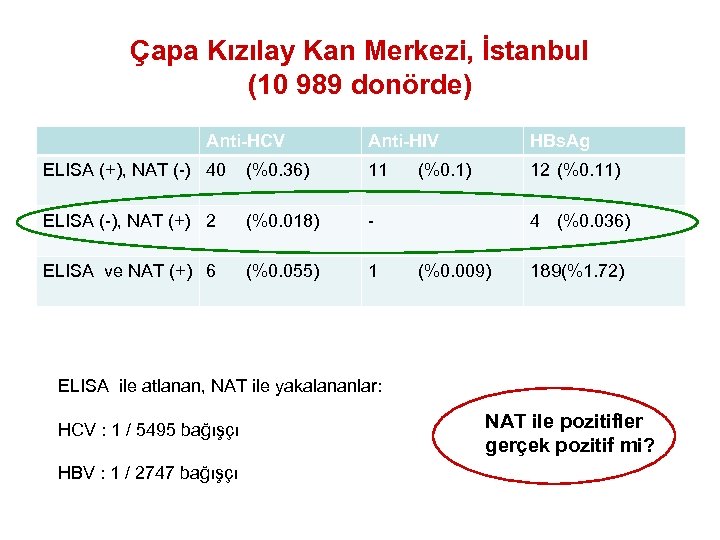
Çapa Kızılay Kan Merkezi, İstanbul (10 989 donörde) Anti-HCV Anti-HIV HBs. Ag ELISA (+), NAT (-) 40 (%0. 36) 11 (%0. 1) 12 (%0. 11) ELISA (-), NAT (+) 2 (%0. 018) - 4 (%0. 036) ELISA ve NAT (+) 6 (%0. 055) 1 (%0. 009) 189(%1. 72) ELISA ile atlanan, NAT ile yakalananlar: HCV : 1 / 5495 bağışçı HBV : 1 / 2747 bağışçı NAT ile pozitifler gerçek pozitif mi?

NAT – farklı uygulamalar § MP-NAT ? ID-NAT ? Havuz büyüklüğü ? § MP HBV-NAT’ın HBs. Ag + anti-HBc’ye üstünlüğü yok, ancak ID-NAT olabilir § Bazı ülkelerde sadece HCV ve HIV NAT § Bazı ülkelerde HBV+HCV+HIV NAT § Almanya, Japonya § Önce ELISA, seronegatiflere NAT § Hızlı (kart test), negatiflere ELISA / NAT § SADECE NAT ? ? ? § Ülkemiz için ? ? ? § NAT’a rağmen enfeksiyon bulaşı bildirilmiş

En çok tartışılan ve net kararın olmadığı HBV
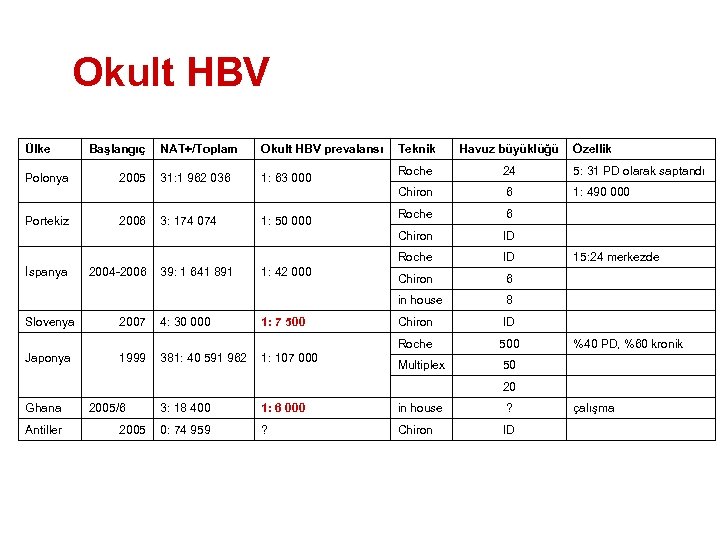
Okult HBV Ülke 2006 Okult HBV prevalansı 31: 1 962 036 1: 63 000 1: 50 000 Portekiz 3: 174 074 İspanya 2004 -2006 39: 1 641 891 1: 42 000 4: 30 000 1: 7 500 Slovenya Japonya Ghana Antiller 2007 1999 Havuz büyüklüğü Roche 24 5: 31 PD olarak saptandı Chiron 6 1: 490 000 Roche 6 Chiron ID ID 15: 24 merkezde Chiron 6 in house 8 Chiron ID Roche 2005 NAT+/Toplam Teknik Roche Polonya Başlangıç Özellik 500 %40 PD, %60 kronik Multiplex 50 20 381: 40 591 962 1: 107 000 2005/6 3: 18 400 1: 6 000 in house ? çalışma 0: 74 959 ? Chiron ID 2005

HBV NAT Kullanmayan Ülkeler

Fransa § Genel popülasyonda kronik taşıyıcı %0, 2 -0, 5 § HBV insidansı 2 -3 bin/yıl yeni olgu § 1994 sonrası rutin aşı § HBs. Ag pozitifliği Düzenli bağışçıda İlk bağışda Ortalama 0, 02: 10 000 9, 3: 10 000 1, 4: 10 000

Fransa § Kan merkezlerinin %50’den fazlası sensitivitesi 0, 05 -0, 08 ng/dl HBs. Ag test kitleri kullanıyor § A-HBc’de de sensitif yöntemler kullanılıyor § Sensitif ELISA ile PD 20, MP NAT ile 15 gün § ELISA ile saptanan 2 olgu MP NAT ile negatif

Fransa § Transfüzyona bağlı HBV son 4 yılda 0 § 1985 -2003 4 olgu, PD, DNA ile saptanmış § Toplam bağış: 2, 5 milyon ünite/yıl § Transfüzyona bağlı residüel risk 1: 1 700 000 § Risk altındaki alıcı sayısı 2

Fransa § HBV enfekte kan alanlarda kronik HBV gelişme riski %4, § Kr KC hastalığından ölüm Kronik HBV enfeksiyonluların %0, 97’si (Pereira ve ark) § Özetle 12 ya da 13 yılda 1 TBHBV görülecek ve 50 yılda 1 kişi Kr KC hastalığından ölecek

İngiltere § HBV riski 1: 60 000 – 250 000 § A-HBc prevalansı %0, 4 § Son 10 yılda PT HBV çok az § NAT düşünülmüyor § NAT’a alternatif A-HBc öneriliyor
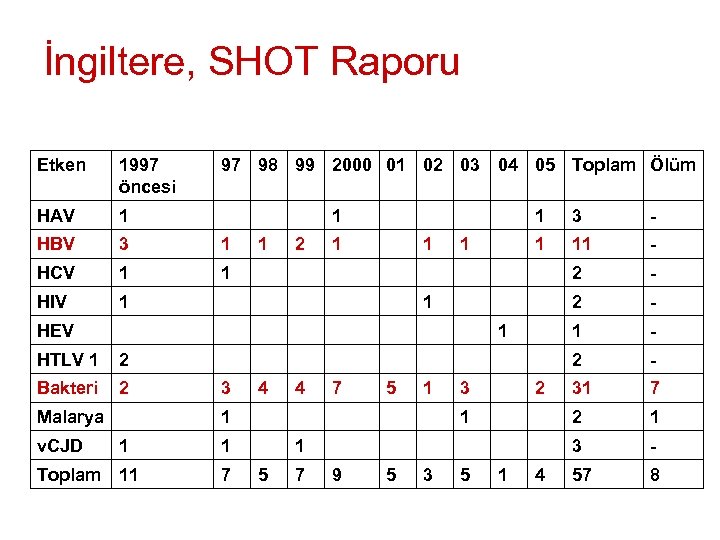
İngiltere, SHOT Raporu Etken 1997 öncesi 97 98 99 2000 01 02 03 04 05 Toplam Ölüm HAV 1 HBV 3 1 HCV 1 1 HIV 1 1 - 2 - 1 - 31 7 2 1 11 1 3 1 - 2 2 3 2 1 1 - 57 8 1 HEV 1 HTLV 1 2 Bakteri 2 Malarya v. CJD 3 4 4 7 5 1 1 1 Toplam 11 2 1 1 7 3 1 5 7 9 5 3 5 1 4

Amerika § FDA, 2005’de 2 HBV DNA kitine onay vermiş § Maliyet etkin bulmuyor ve bağışçılarda kullanmıyor § A-HBc rutin ve NAT’a alternatif § Roche Ampliscreen ile verim 1: 300 000

Amerika HBV DNA Pozitif % Verim Takip 395 4 1. 01 1: 49 000 Yapılmadı 2 3000 19 0. 63 1: 37 000 Yapılmadı 3 2900 12 0. 41 1: 48 942 6 (NAT negatif, 3'ü a-HBs pozitif) Çalışma Test* 1 *: HBs. Ag negatif, a-HBc pozitif örneklerde HBV DNA çalışması. § Amerika’da yayınlanmış üç ayrı çalışmanın verileri

Amerika Test* 63 000 HBs. Ag (+) DNA (+) % HBs. Ag (-) DNA (-) % 1080 2 1874 3 59 797 § Amerikan Kızılhaç’ının üç yıllık çalışma (A-HBc § pozitif bağışçılarda HBV DNA çalışması) verileri Sonuç: A-HBc reaktiflerde DNA pozitifliği %0, 96 95

Norveç § Tüm bağışçılarda HBs. Ag, yeni bağışçılarda (bir önceki bağışın üzerinden 6 ay geçmişse) A-HBc bakılıyor § NAT yerine A-HBc’nin yeterli olduğu düşünülüyor

Kanada § 5 yıllık (2001 -2005) verilerin retrospektif değerlendirilmesi § 4 140 862 tam kan bağışçısında residüel riskler: § § HIV için 1: 7. 8 milyon, HCV için 1: 2, 3 milyon, HBV için 1: 153 000 HIV ve HCV’de residüel risk çok düşük NAT verimi de düşük rutinde kullanımı uygun değil HBV’de durum daha riskli Sensitivitesi yüksek HBs. Ag ve a-HBc testleri kullanılarak risk azaltılmalı NAT uygun değil

HBV NAT Kullanan Ülkeler

Japonya § Tarama yöntemi: Aglütinasyon § Seronegatif donörlerde MP NAT § NAT (+) ise ELISA ile HBs. Ag, A-HBc ve A-HBs § Viral yük belirleme ve DNA sekans analizi
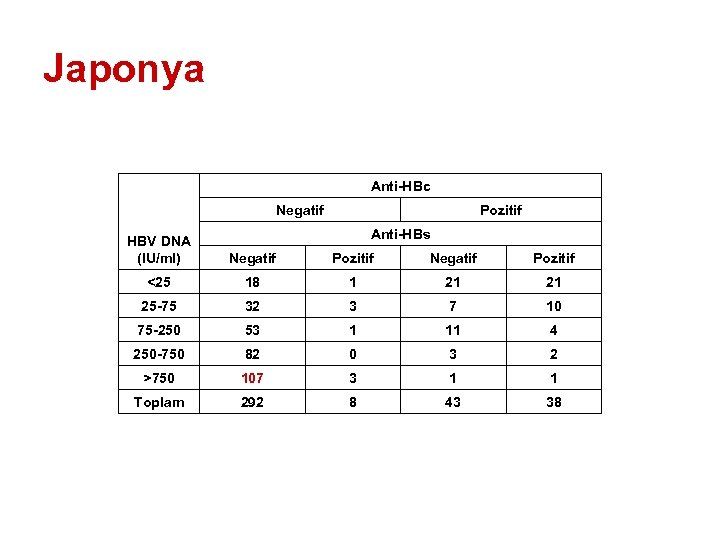
Japonya Anti-HBc Negatif Pozitif Anti-HBs HBV DNA (IU/ml) Negatif Pozitif <25 18 1 21 21 25 -75 32 3 7 10 75 -250 53 1 11 4 250 -750 82 0 3 2 >750 107 3 1 1 Toplam 292 8 43 38

Japonya § 15 721 seronegatif örnekte 158 NAT + § 95 geç dönem (GD), 60 erken dönem (PD) § 60 PD olgudan 22’si incelenmiş 11’i alıcıda serokonversiyon § 95 GD olgudan 33’ü incelenmiş 1’i alıcıda serokonversiyon

İsviçre, Algoritma § İlk bağış: HBs. Ag, A-HBc, HBV NAT MP § A-HBc tekrarlayan reaktifse iki farklı yöntemle konfirmasyon + A-HBs + HBV NAT ID § 262: 18 143 A-HBc +, NAT – § Bağışçı örnekleri 5 yıl boyunca 1 ml ve -30 derecede saklanıyor, hasta örnekleri saklanmıyor

Almanya § Uzun zamandır HBV NAT kullanıyor § In-house NAT ve zenginleştirme ile 2: 3, 6 x 106 pencere dönemi 4: 3, 6 x 106 a-HBc (+) kronik taşıyıcı § Rutinde a-HBc taranmıyor § Karşıt görüş: ID NAT kullanılsa bile a-HBc taranmalıdır: § Geç dönem HBV taşıyıcılarında HBs. Ag ve a-HBc reaktif olsa dahi DNA düzeyi çok düşük olduğundan NAT negatif sonuç verebilir (%3) § HBs. Ag reaktifken NAT negatif ise HBs. Ag’nin yalancı pozitifliği, HBs. Ag kontaminantları veya primerlardan kaçan HBV mutant formları akla gelebilir

NAT her zaman doğruyu bulur mu?

Slovenya Örnek Procleix Ultrio HBs. Ag A-HBc A-HBs Roche Amplicor 1 + + - Gösterilemedi 2 + - - + + Gösterilemedi 3 + + - < 60 IU/ml 4 + + - 491 IU/ml 30 000 örnek / 3 ay 4 HBV DNA pozitif

İngiltere & Gana § 16 yaşta HBs. Ag %15 pozitif § 40 yaşta A-HBc %100 pozitif § Bağışçılarda okult HBV 1: 62 § Viral yük < 500 IU/ml, 10’luk MP NAT %50 yakalıyor § Viral yük < 100 IU/ml iken enfeksiyöz olmadığı kanıtlanamamış

Çin, Bize benzer bir örnek olabilir mi?

Çin, Shenzen § 3 yıllık retrospektif bir çalışma § Kapasitesi 50 000 bağış / yıl olan bir merkez § Bağışçıların %60’ı ilk bağış ve genç popülasyon § Modifiye bir hesaplama ile residüel riskler belirlenmiş § Buna göre: § § HBV için 1: 17 500, HCV için 1: 60 000; HIV için 1: 900 000 A-HBc reaktivitesi ve pahalılığı nedeniyle düşünülmemiş Algoritma: ……….

Çin, Shenzen Test Ulusal Kit İthal Kit A-HCV Hızlı çubuk test 3 rd gen Ortho Konfirmasyon Chiron, RIBA 3 rd HBs. Ag Hızlı çubuk test Auszyme Abbott Ortho, Neurtalization A-HIV Hızlı çubuk test Melia, Organon Melia, WB

Çin, Shenzen Sonuç (residüel riskin azaltılması için öneriler): § Maliyeti fazla artırmadan HBV için 0, 1 ng/ml’den daha duyarlı bir EIA kiti kullanmak § Universal HBV aşılaması yapmak § 4. gen. HCV Ab-Ag kitlerine geçmek § 4. gen. HIV Ab-Ag kitlerine geçmek § Düzenli bağış aralığını 180 gün üzerine çekmek

Yeni Moda A-HBs

Trend…. § A-HBc pozitif § A-HBs’nin yüksek (>100 IU/ml) titre pozitif kan kullanılır Çünkü; yeterli nötralizan antikorların varlığında viral konsantrasyon son derece düşüktür

Kan Kullanılır mı? § CMV, EBV, VZV, HBV, B 19 vb. nin immün direnç baskınlandığında (hatta güçlü sellüler ve nötralizan antikorları olan hastalarda) reaktive olduğu gösterilmiş § Çoğu alıcının immün direnci düşük/baskı altında § Anti-HBs pozitif / HBV DNA negatif bağışçıdan alınan KC’in oldukça zayıf viral yük ve nötralizan antikorlarının varlığına rağmen enfeksiyon bulaştırdığı gösterilmiş

İkinci örnek § § § KLL’li bir erkek hastanın Klorambusil’le tedavisinden 1 yıl sonra Fludarabin başlanmış ve hastada akut HBV gözlenmiş Klinisyen PT hepatit tanısı koymuş ve hastanın öyküsü incelenmiş Yüzlerce ünite transfüzyon almış olan hastanın KLL tanısı almadan önce aşılandığı ve hem a-HBc hem de a-HBs’sinin pozitif olduğu saptanmış Sonraki araştırmalarda enfeksiyonun 25 yıl önce Down sendromlu ve Kr KC hastalıklı bir kardeşi olan eşinden cinsel yolla aldığı belirlenmiş Bu kişi ile hastanın yüksek düzeyde sekans homolojisi gösterdiği saptanmış ve enfeksiyonun 25 yıl sonra reaktive olduğu kanıtlanmıştır İmmün yetmezliğin nedeni ise Klorambusil’e oranla çok daha ciddi etki yapan Fludarabin olarak belirlenmiş

Öneri? ? ? § Transfüzyon almış bir hastada herhangi bir viral enfeksiyon saptandığından sorumlu transfüzyondur § Posttransfüzyon enfeksiyon: transfüzyon bulaşı mı reaktivasyon mu anlaşılmalıdır § O zaman: İmmün sistemi baskılanmış hastalarda transfüzyon öncesi yeterli miktarda örnek alıp saklanmalıdır √ √

SONUÇ Daha güvenli transfüzyon = yüksek teknolojiye bağımlılık = artan maliyetler = iyi organize olma gerekliliği

Aklımızda bulunsun Ülkemizdeki kan bankalarının tümü: § Uygun yöntem kullanıyor mu? § Yöntemi uygun kullanıyor mu? § Algoritma doğru mu? § ALT, Anti-HBc, Neopterin, HCV Core AG gibi testleri uygulayabilir miyiz? § Kalite kontrol? ?

BİZİM GÖRÜŞÜMÜZ § Önce PTH oranlarımızı belirleyelim § Büyük merkezlerde NAT deneyelim § Tarama yöntemimizi ve algoritmamızı netleştirelim § NAT yapıp yapmayacağımıza § Yapacaksak birlikte veya yerine ne yapacağımıza sonuca göre karar verelim
03f6d32f371ba00ba8c79539e2ecc7bd.ppt