мои углеводы.ppt
- Количество слайдов: 35
 Кафедра химии Тема лекции: Углеводы. Моносахариды
Кафедра химии Тема лекции: Углеводы. Моносахариды
 УГЛЕВОДЫ Важнейшие химические соединения растительного и животного мира ( 12 % сухого веса любых организмов составляют углеводы) Состав Сn(H 2 O)m , где n m Примеры: С 6 Н 12 О 6 – глюкоза, С 12 Н 22 О 11 - сахароза, (С 6 Н 10 О 5)х – крахмал, клетчатка Большинство сахаров Сn(H 2 O)n , где n 4 Окончание «оза» - принадлежность к классу углеводов
УГЛЕВОДЫ Важнейшие химические соединения растительного и животного мира ( 12 % сухого веса любых организмов составляют углеводы) Состав Сn(H 2 O)m , где n m Примеры: С 6 Н 12 О 6 – глюкоза, С 12 Н 22 О 11 - сахароза, (С 6 Н 10 О 5)х – крахмал, клетчатка Большинство сахаров Сn(H 2 O)n , где n 4 Окончание «оза» - принадлежность к классу углеводов
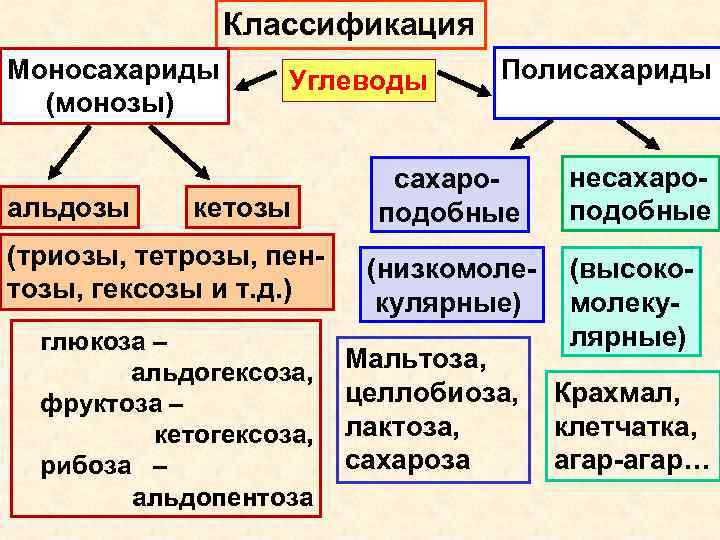 Классификация Моносахариды (монозы) альдозы Углеводы кетозы (триозы, тетрозы, пентозы, гексозы и т. д. ) глюкоза – альдогексоза, фруктоза – кетогексоза, рибоза – альдопентоза Полисахариды сахароподобные (низкомолекулярные) Мальтоза, целлобиоза, лактоза, сахароза несахароподобные (высокомолекулярные) Крахмал, клетчатка, агар-агар…
Классификация Моносахариды (монозы) альдозы Углеводы кетозы (триозы, тетрозы, пентозы, гексозы и т. д. ) глюкоза – альдогексоза, фруктоза – кетогексоза, рибоза – альдопентоза Полисахариды сахароподобные (низкомолекулярные) Мальтоза, целлобиоза, лактоза, сахароза несахароподобные (высокомолекулярные) Крахмал, клетчатка, агар-агар…
![МОНОСАХАРИДЫ Моносахариды – это многоатомные спирты, содержащие карбонильную группу Окисление глицерина: [O] * + МОНОСАХАРИДЫ Моносахариды – это многоатомные спирты, содержащие карбонильную группу Окисление глицерина: [O] * +](https://present5.com/presentation/101307319_182862747/image-4.jpg) МОНОСАХАРИДЫ Моносахариды – это многоатомные спирты, содержащие карбонильную группу Окисление глицерина: [O] * + глицериновый альдегид диоксиацетон альдотриоза кетотриоза глицероза
МОНОСАХАРИДЫ Моносахариды – это многоатомные спирты, содержащие карбонильную группу Окисление глицерина: [O] * + глицериновый альдегид диоксиацетон альдотриоза кетотриоза глицероза
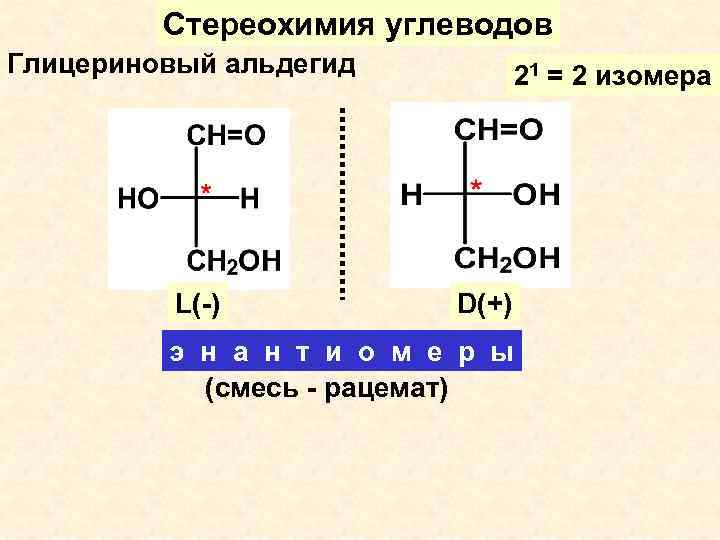 Стереохимия углеводов Глицериновый альдегид L(-) 21 = 2 изомера D(+) э н а н т и о м е р ы (смесь - рацемат)
Стереохимия углеводов Глицериновый альдегид L(-) 21 = 2 изомера D(+) э н а н т и о м е р ы (смесь - рацемат)
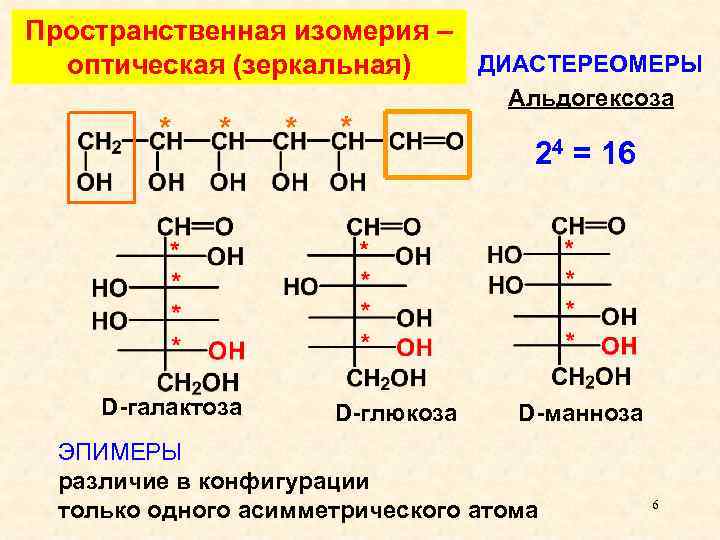 Пространственная изомерия – ДИАСТЕРЕОМЕРЫ оптическая (зеркальная) * * D-галактоза * * D-глюкоза Альдогексоза 24 = 16 D-манноза ЭПИМЕРЫ различие в конфигурации только одного асимметрического атома 6
Пространственная изомерия – ДИАСТЕРЕОМЕРЫ оптическая (зеркальная) * * D-галактоза * * D-глюкоза Альдогексоза 24 = 16 D-манноза ЭПИМЕРЫ различие в конфигурации только одного асимметрического атома 6
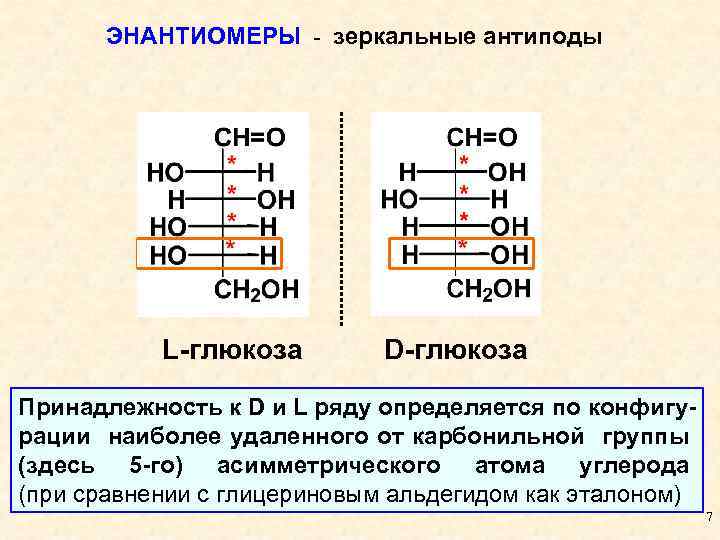 ЭНАНТИОМЕРЫ - зеркальные антиподы L-глюкоза D-глюкоза Принадлежность к D и L ряду определяется по конфигурации наиболее удаленного от карбонильной группы (здесь 5 -го) асимметрического атома углерода (при сравнении с глицериновым альдегидом как эталоном) 7
ЭНАНТИОМЕРЫ - зеркальные антиподы L-глюкоза D-глюкоза Принадлежность к D и L ряду определяется по конфигурации наиболее удаленного от карбонильной группы (здесь 5 -го) асимметрического атома углерода (при сравнении с глицериновым альдегидом как эталоном) 7
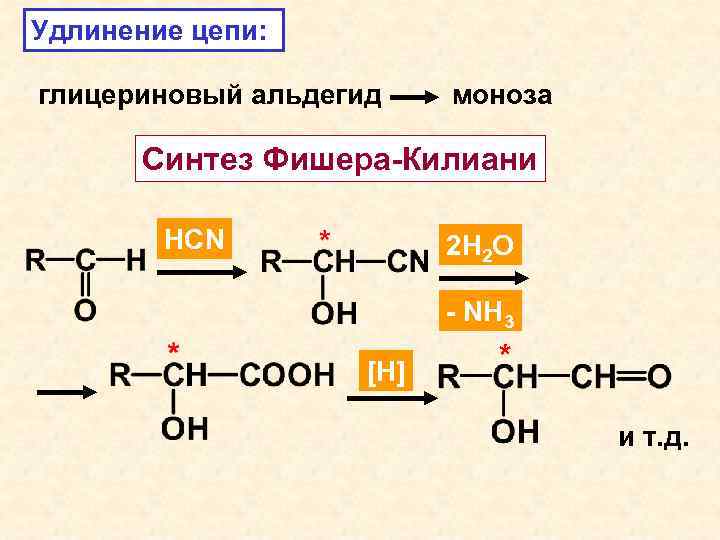 Удлинение цепи: глицериновый альдегид моноза Синтез Фишера-Килиани HCN 2 H 2 O - NH 3 [H] * и т. д.
Удлинение цепи: глицериновый альдегид моноза Синтез Фишера-Килиани HCN 2 H 2 O - NH 3 [H] * и т. д.
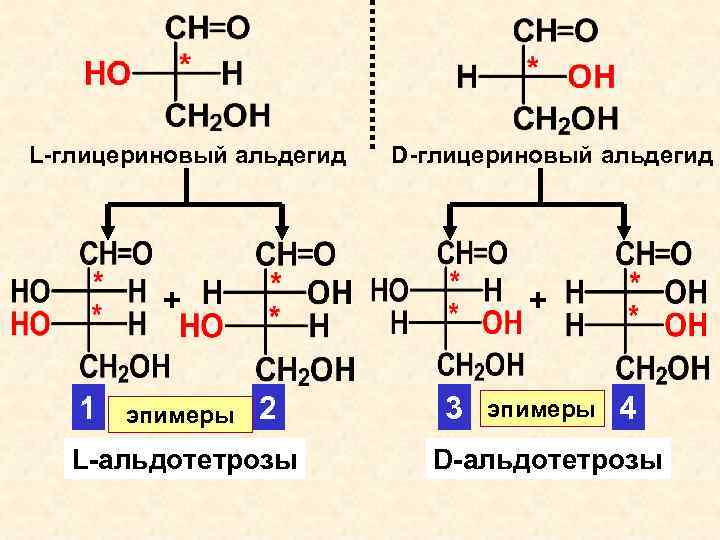 L-глицериновый альдегид D-глицериновый альдегид + + 1 эпимеры 2 L-альдотетрозы 3 эпимеры 4 D-альдотетрозы
L-глицериновый альдегид D-глицериновый альдегид + + 1 эпимеры 2 L-альдотетрозы 3 эпимеры 4 D-альдотетрозы
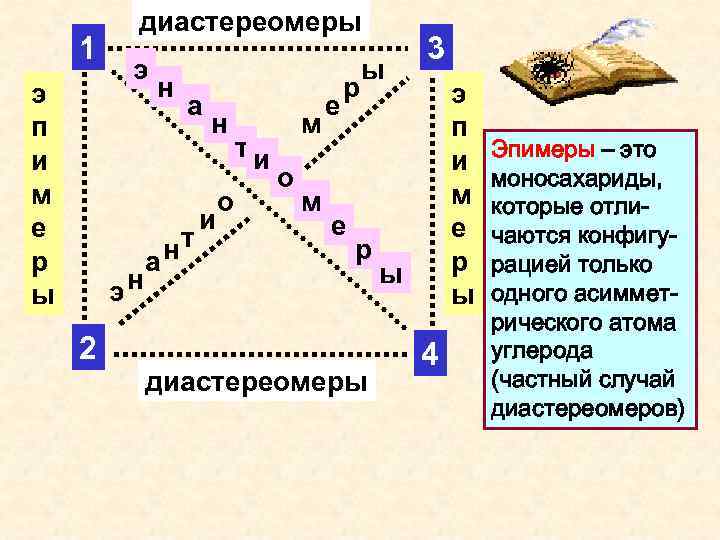 1 э п и м е р ы диастереомеры э эн н а а нт н и о ти м о м е р е ы р 2 диастереомеры 3 э п и м е р ы ы 4 Эпимеры – это моносахариды, которые отличаются конфигурацией только одного асимметрического атома углерода (частный случай диастереомеров)
1 э п и м е р ы диастереомеры э эн н а а нт н и о ти м о м е р е ы р 2 диастереомеры 3 э п и м е р ы ы 4 Эпимеры – это моносахариды, которые отличаются конфигурацией только одного асимметрического атома углерода (частный случай диастереомеров)
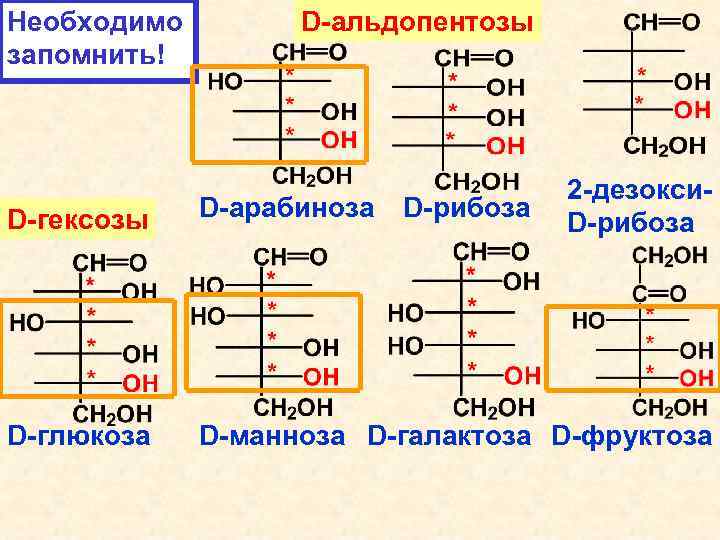 Необходимо запомнить! D-альдопентозы D-рибоза 2 -дезокси. D-рибоза D-гексозы D-арабиноза D-глюкоза D-манноза D-галактоза D-фруктоза
Необходимо запомнить! D-альдопентозы D-рибоза 2 -дезокси. D-рибоза D-гексозы D-арабиноза D-глюкоза D-манноза D-галактоза D-фруктоза
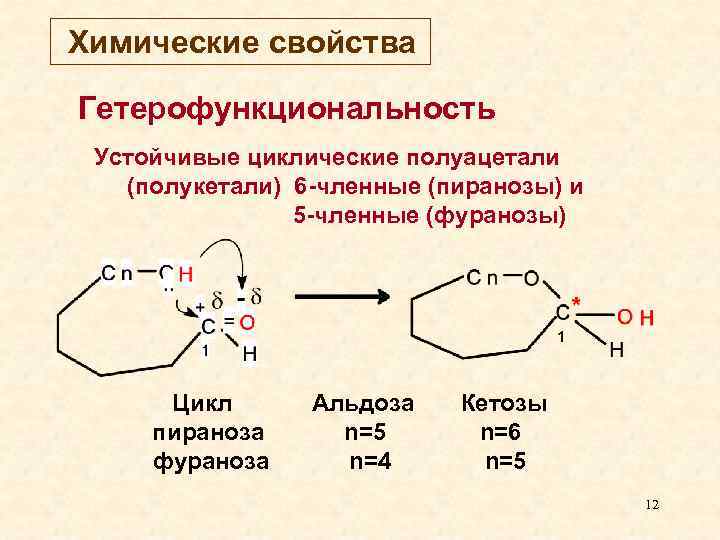 Химические свойства Гетерофункциональность Устойчивые циклические полуацетали (полукетали) 6 -членные (пиранозы) и 5 -членные (фуранозы) Цикл пираноза фураноза Альдоза n=5 n=4 Кетозы n=6 n=5 12
Химические свойства Гетерофункциональность Устойчивые циклические полуацетали (полукетали) 6 -членные (пиранозы) и 5 -членные (фуранозы) Цикл пираноза фураноза Альдоза n=5 n=4 Кетозы n=6 n=5 12
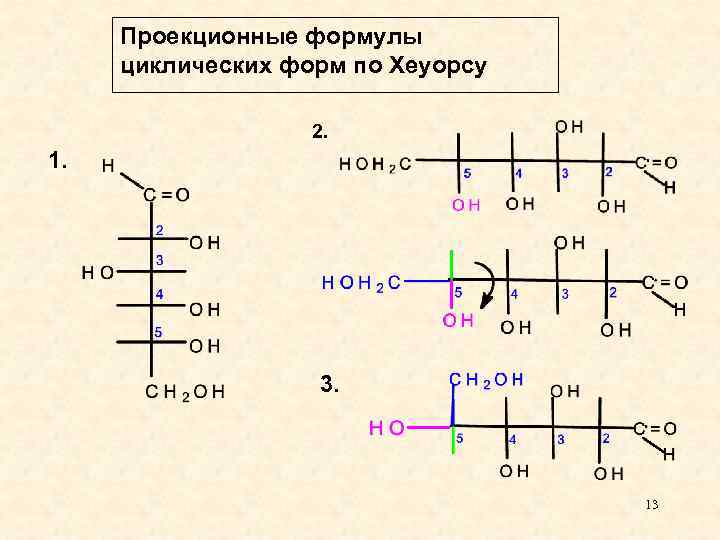 Проекционные формулы циклических форм по Хеуорсу 2. 1. 3. 13
Проекционные формулы циклических форм по Хеуорсу 2. 1. 3. 13
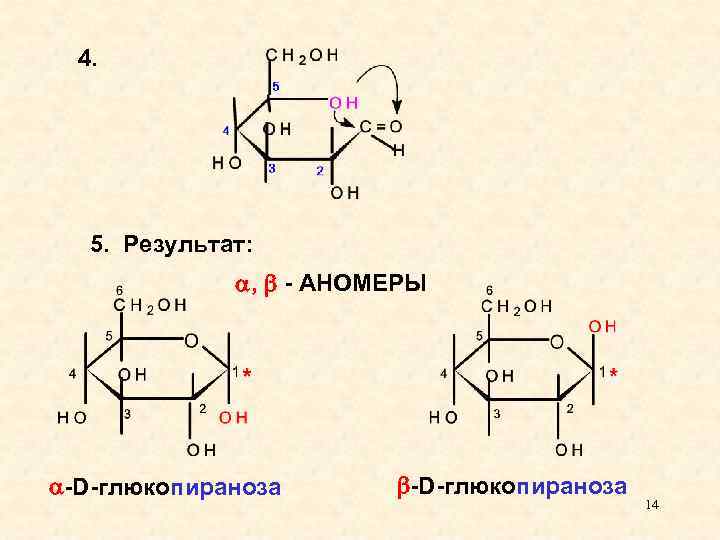 4. 5. Результат: , - АНОМЕРЫ -D-глюкопираноза 14
4. 5. Результат: , - АНОМЕРЫ -D-глюкопираноза 14
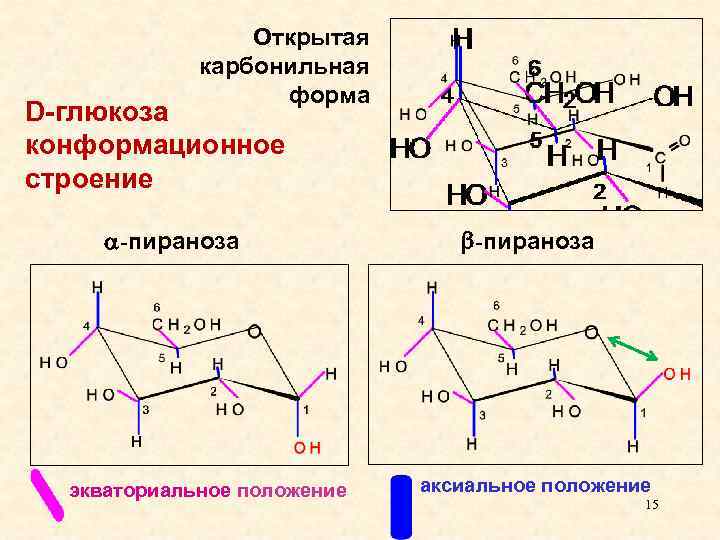 Открытая карбонильная форма D-глюкоза конформационное строение -пираноза экваториальное положение -пираноза аксиальное положение 15
Открытая карбонильная форма D-глюкоза конформационное строение -пираноза экваториальное положение -пираноза аксиальное положение 15
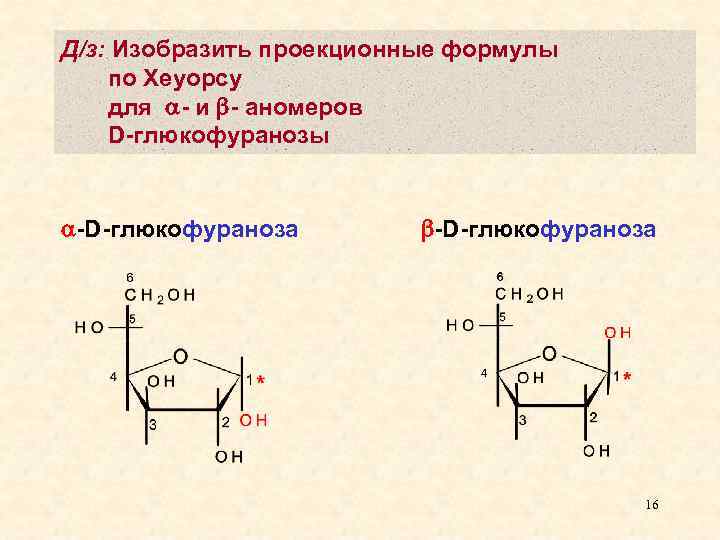 Д/з: Изобразить проекционные формулы по Хеуорсу для - и - аномеров D-глюкофуранозы -D-глюкофураноза 16
Д/з: Изобразить проекционные формулы по Хеуорсу для - и - аномеров D-глюкофуранозы -D-глюкофураноза 16
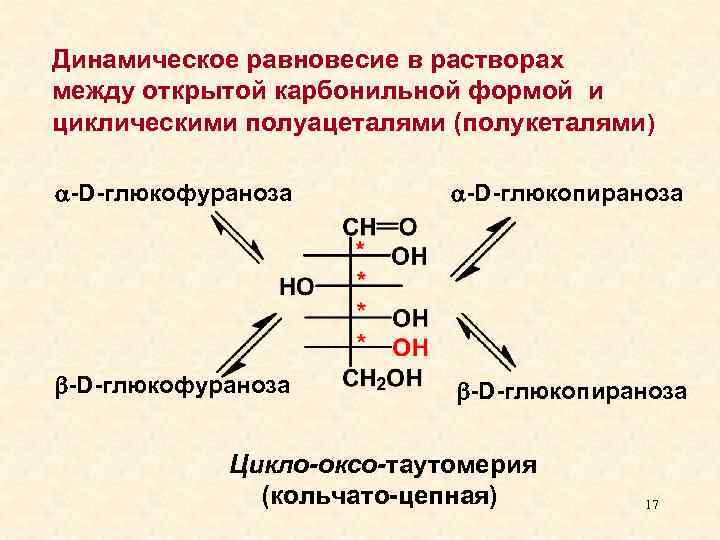 Динамическое равновесие в растворах между открытой карбонильной формой и циклическими полуацеталями (полукеталями) -D-глюкофураноза -D-глюкопираноза Цикло-оксо-таутомерия (кольчато-цепная) 17
Динамическое равновесие в растворах между открытой карбонильной формой и циклическими полуацеталями (полукеталями) -D-глюкофураноза -D-глюкопираноза Цикло-оксо-таутомерия (кольчато-цепная) 17
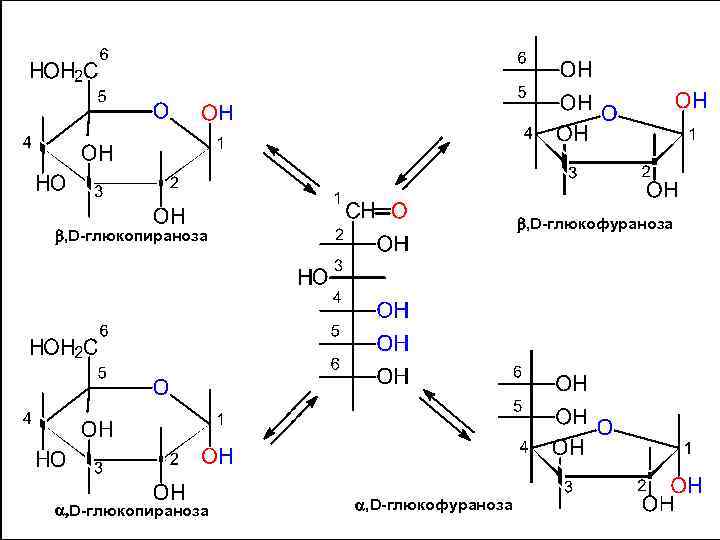 , D-глюкофураноза , D-глюкопираноза , D-глюкофураноза
, D-глюкофураноза , D-глюкопираноза , D-глюкофураноза
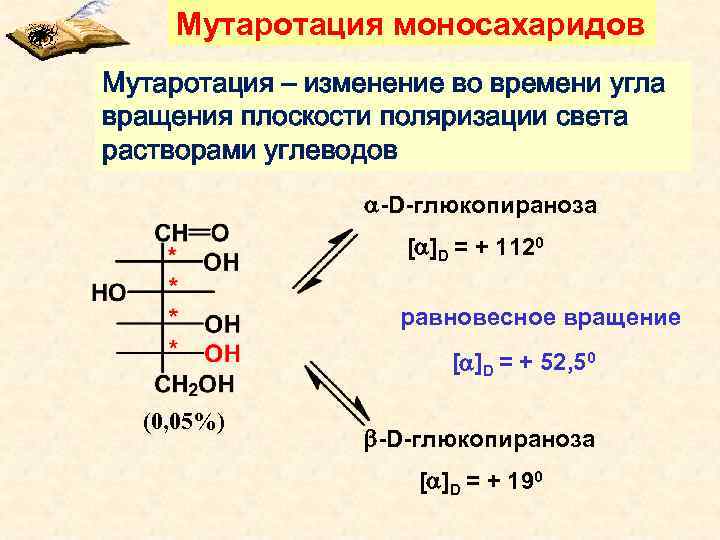 Мутаротация моносахаридов Мутаротация – изменение во времени угла вращения плоскости поляризации света растворами углеводов -D-глюкопираноза [ ]D = + 1120 равновесное вращение [ ]D = + 52, 50 (0, 05%) -D-глюкопираноза [ ]D = + 190
Мутаротация моносахаридов Мутаротация – изменение во времени угла вращения плоскости поляризации света растворами углеводов -D-глюкопираноза [ ]D = + 1120 равновесное вращение [ ]D = + 52, 50 (0, 05%) -D-глюкопираноза [ ]D = + 190
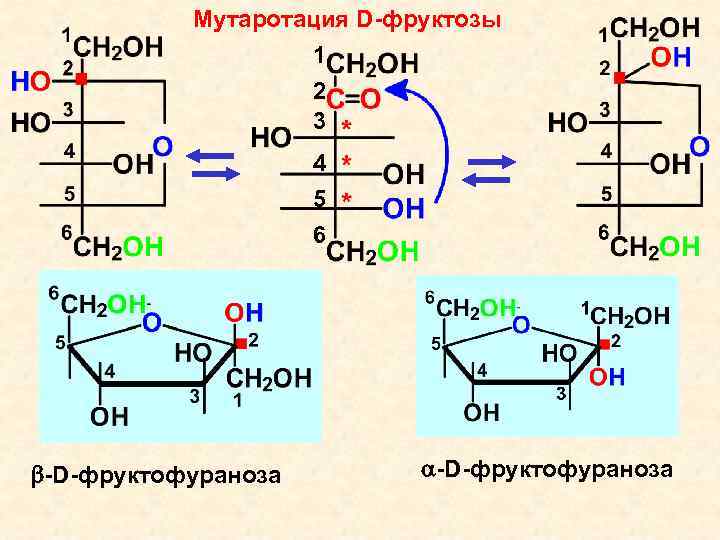 Мутаротация D-фруктозы 1 2 3 4 5 6 -D-фруктофураноза
Мутаротация D-фруктозы 1 2 3 4 5 6 -D-фруктофураноза
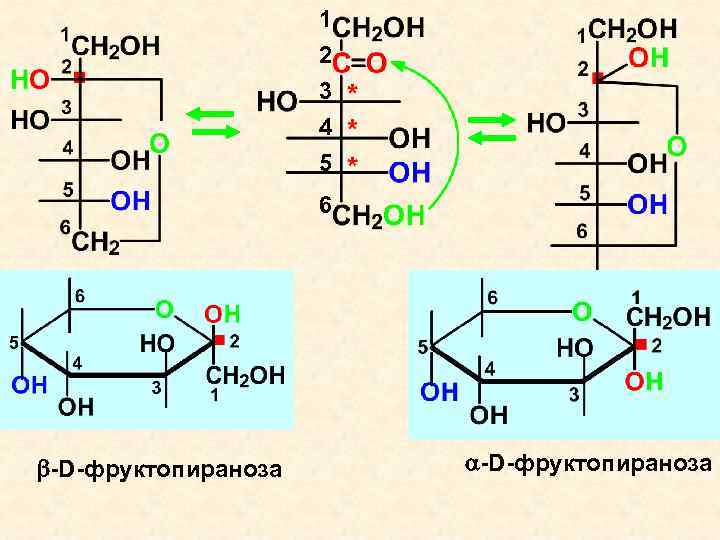 1 2 3 4 5 6 -D-фруктопираноза
1 2 3 4 5 6 -D-фруктопираноза
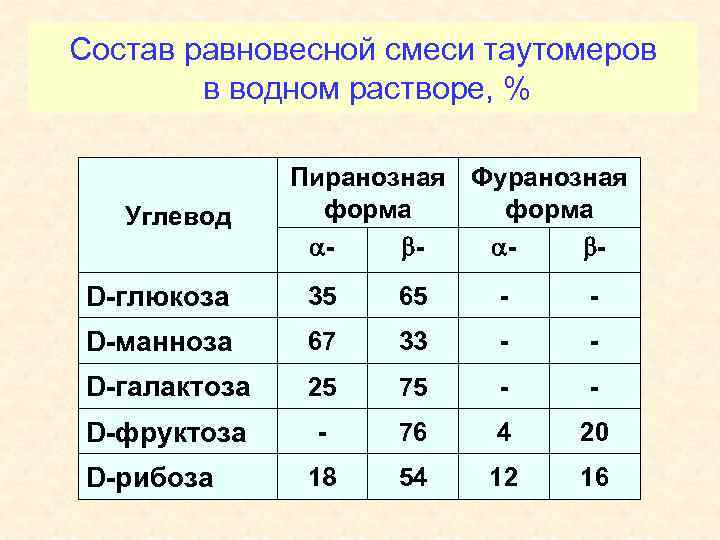 Состав равновесной смеси таутомеров в водном растворе, % Углевод Пиранозная Фуранозная форма - D-глюкоза 35 65 - - D-манноза 67 33 - - D-галактоза 25 75 - - D-фруктоза - 76 4 20 18 54 12 16 D-рибоза
Состав равновесной смеси таутомеров в водном растворе, % Углевод Пиранозная Фуранозная форма - D-глюкоза 35 65 - - D-манноза 67 33 - - D-галактоза 25 75 - - D-фруктоза - 76 4 20 18 54 12 16 D-рибоза
 Химические свойства моносахаридов 1. Свойства полуацеталей (в любой из циклических форм); 2. Свойства многоатомных спиртов (в любой из таутомерных форм); 3. Свойства альдегидов или кетонов (в нециклической форме)
Химические свойства моносахаридов 1. Свойства полуацеталей (в любой из циклических форм); 2. Свойства многоатомных спиртов (в любой из таутомерных форм); 3. Свойства альдегидов или кетонов (в нециклической форме)
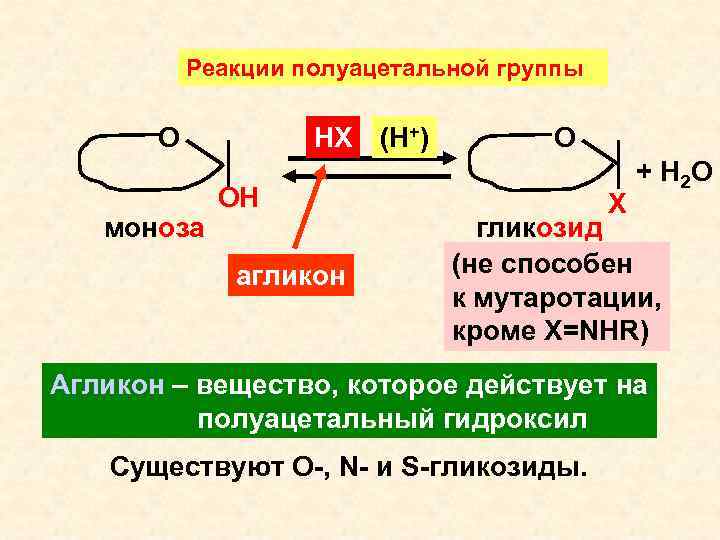 Реакции полуацетальной группы НХ (Н+) О моноза ОН агликон О Х + Н 2 О гликозид (не способен к мутаротации, кроме Х=NHR) Агликон – вещество, которое действует на полуацетальный гидроксил Существуют О-, N- и S-гликозиды.
Реакции полуацетальной группы НХ (Н+) О моноза ОН агликон О Х + Н 2 О гликозид (не способен к мутаротации, кроме Х=NHR) Агликон – вещество, которое действует на полуацетальный гидроксил Существуют О-, N- и S-гликозиды.
 Глико- Агликон Реакции (пример) зид Н 3 РО 4 фосфорилирование ацилирование (растительные гликози. R-COOH ды) ОR-OH, алкилирование (растит. гликозиды) Ar-OH SN- - оза R-SH ди- и полисахариды тиоалкилирование (содерж. в горчице) амины А, Г, Ц, Т, У растительные гликозиды, антибиотики нуклеозиды
Глико- Агликон Реакции (пример) зид Н 3 РО 4 фосфорилирование ацилирование (растительные гликози. R-COOH ды) ОR-OH, алкилирование (растит. гликозиды) Ar-OH SN- - оза R-SH ди- и полисахариды тиоалкилирование (содерж. в горчице) амины А, Г, Ц, Т, У растительные гликозиды, антибиотики нуклеозиды
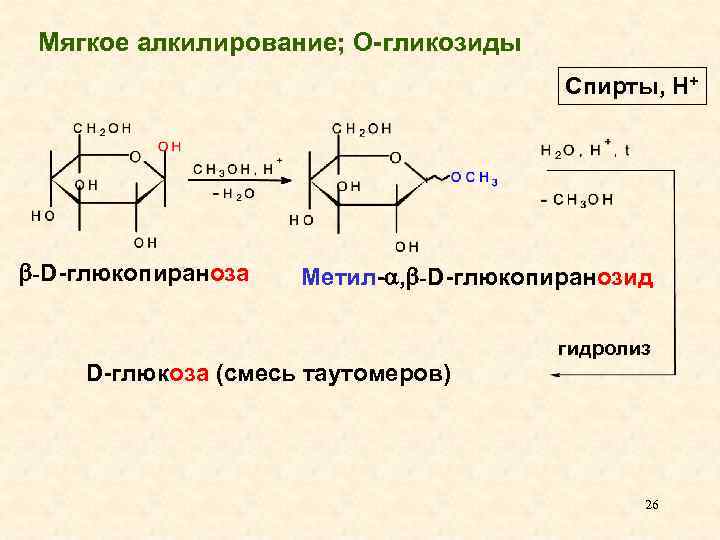 Мягкое алкилирование; О-гликозиды Спирты, Н+ -D-глюкопираноза Метил- , -D-глюкопиранозид гидролиз D-глюкоза (смесь таутомеров) 26
Мягкое алкилирование; О-гликозиды Спирты, Н+ -D-глюкопираноза Метил- , -D-глюкопиранозид гидролиз D-глюкоза (смесь таутомеров) 26
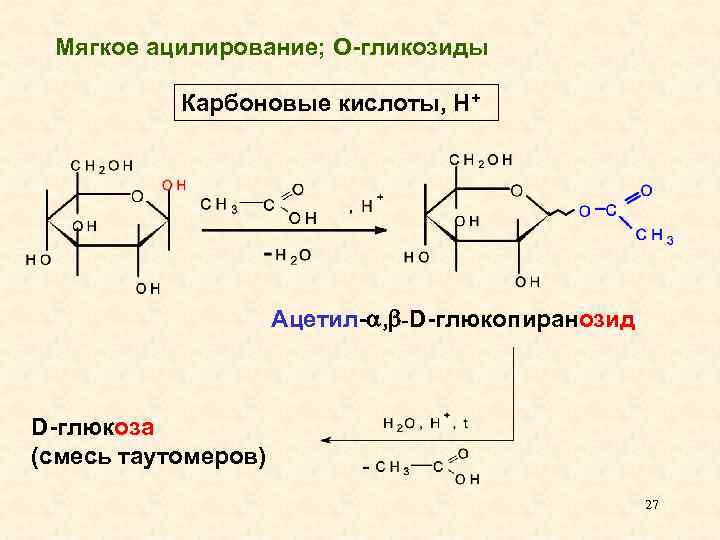 Мягкое ацилирование; О-гликозиды Карбоновые кислоты, Н+ Ацетил- , -D-глюкопиранозид D-глюкоза (смесь таутомеров) 27
Мягкое ацилирование; О-гликозиды Карбоновые кислоты, Н+ Ацетил- , -D-глюкопиранозид D-глюкоза (смесь таутомеров) 27
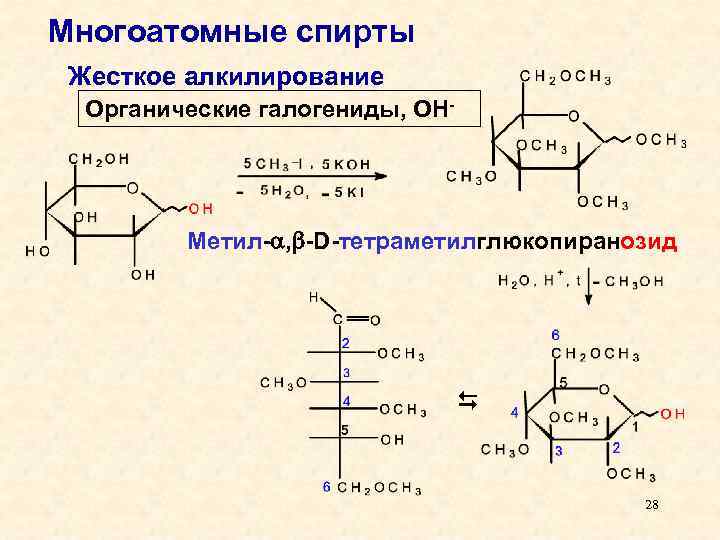 Многоатомные спирты Жесткое алкилирование Органические галогениды, ОН- Метил- , -D-тетраметилглюкопиранозид 28
Многоатомные спирты Жесткое алкилирование Органические галогениды, ОН- Метил- , -D-тетраметилглюкопиранозид 28
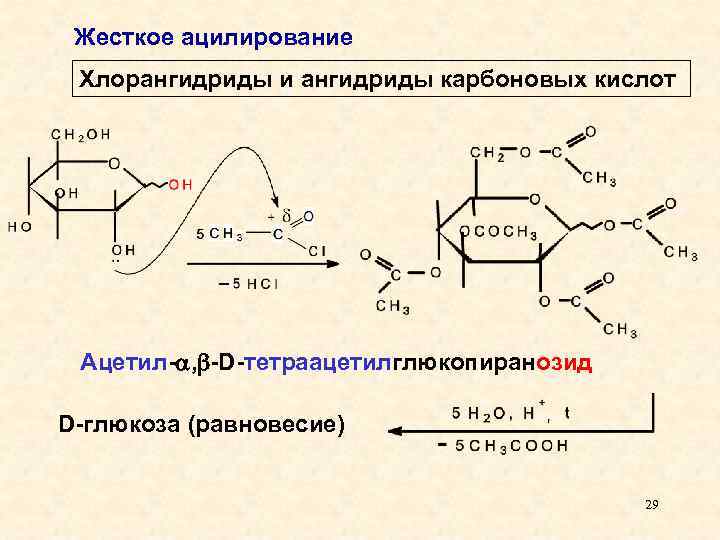 Жесткое ацилирование Хлорангидриды и ангидриды карбоновых кислот Ацетил- , -D-тетраацетилглюкопиранозид D-глюкоза (равновесие) 29
Жесткое ацилирование Хлорангидриды и ангидриды карбоновых кислот Ацетил- , -D-тетраацетилглюкопиранозид D-глюкоза (равновесие) 29
![Реакции с участием С=О группы 1. Восстановление [H] D-глюкоза D-сорбит, D-глюцит D-фруктоза [H] D-манноза Реакции с участием С=О группы 1. Восстановление [H] D-глюкоза D-сорбит, D-глюцит D-фруктоза [H] D-манноза](https://present5.com/presentation/101307319_182862747/image-30.jpg) Реакции с участием С=О группы 1. Восстановление [H] D-глюкоза D-сорбит, D-глюцит D-фруктоза [H] D-манноза D-маннит
Реакции с участием С=О группы 1. Восстановление [H] D-глюкоза D-сорбит, D-глюцит D-фруктоза [H] D-манноза D-маннит
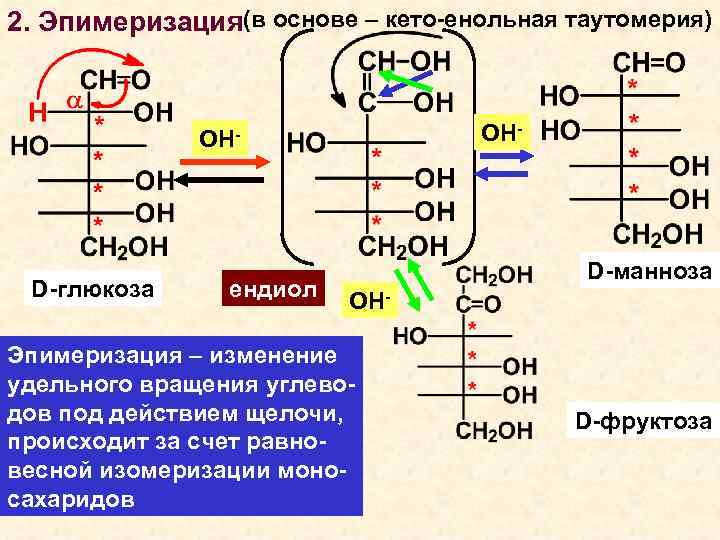 2. Эпимеризация(в основе – кето-енольная таутомерия) ОН- D-глюкоза ендиол D-манноза ОН- Эпимеризация – изменение удельного вращения углеводов под действием щелочи, происходит за счет равновесной изомеризации моносахаридов D-фруктоза
2. Эпимеризация(в основе – кето-енольная таутомерия) ОН- D-глюкоза ендиол D-манноза ОН- Эпимеризация – изменение удельного вращения углеводов под действием щелочи, происходит за счет равновесной изомеризации моносахаридов D-фруктоза
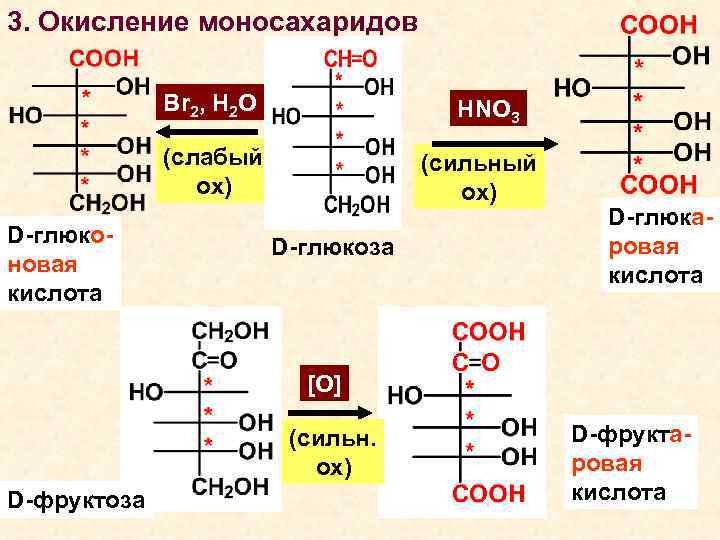 3. Окисление моносахаридов Br 2, H 2 О HNO 3 (слабый ох) D-глюконовая кислота (сильный ох) D-глюкоза D-глюкаровая кислота [O] (сильн. ох) D-фруктоза D-фруктаровая кислота
3. Окисление моносахаридов Br 2, H 2 О HNO 3 (слабый ох) D-глюконовая кислота (сильный ох) D-глюкоза D-глюкаровая кислота [O] (сильн. ох) D-фруктоза D-фруктаровая кислота
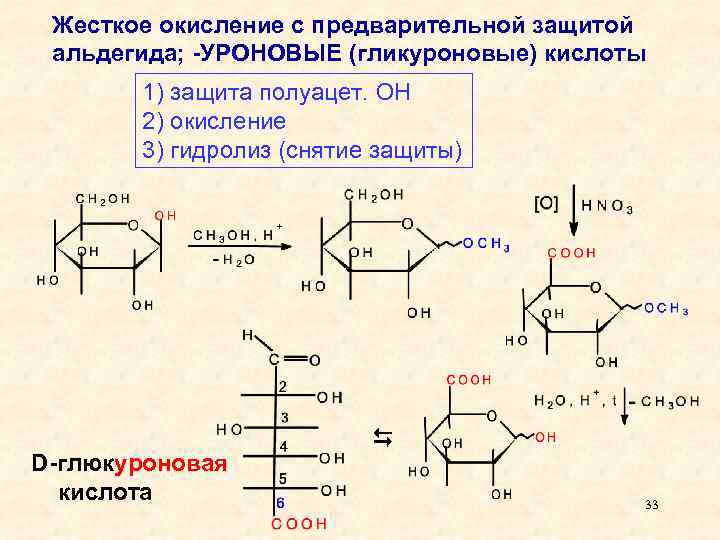 Жесткое окисление с предварительной защитой альдегида; -УРОНОВЫЕ (гликуроновые) кислоты 1) защита полуацет. ОН 2) окисление 3) гидролиз (снятие защиты) D-глюкуроновая кислота 33
Жесткое окисление с предварительной защитой альдегида; -УРОНОВЫЕ (гликуроновые) кислоты 1) защита полуацет. ОН 2) окисление 3) гидролиз (снятие защиты) D-глюкуроновая кислота 33
 4. Реакция с фенилгидразином озазон Озазоны – ярко-желтые кристаллические вещества, использовались для идентификации углеводов
4. Реакция с фенилгидразином озазон Озазоны – ярко-желтые кристаллические вещества, использовались для идентификации углеводов
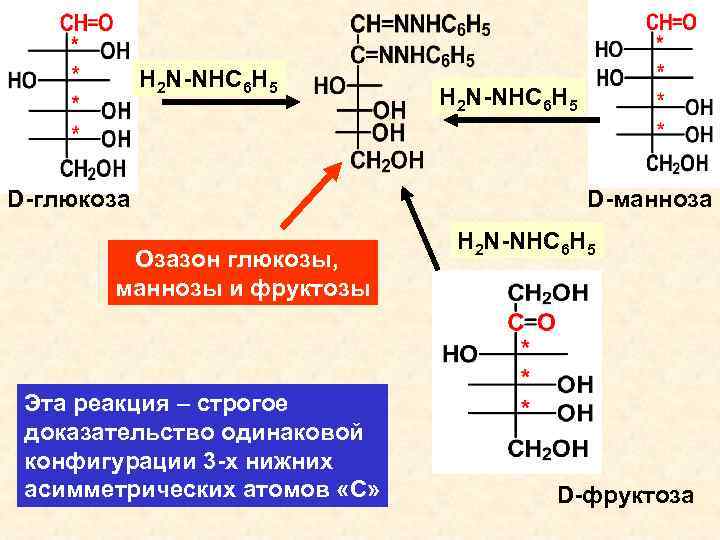 H 2 N-NHC 6 H 5 D-глюкоза Озазон глюкозы, маннозы и фруктозы Эта реакция – строгое доказательство одинаковой конфигурации 3 -х нижних асимметрических атомов «С» H 2 N-NHC 6 H 5 D-манноза H 2 N-NHC 6 H 5 D-фруктоза
H 2 N-NHC 6 H 5 D-глюкоза Озазон глюкозы, маннозы и фруктозы Эта реакция – строгое доказательство одинаковой конфигурации 3 -х нижних асимметрических атомов «С» H 2 N-NHC 6 H 5 D-манноза H 2 N-NHC 6 H 5 D-фруктоза


