Лек13-2-7-новая.PPT
- Количество слайдов: 49

Кафедра химии Тема лекции: АМИНОКИСЛОТЫ. БЕЛКИ 1
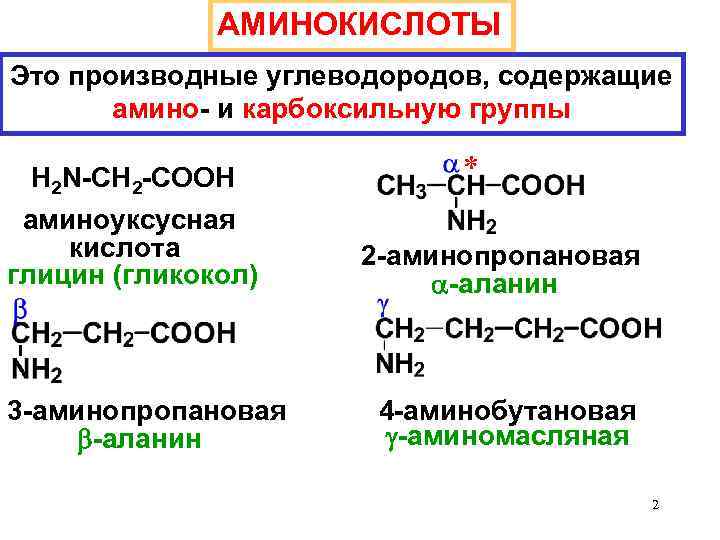
АМИНОКИСЛОТЫ Это производные углеводородов, содержащие амино- и карбоксильную группы H 2 N-CH 2 -COOH аминоуксусная кислота глицин (гликокол) 3 -аминопропановая -аланин 2 -аминопропановая -аланин 4 -аминобутановая -аминомасляная 2
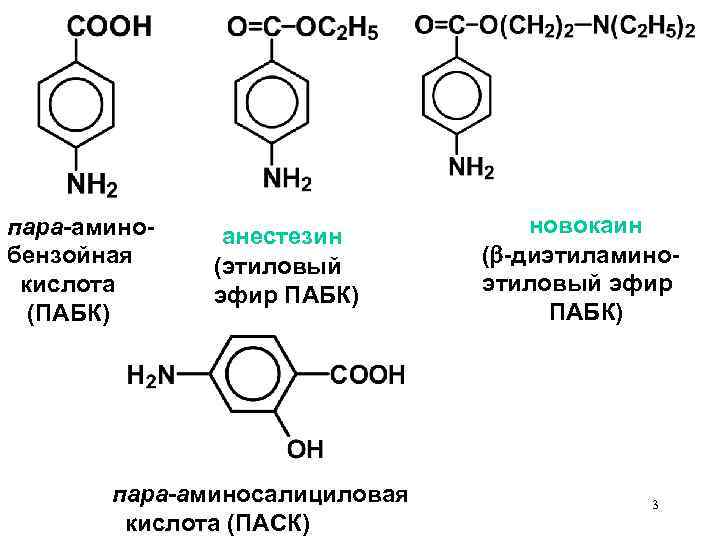
пара-аминобензойная кислота (ПАБК) анестезин (этиловый эфир ПАБК) пара-аминосалициловая кислота (ПАСК) новокаин ( -диэтиламиноэтиловый эфир ПАБК) 3
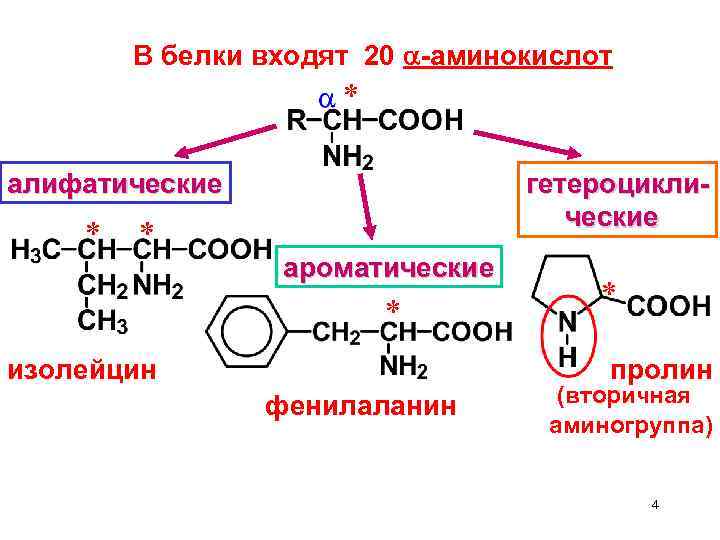
В белки входят 20 -аминокислот алифатические гетероциклические ароматические изолейцин пролин фенилаланин (вторичная аминогруппа) 4
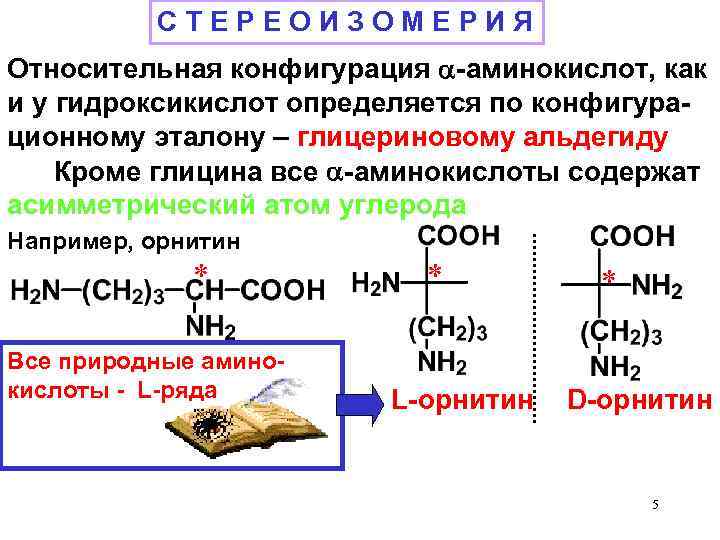
СТЕРЕОИЗОМЕРИЯ Относительная конфигурация -аминокислот, как и у гидроксикислот определяется по конфигурационному эталону – глицериновому альдегиду Кроме глицина все -аминокислоты содержат асимметрический атом углерода Например, орнитин Все природные аминокислоты - L-ряда L-орнитин D-орнитин 5

Некоторые аминокислоты, например изолейцин, треонин, цистин и гидроксипролин содержат 2 асимметрических атома углерода, поэтому они существуют в виде 4 оптических изомеров [кроме цистина, у которого есть ось симметрии, т. е. изомеров – меньше (3)] 6
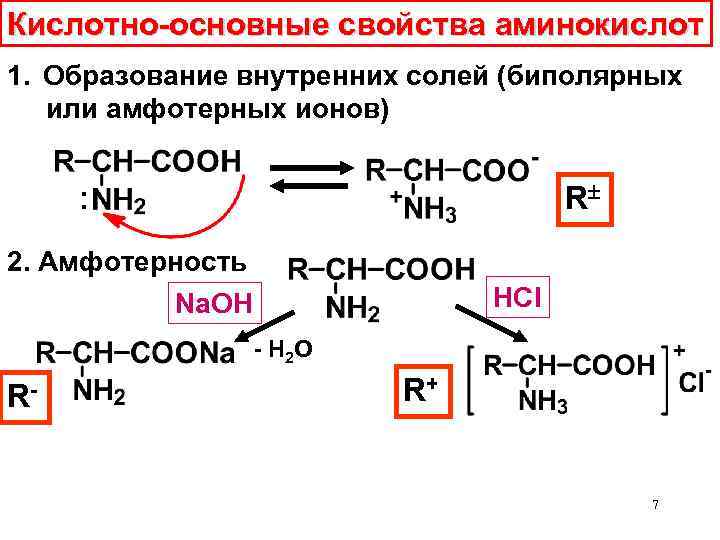
Кислотно-основные свойства аминокислот 1. Образование внутренних солей (биполярных или амфотерных ионов) R : 2. Амфотерность HCl Na. OH - Н 2 О R- R+ 7
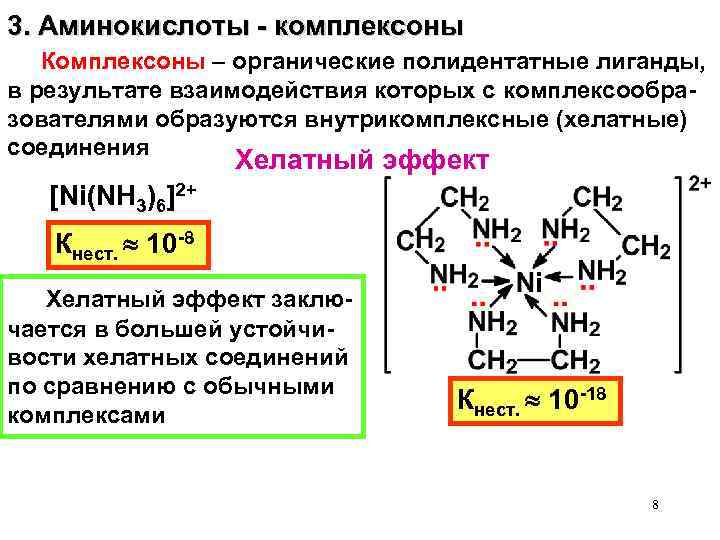
3. Аминокислоты - комплексоны Комплексоны – органические полидентатные лиганды, в результате взаимодействия которых с комплексообразователями образуются внутрикомплексные (хелатные) соединения Хелатный эффект [Ni(NH 3)6]2+ Кнест. 10 -8 Хелатный эффект заключается в большей устойчивости хелатных соединений по сравнению с обычными комплексами Кнест. 10 -18 8
![комплексон [Cu(H 2 O)4]2+ + 2 Гли хелат Cu(Гли)2 +4 H 2 О +2 комплексон [Cu(H 2 O)4]2+ + 2 Гли хелат Cu(Гли)2 +4 H 2 О +2](https://present5.com/presentation/101307319_158988276/image-9.jpg)
комплексон [Cu(H 2 O)4]2+ + 2 Гли хелат Cu(Гли)2 +4 H 2 О +2 Н+ 9
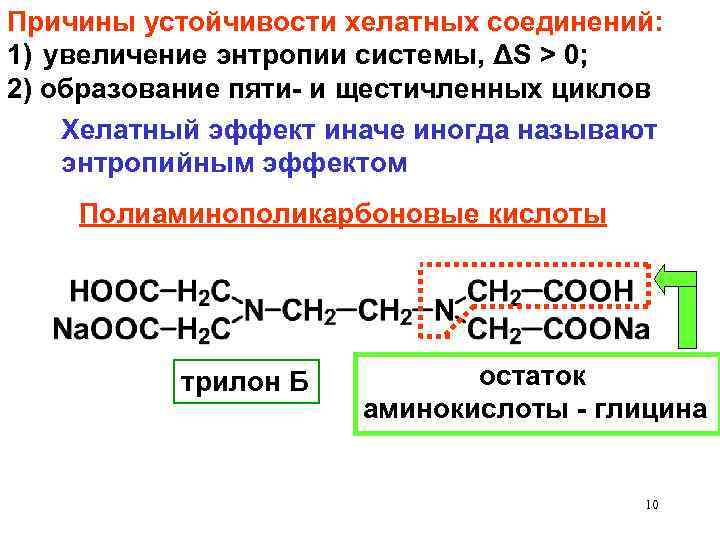
Причины устойчивости хелатных соединений: 1) увеличение энтропии системы, ΔS > 0; 2) образование пяти- и щестичленных циклов Хелатный эффект иначе иногда называют энтропийным эффектом Полиаминополикарбоновые кислоты трилон Б остаток аминокислоты - глицина 10
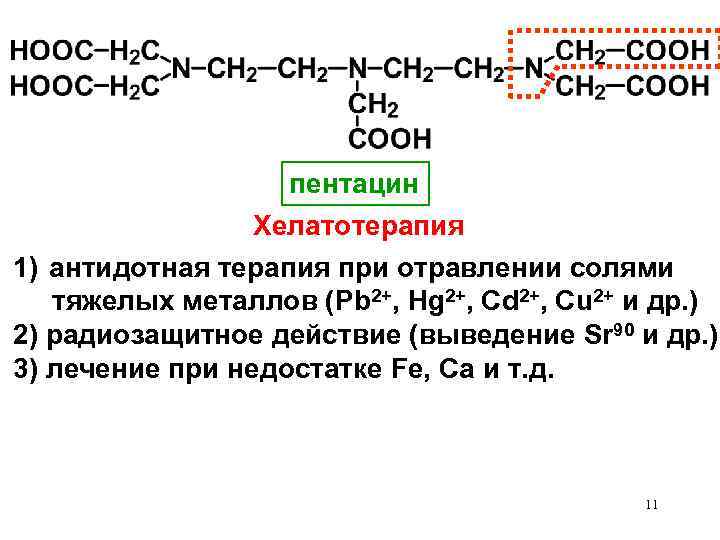
пентацин Хелатотерапия 1) антидотная терапия при отравлении солями тяжелых металлов (Pb 2+, Hg 2+, Cd 2+, Cu 2+ и др. ) 2) радиозащитное действие (выведение Sr 90 и др. ) 3) лечение при недостатке Fe, Ca и т. д. 11
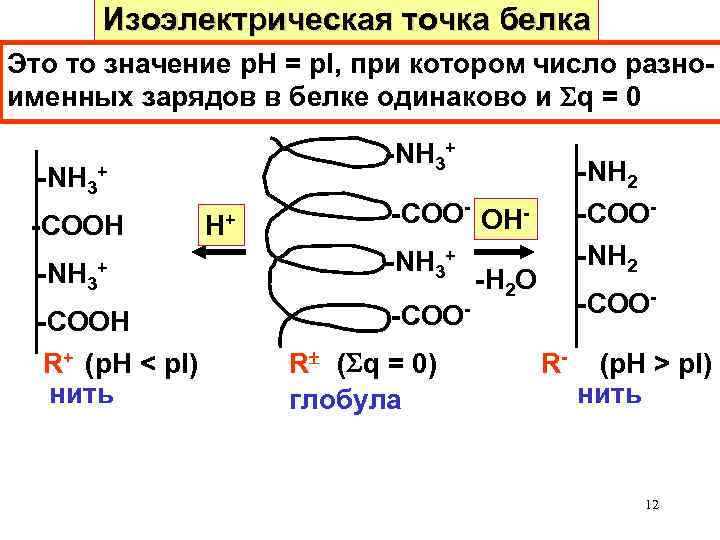
Изоэлектрическая точка белка Это то значение р. Н = р. I, при котором число разноименных зарядов в белке одинаково и q = 0 -NH 3+ -COOН R+ (р. Н < р. I) нить Н+ -NH 2 -COO- ОН-NH 3+ -H 2 O -COOR ( q = 0) глобула -COOR- (р. Н > р. I) нить 12
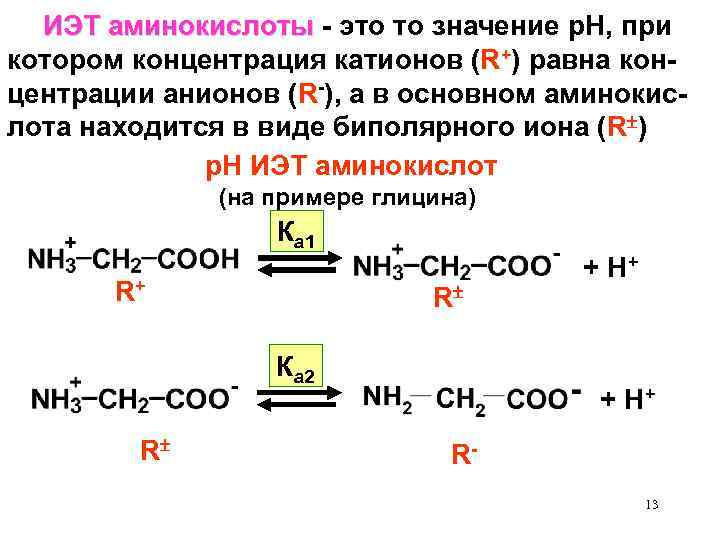
ИЭТ аминокислоты - это то значение р. Н, при котором концентрация катионов (R+) равна концентрации анионов (R-), а в основном аминокислота находится в виде биполярного иона (R ) р. Н ИЭТ аминокислот (на примере глицина) Ка 1 R+ R Ка 2 R + Н+ R 13
![[Н+] = Ка 1 . К а 2 ; p. Ка 1 + p. [Н+] = Ка 1 . К а 2 ; p. Ка 1 + p.](https://present5.com/presentation/101307319_158988276/image-14.jpg)
[Н+] = Ка 1 . К а 2 ; p. Ка 1 + p. Ка 2 р. Н = р. I = 2 Для глицина: р. I = 2, 6 + 9, 8 2 = 6, 2 14
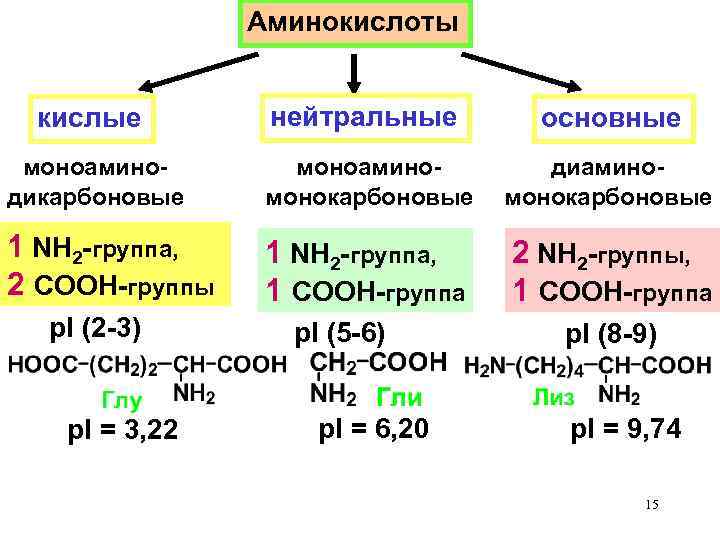
Аминокислоты кислые нейтральные основные моноаминодикарбоновые моноаминомонокарбоновые диаминомонокарбоновые 1 NH 2 -группа, 2 COOН-группы 1 NH 2 -группа, 1 COOН-группа 2 NH 2 -группы, 1 COOН-группа р. I (2 -3) р. I = 3, 22 р. I (5 -6) р. I = 6, 20 р. I (8 -9) р. I = 9, 74 15
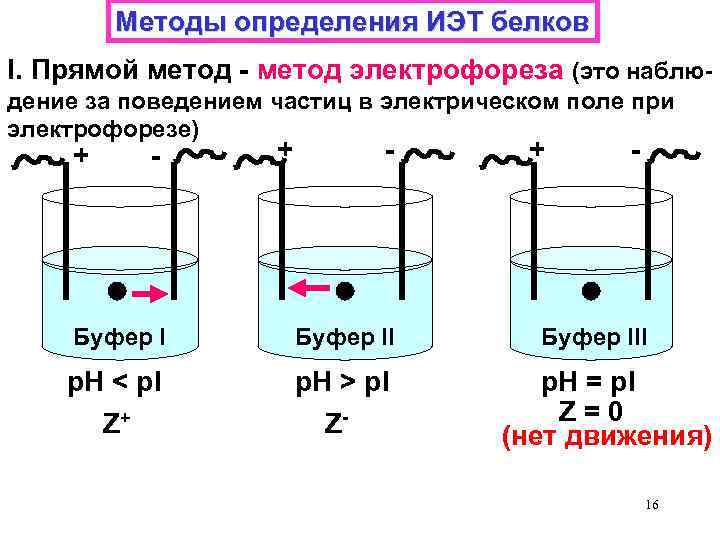
Методы определения ИЭТ белков I. Прямой метод - метод электрофореза (это наблюдение за поведением чaстиц в электрическом поле при электрофорезе) + - Буфер II р. Н < р. I Z+ р. Н > р. I Z- + - Буфер III р. Н = р. I Z=0 (нет движения) 16
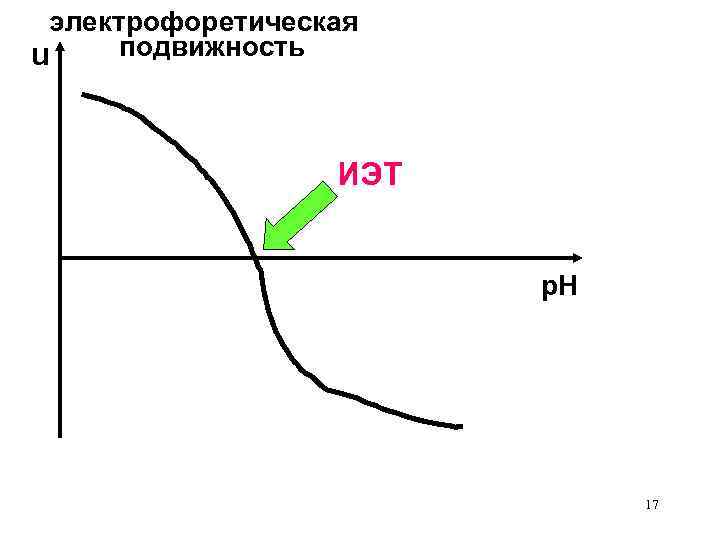
электрофоретическая подвижность u ИЭТ р. Н 17

II. Косвенные методы Ряд свойств белков экстремален (max или min) в изоэлектрической точке 1. Гидратация - min 2. Растворимость - min 3. Коагуляция (под действием спирта) – mах (метод максимальной мутности) 4. Вязкость - min 5. Осмотическое давление - min 6. Набухание - min 7. Застудневание - процесс превращения вещества из текучего состояния в структурированное (время 18 застудневания tзаст. - min)
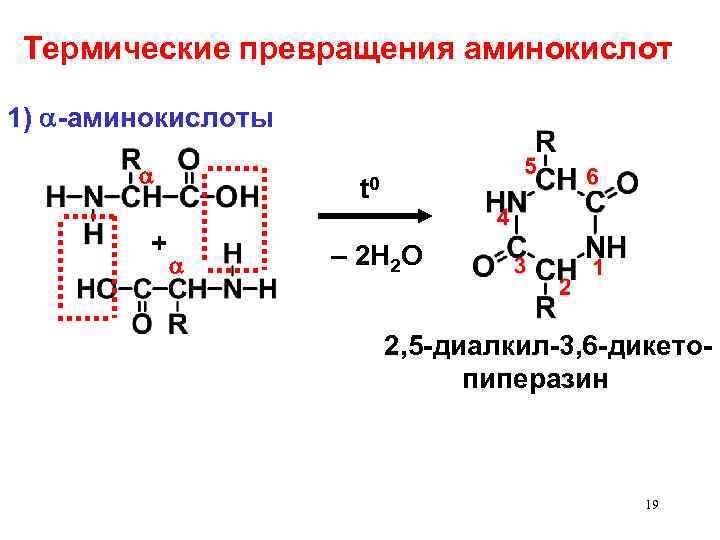
Термические превращения аминокислот 1) -аминокислоты + t 0 – 2 H 2 O 2, 5 -диалкил-3, 6 -дикетопиперазин 19
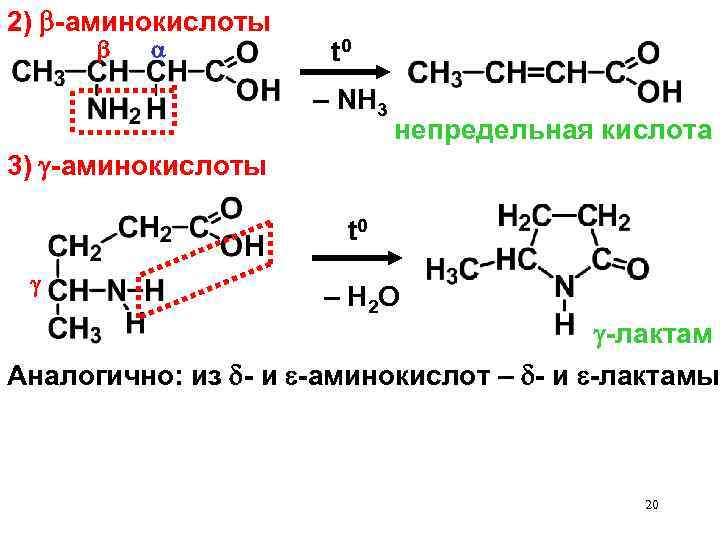
2) -аминокислоты t 0 – NH 3 непредельная кислота 3) -аминокислоты t 0 – H 2 O -лактам Аналогично: из - и -аминокислот – - и -лактамы 20
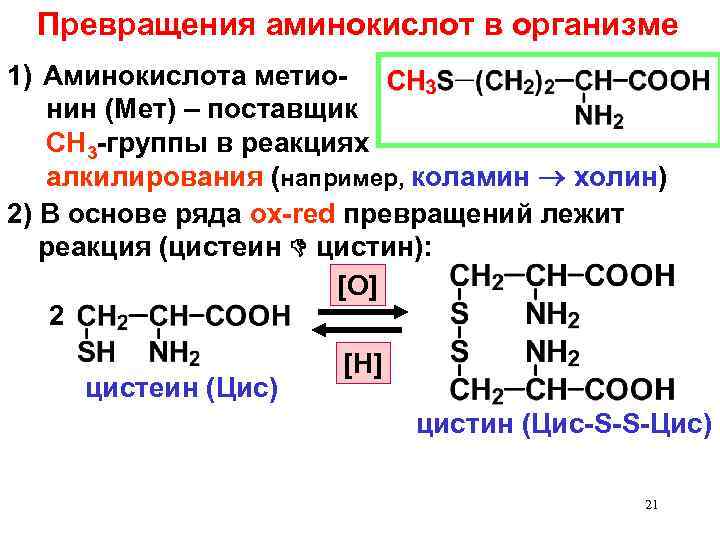
Превращения аминокислот в организме 1) Аминокислота метионин (Мет) – поставщик СН 3 -группы в реакциях алкилирования (например, коламин холин) 2) В основе ряда ох-red превращений лежит реакция (цистеин D цистин): [O] 2 цистеин (Цис) [H] цистин (Цис-S-S-Цис) 21
![3) Дезаминирование (генетическая связь -аланина, молочной кислоты и ПВК) Н 2 O [O] NН 3) Дезаминирование (генетическая связь -аланина, молочной кислоты и ПВК) Н 2 O [O] NН](https://present5.com/presentation/101307319_158988276/image-22.jpg)
3) Дезаминирование (генетическая связь -аланина, молочной кислоты и ПВК) Н 2 O [O] NН 3 [H] 4) Декарбоксилирование лизин (Лиз) – СО 2 фермент (при гниении) H 2 N-(CH 2)5 -NH 2 кадаверин – СО 2 фермент гистидин (Гис) гистамин 5) Реакции восстановительного аминирования и реакции трансаминирования – см. лекцию 22 «Карбонильные соединения»
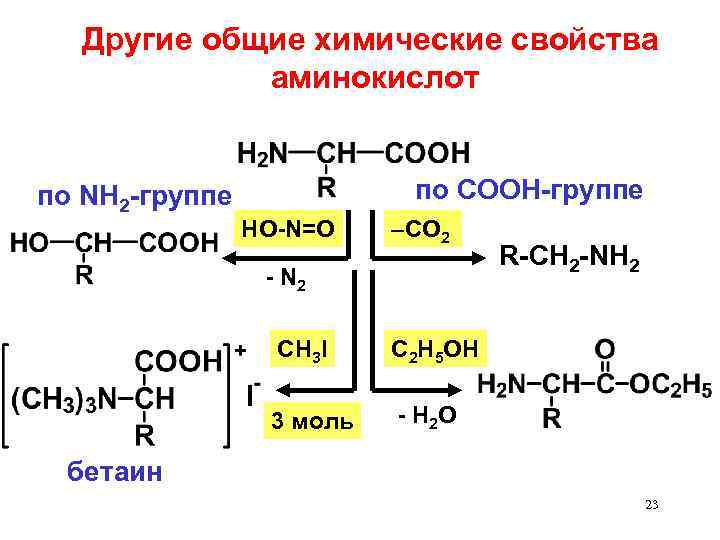
Другие общие химические свойства аминокислот по NH 2 -группе по СООН-группе HO-N=O –СО 2 - N 2 CH 3 I C 2 H 5 OH 3 моль R-CH 2 -NH 2 - H 2 O бетаин 23
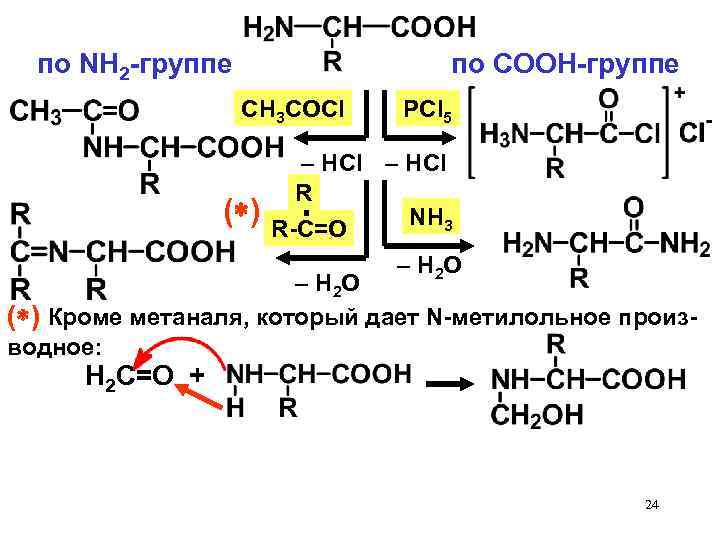
по NH 2 -группе по СООН-группе CH 3 COCl PCl 5 – HCl R ( ) NH 3 R-C=O – H 2 O ( ) Кроме метаналя, который дает N-метилольное производное: Н 2 С=О + 24
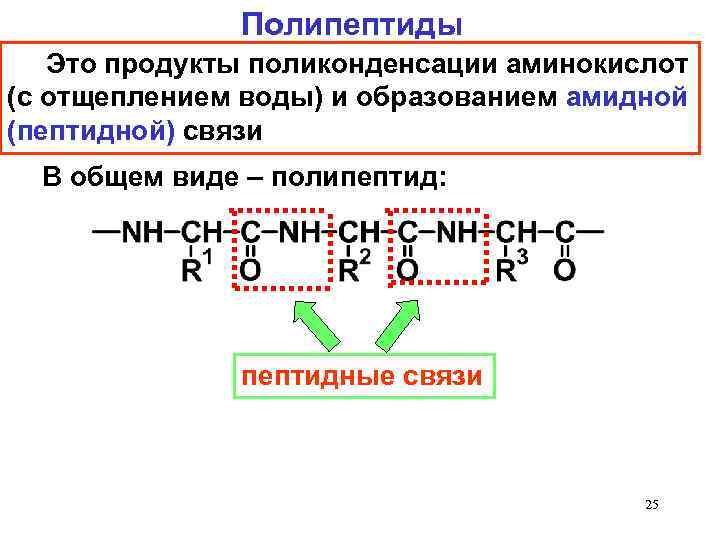
Полипептиды Это продукты поликонденсации аминокислот (с отщеплением воды) и образованием амидной (пептидной) связи В общем виде – полипептид: пептидные связи 25
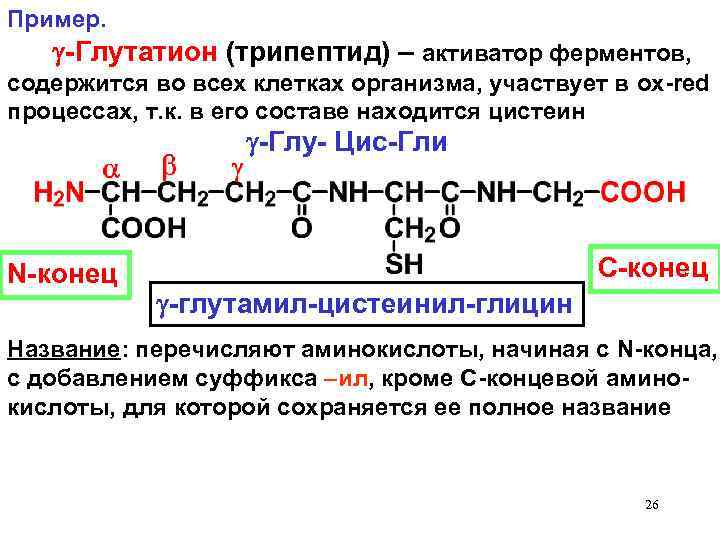
Пример. -Глутатион (трипептид) – активатор ферментов, содержится во всех клетках организма, участвует в ox-red процессах, т. к. в его составе находится цистеин -Глу- Цис-Гли N-конец С-конец -глутамил-цистеинил-глицин Название: перечисляют аминокислоты, начиная с N-конца, с добавлением суффикса –ил, кроме С-концевой аминокислоты, для которой сохраняется ее полное название 26

Специфичность белков определяется: 1) аминокислотным составом – природой и количеством аминокислот 2) аминокислотной последовательностью – первичной структурой белка В настоящее время установлена структура > 600 белков, Например, гормоны – инсулин (51 аминокислота), окситоцин и вазопрессин (нонапептиды), фермент – рибонуклеаза (124 аминокислоты) и др. Сложности искусственного синтеза пептидов: а) много вариантов сочетания, б) маленький выход конечного продукта (т. к. много стадий) 27

Пространственное строение полипептидов Вторичная структура белка 1. Пептидная связь а) частичная двоесвязанность (из-за р- сопряжения электронной пары азота с -электронами С=О связи) 14 к. Дж/моль 100 к. Дж/моль 40 -80 к. Дж/моль Наличие плоской cопряженной структуры – причина затруднения вращения вокруг связи С-N 28
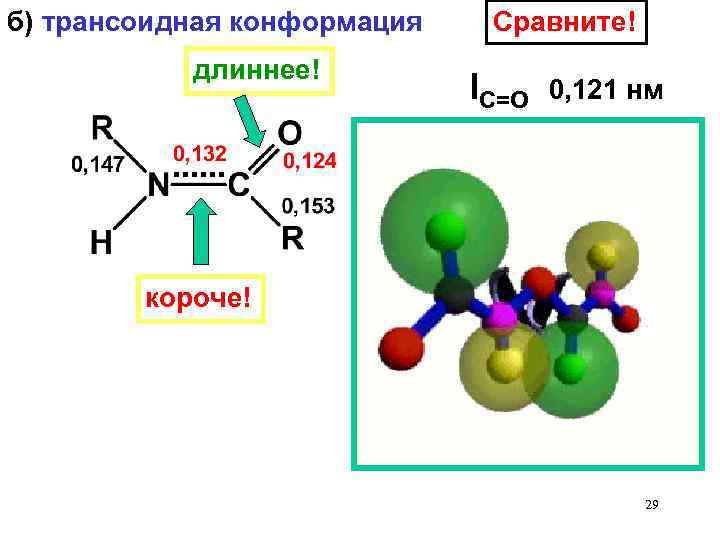
б) трансоидная конформация длиннее! Сравните! l. С=O 0, 121 нм l. N-С 0, 147 нм короче! 29
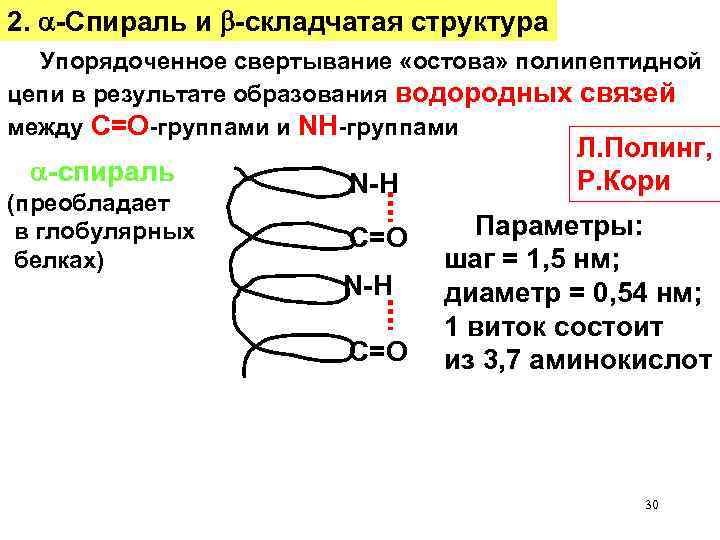
2. -Спираль и -складчатая структура Упорядоченное свертывание «остова» полипептидной цепи в результате образования водородных связей между С=О-группами и NH-группами -спираль (преобладает в глобулярных белках) N-H C=O Л. Полинг, Р. Кори Параметры: шаг = 1, 5 нм; диаметр = 0, 54 нм; 1 виток состоит из 3, 7 аминокислот 30
31
-Спираль 32
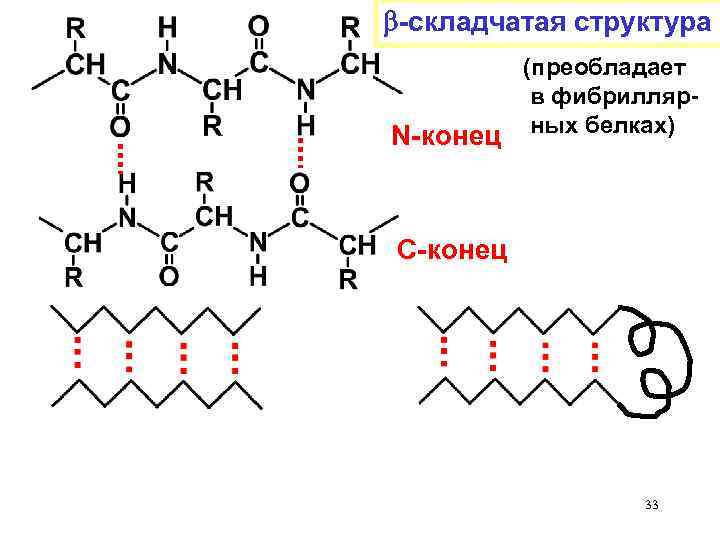
-складчатая структура N-конец (преобладает в фибриллярных белках) С-конец 33
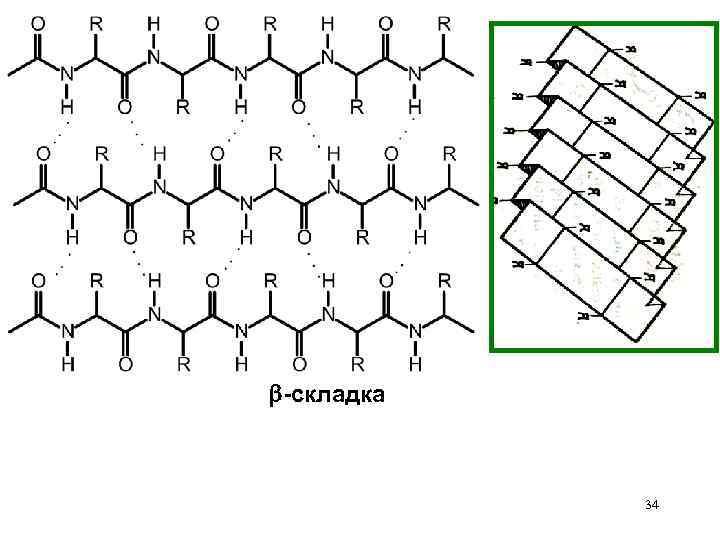
-складка 34
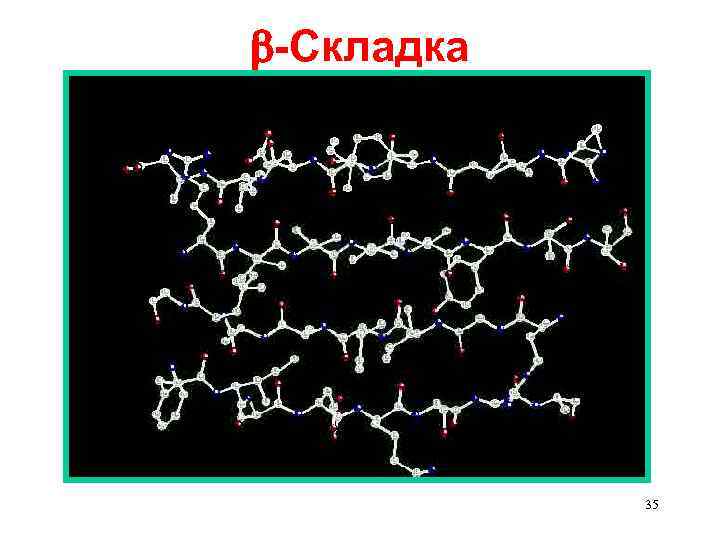
-Складка 35

Следует иметь в виду, что изгибы полипептидной цепи обусловлены наличием аминокислот со вторичной аминогруппой – пролина и гидроксипролина; в этих случаях пептидная связь не содержит водорода, поэтому невозможна стабилизация пространственной структуры за счет водородной связи Про Х=Н Про Х=ОН Про-ОН нарушение регулярности 36
Полипептид 37
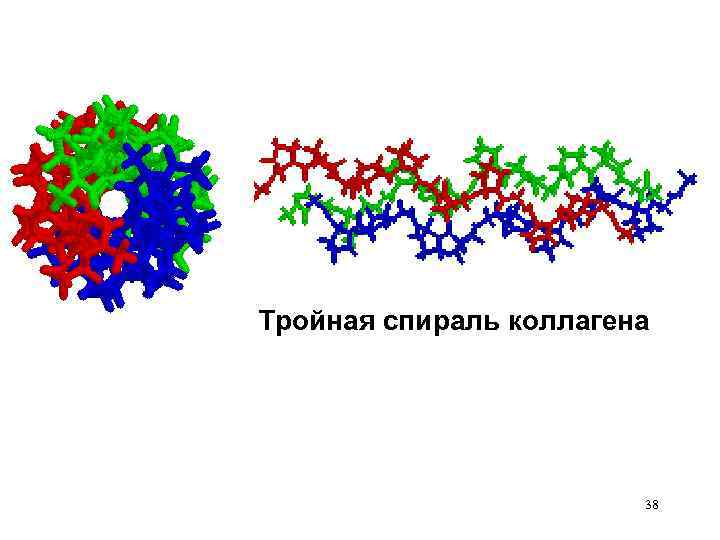
Тройная спираль коллагена 38


Третичная структура белка Трехмерное свертывание полипептидной цепи, приводящее к наложению одних участков -спирали или -складчатой структуры на другие участки цепи Это происходит за счет различных взаимодействий: 1) водородные связи; 2) дисульфидные мостики; 3) электростатические взаимодействия; 4) гидрофобные взаимодействия 40

41
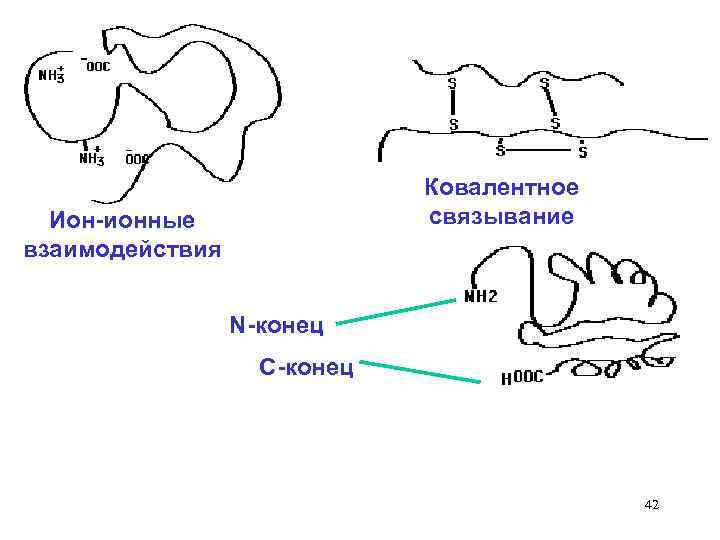
Ковалентное связывание Ион-ионные взаимодействия N-конец С-конец 42

Четвертичная структура белка Некоторые белки, например гемоглобин, обладают четвертичной структурой; при этом одинаковые или сходные субъединицы соединяются в единое целое с симметричным пространственным расположением Четвертичная структура стабилизируется, как правило, водородными связями и гидрофобными взаимодействиями 43
Полипептид 44
45
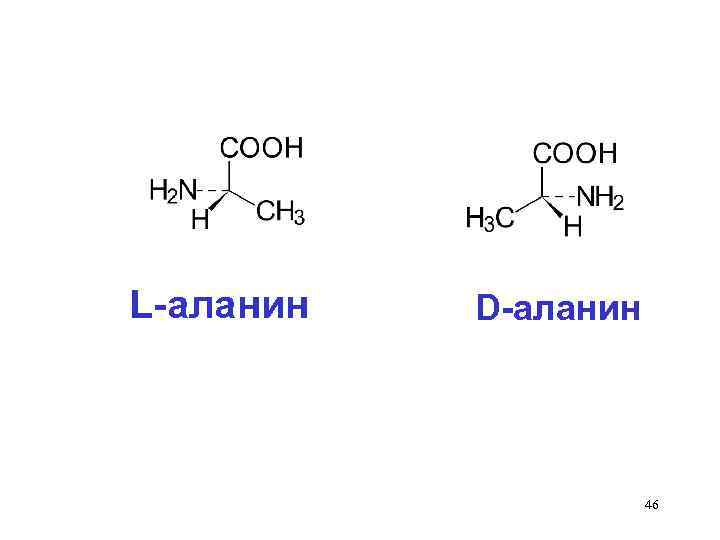
L-аланин D-аланин 46
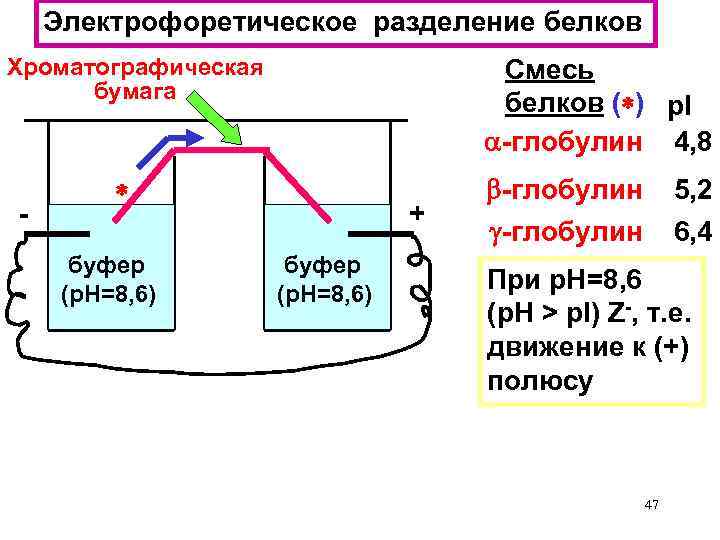
Электрофоретическое разделение белков Хроматографическая бумага - Смесь белков ( ) р. I -глобулин 4, 8 буфер (р. Н=8, 6) + буфер (р. Н=8, 6) -глобулин 5, 2 6, 4 При р. Н=8, 6 (p. H > p. I) Z-, т. е. движение к (+) полюсу 47
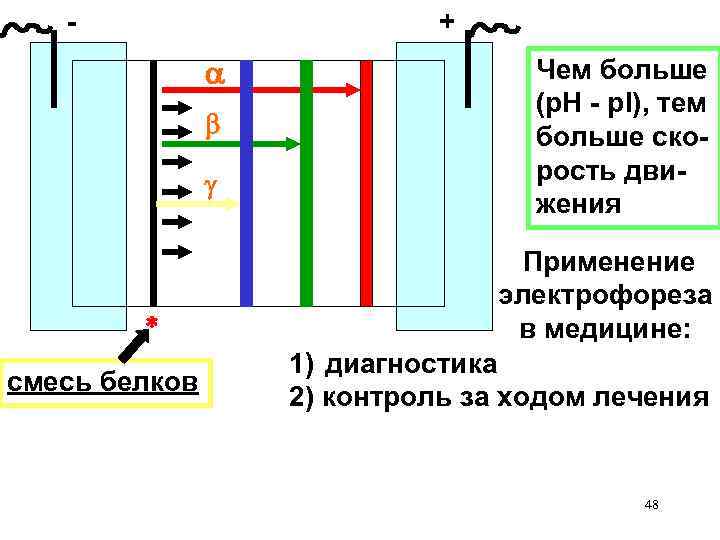
- + смесь белков Чем больше (p. H - p. I), тем больше скорость движения Применение электрофореза в медицине: 1) диагностика 2) контроль за ходом лечения 48
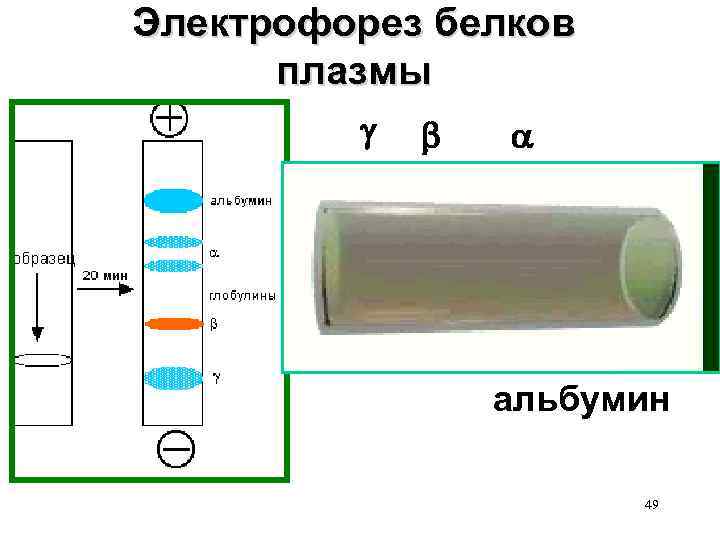
Электрофорез белков плазмы альбумин 49
Лек13-2-7-новая.PPT