Н ОН.pptx
- Количество слайдов: 50
 Кафедра химии КИСЛОТНОСТЬ И ОСНОВНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Минаева Н. Н.
Кафедра химии КИСЛОТНОСТЬ И ОСНОВНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Минаева Н. Н.
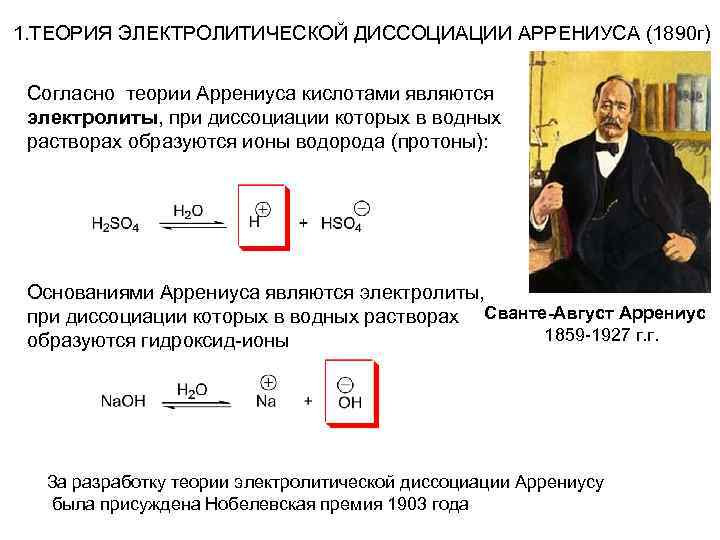 1. ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ АРРЕНИУСА (1890 г) Согласно теории Аррениуса кислотами являются электролиты, при диссоциации которых в водных растворах образуются ионы водорода (протоны): Основаниями Аррениуса являются электролиты, при диссоциации которых в водных растворах Сванте-Август Аррениус 1859 1927 г. г. образуются гидроксид ионы За разработку теории электролитической диссоциации Аррениусу была присуждена Нобелевская премия 1903 года
1. ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ АРРЕНИУСА (1890 г) Согласно теории Аррениуса кислотами являются электролиты, при диссоциации которых в водных растворах образуются ионы водорода (протоны): Основаниями Аррениуса являются электролиты, при диссоциации которых в водных растворах Сванте-Август Аррениус 1859 1927 г. г. образуются гидроксид ионы За разработку теории электролитической диссоциации Аррениусу была присуждена Нобелевская премия 1903 года
 Классическая теория электролитической диссоциации Аррениуса применима только к водным растворам электролитов, а многие органические реакции протекают с участием электролитов в неводных средах. Известны соединения, которые не подходят под определение кислот и оснований по Аррениусу, однако проявляют кислотные или основные свойства, например, аммиак (NH 3 ) не имеет гидроксид иона, но проявляет свойства основания, хлорид алюминия проявляет кислотные свойства
Классическая теория электролитической диссоциации Аррениуса применима только к водным растворам электролитов, а многие органические реакции протекают с участием электролитов в неводных средах. Известны соединения, которые не подходят под определение кислот и оснований по Аррениусу, однако проявляют кислотные или основные свойства, например, аммиак (NH 3 ) не имеет гидроксид иона, но проявляет свойства основания, хлорид алюминия проявляет кислотные свойства
 2. Протонная (ПРОТОЛИТИЧЕСКАЯ) теория, или теория кислoт и оснований Бренстеда – Лоури (1923) Йоханнес-Николаус Брёнстед (1879 1947) датский физикохимик Томас Мартин Лоури (1874 1936) английский химик
2. Протонная (ПРОТОЛИТИЧЕСКАЯ) теория, или теория кислoт и оснований Бренстеда – Лоури (1923) Йоханнес-Николаус Брёнстед (1879 1947) датский физикохимик Томас Мартин Лоури (1874 1936) английский химик
 Согласно теории Бренстеда Лоури 1. кислота является донором, а основание акцептором протонов (отсюда теория получила название «протонной» или «протолитической» ) 2. кислоты и основания существуют только как сопряженные пары A H /A и H B+/B; 3. протон не существует в растворе в свободном виде, в воде он образует катион оксония (гидроксония Н 2 О+ )
Согласно теории Бренстеда Лоури 1. кислота является донором, а основание акцептором протонов (отсюда теория получила название «протонной» или «протолитической» ) 2. кислоты и основания существуют только как сопряженные пары A H /A и H B+/B; 3. протон не существует в растворе в свободном виде, в воде он образует катион оксония (гидроксония Н 2 О+ )
 Кислота А-Н, отдав протон, превращается в основание А¯, которое называется сопряженным основанием данной кислоты. Основание ꞉B, присоединив протон, переходит в сопряженную кислоту B+-Н. Кислота А-Н и основание А¯ , а также основание ꞉B и кислота B+-Н являются сопряженными кислотно основными парами: A H/A и H B+/B. В таких сопряжённых кислотно-основных парах чем сильнее кислота, тем слабее сопряженное ей основание, и чем сильнее основание, тем слабее сопряженная ему кислота. Кислоты и основания проявляют свои свойства только в присутствие друга: ни одно вещество не будет отдавать протон, если в системе нет акцептора протона – основания, и наоборот. Нейтральные молекулы и заряженные частицы, способные в зависи мости от условий проявлять свойства как кислоты, так и основания, называются амфотеpными.
Кислота А-Н, отдав протон, превращается в основание А¯, которое называется сопряженным основанием данной кислоты. Основание ꞉B, присоединив протон, переходит в сопряженную кислоту B+-Н. Кислота А-Н и основание А¯ , а также основание ꞉B и кислота B+-Н являются сопряженными кислотно основными парами: A H/A и H B+/B. В таких сопряжённых кислотно-основных парах чем сильнее кислота, тем слабее сопряженное ей основание, и чем сильнее основание, тем слабее сопряженная ему кислота. Кислоты и основания проявляют свои свойства только в присутствие друга: ни одно вещество не будет отдавать протон, если в системе нет акцептора протона – основания, и наоборот. Нейтральные молекулы и заряженные частицы, способные в зависи мости от условий проявлять свойства как кислоты, так и основания, называются амфотеpными.
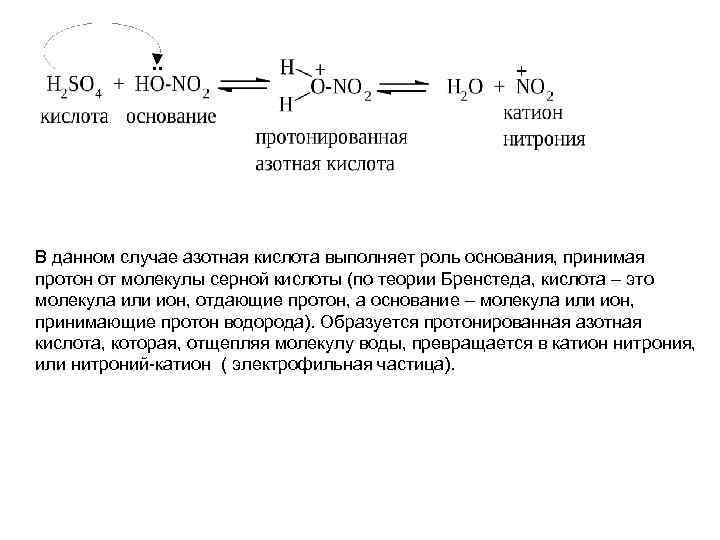 В данном случае азотная кислота выполняет роль основания, принимая протон от молекулы серной кислоты (по теории Бренстеда, кислота – это молекула или ион, отдающие протон, а основание – молекула или ион, принимающие протон водорода). Образуется протонированная азотная кислота, которая, отщепляя молекулу воды, превращается в катион нитрония, или нитроний катион ( электрофильная частица).
В данном случае азотная кислота выполняет роль основания, принимая протон от молекулы серной кислоты (по теории Бренстеда, кислота – это молекула или ион, отдающие протон, а основание – молекула или ион, принимающие протон водорода). Образуется протонированная азотная кислота, которая, отщепляя молекулу воды, превращается в катион нитрония, или нитроний катион ( электрофильная частица).
 Мерой силы кислоты А—Н является константа кислотности (a от англ. acid - кислота), которая обычно определяется по отношению к стандартному основанию — воде: Kа А – Н + Н 2 О ↔ А¯ + Н 2 О+ В сильно разбавленном растворе Kа рассчитывают по формуле: Ka=[A ] [H 3 O+]/[AH], чем больше значение Kа, тем сильнее кислота. Как правило константы кислотности очень малы. Для уксусной кислоты Kа при 250 С равна 1, 76· 10– 5. Оперировать такими малыми числами неудобно, поэтому в практической работе чаще пользуются величинами р. Kа ( показатель кислотности: р. Kа = –lg. Ka, р. Kа уксусной кислоты равна 4, 75. Чем меньше значение р. Kа, тем сильнее кислота.
Мерой силы кислоты А—Н является константа кислотности (a от англ. acid - кислота), которая обычно определяется по отношению к стандартному основанию — воде: Kа А – Н + Н 2 О ↔ А¯ + Н 2 О+ В сильно разбавленном растворе Kа рассчитывают по формуле: Ka=[A ] [H 3 O+]/[AH], чем больше значение Kа, тем сильнее кислота. Как правило константы кислотности очень малы. Для уксусной кислоты Kа при 250 С равна 1, 76· 10– 5. Оперировать такими малыми числами неудобно, поэтому в практической работе чаще пользуются величинами р. Kа ( показатель кислотности: р. Kа = –lg. Ka, р. Kа уксусной кислоты равна 4, 75. Чем меньше значение р. Kа, тем сильнее кислота.
 ТИПЫ ОРГАНИЧЕСКИХ КИСЛОТ Органические кислоты классифицируют в зависимости от природы кислотного центра (атома элемента, с которым связан атом водорода, обусловливающий кислотные свойства): • О-Н кислоты: карбоновые кислоты (RCOOH), спирты (ROH), фенолы (Ar OH), вода (HOH) и др. • S-Н кислоты: тиолы (RSH) и др. • N-Н кислоты: амины (R NH 2 ), амиды кислот (RСОNH 2 и др. • С-Н кислоты: углеводороды (алканы, алкены =С Н, алкины ≡С Н)
ТИПЫ ОРГАНИЧЕСКИХ КИСЛОТ Органические кислоты классифицируют в зависимости от природы кислотного центра (атома элемента, с которым связан атом водорода, обусловливающий кислотные свойства): • О-Н кислоты: карбоновые кислоты (RCOOH), спирты (ROH), фенолы (Ar OH), вода (HOH) и др. • S-Н кислоты: тиолы (RSH) и др. • N-Н кислоты: амины (R NH 2 ), амиды кислот (RСОNH 2 и др. • С-Н кислоты: углеводороды (алканы, алкены =С Н, алкины ≡С Н)
 Сила кислот определяется устойчивостью образующихся после отщепления протона сопряженных оснований (анионов). Чем устойчивее сопряженное основание (анион), тем сильнее кислота. Устойчивость же аниона обусловлена степенью делокализации отрицательного заряда и зависит от факторов: природы кислотного центра (электроотрицательности и поляризуемости кислотного центра); характера заместителя, связанного с кислотным центром (электронные эффекты заместителя –ЭД или ЭА); сольватационных эффектов (природа растворителя).
Сила кислот определяется устойчивостью образующихся после отщепления протона сопряженных оснований (анионов). Чем устойчивее сопряженное основание (анион), тем сильнее кислота. Устойчивость же аниона обусловлена степенью делокализации отрицательного заряда и зависит от факторов: природы кислотного центра (электроотрицательности и поляризуемости кислотного центра); характера заместителя, связанного с кислотным центром (электронные эффекты заместителя –ЭД или ЭА); сольватационных эффектов (природа растворителя).
 Электроотрицательность имеет значение, когда сравнивается кис лотность соединений, имеющих одинаковые радикалы и элементы кислотного центра, относящиеся к одному и тому же периоду перио дической системы Д. И. Менделеева (т. е. когда практически не изменяется поляризуемость): С 2 Н 5 -Х-Н + НОН ↔ С 2 Н 5 -Х- + Н 3 О+ С–Н кислота N–H кислота О–Н кислота С 2 Н 5 СH 2–Н пропан С 2 Н 5 NH–H этиламин С 2 Н 5 О–Н этанол р. Ка = 50 р. Ка = 30 р. Ка = 16 С 2 Н 5 –СН 2 - С 2 Н 5 –NH- С 2 Н 5 -O- В пределах периода периодической системы электроотрицательность атомов возрастает слева направо (поляризуемость не изменяется), поэтому ОН кислоты сильнее соответствующих NН кислот, а те, в свою очередь, сильнее СН кислот.
Электроотрицательность имеет значение, когда сравнивается кис лотность соединений, имеющих одинаковые радикалы и элементы кислотного центра, относящиеся к одному и тому же периоду перио дической системы Д. И. Менделеева (т. е. когда практически не изменяется поляризуемость): С 2 Н 5 -Х-Н + НОН ↔ С 2 Н 5 -Х- + Н 3 О+ С–Н кислота N–H кислота О–Н кислота С 2 Н 5 СH 2–Н пропан С 2 Н 5 NH–H этиламин С 2 Н 5 О–Н этанол р. Ка = 50 р. Ка = 30 р. Ка = 16 С 2 Н 5 –СН 2 - С 2 Н 5 –NH- С 2 Н 5 -O- В пределах периода периодической системы электроотрицательность атомов возрастает слева направо (поляризуемость не изменяется), поэтому ОН кислоты сильнее соответствующих NН кислот, а те, в свою очередь, сильнее СН кислот.
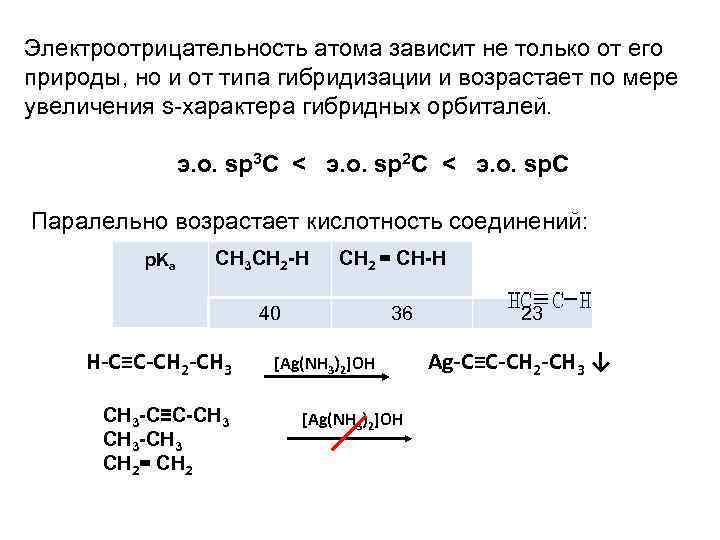 Электроотрицательность атома зависит не только от его природы, но и от типа гибридизации и возрастает по мере увеличения s характера гибридных орбиталей. э. о. sp 3 C < э. о. sp 2 C < э. о. sp. C Паралельно возрастает кислотность соединений: CH 3 CH 2 -H CH 2 = CH-H p. Ka 40 36 23 H-C≡C-CH 2 -CH 3 Ag-C≡C-CH 2 -CH 3 ↓ [Ag(NH 3)2]OH CH 3 -C≡C-CH 3 -CH 3 CH 2= CH 2 [Ag(NH 3)2]OH
Электроотрицательность атома зависит не только от его природы, но и от типа гибридизации и возрастает по мере увеличения s характера гибридных орбиталей. э. о. sp 3 C < э. о. sp 2 C < э. о. sp. C Паралельно возрастает кислотность соединений: CH 3 CH 2 -H CH 2 = CH-H p. Ka 40 36 23 H-C≡C-CH 2 -CH 3 Ag-C≡C-CH 2 -CH 3 ↓ [Ag(NH 3)2]OH CH 3 -C≡C-CH 3 -CH 3 CH 2= CH 2 [Ag(NH 3)2]OH
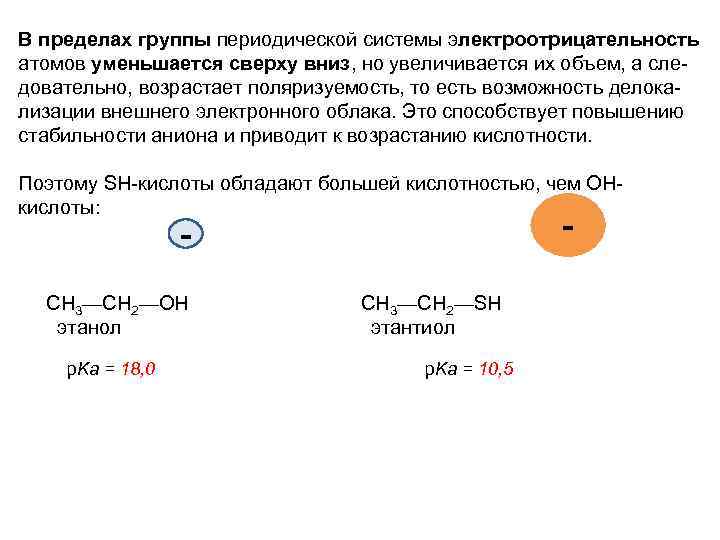 В пределах группы периодической системы электроотрицательность атомов уменьшается сверху вниз, но увеличивается их объем, а сле довательно, возрастает поляризуемость, то есть возможность делока лизации внешнего электронного облака. Это способствует повышению стабильности аниона и приводит к возрастанию кислотности. Поэтому SН кислоты обладают большей кислотностью, чем ОН кислоты: - - CH 3—CH 2—OH CH 3—CH 2—SH этанол этантиол р. Kа = 18, 0 р. Kа = 10, 5
В пределах группы периодической системы электроотрицательность атомов уменьшается сверху вниз, но увеличивается их объем, а сле довательно, возрастает поляризуемость, то есть возможность делока лизации внешнего электронного облака. Это способствует повышению стабильности аниона и приводит к возрастанию кислотности. Поэтому SН кислоты обладают большей кислотностью, чем ОН кислоты: - - CH 3—CH 2—OH CH 3—CH 2—SH этанол этантиол р. Kа = 18, 0 р. Kа = 10, 5
 Тиолы, как более сильные кислоты, в отличие от спиртов, реагируют не только со щелочными металлами, но и со щелочами, а также оксидами и солями тяжелых металлов (ртуть, свинец, мышьяк, хром, висмут и др. ): Меркаптиды ртути, серебра нерастворимы в воде, поэтому эта реакция лежит в основе определения тиолов в биологических жидкостях. Тиолы, например, 2, 3 димеркаптопропанол, используются в качестве антидотов при отравлении солями тяжелых металлов, люизитом.
Тиолы, как более сильные кислоты, в отличие от спиртов, реагируют не только со щелочными металлами, но и со щелочами, а также оксидами и солями тяжелых металлов (ртуть, свинец, мышьяк, хром, висмут и др. ): Меркаптиды ртути, серебра нерастворимы в воде, поэтому эта реакция лежит в основе определения тиолов в биологических жидкостях. Тиолы, например, 2, 3 димеркаптопропанол, используются в качестве антидотов при отравлении солями тяжелых металлов, люизитом.
 Органические кислоты с одинаковыми радикалами в зависимости от природы кислотного центра можно расположить по возрастанию кислотности: SН-кислоты > ОН-кислоты > NН-кислоты > СН-кислоты С 2 Н 5 S–H > С 2 Н 5 О–H > С 2 Н 5 NH 2 > С 2 Н 5 СH 3 Тиолы более сильные кислоты, чем алифатические спирты, амины и углеводороды, соответственно
Органические кислоты с одинаковыми радикалами в зависимости от природы кислотного центра можно расположить по возрастанию кислотности: SН-кислоты > ОН-кислоты > NН-кислоты > СН-кислоты С 2 Н 5 S–H > С 2 Н 5 О–H > С 2 Н 5 NH 2 > С 2 Н 5 СH 3 Тиолы более сильные кислоты, чем алифатические спирты, амины и углеводороды, соответственно
 В пределах одного типа кислотность зависит от строения ради кала, связанного с кислотным центром. Алкильные радикалы, благода ря +I эффекту, увеличивают электронную плотность в кислотном центре и тем самым дестабилизируют анион, что приводит к умень шению кислотности. Ароматические радикалы, наоборот, повышают устойчивость аниона за счет делокализации отрицательного заряда и способствуют увеличению кислотных свойств. Фенолы по сравнению со спиртами проявляют более заметные кислот ные свойства: 0, 1 М водный раствор фенола имеет р. Н 5, 4. Повышен ная кислотность фенолов обусловлена лучшей делокализацией заряда в феноксид ионе, чем в алкоксид ионах, благодаря р, π сопряжению
В пределах одного типа кислотность зависит от строения ради кала, связанного с кислотным центром. Алкильные радикалы, благода ря +I эффекту, увеличивают электронную плотность в кислотном центре и тем самым дестабилизируют анион, что приводит к умень шению кислотности. Ароматические радикалы, наоборот, повышают устойчивость аниона за счет делокализации отрицательного заряда и способствуют увеличению кислотных свойств. Фенолы по сравнению со спиртами проявляют более заметные кислот ные свойства: 0, 1 М водный раствор фенола имеет р. Н 5, 4. Повышен ная кислотность фенолов обусловлена лучшей делокализацией заряда в феноксид ионе, чем в алкоксид ионах, благодаря р, π сопряжению
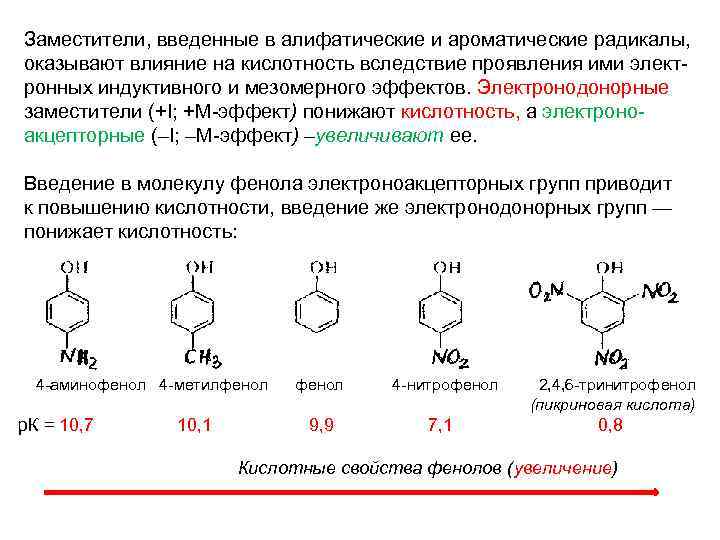 Заместители, введенные в алифатические и ароматические радикалы, оказывают влияние на кислотность вследствие проявления ими элект ронных индуктивного и мезомерного эффектов. Электронодонорные заместители (+І; +М эффект) понижают кислотность, а электроно акцепторные (–І; –М эффект) –увеличивают ее. Введение в молекулу фенола электроноакцепторных групп приводит к повышению кислотности, введение же электронодонорных групп — понижает кислотность: 4 аминофенол 4 метилфенол 4 нитрофенол 2, 4, 6 тринитрофенол (пикриновая кислота) р. К = 10, 7 10, 1 9, 9 7, 1 0, 8 Кислотные свойства фенолов (увеличение)
Заместители, введенные в алифатические и ароматические радикалы, оказывают влияние на кислотность вследствие проявления ими элект ронных индуктивного и мезомерного эффектов. Электронодонорные заместители (+І; +М эффект) понижают кислотность, а электроно акцепторные (–І; –М эффект) –увеличивают ее. Введение в молекулу фенола электроноакцепторных групп приводит к повышению кислотности, введение же электронодонорных групп — понижает кислотность: 4 аминофенол 4 метилфенол 4 нитрофенол 2, 4, 6 тринитрофенол (пикриновая кислота) р. К = 10, 7 10, 1 9, 9 7, 1 0, 8 Кислотные свойства фенолов (увеличение)
 В карбоновых кислотах при диссоциации образуются карбоксилат ионы – самые стабильные органические анионы. В карбоксилат ионе отрицательный заряд за счет р, π сопряжения расп ределён поровну между двумя атомами кислорода, т. е. он делокализо ван и соответственно менее концентрирован, поэтому в карбоновых кислотах кислотный центр более сильный, чем в спиртах и фенолах. С увеличением углеводородного радикала, который выполняет роль э. д. кислотность монокарбоновых кислот снижается за счет уменьшения δ+ на атоме углерода карбоксильной группы. Поэтому в гомологическом ряду кислот самой сильной является муравьиная кислота.
В карбоновых кислотах при диссоциации образуются карбоксилат ионы – самые стабильные органические анионы. В карбоксилат ионе отрицательный заряд за счет р, π сопряжения расп ределён поровну между двумя атомами кислорода, т. е. он делокализо ван и соответственно менее концентрирован, поэтому в карбоновых кислотах кислотный центр более сильный, чем в спиртах и фенолах. С увеличением углеводородного радикала, который выполняет роль э. д. кислотность монокарбоновых кислот снижается за счет уменьшения δ+ на атоме углерода карбоксильной группы. Поэтому в гомологическом ряду кислот самой сильной является муравьиная кислота.
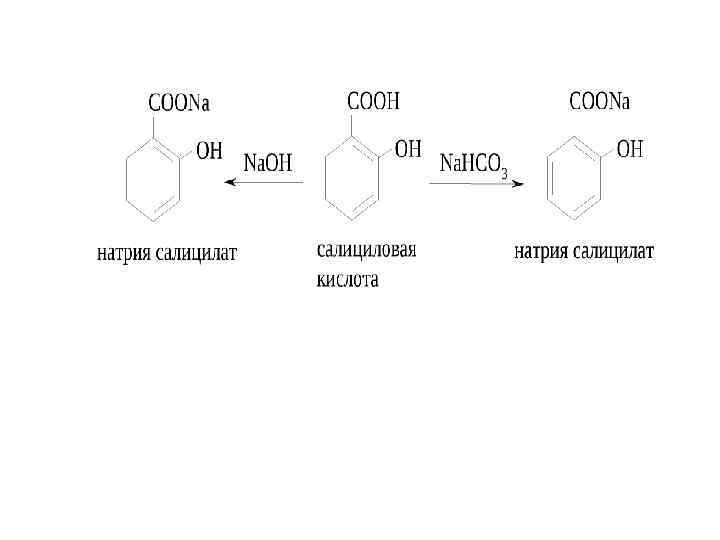
 В алифатическом ряду наиболее сильное влияние на кислотность оказывают заместители, расположенные ближе к кислотному центру Cl. CH 2 COOH Cl. CH 2 COOH хлоруксусная 3 хлорпропановая 4 хлорбутановая (β хлорпропионовая) (γ – масляная) p. Ka = 2, 86 p. Ka = 4, 1 p. Ka = 4, 5
В алифатическом ряду наиболее сильное влияние на кислотность оказывают заместители, расположенные ближе к кислотному центру Cl. CH 2 COOH Cl. CH 2 COOH хлоруксусная 3 хлорпропановая 4 хлорбутановая (β хлорпропионовая) (γ – масляная) p. Ka = 2, 86 p. Ka = 4, 1 p. Ka = 4, 5
 В алифатическом ряду наиболее оказывает влияние и количество заместителей; хлоруксусная дихлоруксусная трихлоруксусная p. Ka = 2, 86 1, 3 0, 66
В алифатическом ряду наиболее оказывает влияние и количество заместителей; хлоруксусная дихлоруксусная трихлоруксусная p. Ka = 2, 86 1, 3 0, 66
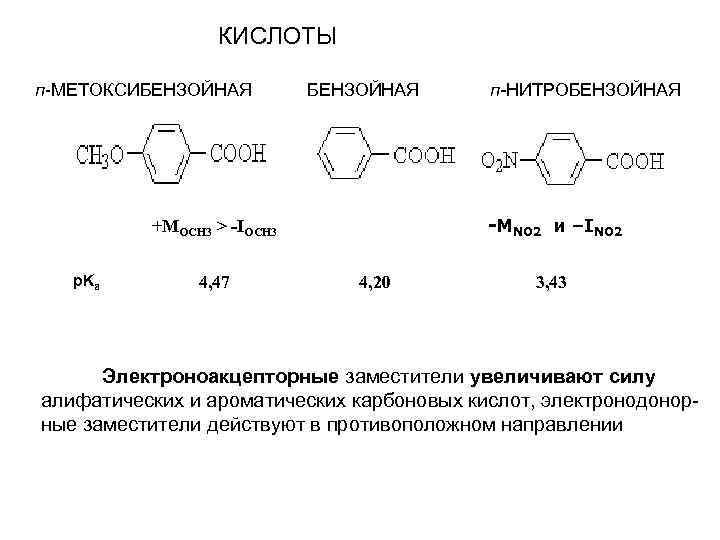 КИСЛОТЫ п МЕТОКСИБЕНЗОЙНАЯ п-НИТРОБЕНЗОЙНАЯ p. Ka +MOCH 3 > -IOCH 3 4, 47 -MNO 2 и –INO 2 4, 20 3, 43 Электроноакцепторные заместители увеличивают силу алифатических и ароматических карбоновых кислот, электронодонор ные заместители действуют в противоположном направлении
КИСЛОТЫ п МЕТОКСИБЕНЗОЙНАЯ п-НИТРОБЕНЗОЙНАЯ p. Ka +MOCH 3 > -IOCH 3 4, 47 -MNO 2 и –INO 2 4, 20 3, 43 Электроноакцепторные заместители увеличивают силу алифатических и ароматических карбоновых кислот, электронодонор ные заместители действуют в противоположном направлении
 Наряду с природой кислотного центра и строением радикала значи тельное влияние на проявление кислотных свойств оказывает растворитель. Влияние растворителя определяют его диэлектричес кой проницаемостью и способностью сольватировать растворенные частицы. Чем выше сольватационный эффект, тем стабильнее ионы в растворе. При равных прочих условиях сольватация аниона протекает тем сильнее, чем меньше его размер и менее делокализован в нем заряд, т. е. влияние сольватационного эффекта растворителя и влияние заместителей на кислотность противоположны другу. Наиболее эффективным растворителем является вода, обладающая высокой диэлектрической проницаемостью (ε = 80 при 20 °С) и способностью к сольватации растворенных частиц.
Наряду с природой кислотного центра и строением радикала значи тельное влияние на проявление кислотных свойств оказывает растворитель. Влияние растворителя определяют его диэлектричес кой проницаемостью и способностью сольватировать растворенные частицы. Чем выше сольватационный эффект, тем стабильнее ионы в растворе. При равных прочих условиях сольватация аниона протекает тем сильнее, чем меньше его размер и менее делокализован в нем заряд, т. е. влияние сольватационного эффекта растворителя и влияние заместителей на кислотность противоположны другу. Наиболее эффективным растворителем является вода, обладающая высокой диэлектрической проницаемостью (ε = 80 при 20 °С) и способностью к сольватации растворенных частиц.
 Влияние растворителя Взаимодействие молекул или ионов растворенного вещества с растворителем называется процессом сольватации. Стабильность аниона существенно зависит от его сольватации в растворе: чем больше ион сольватирован, тем он устойчивее, а сольватация тем больше, чем меньше размер иона и чем меньше делокализация в нем отрицательного заряда. В ряду карбоновых кислот с увеличением длины алифатического (гидрофобного) радикала кислотность уменьшается. р. Ка НСООН муравьиная 3, 7 СН 3 СООН уксусная 4, 8 СН 3–СН 2–СООН пропановая 4, 9 С 15 Н 31–СООН пальмитиновая Эффект сольватации может оказать более сильное воздействие на кислотность, чем электронные эффекты заместителей.
Влияние растворителя Взаимодействие молекул или ионов растворенного вещества с растворителем называется процессом сольватации. Стабильность аниона существенно зависит от его сольватации в растворе: чем больше ион сольватирован, тем он устойчивее, а сольватация тем больше, чем меньше размер иона и чем меньше делокализация в нем отрицательного заряда. В ряду карбоновых кислот с увеличением длины алифатического (гидрофобного) радикала кислотность уменьшается. р. Ка НСООН муравьиная 3, 7 СН 3 СООН уксусная 4, 8 СН 3–СН 2–СООН пропановая 4, 9 С 15 Н 31–СООН пальмитиновая Эффект сольватации может оказать более сильное воздействие на кислотность, чем электронные эффекты заместителей.
 ОСНОВНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Органические соединения, в состав молекулы которых входят атомы азота, кислорода, серы, могут выступать в роли оснований, присоединяя протон водорода за счет неподеленной пары электронов на внешнем энергетическом уровне. Такие атомы в молекуле органического вещества, присоединяющие протон, называются центрами основности. Основания по Бренстеду Лоури делятся на n – основания и π – основания. n – Основания могут быть нейтральными или отрицательно заряженными частицами. π - Основания (алкины, алкены, диены, арены) – центр основности электроны π связи.
ОСНОВНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Органические соединения, в состав молекулы которых входят атомы азота, кислорода, серы, могут выступать в роли оснований, присоединяя протон водорода за счет неподеленной пары электронов на внешнем энергетическом уровне. Такие атомы в молекуле органического вещества, присоединяющие протон, называются центрами основности. Основания по Бренстеду Лоури делятся на n – основания и π – основания. n – Основания могут быть нейтральными или отрицательно заряженными частицами. π - Основания (алкины, алкены, диены, арены) – центр основности электроны π связи.
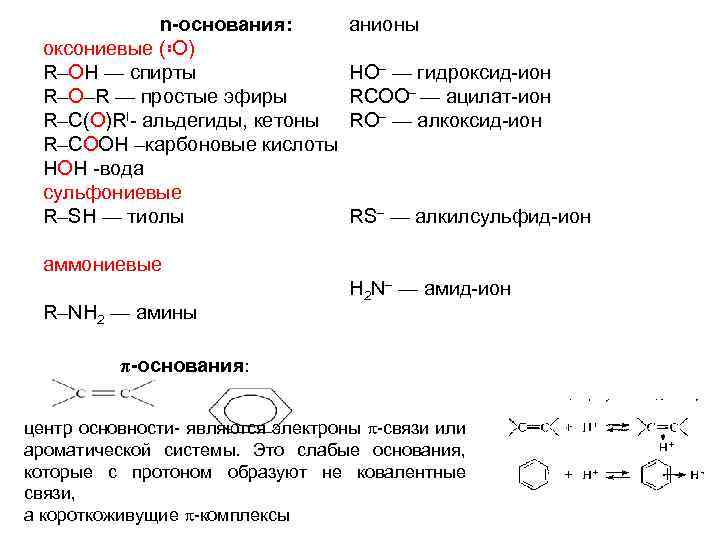 n-основания: оксониевые (꞉О) R–ОН — спирты R–O–R — простые эфиры R–С(О)RI альдегиды, кетоны R–СООН –карбоновые кислоты НОН вода сульфониевые R–SH — тиолы анионы НО — гидроксид ион RCOO — ацилат ион RO — алкоксид ион RS — алкилсульфид ион аммониевые R–NH 2 — амины H 2 N — амид ион π-основания: центр основности являются электроны связи или ароматической системы. Это слабые основания, которые с протоном образуют не ковалентные связи, а короткоживущие комплексы
n-основания: оксониевые (꞉О) R–ОН — спирты R–O–R — простые эфиры R–С(О)RI альдегиды, кетоны R–СООН –карбоновые кислоты НОН вода сульфониевые R–SH — тиолы анионы НО — гидроксид ион RCOO — ацилат ион RO — алкоксид ион RS — алкилсульфид ион аммониевые R–NH 2 — амины H 2 N — амид ион π-основания: центр основности являются электроны связи или ароматической системы. Это слабые основания, которые с протоном образуют не ковалентные связи, а короткоживущие комплексы
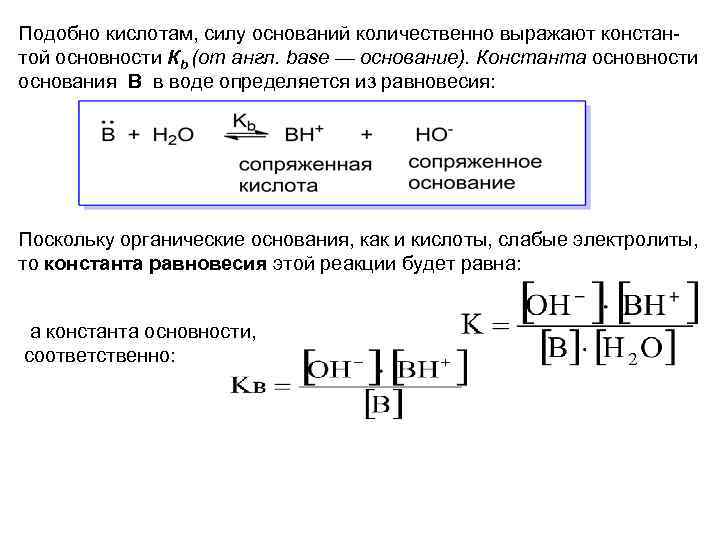 Подобно кислотам, силу оснований количественно выражают констан той основности Кb (от англ. base — основание). Константа основности основания В в воде определяется из равновесия: Поскольку органические основания, как и кислоты, слабые электролиты, то константа равновесия этой реакции будет равна: а константа основности, соответственно:
Подобно кислотам, силу оснований количественно выражают констан той основности Кb (от англ. base — основание). Константа основности основания В в воде определяется из равновесия: Поскольку органические основания, как и кислоты, слабые электролиты, то константа равновесия этой реакции будет равна: а константа основности, соответственно:
 Чем больше Kb, тем сильнее основание. Как и в случае с кислотами, для удобства силу оснований выражают обычно величиной р. Kb: р. Kb= – lg. Kb. Чем меньше р. Kb, тем сильнее соответствующее основание. Так кислота отщепляет протон, а основание его присоединяет, то кислотные и основные свойства можно количественно характеризовать одной величиной сродством к иону водорода. Это позволяет применять константы кислотной ионизации как для кислот, так и для оснований; т. е. силу оснований оценивают константой кислотности сопряженной основанию кислоты ВН+, обозначаемую как р. KВН+. Чем больше значение р. KВН+, тем сильнее основание (A H /A и H B+/B)
Чем больше Kb, тем сильнее основание. Как и в случае с кислотами, для удобства силу оснований выражают обычно величиной р. Kb: р. Kb= – lg. Kb. Чем меньше р. Kb, тем сильнее соответствующее основание. Так кислота отщепляет протон, а основание его присоединяет, то кислотные и основные свойства можно количественно характеризовать одной величиной сродством к иону водорода. Это позволяет применять константы кислотной ионизации как для кислот, так и для оснований; т. е. силу оснований оценивают константой кислотности сопряженной основанию кислоты ВН+, обозначаемую как р. KВН+. Чем больше значение р. KВН+, тем сильнее основание (A H /A и H B+/B)
 По аналогии с кислотами сила оснований зависит от ряда факторов: - природы основного центра; - характера заместителя, связанного с основным центром: природы растворителя. При равных других факторах с увеличением электроотрицательности атома основного центра, в пределах одного и того же периода, непо деленная пара электронов удерживается прочнее, а следовательно, основность соединения уменьшается. Поэтому оксониевые основания слабее аммониевых. В пределах группы периодической системы с увеличением поляризу емости атома основного центра усиливается делокализация неподе ленной электронной пары и соответственно уменьшается основность соединения. Поэтому сульфониевые основания слабее оксониевых. Еще более слабыми основными свойствами обладают π основания, в которых электронная пара, присоединяющая протон, не является свободной
По аналогии с кислотами сила оснований зависит от ряда факторов: - природы основного центра; - характера заместителя, связанного с основным центром: природы растворителя. При равных других факторах с увеличением электроотрицательности атома основного центра, в пределах одного и того же периода, непо деленная пара электронов удерживается прочнее, а следовательно, основность соединения уменьшается. Поэтому оксониевые основания слабее аммониевых. В пределах группы периодической системы с увеличением поляризу емости атома основного центра усиливается делокализация неподе ленной электронной пары и соответственно уменьшается основность соединения. Поэтому сульфониевые основания слабее оксониевых. Еще более слабыми основными свойствами обладают π основания, в которых электронная пара, присоединяющая протон, не является свободной
 Качественно выраженность основных свойств зависит от тех же факторов, что и кислотных, но влияние их противоположно. В пределах одного и того же периода таблицы Менделеева, чем больше электроотрицательность элемента основного центра, тем прочнее он удержи вает неподеленную пару электронов, и тем менее она доступна для протона. Поэтому, если сравнивать основность соединений с одинаковыми радикалами (диметиловый эфир и диметиламин), то оксониевое метиламин). основание(метокиметан) будет слабее аммониевого(N В тиониевых (сульфониевых) основаниях, например, СН 3 S СН 3 (диметил сульфид) электронная плотность атома серы рассредоточена в большем объеме (поляризуемость атома серы больше, чем кислорода), и плотность заряда значительно меньше. Поэтому сульфониевые основания слабее оксониевых и не способны образовывать прочные связи с протоном. В целом, сила n-оснований с одинаковыми радикалами уменьшается в ряду: N > O > S. Наибольшую основность среди органических соединений проявляют амины.
Качественно выраженность основных свойств зависит от тех же факторов, что и кислотных, но влияние их противоположно. В пределах одного и того же периода таблицы Менделеева, чем больше электроотрицательность элемента основного центра, тем прочнее он удержи вает неподеленную пару электронов, и тем менее она доступна для протона. Поэтому, если сравнивать основность соединений с одинаковыми радикалами (диметиловый эфир и диметиламин), то оксониевое метиламин). основание(метокиметан) будет слабее аммониевого(N В тиониевых (сульфониевых) основаниях, например, СН 3 S СН 3 (диметил сульфид) электронная плотность атома серы рассредоточена в большем объеме (поляризуемость атома серы больше, чем кислорода), и плотность заряда значительно меньше. Поэтому сульфониевые основания слабее оксониевых и не способны образовывать прочные связи с протоном. В целом, сила n-оснований с одинаковыми радикалами уменьшается в ряду: N > O > S. Наибольшую основность среди органических соединений проявляют амины.
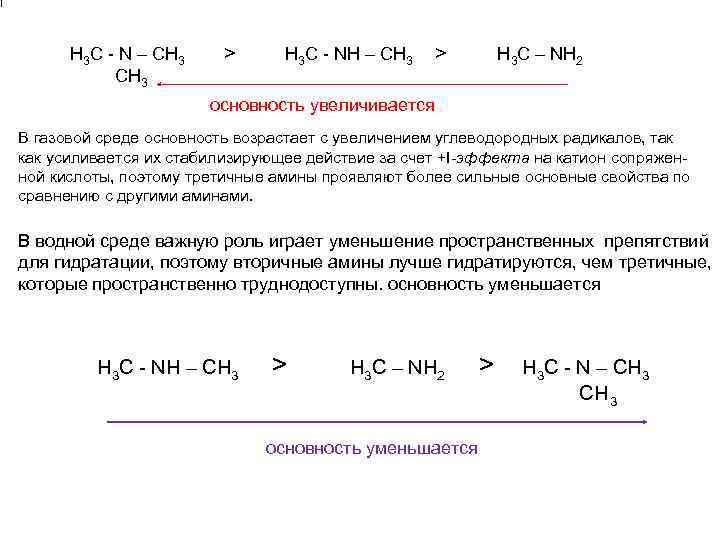 Н 3 C N – CH 3 > H 3 C NH – CH 3 > H 3 C – NH 2 CH 3 основность увеличивается В газовой среде основность возрастает с увеличением углеводородных радикалов, так как усиливается их стабилизирующее действие за счет +I эффекта на катион сопряжен ной кислоты, поэтому третичные амины проявляют более сильные основные свойства по сравнению с другими аминами. В водной среде важную роль играет уменьшение пространственных препятствий для гидратации, поэтому вторичные амины лучше гидратируются, чем третичные, которые пространственно труднодоступны. основность уменьшается H 3 C NH – CH 3 > H 3 C – NH 2 > H 3 C N – CH 3 CH 3 основность уменьшается
Н 3 C N – CH 3 > H 3 C NH – CH 3 > H 3 C – NH 2 CH 3 основность увеличивается В газовой среде основность возрастает с увеличением углеводородных радикалов, так как усиливается их стабилизирующее действие за счет +I эффекта на катион сопряжен ной кислоты, поэтому третичные амины проявляют более сильные основные свойства по сравнению с другими аминами. В водной среде важную роль играет уменьшение пространственных препятствий для гидратации, поэтому вторичные амины лучше гидратируются, чем третичные, которые пространственно труднодоступны. основность уменьшается H 3 C NH – CH 3 > H 3 C – NH 2 > H 3 C N – CH 3 CH 3 основность уменьшается
 Основность органических соединений тем выше, чем больше элект ронная плотности на атоме, который является акцептором протонов. Поэтому основность увеличивается в следующем ряду аминов:
Основность органических соединений тем выше, чем больше элект ронная плотности на атоме, который является акцептором протонов. Поэтому основность увеличивается в следующем ряду аминов:
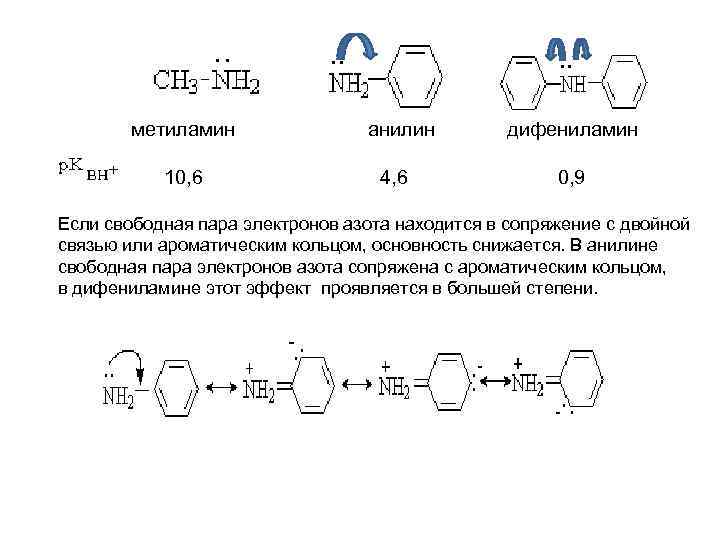 метиламин анилин дифениламин 10, 6 4, 6 0, 9 Если свободная пара электронов азота находится в сопряжение с двойной связью или ароматическим кольцом, основность снижается. В анилине свободная пара электронов азота сопряжена с ароматическим кольцом, в дифениламине этот эффект проявляется в большей степени.
метиламин анилин дифениламин 10, 6 4, 6 0, 9 Если свободная пара электронов азота находится в сопряжение с двойной связью или ароматическим кольцом, основность снижается. В анилине свободная пара электронов азота сопряжена с ароматическим кольцом, в дифениламине этот эффект проявляется в большей степени.
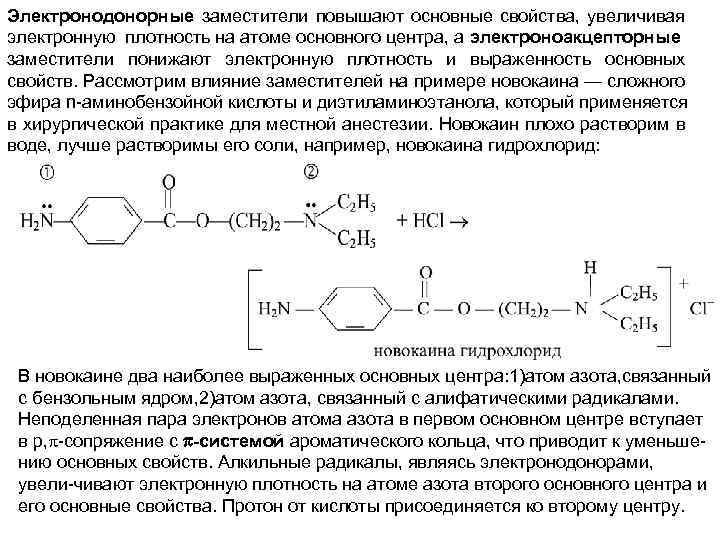 Электронодонорные заместители повышают основные свойства, увеличивая электронную плотность на атоме основного центра, а электроноакцепторные заместители понижают электронную плотность и выраженность основных свойств. Рассмотрим влияние заместителей на примере новокаина — сложного эфира n аминобензойной кислоты и диэтиламиноэтанола, который применяется в хирургической практике для местной анестезии. Новокаин плохо растворим в воде, лучше растворимы его соли, например, новокаина гидрохлорид: В новокаине два наиболее выраженных основных центра: 1)атом азота, связанный с бензольным ядром, 2)атом азота, связанный с алифатическими радикалами. Неподеленная пара электронов атома азота в первом основном центре вступает в р, сопряжение с -системой ароматического кольца, что приводит к уменьше нию основных свойств. Алкильные радикалы, являясь электронодонорами, увели чивают электронную плотность на атоме азота второго основного центра и его основные свойства. Протон от кислоты присоединяется ко второму центру.
Электронодонорные заместители повышают основные свойства, увеличивая электронную плотность на атоме основного центра, а электроноакцепторные заместители понижают электронную плотность и выраженность основных свойств. Рассмотрим влияние заместителей на примере новокаина — сложного эфира n аминобензойной кислоты и диэтиламиноэтанола, который применяется в хирургической практике для местной анестезии. Новокаин плохо растворим в воде, лучше растворимы его соли, например, новокаина гидрохлорид: В новокаине два наиболее выраженных основных центра: 1)атом азота, связанный с бензольным ядром, 2)атом азота, связанный с алифатическими радикалами. Неподеленная пара электронов атома азота в первом основном центре вступает в р, сопряжение с -системой ароматического кольца, что приводит к уменьше нию основных свойств. Алкильные радикалы, являясь электронодонорами, увели чивают электронную плотность на атоме азота второго основного центра и его основные свойства. Протон от кислоты присоединяется ко второму центру.
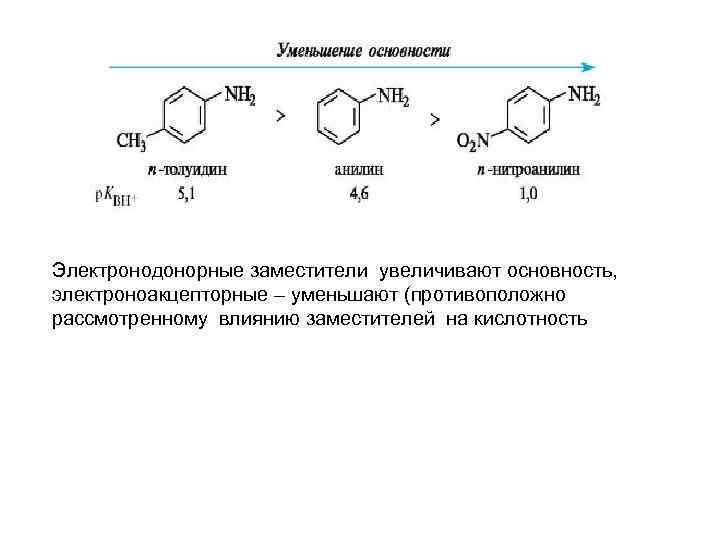 Электронодонорные заместители увеличивают основность, электроноакцепторные – уменьшают (противоположно рассмотренному влиянию заместителей на кислотность
Электронодонорные заместители увеличивают основность, электроноакцепторные – уменьшают (противоположно рассмотренному влиянию заместителей на кислотность
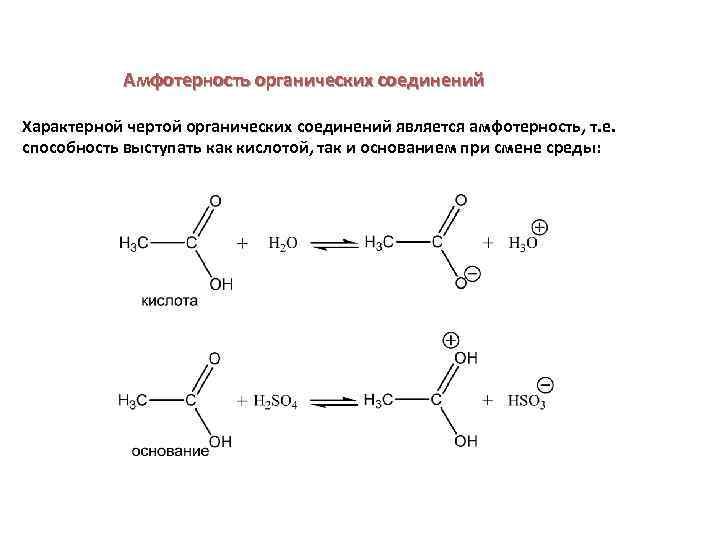 Амфотерность органических соединений Характерной чертой органических соединений является амфотерность, т. е. способность выступать как кислотой, так и основанием при смене среды:
Амфотерность органических соединений Характерной чертой органических соединений является амфотерность, т. е. способность выступать как кислотой, так и основанием при смене среды:
 3. Электронная теория кислот и оснований, или Теория Льиса (1926) ( Электронная теория кислот и оснований является наиболее общей теорией кислот и оснований По Льюису кислоты это вещества, способные принимать электронную пару (акцетор электронной пары), а основания вещества, способные давать электронную пару (доноры электронной пары) Джилберт Ньютон Льюис 1875 1946 г. американский физикохимик К кислотам Льюиса относятся не только протон H+, но и все катионы, а также галогениды металлов 2 и 3 групп таблицы Менделеева: Al. X 3, Fe. X 3, BX 3, Sb. X 5, Sn. X 4, Zn. X 2 (X=F, Cl, Br, I). К основаниям Льюиса - все анионы OH-, OR-, CH 3 COO-, NH 2 - и т. д. и нейтральные соединения, имеющие неподеленные электронные пары или π- связи - H 2 O, ROH, ROR, RCH=O, RSH, NH 3, R 3 N, RCH=CH 2, R-C 6 H 5 и др.
3. Электронная теория кислот и оснований, или Теория Льиса (1926) ( Электронная теория кислот и оснований является наиболее общей теорией кислот и оснований По Льюису кислоты это вещества, способные принимать электронную пару (акцетор электронной пары), а основания вещества, способные давать электронную пару (доноры электронной пары) Джилберт Ньютон Льюис 1875 1946 г. американский физикохимик К кислотам Льюиса относятся не только протон H+, но и все катионы, а также галогениды металлов 2 и 3 групп таблицы Менделеева: Al. X 3, Fe. X 3, BX 3, Sb. X 5, Sn. X 4, Zn. X 2 (X=F, Cl, Br, I). К основаниям Льюиса - все анионы OH-, OR-, CH 3 COO-, NH 2 - и т. д. и нейтральные соединения, имеющие неподеленные электронные пары или π- связи - H 2 O, ROH, ROR, RCH=O, RSH, NH 3, R 3 N, RCH=CH 2, R-C 6 H 5 и др.
 Если в теории Брёнстеда кислота — это донор протона, то согласно теории Льюиса сам протон является кислотой, поскольку имеет вакантную орбиталь. Таким образом, в представлении электронной теории кислота Брёнстеда явля ется соединением, которое образует кислоту Льюиса. Поэтому согласно теории Льюиса к кислотам относят не только соединения, отщепляющие протон (протонные кислоты), но и другие вещества, имеющие вакантную орбиталь и способные принимать пару электронов. Кислотно основный процесс по Льюису состоит в образовании ковалентной связи между основанием и кислотой за счет электронной пары основания и ва кантной орбитали кислоты. Основания Льюиса, имеющие неподеленные пары электронов, образуют с кислотами Льюиса π –комплексы: Основания Льюиса, содержащие в своей структуре π-связь, образуют с кислотами π –комплексы
Если в теории Брёнстеда кислота — это донор протона, то согласно теории Льюиса сам протон является кислотой, поскольку имеет вакантную орбиталь. Таким образом, в представлении электронной теории кислота Брёнстеда явля ется соединением, которое образует кислоту Льюиса. Поэтому согласно теории Льюиса к кислотам относят не только соединения, отщепляющие протон (протонные кислоты), но и другие вещества, имеющие вакантную орбиталь и способные принимать пару электронов. Кислотно основный процесс по Льюису состоит в образовании ковалентной связи между основанием и кислотой за счет электронной пары основания и ва кантной орбитали кислоты. Основания Льюиса, имеющие неподеленные пары электронов, образуют с кислотами Льюиса π –комплексы: Основания Льюиса, содержащие в своей структуре π-связь, образуют с кислотами π –комплексы
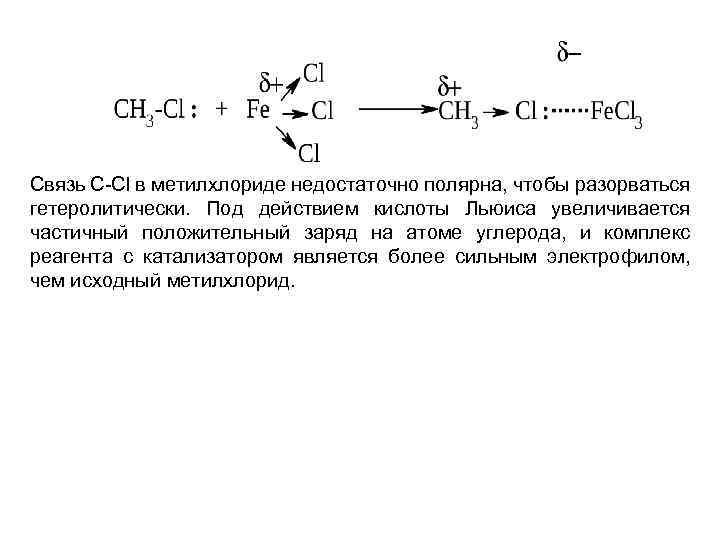 Связь C Cl в метилхлориде недостаточно полярна, чтобы разорваться гетеролитически. Под действием кислоты Льюиса увеличивается частичный положительный заряд на атоме углерода, и комплекс реагента с катализатором является более сильным электрофилом, чем исходный метилхлорид.
Связь C Cl в метилхлориде недостаточно полярна, чтобы разорваться гетеролитически. Под действием кислоты Льюиса увеличивается частичный положительный заряд на атоме углерода, и комплекс реагента с катализатором является более сильным электрофилом, чем исходный метилхлорид.
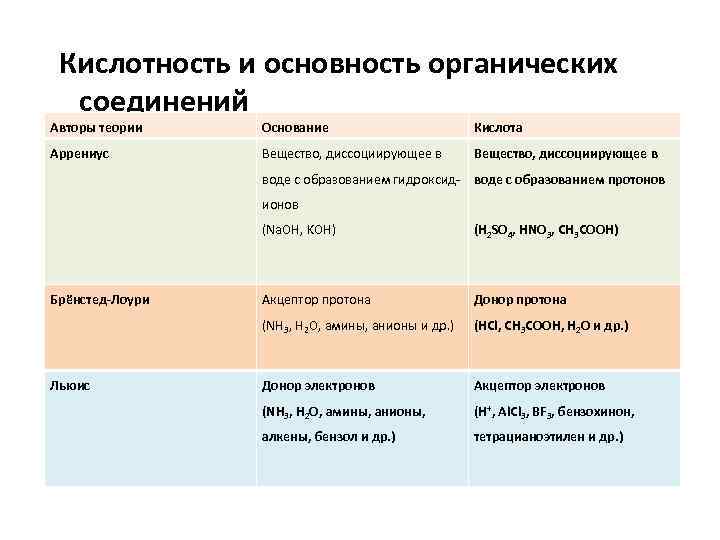 Кислотность и основность органических соединений Авторы теории Основание Кислота Аррениус Вещество, диссоциирующее в воде с образованием гидроксид- воде с образованием протонов ионов (Na. OH, KOH) Льюис (H 2 SO 4, HNO 3, CH 3 COOH) Акцептор протона Донор протона (NH 3, H 2 O, амины, анионы и др. ) Брёнстед-Лоури (HCl, CH 3 COOH, H 2 O и др. ) Донор электронов Акцептор электронов (NH 3, H 2 O, амины, анионы, (H+, Al. Cl 3, BF 3, бензохинон, алкены, бензол и др. ) тетрацианоэтилен и др. )
Кислотность и основность органических соединений Авторы теории Основание Кислота Аррениус Вещество, диссоциирующее в воде с образованием гидроксид- воде с образованием протонов ионов (Na. OH, KOH) Льюис (H 2 SO 4, HNO 3, CH 3 COOH) Акцептор протона Донор протона (NH 3, H 2 O, амины, анионы и др. ) Брёнстед-Лоури (HCl, CH 3 COOH, H 2 O и др. ) Донор электронов Акцептор электронов (NH 3, H 2 O, амины, анионы, (H+, Al. Cl 3, BF 3, бензохинон, алкены, бензол и др. ) тетрацианоэтилен и др. )
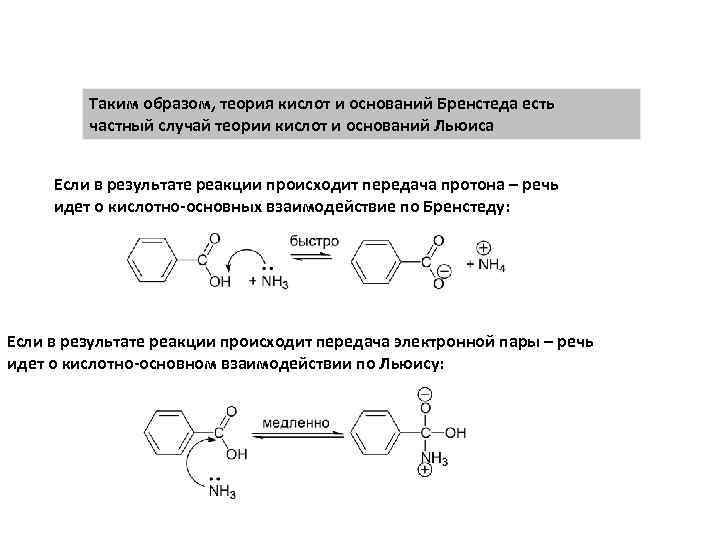 Таким образом, теория кислот и оснований Бренстеда есть частный случай теории кислот и оснований Льюиса Если в результате реакции происходит передача протона – речь идет о кислотно-основных взаимодействие по Бренстеду: Если в результате реакции происходит передача электронной пары – речь идет о кислотно-основном взаимодействии по Льюису:
Таким образом, теория кислот и оснований Бренстеда есть частный случай теории кислот и оснований Льюиса Если в результате реакции происходит передача протона – речь идет о кислотно-основных взаимодействие по Бренстеду: Если в результате реакции происходит передача электронной пары – речь идет о кислотно-основном взаимодействии по Льюису:
 Легкость протекания кислотно основной реакции определяется силой кислоты и основания, а также жесткостью или мягкостью кислоты и основания. Представление о жестких и мягких кислотах и основаниях (ЖМКО), введенное Р. Пирсоном, по существу является дальнейшим развитием теории Льюиса. Согласно концепции Пирсона кислоты и основания Льюиса делятся на жесткие и мягкие. К жестким кислотам относят кислоты Льюиса, в которых атомы акцепторы имеют малый объем и несут высокий положительный заряд, а следовательно, обладают высокой электроотрицательностью и низкой поляризуемостью (Н+, Li+, Na+, K+, Mg 2+, Ca 2+, Mn 2+, Al+3, Fe+3, Al. Cl 3, R—C+ =0). Нижняя свободная молекулярная орбиталь (НСМО) в жестких кислотах имеет низкую энергию. К мягкиv кислотам относятся кислоты Льюиса, в которых атомы акцепторы имеют большой объем и несут низкий положительный заряд, а поэтому обладают низкой электроотрицательностью и высокой поляризуемостью (Cu+, Ag+ , Hg 2+, Pt 2+, J 2, Br 9 и др. ). НСМО в мягких кислотах имеет высокую энергию.
Легкость протекания кислотно основной реакции определяется силой кислоты и основания, а также жесткостью или мягкостью кислоты и основания. Представление о жестких и мягких кислотах и основаниях (ЖМКО), введенное Р. Пирсоном, по существу является дальнейшим развитием теории Льюиса. Согласно концепции Пирсона кислоты и основания Льюиса делятся на жесткие и мягкие. К жестким кислотам относят кислоты Льюиса, в которых атомы акцепторы имеют малый объем и несут высокий положительный заряд, а следовательно, обладают высокой электроотрицательностью и низкой поляризуемостью (Н+, Li+, Na+, K+, Mg 2+, Ca 2+, Mn 2+, Al+3, Fe+3, Al. Cl 3, R—C+ =0). Нижняя свободная молекулярная орбиталь (НСМО) в жестких кислотах имеет низкую энергию. К мягкиv кислотам относятся кислоты Льюиса, в которых атомы акцепторы имеют большой объем и несут низкий положительный заряд, а поэтому обладают низкой электроотрицательностью и высокой поляризуемостью (Cu+, Ag+ , Hg 2+, Pt 2+, J 2, Br 9 и др. ). НСМО в мягких кислотах имеет высокую энергию.
 К жестким основаниям относят основания Льюиса, в которых атомы доноры имеют высокую электроотрицательность и низкую поляризуемость (Н 20, ОН , F , CI , CH 3 COO , R—OH, R—О—R, NH 3, R—NH 2, H 2 N—NH 2, и др. ). Верхняя занятая молекулярная орбиталь (ВЗМО) в жестких основаниях обладает низкой энергией. К мягким основаниям относят основания Льюиса, в которых атомы доноры имеют низкую электроотрицательность и высокую поляризуемость (RSH, RS , R—S—R, HS , CN , R—CN, С 2 Н 4, С 6 Н 6 , Н , R и др. ), ВЗМО в мягких основаниях обладает высокой энергией. Исходя из общего положения о том, что более эффективно протекает взаи модействие между орбиталями с близкими энергиями, жесткие кислоты преимущественно реагируют с жесткими основаниями, а мягкие кислоты — с мягкими основаниями (принцип ЖМКО). Следует отметить, что понятия «жесткие» и «мягкие» кислоты и основания не связаны с понятиями «сильные» и «слабые» кислоты и основания. Так, мягкое основание Н- и жесткое "— С 2 Н 50_ — являются сильными, а мягкое основание HS и жесткое СН СОО слабыми основаниями.
К жестким основаниям относят основания Льюиса, в которых атомы доноры имеют высокую электроотрицательность и низкую поляризуемость (Н 20, ОН , F , CI , CH 3 COO , R—OH, R—О—R, NH 3, R—NH 2, H 2 N—NH 2, и др. ). Верхняя занятая молекулярная орбиталь (ВЗМО) в жестких основаниях обладает низкой энергией. К мягким основаниям относят основания Льюиса, в которых атомы доноры имеют низкую электроотрицательность и высокую поляризуемость (RSH, RS , R—S—R, HS , CN , R—CN, С 2 Н 4, С 6 Н 6 , Н , R и др. ), ВЗМО в мягких основаниях обладает высокой энергией. Исходя из общего положения о том, что более эффективно протекает взаи модействие между орбиталями с близкими энергиями, жесткие кислоты преимущественно реагируют с жесткими основаниями, а мягкие кислоты — с мягкими основаниями (принцип ЖМКО). Следует отметить, что понятия «жесткие» и «мягкие» кислоты и основания не связаны с понятиями «сильные» и «слабые» кислоты и основания. Так, мягкое основание Н- и жесткое "— С 2 Н 50_ — являются сильными, а мягкое основание HS и жесткое СН СОО слабыми основаниями.
 Концепция Пирсона Химические соединения Кислоты Льюиса жесткое мягкое Основания Льюиса жесткое мягкое
Концепция Пирсона Химические соединения Кислоты Льюиса жесткое мягкое Основания Льюиса жесткое мягкое
 Концепция Пирсона Жесткие кислоты более легко и с образованием более прочных связей реагируют с жесткими основаниями, а мягкие кислоты с мягкими основаниями
Концепция Пирсона Жесткие кислоты более легко и с образованием более прочных связей реагируют с жесткими основаниями, а мягкие кислоты с мягкими основаниями
 Жесткие кислоты Жесткие основания -низкая поляризуемость -малый объем -высокое сродство к (e) -высокий потенциал Ip -высокая НВМО -низкая ВЗМО -большой (+) заряд -малый (-) заряд
Жесткие кислоты Жесткие основания -низкая поляризуемость -малый объем -высокое сродство к (e) -высокий потенциал Ip -высокая НВМО -низкая ВЗМО -большой (+) заряд -малый (-) заряд
 Мягкие кислоты -высокая поляризуемость -большой объем -низкая НВМО -малое сродство к (е) -малый (+) заряд Мягкие основания -высокая поляризуемость -большой объем -высокая ВЗМО -малый IP -большой (-)заряд Поляризуемость мягких кислот и оснований: в большом атоме (или ионе с малым эффективным зарядом ядра) относительно легко «искажается» электронное облако (частица поляризуется)
Мягкие кислоты -высокая поляризуемость -большой объем -низкая НВМО -малое сродство к (е) -малый (+) заряд Мягкие основания -высокая поляризуемость -большой объем -высокая ВЗМО -малый IP -большой (-)заряд Поляризуемость мягких кислот и оснований: в большом атоме (или ионе с малым эффективным зарядом ядра) относительно легко «искажается» электронное облако (частица поляризуется)
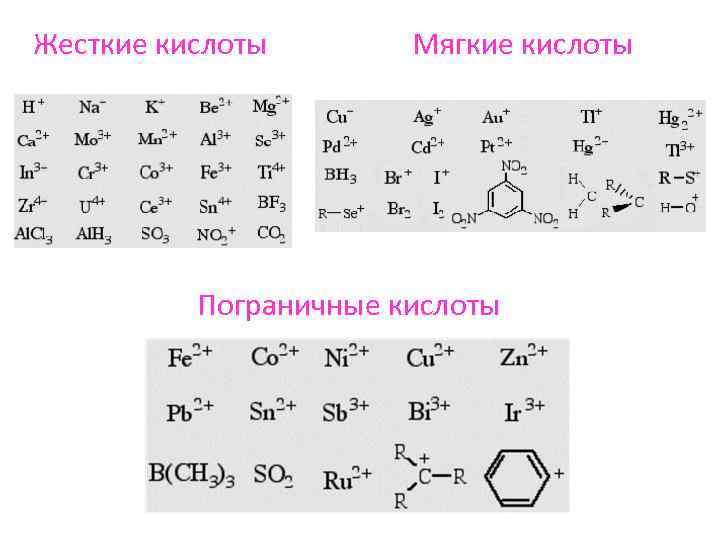 Жесткие кислоты Мягкие кислоты Пограничные кислоты
Жесткие кислоты Мягкие кислоты Пограничные кислоты
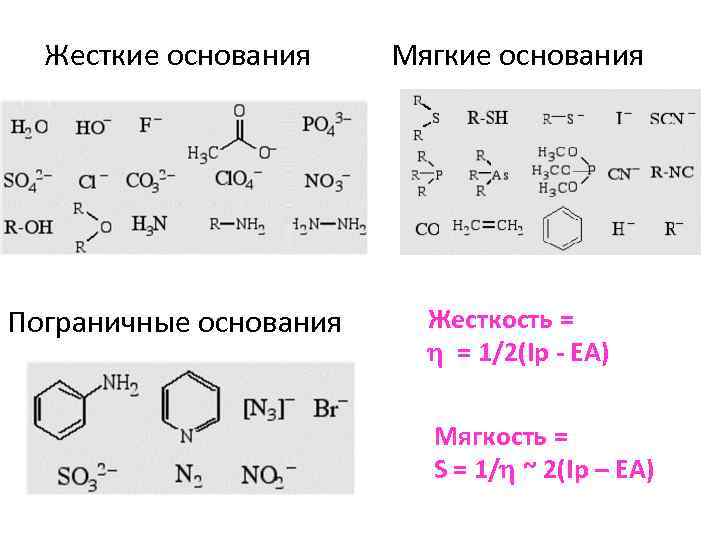 Жесткие основания Мягкие основания Пограничные основания Жесткость = h = 1/2(Ip - EA) Мягкость = S = 1/h ~ 2(Ip – EA)
Жесткие основания Мягкие основания Пограничные основания Жесткость = h = 1/2(Ip - EA) Мягкость = S = 1/h ~ 2(Ip – EA)
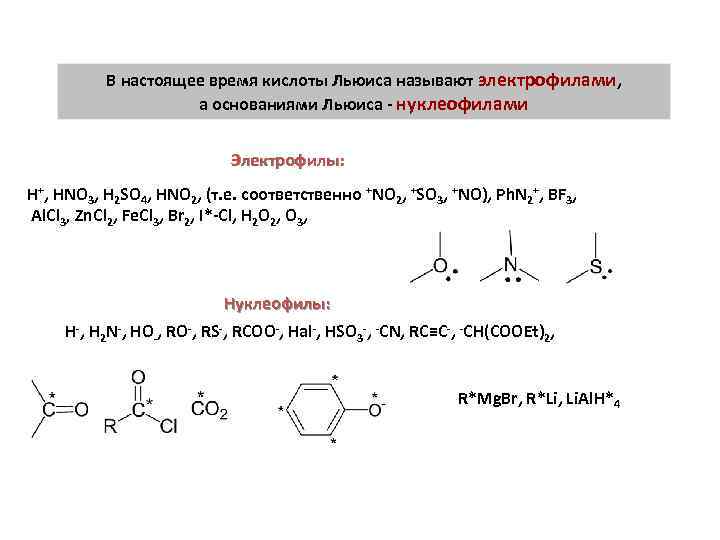 В настоящее время кислоты Льюиса называют электрофилами, а основаниями Льюиса - нуклеофилами Электрофилы: H+, HNO 3, H 2 SO 4, HNO 2, (т. е. соответственно +NO 2, +SO 3, +NO), Ph. N 2+, BF 3, Al. Cl 3, Zn. Cl 2, Fe. Cl 3, Br 2, I*-Cl, H 2 O 2, O 3, Нуклеофилы: H-, H 2 N-, HO-, RS-, RCOO-, Hal-, HSO 3 -, -CN, RC≡C-, -CH(COOEt)2, R*Mg. Br, R*Li, Li. Al. H*4
В настоящее время кислоты Льюиса называют электрофилами, а основаниями Льюиса - нуклеофилами Электрофилы: H+, HNO 3, H 2 SO 4, HNO 2, (т. е. соответственно +NO 2, +SO 3, +NO), Ph. N 2+, BF 3, Al. Cl 3, Zn. Cl 2, Fe. Cl 3, Br 2, I*-Cl, H 2 O 2, O 3, Нуклеофилы: H-, H 2 N-, HO-, RS-, RCOO-, Hal-, HSO 3 -, -CN, RC≡C-, -CH(COOEt)2, R*Mg. Br, R*Li, Li. Al. H*4


