4622_2011.ppt
- Количество слайдов: 50
 Кафедра ТИ-6 «Материаловедение и технологии материалов и покрытий» т. 268 -00 -32 ti 6@mgupi. edu 4622 Материаловедение Терновых Александр Михайлович ternovam 3@ya. ru
Кафедра ТИ-6 «Материаловедение и технологии материалов и покрытий» т. 268 -00 -32 ti 6@mgupi. edu 4622 Материаловедение Терновых Александр Михайлович ternovam 3@ya. ru
 Тема 1. ТЕХНИЧЕСКИЕ ПАРАМЕТРЫ МАТЕРИАЛОВ 1. ОБЪЕМНО-СТРУКТУРНЫЕ ПАРАМЕТРЫ. 1. 1. Плотность-d. Универсальный параметр. d = m/V [кг/м 3], где m - масса; V – объем тела. Поскольку объем материала зависит от температуры, то и плотность является функцией температуры. Чаще всего плотность измеряют при комнатной температуре, т. е. при 250 С или 298 К. Если же она измерена при другой температуре, то это указывается так: d 350. “ 350” – это температура в Кельвинах 1. 2. Компонентный состав. Универсальный параметр Компонентный состав определяет количество различных химических элементов и соединений, содержащихся в материале. • химические элементы: Al, Fe, Cu, Si, Ge и др. • химические соединения: Si. C, Fe 3 C, Al 2 O 3 и др. • растворы: Gax. In 1 -x. As, Ga. Sby. As 1 -y и др. 2
Тема 1. ТЕХНИЧЕСКИЕ ПАРАМЕТРЫ МАТЕРИАЛОВ 1. ОБЪЕМНО-СТРУКТУРНЫЕ ПАРАМЕТРЫ. 1. 1. Плотность-d. Универсальный параметр. d = m/V [кг/м 3], где m - масса; V – объем тела. Поскольку объем материала зависит от температуры, то и плотность является функцией температуры. Чаще всего плотность измеряют при комнатной температуре, т. е. при 250 С или 298 К. Если же она измерена при другой температуре, то это указывается так: d 350. “ 350” – это температура в Кельвинах 1. 2. Компонентный состав. Универсальный параметр Компонентный состав определяет количество различных химических элементов и соединений, содержащихся в материале. • химические элементы: Al, Fe, Cu, Si, Ge и др. • химические соединения: Si. C, Fe 3 C, Al 2 O 3 и др. • растворы: Gax. In 1 -x. As, Ga. Sby. As 1 -y и др. 2
 1. 3. Фазовый состав. Специальный параметр для гетерогенных материалов. Фазой называется однородная часть вещества, отделенная от других поверхностью раздела, при переходе через которую скачкообразно изменяются свойства материала. Непрерывная фаза называется дисперсионной средой или матрицей, а дискретная (распределенная) фаза, называется дисперсной фазой. Материал, состоящий из нескольких фаз, называется гетерогенным или композиционным, из одной - гомогенным. Количество дисперсной фазы выражается через ее объемную долю в материале j: j = V д / V , где Vд -объем дисперсной фазы, V - общий объем материала. Схема двухфазной системы 1 -дисперсионная среда 2 -дисперсная фаза Диаграмма фазового состояния. 1. 4. Постоянная решетки–а [нм]. Специальный параметр для кристаллических материалов. Этот параметр определяет период идентичности (повторяемости) 3 кристаллической решетки.
1. 3. Фазовый состав. Специальный параметр для гетерогенных материалов. Фазой называется однородная часть вещества, отделенная от других поверхностью раздела, при переходе через которую скачкообразно изменяются свойства материала. Непрерывная фаза называется дисперсионной средой или матрицей, а дискретная (распределенная) фаза, называется дисперсной фазой. Материал, состоящий из нескольких фаз, называется гетерогенным или композиционным, из одной - гомогенным. Количество дисперсной фазы выражается через ее объемную долю в материале j: j = V д / V , где Vд -объем дисперсной фазы, V - общий объем материала. Схема двухфазной системы 1 -дисперсионная среда 2 -дисперсная фаза Диаграмма фазового состояния. 1. 4. Постоянная решетки–а [нм]. Специальный параметр для кристаллических материалов. Этот параметр определяет период идентичности (повторяемости) 3 кристаллической решетки.
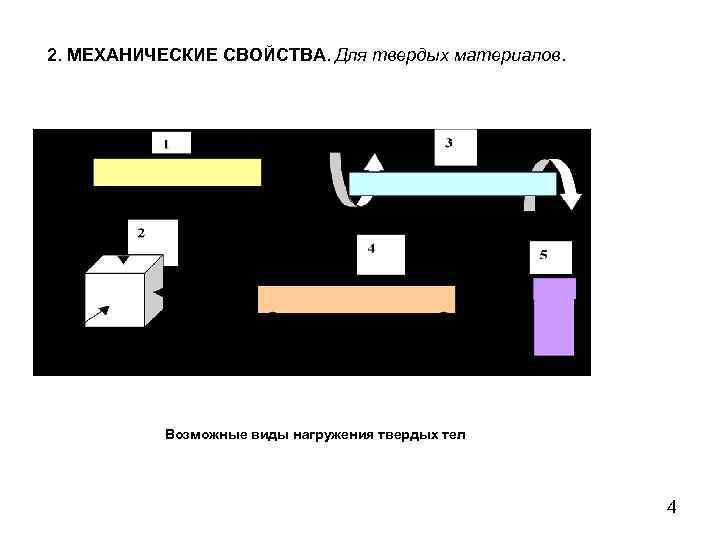 2. МЕХАНИЧЕСКИЕ СВОЙСТВА. Для твердых материалов. Возможные виды нагружения твердых тел 4
2. МЕХАНИЧЕСКИЕ СВОЙСТВА. Для твердых материалов. Возможные виды нагружения твердых тел 4
 2. 1. Прочность 2. 1. 1. Кратковременная прочность при растяжении F-растягивающее усилие, S- площадь поперечного сечения образца, l 0 - длина образца при F=0, l - длина образца при F>0, l=l l 0 -абсолютная деформация (удлинение), l/l 0= - относительная деформация, F/S= - растягивающее напряжение [Па]. п - предел пропорциональности. 0, 2 - условный предел текучести. т- предел текучести. p- разрушающее напряжение. . р- относительное удлинение при разрыве. Кривая прочности при растяжении 5
2. 1. Прочность 2. 1. 1. Кратковременная прочность при растяжении F-растягивающее усилие, S- площадь поперечного сечения образца, l 0 - длина образца при F=0, l - длина образца при F>0, l=l l 0 -абсолютная деформация (удлинение), l/l 0= - относительная деформация, F/S= - растягивающее напряжение [Па]. п - предел пропорциональности. 0, 2 - условный предел текучести. т- предел текучести. p- разрушающее напряжение. . р- относительное удлинение при разрыве. Кривая прочности при растяжении 5
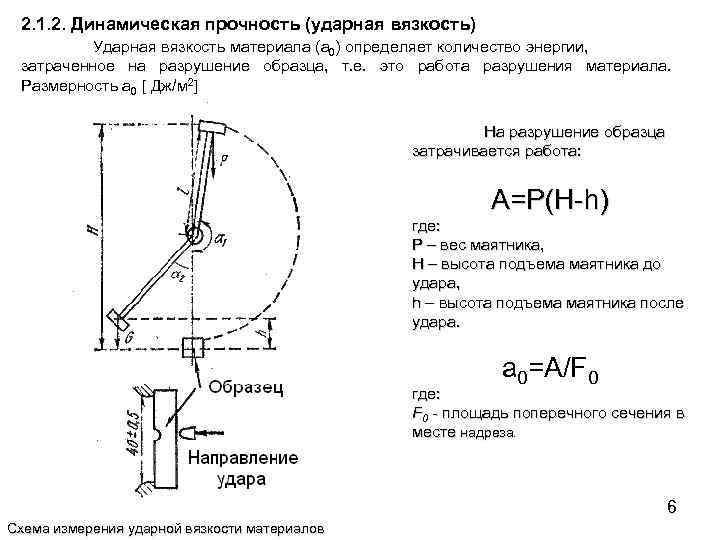 2. 1. 2. Динамическая прочность (ударная вязкость) Ударная вязкость материала (а 0) определяет количество энергии, затраченное на разрушение образца, т. е. это работа разрушения материала. Размерность а 0 [ Дж/м 2] На разрушение образца затрачивается работа: A=P(H-h) где: Р – вес маятника, Н – высота подъема маятника до удара, h – высота подъема маятника после удара. а 0=A/F 0 где: F 0 - площадь поперечного сечения в месте надреза. 6 Схема измерения ударной вязкости материалов
2. 1. 2. Динамическая прочность (ударная вязкость) Ударная вязкость материала (а 0) определяет количество энергии, затраченное на разрушение образца, т. е. это работа разрушения материала. Размерность а 0 [ Дж/м 2] На разрушение образца затрачивается работа: A=P(H-h) где: Р – вес маятника, Н – высота подъема маятника до удара, h – высота подъема маятника после удара. а 0=A/F 0 где: F 0 - площадь поперечного сечения в месте надреза. 6 Схема измерения ударной вязкости материалов
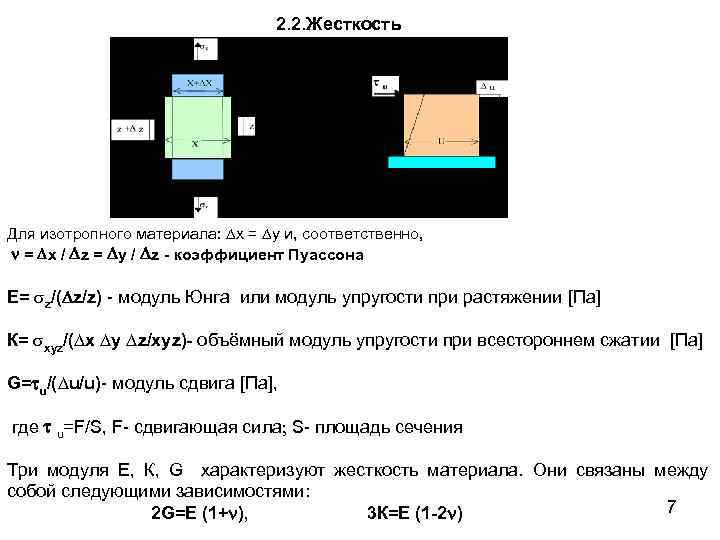 2. 2. Жесткость Для изотропного материала: x = y и, соответственно, = x / z = y / z - коэффициент Пуассона E= z/( z/z) - модуль Юнга или модуль упругости при растяжении [Па] К= xyz/( x y z/xyz)- объёмный модуль упругости при всестороннем сжатии [Па] G= u/( u/u)- модуль сдвига [Па], где u=F/S, F- сдвигающая сила; S- площадь сечения Три модуля Е, К, G характеризуют жесткость материала. Они связаны между собой следующими зависимостями: 7 2 G=E (1+ ), 3 К=E (1 -2 )
2. 2. Жесткость Для изотропного материала: x = y и, соответственно, = x / z = y / z - коэффициент Пуассона E= z/( z/z) - модуль Юнга или модуль упругости при растяжении [Па] К= xyz/( x y z/xyz)- объёмный модуль упругости при всестороннем сжатии [Па] G= u/( u/u)- модуль сдвига [Па], где u=F/S, F- сдвигающая сила; S- площадь сечения Три модуля Е, К, G характеризуют жесткость материала. Они связаны между собой следующими зависимостями: 7 2 G=E (1+ ), 3 К=E (1 -2 )
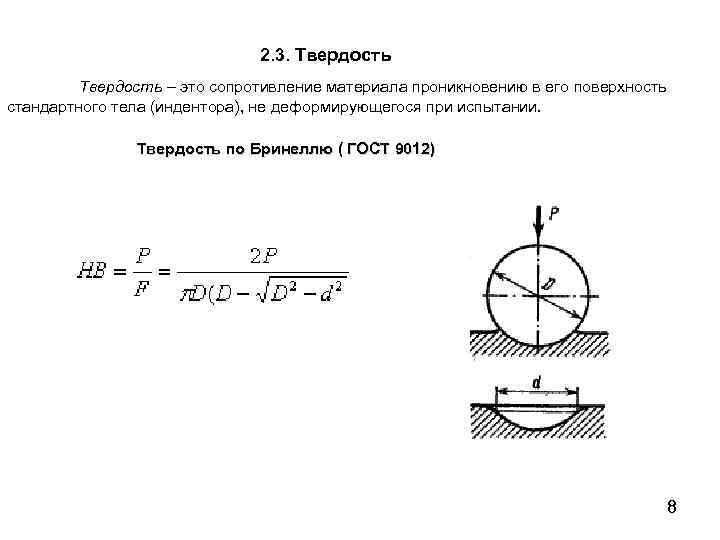 2. 3. Твердость – это сопротивление материала проникновению в его поверхность стандартного тела (индентора), не деформирующегося при испытании. Твердость по Бринеллю ( ГОСТ 9012) 8
2. 3. Твердость – это сопротивление материала проникновению в его поверхность стандартного тела (индентора), не деформирующегося при испытании. Твердость по Бринеллю ( ГОСТ 9012) 8
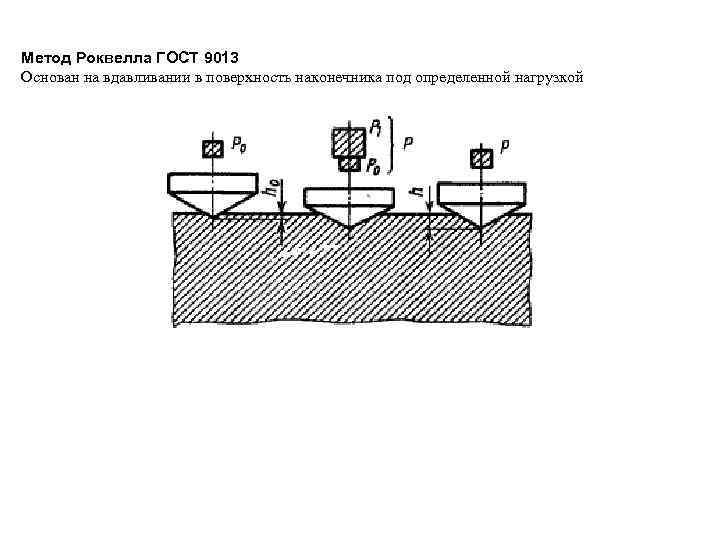 Метод Роквелла ГОСТ 9013 Основан на вдавливании в поверхность наконечника под определенной нагрузкой
Метод Роквелла ГОСТ 9013 Основан на вдавливании в поверхность наконечника под определенной нагрузкой
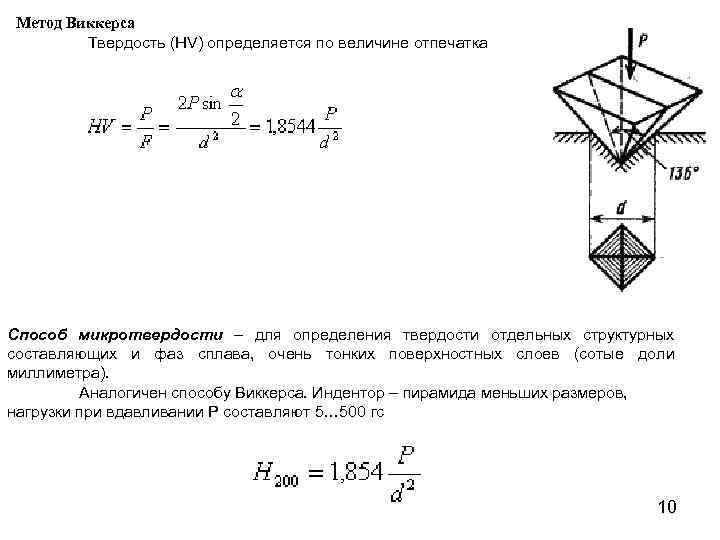 Метод Виккерса Твердость (HV) определяется по величине отпечатка Способ микротвердости – для определения твердости отдельных структурных составляющих и фаз сплава, очень тонких поверхностных слоев (сотые доли миллиметра). Аналогичен способу Виккерса. Индентор – пирамида меньших размеров, нагрузки при вдавливании Р составляют 5… 500 гс 10
Метод Виккерса Твердость (HV) определяется по величине отпечатка Способ микротвердости – для определения твердости отдельных структурных составляющих и фаз сплава, очень тонких поверхностных слоев (сотые доли миллиметра). Аналогичен способу Виккерса. Индентор – пирамида меньших размеров, нагрузки при вдавливании Р составляют 5… 500 гс 10
 2. 4. Трибологическе параметры. Специальные параметры для твердых материалов. (Трибология - это наука о физических эффектах, возникающих при трении материалов. ) 2. 4. 1. Коэффициент трения – f = F/N, где F -сила трения, N -нормальная нагрузка Материалы с большим f азывают фрикционными. Материалы с низким f называют антифрикционными. 2. 4. 2. Интенсивность износа ( истирания ) – J = h/l, где h - толщина унесенного слоя, l - путь трения 2. 5. Адгезионные параметры. Универсальный параметр 2. 5. 1. Работа рассчитывается. сил адгезии Wa [Дж/м 2]- 2. 5. 2. Адгезионная прочность А – измеряется. Существует несколько схем измерения адгезионной прочности. Они показаны на рис. 1. 6 и 1. 7. 2. 5. 3. Характер разрушения адгезионного соединения При нарушении целостности адгезионного соединения различают разрушение адгезионное, когда плоскость разрушения совпадает с плоскостью контакта двух тел, и когезионное, когда разрушение происходит по какому-то одному материалу (рис. 1. 8). Рис. 1. 6. Схемы измерения адгезионной прочности. 1 - нормальный отрыв 2 сдвиг 3 - кручение A=F/S[H/м 2], где F- разрушающая сила S- площадь адгезионной связи Рис. 1. 7. Схема измерения усилия отслаивания А=F/h [H/м], где F- сила отслаивания, h-ширина полоски отслаиваемой пленки. Рис. 1. 8. Схемы разрушения адгезионного соединения 11
2. 4. Трибологическе параметры. Специальные параметры для твердых материалов. (Трибология - это наука о физических эффектах, возникающих при трении материалов. ) 2. 4. 1. Коэффициент трения – f = F/N, где F -сила трения, N -нормальная нагрузка Материалы с большим f азывают фрикционными. Материалы с низким f называют антифрикционными. 2. 4. 2. Интенсивность износа ( истирания ) – J = h/l, где h - толщина унесенного слоя, l - путь трения 2. 5. Адгезионные параметры. Универсальный параметр 2. 5. 1. Работа рассчитывается. сил адгезии Wa [Дж/м 2]- 2. 5. 2. Адгезионная прочность А – измеряется. Существует несколько схем измерения адгезионной прочности. Они показаны на рис. 1. 6 и 1. 7. 2. 5. 3. Характер разрушения адгезионного соединения При нарушении целостности адгезионного соединения различают разрушение адгезионное, когда плоскость разрушения совпадает с плоскостью контакта двух тел, и когезионное, когда разрушение происходит по какому-то одному материалу (рис. 1. 8). Рис. 1. 6. Схемы измерения адгезионной прочности. 1 - нормальный отрыв 2 сдвиг 3 - кручение A=F/S[H/м 2], где F- разрушающая сила S- площадь адгезионной связи Рис. 1. 7. Схема измерения усилия отслаивания А=F/h [H/м], где F- сила отслаивания, h-ширина полоски отслаиваемой пленки. Рис. 1. 8. Схемы разрушения адгезионного соединения 11
 3. ТЕПЛОФИЗИЧЕСКИЕ СВОЙСТВА 3. 1. Термическое расширение Универсальный параметр al - коэффициент линейного термического расширения Если при температуре Т 1 длина тела - l 1, а при T 2 - l 2 , то l= l 2 - l 1, T=T 2 -T 1 -1 al = l/(l 1 T) [К ] av- коэффициент объемного термического расширения: av = V/(V 1 T) [К-1] Для изотропных тел: av=3 al 3. 2. Теплоемкость Универсальный параметр Теплоёмкость (С) - характеризует количество теплоты , которое необходимо подвести к материалу для увеличения его температуры на один градус. [Дж/град], где Сp- изобарная теплоёмкость (при постоянном давлении ), Сv- изохорная теплоёмкость (при постоянном объеме), H- энтальпия или теплосодержание, U- внутренняя энергия. На практике чаще используют удельную теплоёмкость, т. е. теплоёмкости единицы массы материалов: cp= Cp /m; cv= Cv/m [Дж/кг гр] 12
3. ТЕПЛОФИЗИЧЕСКИЕ СВОЙСТВА 3. 1. Термическое расширение Универсальный параметр al - коэффициент линейного термического расширения Если при температуре Т 1 длина тела - l 1, а при T 2 - l 2 , то l= l 2 - l 1, T=T 2 -T 1 -1 al = l/(l 1 T) [К ] av- коэффициент объемного термического расширения: av = V/(V 1 T) [К-1] Для изотропных тел: av=3 al 3. 2. Теплоемкость Универсальный параметр Теплоёмкость (С) - характеризует количество теплоты , которое необходимо подвести к материалу для увеличения его температуры на один градус. [Дж/град], где Сp- изобарная теплоёмкость (при постоянном давлении ), Сv- изохорная теплоёмкость (при постоянном объеме), H- энтальпия или теплосодержание, U- внутренняя энергия. На практике чаще используют удельную теплоёмкость, т. е. теплоёмкости единицы массы материалов: cp= Cp /m; cv= Cv/m [Дж/кг гр] 12
![3. 3. Теплопроводность- λ [Вт/м×К] Универсальный параметр Теплопроводность характеризует скорость распространения тепловой энергии в 3. 3. Теплопроводность- λ [Вт/м×К] Универсальный параметр Теплопроводность характеризует скорость распространения тепловой энергии в](https://present5.com/presentation/67943771_131485604/image-13.jpg) 3. 3. Теплопроводность- λ [Вт/м×К] Универсальный параметр Теплопроводность характеризует скорость распространения тепловой энергии в материале. Q= - λ×grad T, где Q - тепловой поток, T - температура, grad T- распределение температуры, l - коэффициент теплопроводности 3. 4. Температурапроводность - а [м 2/c] Универсальный параметр Температурапроводность характеризует скорость распространения температуры при стационарном тепловом потоке. a = λ /(cp×d) 3. 5. Теплостойкость материала Универсальный параметр При нагревании материала в нем происходят определенные изменения. Если температура такова, что изделия из данного материала становятся неработоспособными, то значит теплостойкость материала не превышает данной температуры. Теплостойкостью называют способность материалов сохранять свои функциональные параметры при повышенных температурах. Измеряется в градусах по Цельсию. 3. 6. Температура фазовых переходов Это температура, при которой в материале происходят структурные изменения, приводящие к переходу его в другое фазовое состояние. Примерами таких температур могут служить: Тпл- температура плавления, Тс- температура стеклования, Тк- температура Кюри для магнитных материалов. Измеряется в [K] или [0 C]. Соотношение температурных шкал по Кельвину и Цельсию выражается уравнением: ТК=Т 0 С+273. 13
3. 3. Теплопроводность- λ [Вт/м×К] Универсальный параметр Теплопроводность характеризует скорость распространения тепловой энергии в материале. Q= - λ×grad T, где Q - тепловой поток, T - температура, grad T- распределение температуры, l - коэффициент теплопроводности 3. 4. Температурапроводность - а [м 2/c] Универсальный параметр Температурапроводность характеризует скорость распространения температуры при стационарном тепловом потоке. a = λ /(cp×d) 3. 5. Теплостойкость материала Универсальный параметр При нагревании материала в нем происходят определенные изменения. Если температура такова, что изделия из данного материала становятся неработоспособными, то значит теплостойкость материала не превышает данной температуры. Теплостойкостью называют способность материалов сохранять свои функциональные параметры при повышенных температурах. Измеряется в градусах по Цельсию. 3. 6. Температура фазовых переходов Это температура, при которой в материале происходят структурные изменения, приводящие к переходу его в другое фазовое состояние. Примерами таких температур могут служить: Тпл- температура плавления, Тс- температура стеклования, Тк- температура Кюри для магнитных материалов. Измеряется в [K] или [0 C]. Соотношение температурных шкал по Кельвину и Цельсию выражается уравнением: ТК=Т 0 С+273. 13
![4. ЭЛЕКТРИЧЕСКИЕ СВОЙСТВА 4. 1. Удельное объёмное электрическое сопротивление - r [Oм×м] Универсальный параметр 4. ЭЛЕКТРИЧЕСКИЕ СВОЙСТВА 4. 1. Удельное объёмное электрическое сопротивление - r [Oм×м] Универсальный параметр](https://present5.com/presentation/67943771_131485604/image-14.jpg) 4. ЭЛЕКТРИЧЕСКИЕ СВОЙСТВА 4. 1. Удельное объёмное электрическое сопротивление - r [Oм×м] Универсальный параметр U = R×I, где R- сопротивление материалов [Oм], U - напряжение, I - сила тока r = RS/l, где S - площадь поперечного сечения, l - длина. r может изменяться в пределах от 10 -8 до 1016 Ом×м. 4. 2. Температурный коэффициент электрического сопротивления: ar [Oм×м/К] Универсальный параметр ar = r / T ar > 0 - для проводников ar < 0 - для полупроводников 4. 3. Диэлектрическая проницаемость - . Специальный параметр для диэлектриков = Cм/C 0 , где Cм - ёмкость конденсатора , в котором между обкладками находится материал, С 0 - ёмкость конденсатора , в котором между обкладками находится вакуум. 4. 4. Тангенс угла диэлектрических потерь tg. Специальный параметр для диэлектриков Характеризует ту часть энергии переменного электрического поля, которая рассеивается в диэлектрике в виде тепла. 4. 5. Электрическая прочность - Епр. [МВ/м] Специальный параметр для диэлектриков Электрическая прочность - это та минимальная напряженность электрического поля, при котором происходит нарушение работы диэлектрика пробой. Епр= Uпр/ h , где h- толщина (расстояние между электродами), Uпр- напряжение пробоя 14
4. ЭЛЕКТРИЧЕСКИЕ СВОЙСТВА 4. 1. Удельное объёмное электрическое сопротивление - r [Oм×м] Универсальный параметр U = R×I, где R- сопротивление материалов [Oм], U - напряжение, I - сила тока r = RS/l, где S - площадь поперечного сечения, l - длина. r может изменяться в пределах от 10 -8 до 1016 Ом×м. 4. 2. Температурный коэффициент электрического сопротивления: ar [Oм×м/К] Универсальный параметр ar = r / T ar > 0 - для проводников ar < 0 - для полупроводников 4. 3. Диэлектрическая проницаемость - . Специальный параметр для диэлектриков = Cм/C 0 , где Cм - ёмкость конденсатора , в котором между обкладками находится материал, С 0 - ёмкость конденсатора , в котором между обкладками находится вакуум. 4. 4. Тангенс угла диэлектрических потерь tg. Специальный параметр для диэлектриков Характеризует ту часть энергии переменного электрического поля, которая рассеивается в диэлектрике в виде тепла. 4. 5. Электрическая прочность - Епр. [МВ/м] Специальный параметр для диэлектриков Электрическая прочность - это та минимальная напряженность электрического поля, при котором происходит нарушение работы диэлектрика пробой. Епр= Uпр/ h , где h- толщина (расстояние между электродами), Uпр- напряжение пробоя 14
![5. МАГНИТНЫЕ СВОЙСТВА 5. 1. Намагниченность - Jm. [A/м] Универсальный параметр Jm=M/V, где М-магнитный 5. МАГНИТНЫЕ СВОЙСТВА 5. 1. Намагниченность - Jm. [A/м] Универсальный параметр Jm=M/V, где М-магнитный](https://present5.com/presentation/67943771_131485604/image-15.jpg) 5. МАГНИТНЫЕ СВОЙСТВА 5. 1. Намагниченность - Jm. [A/м] Универсальный параметр Jm=M/V, где М-магнитный момент единицы объема V материала. 5. 2. Магнитная восприимчивость - km. Универсальный параметр km= Jm/H, где Н - напряженность магнитного поля [А/м]. 5. 3. Магнитная проницаемость-. Универсальный параметр Рис. 1. 9. Петля магнитного гистерезиса =В/( 0 Н), где В-магнитная индукция [Тл], Н-напряженность магнитного поля [А/м], 0 -магнитная постоянная или проницаемость вакуума, равная 4 10 -7 Гн/м. 5. 4. Индукция насыщения-Bs. [Тл] Специальный параметр для магнетиков. Индукция насыщения -это максимальная индукция при намагничивании материала. 5. 5. Остаточная индукция-Br. [Тл] Специальный параметр для магнетиков Остаточная индукция- это та индукция, которая остаётся в материале после снятия внешнего магнитного поля (Рис. 1. 9). 5. 6. Коэрцитивная сила-Hc [A/м] Специальный параметр для магнетиков Коэрцитивная сила - это та напряженность магнитного поля, при которой магнитная индукция в материале исчезает, т. е. Н при B = 0. 15
5. МАГНИТНЫЕ СВОЙСТВА 5. 1. Намагниченность - Jm. [A/м] Универсальный параметр Jm=M/V, где М-магнитный момент единицы объема V материала. 5. 2. Магнитная восприимчивость - km. Универсальный параметр km= Jm/H, где Н - напряженность магнитного поля [А/м]. 5. 3. Магнитная проницаемость-. Универсальный параметр Рис. 1. 9. Петля магнитного гистерезиса =В/( 0 Н), где В-магнитная индукция [Тл], Н-напряженность магнитного поля [А/м], 0 -магнитная постоянная или проницаемость вакуума, равная 4 10 -7 Гн/м. 5. 4. Индукция насыщения-Bs. [Тл] Специальный параметр для магнетиков. Индукция насыщения -это максимальная индукция при намагничивании материала. 5. 5. Остаточная индукция-Br. [Тл] Специальный параметр для магнетиков Остаточная индукция- это та индукция, которая остаётся в материале после снятия внешнего магнитного поля (Рис. 1. 9). 5. 6. Коэрцитивная сила-Hc [A/м] Специальный параметр для магнетиков Коэрцитивная сила - это та напряженность магнитного поля, при которой магнитная индукция в материале исчезает, т. е. Н при B = 0. 15
 6. ХИМИЧЕСКАЯ СТОЙКОСТЬ Универсальный параметр Химической стойкостью называется способность материала противостоять воздействию химически-активных сред. Химически-активными средами являются кислоты, щелочи, их водные растворы, окислители и т. д. Кислотность или щелочность водных растворов характеризуют с помощью так называемого водородного показателя p. H, который отражает активность ионов водорода в данной среде. Диапазон изменения p. H: от 0 до 14. Если p. H =7, то это нейтральная среда (т. е. дистиллированная вода), если p. H 7 -кислая среда, если p. H 7 -щелочная среда. Как правило, чем больше p. H отличается от 7, тем жидкость химически более активна. Химическая стойкость - это комплексный и, в основном, качественный параметр, определяющий возможность нормального функционирования изделий в контакте с агрессивной средой. 7. ГОРЮЧЕСТЬ МАТЕРИАЛОВ. Специальный параметр для органических материалов. Горючесть - это комплексная характеристика материала, включающая следующее: способность к воспламенению или самовоспламенению; скорость горения или распостранения пламени; параметры, определяющие условия, при которых возможен самоподдерживающийся процесс горения. Одной из характеристик горючести является показатель горючести - К, равный отношению количества теплоты, выделившейся при горении материала, к количеству тепла, необходимому для его поддержания. По этому показателю все материалы подразделяются на: негорючие (К 0, 1) трудногорючие (0, 1 К 0, 5) горючие (К 0, 5) 16
6. ХИМИЧЕСКАЯ СТОЙКОСТЬ Универсальный параметр Химической стойкостью называется способность материала противостоять воздействию химически-активных сред. Химически-активными средами являются кислоты, щелочи, их водные растворы, окислители и т. д. Кислотность или щелочность водных растворов характеризуют с помощью так называемого водородного показателя p. H, который отражает активность ионов водорода в данной среде. Диапазон изменения p. H: от 0 до 14. Если p. H =7, то это нейтральная среда (т. е. дистиллированная вода), если p. H 7 -кислая среда, если p. H 7 -щелочная среда. Как правило, чем больше p. H отличается от 7, тем жидкость химически более активна. Химическая стойкость - это комплексный и, в основном, качественный параметр, определяющий возможность нормального функционирования изделий в контакте с агрессивной средой. 7. ГОРЮЧЕСТЬ МАТЕРИАЛОВ. Специальный параметр для органических материалов. Горючесть - это комплексная характеристика материала, включающая следующее: способность к воспламенению или самовоспламенению; скорость горения или распостранения пламени; параметры, определяющие условия, при которых возможен самоподдерживающийся процесс горения. Одной из характеристик горючести является показатель горючести - К, равный отношению количества теплоты, выделившейся при горении материала, к количеству тепла, необходимому для его поддержания. По этому показателю все материалы подразделяются на: негорючие (К 0, 1) трудногорючие (0, 1 К 0, 5) горючие (К 0, 5) 16
 8. ОПТИЧЕСКИЕ ПАРАМЕТРЫ. 8. 1. Цвет Универсальный параметр Это универсальный параметр, определяющий спектр волн поглощения и отражения поверхности мателиала при воздействии оптического излучения. 8. 2. Коэффициент преломления - n. Специальный параметр для оптически прозрачных тел. n. D 20 = sin α / sinβ , где sin α- угол падения лучей, sin β - угол преломления, D- полоса излучения атома Na, длина волны которого равна 582 нм, 20 - это температура измерения в 0 С. 8. 3. Коэффициент пропускания – j. Специальный параметр для оптически прозрачных тел. Коэффициент пропускания равен отношению интенсивности проходящего света, к интенсивности падающего света: j=Iпр/I 0. Если j = 0, то это - непрозрачный материал, если j = 1 - оптически прозрачный материал. 17
8. ОПТИЧЕСКИЕ ПАРАМЕТРЫ. 8. 1. Цвет Универсальный параметр Это универсальный параметр, определяющий спектр волн поглощения и отражения поверхности мателиала при воздействии оптического излучения. 8. 2. Коэффициент преломления - n. Специальный параметр для оптически прозрачных тел. n. D 20 = sin α / sinβ , где sin α- угол падения лучей, sin β - угол преломления, D- полоса излучения атома Na, длина волны которого равна 582 нм, 20 - это температура измерения в 0 С. 8. 3. Коэффициент пропускания – j. Специальный параметр для оптически прозрачных тел. Коэффициент пропускания равен отношению интенсивности проходящего света, к интенсивности падающего света: j=Iпр/I 0. Если j = 0, то это - непрозрачный материал, если j = 1 - оптически прозрачный материал. 17
 9. РЕОЛОГИЧЕСКИЕ ПАРАМЕТРЫ. Специальные материалов (Реология - это наука о течении). параметры для жидких 9. 1. Динамическая вязкость- [Па с]. Сила внутреннего трения между слоями жидкости F выражается уравнением Ньютона: F=S (d. V/dx), где S-поверхность трущихся слоев, (d. V/dx)-градиент скорости в направлении x, перпендикулярном напрвлению движения жидкости. 9. 2. Кинематическая вязкость- [м 2/с]. Иногда вместо динамической вязкости используют так называемую кинематическую вязкость под которой понимают отношение к плотности жидкости: = /d. 9. 3. Энергия активации вязкого течения- Е [к. Дж/моль]. Вязкость жидкости зависит от температуры. Температурная зависимость является экспоненциальной = 0 exp(E/RT), где Е-энергия активации вязкого течения, 0 -предэкспоненциальный множитель, R-универсальная газовая постоянная, равная 8, 31 Дж/(моль град), Tабсолютная температура, т. е. температура, выраженная в градусах Кельвина. 18
9. РЕОЛОГИЧЕСКИЕ ПАРАМЕТРЫ. Специальные материалов (Реология - это наука о течении). параметры для жидких 9. 1. Динамическая вязкость- [Па с]. Сила внутреннего трения между слоями жидкости F выражается уравнением Ньютона: F=S (d. V/dx), где S-поверхность трущихся слоев, (d. V/dx)-градиент скорости в направлении x, перпендикулярном напрвлению движения жидкости. 9. 2. Кинематическая вязкость- [м 2/с]. Иногда вместо динамической вязкости используют так называемую кинематическую вязкость под которой понимают отношение к плотности жидкости: = /d. 9. 3. Энергия активации вязкого течения- Е [к. Дж/моль]. Вязкость жидкости зависит от температуры. Температурная зависимость является экспоненциальной = 0 exp(E/RT), где Е-энергия активации вязкого течения, 0 -предэкспоненциальный множитель, R-универсальная газовая постоянная, равная 8, 31 Дж/(моль град), Tабсолютная температура, т. е. температура, выраженная в градусах Кельвина. 18
![10. ЭНЕРГЕТИЧЕСКИЕ ПАРАМЕТРЫ 10. 1. Работа выхода электрона -Ае [э. В] Специальный параметр для 10. ЭНЕРГЕТИЧЕСКИЕ ПАРАМЕТРЫ 10. 1. Работа выхода электрона -Ае [э. В] Специальный параметр для](https://present5.com/presentation/67943771_131485604/image-19.jpg) 10. ЭНЕРГЕТИЧЕСКИЕ ПАРАМЕТРЫ 10. 1. Работа выхода электрона -Ае [э. В] Специальный параметр для металлов. Это та энергия, которую необходимо подвести к материалу, чтобы удалить электроны на бесконечное расстояние от поверхности материала. Рис. 1. 10. Схема определения краевого угла смачивания. 10. 2. Ширина запрещенной зоны-Hg [э. В] Универсальный параметр Шириной запрещённой зоны называют ту энергию, которую необходимо подвести к материалу, чтобы создать в нём дополнительные носители заряды - электроны , дырки. Hg = 0 – проводники Hg <2 э. В – полупроводники Hg >2 э. В – диэлектрики 10. 3. Поверхностное натяжение - [H м]. Универсальный параметр. Характеризует энергию поверхностного слоя материала. 10. 4. Краевой угол смачивания-. Специальный параметр для твердых материалов. Краевой угол смачивания характеризует взаимодействие поверхности данного материала с каким - либо жидким веществом. [°] - в градусах. Если 0, то капля жидкости полностью растекается по поверхности , что говорит о хорошей смачиваемости данного материала. Если > π/2 - материал плохо смачивается данной жидкостью. 10. 5. Дипольный момент- [Кл м] Специальный параметр для молекул и молекулярных фрагментов. = q l, где q- заряд диполя, l - расстояние между зарядами Если дипольный момент молекул вещества равен нулю, то такой материал называют неполярным. Если дипольный момент больше нуля –материал полярный и полярность тем 19 выше, чем больше m.
10. ЭНЕРГЕТИЧЕСКИЕ ПАРАМЕТРЫ 10. 1. Работа выхода электрона -Ае [э. В] Специальный параметр для металлов. Это та энергия, которую необходимо подвести к материалу, чтобы удалить электроны на бесконечное расстояние от поверхности материала. Рис. 1. 10. Схема определения краевого угла смачивания. 10. 2. Ширина запрещенной зоны-Hg [э. В] Универсальный параметр Шириной запрещённой зоны называют ту энергию, которую необходимо подвести к материалу, чтобы создать в нём дополнительные носители заряды - электроны , дырки. Hg = 0 – проводники Hg <2 э. В – полупроводники Hg >2 э. В – диэлектрики 10. 3. Поверхностное натяжение - [H м]. Универсальный параметр. Характеризует энергию поверхностного слоя материала. 10. 4. Краевой угол смачивания-. Специальный параметр для твердых материалов. Краевой угол смачивания характеризует взаимодействие поверхности данного материала с каким - либо жидким веществом. [°] - в градусах. Если 0, то капля жидкости полностью растекается по поверхности , что говорит о хорошей смачиваемости данного материала. Если > π/2 - материал плохо смачивается данной жидкостью. 10. 5. Дипольный момент- [Кл м] Специальный параметр для молекул и молекулярных фрагментов. = q l, где q- заряд диполя, l - расстояние между зарядами Если дипольный момент молекул вещества равен нулю, то такой материал называют неполярным. Если дипольный момент больше нуля –материал полярный и полярность тем 19 выше, чем больше m.
 11. ДИФФУЗИОННЫЕ ПАРАМЕТРЫ Проницаемост характеризует способность материала пропускать через себя другое вещество, атомы и молекулы. Если происходит перемещение вещества как единого целого, то говорят о фазовом потоке, который описывается законами аэро- и гидродинамики. Если же наблюдается перемещение в материале отдельных частиц (атомов, молекул, ионов и др. ), то говорят о диффузионном потоке, который описывается двумя уравнениями Фика. Первый закон Фика (для стационарной диффузии) I = D grad. C= D(d. C/dx) где I диффузионный поток, D коэффициент диффузии, С концентрация диффузанта, х координата Второй закон Фика (для нестационарной диффузии) где t время Коэффициент диффузии D является важным техническим параметром материала. Он зависит от температуры по экспоненциальной зависимости: D=D 0 exp( U/RT) где D 0 предэкспоненциальный множитель, U энергия активации, R универсальная газовая постоянная, Т абсолютная температура 20
11. ДИФФУЗИОННЫЕ ПАРАМЕТРЫ Проницаемост характеризует способность материала пропускать через себя другое вещество, атомы и молекулы. Если происходит перемещение вещества как единого целого, то говорят о фазовом потоке, который описывается законами аэро- и гидродинамики. Если же наблюдается перемещение в материале отдельных частиц (атомов, молекул, ионов и др. ), то говорят о диффузионном потоке, который описывается двумя уравнениями Фика. Первый закон Фика (для стационарной диффузии) I = D grad. C= D(d. C/dx) где I диффузионный поток, D коэффициент диффузии, С концентрация диффузанта, х координата Второй закон Фика (для нестационарной диффузии) где t время Коэффициент диффузии D является важным техническим параметром материала. Он зависит от температуры по экспоненциальной зависимости: D=D 0 exp( U/RT) где D 0 предэкспоненциальный множитель, U энергия активации, R универсальная газовая постоянная, Т абсолютная температура 20
 Тема 2. СТРУКТУРА МАТЕРИАЛОВ Химические связи. üионная (гетерополярная) üковалентная (гомеополярная) üметаллическая üмолекулярная (ван-дер-ваальсовская) 21
Тема 2. СТРУКТУРА МАТЕРИАЛОВ Химические связи. üионная (гетерополярная) üковалентная (гомеополярная) üметаллическая üмолекулярная (ван-дер-ваальсовская) 21
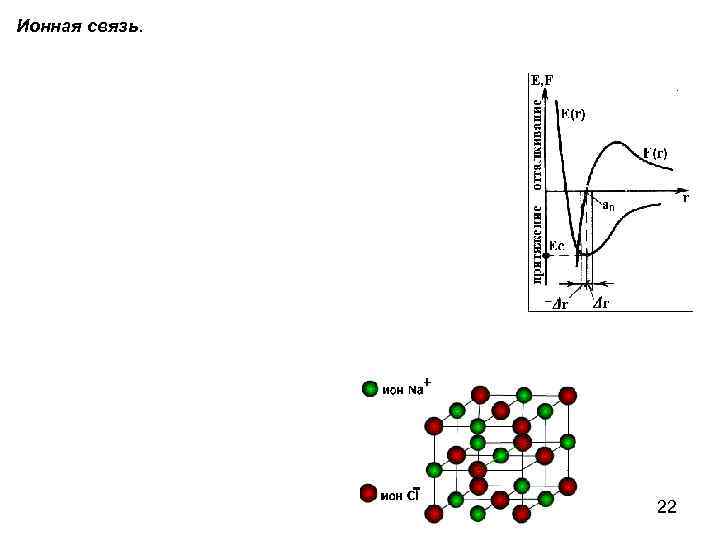 Ионная связь. 22
Ионная связь. 22
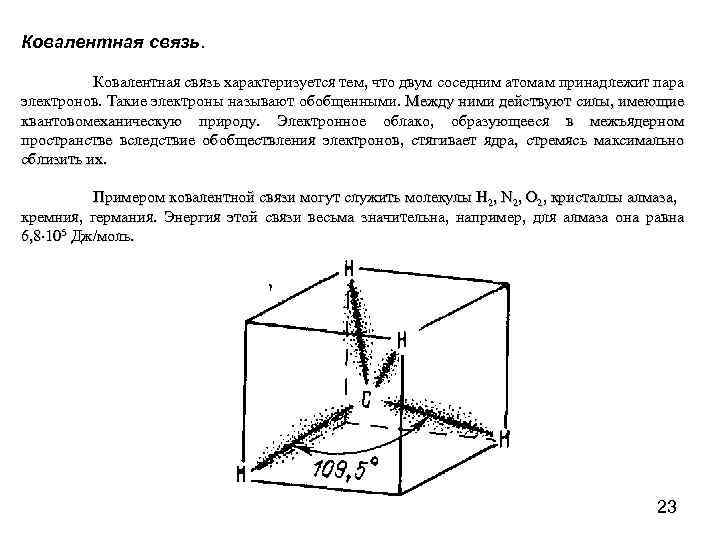 Ковалентная связь. Ковалентная связь характеризуется тем, что двум соседним атомам принадлежит пара электронов. Такие электроны называют обобщенными. Между ними действуют силы, имеющие квантовомеханическую природу. Электронное облако, образующееся в межъядерном пространстве вследствие обобществления электронов, стягивает ядра, стремясь максимально сблизить их. Примером ковалентной связи могут служить молекулы Н 2, N 2, O 2, кристаллы алмаза, кремния, германия. Энергия этой связи весьма значительна, например, для алмаза она равна 6, 8 105 Дж/моль. 23
Ковалентная связь. Ковалентная связь характеризуется тем, что двум соседним атомам принадлежит пара электронов. Такие электроны называют обобщенными. Между ними действуют силы, имеющие квантовомеханическую природу. Электронное облако, образующееся в межъядерном пространстве вследствие обобществления электронов, стягивает ядра, стремясь максимально сблизить их. Примером ковалентной связи могут служить молекулы Н 2, N 2, O 2, кристаллы алмаза, кремния, германия. Энергия этой связи весьма значительна, например, для алмаза она равна 6, 8 105 Дж/моль. 23
 Металлическая связь. В металлах действует особый вид связи, получивший название металлической. Структуру металлического кристалла можно представить в виде ионного остова, погруженного в газ из обобществленных валентных электронов. 24
Металлическая связь. В металлах действует особый вид связи, получивший название металлической. Структуру металлического кристалла можно представить в виде ионного остова, погруженного в газ из обобществленных валентных электронов. 24
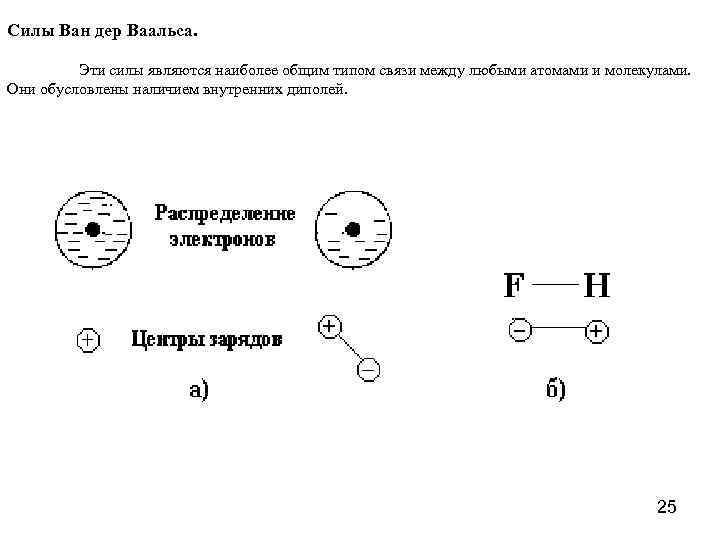 Силы Ван дер Ваальса. Эти силы являются наиболее общим типом связи между любыми атомами и молекулами. Они обусловлены наличием внутренних диполей. 25
Силы Ван дер Ваальса. Эти силы являются наиболее общим типом связи между любыми атомами и молекулами. Они обусловлены наличием внутренних диполей. 25
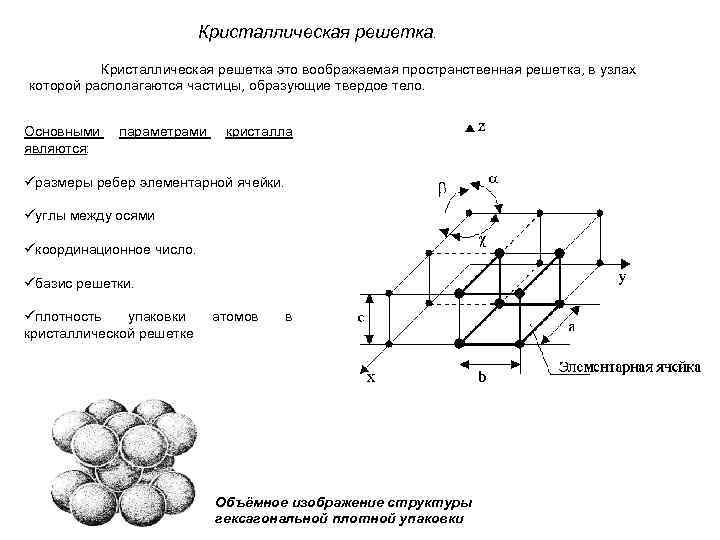 Кристаллическая решетка. Кристаллическая решетка это воображаемая пространственная решетка, в узлах которой располагаются частицы, образующие твердое тело. Основными являются: параметрами кристалла üразмеры ребер элементарной ячейки. üуглы между осями üкоординационное число. üбазис решетки. üплотность упаковки кристаллической решетке атомов в Объёмное изображение структуры гексагональной плотной упаковки
Кристаллическая решетка. Кристаллическая решетка это воображаемая пространственная решетка, в узлах которой располагаются частицы, образующие твердое тело. Основными являются: параметрами кристалла üразмеры ребер элементарной ячейки. üуглы между осями üкоординационное число. üбазис решетки. üплотность упаковки кристаллической решетке атомов в Объёмное изображение структуры гексагональной плотной упаковки
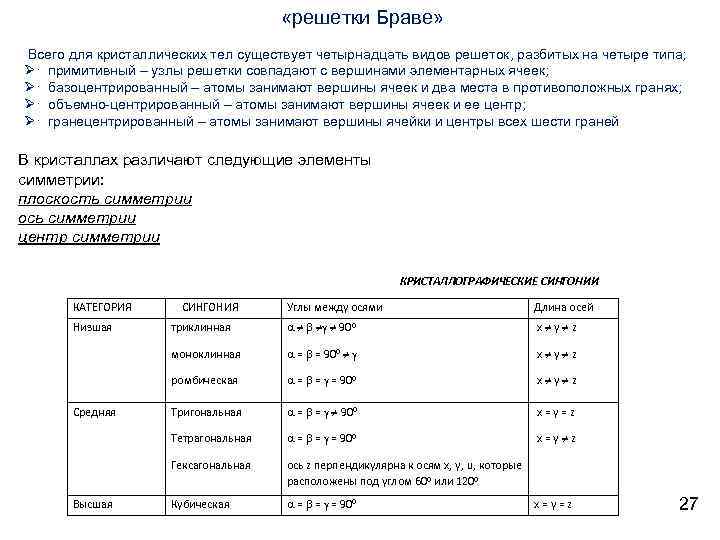 «решетки Браве» Всего для кристаллических тел существует четырнадцать видов решеток, разбитых на четыре типа; Ø· примитивный – узлы решетки совпадают с вершинами элементарных ячеек; Ø· базоцентрированный – атомы занимают вершины ячеек и два места в противоположных гранях; Ø· объемно-центрированный – атомы занимают вершины ячеек и ее центр; Ø· гранецентрированный – атомы занимают вершины ячейки и центры всех шести граней В кристаллах различают следующие элементы симметрии: плоскость симметрии ось симметрии центр симметрии КРИСТАЛЛОГРАФИЧЕСКИЕ СИНГОНИИ КАТЕГОРИЯ триклинная 900 x y z = = = 900 x y z Тригональная = = 900 x=y=z Тетрагональная = = = 900 x=y z Гексагональная Высшая Длина осей ромбическая Средняя Углы между осями моноклинная Низшая СИНГОНИЯ ось z перпендикулярна к осям х, у, u, которые расположены под углом 60 0 или 1200 Кубическая = = = 900 x=y=z 27
«решетки Браве» Всего для кристаллических тел существует четырнадцать видов решеток, разбитых на четыре типа; Ø· примитивный – узлы решетки совпадают с вершинами элементарных ячеек; Ø· базоцентрированный – атомы занимают вершины ячеек и два места в противоположных гранях; Ø· объемно-центрированный – атомы занимают вершины ячеек и ее центр; Ø· гранецентрированный – атомы занимают вершины ячейки и центры всех шести граней В кристаллах различают следующие элементы симметрии: плоскость симметрии ось симметрии центр симметрии КРИСТАЛЛОГРАФИЧЕСКИЕ СИНГОНИИ КАТЕГОРИЯ триклинная 900 x y z = = = 900 x y z Тригональная = = 900 x=y=z Тетрагональная = = = 900 x=y z Гексагональная Высшая Длина осей ромбическая Средняя Углы между осями моноклинная Низшая СИНГОНИЯ ось z перпендикулярна к осям х, у, u, которые расположены под углом 60 0 или 1200 Кубическая = = = 900 x=y=z 27
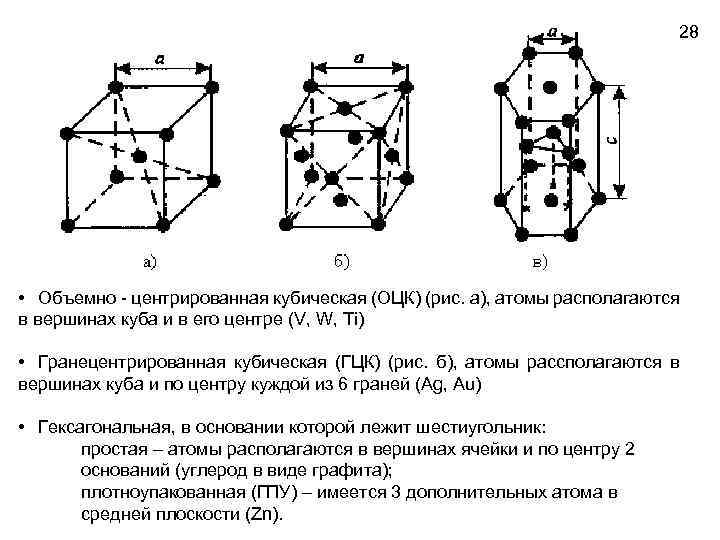 28 • Объемно - центрированная кубическая (ОЦК) (рис. а), атомы располагаются в вершинах куба и в его центре (V, W, Ti) • Гранецентрированная кубическая (ГЦК) (рис. б), атомы рассполагаются в вершинах куба и по центру куждой из 6 граней (Ag, Au) • Гексагональная, в основании которой лежит шестиугольник: простая – атомы располагаются в вершинах ячейки и по центру 2 оснований (углерод в виде графита); плотноупакованная (ГПУ) – имеется 3 дополнительных атома в средней плоскости (Zn).
28 • Объемно - центрированная кубическая (ОЦК) (рис. а), атомы располагаются в вершинах куба и в его центре (V, W, Ti) • Гранецентрированная кубическая (ГЦК) (рис. б), атомы рассполагаются в вершинах куба и по центру куждой из 6 граней (Ag, Au) • Гексагональная, в основании которой лежит шестиугольник: простая – атомы располагаются в вершинах ячейки и по центру 2 оснований (углерод в виде графита); плотноупакованная (ГПУ) – имеется 3 дополнительных атома в средней плоскости (Zn).
![Индексы Миллера. 29 Индексы узла: [[uvw]] Для отрицательного индекса ставится черта над индексом. Например, Индексы Миллера. 29 Индексы узла: [[uvw]] Для отрицательного индекса ставится черта над индексом. Например,](https://present5.com/presentation/67943771_131485604/image-29.jpg) Индексы Миллера. 29 Индексы узла: [[uvw]] Для отрицательного индекса ставится черта над индексом. Например, положение центра элементарной ячейки определяется индексом [[½ ½ ½ ]] положение центра грани, лежащей в плоскости хоу, — индексом [[½ ½ 0]]. Индекс направления: [uvw] определяется координатами вектора, выходящего из начала координат и параллельного заданному направлению. Ураванение плоскости: х/u + у/v + z/w = 1 или hx + ky + lz = 1 Индекс плоскости: (hkl) находят следующим образом: определяют точки пересечения плоскости с координатными осями, затем отрезки u, v, w и обратные значения h, k, I, которые приводят к наименьшим целым числам и записывают в круглых скобках. Индексы (1/2 1/3 1) и (326), (2 ½ 3) и (416), (224) и (112) обозначают соответственно одни и те же плоскости.
Индексы Миллера. 29 Индексы узла: [[uvw]] Для отрицательного индекса ставится черта над индексом. Например, положение центра элементарной ячейки определяется индексом [[½ ½ ½ ]] положение центра грани, лежащей в плоскости хоу, — индексом [[½ ½ 0]]. Индекс направления: [uvw] определяется координатами вектора, выходящего из начала координат и параллельного заданному направлению. Ураванение плоскости: х/u + у/v + z/w = 1 или hx + ky + lz = 1 Индекс плоскости: (hkl) находят следующим образом: определяют точки пересечения плоскости с координатными осями, затем отрезки u, v, w и обратные значения h, k, I, которые приводят к наименьшим целым числам и записывают в круглых скобках. Индексы (1/2 1/3 1) и (326), (2 ½ 3) и (416), (224) и (112) обозначают соответственно одни и те же плоскости.
 Дефекты кристаллических структур. Дефекты в кристаллах классифицируют по их размерам: üточечные (или атомные, нульмерные), üлинейные (одномерные) üповерхностные (двумерные). 30
Дефекты кристаллических структур. Дефекты в кристаллах классифицируют по их размерам: üточечные (или атомные, нульмерные), üлинейные (одномерные) üповерхностные (двумерные). 30
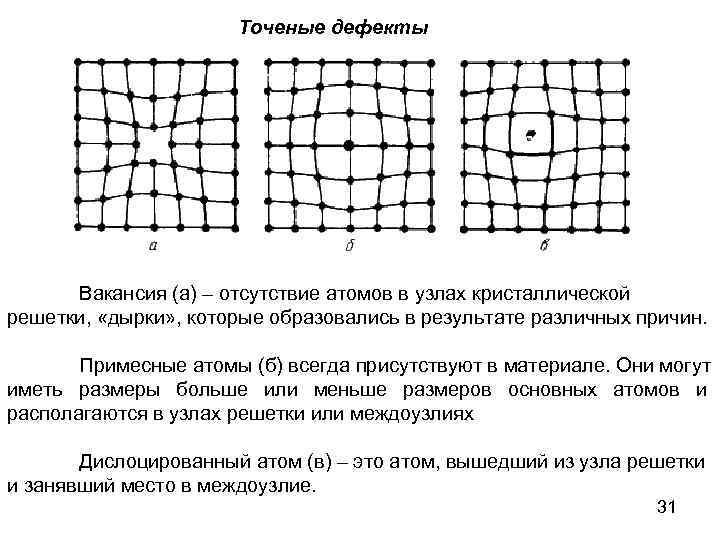 Точеные дефекты Вакансия (а) – отсутствие атомов в узлах кристаллической решетки, «дырки» , которые образовались в результате различных причин. Примесные атомы (б) всегда присутствуют в материале. Они могут иметь размеры больше или меньше размеров основных атомов и располагаются в узлах решетки или междоузлиях Дислоцированный атом (в) – это атом, вышедший из узла решетки и занявший место в междоузлие. 31
Точеные дефекты Вакансия (а) – отсутствие атомов в узлах кристаллической решетки, «дырки» , которые образовались в результате различных причин. Примесные атомы (б) всегда присутствуют в материале. Они могут иметь размеры больше или меньше размеров основных атомов и располагаются в узлах решетки или междоузлиях Дислоцированный атом (в) – это атом, вышедший из узла решетки и занявший место в междоузлие. 31
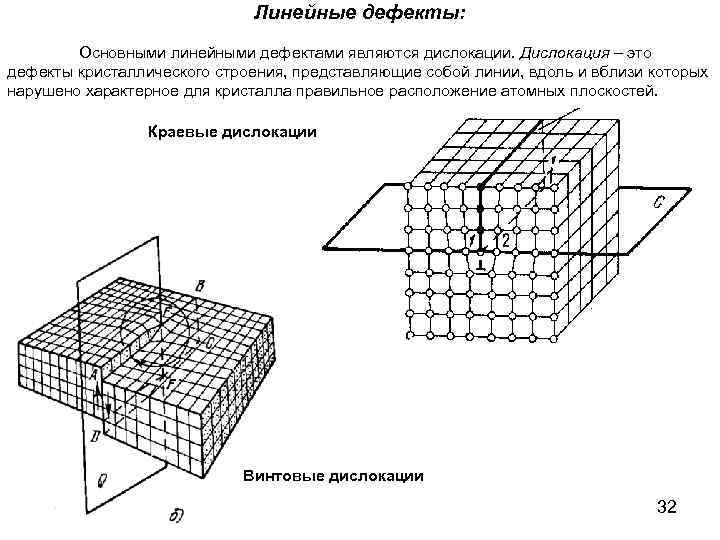 Линейные дефекты: Основными линейными дефектами являются дислокации. Дислокация – это дефекты кристаллического строения, представляющие собой линии, вдоль и вблизи которых нарушено характерное для кристалла правильное расположение атомных плоскостей. Краевые дислокации Винтовые дислокации 32
Линейные дефекты: Основными линейными дефектами являются дислокации. Дислокация – это дефекты кристаллического строения, представляющие собой линии, вдоль и вблизи которых нарушено характерное для кристалла правильное расположение атомных плоскостей. Краевые дислокации Винтовые дислокации 32
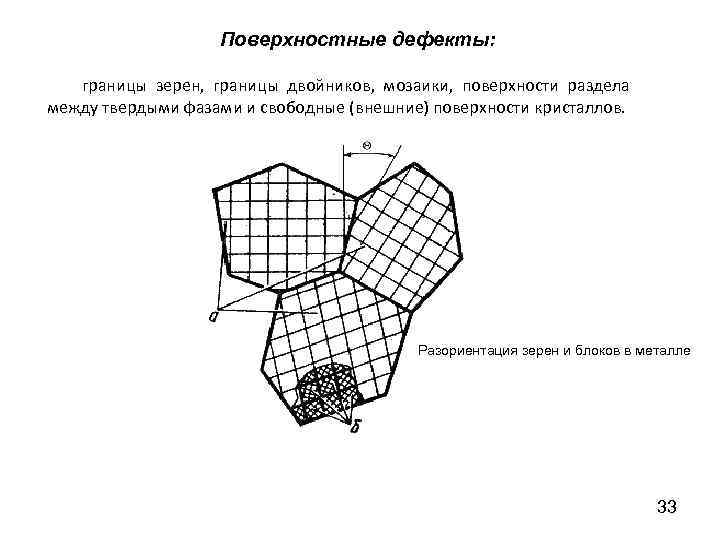 Поверхностные дефекты: границы зерен, границы двойников, мозаики, поверхности раздела между твердыми фазами и свободные (внешние) поверхности кристаллов. Разориентация зерен и блоков в металле 33
Поверхностные дефекты: границы зерен, границы двойников, мозаики, поверхности раздела между твердыми фазами и свободные (внешние) поверхности кристаллов. Разориентация зерен и блоков в металле 33
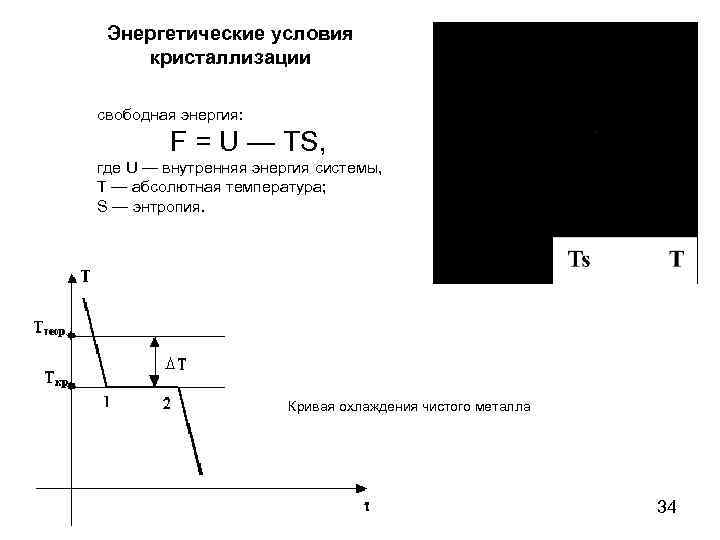 Энергетические условия кристаллизации свободная энергия: F = U — TS, где U — внутренняя энергия системы, Т — абсолютная температура; S — энтропия. Кривая охлаждения чистого металла 34
Энергетические условия кристаллизации свободная энергия: F = U — TS, где U — внутренняя энергия системы, Т — абсолютная температура; S — энтропия. Кривая охлаждения чистого металла 34
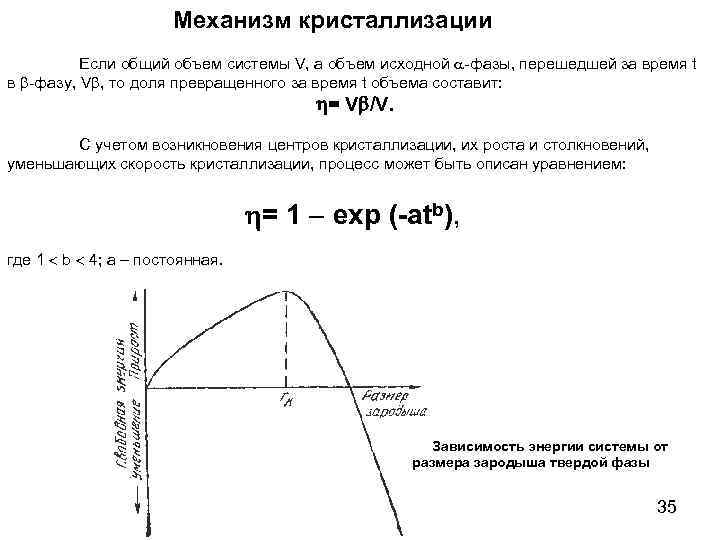 Механизм кристаллизации Если общий объем системы V, а объем исходной -фазы, перешедшей за время t в -фазу, V , то доля превращенного за время t объема составит: = V /V. С учетом возникновения центров кристаллизации, их роста и столкновений, уменьшающих скорость кристаллизации, процесс может быть описан уравнением: = 1 exp (-atb), где 1 b 4; а – постоянная. Зависимость энергии системы от размера зародыша твердой фазы 35
Механизм кристаллизации Если общий объем системы V, а объем исходной -фазы, перешедшей за время t в -фазу, V , то доля превращенного за время t объема составит: = V /V. С учетом возникновения центров кристаллизации, их роста и столкновений, уменьшающих скорость кристаллизации, процесс может быть описан уравнением: = 1 exp (-atb), где 1 b 4; а – постоянная. Зависимость энергии системы от размера зародыша твердой фазы 35
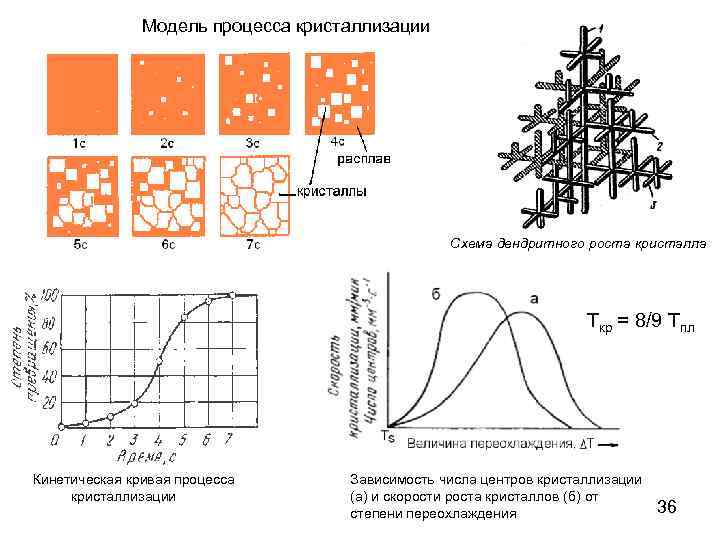 Модель процесса кристаллизации Схема дендритного роста кристалла Ткр = 8/9 Тпл Кинетическая кривая процесса кристаллизации Зависимость числа центров кристаллизации (а) и скорости роста кристаллов (б) от степени переохлаждения 36
Модель процесса кристаллизации Схема дендритного роста кристалла Ткр = 8/9 Тпл Кинетическая кривая процесса кристаллизации Зависимость числа центров кристаллизации (а) и скорости роста кристаллов (б) от степени переохлаждения 36
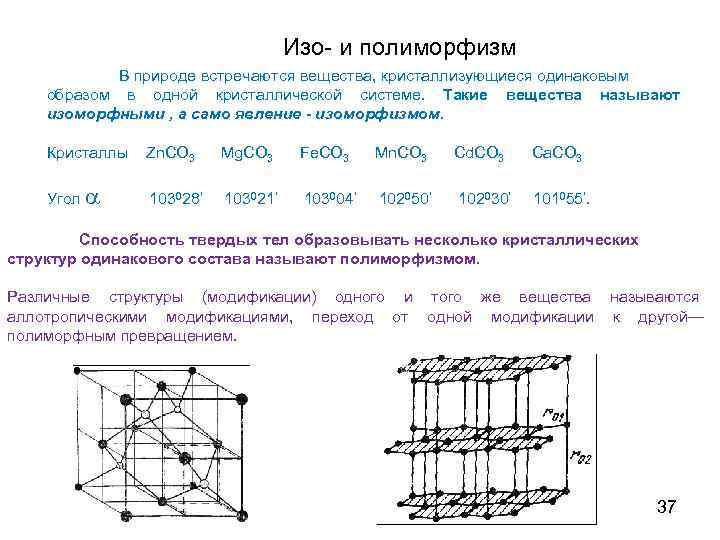 Изо- и полиморфизм В природе встречаются вещества, кристаллизующиеся одинаковым образом в одной кристаллической системе. Такие вещества называют изоморфными , а само явление - изоморфизмом. Кристаллы Zn. CO 3 Mg. CO 3 Fe. CO 3 Mn. CO 3 Cd. CO 3 Ca. CO 3 Угол 103028’ 103021’ 103004’ 102050’ 102030’ 101055’. Способность твердых тел образовывать несколько кристаллических структур одинакового состава называют полиморфизмом. Различные структуры (модификации) одного и того же вещества называются аллотропическими модификациями, переход от одной модификации к другой— полиморфным превращением. 37
Изо- и полиморфизм В природе встречаются вещества, кристаллизующиеся одинаковым образом в одной кристаллической системе. Такие вещества называют изоморфными , а само явление - изоморфизмом. Кристаллы Zn. CO 3 Mg. CO 3 Fe. CO 3 Mn. CO 3 Cd. CO 3 Ca. CO 3 Угол 103028’ 103021’ 103004’ 102050’ 102030’ 101055’. Способность твердых тел образовывать несколько кристаллических структур одинакового состава называют полиморфизмом. Различные структуры (модификации) одного и того же вещества называются аллотропическими модификациями, переход от одной модификации к другой— полиморфным превращением. 37
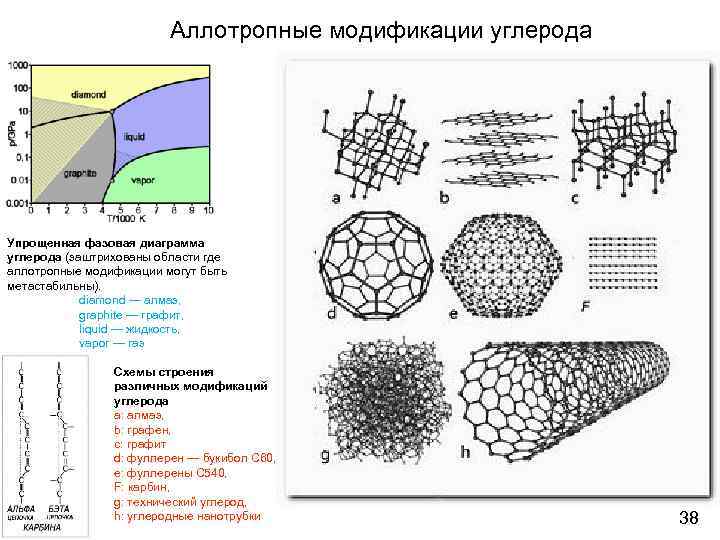 Аллотропные модификации углерода Упрощенная фазовая диаграмма углерода (заштрихованы области где аллотропные модификации могут быть метастабильны). diamond — алмаз, graphite — графит, liquid — жидкость, vapor — газ Схемы строения различных модификаций углерода a: алмаз, b: графен, c: графит d: фуллерен — букибол C 60, e: фуллерены C 540, F: карбин, g: технический углерод, h: углеродные нанотрубки 38
Аллотропные модификации углерода Упрощенная фазовая диаграмма углерода (заштрихованы области где аллотропные модификации могут быть метастабильны). diamond — алмаз, graphite — графит, liquid — жидкость, vapor — газ Схемы строения различных модификаций углерода a: алмаз, b: графен, c: графит d: фуллерен — букибол C 60, e: фуллерены C 540, F: карбин, g: технический углерод, h: углеродные нанотрубки 38
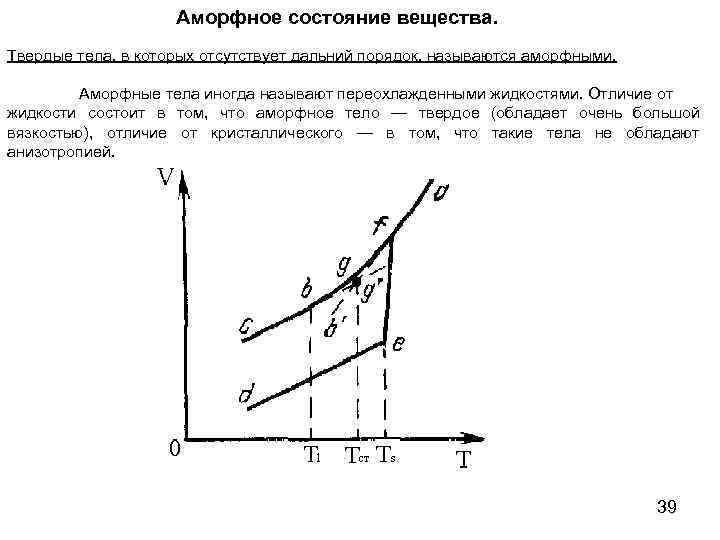 Аморфное состояние вещества. Твердые тела, в которых отсутствует дальний порядок, называются аморфными. Аморфные тела иногда называют переохлажденными жидкостями. Отличие от жидкости состоит в том, что аморфное тело — твердое (обладает очень большой вязкостью), отличие от кристаллического — в том, что такие тела не обладают анизотропией. 39
Аморфное состояние вещества. Твердые тела, в которых отсутствует дальний порядок, называются аморфными. Аморфные тела иногда называют переохлажденными жидкостями. Отличие от жидкости состоит в том, что аморфное тело — твердое (обладает очень большой вязкостью), отличие от кристаллического — в том, что такие тела не обладают анизотропией. 39
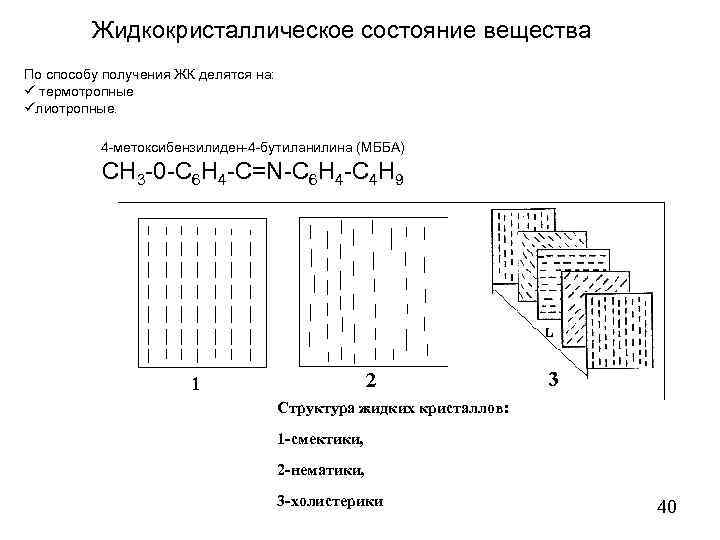 Жидкокристаллическое состояние вещества По способу получения ЖК делятся на: ü термотропные üлиотропные. 4 -метоксибензилиден-4 -бутиланилина (МББА) СН 3 -0 -С 6 Н 4 -С=N-С 6 Н 4 -С 4 Н 9 Структура жидких кристаллов: 1 -смектики, 2 -нематики, 3 -холистерики 40
Жидкокристаллическое состояние вещества По способу получения ЖК делятся на: ü термотропные üлиотропные. 4 -метоксибензилиден-4 -бутиланилина (МББА) СН 3 -0 -С 6 Н 4 -С=N-С 6 Н 4 -С 4 Н 9 Структура жидких кристаллов: 1 -смектики, 2 -нематики, 3 -холистерики 40
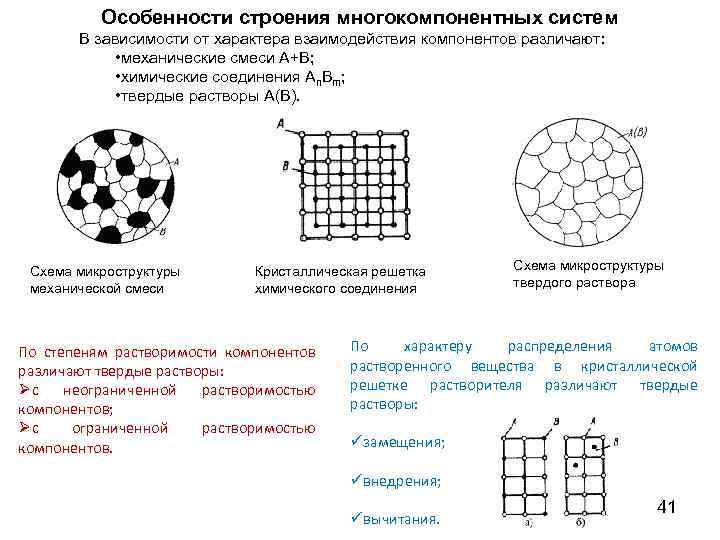 Особенности строения многокомпонентных систем В зависимости от характера взаимодействия компонентов различают: • механические смеси А+В; • химические соединения Аn. Вm; • твердые растворы А(В). Схема микроструктуры механической смеси Кристаллическая решетка химического соединения По степеням растворимости компонентов различают твердые растворы: Øс неограниченной растворимостью компонентов; Øс ограниченной растворимостью компонентов. Схема микроструктуры твердого раствора По характеру распределения атомов растворенного вещества в кристаллической решетке растворителя различают твердые растворы: üзамещения; üвнедрения; üвычитания. 41
Особенности строения многокомпонентных систем В зависимости от характера взаимодействия компонентов различают: • механические смеси А+В; • химические соединения Аn. Вm; • твердые растворы А(В). Схема микроструктуры механической смеси Кристаллическая решетка химического соединения По степеням растворимости компонентов различают твердые растворы: Øс неограниченной растворимостью компонентов; Øс ограниченной растворимостью компонентов. Схема микроструктуры твердого раствора По характеру распределения атомов растворенного вещества в кристаллической решетке растворителя различают твердые растворы: üзамещения; üвнедрения; üвычитания. 41
 Фазовое состояние материалов Фазовое состояние описывается правилом фаз Гиббса, которое формулируется так: в равновесной гетерогенной системе, на которую из внешних факторов действуют только температура и давление, число фаз (Ф) плюс число степеней свободы (С), равно числу компонентов (К) плюс два. Ф +С=К + 2 42
Фазовое состояние материалов Фазовое состояние описывается правилом фаз Гиббса, которое формулируется так: в равновесной гетерогенной системе, на которую из внешних факторов действуют только температура и давление, число фаз (Ф) плюс число степеней свободы (С), равно числу компонентов (К) плюс два. Ф +С=К + 2 42
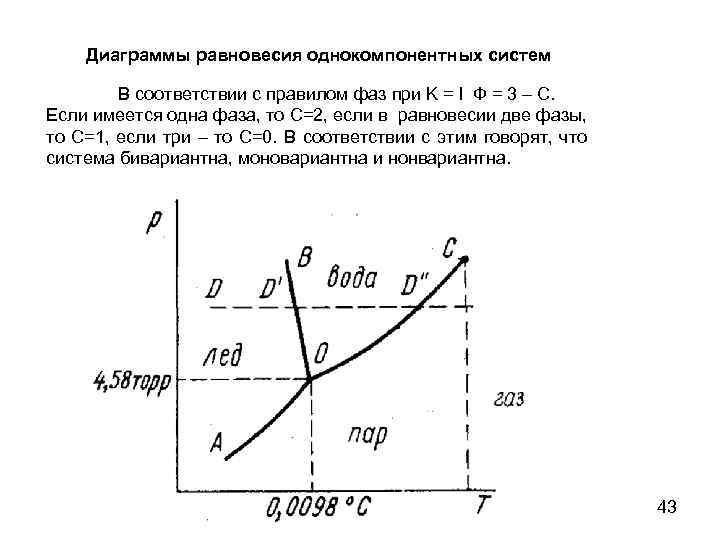 Диаграммы равновесия однокомпонентных систем В соответствии с правилом фаз при K = l Ф = 3 С. Если имеется одна фаза, то С=2, если в равновесии две фазы, то С=1, если три то С=0. В соответствии с этим говорят, что система бивариантна, моновариантна и нонвариантна. 43
Диаграммы равновесия однокомпонентных систем В соответствии с правилом фаз при K = l Ф = 3 С. Если имеется одна фаза, то С=2, если в равновесии две фазы, то С=1, если три то С=0. В соответствии с этим говорят, что система бивариантна, моновариантна и нонвариантна. 43
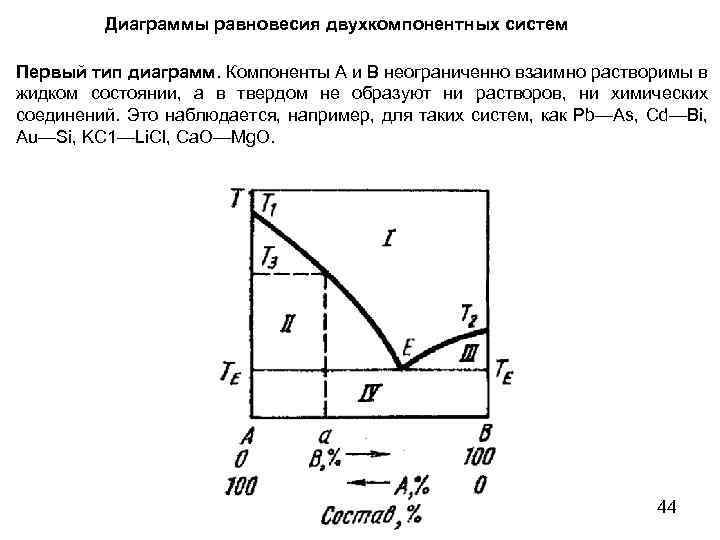 Диаграммы равновесия двухкомпонентных систем Первый тип диаграмм. Компоненты А и В неограниченно взаимно растворимы в жидком состоянии, а в твердом не образуют ни растворов, ни химических соединений. Это наблюдается, например, для таких систем, как Pb—As, Cd—Bi, Au—Si, KC 1—Li. Cl, Ca. O—Mg. O. 44
Диаграммы равновесия двухкомпонентных систем Первый тип диаграмм. Компоненты А и В неограниченно взаимно растворимы в жидком состоянии, а в твердом не образуют ни растворов, ни химических соединений. Это наблюдается, например, для таких систем, как Pb—As, Cd—Bi, Au—Si, KC 1—Li. Cl, Ca. O—Mg. O. 44
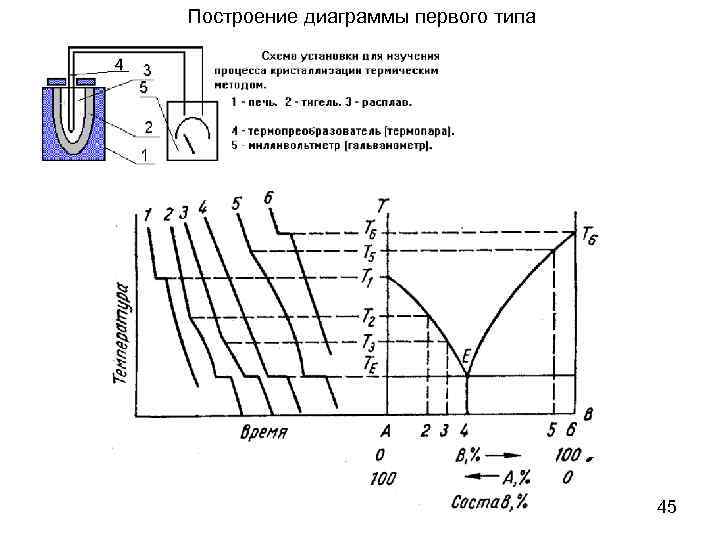 Построение диаграммы первого типа 45
Построение диаграммы первого типа 45
 Правило рычага Для сплава состава 1 при температуре Т 1 отношение массы жидкости Qж к массе выделившихся кристаллов компонента A QT равно отношению отрезков T 1 b 1, и b 1 l 1: Qж/QT = T 1 b 1/b 1 l 1. При температуре Т 2 для того же сплава Qж/QT = T 2 b 2/b 2 l 2. Чем ближе состав расплава к эвтектическому, тем больше доля жидкой фазы при данной температуре. Поэтому горизонтальные участки на кривых охлаждения при температуре ТЕ тем больше, чем ближе состав расплава к эвтектическому, т. е. чем больше жидкости остается при этой температуре. 46
Правило рычага Для сплава состава 1 при температуре Т 1 отношение массы жидкости Qж к массе выделившихся кристаллов компонента A QT равно отношению отрезков T 1 b 1, и b 1 l 1: Qж/QT = T 1 b 1/b 1 l 1. При температуре Т 2 для того же сплава Qж/QT = T 2 b 2/b 2 l 2. Чем ближе состав расплава к эвтектическому, тем больше доля жидкой фазы при данной температуре. Поэтому горизонтальные участки на кривых охлаждения при температуре ТЕ тем больше, чем ближе состав расплава к эвтектическому, т. е. чем больше жидкости остается при этой температуре. 46
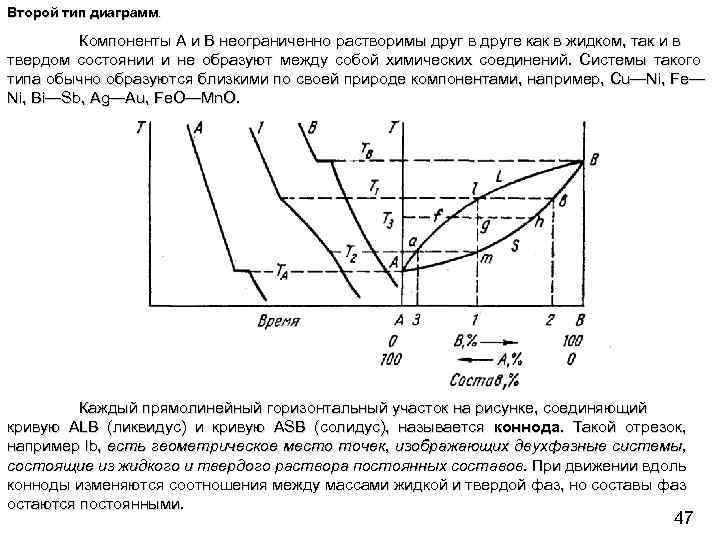 Второй тип диаграмм. Компоненты А и В неограниченно растворимы друг в друге как в жидком, так и в твердом состоянии и не образуют между собой химических соединений. Системы такого типа обычно образуются близкими по своей природе компонентами, например, Сu—Ni, Fe— Ni, Bi—Sb, Ag—Au, Fe. O—Mn. O. Каждый прямолинейный горизонтальный участок на рисунке, соединяющий кривую ALB (ликвидус) и кривую ASB (солидус), называется коннода. Такой отрезок, например lb, есть геометрическое место точек, изображающих двухфазные системы, состоящие из жидкого и твердого раствора постоянных составов. При движении вдоль конноды изменяются соотношения между массами жидкой и твердой фаз, но составы фаз остаются постоянными. 47
Второй тип диаграмм. Компоненты А и В неограниченно растворимы друг в друге как в жидком, так и в твердом состоянии и не образуют между собой химических соединений. Системы такого типа обычно образуются близкими по своей природе компонентами, например, Сu—Ni, Fe— Ni, Bi—Sb, Ag—Au, Fe. O—Mn. O. Каждый прямолинейный горизонтальный участок на рисунке, соединяющий кривую ALB (ликвидус) и кривую ASB (солидус), называется коннода. Такой отрезок, например lb, есть геометрическое место точек, изображающих двухфазные системы, состоящие из жидкого и твердого раствора постоянных составов. При движении вдоль конноды изменяются соотношения между массами жидкой и твердой фаз, но составы фаз остаются постоянными. 47
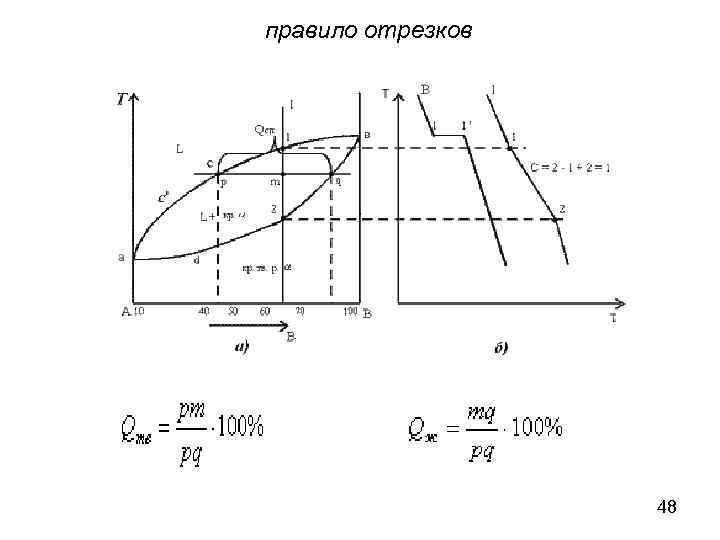 правило отрезков 48
правило отрезков 48
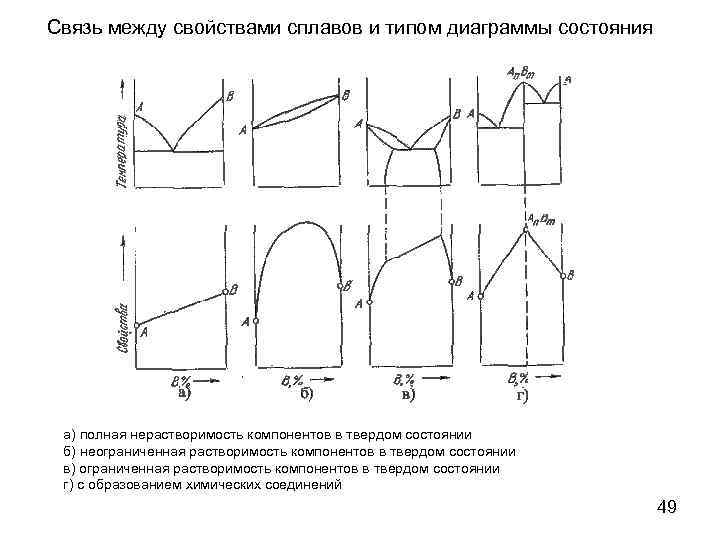 Связь между свойствами сплавов и типом диаграммы состояния а) полная нерастворимость компонентов в твердом состоянии б) неограниченная растворимость компонентов в твердом состоянии в) ограниченная растворимость компонентов в твердом состоянии г) с образованием химических соединений 49
Связь между свойствами сплавов и типом диаграммы состояния а) полная нерастворимость компонентов в твердом состоянии б) неограниченная растворимость компонентов в твердом состоянии в) ограниченная растворимость компонентов в твердом состоянии г) с образованием химических соединений 49
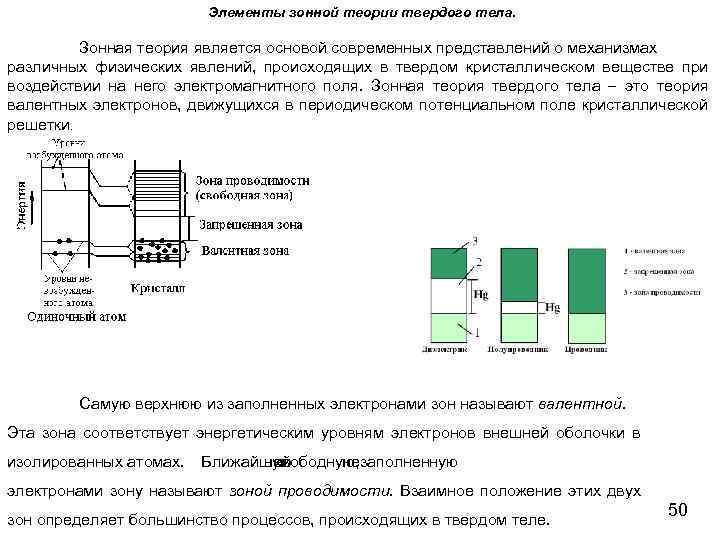 Элементы зонной теории твердого тела. Зонная теория является основой современных представлений о механизмах различных физических явлений, происходящих в твердом кристаллическом веществе при воздействии на него электромагнитного поля. Зонная теория твердого тела это теория валентных электронов, движущихся в периодическом потенциальном поле кристаллической решетки. Самую верхнюю из заполненных электронами зон называют валентной. Эта зона соответствует энергетическим уровням электронов внешней оболочки в изолированных атомах. Ближайшую ней свободную, к незаполненную электронами зону называют зоной проводимости. Взаимное положение этих двух зон определяет большинство процессов, происходящих в твердом теле. 50
Элементы зонной теории твердого тела. Зонная теория является основой современных представлений о механизмах различных физических явлений, происходящих в твердом кристаллическом веществе при воздействии на него электромагнитного поля. Зонная теория твердого тела это теория валентных электронов, движущихся в периодическом потенциальном поле кристаллической решетки. Самую верхнюю из заполненных электронами зон называют валентной. Эта зона соответствует энергетическим уровням электронов внешней оболочки в изолированных атомах. Ближайшую ней свободную, к незаполненную электронами зону называют зоной проводимости. Взаимное положение этих двух зон определяет большинство процессов, происходящих в твердом теле. 50


