НЕОПЛАЗИЯ КАК ТИПОВОЙ ПАТОЛОГИЧЕСКИЙ ПРОЦЕСС.ppt
- Количество слайдов: 56
Кафедра патологии медицинского факультета Санкт-Петербургского государственного университета Л. П. Чурилов НЕОПЛАЗИЯ КАК ТИПОВОЙ ПАТОЛОГИЧЕСКИЙ ПРОЦЕСС Этиология и патогенез новообразований
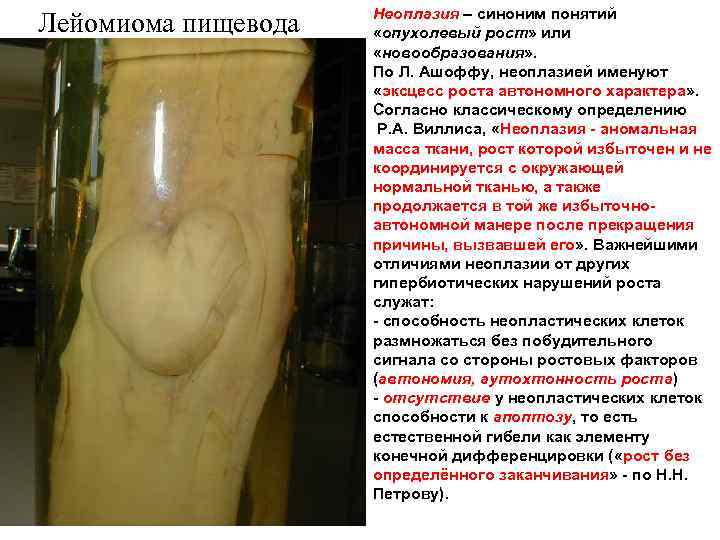
Лейомиома пищевода Неоплазия – синоним понятий «опухолевый рост» или «новообразования» . По Л. Ашоффу, неоплазией именуют «эксцесс роста автономного характера» . Согласно классическому определению Р. А. Виллиса, «Неоплазия - аномальная масса ткани, рост которой избыточен и не координируется с окружающей нормальной тканью, а также продолжается в той же избыточноавтономной манере после прекращения причины, вызвавшей его» . Важнейшими отличиями неоплазии от других гипербиотических нарушений роста служат: - способность неопластических клеток размножаться без побудительного сигнала со стороны ростовых факторов (автономия, аутохтонность роста) - отсутствие у неопластических клеток способности к апоптозу, то есть естественной гибели как элементу конечной дифференцировки ( «рост без определённого заканчивания» - по Н. Н. Петрову).

КЛАССИКИ МИРОВОЙ ОНКОЛОГИИ Карл Альберт Людвиг Ашофф (1866 -1942) – дал самое краткое и емкое определение неоплазии, заложил основы учения о ретикулоэндотелиальной системе и противоопухолевом иммунитете. Кроме заслуг в онкологии, описал ревматические гранулёмы и строение проводящей системы сердца. "Я требую лишь, чтобы мои ассистенты работали по двадцать четыре часа в сутки, а что они делают все свободное время -меня абсолютно не касается!" Теодор Бовери (1862 1915) – сформулировал гипотезу о том, что неоплазия – всегда результат анеуплоидии клеток. В современной онкологии ее развивает Питер Дюсберг, указывающий, что некоторые канцерогены не вызывают иных мутаций, кроме анеуплоидии и считающий, что именно этот вид мутаций нарушает взаимоотношения онкогенов и опухолевых супрессоров Николай Николаевич Петров (1876 1964) – первым сформулировал правило, что неоплазия – всегда результат соматической мутации. Основал первую в мире общенациональную диспансерную онкологическую службу. Альфред Г. Кнудсон (род. 1922) – крупнейший детский онколог современности, создатель теории многошагового канцерогенеза. Объяснил взаимоотношения между наследственными и приобретенными неоплазиями, предсказал существование антионкогенов.

КЛАССИКИ МИРОВОЙ ОНКОЛОГИИ Френсис Пейтон Раус (18791970). В 1911 г. получил перевивкой бесклеточного фильтрата модель саркомы у кур и через 55 лет (!) был удостоен за это Нобелевской премии, как первооткрыватель вирусного канцерогенеза. Лев Александрович Зильбер (1894 -1966). Создатель вирусногенетической теории канцерогенеза и учения о противоопухолевом иммунитете. Руперт Аллен Виллис (1898 -1980) Майкл Дж. Бишоп (род. 1936) Создатель наиболее авторитетного в мире руководства «Патология опухолей» (1948), на котором воспитывались поколения Гарольд Э. Вэрмюс (род. 1939) онкологов. Сформулировал критерии неоплазии, Экспериментально обосновали онкогенную теорию канцерогенеза (Нобелевская премия по медицине 1989 г. Изучал распространение, классификацию и гистогенез опухолей, пограничные вопросы
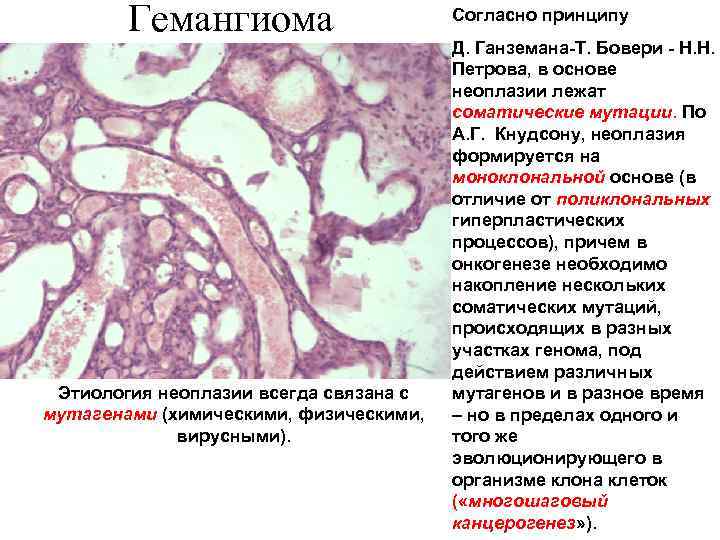
Гемангиома Этиология неоплазии всегда связана с мутагенами (химическими, физическими, вирусными). Согласно принципу Д. Ганземана-Т. Бовери - Н. Н. Петрова, в основе неоплазии лежат соматические мутации. По А. Г. Кнудсону, неоплазия формируется на моноклональной основе (в отличие от поликлональных гиперпластических процессов), причем в онкогенезе необходимо накопление нескольких соматических мутаций, происходящих в разных участках генома, под действием различных мутагенов и в разное время – но в пределах одного и того же эволюционирующего в организме клона клеток ( «многошаговый канцерогенез» ).
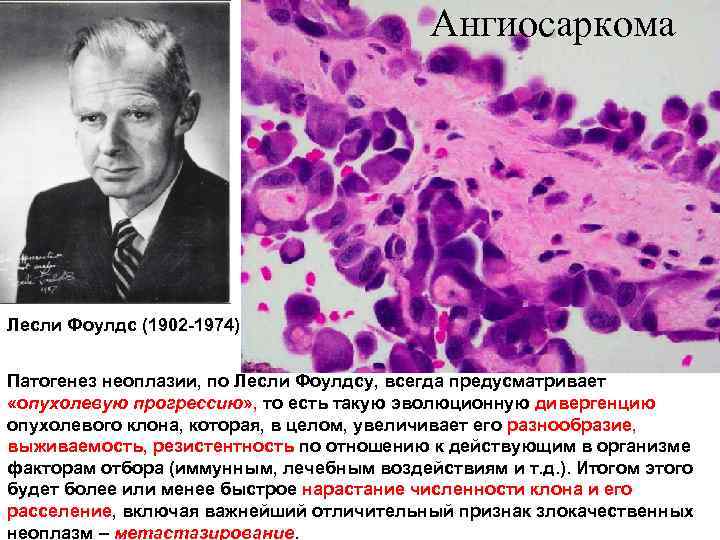
Ангиосаркома Лесли Фоулдс (1902 -1974) Патогенез неоплазии, по Лесли Фоулдсу, всегда предусматривает «опухолевую прогрессию» , то есть такую эволюционную дивергенцию опухолевого клона, которая, в целом, увеличивает его разнообразие, выживаемость, резистентность по отношению к действующим в организме факторам отбора (иммунным, лечебным воздействиям и т. д. ). Итогом этого будет более или менее быстрое нарастание численности клона и его расселение, включая важнейший отличительный признак злокачественных неоплазм – метастазирование.
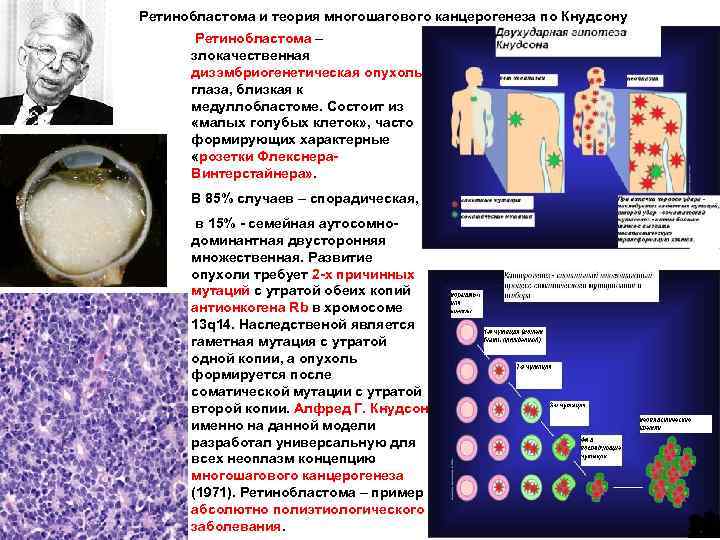
Ретинобластома и теория многошагового канцерогенеза по Кнудсону Ретинобластома – злокачественная дизэмбриогенетическая опухоль глаза, близкая к медуллобластоме. Состоит из «малых голубых клеток» , часто формирующих характерные «розетки Флекснера. Винтерстайнера» . В 85% случаев – спорадическая, в 15% - семейная аутосомнодоминантная двусторонняя множественная. Развитие опухоли требует 2 -х причинных мутаций с утратой обеих копий антионкогена Rb в хромосоме 13 q 14. Наследственой является гаметная мутация с утратой одной копии, а опухоль формируется после соматической мутации с утратой второй копии. Алфред Г. Кнудсон именно на данной модели разработал универсальную для всех неоплазм концепцию многошагового канцерогенеза (1971). Ретинобластома – пример абсолютно полиэтиологического заболевания.
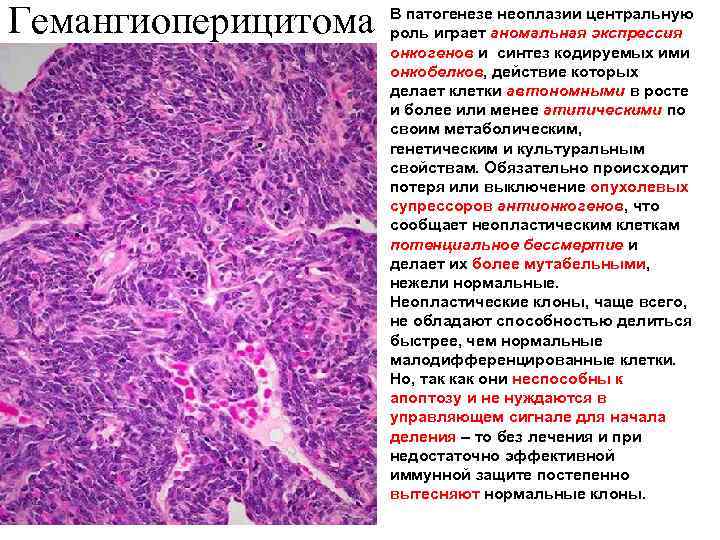
Гемангиоперицитома В патогенезе неоплазии центральную роль играет аномальная экспрессия онкогенов и синтез кодируемых ими онкобелков, действие которых делает клетки автономными в росте и более или менее атипическими по своим метаболическим, генетическим и культуральным свойствам. Обязательно происходит потеря или выключение опухолевых супрессоров антионкогенов, что сообщает неопластическим клеткам потенциальное бессмертие и делает их более мутабельными, нежели нормальные. Неопластические клоны, чаще всего, не обладают способностью делиться быстрее, чем нормальные малодифференцированные клетки. Но, так как они неспособны к апоптозу и не нуждаются в управляющем сигнале для начала деления – то без лечения и при недостаточно эффективной иммунной защите постепенно вытесняют нормальные клоны.
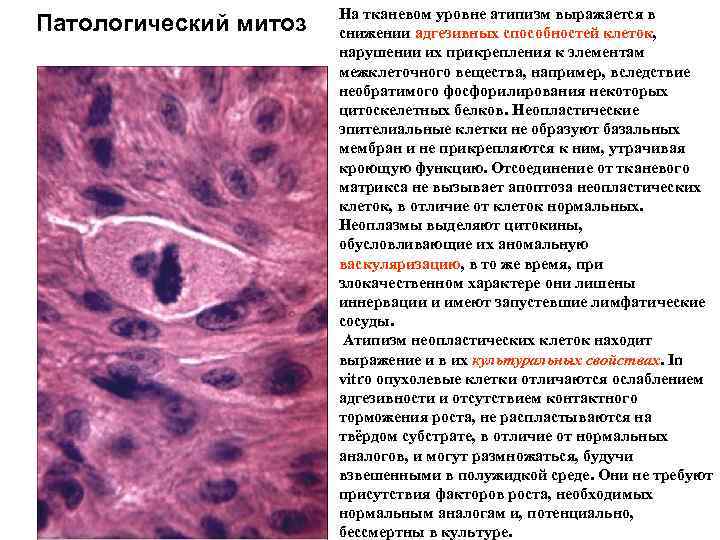
Патологический митоз На тканевом уровне атипизм выражается в снижении адгезивных способностей клеток, нарушении их прикрепления к элементам межклеточного вещества, например, вследствие необратимого фосфорилирования некоторых цитоскелетных белков. Неопластические эпителиальные клетки не образуют базальных мембран и не прикрепляются к ним, утрачивая кроющую функцию. Отсоединение от тканевого матрикса не вызывает апоптоза неопластических клеток, в отличие от клеток нормальных. Неоплазмы выделяют цитокины, обусловливающие их аномальную васкуляризацию, в то же время, при злокачественном характере они лишены иннервации и имеют запустевшие лимфатические сосуды. Атипизм неопластических клеток находит выражение и в их культуральных свойствах. In vitro опухолевые клетки отличаются ослаблением адгезивности и отсутствием контактного торможения роста, не распластываются на твёрдом субстрате, в отличие от нормальных аналогов, и могут размножаться, будучи взвешенными в полужидкой среде. Они не требуют присутствия факторов роста, необходимых нормальным аналогам и, потенциально, бессмертны в культуре.
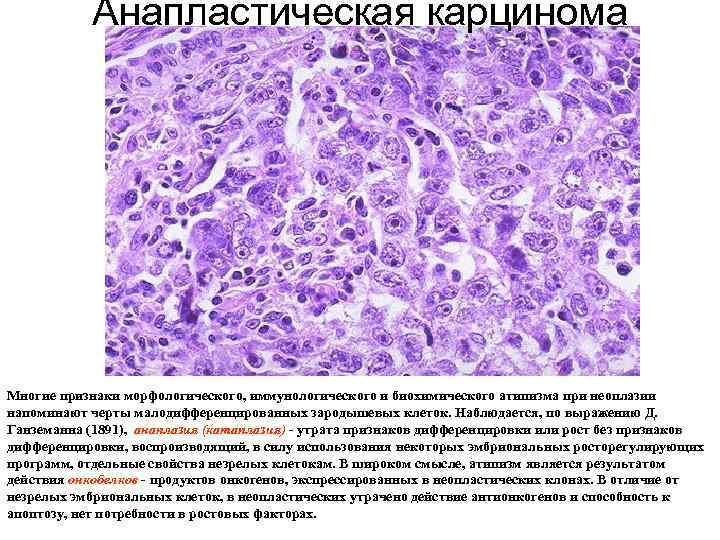
Анапластическая карцинома Многие признаки морфологического, иммунологического и биохимического атипизма при неоплазии напоминают черты малодифференцированных зародышевых клеток. Наблюдается, по выражению Д. Ганземанна (1891), анаплазия (катаплазия) утрата признаков дифференцировки или рост без признаков дифференцировки, воспроизводящий, в силу использования некоторых эмбриональных росторегулирующих программ, отдельные свойства незрелых клетокам. В широком смысле, атипизм является результатом действия онкобелков продуктов онкогенов, экспрессированных в неопластических клонах. В отличие от незрелых эмбриональных клеток, в неопластических утрачено действие антионкогенов и способность к апоптозу, нет потребности в ростовых факторах.
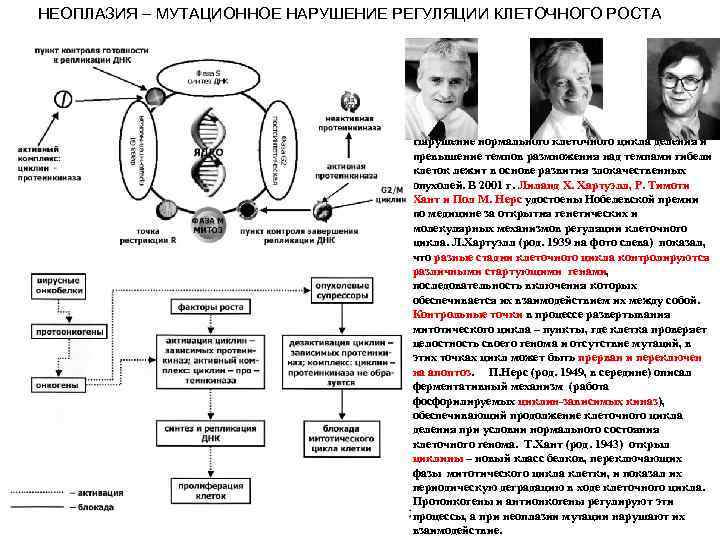
НЕОПЛАЗИЯ – МУТАЦИОННОЕ НАРУШЕНИЕ РЕГУЛЯЦИИ КЛЕТОЧНОГО РОСТА Нарушение нормального клеточного цикла деления и превышение темпов размножения над темпами гибели клеток лежит в основе развития злокачественных опухолей. В 2001 г. Лиланд Х. Хартуэлл, Р. Тимоти Хант и Пол М. Нерс удостоены Нобелевской премии по медицине за открытия генетических и молекулярных механизмов регуляции клеточного цикла. Л. Хартуэлл (род. 1939 на фото слева) показал, что разные стадии клеточного цикла контролируются различными стартующими генами, последовательность включения которых обеспечивается их взаимодействием их между собой. Контрольные точки в процессе развертывания митотического цикла – пункты, где клетка проверяет целостность своего генома и отсутствие мутаций, в этих точках цикл может быть прерван и переключен на апоптоз. П. Нерс (род. 1949, в середине) описал ферментативный механизм (работа фосфорилируемых циклин зависимых киназ), обеспечивающий продолжение клеточного цикла деления при условии нормального состояния клеточного генома. Т. Хант (род. 1943) открыл циклины – новый класс белков, переключающих фазы митотического цикла клетки, и показал их периодическую деградацию в ходе клеточного цикла. Протонкогены и антионкогены регулируют эти процессы, а при неоплазии мутации нарушают их взаимодействие.
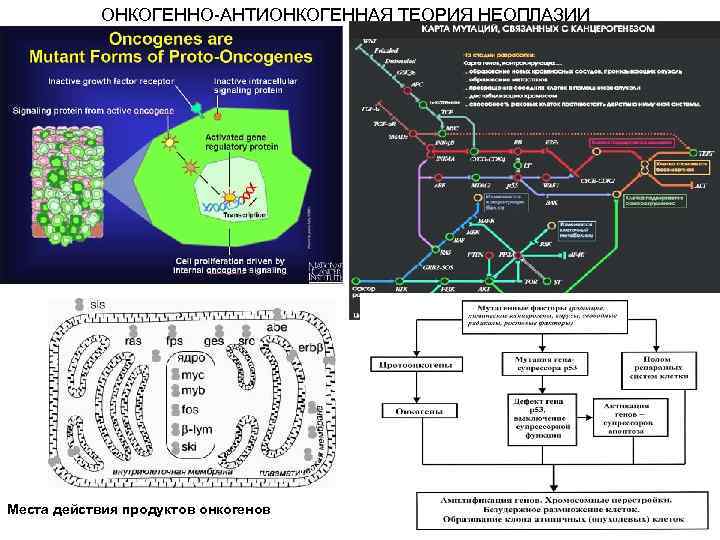
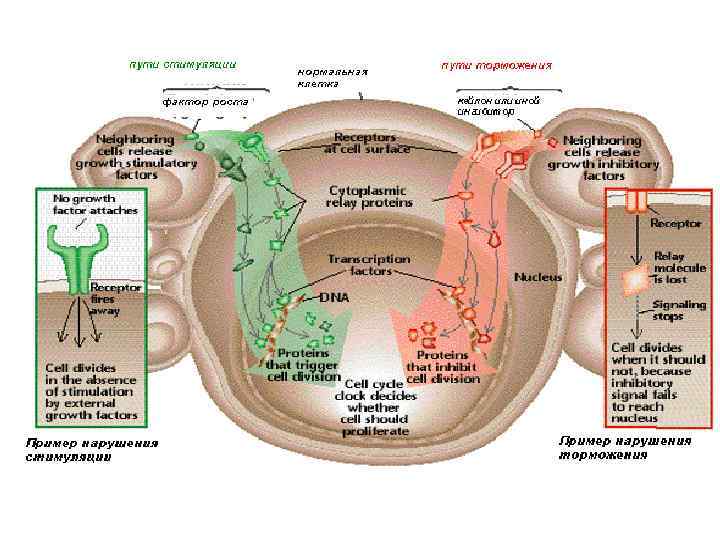
ОНКОГЕННО-АНТИОНКОГЕННАЯ ТЕОРИЯ НЕОПЛАЗИИ Места действия продуктов онкогенов
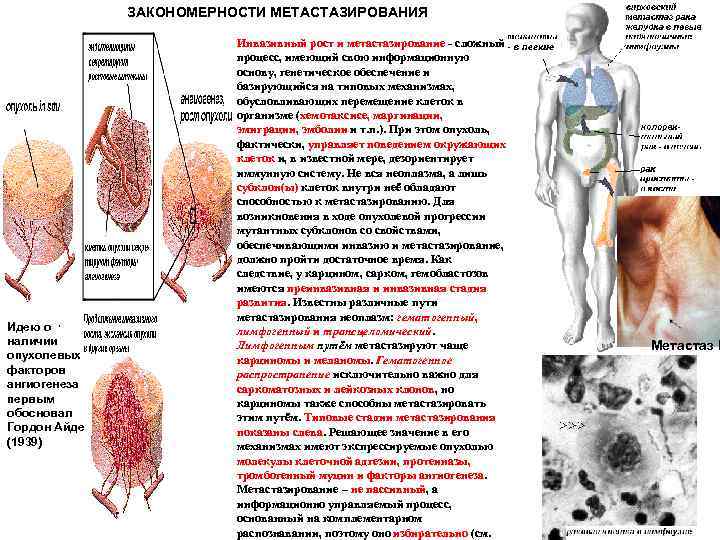
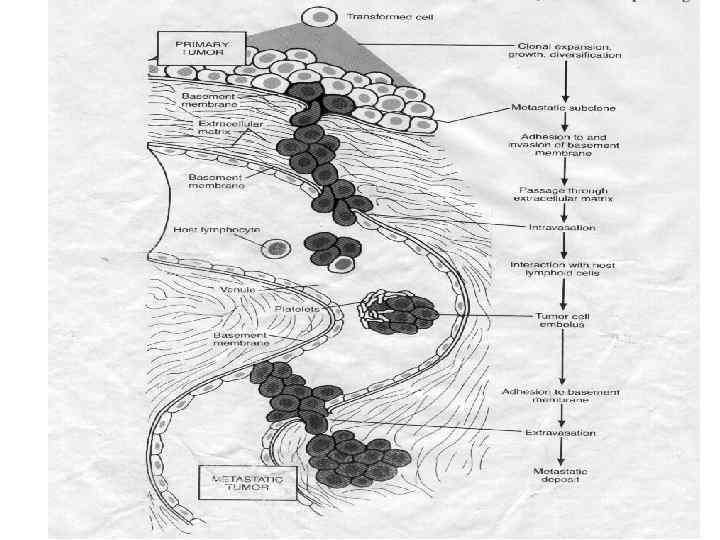
ЗАКОНОМЕРНОСТИ МЕТАСТАЗИРОВАНИЯ Идею о наличии опухолевых факторов ангиогенеза первым обосновал Гордон Айде (1939) Инвазивный рост и метастазирование сложный процесс, имеющий свою информационную основу, генетическое обеспечение и базирующийся на типовых механизмах, обусловливающих перемещение клеток в организме (хемотаксисе, маргинации, эмиграции, эмболии и т. п. ). При этом опухоль, фактически, управляет поведением окружающих клеток и, в известной мере, дезориентирует иммунную систему. Не вся неоплазма, а лишь субклон(ы) клеток внутри неё обладают способностью к метастазированию. Для возникновения в ходе опухолевой прогрессии мутантных субклонов со свойствами, обеспечивающими инвазию и метастазирование, должно пройти достаточное время. Как следствие, у карцином, сарком, гемобластозов имеются преинвазивная и инвазивная стадия развития. Известны различные пути метастазирования неоплазм: гематогенный, лимфогенный и трансцеломический. Лимфогенным путём метастазируют чаще карциномы и меланомы. Гематогенное распространение исключительно важно для саркоматозных и лейкозных клонов, но карциномы также способны метастазировать этим путём. Типовые стадии метастазирования показаны слева. Решающее значение в его механизмах имеют экспрессируемые опухолью молекулы клеточной адгезии, протеиназы, тромбогенный муцин и факторы ангиогенеза. Метастазирование – не пассивный, а информационно управляемый процесс, основанный на комплементарном распознавании, поэтому оно избирательно (см. Метастаз В
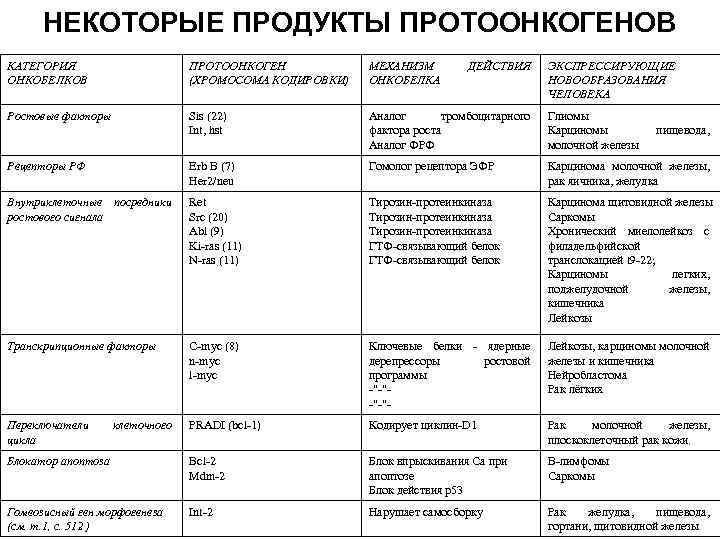
НЕКОТОРЫЕ ПРОДУКТЫ ПРОТООНКОГЕНОВ КАТЕГОРИЯ ОНКОБЕЛКОВ ПРОТООНКОГЕН (ХРОМОСОМА КОДИРОВКИ) МЕХАНИЗМ ОНКОБЕЛКА Ростовые факторы Sis (22) Int, hst Аналог тромбоцитарного фактора роста Аналог ФРФ Глиомы Карциномы молочной железы Рецепторы РФ Erb B (7) Her 2/neu Гомолог рецептора ЭФР Карцинома молочной железы, рак яичника, желудка Внутриклеточные посредники ростового сигнала Ret Src (20) Abl (9) Ki-ras (11) N-ras (11) Тирозин-протеинкиназа ГТФ-связывающий белок Карцинома щитовидной железы Саркомы Хронический миелолейкоз с филадельфийской транслокацией t 9 -22; Карциномы легких, поджелудочной железы, кишечника Лейкозы Транскрипционные факторы С-myc (8) n-myc l-myc Ключевые белки - ядерные дерепрессоры ростовой программы -"-"- Лейкозы, карциномы молочной железы и кишечника Нейробластома Рак лёгких Переключатели цикла PRADI (bcl-1) Кодирует циклин-D 1 Рак молочной железы, плоскоклеточный рак кожи. Блокатор апоптоза Bcl-2 Mdm-2 Блок впрыскивания Ca при апоптозе Блок действия р53 В-лимфомы Саркомы Гомеозисный ген морфогенеза (см. т. 1, с. 512 ) Int-2 Нарушает самосборку Рак желудка, пищевода, гортани, щитовидной железы клеточного ДЕЙСТВИЯ ЭКСПРЕССИРУЮЩИЕ НОВООБРАЗОВАНИЯ ЧЕЛОВЕКА пищевода,
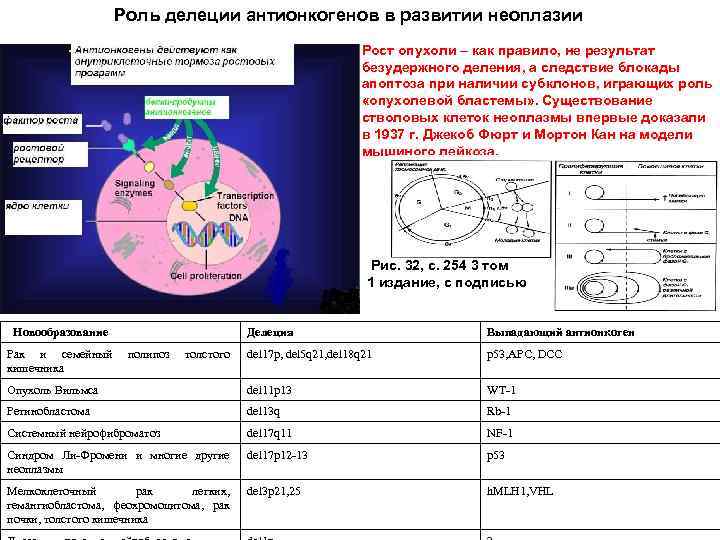
Роль делеции антионкогенов в развитии неоплазии Рост опухоли – как правило, не результат безудержного деления, а следствие блокады апоптоза при наличии субклонов, играющих роль «опухолевой бластемы» . Существование стволовых клеток неоплазмы впервые доказали в 1937 г. Джекоб Фюрт и Мортон Кан на модели мышиного лейкоза. Рис. 32, с. 254 3 том 1 издание, с подписью Новообразование Делеция Выпадающий антионкоген del 17 p, del 5 q 21, del 18 q 21 р53, APC, DCC Опухоль Вильмса del 11 p 13 WT-1 Ретинобластома del 13 q Rb-1 Системный нейрофиброматоз del 17 q 11 NF-1 Синдром Ли-Фромени и многие другие неоплазмы del 17 p 12 -13 р53 Мелкоклеточный рак легких, гемангиобластома, феохромоцитома, рак почки, толстого кишечника del 3 р21, 25 h. MLH 1, VHL Рак и семейный кишечника полипоз толстого
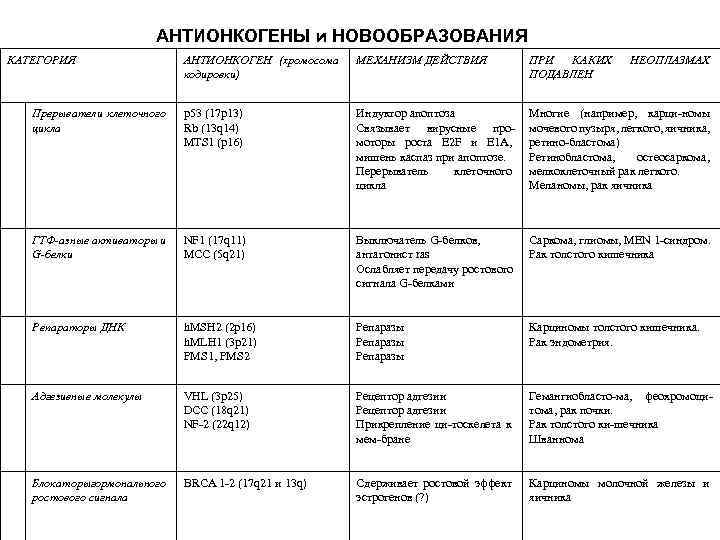
АНТИОНКОГЕНЫ и НОВООБРАЗОВАНИЯ КАТЕГОРИЯ АНТИОНКОГЕН (хромосома кодировки) МЕХАНИЗМ ДЕЙСТВИЯ ПРИ КАКИХ ПОДАВЛЕН Прерыватели клеточного цикла р53 (17 р13) Rb (13 q 14) MTS 1 (p 16) Индуктор апоптоза Связывает вирусные промоторы роста Е 2 F и E 1 A, мишень каспаз при апоптозе. Перерыватель клеточного цикла Многие (например, карци-номы мочевого пузыря, легкого, яичника, ретино-бластома) Ретинобластома, остеосаркома, мелкоклеточный рак легкого. Меланомы, рак яичника ГТФ-азные активаторы и G-белки NF 1 (17 q 11) MCC (5 q 21) Выключатель G-белков, антагонист ras Ослабляет передачу ростового сигнала G-белками Саркома, глиомы, MEN 1 -синдром. Рак толстого кишечника Репараторы ДНК h. MSH 2 (2 р16) h. MLH 1 (3 p 21) PMS 1, PMS 2 Репаразы Карциномы толстого кишечника. Рак эндометрия. Адгезивные молекулы VHL (3 p 25) DСС (18 q 21) NF-2 (22 q 12) Рецептор адгезии Прикрепление ци-тоскелета к мем-бране Гемангиобласто-ма, феохромоцитома, рак почки. Рак толстого ки-шечника Шваннома Блокаторыгормонального ростового сигнала BRCA 1 -2 (17 q 21 и 13 q) Сдерживает ростовой эффект эстрогенов (? ) Карциномы молочной железы и яичника НЕОПЛАЗМАХ
Лимфангиома И сами опухолевые клетки и борющаяся с ними иммунная система вырабатывают сигнальные молекулы – цитокины, нарушающие в организме обмен веществ и физиологические функции, что ведет к «паранеопластическим явлениям» : раковая кахексия, мигрирующий тромбофлебит, остеопороз и др. . Неопластические клетки с их атиаичным метаболизмом – ловушки глюкозы, аспарагиновой кислоты и биогенного азота. Этим и объясняется вредоносное действие неоплазмы, как «эндогенного колоииального паразита» (М. Мирча), на организм носителя опухоли.
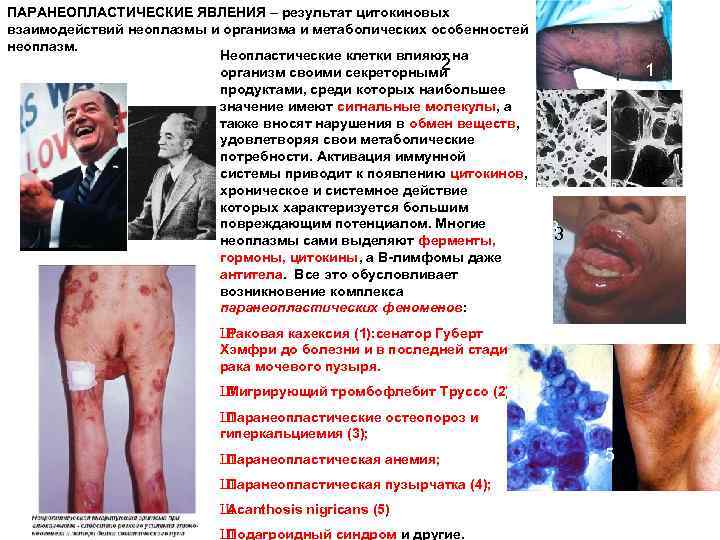
ПАРАНЕОПЛАСТИЧЕСКИЕ ЯВЛЕНИЯ – результат цитокиновых взаимодействий неоплазмы и организма и метаболических особенностей неоплазм. Неопластические клетки влияют на 2 организм своими секреторными продуктами, среди которых наибольшее значение имеют сигнальные молекулы, а также вносят нарушения в обмен веществ, удовлетворяя свои метаболические потребности. Активация иммунной системы приводит к появлению цитокинов, хроническое и системное действие которых характеризуется большим повреждающим потенциалом. Многие неоплазмы сами выделяют ферменты, гормоны, цитокины, а В-лимфомы даже антитела. Все это обусловливает возникновение комплекса паранеопластических феноменов: 1 1 1 3 3 4 Ш Раковая кахексия (1): сенатор Губерт Хэмфри до болезни и в последней стадии рака мочевого пузыря. Ш Мигрирующий тромбофлебит Труссо (2); Ш Паранеопластические остеопороз и гиперкальциемия (3); Ш Паранеопластическая анемия; Ш Паранеопластическая пузырчатка (4); Ш Acanthosis nigricans (5) Ш Подагроидный синдром и другие. 5
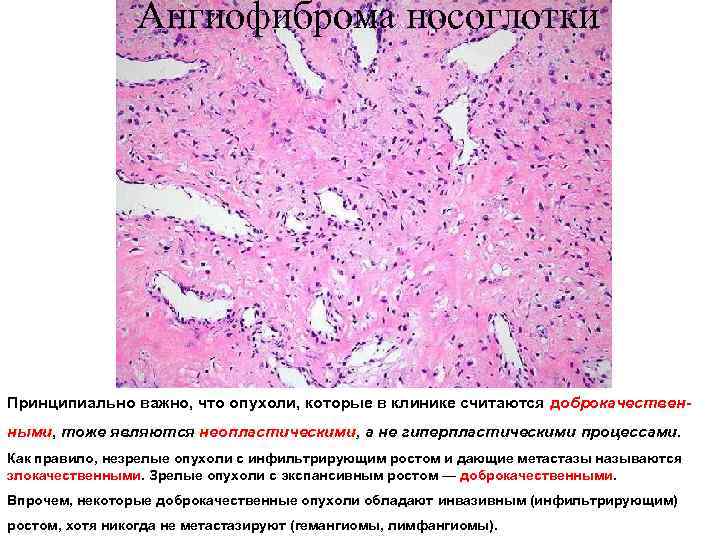
Ангиофиброма носоглотки Принципиально важно, что опухоли, которые в клинике считаются доброкачественными, тоже являются неопластическими, а не гиперпластическими процессами. Как правило, незрелые опухоли с инфильтрирующим ростом и дающие метастазы называются злокачественными. Зрелые опухоли с экспансивным ростом — доброкачественными. Впрочем, некоторые доброкачественные опухоли обладают инвазивным (инфильтрирующим) ростом, хотя никогда не метастазируют (гемангиомы, лимфангиомы).
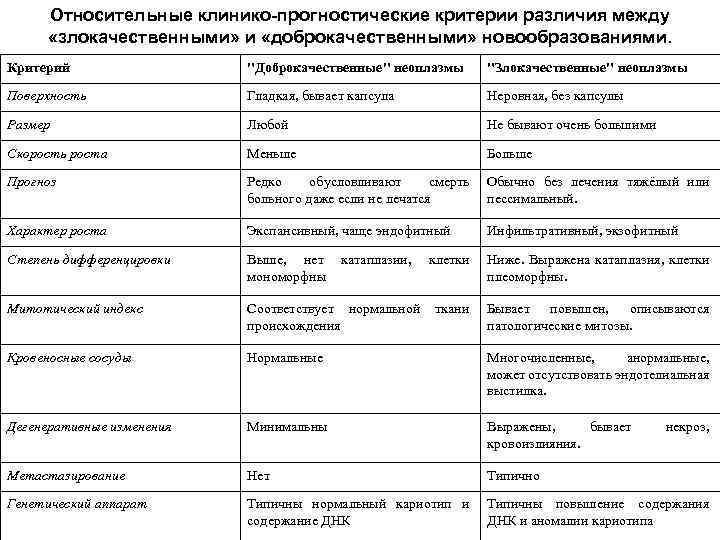
Относительные клинико-прогностические критерии различия между «злокачественными» и «доброкачественными» новообразованиями. Критерий "Доброкачественные" неоплазмы "Злокачественные" неоплазмы Поверхность Гладкая, бывает капсула Неровная, без капсулы Размер Любой Не бывают очень большими Скорость роста Меньше Больше Прогноз Редко обусловливают смерть больного даже если не лечатся Обычно без лечения тяжёлый или пессимальный. Характер роста Экспансивный, чаще эндофитный Инфильтративный, экзофитный Степень дифференцировки Выше, нет мономорфны клетки Ниже. Выражена катаплазия, клетки плеоморфны. Митотический индекс Соответствует нормальной ткани происхождения Бывает повышен, описываются патологические митозы. Кровеносные сосуды Нормальные Многочисленные, анормальные, может отсутствовать эндотелиальная выстилка. Дегенеративные изменения Минимальны Выражены, бывает кровоизлияния. Метастазирование Нет Типично Генетический аппарат Типичны нормальный кариотип и содержание ДНК Типичны повышение содержания ДНК и аномалии кариотипа катаплазии, некроз,
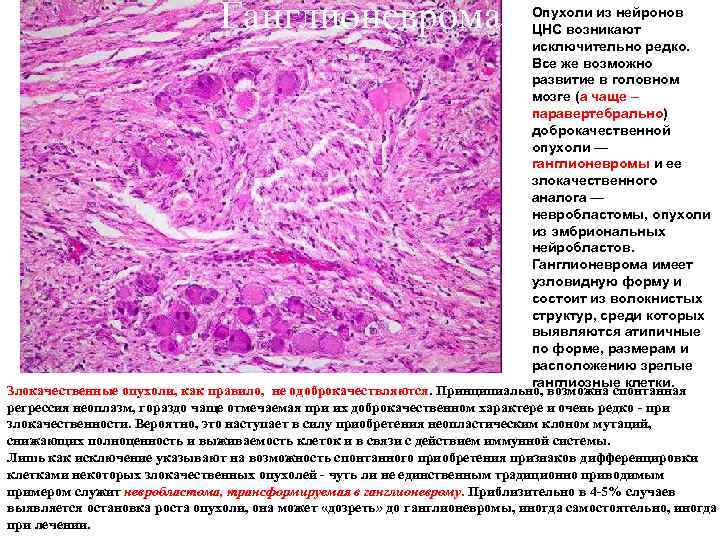
Ганглионеврома Опухоли из нейронов ЦНС возникают исключительно редко. Все же возможно развитие в головном мозге (а чаще – паравертебрально) доброкачественной опухоли — ганглионевромы и ее злокачественного аналога — невробластомы, опухоли из эмбриональных нейробластов. Ганглионеврома имеет узловидную форму и состоит из волокнистых структур, среди которых выявляются атипичные по форме, размерам и расположению зрелые ганглиозные клетки. Злокачественные опухоли, как правило, не одоброкачествляются. Принципиально, возможна спонтанная регрессия неоплазм, гораздо чаще отмечаемая при их доброкачественном характере и очень редко при злокачественности. Вероятно, это наступает в силу приобретения неопластическим клоном мутаций, снижающих полноценность и выживаемость клеток и в связи с действием иммунной системы. Лишь как исключение указывают на возможность спонтанного приобретения признаков дифференцировки клетками некоторых злокачественных опухолей чуть ли не единственным традиционно приводимым примером служит невробластома, трансформируемая в ганглионеврому. Приблизительно в 4 5% случаев выявляется остановка роста опухоли, она может «дозреть» до ганглионевромы, иногда самостоятельно, иногда при лечении.
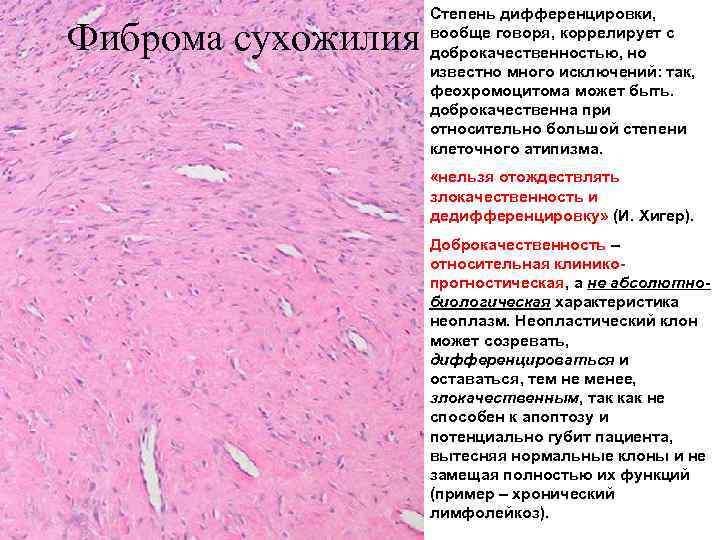
Фиброма сухожилия Степень дифференцировки, вообще говоря, коррелирует с доброкачественностью, но известно много исключений: так, феохромоцитома может быть. доброкачественна при относительно большой степени клеточного атипизма. «нельзя отождествлять злокачественность и дедифференцировку» (И. Хигер). Доброкачественность – относительная клиникопрогностическая, а не абсолютнобиологическая характеристика неоплазм. Неопластический клон может созревать, дифференцироваться и оставаться, тем не менее, злокачественным, так как не способен к апоптозу и потенциально губит пациента, вытесняя нормальные клоны и не замещая полностью их функций (пример – хронический лимфолейкоз).
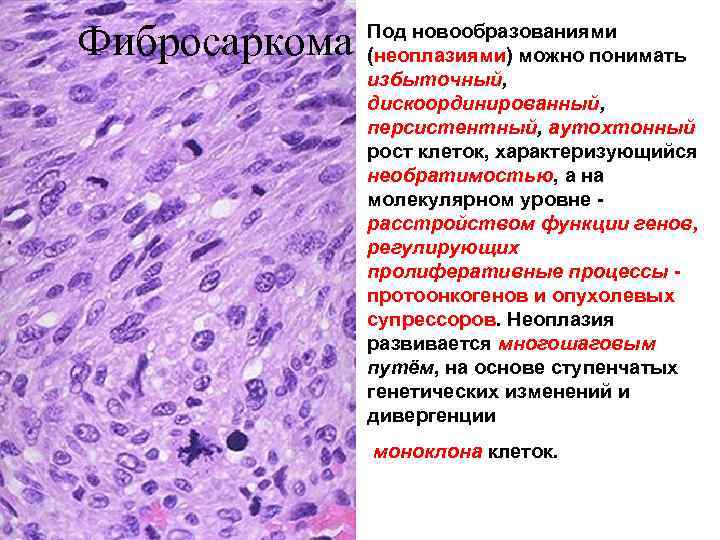
Фибросаркома Под новообразованиями (неоплазиями) можно понимать избыточный, дискоординированный, персистентный, аутохтонный рост клеток, характеризующийся необратимостью, а на молекулярном уровне расстройством функции генов, регулирующих пролиферативные процессы протоонкогенов и опухолевых супрессоров. Неоплазия развивается многошаговым путём, на основе ступенчатых генетических изменений и дивергенции моноклона клеток.
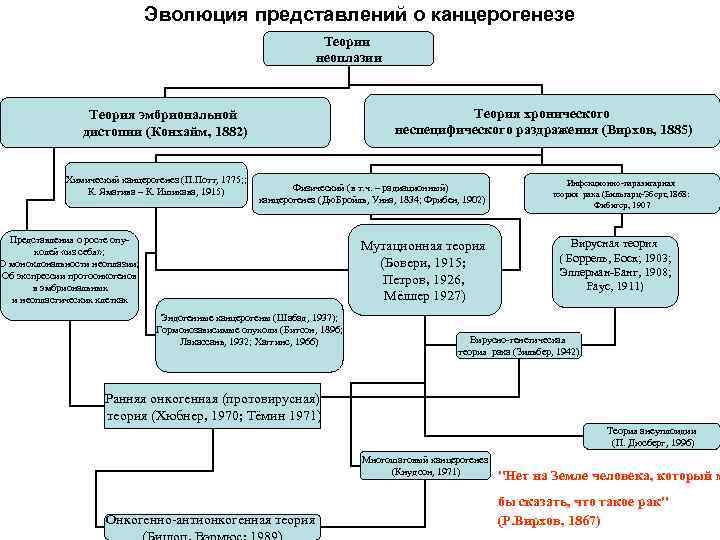
Эволюция представлений о канцерогенезе Теории неоплазии Теория хронического неспецифического раздражения (Вирхов, 1885) Теория эмбриональной дистопии (Конхайм, 1882) Химический канцерогенез (П. Потт, 1775; ; К. Ямагива – К. Ишикава, 1915) Физический (в т. ч. – радиационный) канцерогенез (Дю. Бройль, Унна, 1834; Фрибен, 1902) Представления о росте опухолей «из себя» ; О моноклональности неоплазии; Об экспрессии протоонкогенов в эмбриональных и неопластических клетках Мутационная теория (Бовери, 1915; Петров, 1926, Мёллер 1927) Эндогенные канцерогены (Шабад, 1937); Гормонозависимые опухоли (Битсон, 1896; Лакассань, 1932; Хаггинс, 1966) Инфекционно-паразитарная теория рака (Бильгарц-Эберт, 1868: Фибигер, 1907 Вирусная теория ( Боррель, Боск; 1903; Эллерман-Банг, 1908; Раус, 1911) Вирусно-генетическая теория рака (Зильбер, 1942) Ранняя онкогенная (протовирусная) теория (Хюбнер, 1970; Тёмин 1971) Теория анеуплоидии (П. Дюсберг, 1996) Многошаговый канцерогенез (Кнудсон, 1971) Онкогенно-антионкогенная теория "Нет на Земле человека, который м бы сказать, что такое рак" (Р. Вирхов, 1867)
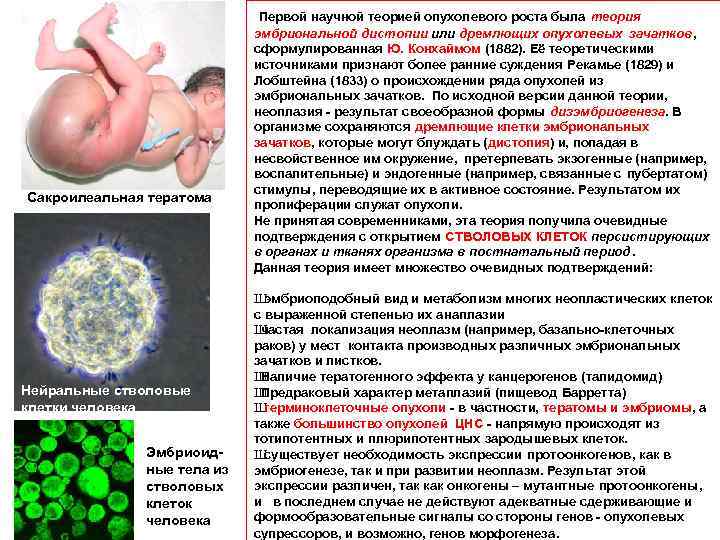
Первой научной теорией опухолевого роста была теория Сакроилеальная тератома Нейральные стволовые клетки человека Эмбриоидные тела из стволовых клеток человека эмбриональной дистопии или дремлющих опухолевых зачатков, сформулированная Ю. Конхаймом (1882). Её теоретическими источниками признают более ранние суждения Рекамье (1829) и Лобштейна (1833) о происхождении ряда опухолей из эмбриональных зачатков. По исходной версии данной теории, неоплазия - результат своеобразной формы дизэмбриогенеза. В организме сохраняются дремлющие клетки эмбриональных зачатков, которые могут блуждать (дистопия) и, попадая в несвойственное им окружение, претерпевать экзогенные (например, воспалительные) и эндогенные (например, связанные с пубертатом) стимулы, переводящие их в активное состояние. Результатом их пролиферации служат опухоли. Не принятая современниками, эта теория получила очевидные подтверждения с открытием СТВОЛОВЫХ КЛЕТОК персистирующих в органах и тканях организма в постнатальный период. Данная теория имеет множество очевидных подтверждений: Ш эмбриоподобный вид и метаболизм многих неопластических клеток с выраженной степенью их анаплазии Ш частая локализация неоплазм (например, базально-клеточных раков) у мест контакта производных различных эмбриональных зачатков и листков. Ш Наличие тератогенного эффекта у канцерогенов (талидомид) Ш Предраковый характер метаплазий (пищевод Барретта) Ш герминоклеточные опухоли - в частности, тератомы и эмбриомы, а также большинство опухолей ЦНС - напрямую происходят из тотипотентных и плюрипотентных зародышевых клеток. Ш существует необходимость экспрессии протоонкогенов, как в эмбриогенезе, так и при развитии неоплазм. Результат этой экспрессии различен, так как онкогены – мутантные протоонкогены, и в последнем случае не действуют адекватные сдерживающие и формообразовательные сигналы со стороны генов - опухолевых супрессоров, и возможно, генов морфогенеза.

Канадский патолог Джон Джордж Адами (1862 1926), основываясь на теории эмбриональной дистопии, предложил в 1912 г. классификацию опухолей, актуальную доныне. 3. Опухоли из дифференцированных клеток, утративших часть или все признаки дифференцировки и подвергшихся анаплазии, составляют большинство новообразований у взрослых. 1. Из прогаметных тотипотентных клеток, то есть клеток, принципиально способных дифференцироваться по любому пути. Тотипотентные клетки при нарушении генетической регуляции их роста дают неоплазмы, клетки которых могут дифференцироваться "во что угодно" точнее, в любую ткань зародыша и в ткань провизорных органов (зрелые тератомы, незрелые тератомы). Незрелые тератомы иногда, практически, не обладают признаками дифференцировки, сохраняя свойства примитивных прогамет (семинома или герминома). Чаще они проявляют начальную трофобластическую дифференцировку. К этой подгруппе относится хориокарцинома (направление дифференцировки в цитотрофобласт и синцитиотрофобласт). При эндодермальном направлении начальной дифференцировки образуется карцинома желточного мешка, содержащая его примитивные клетки. Начальная эктодермальная дифференцировка тотипотентных неопластических клеток ведёт к формированию эмбриокарциномы, содержащей солидные массы малодифференцированных эпителиальных клеток. 2. Опухоли из эмбриональных полипотентных (стволовых) клеток возникают из элементов органных зачатков. Опухоли данной группы носят название эмбриомы или бластомы. Они всегда исключительно злокачественны и именуются по названию соответствующего органного зачатка (ретинобластома, нефробластома – ОПУХОЛЬ ВИЛЬМСА, гепатобластома, невробластома, медуллобластома, пинеобластома, эмбриональная рабдомиосаркома и др. ). Бластомы сходны между собой по типу своих клеток, но часто содержат отдельные признаки органоподобной структуры например, трубочки в нефробластоме или ганглионарные клетки в невробластоме.
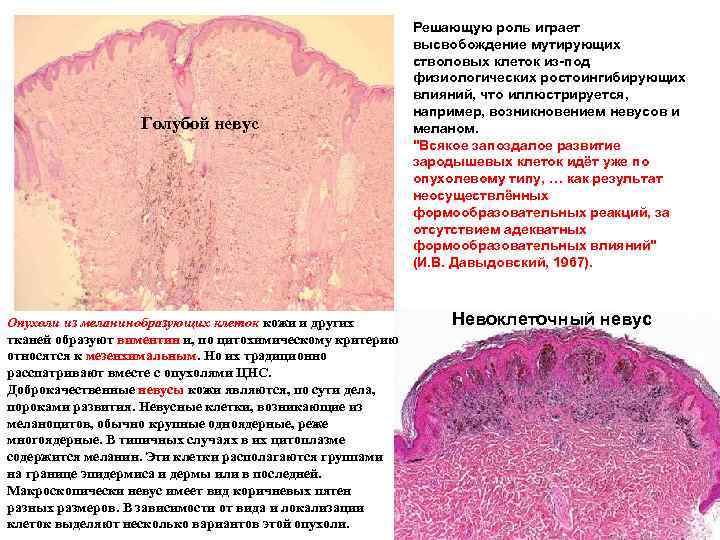
Голубой невус Опухоли из меланинобразующих клеток кожи и других тканей образуют виментин и, по цитохимическому критерию относятся к мезенхимальным. Но их традиционно расспатривают вместе с опухолями ЦНС. Доброкачественные невусы кожи являются, по сути дела, пороками развития. Невусные клетки, возникающие из меланоцитов, обычно крупные одноядерные, реже многоядерные. В типичных случаях в их цитоплазме содержится меланин. Эти клетки располагаются группами на границе эпидермиса и дермы или в последней. Макроскопически невус имеет вид коричневых пятен разных размеров. В зависимости от вида и локализации клеток выделяют несколько вариантов этой опухоли. Решающую роль играет высвобождение мутирующих стволовых клеток из-под физиологических ростоингибирующих влияний, что иллюстрируется, например, возникновением невусов и меланом. "Всякое запоздалое развитие зародышевых клеток идёт уже по опухолевому типу, … как результат неосуществлённых формообразовательных реакций, за отсутствием адекватных формообразовательных влияний" (И. В. Давыдовский, 1967). Невоклеточный невус
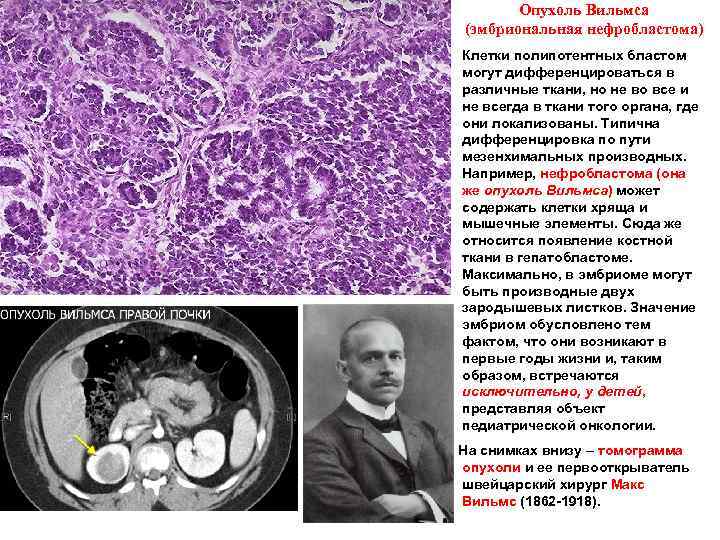
Опухоль Вильмса (эмбриональная нефробластома) Клетки полипотентных бластом могут дифференцироваться в различные ткани, но не во все и не всегда в ткани того органа, где они локализованы. Типична дифференцировка по пути мезенхимальных производных. Например, нефробластома (она же опухоль Вильмса) может содержать клетки хряща и мышечные элементы. Сюда же относится появление костной ткани в гепатобластоме. Максимально, в эмбриоме могут быть производные двух зародышевых листков. Значение эмбриом обусловлено тем фактом, что они возникают в первые годы жизни и, таким образом, встречаются исключительно, у детей, представляя объект педиатрической онкологии. На снимках внизу – томограмма опухоли и ее первооткрыватель швейцарский хирург Макс Вильмс (1862 -1918).
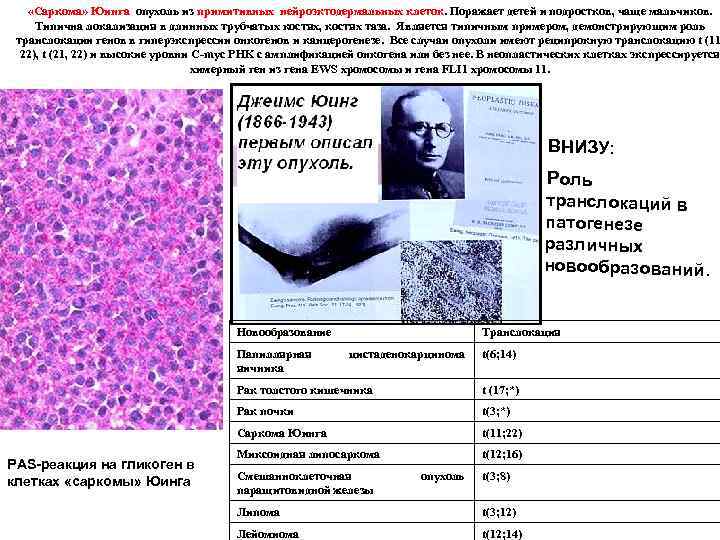
«Саркома» Юинга опухоль из примитивных нейроэктодермальных клеток. Поражает детей и подростков, чаще мальчиков. Типична локализация в длинных трубчатых костях, костях таза. Является типичным примером, демонстрирующим роль транслокации генов в гиперэкспрессии онкогенов и канцерогенезе. Все случаи опухоли имеют реципрокную транслокацию t (11 22), t (21, 22) и высокие уровни C myc РHK с амплификацией онкогена или без нее. В неопластических клетках экспрессируется химерный ген из гена EWS хромосомы и гена FLI 1 хромосомы 11. ВНИЗУ: Роль транслокаций в патогенезе различных новообразований. Новообразование Папиллярная яичника Транслокация цистаденокарцинома t(6; 14) Рак толстого кишечника Рак почки t(3; *) Cаркома Юинга PAS-реакция на гликоген в клетках «саркомы» Юинга t (17; *) t(11; 22) Миксоидная липосаркома t(12; 16) Смешанноклеточная паращитовидной железы опухоль t(3; 8) Липома t(3; 12) Лейомиома t(12; 14)

ТЕОРИЯ НЕСПЕЦИФИЧЕСКОГО РАЗДРАЖЕНИЯ Р. ВИРХОВА "Если раздражение незначительно, то и последствия его будут простейшие: хроническое воспаление, гиперплазия, гипертрофия. Специфические же формы проявляются только при особой форме или силе раздражения. Опыт же учит, что именно самые злокачественные опухоли, чаще всего, встречаются на таких органах, которые более всего подвергаются внешним раздражениям, имеют незащищённые поверхности, все же другие органы, не представляющие таких условий, редко заболевают…. Природа раздражения различна, смотря по тому, влияет ли особое химическое вещество или механические раздражители. Направление же, в котором совершается развитие новых тканей вследствие раздражений, в свою очередь, неодинаково, во -первых, вследствие различия самих тканей, подвергшихся раздражению, во-вторых, по влияющему веществу, могущему определённым образом оказывать химическое воздействие, вследствие которого раздражаемая ткань, подобно тому, как это происходит при действии семени на яйцо, приобретает совершенно особые качества « (1885) Всё развитие теории раздражения от первоначального представления о связи рака с механическим раздражением, через признание роли химических и иных немеханических повреждающих факторов как канцерогенов, пришло к идее необходимости генетического повреждения, как единой основы патогенеза полиэтиологических неоплазий. И разве не содержится эта генеральная линия уже в первой формулировке теории, данной Вирховым? Ведь процессы, происхдящие при действии семени на яйцо есть процессы генетические, связанные с неокомбинаторикой генов !
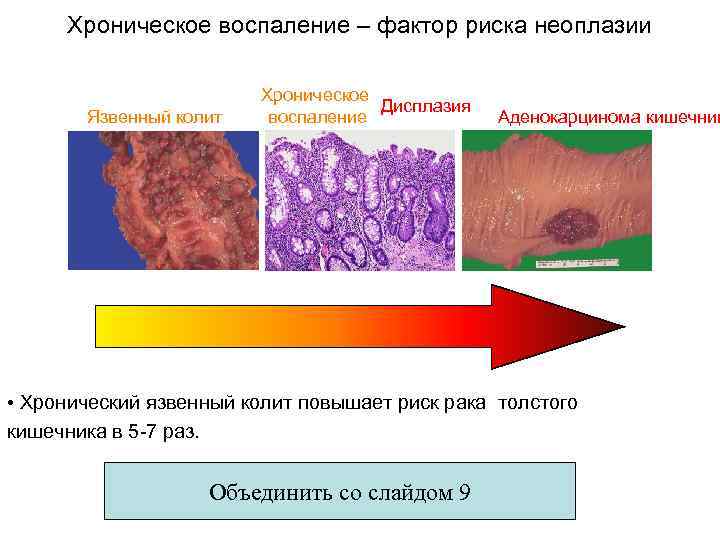
Хроническое воспаление – фактор риска неоплазии Язвенный колит Хроническое Дисплазия воспаление Аденокарцинома кишечник • Хронический язвенный колит повышает риск рака толстого кишечника в 5 -7 раз. Объединить со слайдом 9
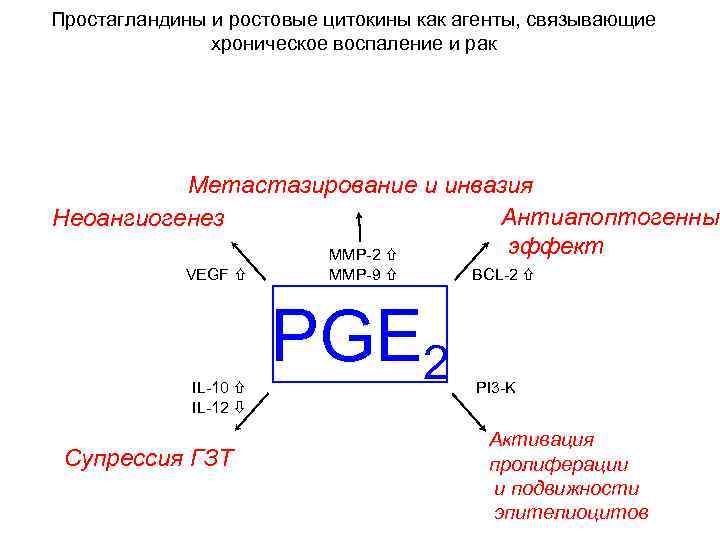
Простагландины и ростовые цитокины как агенты, связывающие хроническое воспаление и рак Метастазирование и инвазия Антиапоптогенный Неоангиогенез эффект MMP-2 VEGF IL-10 IL-12 Супрессия ГЗТ MMP-9 PGE 2 BCL-2 PI 3 -K Активация пролиферации и подвижности эпителиоцитов
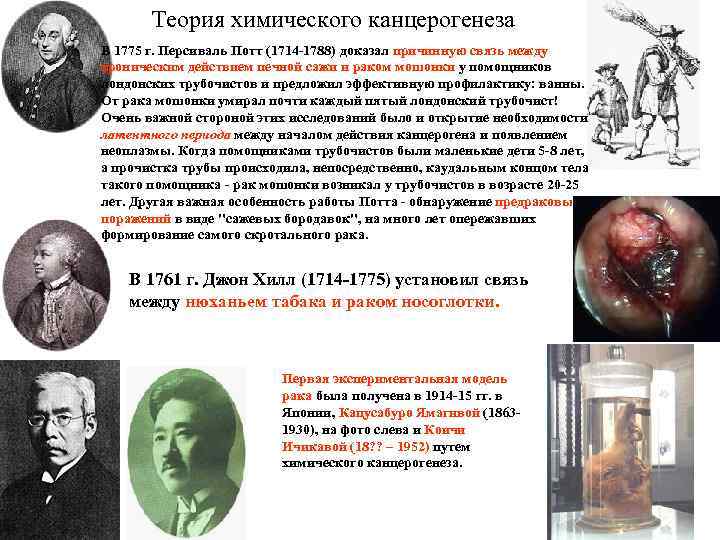
Теория химического канцерогенеза В 1775 г. Персиваль Потт (1714 1788) доказал причинную связь между хроническим действием печной сажи и раком мошонки у помощников лондонских трубочистов и предложил эффективную профилактику: ванны. От рака мошонки умирал почти каждый пятый лондонский трубочист! Очень важной стороной этих исследований было и открытие необходимости латентного периода между началом действия канцерогена и появлением неоплазмы. Когда помощниками трубочистов были маленькие дети 5 8 лет, а прочистка трубы происходила, непосредственно, каудальным концом тела такого помощника рак мошонки возникал у трубочистов в возрасте 20 25 лет. Другая важная особенность работы Потта обнаружение предраковых поражений в виде "сажевых бородавок", на много лет опережавших формирование самого скротального рака. В 1761 г. Джон Хилл (1714 1775) установил связь между нюханьем табака и раком носоглотки. Первая экспериментальная модель рака была получена в 1914 15 гг. в Японии, Кацусабуро Ямагивой (1863 1930), на фото слева и Коичи Ичикавой (18? ? – 1952) путем химического канцерогенеза.

Экспериментальная модель химического канцерогенеза В 1914 -1915 гг. Кацусабуро Ямагива и Коичи Ичикава получили экспериментальную модель папилломы и плоскоклеточного рака у кроликов, применяя хронические аппликации каменнноугольной смолы. Повторные многократные аппликации дёгтя или гудрона на кожу уха вызывали сначала воспаление и гиперплазию в виде гиперкератоза, затем (к 70 дню) формировалась доброкачественная папиллома, а при продолжении аппликаций - и плоскоклеточная карцинома кожи уха, вначале - неинвазивная, а затем - инвазивнометастазирующая. Весь процесс занимал от 1 до 6 месяцев, а озлокачествление наблюдалось в интервале от 103 до 506 дней. Характерным являлся длительный латентный период и многошаговая постепенность перехода от реактивных изменений и гиперплазии к неоплазии с возрастающей злокачественностью. Японские авторы показали и возможность комбинированного действия
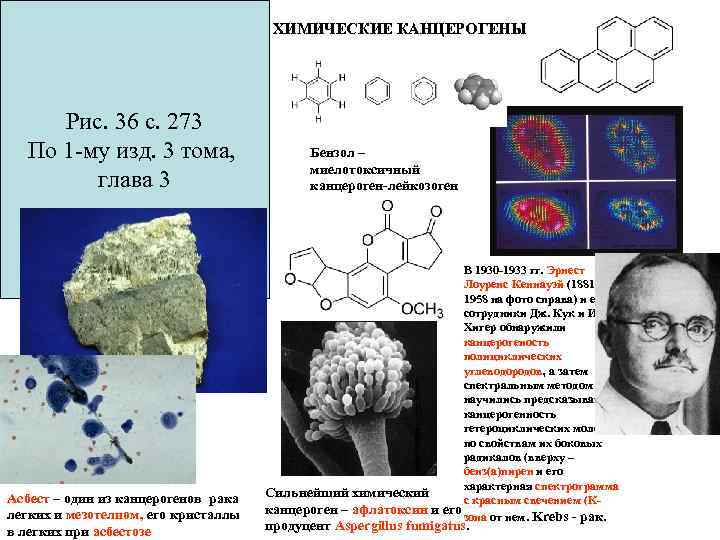
ХИМИЧЕСКИЕ КАНЦЕРОГЕНЫ Рис. 36 с. 273 По 1 -му изд. 3 тома, глава 3 Асбест – один из канцерогенов рака легких и мезотелиом, его кристаллы в легких при асбестозе Бензол – миелотоксичный канцероген лейкозоген В 1930 1933 гг. Эрнест Лоуренс Кеннауэй (1881 1958 на фото справа) и его сотрудники Дж. Кук и И. Хигер обнаружили канцерогеность полициклических углеводородов, а затем спектральным методом научились предсказывать канцерогенность гетероциклических молекул по свойствам их боковых радикалов (вверху – бенз(а)пирен и его характерная спектрограмма Сильнейший химический с красным свечением (K канцероген – афлатоксин и его зона от нем. Krebs рак. продуцент Aspergillus fumigatus.
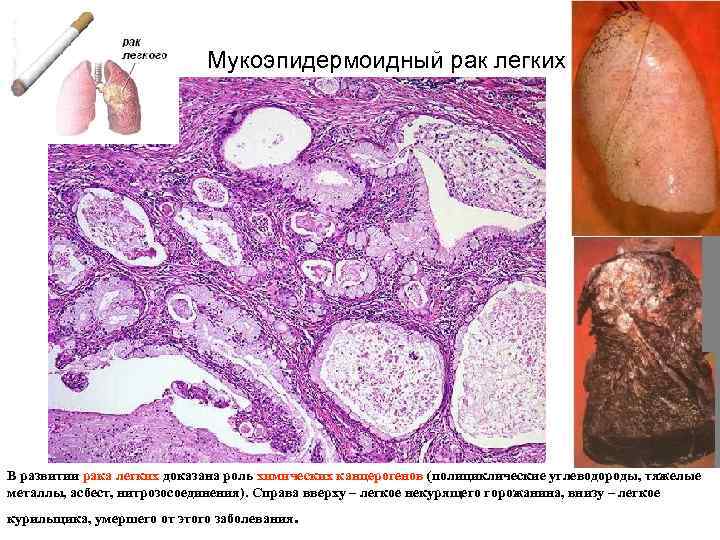
Мукоэпидермоидный рак легких В развитии рака легких доказана роль химических канцерогенов (полициклические углеводороды, тяжелые металлы, асбест, нитрозосоединения). Справа вверху – легкое некурящего горожанина, внизу – легкое курильщика, умершего от этого заболевания .

Основатель профпатологии Бернардо Рамаццини (1633 1714) первым указал на низкую частоту рака шейки матки и повышенную – рака молочных желез у монахинь и предположил, что это может быть результатом целибата. Эндогенный и гормонозависимый канцерогенез Британский хирург сэр Джордж Томас Битсон (1848 1933) успешно применил овариэктомию для замедления развития рака молочных желез (1896) В 1920 г. русский хирург Николай Александрович Вельяминов (1855 1920) предсказал гормонозависимость рака молочной железы. В 1932 г. Антуан Лакассань (1884 1971) получил модель рака молочных желез у самцов мышей под действием эстрогенного препарата фолликулина. В 1941 1953 гг. Чарльз Брентон Хаггинс (1901 1997) показал гормонозависимость рака В 1937 г. Леон Манусович Шабад ( 1902 1982) обратил внимание на простаты, обнаружил близость химической структуры важнейших экзогенных химических провоцирующую роль канцерогенов и естественных метаболитов организма так, андрогенов при этом метилхолантрен может быть получен из дезоксихолевой кислоты и, заболевании и успешно действительно, имеется в желчи и фекалиях человека. применил эстрогены для Канцерогеноподобные ароматические амины и индольные его терапии (Нобелевская соединения формируются при гниении белка, каловой премия по медицине аутоинтоксикации, фенилкетонурии. Шабад экспериментально 1966 г. ) показал канцерогенность некоторых эндогенных метаболитов.
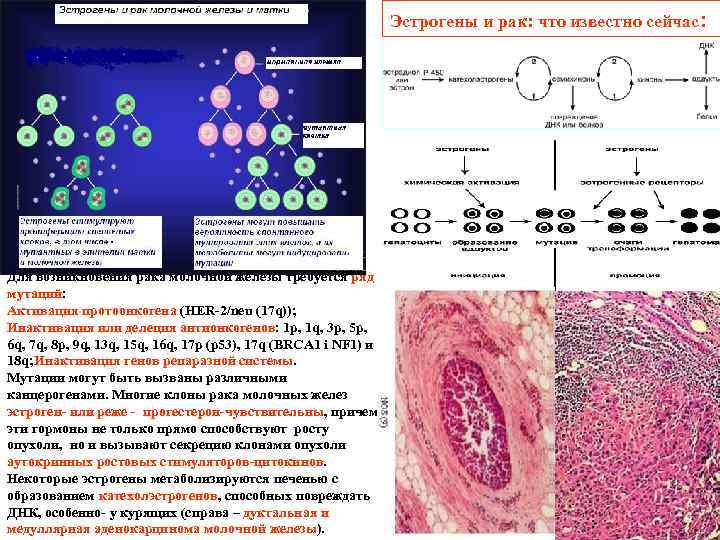
Эстрогены и рак: что известно сейчас: Для возникновения рака молочной железы требуется ряд мутаций: Активация протоонкогена (HER 2/neu (17 q)); Инактивация или делеция антионкогенов: 1 p, 1 q, 3 p, 5 p, 6 q, 7 q, 8 p, 9 q, 13 q, 15 q, 16 q, 17 p (p 53), 17 q (BRCA 1 i NF 1) и 18 q; Инактивация генов репаразной системы. Мутации могут быть вызваны различными канцерогенами. Многие клоны рака молочных желез эстроген или реже прогестерон чувствительны, причем эти гормоны не только прямо способствуют росту опухоли, но и вызывают секрецию клонами опухоли аутокринных ростовых стимуляторов цитокинов. Некоторые эстрогены метаболизируются печенью с образованием катехолэстрогенов, способных повреждать ДНК, особенно у курящих (справа – дуктальная и медуллярная аденокарцинома молочной железы).
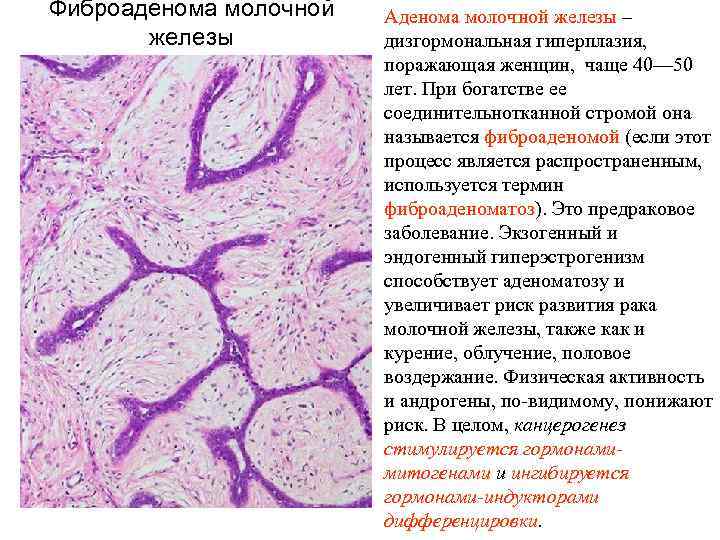
Фиброаденома молочной железы Аденома молочной железы – дизгормональная гиперплазия, поражающая женщин, чаще 40— 50 лет. При богатстве ее соединительнотканной стромой она называется фиброаденомой (если этот процесс является распространенным, используется термин фиброаденоматоз). Это предраковое заболевание. Экзогенный и эндогенный гиперэстрогенизм способствует аденоматозу и увеличивает риск развития рака молочной железы, также как и курение, облучение, половое воздержание. Физическая активность и андрогены, по-видимому, понижают риск. В целом, канцерогенез стимулируется гормонамимитогенами и ингибируется гормонами-индукторами дифференцировки.

Теория паразитарно-инфекционного канцерогенеза Впервые идею об инфекционной (точнее инвазионной) этиологии опухолей выдвинули, вероятно, исследователи бильгарциоза – Теодор Максимилиан Бильгарц (1851) и Карл Йозеф Эберт (1868). Бильгарциоз (разновидность шистоматоза) древнейшее паразитарное заболевание, вызываемое печёночной двуусткой Shistomum haematoium Bilharzii (справа). На месте локализации яиц двуустки (легкие, печень, толстая кишка, мочевой пузырь) с высокой К. Й. Эберт частотой отмечается рак и саркомы (1835 1926) Т. М. Бильгарц (1825 1862) . Амеде Боррель (1867 1936) в 1903 г. первым высказал идею о вирусной этиологии рака, он же установил связь цистицеркоза и саркомы печени (1906). Считал, что паразиты передают канцерогенный вирус. Йоханнес Андреас Гриб Фибигер (1867 1928) доказал, что паразит Spiroptera neoplastica, циркулирующий у тараканов и крыс, вызывает у последних папилломы и плоскоклеточный рак желудка (слева – препарат Фибигера) и языка (Нобелевская премия по медицине 1926 г. )
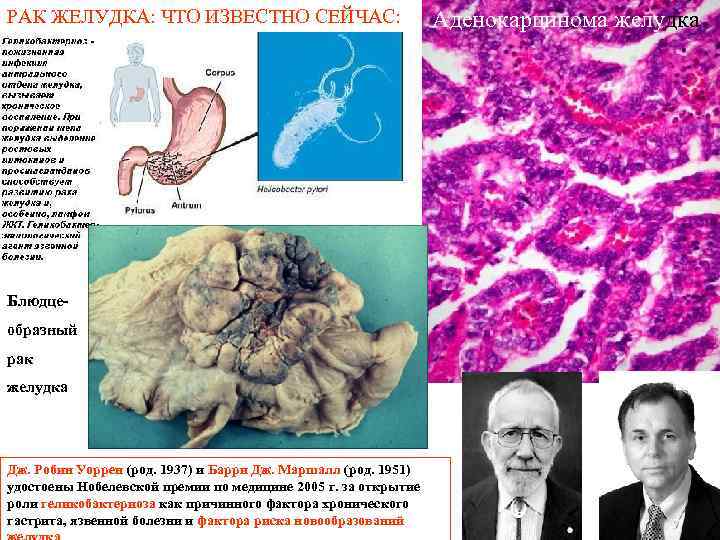
РАК ЖЕЛУДКА: ЧТО ИЗВЕСТНО СЕЙЧАС: Блюдце образный рак желудка Дж. Робин Уоррен (род. 1937) и Барри Дж. Маршалл (род. 1951) удостоены Нобелевской премии по медицине 2005 г. за открытие роли геликобактериоза как причинного фактора хронического гастрита, язвенной болезни и фактора риска новообразований Аденокарцинома желудка
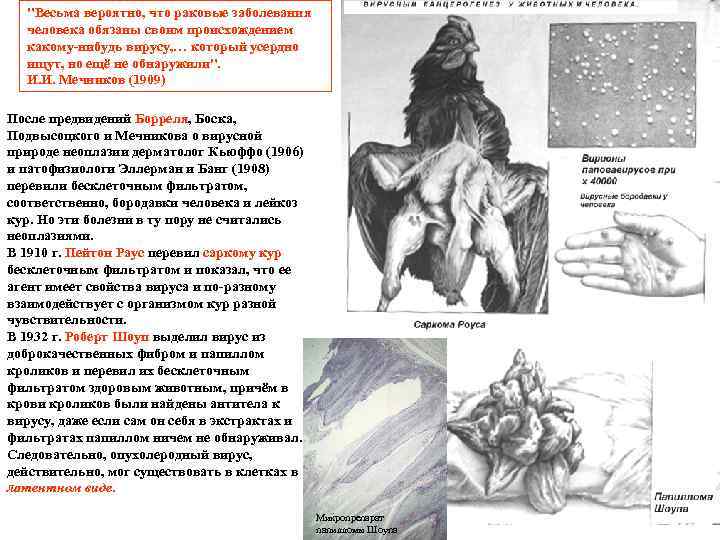
"Весьма вероятно, что раковые заболевания человека обязаны своим происхождением какому нибудь вирусу, … который усердно ищут, но ещё не обнаружили". И. И. Мечников (1909) После предвидений Борреля, Боска, Подвысоцкого и Мечникова о вирусной природе неоплазии дерматолог Кьюффо (1906) и патофизиологи Эллерман и Банг (1908) перевили бесклеточным фильтратом, соответственно, бородавки человека и лейкоз кур. Но эти болезни в ту пору не считались неоплазиями. В 1910 г. Пейтон Раус перевил саркому кур бесклеточным фильтратом и показал, что ее агент имеет свойства вируса и по разному взаимодействует с организмом кур разной чувствительности. В 1932 г. Роберт Шоуп выделил вирус из доброкачественных фибром и папиллом кроликов и перевил их бесклеточным фильтратом здоровым животным, причём в крови кроликов были найдены антитела к вирусу, даже если сам он себя в экстрактах и фильтратах папиллом ничем не обнаруживал. Следовательно, опухолеродный вирус, действительно, мог существовать в клетках в латентном виде. Микропрепарат папилломы Шоупа

Дж. Биттнер ВИРУСНЫЙ КАНЦЕРОГЕНЕЗ Джеймс Джон Биттнер (1904 1961) продемонстрировал роль фактора со свойствами вируса, передаваемого через молоко, в развитии рака молочной железы мышей (1934). Мышата высокораковых линий не давали высокой частоты спонтанного рака данной локализации, если вскармливались матерями низкораковых линий. Напротив, частота рака повышалась у потомства низкораковой линии, вскармливавшегося высокораковой матерью. При этом не было связи с тем, из какой линии происходил отец мышат. Уровень эстрогенов оказывал пермиссивный эффект при достаточно большой эстрогенизации рак молочной железы мог быть получен даже у самцов мышей, вскармливавшихся молоком матери из высокораковой линии, а у самок высокораковой линии рак наступал тем раньше, чем чаще они рожали. В молоке и клетках опухолей были обнаружены вирусоподобные частицы. Вирус размножался в эксплантатах и не передавался через плаценту. Опухоли развивались с большим латентным периодом, равным, примерно, половине средней продолжительности жизни мышей, что коррелирует с длительным lag периодом новообразований у человека. В настоящее время установлено, что рак молочной железы у мышей вызывается ретровирусом типа В (ММТV), а модель Биттнера имеет много черт, адекватных особенностям рака молочной железы человека, при котором в 40% случаев в опухоли обнаруживается человеческий ретровирус гомолог биттнеровского (HHMMTV). MMTV Лев Александрович Зильбер (1894 1966) на фото внизу в 1941 1946 гг. первым осознал принципиальные отличия между вирусной инфекцией и вирусным канцерогенезом и создал ВИРУСНО ГЕНЕТИЧЕСКУЮ теорию рака. “. . . роль вируса в развитии опухолевого процесса сводится к тому, что он изменяет наследственные свойства клетки, превращая ее из нормальной в опухолевую, а образовавшаяся таким образом опухолевая клетка служит источником роста опухоли; вирус же, вызвавший это превращение, или элиминируется из опухоли благодаря тому, что измененная клетка является неподходящей средой для его развития, или теряет свою болезнетворность и поэтому не может быть обнаружен при дальнейшем росте опухоли. . . Можно также предположить, что мутация, которая имеет место при превращении нормальной клетки в опухолевую, обусловлена генетическим аппаратом клетки. . . Если некоторые неопухолевые вирусы и другие инфекционные агенты способны вызывать клеточную пролиферацию, то это еще не значит, что они способны вызывать наследственные изменения свойств клетки. Последняя способность присуща только опухолевым вирусам и характер их воздействия на клетку принципиально отличается от характера воздействия инфекционных агентов, вызывающих в основном воспалительные и
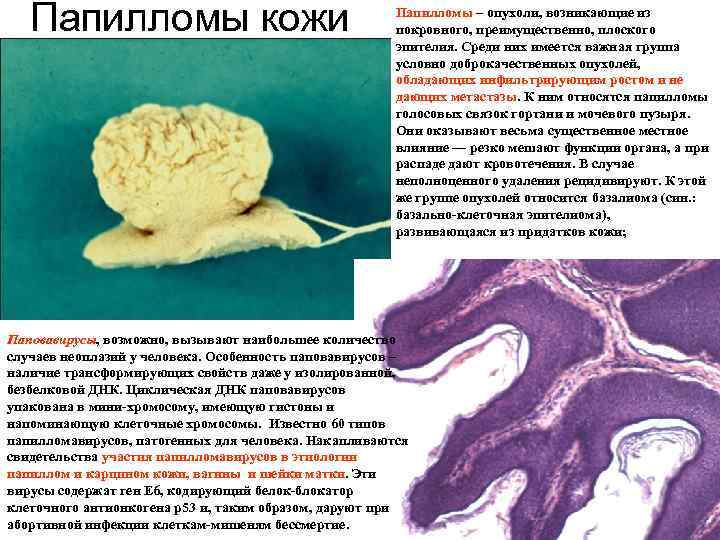
Папилломы кожи Папилломы – опухоли, возникающие из покровного, преимущественно, плоского эпителия. Среди них имеется важная группа условно доброкачественных опухолей, обладающих инфильтрирующим ростом и не дающих метастазы. К ним относятся папилломы голосовых связок гортани и мочевого пузыря. Они оказывают весьма существенное местное влияние — резко мешают функции органа, а при распаде дают кровотечения. В случае неполноценного удаления рецидивируют. К этой же группе опухолей относится базалиома (син. : базально клеточная эпителиома), развивающаяся из придатков кожи; Паповавирусы, возможно, вызывают наибольшее количество случаев неоплазий у человека. Особенность паповавирусов – наличие трансформирующих свойств даже у изолированной, безбелковой ДНК. Циклическая ДНК паповавирусов упакована в мини хромосому, имеющую гистоны и напоминающую клеточные хромосомы. Известно 60 типов папилломавирусов, патогенных для человека. Накапливаются свидетельства участия папилломавирусов в этиологии папиллом и карцином кожи, вагины и шейки матки. Эти вирусы содержат ген Е 6, кодирующий белок блокатор клеточного антионкогена р53 и, таким образом, даруют при абортивной инфекции клеткам мишеням бессмертие.

РЕТРОВИРУСНЫЙ КАНЦЕРОГЕНЕЗ Лауреаты Нобелевской премии по медицине 1975 г. Ренато Дульбекко (слева) выяснил что при онкогенезе вирусная ДНК включается в клеточную при участии фермента никазы, причём синтез клеточной ДНК подавляется, транскрипции в клетке подвергается часть вирусных генов. ДНК содержащие опухолеродные вирусы имеют гены-промоторы, которые способны инициировать транскрипцию генов, следующих в ДНК за ними. ДНК содержащие опухолеродные вирусы, как правило, сами не располагают вирусными онкогенами, но имеют возможность встраивать в геном эти регуляторы экспрессии протоонкогенов клеточных (как исключение, отмечают наличие онкогенов у некоторых папилломавирусов). Говард Тёмин (в центре) и Дэвид Бэлтимор описали обратную транскрипцию, обеспечивающую встраивание онкогенных РНК ретровирусов в клеточный геном. В настоящее время считается, что онкогенный потенциал ретровирусов связан с наличием в их геноме v-онкогенов, которые они, по предположению Тёмина, могут приобретать, перенося предсуществующие во всех клетках клеточные К настоящему времени известно несколько РНК и ДНК вирусов, которые ответственны за возникновение около 15% всех опухолей человека. К их числу следует отнести вирусы прямого действия вирусы папиллом , которые являются этиологическим фактором опухолей шейки матки и содержат собственные трансформирующие гены, два типа ДНК содержащих вирусов вирус гепатита В , ассоциированный с опухолями печени , и два герпес вируса Эпстайна Барр , ассоциированные с раком носоглотки и лимфомой Беркитта , вирус герпеса типа 8 , связанный с саркомой Капоши. Вирусы гепатита B (HBV) и вирусы гепатита С (HCV) способствуют развитию карциномы печени, они относится к числу вирусов непрямого действия, поскольку не содержит в своем составе онкогена, а онкогенный потенциал проявляют путем активации клеточных генов, участвующих в процессах пролиферации. Идентифицирован также один РНК содержащий ретровирус Т клеточного лейкоза взрослых ( HTLV I ), который охарактеризован как этиологический фактор у больных со сравнительно редким и эндемичным видом лейкоза ( Т клеточный лейкоз взрослых ATL ). Этот вирус также не имеет собственного онкогена, но содержит ген, который кодирует несколько белков, способных активировать различные факторы, в том числе цитокины , стимулирующие клетки к активной пролиферации Экспрессия маркера пролиферации Ki 67 в клетках аденокарциномы печени, осложнившей хронический вирусный гепатит В. Препарат доцента каф. патологии медфака СПб. ГУ В. Е. Карева
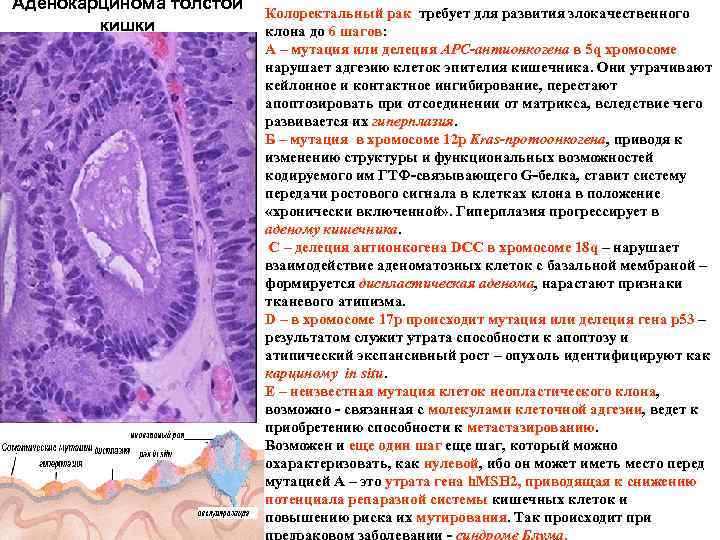
Аденокарцинома толстой кишки Колоректальный рак требует для развития злокачественного клона до 6 шагов: А – мутация или делеция APC-антионкогена в 5 q хромосоме нарушает адгезию клеток эпителия кишечника. Они утрачивают кейлонное и контактное ингибирование, перестают апоптозировать при отсоединении от матрикса, вследствие чего развивается их гиперплазия. Б – мутация в хромосоме 12 р Kras-протоонкогена, приводя к изменению структуры и функциональных возможностей кодируемого им ГТФ связывающего G белка, ставит систему передачи ростового сигнала в клетках клона в положение «хронически включенной» . Гиперплазия прогрессирует в аденому кишечника. С – делеция антионкогена DСС в хромосоме 18 q – нарушает взаимодействие аденоматозных клеток с базальной мембраной – формируется диспластическая аденома, нарастают признаки тканевого атипизма. D – в хромосоме 17 p происходит мутация или делеция гена р53 – результатом служит утрата способности к апоптозу и атипический экспансивный рост – опухоль идентифицируют как карциному in situ. Е – неизвестная мутация клеток неопластического клона, возможно связанная с молекулами клеточной адгезии, ведет к приобретению способности к метастазированию. Возможен и еще один шаг еще шаг, который можно охарактеризовать, как нулевой, ибо он может иметь место перед мутацией А – это утрата гена h. MSH 2, приводящая к cнижению потенциала репаразной системы кишечных клеток и повышению риска их мутирования. Так происходит при

Теория физического и радиационного канцерогенеза Физические мутагены, в частности, ионизирующее излучение, в том числе естественное, могут сами или через оксиданты, генерируемые при радиолизе воды в ядре клетки, вызывать различные мутации (в том числе, и наступающие не в момент лучевого воздействия а позже, при попытке восстановления структуры Вильям Конрад Рентген (1845 ДНК репаразами). При этом вероятность 1923) Лауреат Нобелевской мутаций повышается дозозависимо, но минимальной, вовсе немутагенной дозы, премии по физике 1901 г. , отличной от нуля, теоретически не существует. инициатор широкого Мутации, индуцируемые радиацией, могут быть применения Х лучей в летальными для клеток, а в случае их медицине и промышленности выживания приводят к появлению соматических мутантных клонов с измененными свойствами. Если радиационная мутация способствует экспрессии протоонкогенов и депрессии антионкогенов она может быть канцерогенной. Согласно современной оценке, не менее 3% случаев неоплазий являются результатом радиационного канцерогенеза. Помимо прямого и прооксидант опосредованного мутагенеза, вызываемого радиацией, дополнительное значение могут иметь ее иммуносупрессорные эффекты, снижающие противоопухолевый иммунитет. При проникающем действии наиболее мутагенны гамма лучи и Х лучи, но при инкорпорации радионуклидов – альфа излучатели. Альфа излучатель в клетках. Радиоавтограф. Германн Дж. Мёллер Пауль Герзон Унна (1850 1929) еще в (1890 -1967) 1889 г. первым в 1926 г. доказал предположил, Реактор Чернобыльской АЭС. что мутагенность ультрафиолетовое радиации, лауреат излучение Нобелевской канцерогенно для премии по кожи медицине 1946 г. В заброшенной школе в Чернобыльс зоне. Фото Л. П. Чурилова
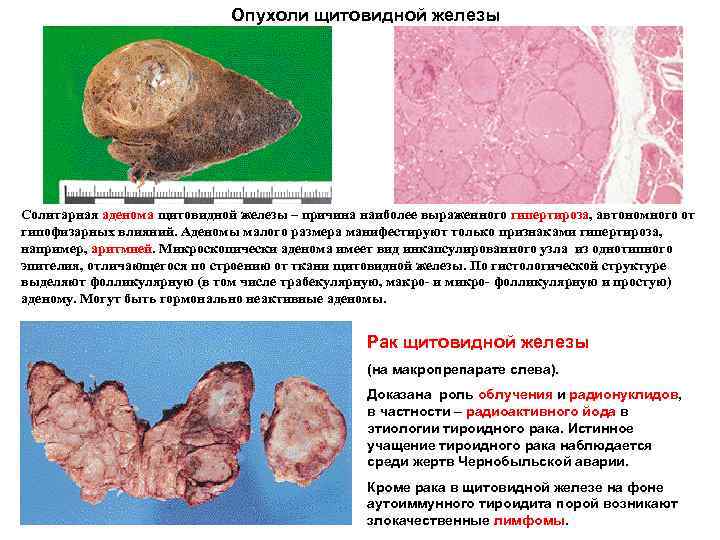
Опухоли щитовидной железы Солитарная аденома щитовидной железы – причина наиболее выраженного гипертироза, автономного от гипофизарных влияний. Аденомы малого размера манифестируют только признаками гипертироза, например, аритмией. Микроскопически аденома имеет вид инкапсулированного узла из однотипного эпителия, отличающегося по строению от ткани щитовидной железы. По гистологической структуре выделяют фолликулярную (в том числе трабекулярную, макро и микро фолликулярную и простую) аденому. Могут быть гормонально неактивные аденомы. Рак щитовидной железы (на макропрепарате слева). Доказана роль облучения и радионуклидов, в частности – радиоактивного йода в этиологии тироидного рака. Истинное учащение тироидного рака наблюдается среди жертв Чернобыльской аварии. Кроме рака в щитовидной железе на фоне аутоиммунного тироидита порой возникают злокачественные лимфомы.
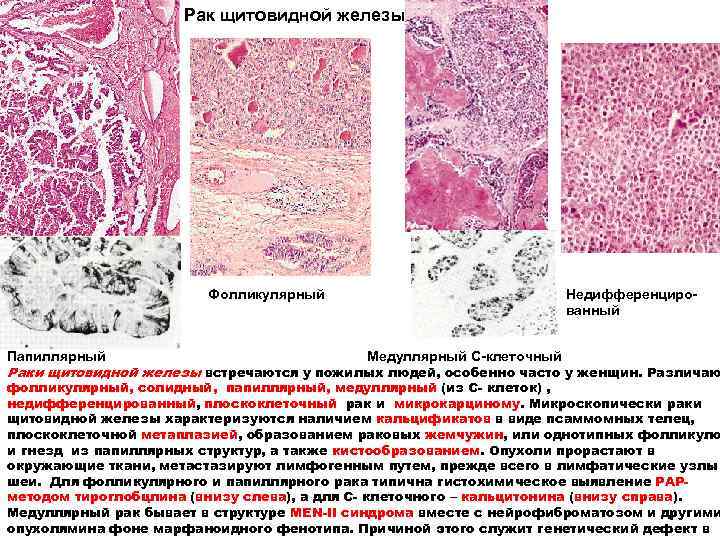
Рак щитовидной железы Фолликулярный Недифференцированный Папиллярный Медуллярный С-клеточный Раки щитовидной железы встречаются у пожилых людей, особенно часто у женщин. Различаю фолликулярный, солидный, папиллярный, медуллярный (из С- клеток) , недифференцированный, плоскоклеточный рак и микрокарциному. Микроскопически раки щитовидной железы характеризуются наличием кальцификатов в виде псаммомных телец, плоскоклеточной метаплазией, образованием раковых жемчужин, или однотипных фолликуло и гнезд из папиллярных структур, а также кистообразованием. Опухоли прорастают в окружающие ткани, метастазируют лимфогенным путем, прежде всего в лимфатические узлы шеи. Для фолликулярного и папиллярного рака типична гистохимическое выявление PAPметодом тироглобцлина (внизу слева), а для С- клеточного – кальцитонина (внизу справа). Медуллярный рак бывает в структуре MEN-II синдрома вместе с нейрофиброматозом и другими опухолямина фоне марфаноидного фенотипа. Причиной этого служит генетический дефект в
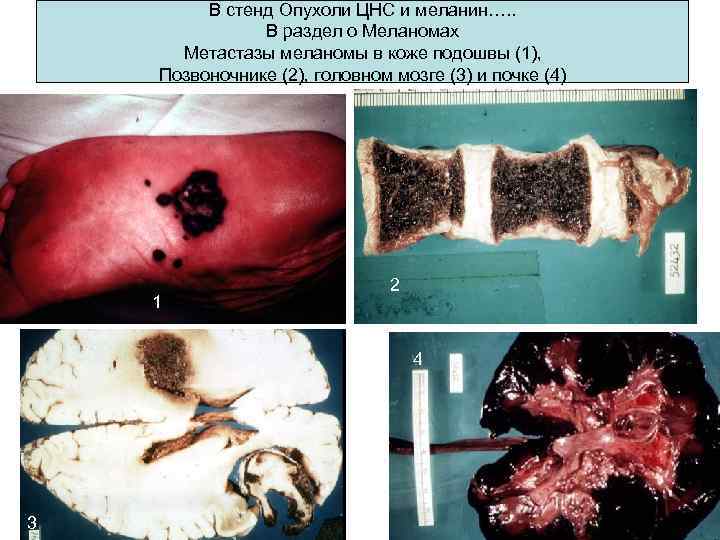
В стенд Опухоли ЦНС и меланин…. . В раздел о Меланомах Метастазы меланомы в коже подошвы (1), Позвоночнике (2), головном мозге (3) и почке (4) 1 2 4 3
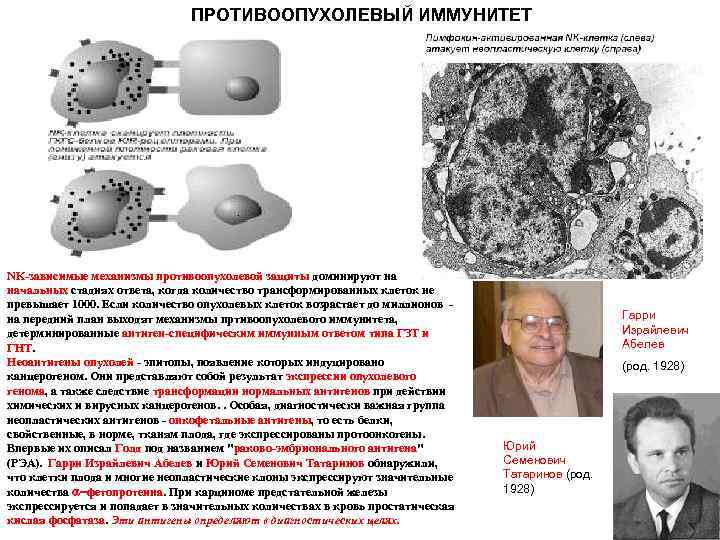
ПРОТИВООПУХОЛЕВЫЙ ИММУНИТЕТ NK зависимые механизмы противоопухолевой защиты доминируют на начальных стадиях ответа, когда количество трансформированных клеток не превышает 1000. Если количество опухолевых клеток возрастает до миллионов на передний план выходят механизмы пртивоопухолевого иммунитета, детерминированные антиген специфическим иммунным ответом типа ГЗТ и ГНТ. Неоантигены опухолей эпитопы, появление которых индуцировано канцерогеном. Они представляют собой результат экспрессии опухолевого генома, а также следствие трансформации нормальных антигенов при действии химических и вирусных канцерогенов. . Особая, диагностически важная группа неопластических антигенов онкофетальные антигены, то есть белки, свойственные, в норме, тканям плода, где экспрессированы протоонкогены. Впервые их описал Голд под названием "раково эмбрионального антигена" (РЭА). Гарри Израйлевич Абелев и Юрий Семенович Татаринов обнаружили, что клетки плода и многие неопластические клоны экспрессируют значительные количества фетопротеина. При карциноме предстательной железы экспрессируется и попадает в значительных количествах в кровь простатическая кислая фосфатаза. Эти антигены определяют в диагностических целях. Гарри Израйлевич Абелев (род. 1928) Юрий Семенович Татаринов (род. 1928)

Апоптоз и неоплазия Карл Фогт (1817 -1895) Вальтер Флемминг (1843 -1905) Джон Ф. Р. Керр (род. 1934) Швейцарец Карл Фогт еще в 1842 г. предположил, что при метаморфозе амфибий клетки самоустраняются не путем некроза, а иначе. Немец Вальтер Флемминг уже в 1885 г. первым описал апоптоз и зарисовал апоптотически гибнущие клетки с фрагментацией ядер ( «хроматолиз» ). У растений апоптоз – доминирующий способ клеточной гибели. В 1914 г. другой немецкий ученый - Людвиг Грепер указал на его общебиологическую роль и у животных. Однако, значение апоптоза в животном организме и, в частности, в онкологии, оставалось недооцененным более 100 лет. Апоптоз был не в моде, в тени некробиоза… до работ австралийца Джона Фокстона Росса Керра, в 1965 -1972 гг. заново описавшего апоптоз и предсказавшего роль в патогенезе компенсаторноприспособительных процессов и неоплазии. Эмбриональные клетки похожи на неопластические, но их фундаментальным отличием является сохранная способность к программированной гибели.
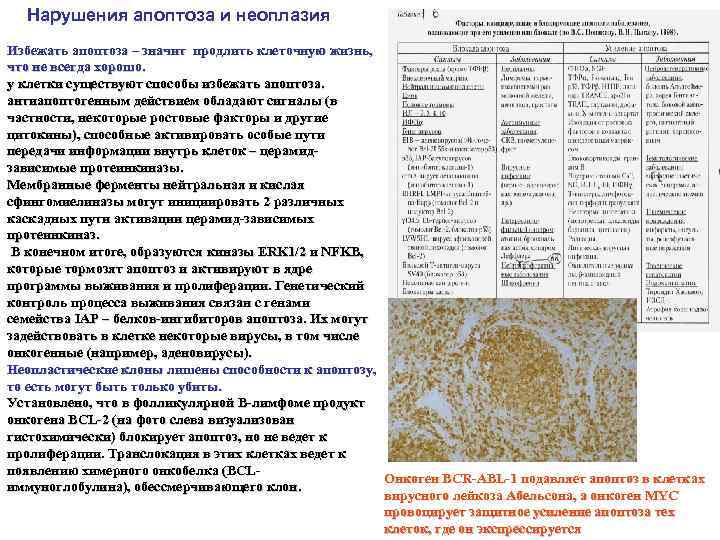
Нарушения апоптоза и неоплазия Избежать апоптоза – значит продлить клеточную жизнь, что не всегда хорошо. у клетки существуют способы избежать апоптоза. антиапоптогенным действием обладают сигналы (в частности, некоторые ростовые факторы и другие цитокины), способные активировать особые пути передачи информации внутрь клеток – церамид зависимые протеинкиназы. Мембранные ферменты нейтральная и кислая сфингомиелиназы могут инициировать 2 различных каскадных пути активации церамид зависимых протеинкиназ. В конечном итоге, образуются киназы ERK 1/2 и NFKB, которые тормозят апоптоз и активируют в ядре программы выживания и пролиферации. Генетический контроль процесса выживания связан с генами семейства IAP – белков ингибиторов апоптоза. Их могут задействовать в клетке некоторые вирусы, в том числе онкогенные (например, аденовирусы). Неопластические клоны лишены способности к апоптозу, то есть могут быть только убиты. Установлено, что в фолликулярной В лимфоме продукт онкогена BCL 2 (на фото слева визуализован гистохимически) блокирует апоптоз, но не ведет к пролиферации. Транслокация в этих клетках ведет к появлению химерного онкобелка (BCL Онкоген BCR ABL 1 подавляет апоптоз в клетках иммуноглобулина), обессмерчивающего клон. вирусного лейкоза Абельсона, а онкоген MYC провоцирует защитное усиление апоптоза тех клеток, где он экспрессируется
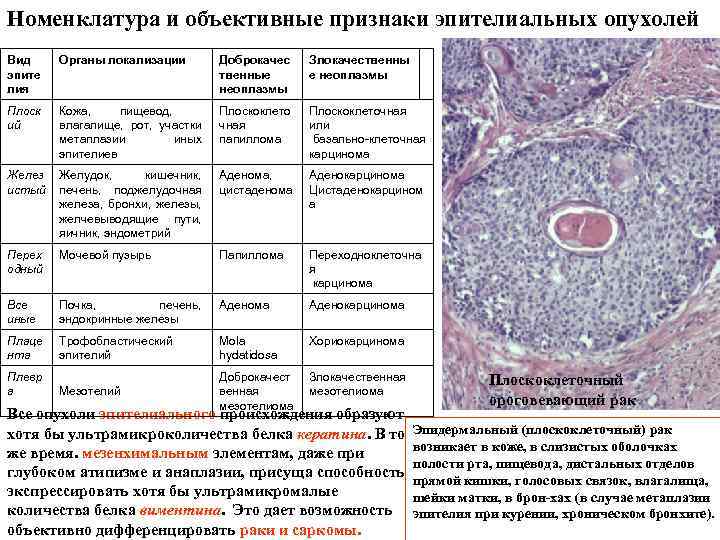
Номенклатура и объективные признаки эпителиальных опухолей Вид эпите лия Органы локализации Доброкачес твенные неоплазмы Злокачественны е неоплазмы Плоск ий Кожа, пищевод, влагалище, рот, участки метаплазии иных эпителиев Плоскоклето чная папиллома Плоскоклеточная или базально-клеточная карцинома Желез истый Желудок, кишечник, печень, поджелудочная железа, бронхи, железы, желчевыводящие пути, яичник, эндометрий Аденома, цистаденома Аденокарцинома Цистаденокарцином а Перех одный Мочевой пузырь Папиллома Переходноклеточна я карцинома Все иные Почка, печень, эндокринные железы Аденома Аденокарцинома Плаце нта Трофобластический эпителий Моla hydatidosa Хориокарцинома Плевр а Мезотелий Доброкачест венная мезотелиома Злокачественная мезотелиома Все опухоли эпителиального происхождения образуют хотя бы ультрамикроколичества белка кератина. В то же время. мезенхимальным элементам, даже при глубоком атипизме и анаплазии, присуща способность экспрессировать хотя бы ультрамикромалые количества белка виментина. Это дает возможность объективно дифференцировать раки и саркомы. Плоскоклеточный ороговевающий рак Эпидермальный (плоскоклеточный) рак возникает в коже, в слизистых оболочках полости рта, пищевода, дистальных отделов прямой кишки, голосовых связок, влагалища, шейки матки, в брон хах (в случае метаплазии эпителия при курении, хроническом бронхите).
НЕОПЛАЗИЯ КАК ТИПОВОЙ ПАТОЛОГИЧЕСКИЙ ПРОЦЕСС.ppt