лекц4 конформации.ppt
- Количество слайдов: 125
Кафедра органической и биоорганической химии БГМУ Тема лекции 4: l КОФОРМАЦИОННАЯ l СТЕРЕОИЗОМЕРИЯ

СТЕРЕОХИМИЯ –раздел химической науки, изучающий пространственное строение органических соединений и его влияние на физические и химические свойства, механизм реакций. Изомерами называются соединения с одинаковым элементным составом, но отличающиеся последовательностью связывания атомов и (или) расположением их в пространстве

КОНФОРМАЦИОННАЯ СТЕРЕОИЗОМЕРИЯ Д. Бартон Конформационные стереоизомеры, или просто конформации, чаще всего возникают в результате вращения отдельных фрагментов молекул вокруг простых связей. Конформации могут существовать только все вместе в виде единого множества геометрических форм молекулы с различным взаимным расположением в пространстве отдельных атомов и атомных групп. Основы конформационных представлений были разработаны и опубликованы в 1950 г. английским химиком Д. Бартоном. Они легли в основу конформационного анализа , который занимается изучением свойств соединений в зависимости от строения и соотношения конформаций, в которых оно может существовать. Значимость этих представлений характеризует высказывание известного американского химика Э. Илиела «химик не понимающий конформационного анализа, не понимает органической химии» .
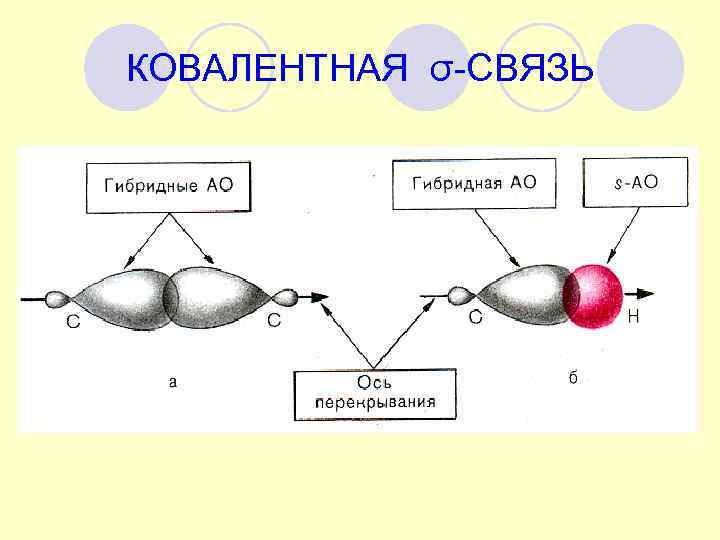
КОВАЛЕНТНАЯ σ-СВЯЗЬ
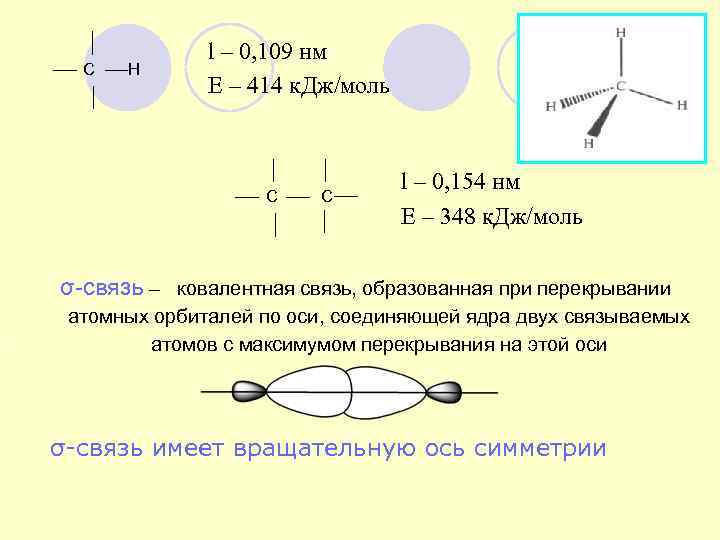
С Н l – 0, 109 нм Е – 414 к. Дж/моль l – 0, 154 нм Е – 348 к. Дж/моль С σ-связь – ковалентная связь, образованная при перекрывании атомных орбиталей по оси, соединяющей ядра двух связываемых атомов с максимумом перекрывания на этой оси σ-связь имеет вращательную ось симметрии
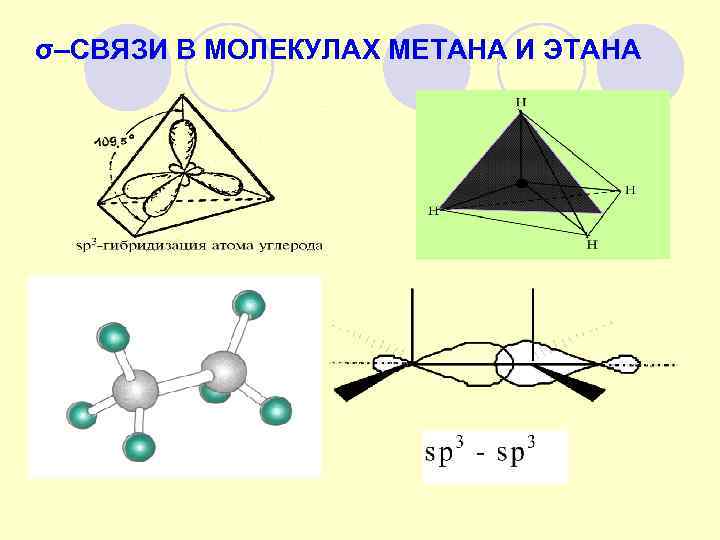
σ–СВЯЗИ В МОЛЕКУЛАХ МЕТАНА И ЭТАНА
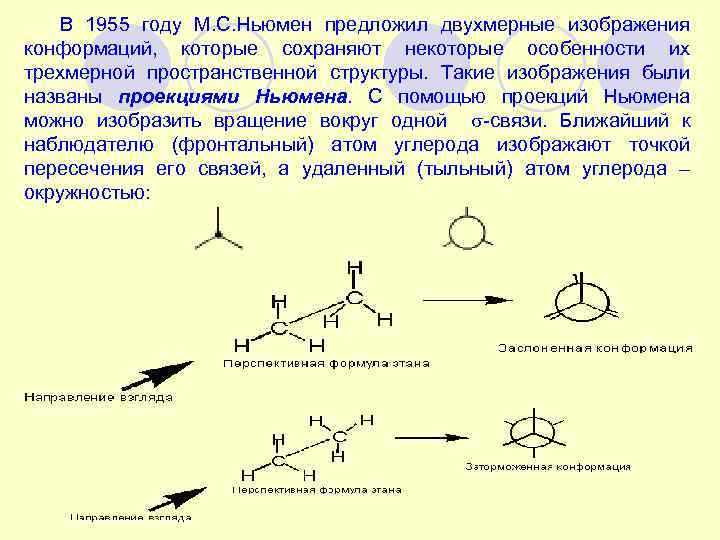
В 1955 году М. С. Ньюмен предложил двухмерные изображения конформаций, которые сохраняют некоторые особенности их , трехмерной пространственной структуры. Такие изображения были названы проекциями Ньюмена. С помощью проекций Ньюмена можно изобразить вращение вокруг одной -связи. Ближайший к . наблюдателю (фронтальный) атом углерода изображают точкой пересечения его связей, а удаленный (тыльный) атом углерода – окружностью:
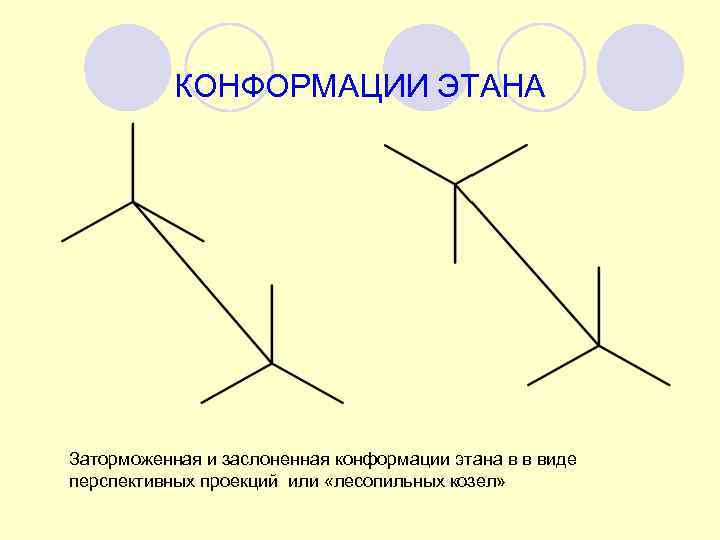
КОНФОРМАЦИИ ЭТАНА Заторможенная и заслоненная конформации этана в в виде перспективных проекций или «лесопильных козел»
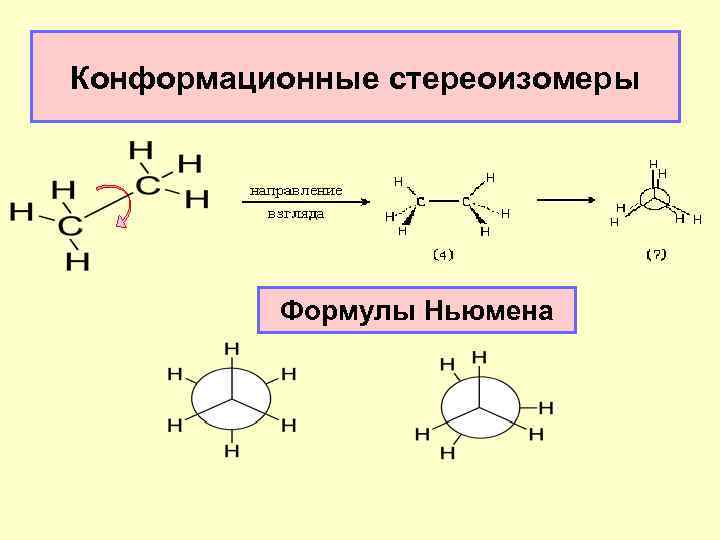
Конформационные стереоизомеры Формулы Ньюмена

Определение конформаций l Различные пространственные формы молекул, возникающие в результате вращения одних групп в молекуле относительно других по линии σ связей и отличающиеся запасом энергии (термодинамической устойчивостью).
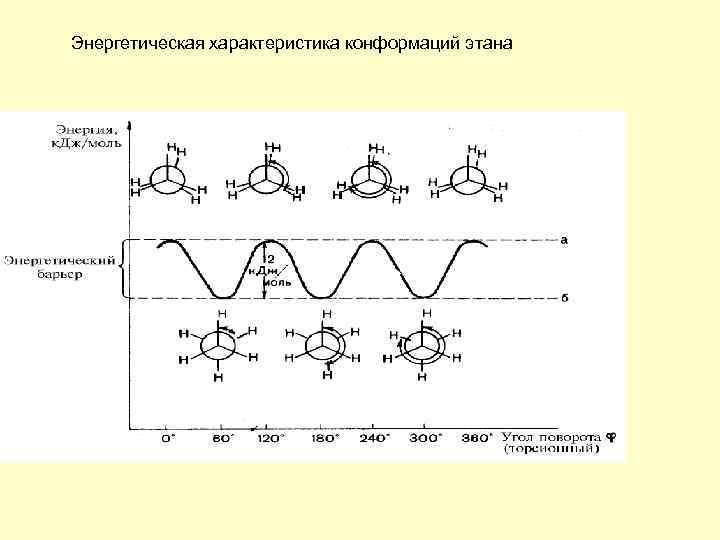
Энергетическая характеристика конформаций этана
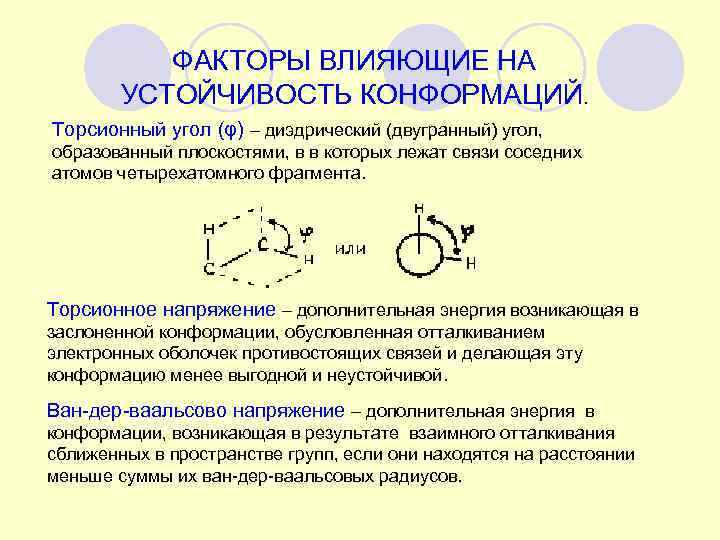
ФАКТОРЫ ВЛИЯЮЩИЕ НА УСТОЙЧИВОСТЬ КОНФОРМАЦИЙ. Торсионный угол (φ) – диэдрический (двугранный) угол, образованный плоскостями, в в которых лежат связи соседних атомов четырехатомного фрагмента. Торсионное напряжение – дополнительная энергия возникающая в заслоненной конформации, обусловленная отталкиванием электронных оболочек противостоящих связей и делающая эту конформацию менее выгодной и неустойчивой. Ван-дер-ваальсово напряжение – дополнительная энергия в конформации, возникающая в результате взаимного отталкивания сближенных в пространстве групп, если они находятся на расстоянии меньше суммы их ван-дер-ваальсовых радиусов.

ВАН-ДЕР-ВААЛЬСОВЫ РАДИУСЫ ЭЛЕМЕНТОВ- ОРГАНОГЕНОВ l Атом или группа Ван-дер-ваальсов радиус , нм l l l l l Н 0, 12 С 0, 18 СН 2 0, 20 СН 3 0, 20 N 0, 15 О 0, 14 Cl 0, 18 F 0, 135 Br 0, 195 J 0, 215 l
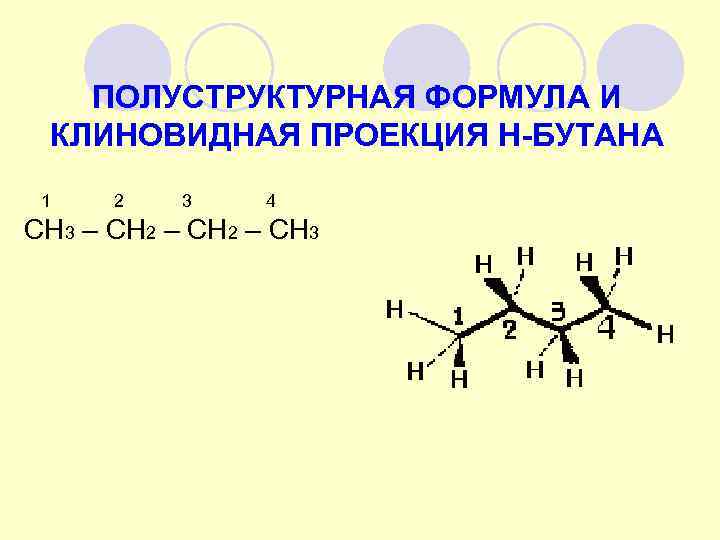
ПОЛУСТРУКТУРНАЯ ФОРМУЛА И КЛИНОВИДНАЯ ПРОЕКЦИЯ Н-БУТАНА 1 2 3 4 СН 3 – СН 2 – СН 3
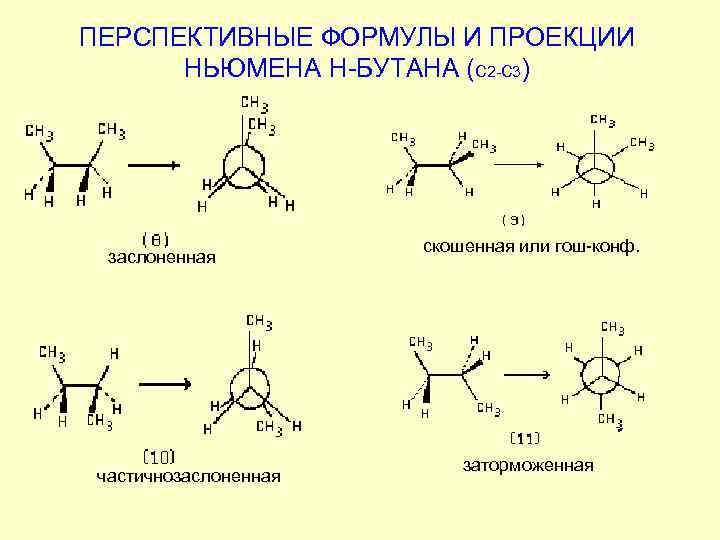
ПЕРСПЕКТИВНЫЕ ФОРМУЛЫ И ПРОЕКЦИИ НЬЮМЕНА Н-БУТАНА (С 2 -С 3) заслоненная частичнозаслоненная скошенная или гош-конф. заторможенная
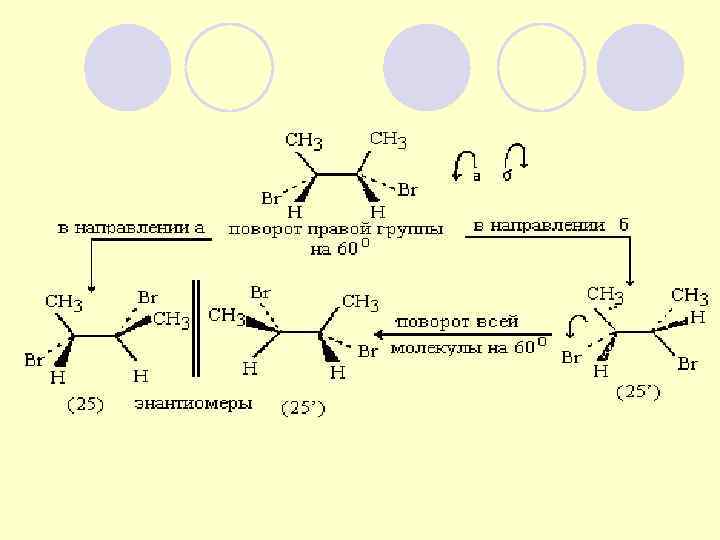
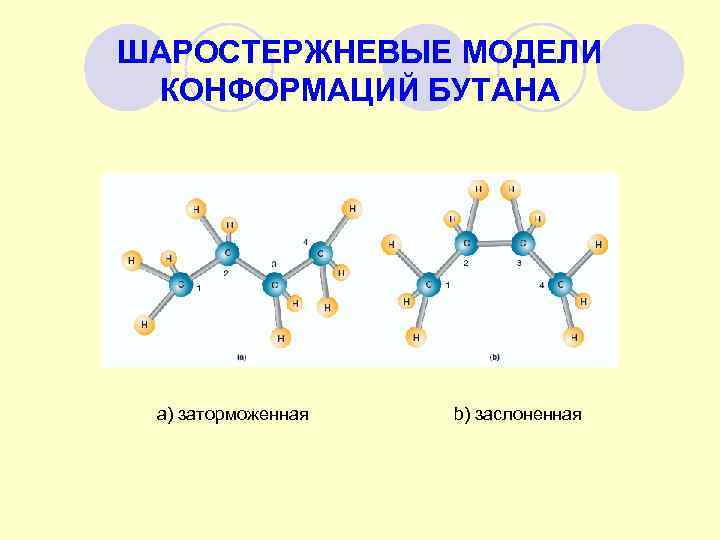
ШАРОСТЕРЖНЕВЫЕ МОДЕЛИ КОНФОРМАЦИЙ БУТАНА а) заторможенная b) заслоненная
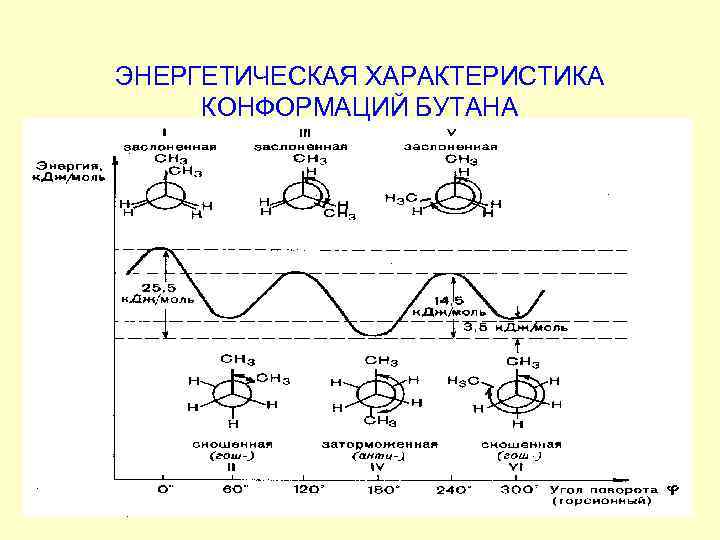
ЭНЕРГЕТИЧЕСКАЯ ХАРАКТЕРИСТИКА КОНФОРМАЦИЙ БУТАНА
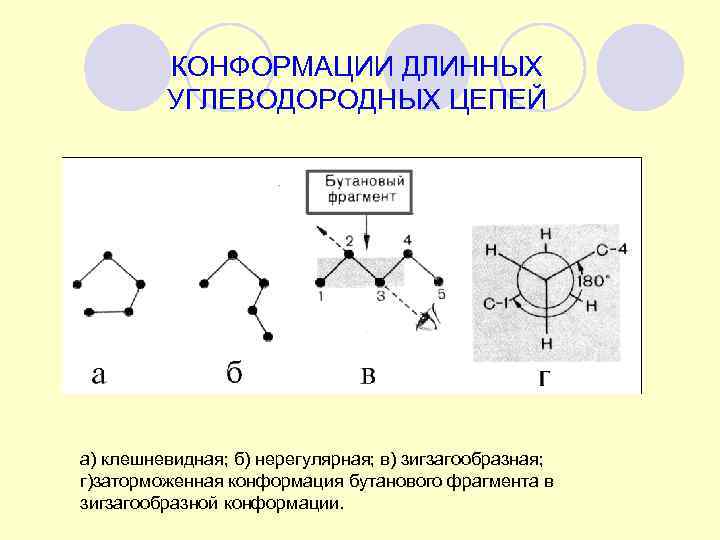
КОНФОРМАЦИИ ДЛИННЫХ УГЛЕВОДОРОДНЫХ ЦЕПЕЙ а) клешневидная; б) нерегулярная; в) зигзагообразная; г)заторможенная конформация бутанового фрагмента в зигзагообразной конформации.

КОНФОРМАЦИИ НАСЫЩЕННЫХ ВЫСШИХ ЖИРНЫХ КИСЛОТ
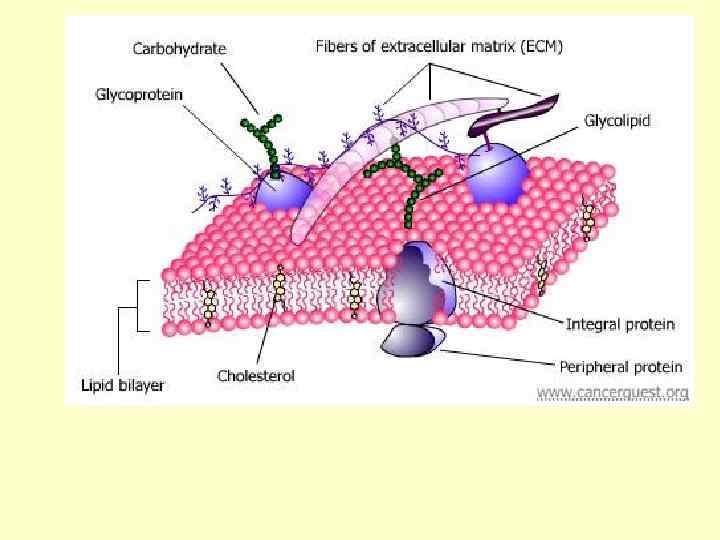
9 -октадеценовая кислота Олеиновая кислота tпл. 16°
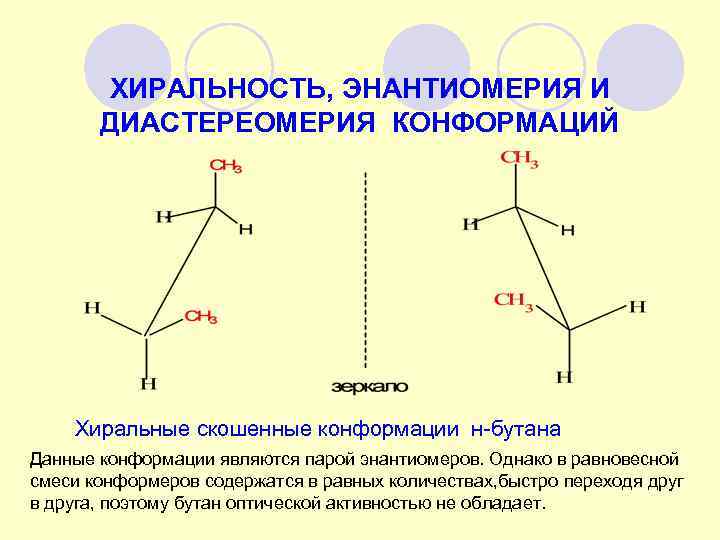
ХИРАЛЬНОСТЬ, ЭНАНТИОМЕРИЯ И ДИАСТЕРЕОМЕРИЯ КОНФОРМАЦИЙ Хиральные скошенные конформации н-бутана Данные конформации являются парой энантиомеров. Однако в равновесной смеси конформеров содержатся в равных количествах, быстро переходя друг в друга, поэтому бутан оптической активностью не обладает.
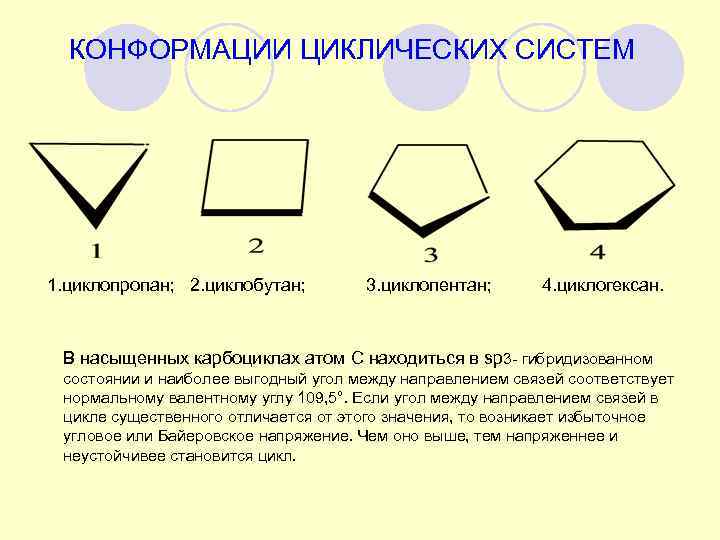
КОНФОРМАЦИИ ЦИКЛИЧЕСКИХ СИСТЕМ 1. циклопропан; 2. циклобутан; 3. циклопентан; 4. циклогексан. В насыщенных карбоциклах атом С находиться в sp 3 - гибридизованном состоянии и наиболее выгодный угол между направлением связей соответствует нормальному валентному углу 109, 5°. Если угол между направлением связей в цикле существенного отличается от этого значения, то возникает избыточное угловое или Байеровское напряжение. Чем оно выше, тем напряженнее и неустойчивее становится цикл.
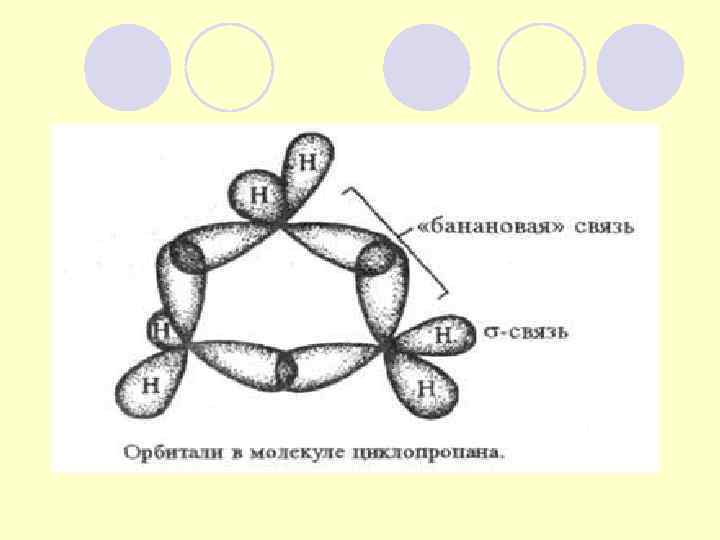

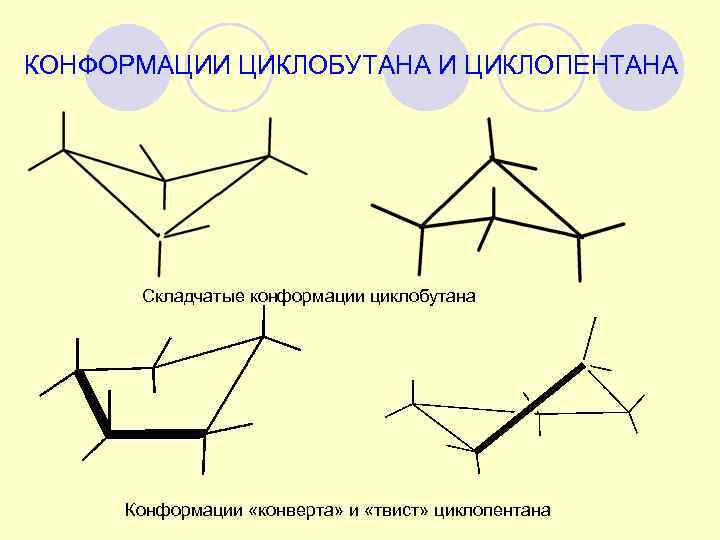
КОНФОРМАЦИИ ЦИКЛОБУТАНА И ЦИКЛОПЕНТАНА Складчатые конформации циклобутана Конформации «конверта» и «твист» циклопентана
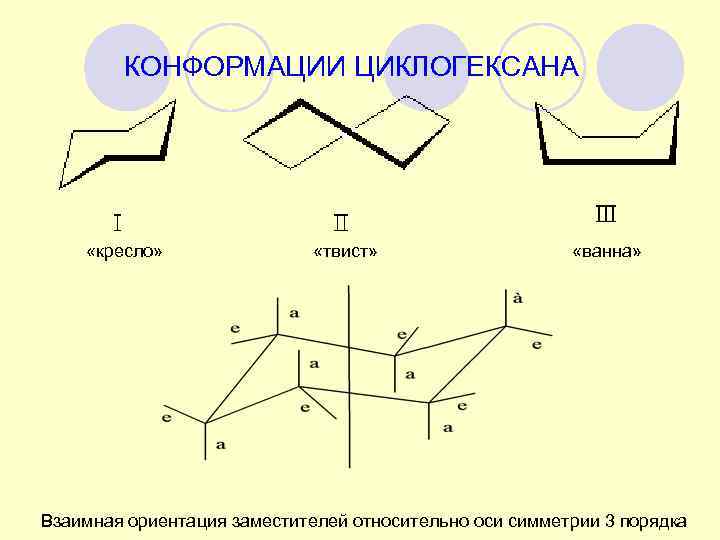
КОНФОРМАЦИИ ЦИКЛОГЕКСАНА «кресло» «твист» «ванна» Взаимная ориентация заместителей относительно оси симметрии 3 порядка
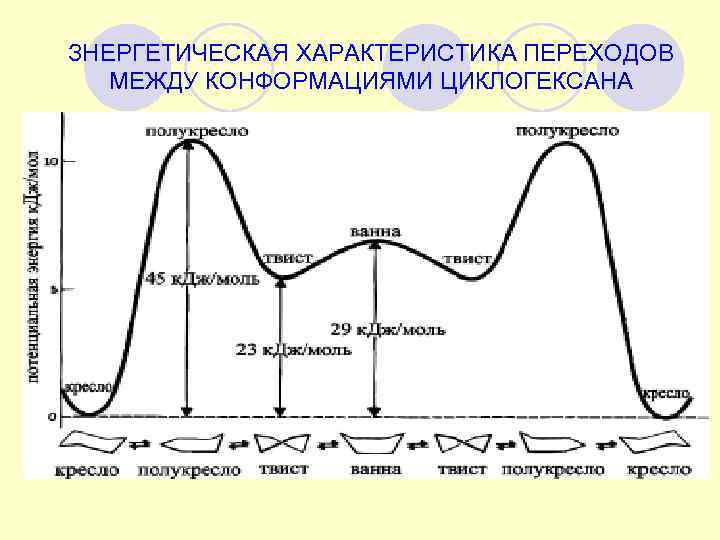
ЗНЕРГЕТИЧЕСКАЯ ХАРАКТЕРИСТИКА ПЕРЕХОДОВ МЕЖДУ КОНФОРМАЦИЯМИ ЦИКЛОГЕКСАНА
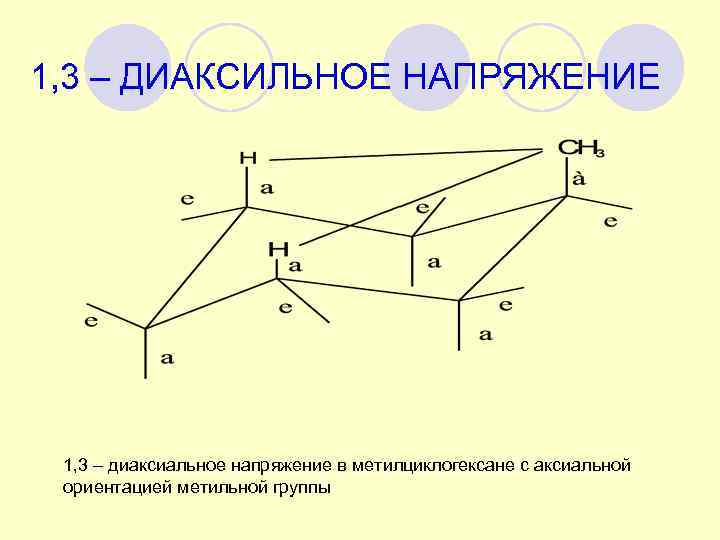
1, 3 – ДИАКСИЛЬНОЕ НАПРЯЖЕНИЕ 1, 3 – диаксиальное напряжение в метилциклогексане с аксиальной ориентацией метильной группы
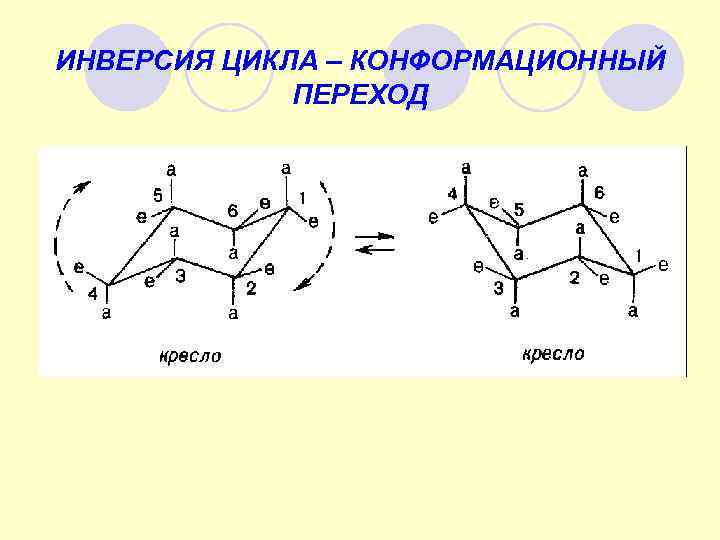
ИНВЕРСИЯ ЦИКЛА – КОНФОРМАЦИОННЫЙ ПЕРЕХОД
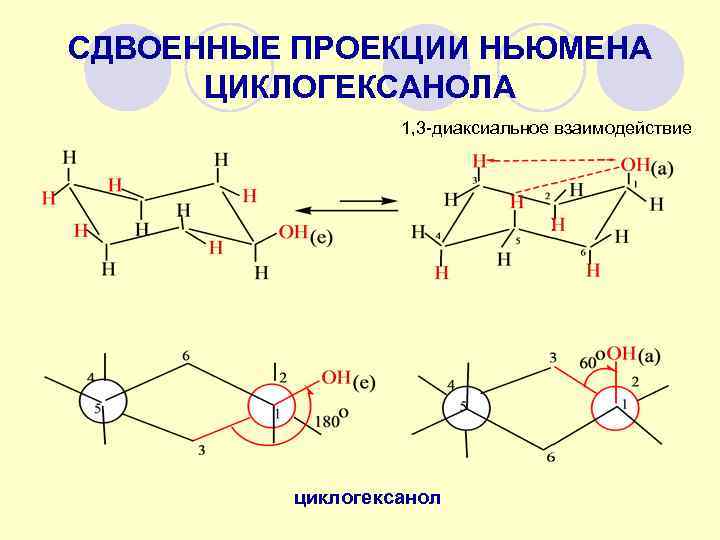
СДВОЕННЫЕ ПРОЕКЦИИ НЬЮМЕНА ЦИКЛОГЕКСАНОЛА 1, 3 -диаксиальное взаимодействие циклогексанол
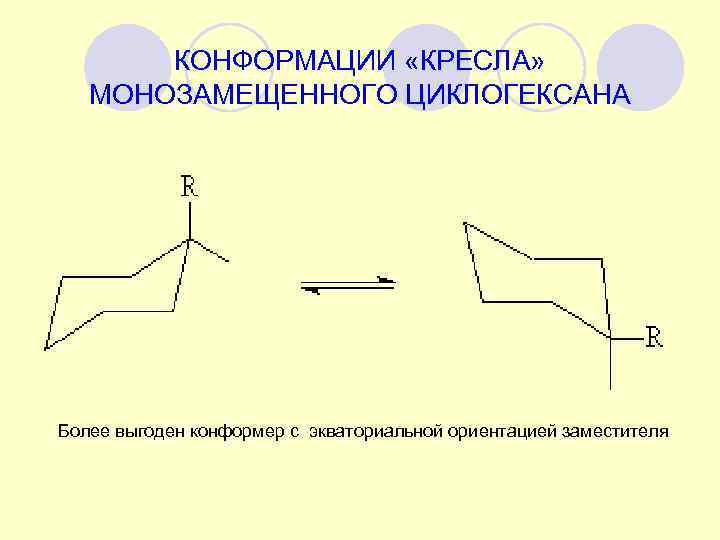
КОНФОРМАЦИИ «КРЕСЛА» МОНОЗАМЕЩЕННОГО ЦИКЛОГЕКСАНА Более выгоден конформер с экваториальной ориентацией заместителя
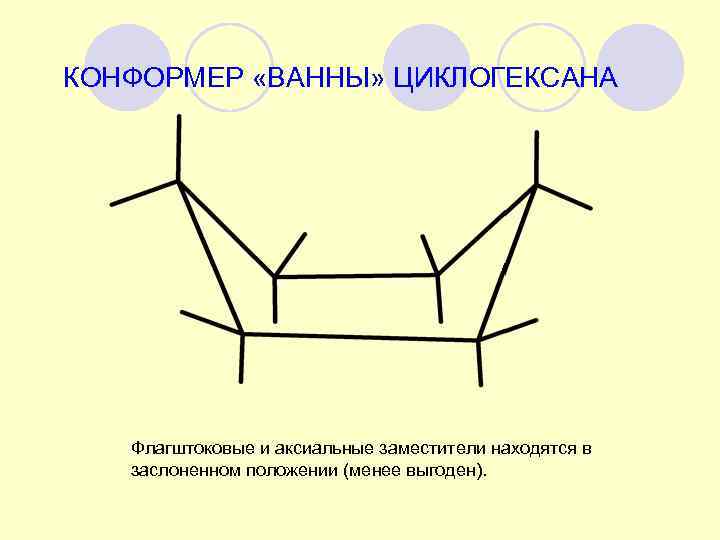
КОНФОРМЕР «ВАННЫ» ЦИКЛОГЕКСАНА Флагштоковые и аксиальные заместители находятся в заслоненном положении (менее выгоден).
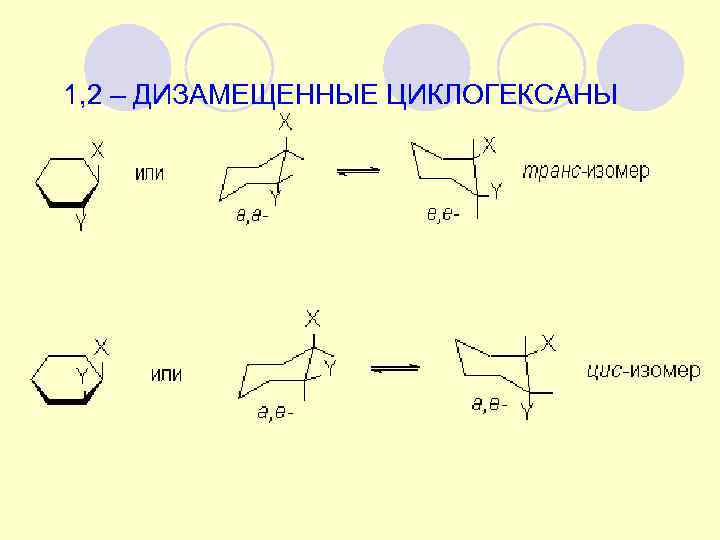
1, 2 – ДИЗАМЕЩЕННЫЕ ЦИКЛОГЕКСАНЫ
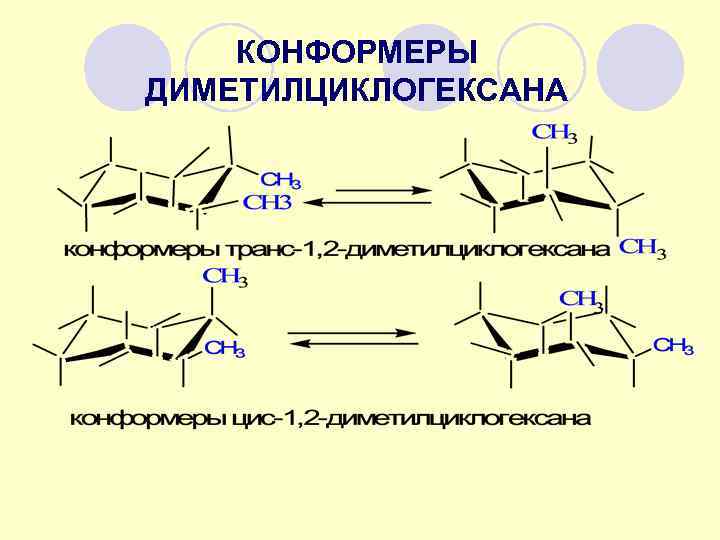
КОНФОРМЕРЫ ДИМЕТИЛЦИКЛОГЕКСАНА
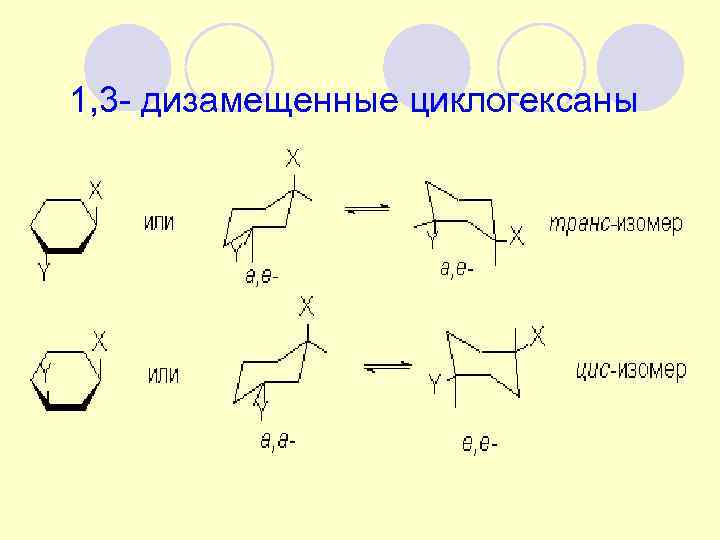
1, 3 - дизамещенные циклогексаны
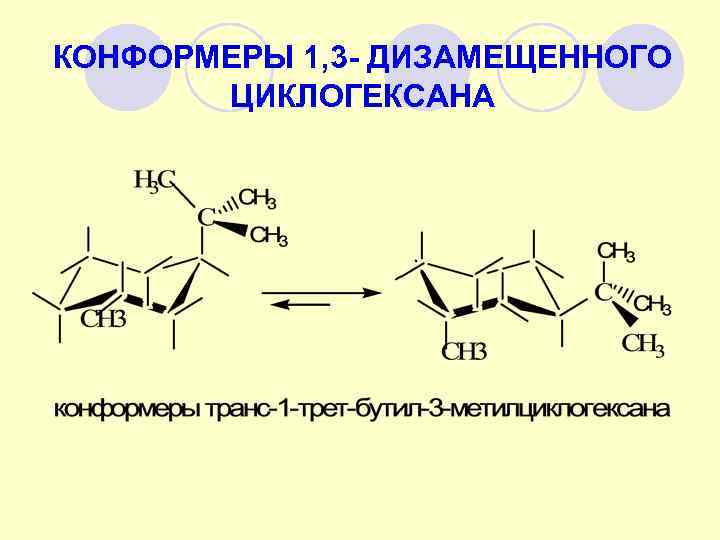
КОНФОРМЕРЫ 1, 3 - ДИЗАМЕЩЕННОГО ЦИКЛОГЕКСАНА
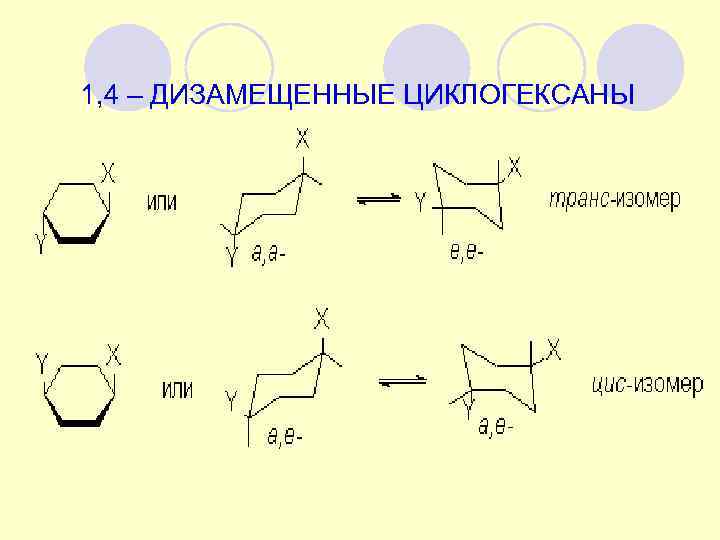
1, 4 – ДИЗАМЕЩЕННЫЕ ЦИКЛОГЕКСАНЫ
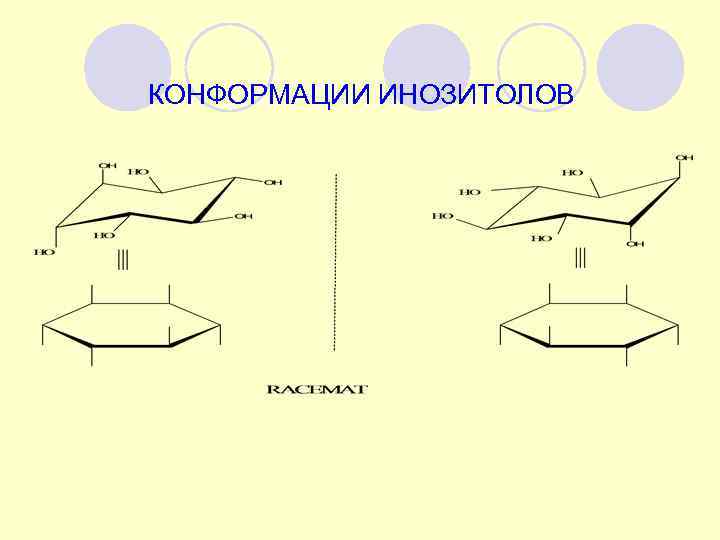
КОНФОРМАЦИИ ИНОЗИТОЛОВ
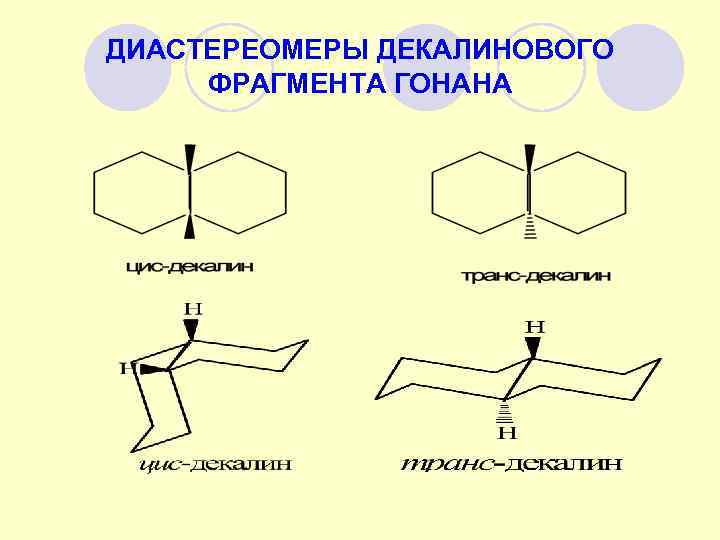
ДИАСТЕРЕОМЕРЫ ДЕКАЛИНОВОГО ФРАГМЕНТА ГОНАНА
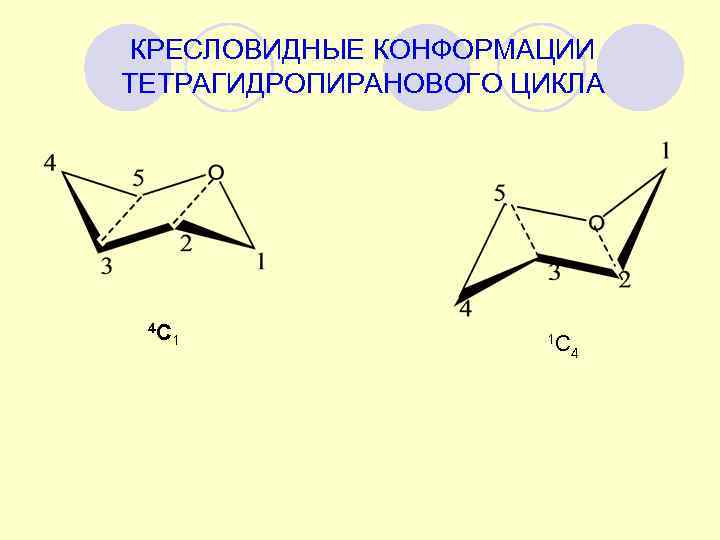
КРЕСЛОВИДНЫЕ КОНФОРМАЦИИ ТЕТРАГИДРОПИРАНОВОГО ЦИКЛА 4 С 1 1 С 4
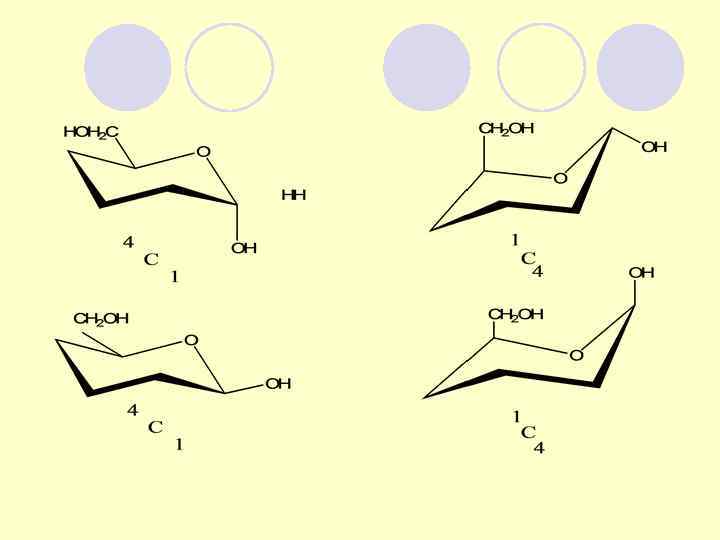
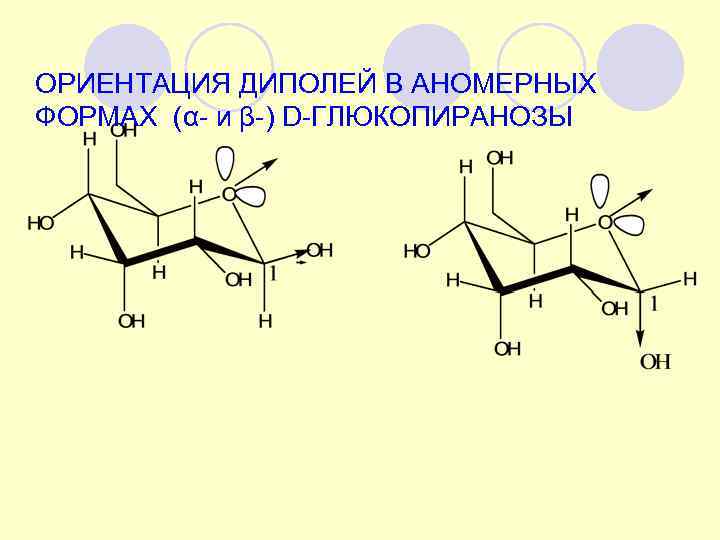
ОРИЕНТАЦИЯ ДИПОЛЕЙ В АНОМЕРНЫХ ФОРМАХ (α- и β-) D-ГЛЮКОПИРАНОЗЫ

СВЯЗЬ ПРОСТРАНСТВЕННОГО СТРОЕНИЯ СОЕДИНЕНИЙ С ИХ БИОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ В организме реакции протекают с участием биокатализаторов – ферментов. Ферменты построены из хиральных молекул α-Lаминокислот, поэтому они чувствительны к хиральности взаимодействующих с ними субстратов. Хиральными молекулами являются также углеводы, фосфолипиды, витамины, гормоны, нуклеиновые кислоты.
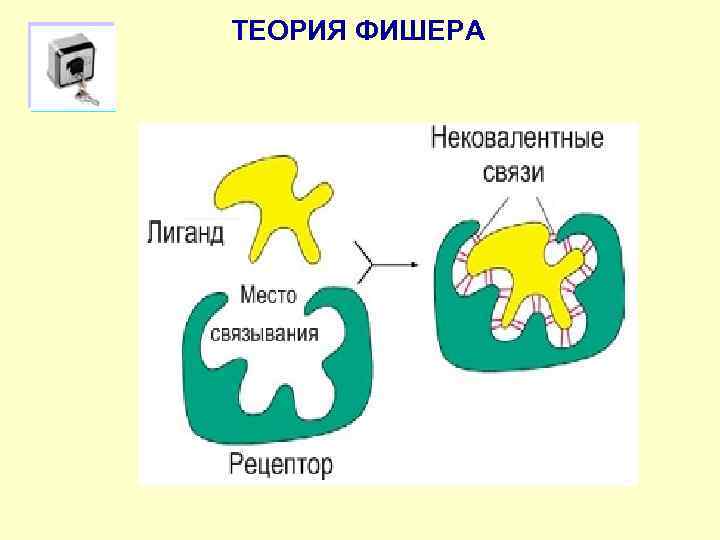
ТЕОРИЯ ФИШЕРА
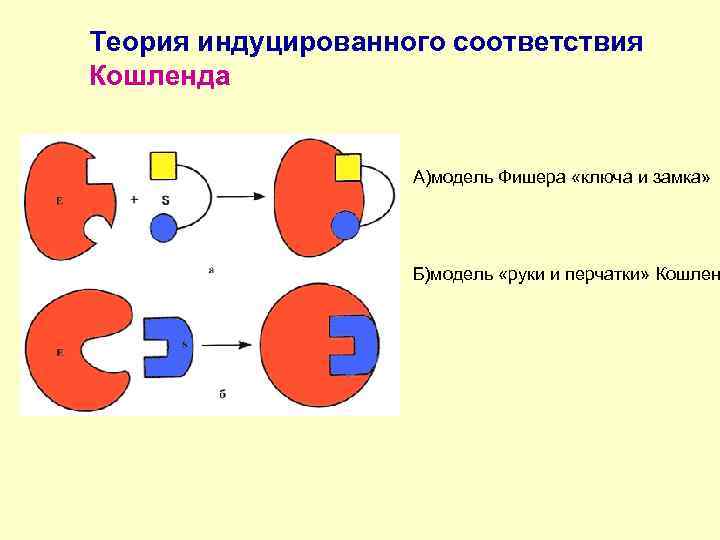
Теория индуцированного соответствия Кошленда А)модель Фишера «ключа и замка» Б)модель «руки и перчатки» Кошлен

Связь пространственного строения соединений с их биологической активностью
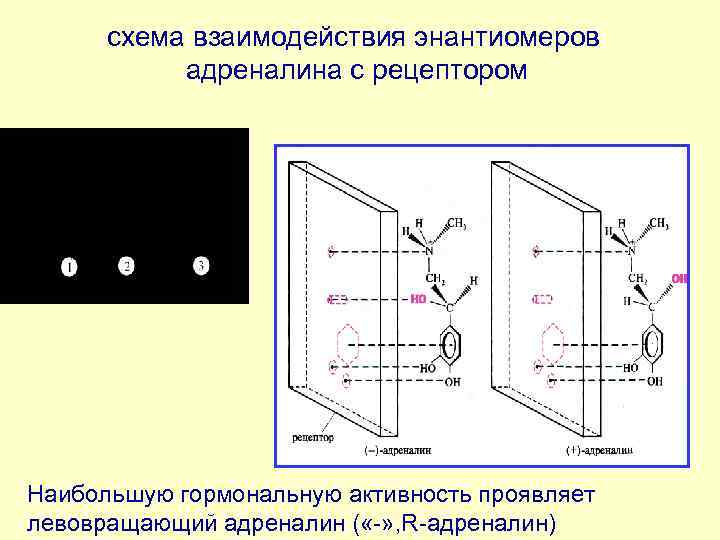
схема взаимодействия энантиомеров адреналина с рецептором Наибольшую гормональную активность проявляет левовращающий адреналин ( «-» , R-адреналин)
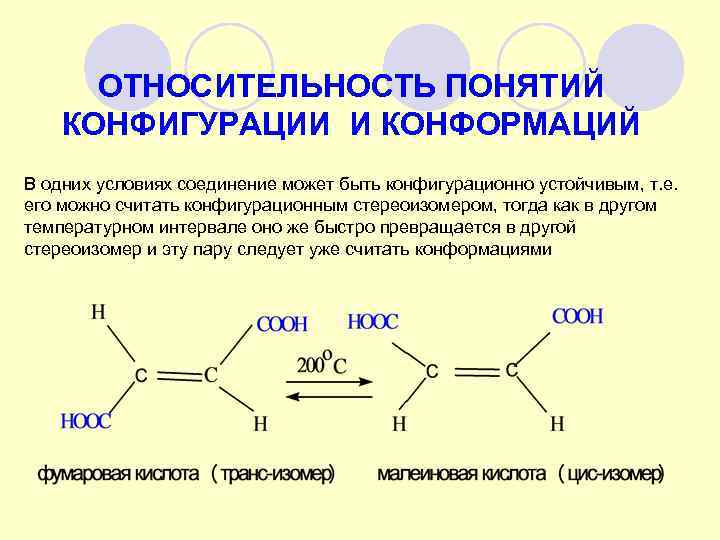
ОТНОСИТЕЛЬНОСТЬ ПОНЯТИЙ КОНФИГУРАЦИИ И КОНФОРМАЦИЙ В одних условиях соединение может быть конфигурационно устойчивым, т. е. его можно считать конфигурационным стереоизомером, тогда как в другом температурном интервале оно же быстро превращается в другой стереоизомер и эту пару следует уже считать конформациями
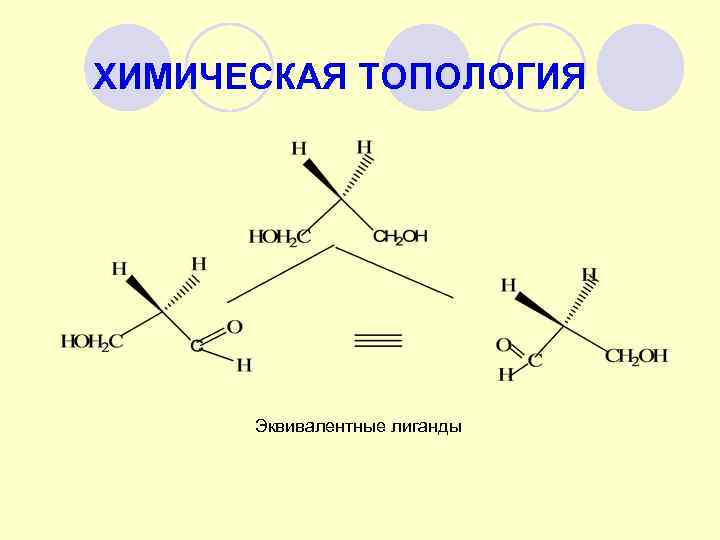
ХИМИЧЕСКАЯ ТОПОЛОГИЯ Эквивалентные лиганды
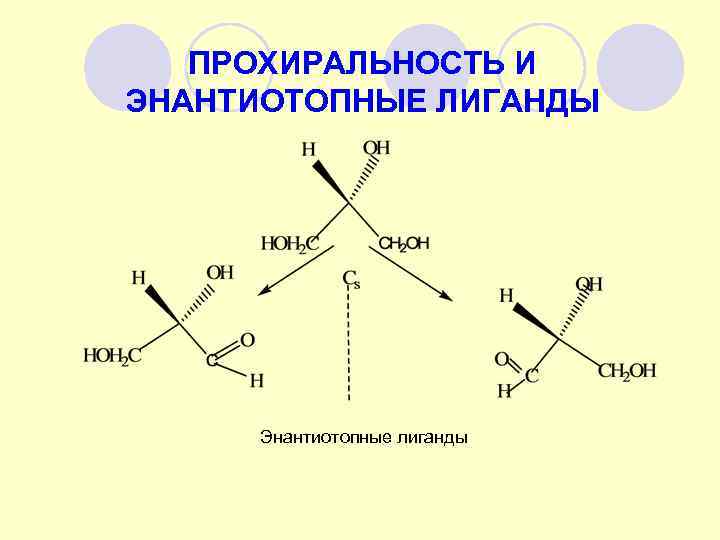
ПРОХИРАЛЬНОСТЬ И ЭНАНТИОТОПНЫЕ ЛИГАНДЫ Энантиотопные лиганды
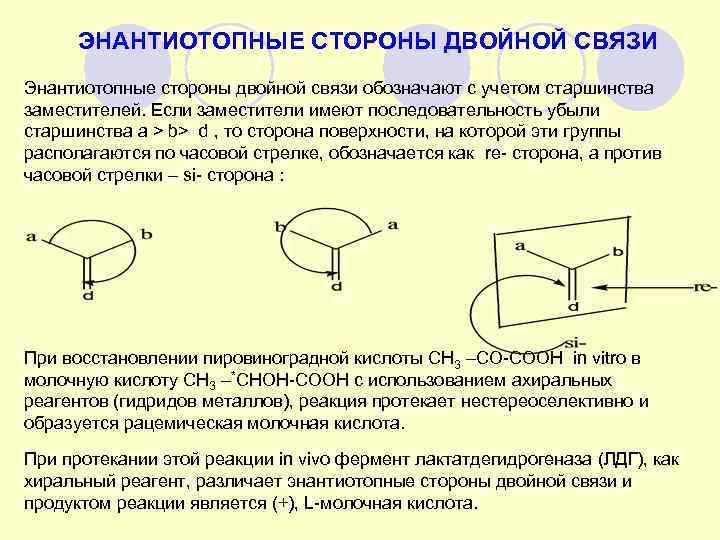
ЭНАНТИОТОПНЫЕ СТОРОНЫ ДВОЙНОЙ СВЯЗИ Энантиотопные стороны двойной связи обозначают с учетом старшинства заместителей. Если заместители имеют последовательность убыли старшинства a > b> d , то сторона поверхности, на которой эти группы располагаются по часовой стрелке, обозначается как re- сторона, а против часовой стрелки – si- сторона : При восстановлении пировиноградной кислоты СН 3 –СО-СООН in vitro в молочную кислоту СН 3 –*СНОН-СООН с использованием ахиральных реагентов (гидридов металлов), реакция протекает нестереоселективно и образуется рацемическая молочная кислота. При протекании этой реакции in vivo фермент лактатдегидрогеназа (ЛДГ), как хиральный реагент, различает энантиотопные стороны двойной связи и продуктом реакции является (+), L-молочная кислота.
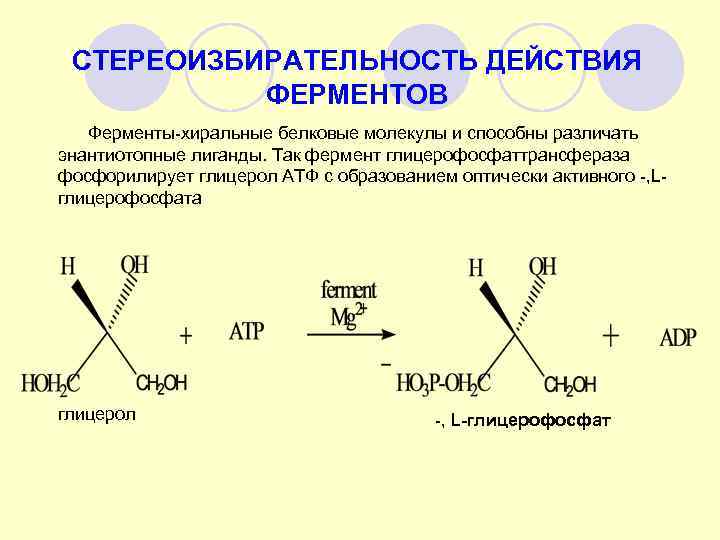
СТЕРЕОИЗБИРАТЕЛЬНОСТЬ ДЕЙСТВИЯ ФЕРМЕНТОВ Ферменты-хиральные белковые молекулы и способны различать энантиотопные лиганды. Так фермент глицерофосфаттрансфераза фосфорилирует глицерол АТФ с образованием оптически активного -, Lглицерофосфата глицерол -, L-глицерофосфат

СТЕРЕСПЕЦИФИЧНОСТЬ ЛЕКАРСТВЕННЫХ СРЕДСТВ Наиболее активный энантиомер, обладающий сродством к рецептору и вызывающий выраженный биологический зффект, называется эутомером. Неактивный или токсичный энантиомер, обладающий меньшим сродством к рецептору, называется дистомером. Показателем эффективности и стереоселективности действия хирального лекарственного средства является : Эудесмическое отношение представляющее собой отношение Аффинитета эутомера /аффинитету дистомера Аффинитет – сродство и прочность соединения между лигандом (гормон, субстрат, антиген, лекарственное средство) и объектом его действия (рецептор, фермент, антитело и т. д. ).
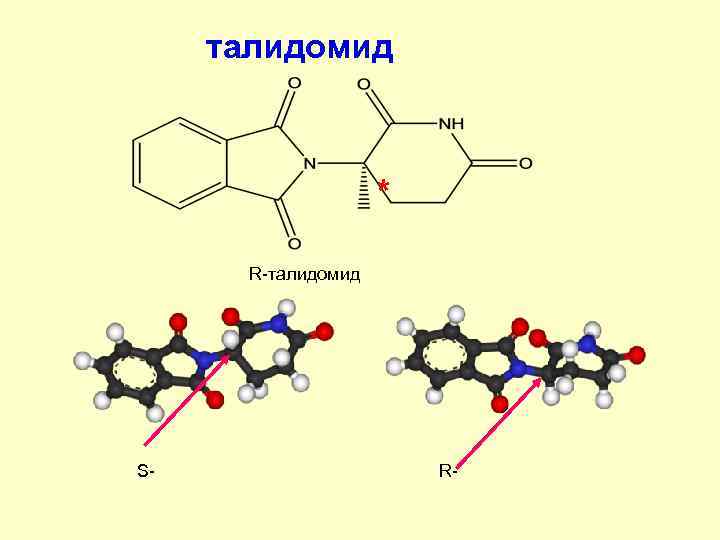
талидомид * R-талидомид S- R-

ПАМЯТНИК ЖЕРТВАМ ТАЛИДОМИДА

БИОИЗОСТЕРИЗМ Стереохимические представления широко используются и в современных подходах при разработке и органическом синтезе лекарственных препаратов. Стратегия заключается в модификации соединения-лидера основанной на биоизостеризме. Биоизостер – соединение, получаемое путем замены одного атома (группы атомов) на другой атом (группу атомов), и сохраняющее биологическую активность исходного соединения. Важными характеристиками биоизостеров является их электронное, пространственное строение и гидрофобность. Классическими биоизостерами являются:


В завершение лекции

Педфаку посвящается l l l l Вы в выгодной, удобной конформации И засветился вдруг экран, Я не совру Вам ни на гран, Поверьте лучшей радости мне нет, И это достоверный факт Чем лекции уж столько лет (с 1969 г. ) Тебе читать любимый мой ПЕДФАК !

К теории топохимического соответствия
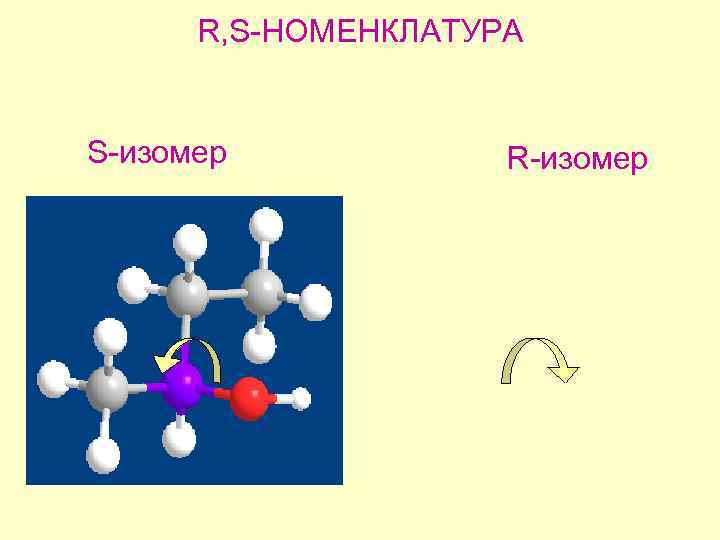
R, S-НОМЕНКЛАТУРА S-изомер R-изомер
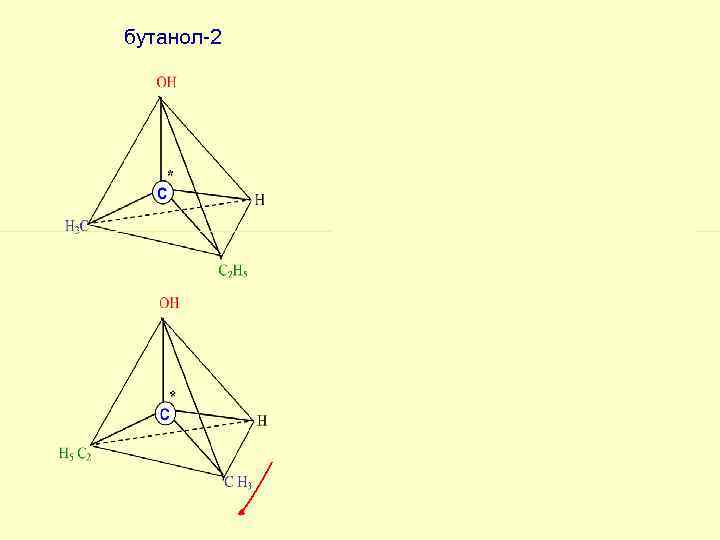
бутанол-2

М. Ломоносов 1751 «Слово о пользе химии» « …медик без довольного знания химии совершенен быть не может…»
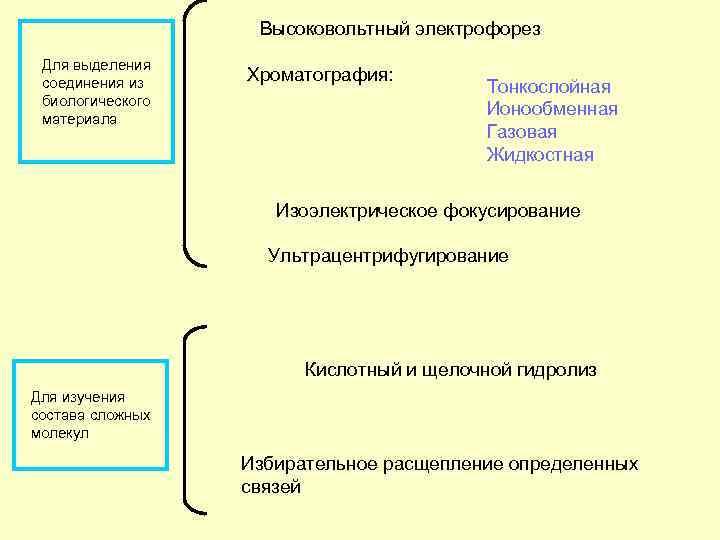
Высоковольтный электрофорез Для выделения соединения из биологического материала Хроматография: Тонкослойная Ионообменная Газовая Жидкостная Изоэлектрическое фокусирование Ультрацентрифугирование Кислотный и щелочной гидролиз Для изучения состава сложных молекул Избирательное расщепление определенных связей

Методы биоорганической химии Для определения структуры соединений Рентгеноструктурный анализ Электронография Электронный парамагнитнгый резонанс - ЭПР Ядерный магнитный резонанс - ЯМР Спектроскопия

Уровни исследования живых организмов 1. 2. Молекулярный Надмолекулярный 3. 4. Клеточный Тканевой, органный Биоорганическая химия Бионеорганическая химия Биофизика Гистология Патанатомия Микробиология Биохимия Клинические дисциплины 5. Организменный 6. 7. Популяционный Биогеоценозный Биология Эпидемиология Генетика 8. Биосферный Экология
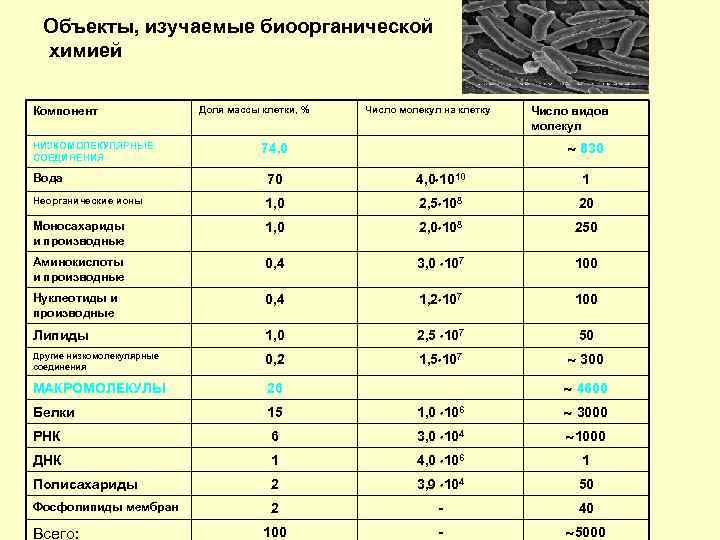
Объекты, изучаемые биоорганической химией Компонент НИЗКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ Доля массы клетки, % Число молекул на клетку Число видов молекул 830 74, 0 Вода 70 4, 0 1010 1 Неорганические ионы 1, 0 2, 5 108 20 Моносахариды и производные 1, 0 2, 0 108 250 Аминокислоты и производные 0, 4 3, 0 107 100 Нуклеотиды и производные 0, 4 1, 2 107 100 Липиды 1, 0 2, 5 107 50 Другие низкомолекулярные соединения 0, 2 1, 5 107 300 МАКРОМОЛЕКУЛЫ 26 Белки 15 1, 0 106 3000 РНК 6 3, 0 104 1000 ДНК 1 4, 0 106 1 Полисахариды 2 3, 9 104 50 Фосфолипиды мембран 2 - 40 100 - 5000 Всего: 4600
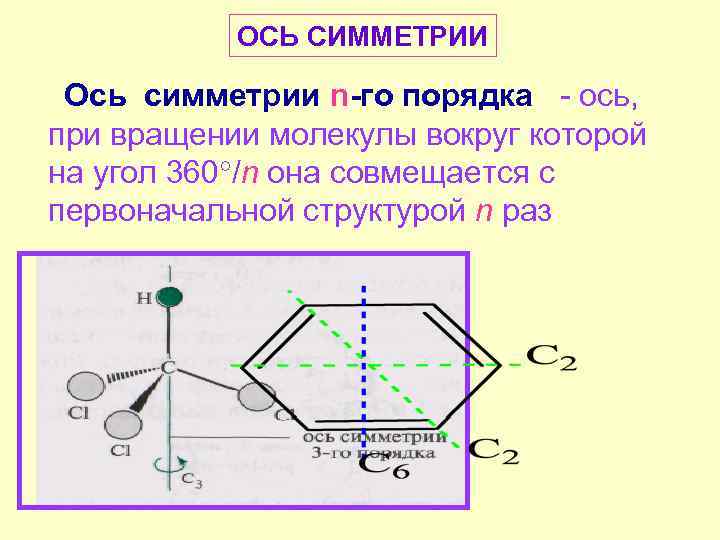
ОСЬ СИММЕТРИИ Ось симметрии n-го порядка - ось, при вращении молекулы вокруг которой на угол 360 /n она совмещается с первоначальной структурой n раз
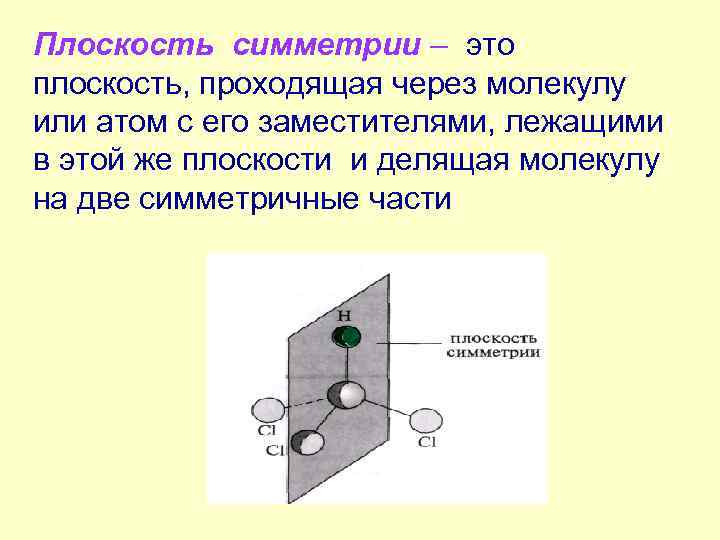
Плоскость симметрии – это плоскость, проходящая через молекулу или атом с его заместителями, лежащими в этой же плоскости и делящая молекулу на две симметричные части

Поляризованный свет l Поляризованный свет состоит из двух право- и лево- циркулярно поляризованных лучей
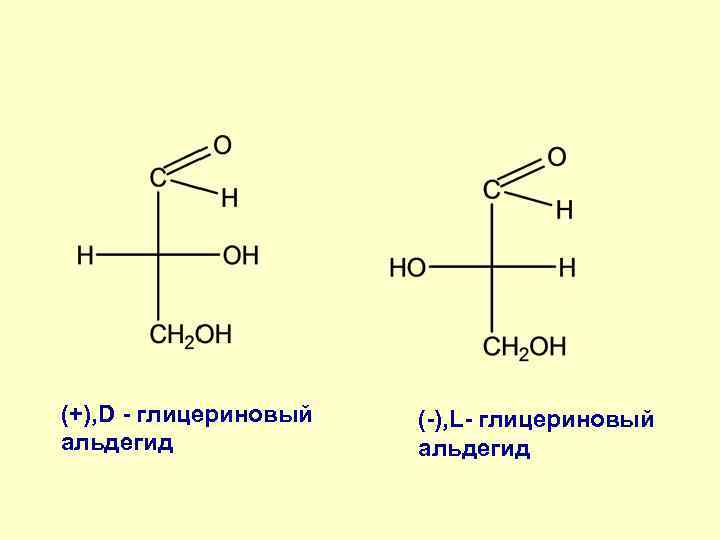
(+), D - глицериновый альдегид (-), L- глицериновый альдегид

Определение комплементарности l Коплементарность - пространствненная взаимодополняемость (стерическое соответствие) поверхностей взаимодействующих молекул или их частей, приводящая, как правило, к образованию вторичных (ван-дер-ваальсовых, водородных, ионных) связей между ними. Уникальность и прочность комплементарных структур определяется высокой избирательностью и значительной площадью гидрофобного взаимодействия на уровне атомных группировок или зарядов по принципу «ключ-замок» или «рукаперчатка» .

СПОСОБЫ РАСЩЕПЛЕНИЯ РАЦЕМАТОВ Механический 1848 г. Л. Пастер вручную разделил энантиоморфные кристаллы Na-NH 4 тартрата
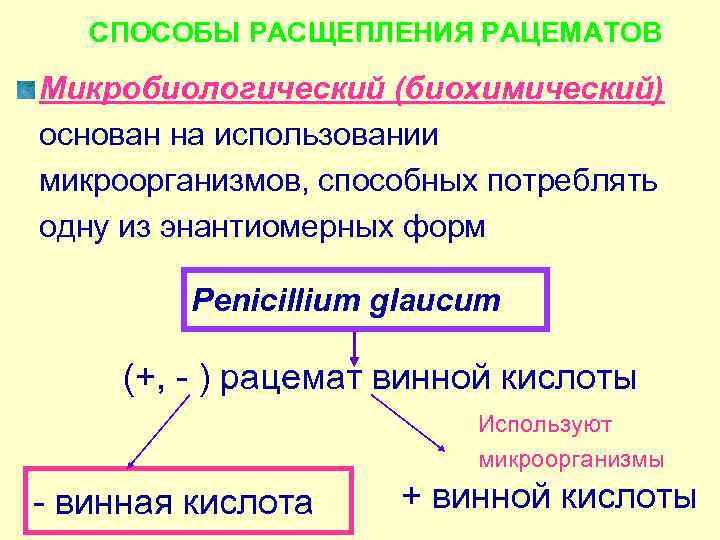
СПОСОБЫ РАСЩЕПЛЕНИЯ РАЦЕМАТОВ Микробиологический (биохимический) основан на использовании микроорганизмов, способных потреблять одну из энантиомерных форм Penicillium glaucum (+, - ) рацемат винной кислоты Используют микроорганизмы - винная кислота + винной кислоты
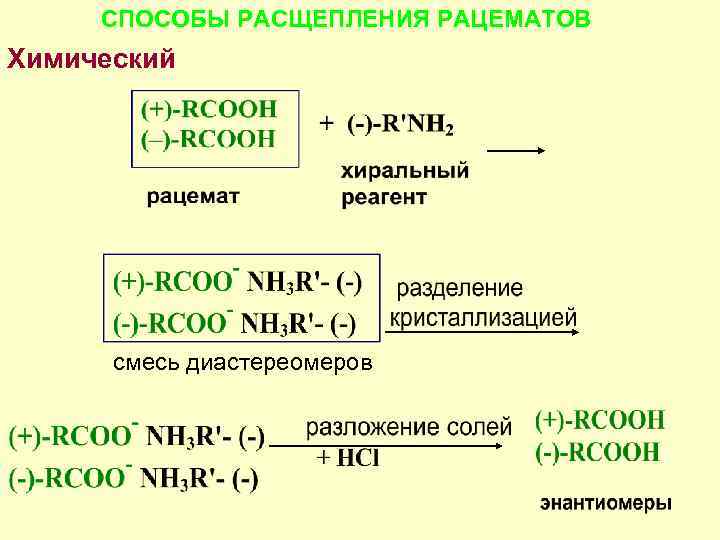
СПОСОБЫ РАСЩЕПЛЕНИЯ РАЦЕМАТОВ Химический - энантиомеры переводят в диастереомеры с последующим их разделением смесь диастереомеров

АФФИННАЯ ХРОМАТОГРАФИЯ разделение рацемической смеси с помощью оптически активных хиральных сорбентов Аффинная хроматография основана на способности хирального сорбента связывать один из энантиомеров смеси Так, в биохимической практике при пропускании через хроматографическую колонку с хиральным сорбентом биоэкстрактов выделяют: белки - ферменты, моноклональные антитела, рецепторные белки и др.

Эпиграф к курсу лекций по БОХ l «Химики и врачи – это те, кто на самом l деле понимают мир» Л. Полинг l
БИООРГАНИЧЕСКАЯ ХИМИЯ Биоорганическая химия — химическая дисциплина, изучающая пространственную структуру, свойства и механизмы превращений углеродистых соединений, лежащих в основе процессов жизнедеятельности и влияющих на них, в непосредственной связи с их биологическими функциями БИООРГАНИЧЕСКАЯ ХИМИЯ Органическая химия природных соединений Молекулярная биология Биологическая химия
Цель изучения биоорганической химии - формирование системных знаний о взаимосвязи между пространственным строением, термодинамической устойчивостью, свойствами и функциями природных органических соединений, являющихся метаболитами и структурными компонентами клеток и тканей (полисахариды, пептиды, белки и нуклеиновые кислоты)

акад. Виталий Гольданский Жизнь – это особая форма существования биополимерных тел (систем), характеризующихся хиральной чистотой и способностью к самоорганизации и саморепликации в условиях постоянного обмена с окружающей средой веществом, энергией и информацией 1986 г.

Специфика биоорганического подхода к изучению жизнедеятельности lиспользование молекулярных моделей, т. е. синтетических пептидов, нуклеотидов, других биологически значимых молекул и биоорегуляторов; lих модифицированных аналогов; lпроведение исследований как in vitro, так и in vivo; lстремление понять и объяснить почему клетка, ее структуры, макромолекулы, биорегуляторы организованы так на основе современных химических представлений.

Объекты, изучаемые биоорганической химией 1. Низкомолекулярные метаболиты и биорегуляторы Оксикислоты Кетокислоты Аминокислоты Моносахариды Высшие жирные кислоты Витамины Гормоны Нуклеотиды и др. 2. Биомакромолекулы Полисахариды Белки Нуклеиновые кислоты Фосфолипиды Синтетические полимерные материалы, применяемые в медицине

Теоретическая основа БОХ l 1. Теория строения А. М. Бутлерова, доп. А)квантовой структурой элементов-органогенов Б)теорией валентных связей Полинга и теорией молекулярных орбиталей Малликена и Хюккеля В)стереохимическими представлениями Вант-Гоффа, Э. Фишера, Бартона. Г)абсолютной конфигурацией стереоизомеров КИП Д)механизмами органич. реакций Н. Семенов, Ингольд и др. Е)теорией кислотности и основности Бренстеда-Лоури, Льюиса.

1 s 22 px 12 py 12 pz 0 1 s 22 s 12 px 12 py 12 pz 1 I валентное состояние - sp 3 - гибридизация II валентное состояние – sp 2 - гибридизация III валентное состояние – sp - гибридизация
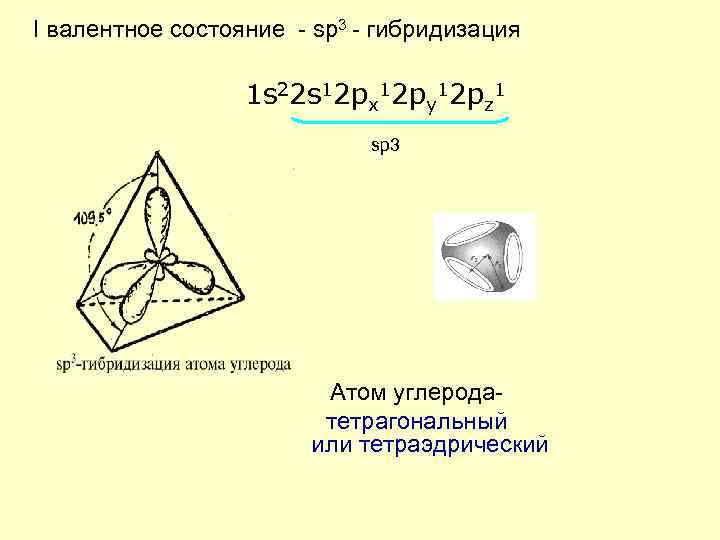
I валентное состояние - sp 3 - гибридизация 1 s 22 s 12 px 12 py 12 pz 1 sp 3 Атом углерода- тетрагональный или тетраэдрический

Химическое строение и структура l Химическое строение (конституция)последовательность соединения атомов в молекуле с учетом характера химических связей между ними. l Структура – взаимное пространственное расположение атомов (их ядер) друг относительно друга.
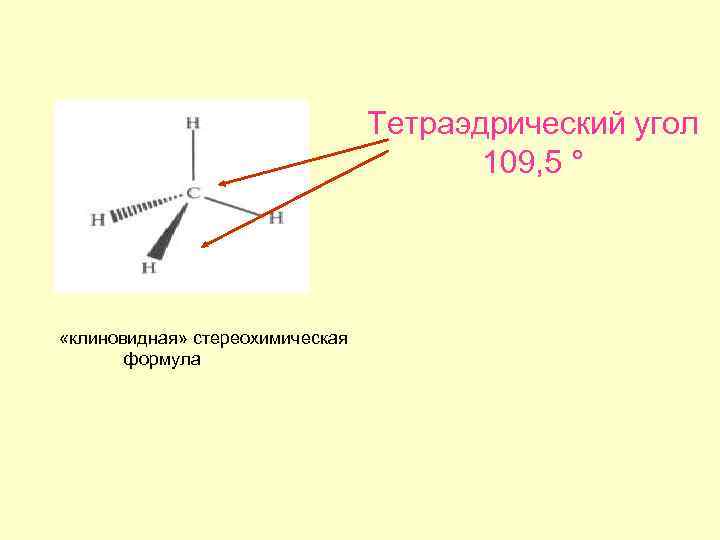
Тетраэдрический угол 109, 5 ° «клиновидная» стереохимическая формула
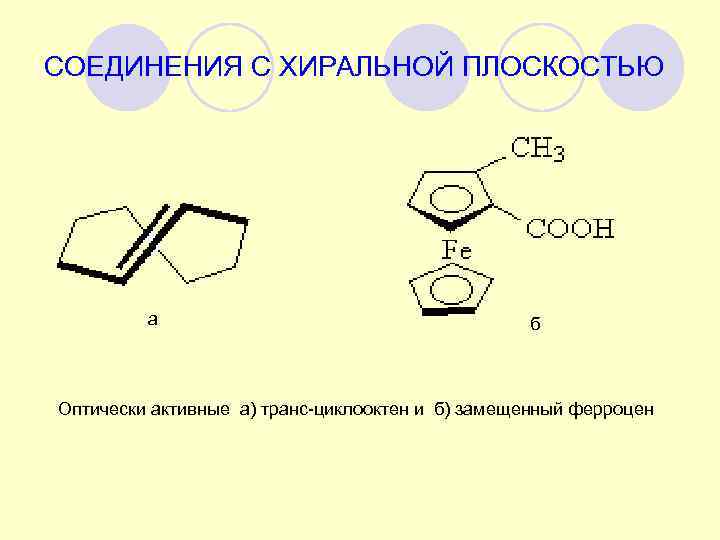
СОЕДИНЕНИЯ С ХИРАЛЬНОЙ ПЛОСКОСТЬЮ а б Оптически активные а) транс-циклооктен и б) замещенный ферроцен
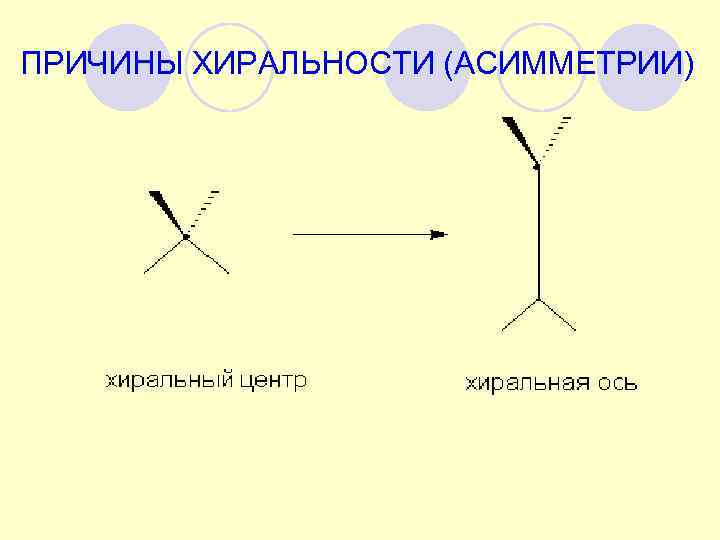
ПРИЧИНЫ ХИРАЛЬНОСТИ (АСИММЕТРИИ)
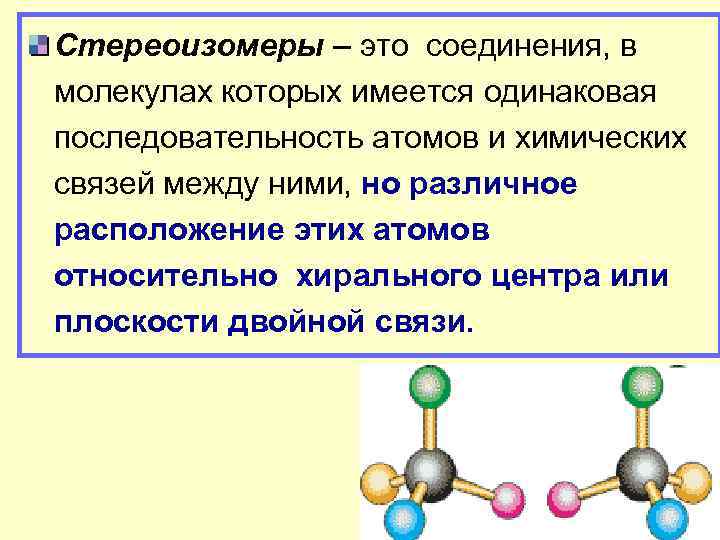
Стереоизомеры – это соединения, в молекулах которых имеется одинаковая последовательность атомов и химических связей между ними, но различное расположение этих атомов относительно хирального центра или плоскости двойной связи.

Основы стереохимии заложены работами Вант-Гоффа и Ле Беля (1874 г. ), которые независимо друг от друга высказали мысль о тетраэдрической конфигурации sp 3 гибридного атома углерода
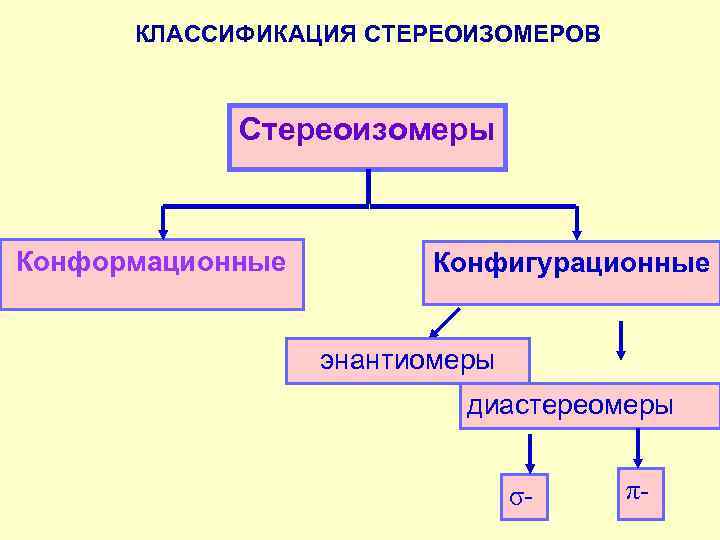
КЛАССИФИКАЦИЯ СТЕРЕОИЗОМЕРОВ Стереоизомеры Конформационные Конфигурационные энантиомеры диастереомеры σ- π-

В стереохимии молекулу рассматривают как геометрическое тело в трехмерном пространстве молекула симметрична, если при перестановке в ней местами атомов или атомных групп не происходит никаких изменений ее структуры

Элементы симметрии : 1 рода - оси симметрии Сn l 2 рода l - плоскости симметрии σ l - центры симметрии i l - оси зеркального отражения Sn l
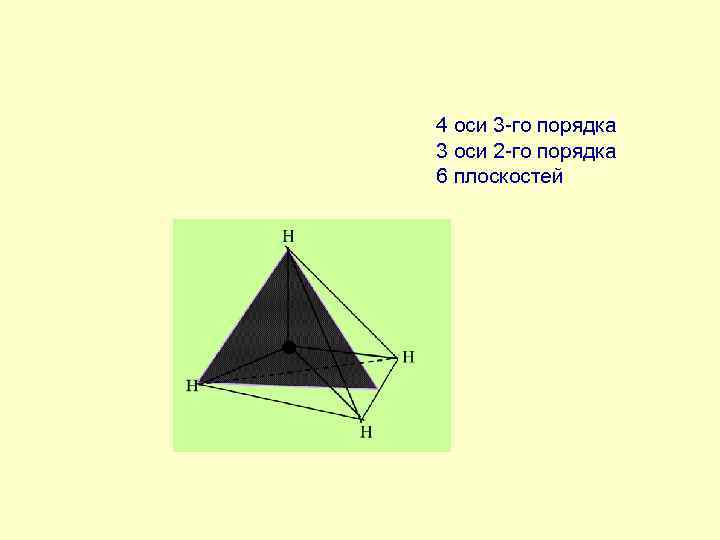
4 оси 3 -го порядка 3 оси 2 -го порядка 6 плоскостей
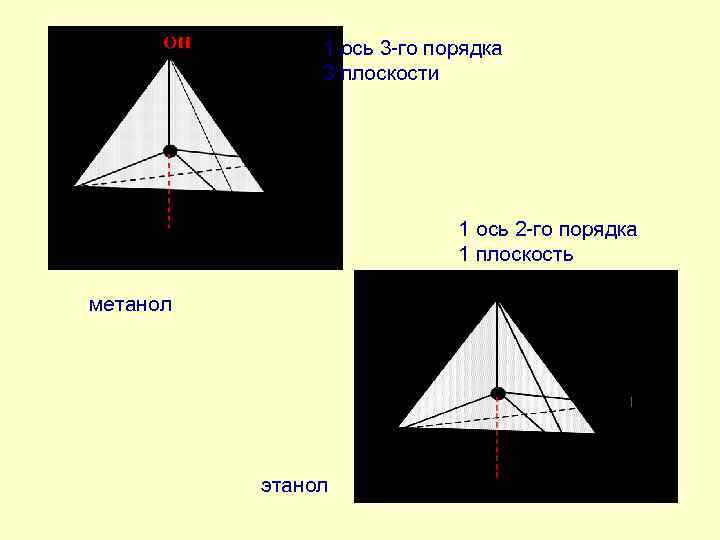
1 ось 3 -го порядка 3 плоскости 1 ось 2 -го порядка 1 плоскость метанол этанол
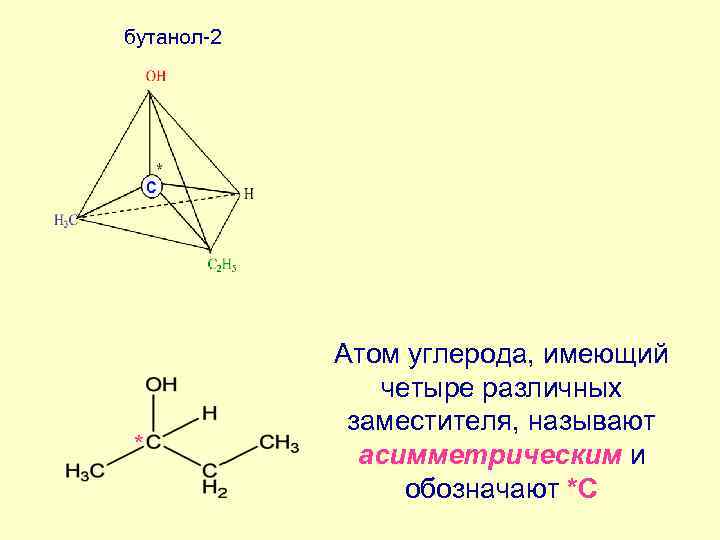
бутанол-2 * Атом углерода, имеющий четыре различных заместителя, называют асимметрическим и обозначают *С

ХИРАЛЬНОСТЬ Молекулы, не обладающие элементами симметрии 2 рода и несовместимые со своим зеркальным изображением, называют хиральными Термин «хиральность» (рукоподобие, сheir – рука, греч. ) заключается в парности существованиии молекул, относящихся друг к другу как правая и левая рука (предмет и его зеркальное отображение). Асимметрический атом углерода – частный случай хирального центра
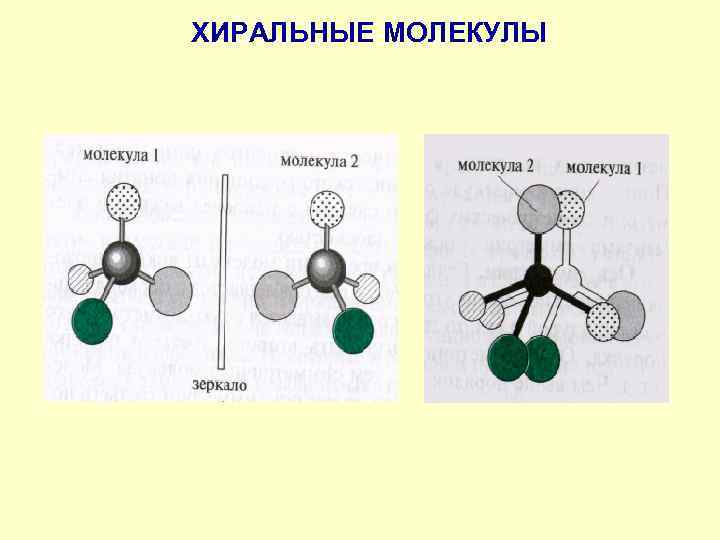
ХИРАЛЬНЫЕ МОЛЕКУЛЫ
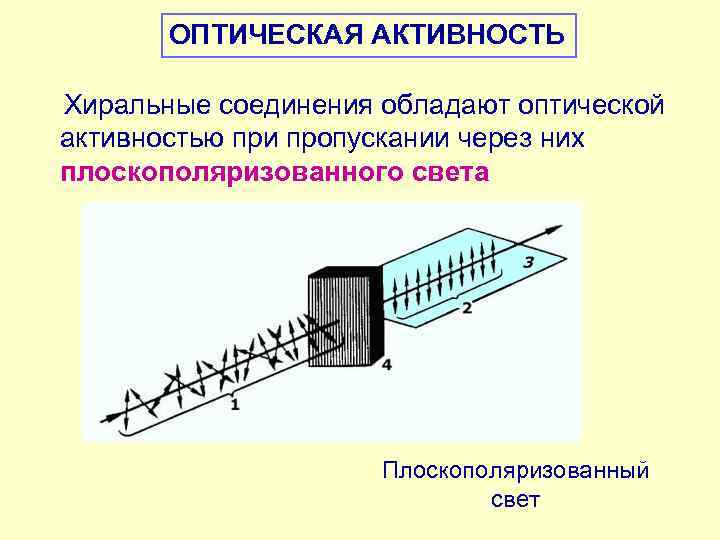
ОПТИЧЕСКАЯ АКТИВНОСТЬ Хиральные соединения обладают оптической активностью при пропускании через них плоскополяризованного света Плоскополяризованный свет
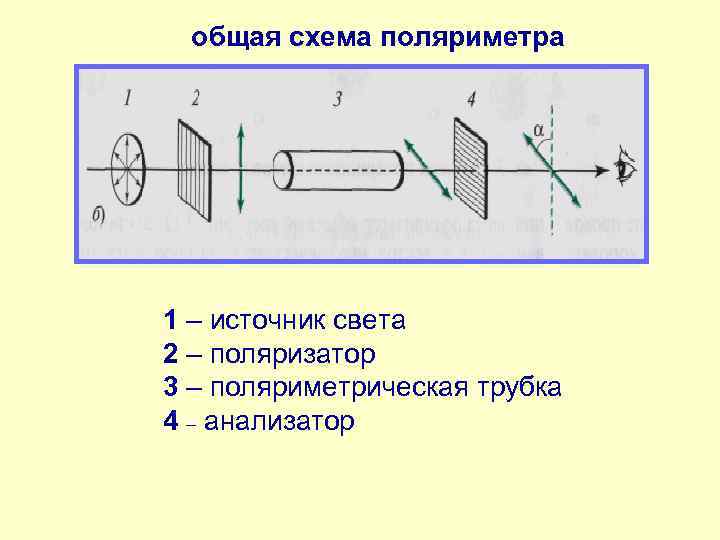
общая схема поляриметра 1 – источник света 2 – поляризатор 3 – поляриметрическая трубка 4 – анализатор
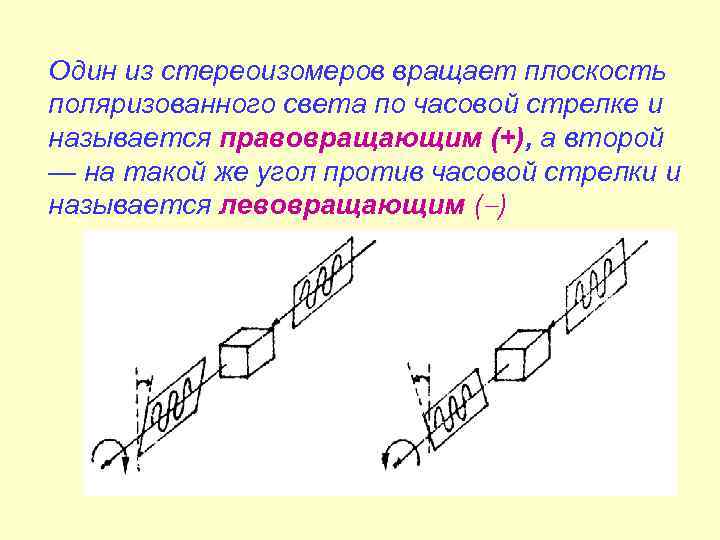
Один из стереоизомеров вращает плоскость поляризованного света по часовой стрелке и называется правовращающим (+), а второй — на такой же угол против часовой стрелки и называется левовращающим ( )
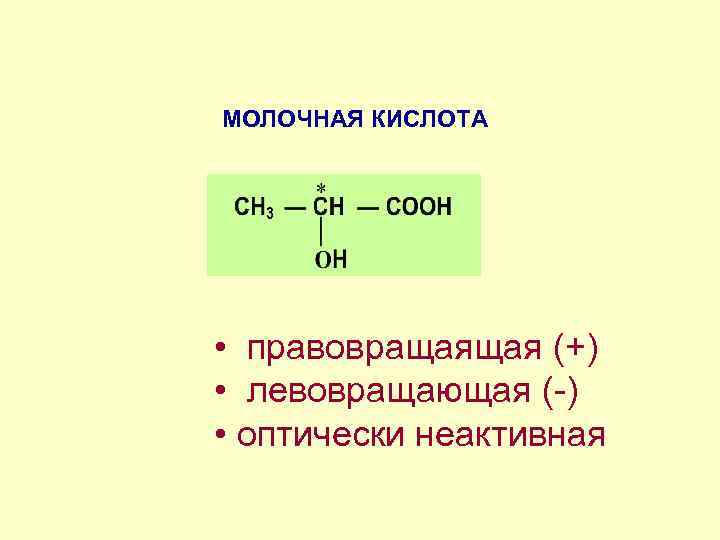
МОЛОЧНАЯ КИСЛОТА • правовращаящая (+) • левовращающая (-) • оптически неактивная

ПРОЕКЦИОННЫЕ ФОРМУЛЫ ФИШЕРА 1. Углеродную цепь располагают вертикально 2. Вверху располагают старшую функциональную группу 3. Хиральный атом углерода переносится на плоскость в точку пересечения горизонтальной и вертикальной линий 4. Расположенные по горизонтали заместители направлены к наблюдателю, а по вертикали – «уходят» от наблюдателя
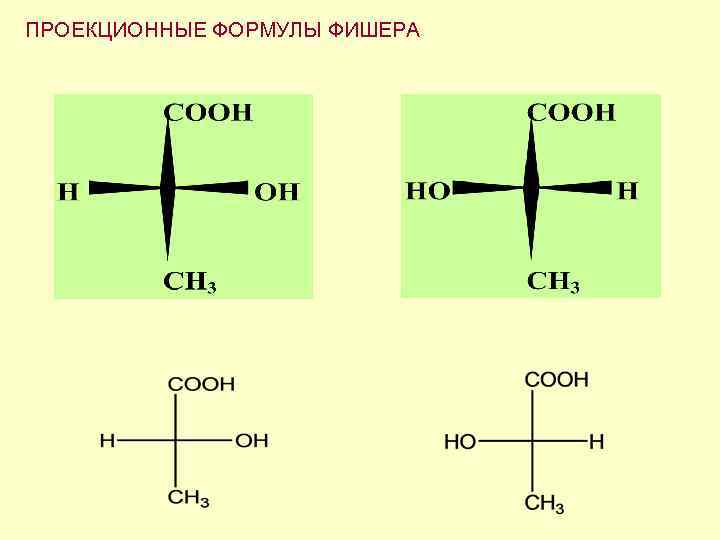
ПРОЕКЦИОННЫЕ ФОРМУЛЫ ФИШЕРА

Относительная D-, L- номенклатура Э. Фишер, М. А. Розанов (1906) (+), D - глицериновый альдегид (-), L- глицериновый альдегид ГЛИЦЕРИНОВЫЙ АЛЬДЕГИД Конформационный стандарт
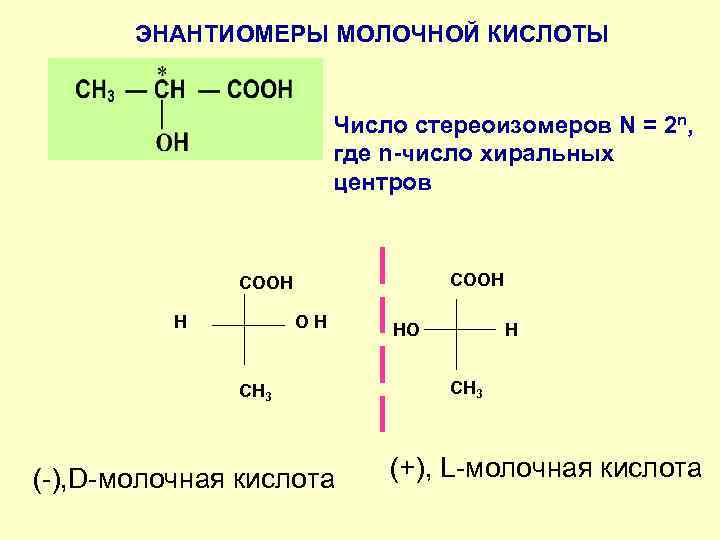
ЭНАНТИОМЕРЫ МОЛОЧНОЙ КИСЛОТЫ Число стереоизомеров N = 2 n, где n-число хиральных центров СOOH H OH СН 3 (-), D-молочная кислота HО H СН 3 (+), L-молочная кислота

Определение конфигурации l Конфигурация- определенное пространственное расположение заместителей относительно хирального центра или плоскости двойной связи без учета различий в структуре за счет вращения групп по линии σ -связей.

ЭНАНТИОМЕРИЯ Энантиомеры – пары стереоизомеров, молекулы которых относятся друг к другу как предмет и несовместимое с ним зеркальное изображение в идеальном плоском зеркале и обладают в ахиральной среде одинаковыми физическими и химическими свойствами, кроме знака оптического вращения

РАЦЕМИЧЕСКАЯ СМЕСЬ Ø Смесь равных количеств энантиомеров называется рацемической (рацематом ) Ø Рацематы не обладают оптической активностью SN 1 l In vivo гликолиз D-глюкоза L(+)-лактат
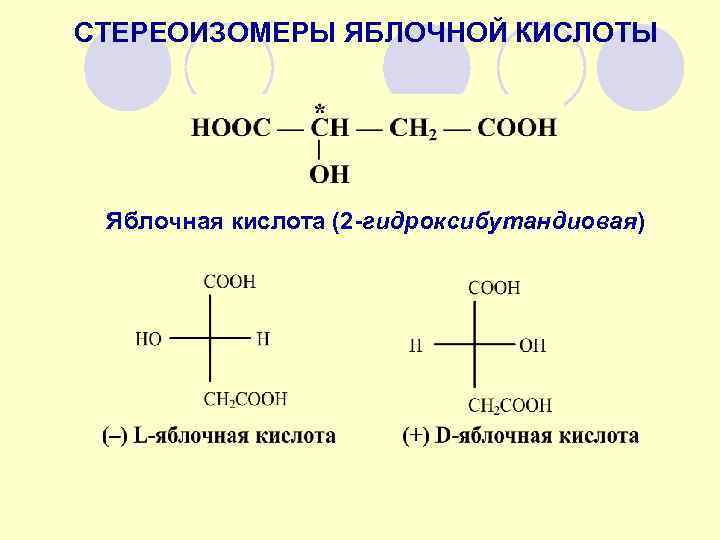
СТЕРЕОИЗОМЕРЫ ЯБЛОЧНОЙ КИСЛОТЫ Яблочная кислота (2 -гидроксибутандиовая)
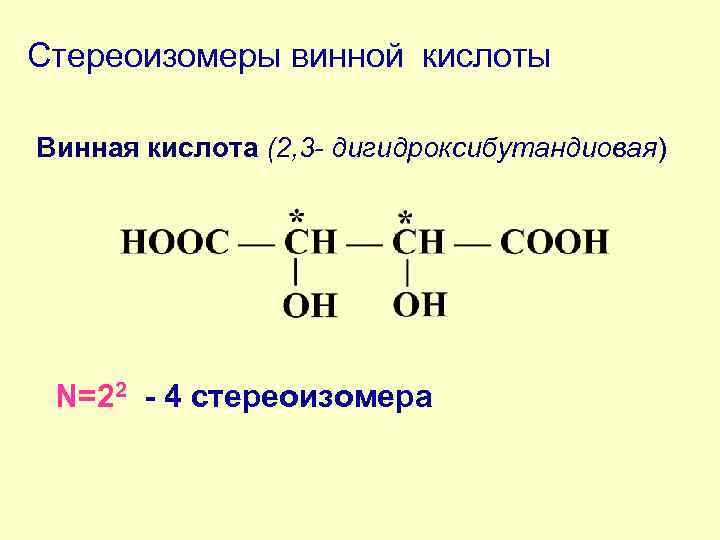
Стереоизомеры винной кислоты Винная кислота (2, 3 - дигидроксибутандиовая) N=22 - 4 стереоизомера
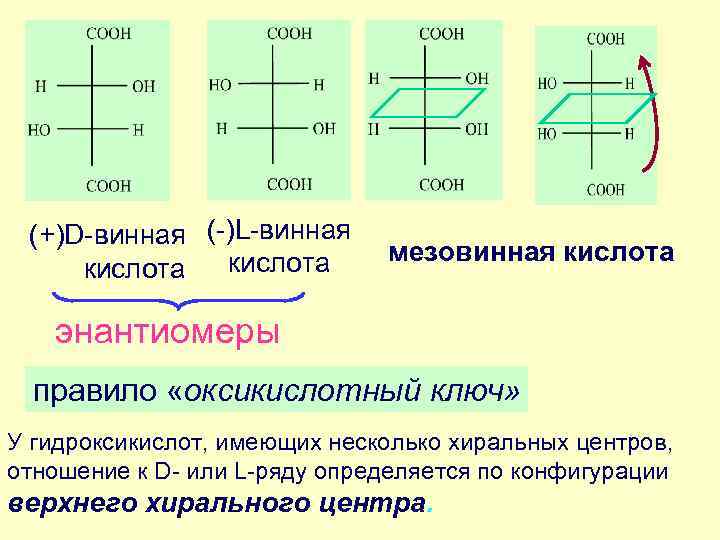
(+)D-винная (-)L-винная кислота мезовинная кислота энантиомеры правило «оксикислотный ключ» У гидроксикислот, имеющих несколько хиральных центров, отношение к D- или L-ряду определяется по конфигурации верхнего хирального центра.

D- и L – винные кислоты - энантиомеры D-винная кислота и мезовинная к-та – диастереомеры L-винная кислота и мезовинная к-та – диастереомеры Диастереомеры — стереоизомеры, не являющиеся зеркальным отражением друга и обладающие различными физическими и химическими свойствами Смесь D- и L - винных кислот называют виноградной кислотой (рацемическая смесь)

Абсолютная конфигурация стереоизомеров l В 1951 году голландский ученый Бийвоет с использованием особого метода рентгеноструктурного анализа определил абсолютную конфигурацию Cs, Rb-соли D-винной кислоты и некоторых солей аминокислот и таким образом подтвердил что правовращающий глицериновый альдегид имеет D-конфигурацию.

R, S-номенклатура (КИП) Кан, Прелог, Ингольд принадлежность к ряду R- или S- определяется порядком убывания старшинства заместителей у хирального центра Старшинство заместителей – по порядковому номеру в табл. Менделеева Убывание по часовой стрелке - R (от лат. rectus правый) Убывание против часовой стрелки - S (от лат. sinister левый).
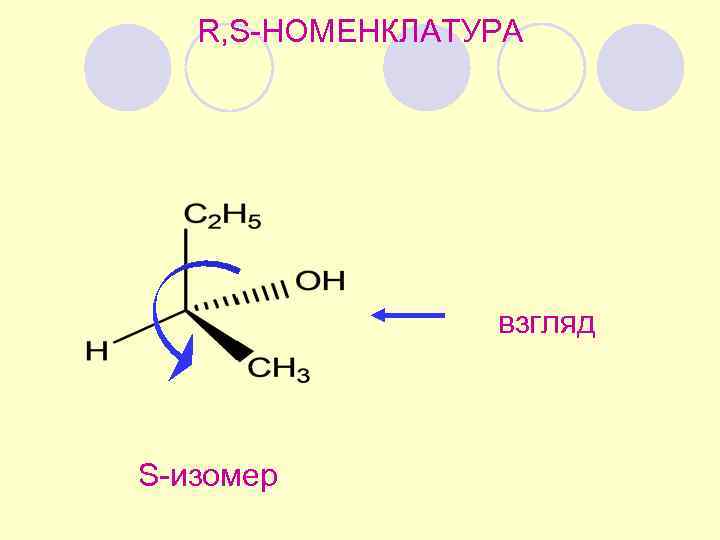
R, S-НОМЕНКЛАТУРА взгляд S-изомер
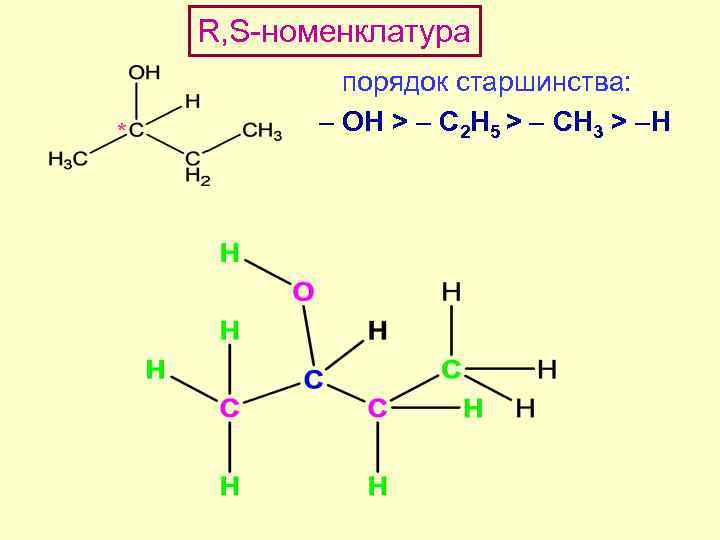
R, S-номенклатура * порядок старшинства: ОН > C 2 H 5 > CH 3 > H
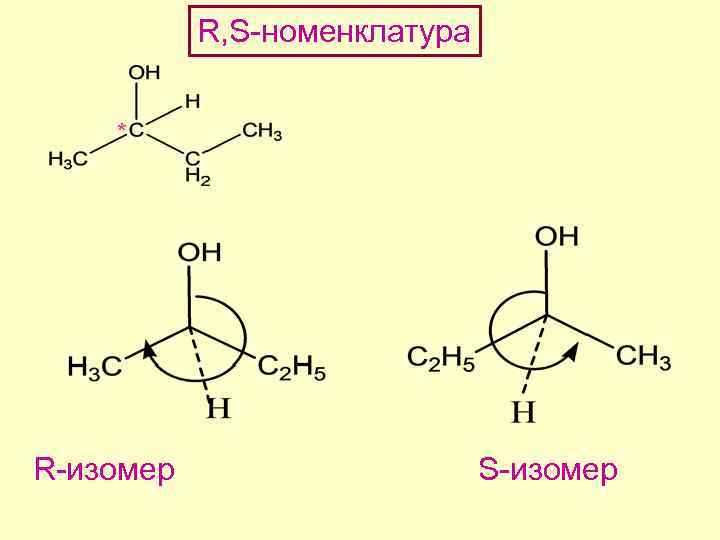
R, S-номенклатура * R-изомер S-изомер
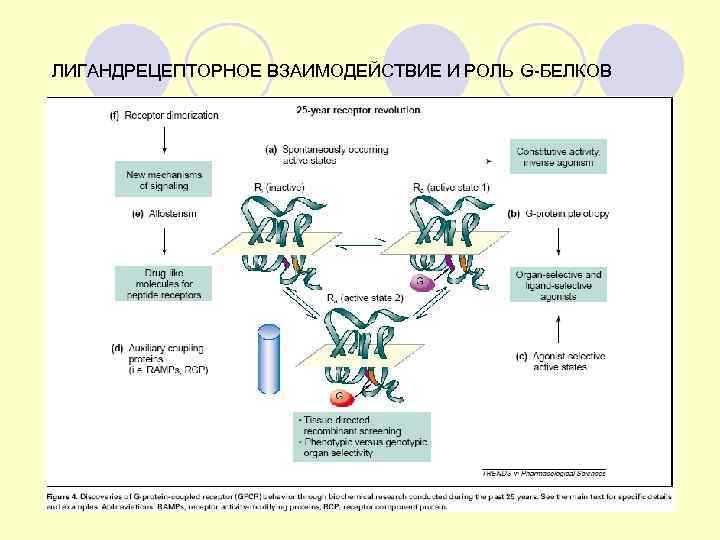
ЛИГАНДРЕЦЕПТОРНОЕ ВЗАИМОДЕЙСТВИЕ И РОЛЬ G-БЕЛКОВ
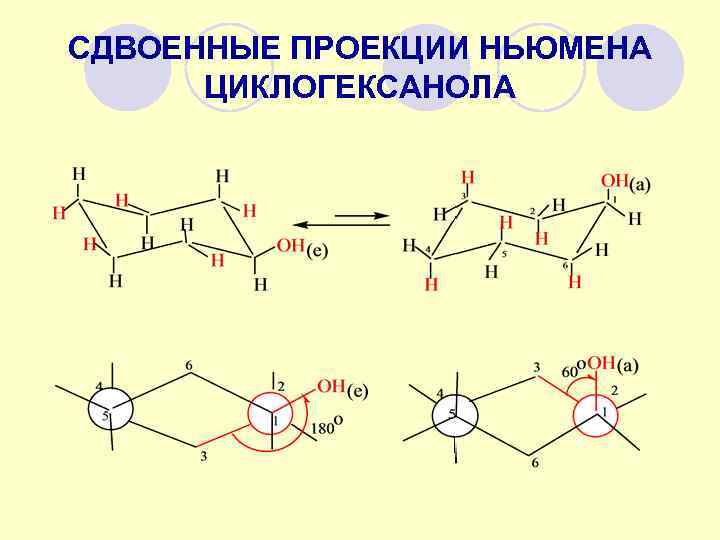
СДВОЕННЫЕ ПРОЕКЦИИ НЬЮМЕНА ЦИКЛОГЕКСАНОЛА
лекц4 конформации.ppt