Slayd_k_l_1.ppt
- Количество слайдов: 28

Кафедра общей и неорганической химии Курс лекций по дисциплине «ХИМИЧЕСКИЕ ОСНОВЫ ПРОИЗВОДСТВА» Читает доцент, кандидат технических наук Брагазина Ольга Александровна 2013 г.

Литература 1. Коржуков Н. Г. Общая химия. 2001 г. 2. Коржуков Н. Г. Общая и неорганическая химия. 2004 г. 3. Глинка Н. Л. Общая химия. 4. Неорганическая химия. Сборник задач (№ 1996). 5. Неорганическая химия. Лабораторный практикум (№ 698).

Лекция № 1 ОСНОВНЫЕ ЗАКОНЫ И ПОНЯТИЯ ХИМИИ

ЗАКОН СОХРАНЕНИЯ МАССЫ ( открытие принадлежит М. В. Ломоносову и Лавуазье) Примеры: 1. В доменном процессе m руды + топлива + воздуха = = m чугуна + шлака + пыли + газа 2. В химической реакции H 2 + Cl 2 = 2 HCl В химико-металлургических процессах закон не знает отклонений

ЗАКОН ПОСТОЯНСТВА СОСТАВА (открыт французским химиком Прустом в 1799 г. ) Пример: 2 H 2 + O 2 = 2 H 2 O Cu. SO 4 5 H 2 O Cu. SO 4 + 5 H 2 O CH 4 + 2 O 2 CO 2 + 2 H 2 O ······ · Тi. O 2: Тi. O 1, 9 -2, 0. Дальтониды и бертоллиды H 2 O 11% Н 89% О

Распространенность элементов в природе Кислород (О) ~ 47% по массе; Кремний (Si) ~ 27% Далее следуют: Al, Fe, Ca, Na, K, Mg, H Все остальные элементы – 2 % Например: С – 0, 15 %; N – 0, 04 %; S – 0, 05 % 98 %

Атомные и молекулярные массы m. Al = 4, 5 10 -23 г m. C = 2 10 -23 г m. H 2 O = 3 10 -23 г 1 а. е. м. = 1/12 m. C = 0, 166 10 -23 г Относительная атомная масса (Аr) Аr Аl = (4, 5 10 -23)/(0, 166 10 -23) = 27 а. е. м. Абсолютная масса атома равна: Аr · 1 а. е. м.

Относительная молекулярная масса вещества (М ) r Мr Н 2 О = (3, 0 10 -23)/(0, 166 10 -23) = 18 а. е. м. Относительная молекулярная масса равна сумме относительных масс атомов, входящих в состав молекулы Mr(Н 2 О) = 2· 1 + 16 = 18 Mr(Н 2 SО 4) = 98 Абсолютная масса молекулы равна: Мr · 1 а. е. м.

Что такое моль? NA =12/(12 0, 166 10 -23) = 6, 022 1023 частиц - число (или постоянная) Авогадро моль-1 Молярная масса (М) –масса 1 моля в-ва г/моль M (Н 2 О) = 18 г/моль M (Н 2 SО 4) = 98 г/моль М = Мr m(молекулы Н 2 О) = М / NA = 18 / 6, 02 · 1023 = 3 · 10 -23 г m(атома Al) = M / NA = 27 / 6, 02 · 1023 = 4, 5 · 10 -23 г

Количество вещества или число молей вещества ( ) или (n) = m / Mr (n) = N / NA

Стехиометрические соотношения в химии Стехиометрия – раздел химии, изучающий объемные и массовые соотношения между реагирующими веществами. 4 Fe. S + 7 O 2 = 2 Fе 2 O 3 + 4 SO 2 Основной закон стехиометрии Отношение количеств реагирующих веществ (в моль) равно отношению соответствующих коэффициентов в уравнении реакции

Что такое эквивалент ? Мэкв. Н = 1 г/моль 9 е. м. Al – 1 е. м. H Мэкв. О = 8 г/моль 9 г Be – 25 г оксида Be Мэкв(Al) = 9 г SO 2 SO 3 8: 8 5, 3 : 8 Мэкв(S) = 5, 3 9 г Be — (25 – 9) г О { х г Вe — 8 г (О) 1 моль экв. Ве — 4, 5 г Fe. Cl 2 Мэкв(Fe) = 56/2 = 28 Мэкв = Аr / B Fe. Cl 3 Мэкв(Fe) = 56/3 19
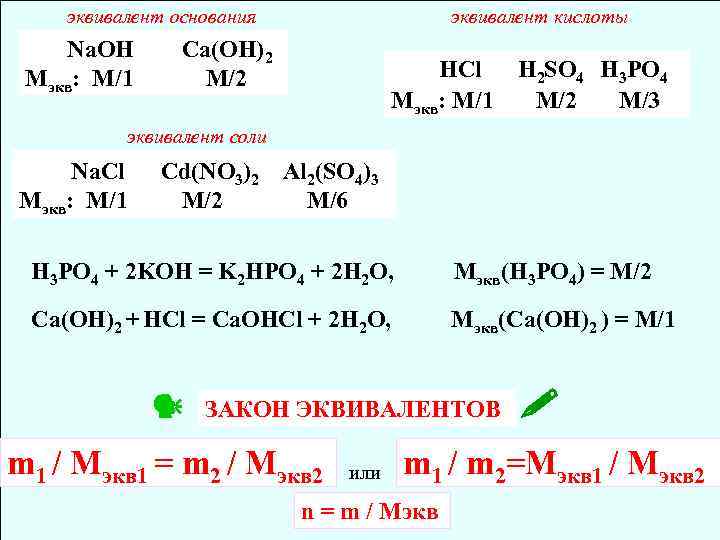
эквивалент основания Na. OH Мэкв: М/1 эквивалент кислоты Са(ОН)2 М/2 НCl Мэкв: М/1 Н 2 SO 4 H 3 PO 4 М/2 М/3 эквивалент соли Na. Cl Мэкв: М/1 Сd(NO 3)2 Al 2(SO 4)3 М/2 М/6 H 3 PO 4 + 2 KOH = K 2 HPO 4 + 2 H 2 O, Мэкв(H 3 PO 4) = M/2 Са(ОН)2 + НCl = Са. ОНCl + 2 H 2 O, Мэкв(Са(ОН)2 ) = M/1 ЗАКОН ЭКВИВАЛЕНТОВ m 1 / Мэкв 1 = m 2 / Мэкв 2 или m 1 / m 2=Мэкв 1 / Мэкв 2 n = m / Мэкв

Газовые законы Закон Авогадро Нормальные условия (н. у. ): Т°= 273, 15 К (0 C) Р°= 101325 Па 101, 325 105 к. Па 105 Па (1 атм. ) Мольный объем газа (VM) = 22, 4 дм 3/моль (л/моль) = V/ 22, 4 - число молей вещества Эквивалентный объём Н 2 и О 2 при н. у. : 2 г Н 2 22, 4 л 1 г Н 2 11, 2 л 32 г О 2 22, 4 л 8 г О 2 5, 6 л

Объединенный (универсальный) газовый закон PV/ T= const PVм / T= R PVм = RT R = (105 22, 4 103)/273 = 8, 31 Дж/(моль K) Уравнение Клапейрона-Менделеева PV = RT Подставляя = (m/Mr) p. V = (m/Mr)RT Уравнение Клапейрона PV/T = po. Vo/To Vo = (PV To) /(T Po)

Определение молекулярной массы газа или пара 1. По ур-ю Клапейрона-Менделеева Mr = m. RT/(PV) 2. Приводим объем газа (V) к н. у. (V ) по у-ю Клапейрона m — Vo х — 22, 4 л, х = Mr 3. По относительной плотности D 1 -2 = m 1 / m 2 при P, V, T = const D 1 -2 = M 1 / M 2 M 1= 2 D(водород) M 1 = 29 D(воздух)

Что такое парциальное давление ? Давление, которое производит одна из составных частей газовой смеси, называется парциальным давлением данной составной части Закон парциальных давлений (закон Дальтона) Общее давление смеси газов, не вступающих друг с другом в химическое взаимодействие, равно сумме парциальных давлений ее составляющих частей Робщее = Р 1 + Р 2 + …+ Рі , где Р 1, Р 2 , … Рі - парциальные давления газов

Более подробные сведения о том, что такое эквивалент и закон эквивалентов смотрите на сайте кафедры Дополнительные материалы к лекциям по курсу «Химические основы производства» Лекция № 1

Дополнительные материалы к лекциям по курсу «Химические основы производства» Лектор доцент кандидат технических наук Брагазина Ольга Александровна

Лекция № 1 ОСНОВНЫЕ ЗАКОНЫ И ПОНЯТИЯ ХИМИИ

Эквивалент элемента (Э) – это такая масса его, которая соединяется с единицей (точнее 1, 008) массы водорода или с 8 единицами массы кислорода или замещает эти количества в их соединениях. ЭН = 1 ЭО = 8 Эквивалент элемента в соединении находится как атомная масса, деленная на валентность элемента или его степень окисления Как находятся эквиваленты сложных веществ (кислот, оснований, солей) – дано на лекции

Закон эквивалентов Массы реагирующих веществ эквиваленты m 1 / m 2= Э 1 / Э 2 относятся как их Вещества реагируют между собой в эквивалентных количествах или число эквивалентов участников процесса есть постоянная величина n 1 = n 2 = n 3 =…соnst где n = m / Э - число г-экв. m – масса вещества, Э – эквивалент вещества

Как рассчитать эквивалент кислоты в химической реакции ? H 2 SO 4 + 2 Na. OH = Na 2 SO 4 + 2 H 2 O H 2 SO 4 + Na. OH = Na. HSO 4 + H 2 O

Как рассчитать эквивалент основания в химической реакции ? Cr(OH)3 + 3 HCl = Cr. Cl 3 + 3 H 2 O Cr(OH)3 + 2 HCl = Cr. OHCl 2 + 2 H 2 O

Как рассчитать эквивалент соли в химической реакции ? Na 2 CO 3 + HCl = Na. HCO 3 + Na. Cl Na 2 CO 3 + 2 HCl = 2 Na. Cl + H 2 CO 3

Э оксида в обменных и кислотно-основных реакциях CO 2 + Na. OH = Na. HCO 3 СО 2 + 2 Na. OH = Na 2 CO 3 + H 2 O

Современная трактовка понятия «Эквивалент» Эквивалентом называют реальную или условную частицу, соответствующую одному протону (Н+), или одному гидроксилу (ОН-), или одному единичному заряду в данной обменной реакции Фактор эквивалентности (f) показывает, какую часть составляет эквивалент от молекулы. 0<f<1 HCl: Э = М/1 f = 1 H 2 SO 4: Э = М/2 f = 1/2 H 3 PO 4: Э = М/3 f = 1/3

“Моль эквивалентов” (моль экв. ) и “молярная масса эквивалента” Мэкв. 1 моль экв. содержит 6, 02 · 1023 эквивалентов Масса 1 моль экв. , выраженная в граммах, называется молярной массой эквивалента (Мэкв) Мэкв = fэкв · М Число моль экв. : nэкв = m / Mэкв [г/моль экв]
Slayd_k_l_1.ppt