lect_org_6-1.ppt
- Количество слайдов: 119

Кафедра общей и медицинской химии Лекция 7 -I Углеводы. Моно- и дисахариды Хроматографические методы исследования. 1

Углево ды — органические вещества, содержащие карбонильную группу и несколько гидроксильных групп. Они входят в состав клеток и тканей всех живых и растительных организмов. Название углеводов сложилось исторически, для многих углеводов (УВ) О: H как в воде и общая формула – Сn(H 2 O)n. Растениями углеводы образуются в процессе фотосинтеза из CO 2 и Н 2 О: 6 CO 2 + 6 Н 2 О C 6 H 12 O 6 По способности к гидролизу УВ делят на простые и сложные. УВ сложные простые (гидролизуются) (не гидролизуются) моносахариды олигосахариды n ≤ 10 Полисахариды n > 10 2
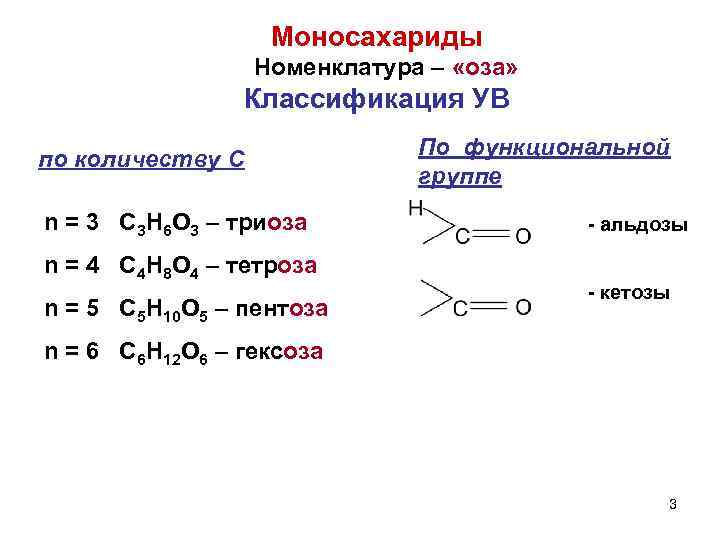
Моносахариды Номенклатура – «оза» Классификация УВ по количеству С По функциональной группе n = 3 C 3 H 6 O 3 – триоза n = 4 C 4 H 8 O 4 – тетроза n = 5 C 5 H 10 O 5 – пентоза - альдозы - кетозы n = 6 C 6 H 12 O 6 – гексоза 3
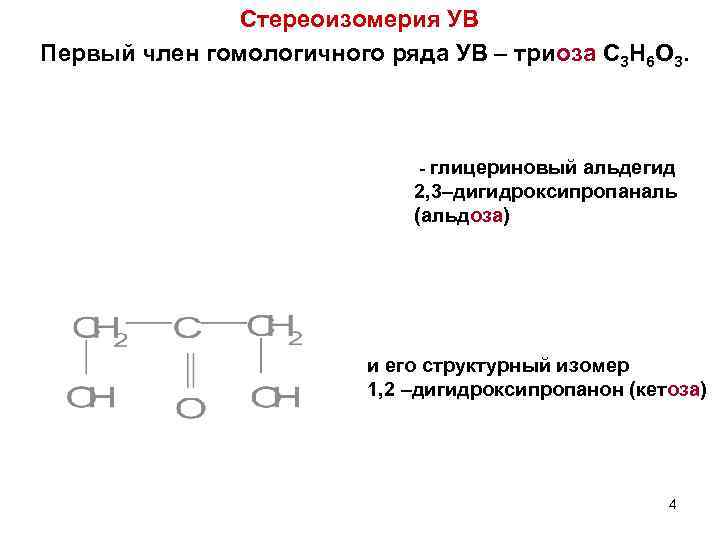
Стереоизомерия УВ Первый член гомологичного ряда УВ – триоза C 3 H 6 O 3. - глицериновый альдегид 2, 3–дигидроксипропаналь (альдоза) и его структурный изомер 1, 2 –дигидроксипропанон (кетоза) 4
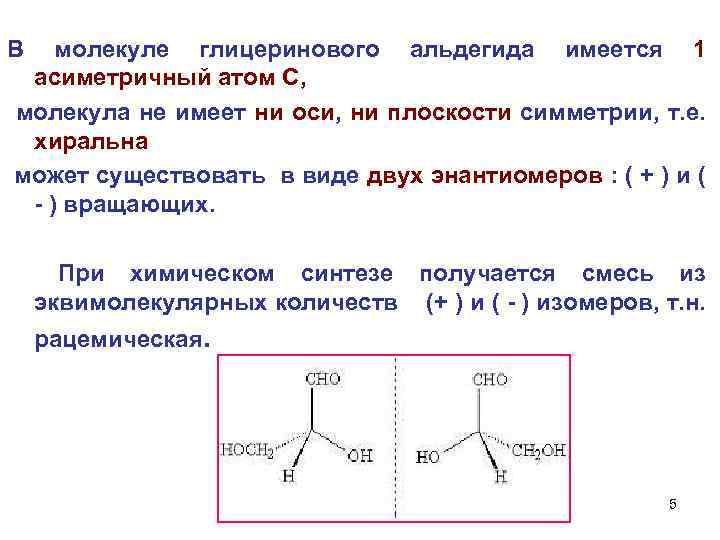
В молекуле глицеринового альдегида имеется 1 асиметричный атом С, молекула не имеет ни оси, ни плоскости симметрии, т. е. хиральна может существовать в виде двух энантиомеров : ( + ) и ( - ) вращающих. При химическом синтезе получается смесь из эквимолекулярных количеств (+ ) и ( - ) изомеров, т. н. рацемическая. 5

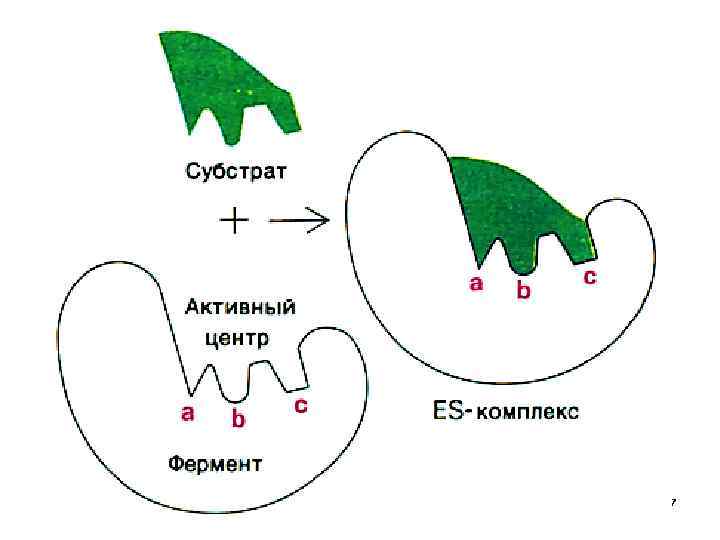
• Реакции, протекающие в живом организме приводят к одному энантиомеру, т. е. стереоселективны. • Необходимо знать конфигурацию атомов в этих энантиомерах, ведь биохимические реакции – ферментативны, а конфигурация фермента должна совпадать с конфигурацией Sb, т. е. они должны подходить друг к другу, как ключ к замку 6
7
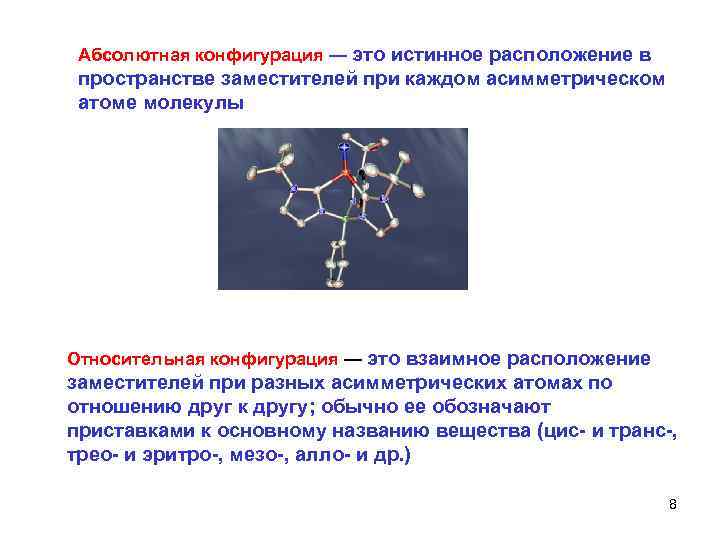
Абсолютная конфигурация — это истинное расположение в пространстве заместителей при каждом асимметрическом атоме молекулы Относительная конфигурация — это взаимное расположение заместителей при разных асимметрических атомах по отношению друг к другу; обычно ее обозначают приставками к основному названию вещества (цис- и транс-, трео- и эритро-, мезо-, алло- и др. ) 8
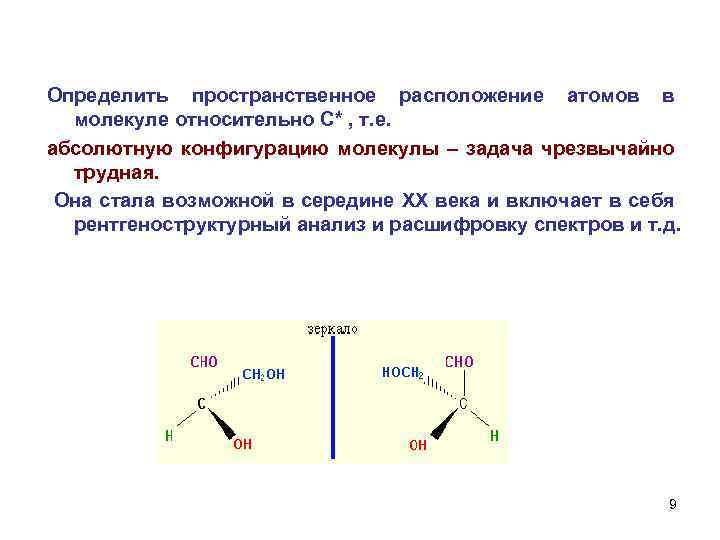
Определить пространственное расположение атомов в молекуле относительно С* , т. е. абсолютную конфигурацию молекулы – задача чрезвычайно трудная. Она стала возможной в середине ХХ века и включает в себя рентгеноструктурный анализ и расшифровку спектров и т. д. 9

Если абсолютную конфигурацию молекулы узнать трудно, то можно определить относительную. Химики в начале ХХ века ввели стереохимические ряды, условно обозначаемые как D и L, 1)выбрали конфигурационный стандарт 2) стали определять относительную конфигурацию изучаемого стереоизомера, сравнивая его со стандартом, 3) относить соединения к D и L стереохимическим рядам. За конфигурационный эталон в 1906 году Розанов А. принял глицериновый альдегид. 10
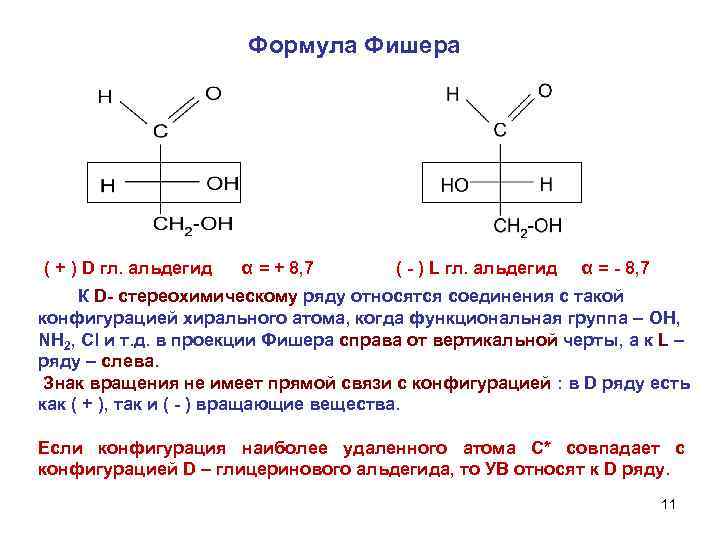
Формула Фишера ( + ) D гл. альдегид α = + 8, 7 ( - ) L гл. альдегид α = - 8, 7 К D- стереохимическому ряду относятся соединения с такой конфигурацией хирального атома, когда функциональная группа – OH, NH 2, Cl и т. д. в проекции Фишера справа от вертикальной черты, а к L – ряду – слева. Знак вращения не имеет прямой связи с конфигурацией : в D ряду есть как ( + ), так и ( - ) вращающие вещества. Если конфигурация наиболее удаленного атома С* совпадает с конфигурацией D – глицеринового альдегида, то УВ относят к D ряду. 11

Для изображения строения проекционные формулы Фишера. мнсх. используют Фишер Эмиль Герман (18521919), немецкий химик-органик, создатель научной школы, основоположник химии природных соединений. 1. Исследовал строение и синтезировал ряд производных пурина: кофеин, гуанин, аденин и др. 2. Ввел номенклатуру, создал рациональную классификацию и осуществил синтез многих углеводов. 3. Открыл специфичность действия ферментов. Основополагающие исследования по химии белков. Нобелевская премия (1902). 12
13
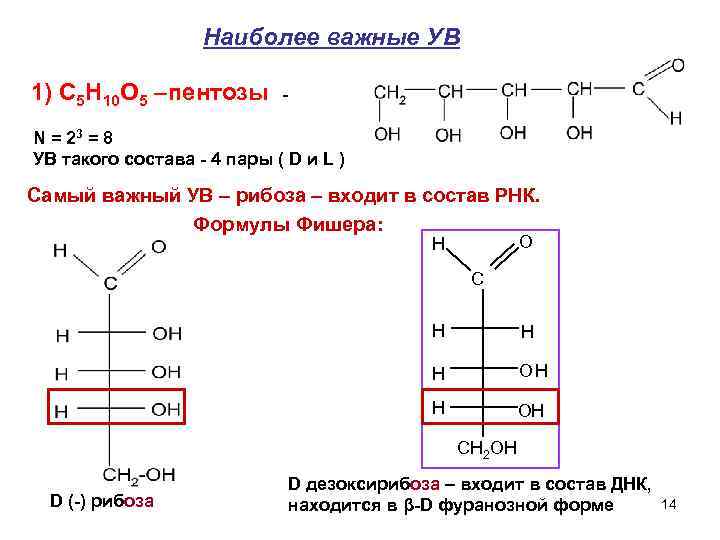
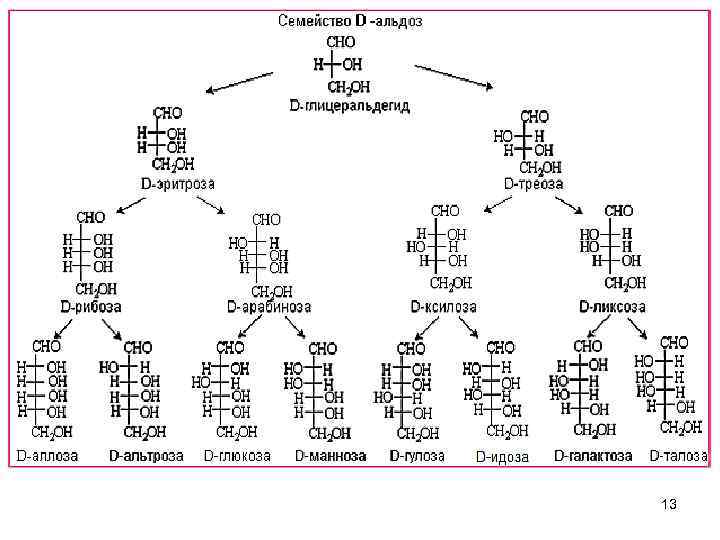
Наиболее важные УВ 1) C 5 H 10 O 5 –пентозы N = 23 = 8 УВ такого состава - 4 пары ( D и L ) Самый важный УВ – рибоза – входит в состав РНК. Формулы Фишера: O H C H H H OH H ОH СН 2 ОН D (-) рибоза D дезоксирибоза – входит в состав ДНК, находится в β-D фуранозной форме 14
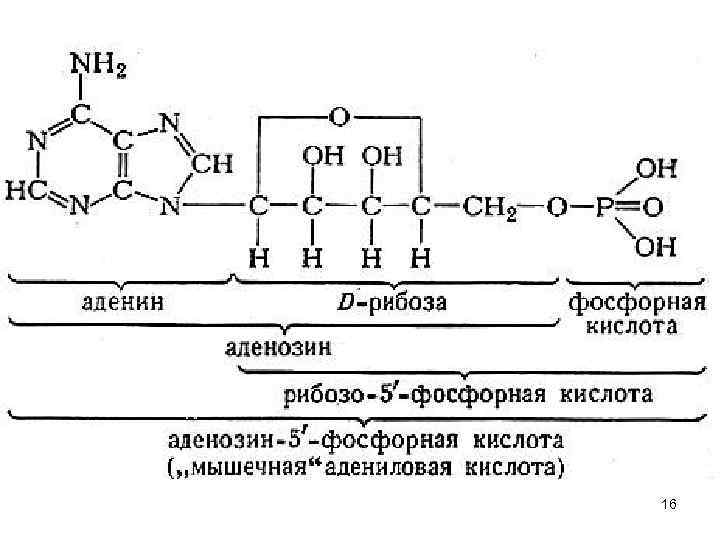
Рибоза входит в состав РНК. Может быть получена их гидролизом. Она используется в синтезе нуклеозидов. . Четыре основных нуклеозида - аденозин, гуанозин, цитидин и уридин - содержат в молекулах остаток рибозы. Из всех нуклеозидов наиболее важным для мышечной деятельности является аденозин, входящий в состав АТФ, основного источника энергии при 15 интенсивной мышечной деятельности.
16
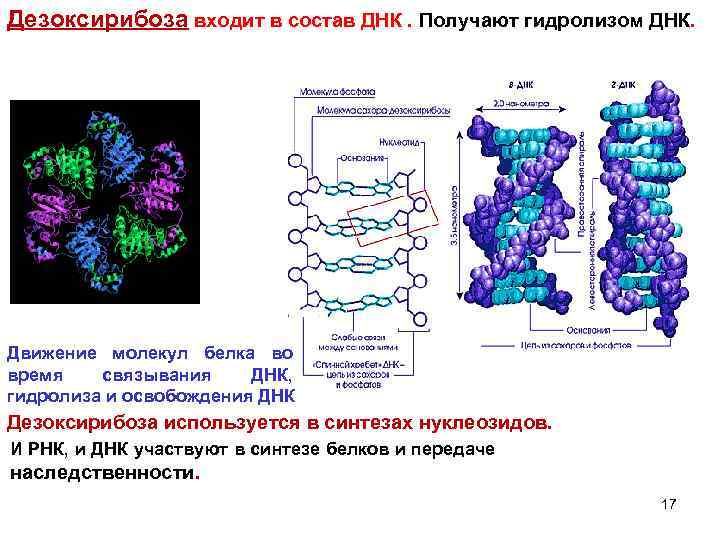
Дезоксирибоза входит в состав ДНК. Получают гидролизом ДНК. Движение молекул белка во время связывания ДНК, гидролиза и освобождения ДНК Дезоксирибоза используется в синтезах нуклеозидов. И РНК, и ДНК участвуют в синтезе белков и передаче наследственности. 17
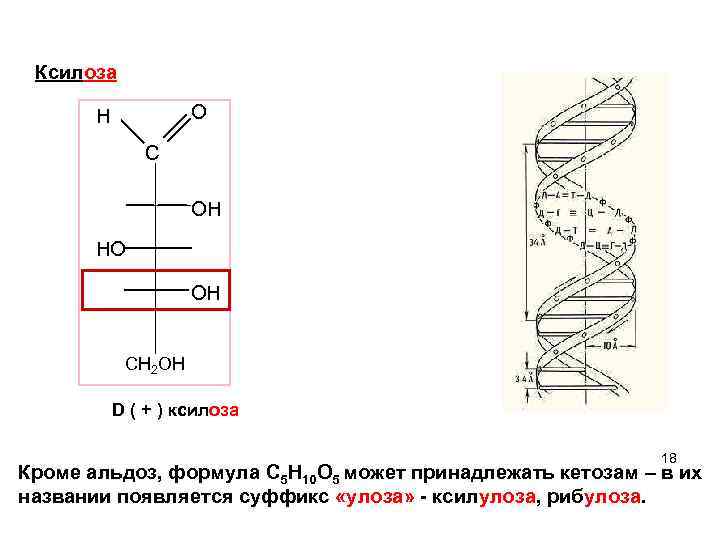
Ксилоза O H C ОH НO OН СН 2 ОН D ( + ) ксилоза 18 Кроме альдоз, формула C 5 H 10 O 5 может принадлежать кетозам – в их названии появляется суффикс «улоза» - ксилулоза, рибулоза. 18
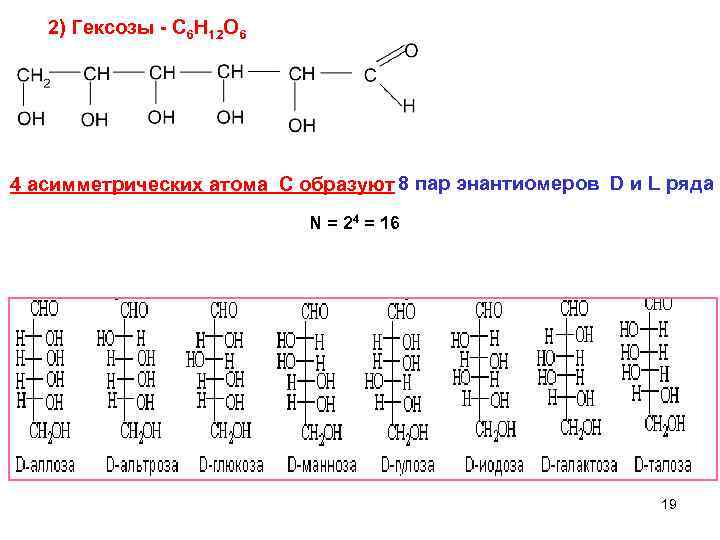
2) Гексозы - C 6 H 12 O 6 4 асимметрических атома С образуют 8 пар энантиомеров D и L ряда N = 24 = 16 19
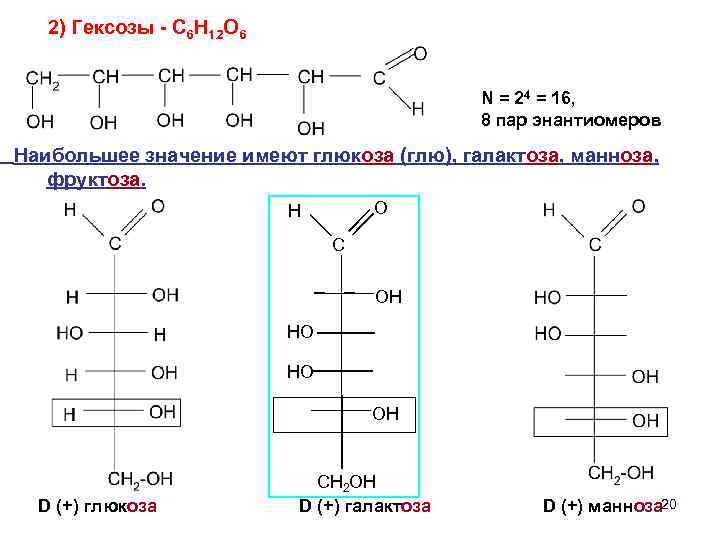
2) Гексозы - C 6 H 12 O 6 N = 24 = 16, 8 пар энантиомеров Наибольшее значение имеют глюкоза (глю), галактоза, манноза, фруктоза. O H C OН HО НO OН D (+) глюкоза СН 2 ОН D (+) галактоза D (+) манноза 20

Глюкоза - самый распространенный моносахарид В свободном виде содержится во фруктовых соках, в качестве составной части входит в молекулы дисахаридов (сахарозы, мальтозы, лактозы, целлобиозы и полисахаридов (крахмал, гликогена, целлюлозы, декстринов 21

Глюкоза Используют глюкозу Ø в пищевой промышленности, Øмедицине , для синтеза глюконовой и аскорбиновой кислот, Ø в качестве восстановителя в текстильной промышленности, Ø для получения этилового спирта. 22

Эпимеры –диастереомеры, которые различаются конфигурацией одного атома. Фруктоза – структурный изомер глюкозы, фруктовый сахар содержится в мёде, фруктах D (-) фру 23

Фруктоза фруктовый или плодовый, сахар, левулёза, β-Dфруктофураноза, бесцветные кристаллы сладкого вкуса (слаще сахарозы в 1, 5 раза и глюкозы в 3 раза), растворимы в воде. Встречается в свободном виде во многих фруктах и плодах: в яблоках, помидорах, пчелином мёде (около 50% ), входит в состав олиго- и полисахаридов. 24
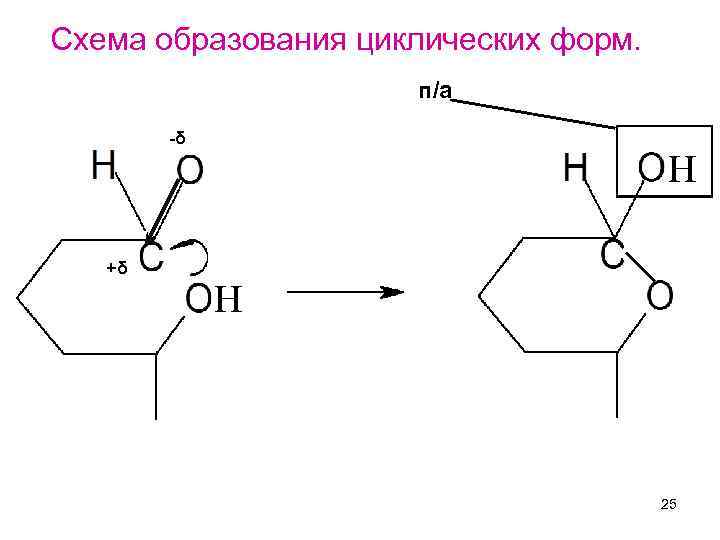
Схема образования циклических форм. п/а -δ +δ Н Н 25
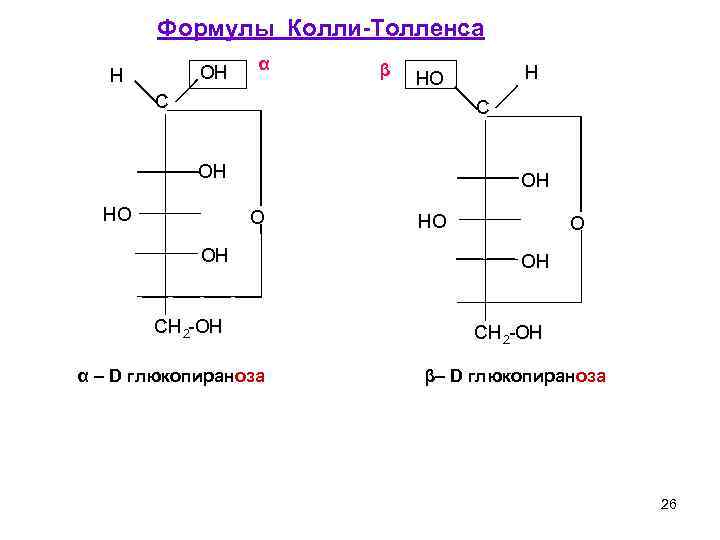
Формулы Колли-Толленса OH H α β H HO C C OH HO OH CH 2 -OH α – D глюкопираноза HO O OH CH 2 -OH β– D глюкопираноза 26
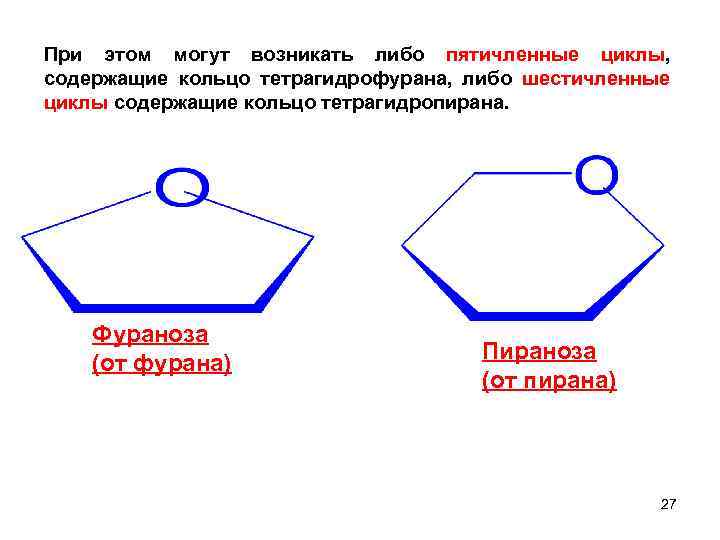
При этом могут возникать либо пятичленные циклы, содержащие кольцо тетрагидрофурана, либо шестичленные циклы содержащие кольцо тетрагидропирана. Фураноза (от фурана) Пираноза (от пирана) 27
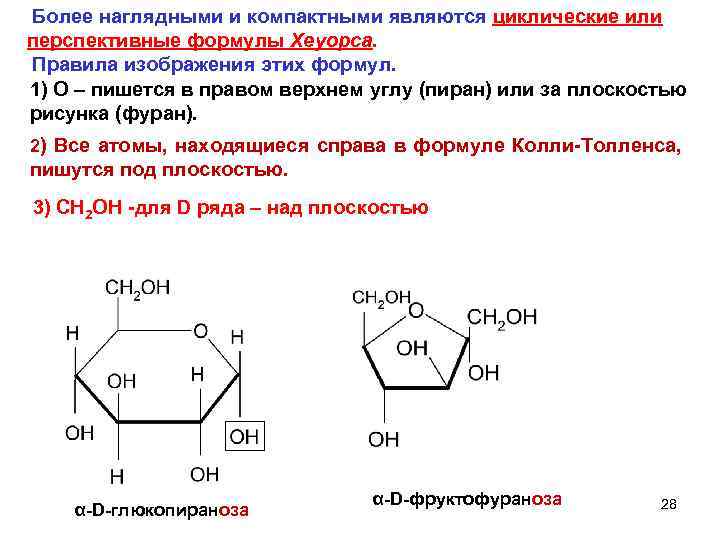
Более наглядными и компактными являются циклические или перспективные формулы Хеуорса. Правила изображения этих формул. 1) О – пишется в правом верхнем углу (пиран) или за плоскостью рисунка (фуран). 2) Все атомы, находящиеся справа в формуле Колли-Толленса, пишутся под плоскостью. 3) CH 2 OH -для D ряда – над плоскостью α-D-глюкопираноза α-D-фруктофураноза 28

Таутомерия. Мутаротация Доказательством существования циклической формы может быть явление мутаротации. твердом состоянии моносахариды имеют циклическое В строение. При растворении моносахаридов первоначальное значение [α] меняется, со временем достигнув определенного значения, которое остается постоянным. Мутаротация – изменение удельного вращения растворов УВ во времени. Сахариметр-поляриметр СУ-5 предназначен для измерения концентрации сахарозы в растворах по углу вращения плоскости поляризации 29

Таутомерия. Мутаротация При растворении моносахарид из одной циклической формы может перейти в другую, но только через открытую. β-D- глюкопираноза D – глю α-D- глюкопираноза α = + 19° равнов. α = 52. 5° α = + 112° Автоматический цифровой поляриметр Сосуществование в динамическом равновесии двух и более изомерных форм называется таутомерией. Таутомерия УВ - окси-оксо, цикло-оксо, или кольчатоцепная. 30
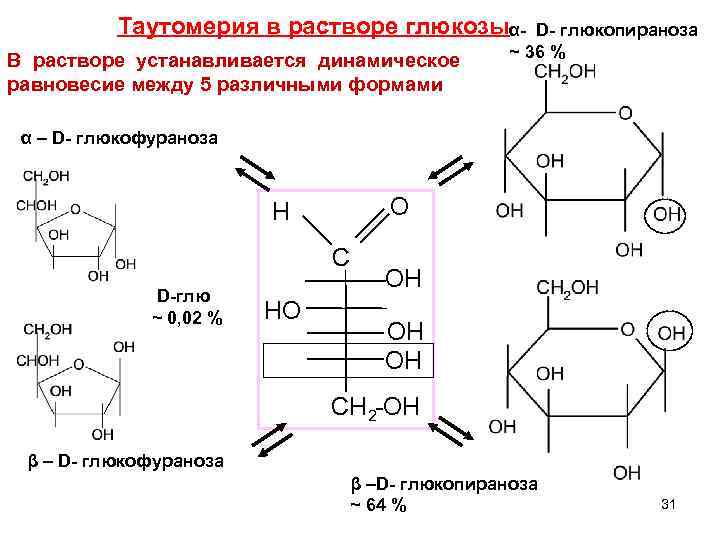
Таутомерия в растворе глюкозыα- D- глюкопираноза В растворе устанавливается динамическое равновесие между 5 различными формами ~ 36 % α – D- глюкофураноза O H C D-глю ~ 0, 02 % HO OH OH OH CH 2 -OH β – D- глюкофураноза β –D- глюкопираноза ~ 64 % 31
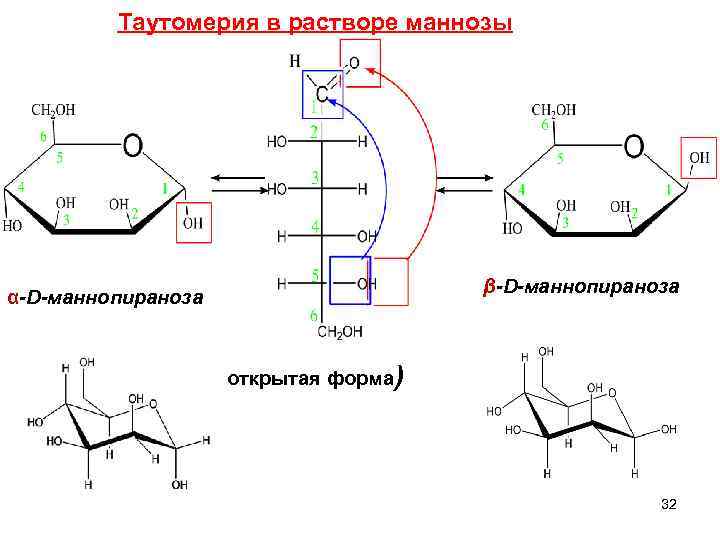
Таутомерия в растворе маннозы β-D-маннопираноза α-D-маннопираноза открытая форма) 32

Манноза – компонент многих полисахаридов и смешанных биополимеров растительного, животного и бактериального происхождения, имеет сладкий вкус. В природе встречается только Dформа. Существует в виде двух аномеров: α- и β- формы. В свободном виде обнаружена в плодах многих цитрусовых, анакардиевых и коринокарповых 33

Манноза Превращения маннозы в организме происходят с помощью активированной формы маннозы – гаунозиндифосфатманнозы (ГДФМ), которая служит донором остатка маннозы при биосинтезе маннанов и других биополимеров. 34
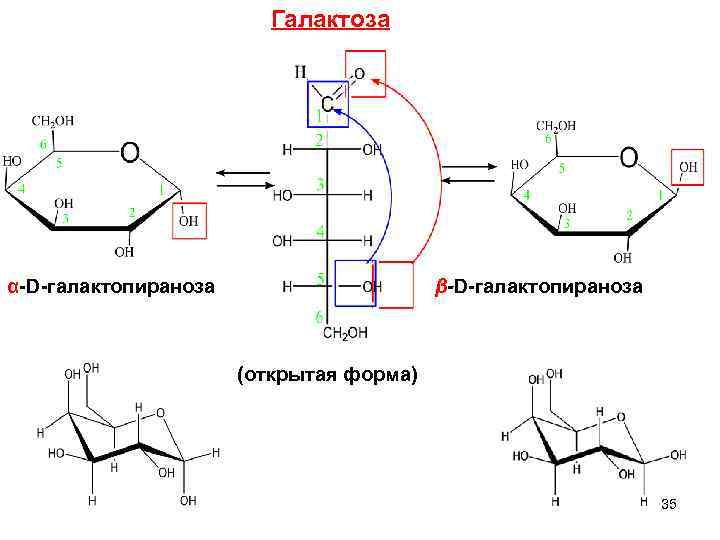
Галактоза α-D-галактопираноза β-D-галактопираноза (открытая форма) 35

Галактоза Встречается в природе в свободном виде, в виде гликозидов, дисахаридов (лактозы), полисахаридов (агар-агара, ). Галактоза входит в состав стероидных алкалоидов, выделенных из растений семейства пасленовых, например саланина содержащегося в картофеле. Агар-агар 36
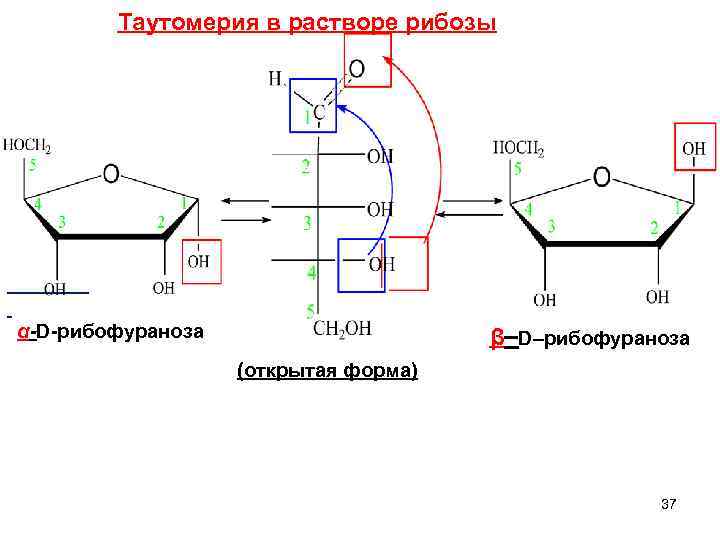
Таутомерия в растворе рибозы β–D–рибофураноза α-D-рибофураноза (открытая форма) 37
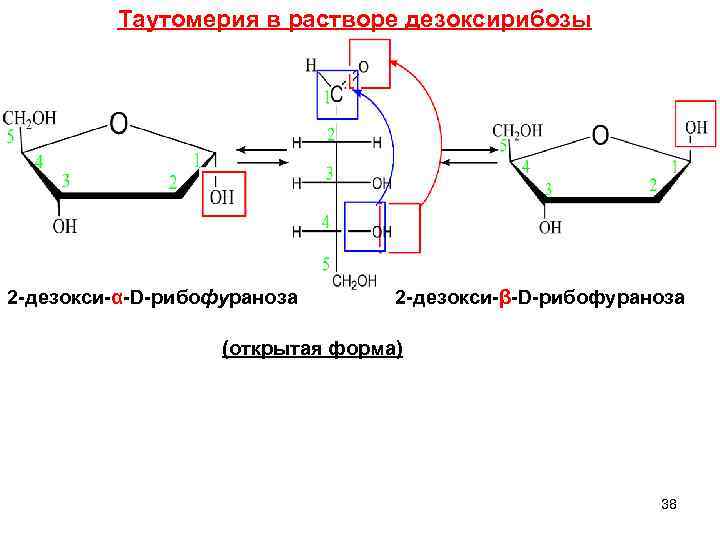
Таутомерия в растворе дезоксирибозы 2 -дезокси-α-D-рибофураноза 2 -дезокси-β-D-рибофураноза (открытая форма) 38
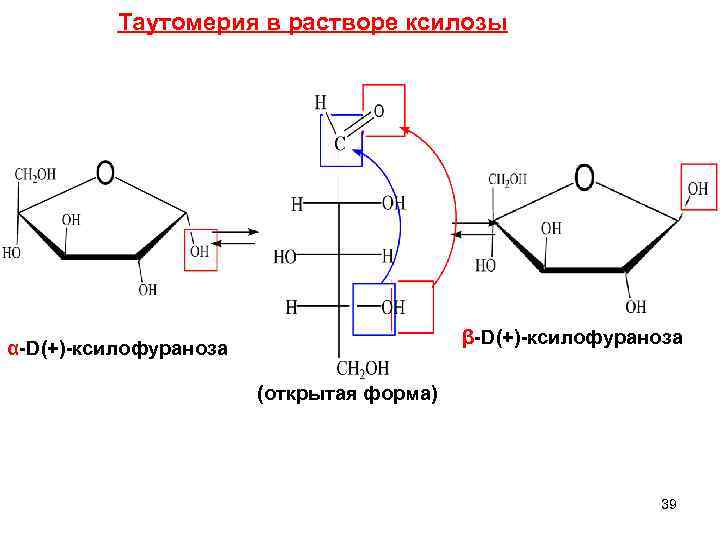
Таутомерия в растворе ксилозы β-D(+)-ксилофураноза α-D(+)-ксилофураноза (открытая форма) 39
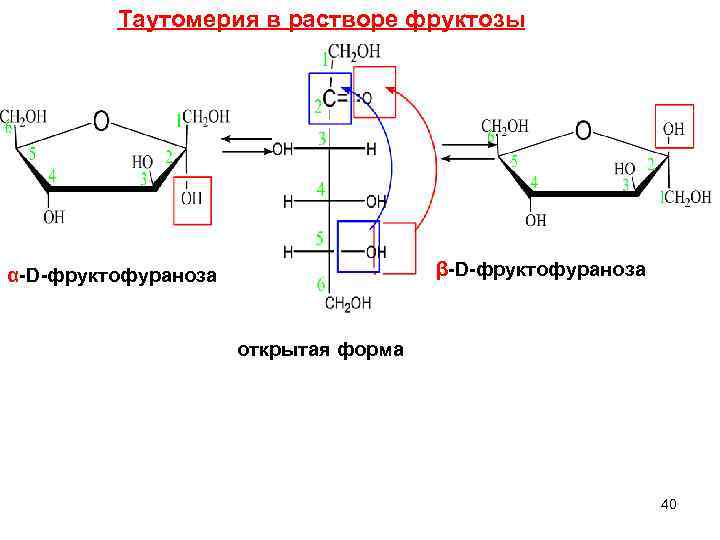
Таутомерия в растворе фруктозы β-D-фруктофураноза α-D-фруктофураноза открытая форма 40

Эпимеризация углеводов ЭПИМЕРИЗАЦИЯ - изменение конфигурации одного хиральных центров молекулы на противоположную из Эпимеры –диастереомеры, отличающиеся конфигурацией только одного асимметрического атома С. В организме эпимеризация происходит ферментативно, in vitro- в щелочной среде. В слабощелочном растворе D-глюкоза находится в равновесии с кетогексозой, D-фруктозой, и альдогексозой, D-маннозой. Глюкоза и манноза различаются конфигурацией при С-2 Связана с открытой формой УВ. Причина – в кислотном характере Н при α. С атоме. Dфру Dглю Dман 41
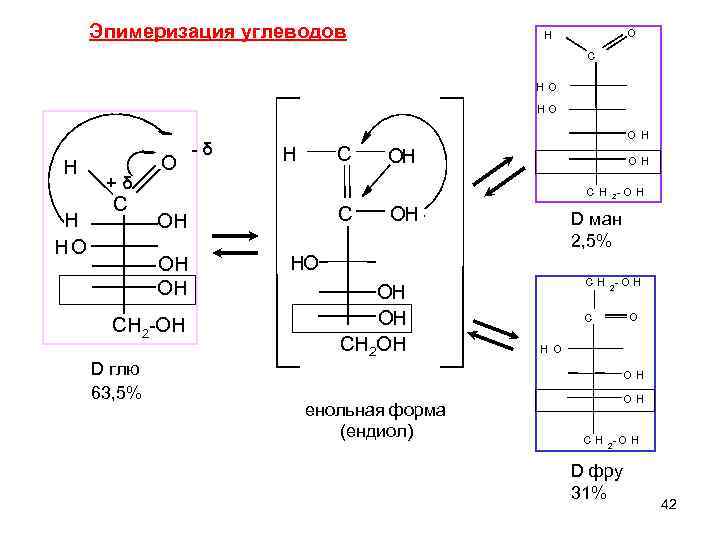
Эпимеризация углеводов O H C H O HO H H HO + δ C O H C OH O H C H 2 -O H C OH OH OH CH 2 -OH D глю 63, 5% - δ O H OH D ман 2, 5% HO OH OH CH 2 OH енольная форма (ендиол) C H 2 - O H O C H O OH OH C H 2 - O H D фру 31% 42
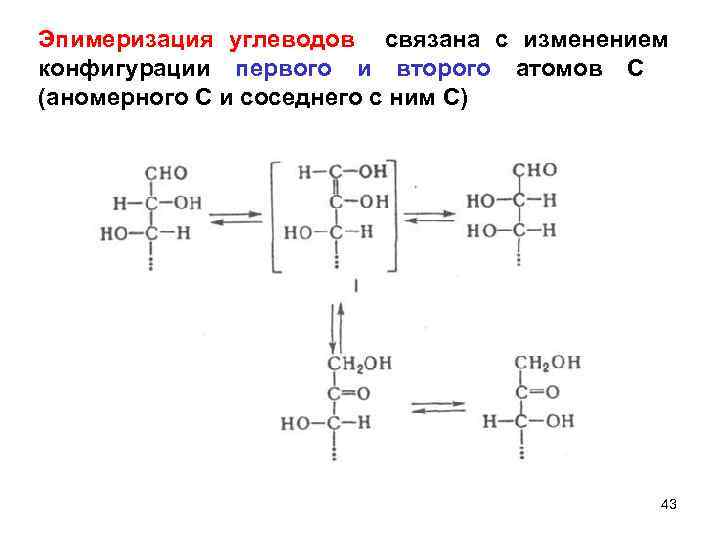
Эпимеризация углеводов связана с изменением конфигурации первого и второго атомов С (аномерного С и соседнего с ним С) 43

Химические свойства УВ Общие реакции для всех углеводордов Ø на ОН- спирт Ø на п/а ОН Ø на > C = O Ø ОВР Специфические реакции (различают пентозы и гексозы) Ø брожение Ø действ. кт. конц. Ø реакция Селиванова 44
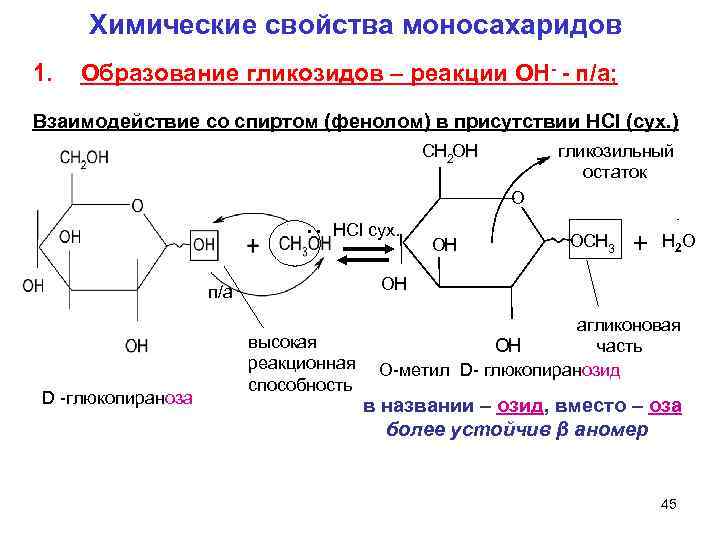
Химические свойства моносахаридов 1. Образование гликозидов – реакции ОН- - п/а; Взаимодействие со спиртом (фенолом) в присутствии HCl (сух. ) гликозильный остаток CH 2 OH . . п/а D -глюкопираноза O HCl сух. OH OCH 3 + Н 2 О OH агликоновая высокая OH часть реакционная О-метил D- глюкопиранозид способность в названии – озид, вместо – оза более устойчив β аномер 45
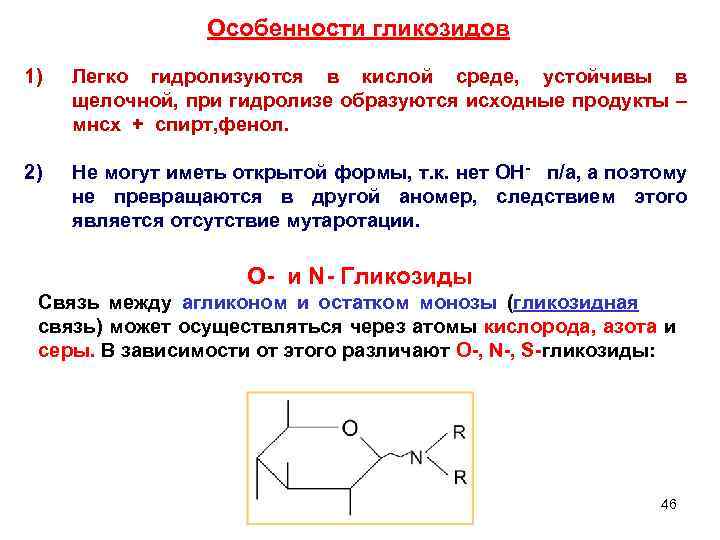
Особенности гликозидов 1) Легко гидролизуются в кислой среде, устойчивы в щелочной, при гидролизе образуются исходные продукты – мнсх + спирт, фенол. 2) Не могут иметь открытой формы, т. к. нет ОН- п/а, а поэтому не превращаются в другой аномер, следствием этого является отсутствие мутаротации. O- и N- Гликозиды Связь между агликоном и остатком монозы (гликозидная связь) может осуществляться через атомы кислорода, азота и серы. В зависимости от этого различают O-, N-, S-гликозиды: 46
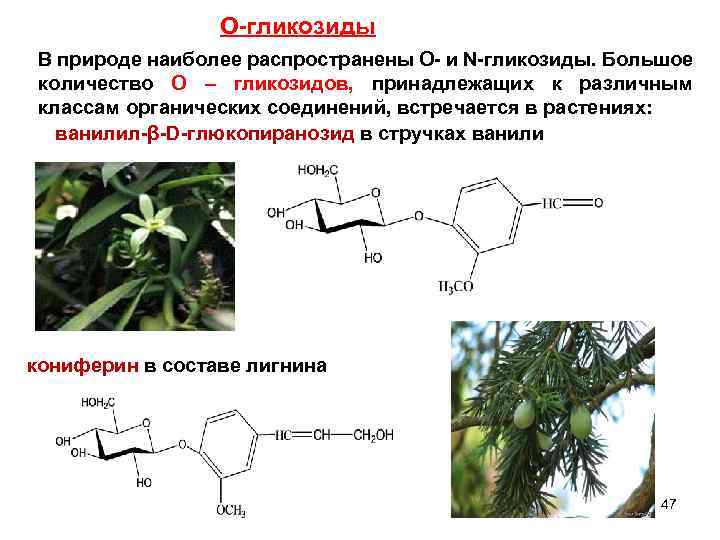
О-гликозиды В природе наиболее распространены O- и N-гликозиды. Большое количество О – гликозидов, принадлежащих к различным классам органических соединений, встречается в растениях: ванилил-β-D-глюкопиранозид в стручках ванили кониферин в составе лигнина 47
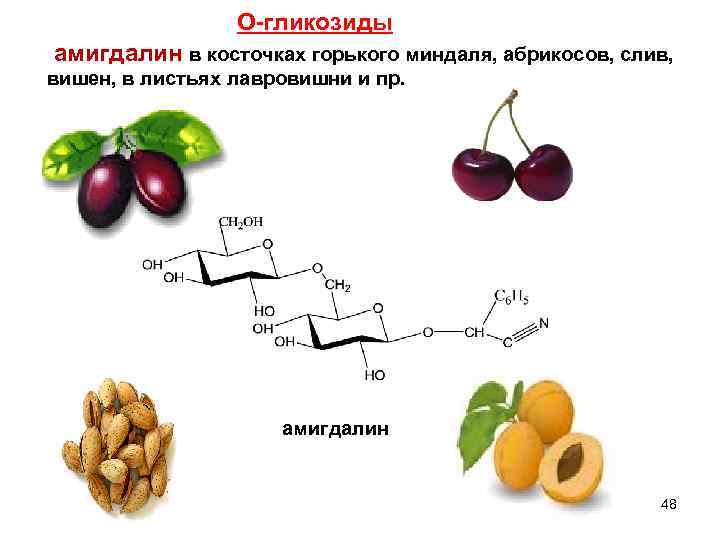
О-гликозиды амигдалин в косточках горького миндаля, абрикосов, слив, вишен, в листьях лавровишни и пр. амигдалин 48

О-гликозиды Витамины К, Р – это О - гликозиды, некоторые лекарственные препараты (стрептомицин), антибиотики, сердечные гликозиды, извлекаемые из ландыша наперстянки. 49
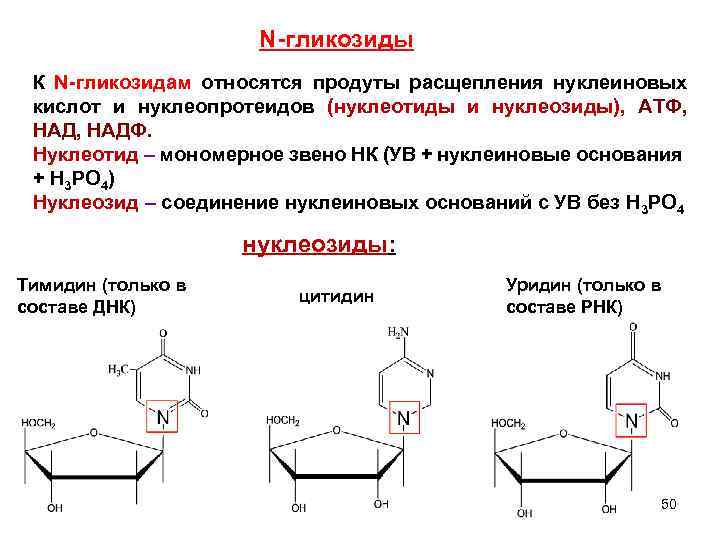
N-гликозиды К N-гликозидам относятся продуты расщепления нуклеиновых кислот и нуклеопротеидов (нуклеотиды и нуклеозиды), АТФ, НАД, НАДФ. Нуклеотид – мономерное звено НК (УВ + нуклеиновые основания + H 3 PO 4) Нуклеозид – соединение нуклеиновых оснований с УВ без H 3 PO 4 нуклеозиды: Тимидин (только в составе ДНК) цитидин Уридин (только в составе РНК) 50
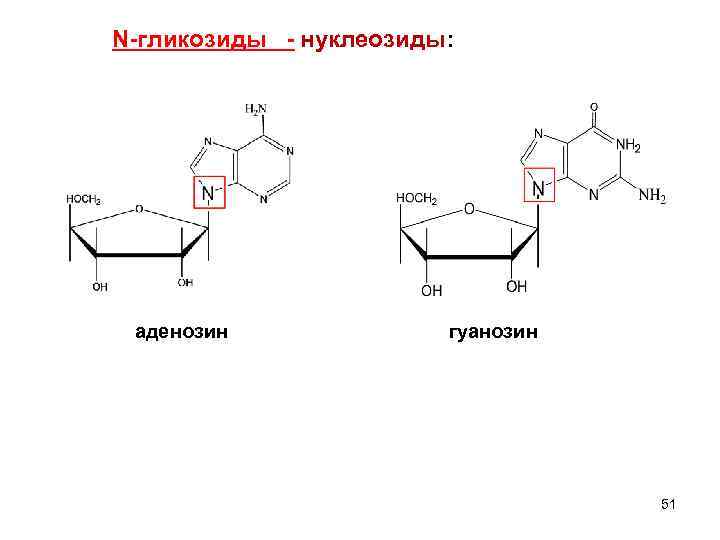
N-гликозиды - нуклеозиды: аденозин гуанозин 51
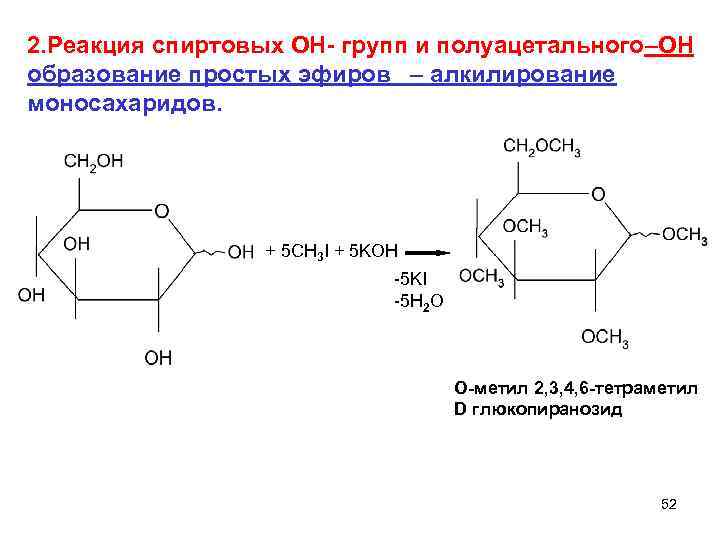
2. Реакция спиртовых ОН- групп и полуацетального–ОН образование простых эфиров – алкилирование моносахаридов. + 5 CH 3 I + 5 KOH -5 KI -5 H 2 O O-метил 2, 3, 4, 6 -тетраметил D глюкопиранозид 52
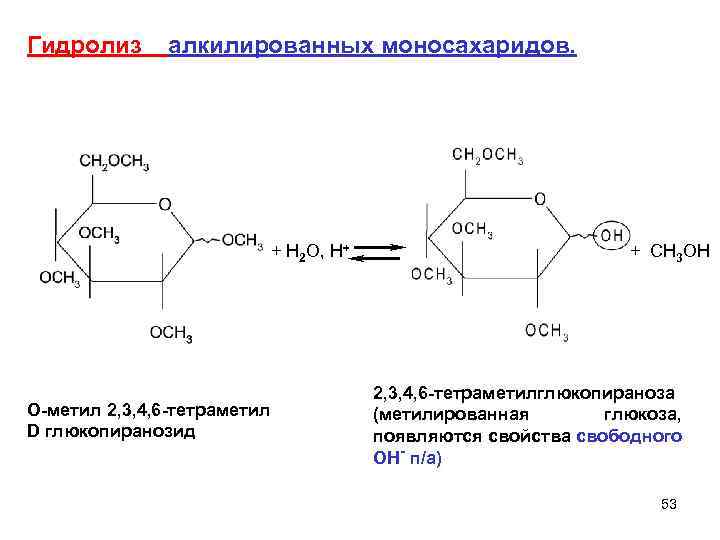
Гидролиз алкилированных моносахаридов. + H 2 O, H+ O-метил 2, 3, 4, 6 -тетраметил D глюкопиранозид + CH 3 OH 2, 3, 4, 6 -тетраметилглюкопираноза (метилированная глюкоза, появляются свойства свободного ОН- п/а) 53

3. Образование сложных эфиров – реакции этерификации или ацилирования моносахаридов. Введение RCO может происходить при помощи RCOCI, (RCO)2 О, RCOOH. Обычно используют ангидриды карбоновых кислот, образуются сложные эфиры + 5 (CH 3 CO)2 O CH 3 CO Ac D гал H+ -5 CH 3 COOH 1, 2, 3, 4, 6 -пентаацетил D галактопираноза (сложный эфир) 54
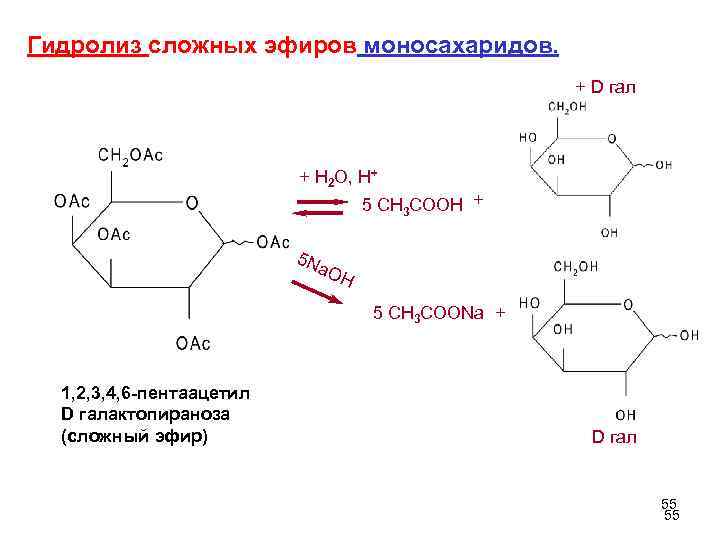
Гидролиз сложных эфиров моносахаридов. + D гал + H 2 O, H+ 5 CH 3 COOH + 5 N a. O H 5 CH 3 COONa + 1, 2, 3, 4, 6 -пентаацетил D галактопираноза (сложный эфир) D гал 55 55

3. Образование сложных эфиров- фосфатов Большое значение имеют эфиры H 3 PO 4 – фосфаты. Это - наиболее метаболически активные формы моносахаридов, содержатся во всех растительных и животных организмах. Фосфаты D глюкозы и D фруктозы). Фосфаты содержатся во всех растительных и животных организмах 56
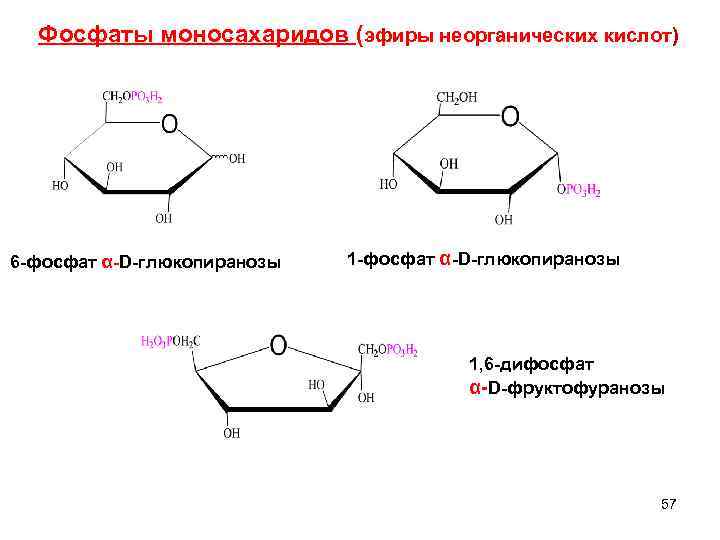
Фосфаты моносахаридов (эфиры неорганических кислот) 6 -фосфат α-D-глюкопиранозы 1, 6 -дифосфат α-D-фруктофуранозы 57
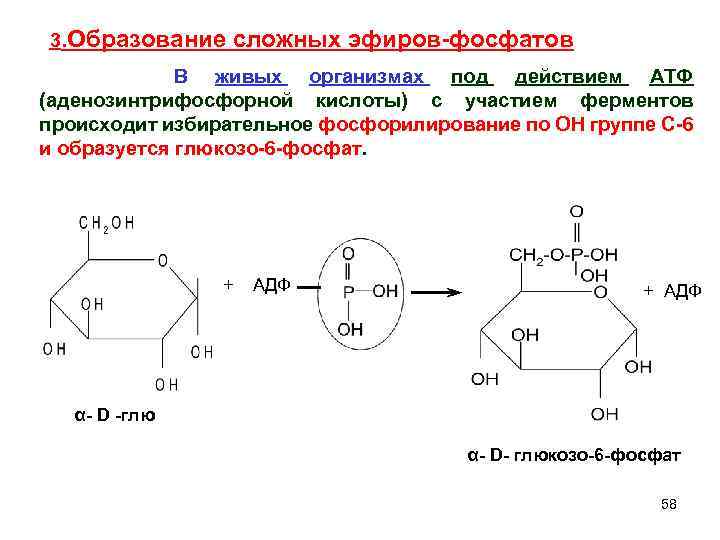
3. Образование сложных эфиров-фосфатов В живых организмах под действием АТФ (аденозинтрифосфорной кислоты) с участием ферментов происходит избирательное фосфорилирование по ОН группе С-6 и образуется глюкозо-6 -фосфат. + АДФ + АДФ α- D -глю α- D- глюкозо-6 -фосфат 58
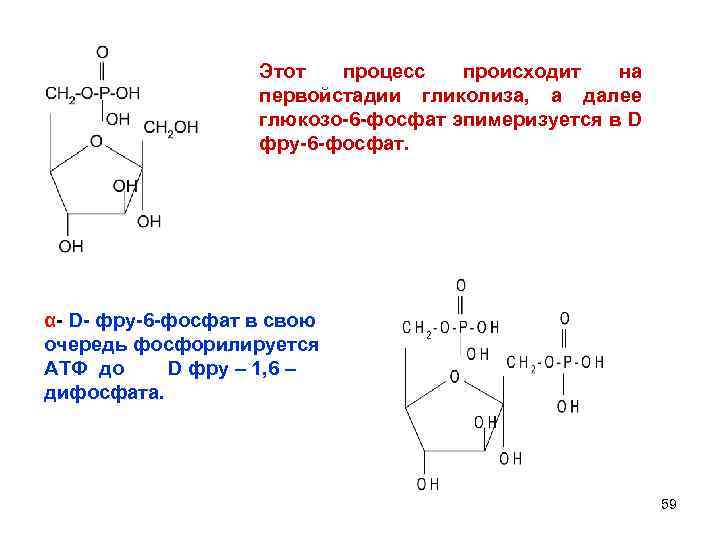
Этот процесс происходит на первойстадии гликолиза, а далее глюкозо-6 -фосфат эпимеризуется в D фру-6 -фосфат. α- D- фру-6 -фосфат в свою очередь фосфорилируется АТФ до D фру – 1, 6 – дифосфата. 59
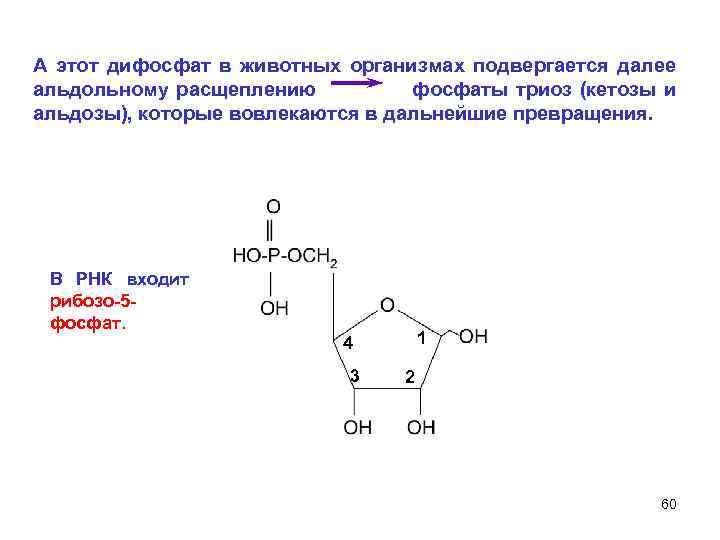
А этот дифосфат в животных организмах подвергается далее альдольному расщеплению фосфаты триоз (кетозы и альдозы), которые вовлекаются в дальнейшие превращения. В РНК входит рибозо-5 фосфат. 1 4 3 2 60

Кроме того, Фруктоза-1, 6 -дифосфат, фруктозо-6 -фосфат Øпромежуточные соединения в темновой фазе фотосинтеза (цикл Кельвина), Øучастники спиртового брожения и Ø биосинтеза углеводов. 61
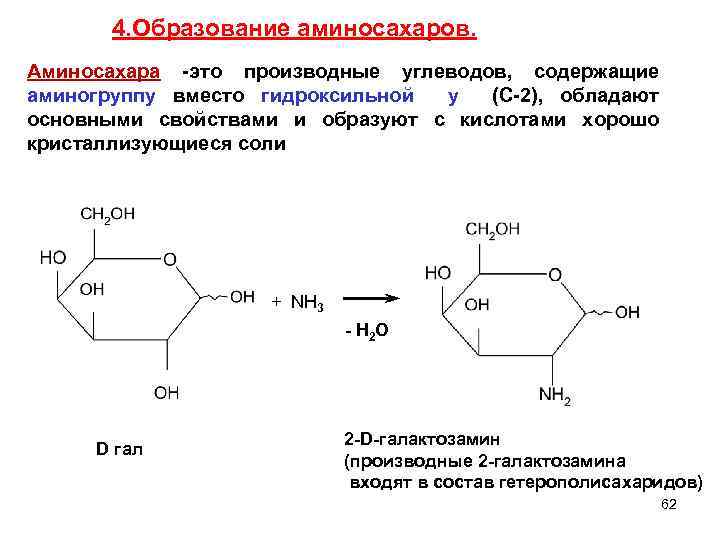
4. Образование аминосахаров. Аминосахара -это производные углеводов, содержащие аминогруппу вместо гидроксильной у (С-2), обладают основными свойствами и образуют с кислотами хорошо кристаллизующиеся соли + NH 3 - Н 2 О D гал 2 -D-галактозамин (производные 2 -галактозамина входят в состав гетерополисахаридов) 62
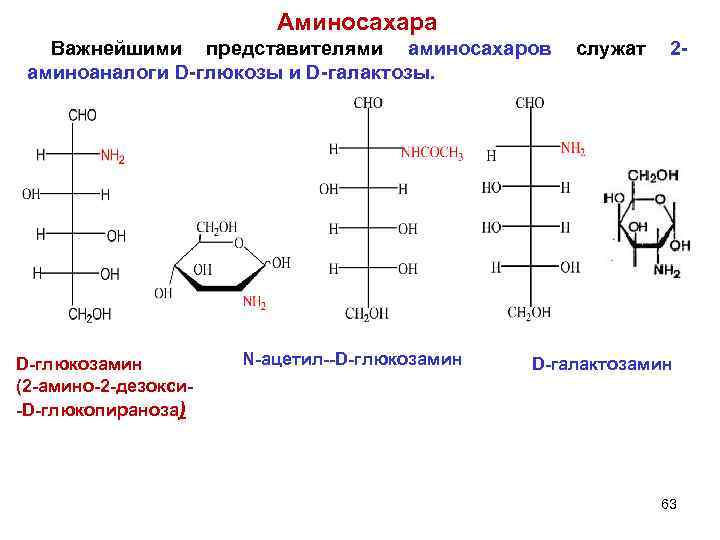
Аминосахара Важнейшими представителями аминосахаров служат 2 аминоаналоги D-глюкозы и D-галактозы. D-глюкозамин (2 -амино-2 -дезокси-D-глюкопираноза) N-ацетил--D-глюкозамин D-галактозамин 63
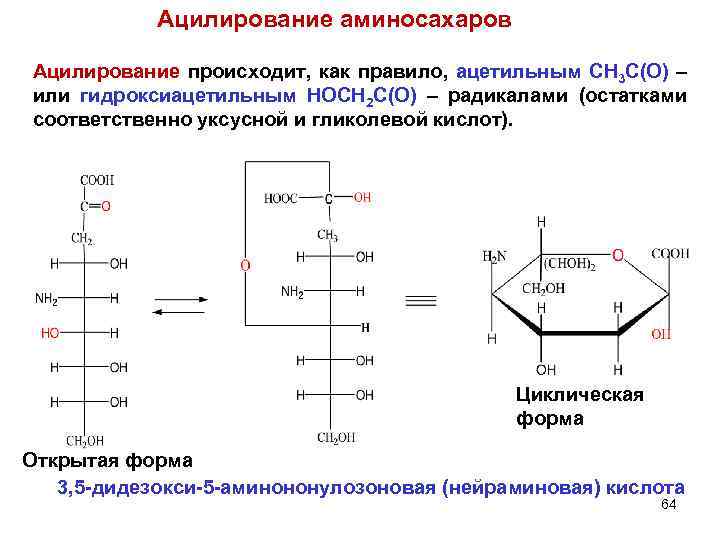
Ацилирование аминосахаров Ацилирование происходит, как правило, ацетильным CH 3 C(O) – или гидроксиацетильным HOCH 2 C(O) – радикалами (остатками соответственно уксусной и гликолевой кислот). Циклическая форма Открытая форма 3, 5 -дидезокси-5 -аминононулозоновая (нейраминовая) кислота 64
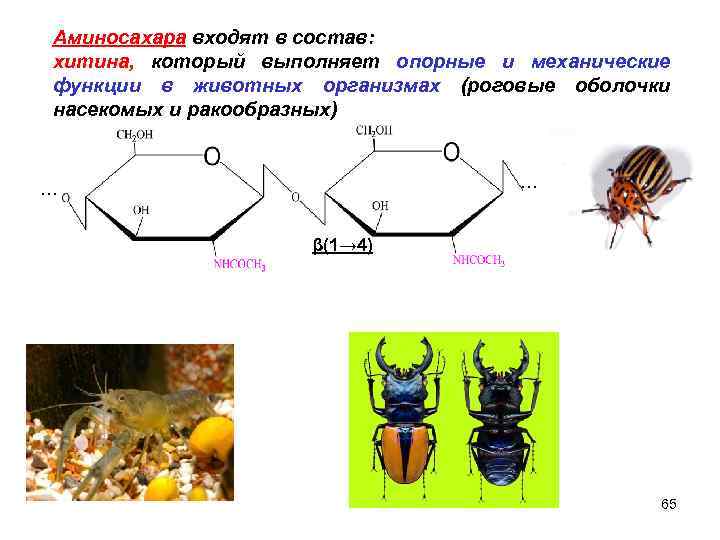
Аминосахара входят в состав: хитина, который выполняет опорные и механические функции в животных организмах (роговые оболочки насекомых и ракообразных) … … β(1→ 4) 65
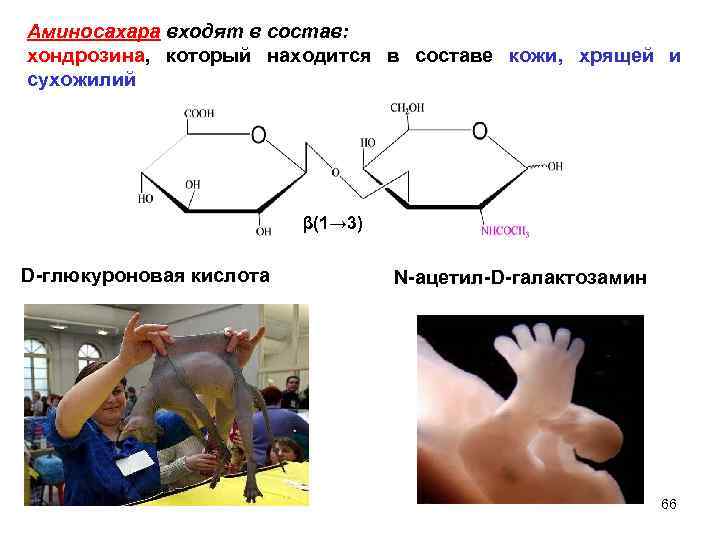
Аминосахара входят в состав: хондрозина, который находится в составе кожи, хрящей и сухожилий β(1→ 3) D-глюкуроновая кислота N-ацетил-D-галактозамин 66
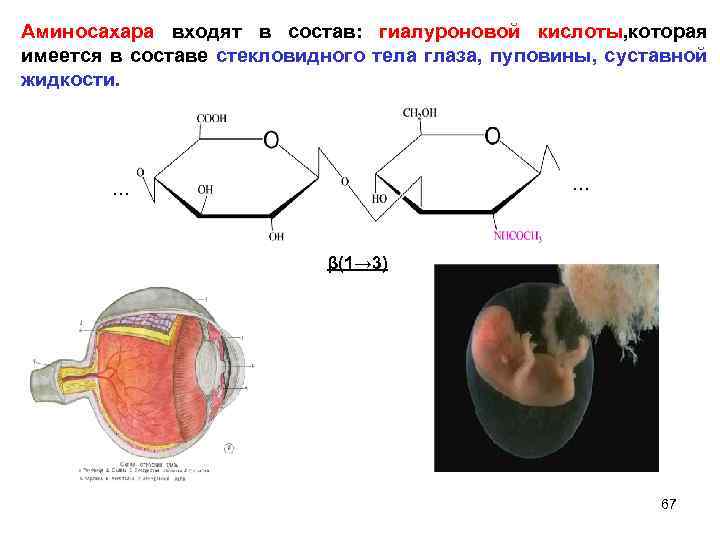
Аминосахара входят в состав: гиалуроновой кислоты, которая имеется в составе стекловидного тела глаза, пуповины, суставной жидкости. … … β(1→ 3) 67
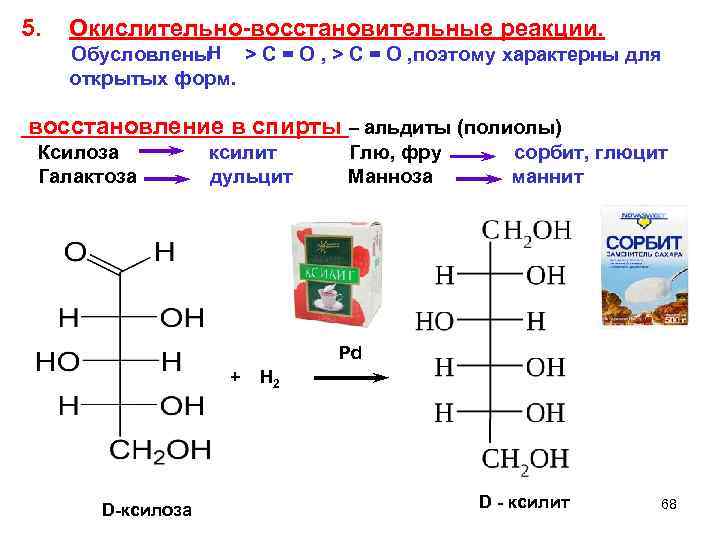
5. Окислительно-восстановительные реакции. Н Обусловлены > C = O , поэтому характерны для открытых форм. восстановление в спирты – альдиты (полиолы) Ксилоза ксилит Глю, фру сорбит, глюцит Галактоза дульцит Манноза маннит Pd + Н 2 D-ксилоза D - ксилит 68
Окисление моносахаридов Реакции окисления используют в структурных исследованиях и биохимических анализах для обнаружения моносахаридов, в частности глюкозы, в биологических жидкостях (моча , кровь). В зависимости от условий окисления образуются различные продукты. 69
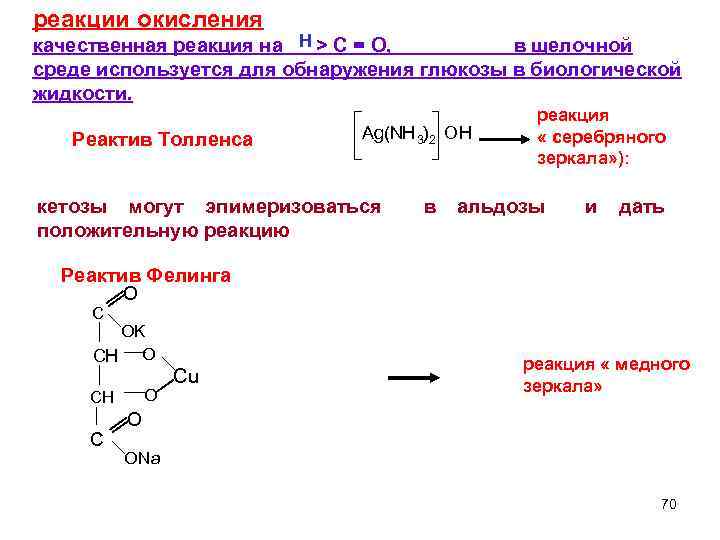
реакции окисления Н качественная реакция на > C = O, в щелочной среде используется для обнаружения глюкозы в биологической жидкости. Реактив Толленса Ag(NH 3) 2 OH реакция « серебряного зеркала» ): кетозы могут эпимеризоваться в альдозы положительную реакцию и дать Реактив Фелинга C O OK CH O O CH C Cu реакция « медного зеркала» O ONa 70

Окисление в щелочной среде (качественная реакция на альдозу) реактивом Толленса (реакция « серебряного зеркала» ): Ag(NH 3)2 OH Продукты окисления (глюконовая кислота) D-Глюкоза 71
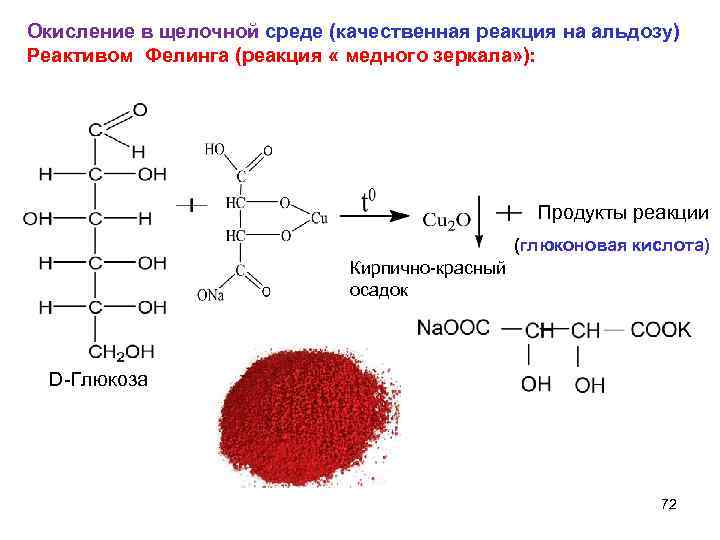
Окисление в щелочной среде (качественная реакция на альдозу) Реактивом Фелинга (реакция « медного зеркала» ): Продукты реакции (глюконовая кислота) Кирпично-красный осадок D-Глюкоза 72
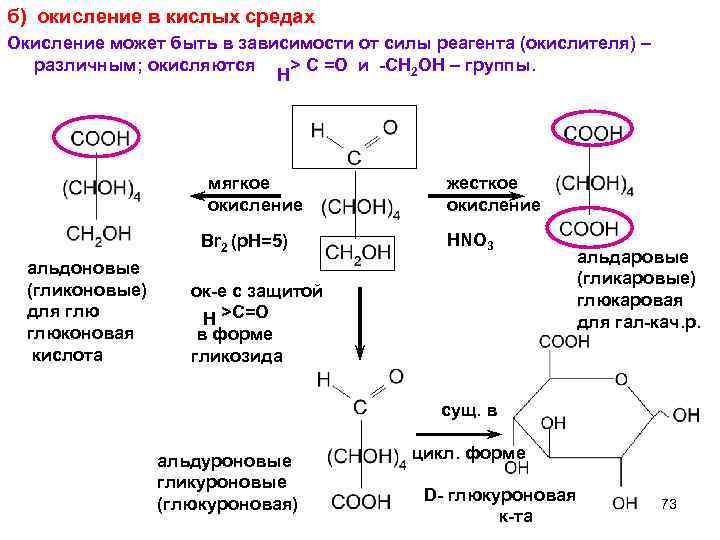
б) окисление в кислых средах Окисление может быть в зависимости от силы реагента (окислителя) – различным; окисляются > C =O и -СН 2 ОН – группы. Н мягкое окисление Br 2 (p. H=5) альдоновые (гликоновые) для глюконовая кислота жесткое окисление HNO 3 ок-е с защитой >C=O Н в форме гликозида альдаровые (гликаровые) глюкаровая для гал-кач. р. сущ. в альдуроновые гликуроновые (глюкуроновая) цикл. форме D- глюкуроновая к-та 73
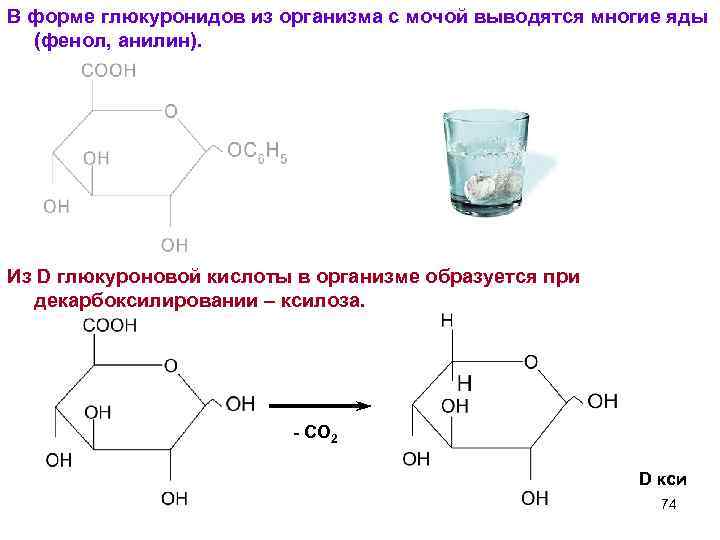
В форме глюкуронидов из организма с мочой выводятся многие яды (фенол, анилин). Из D глюкуроновой кислоты в организме образуется при декарбоксилировании – ксилоза. - СО 2 D кси 74
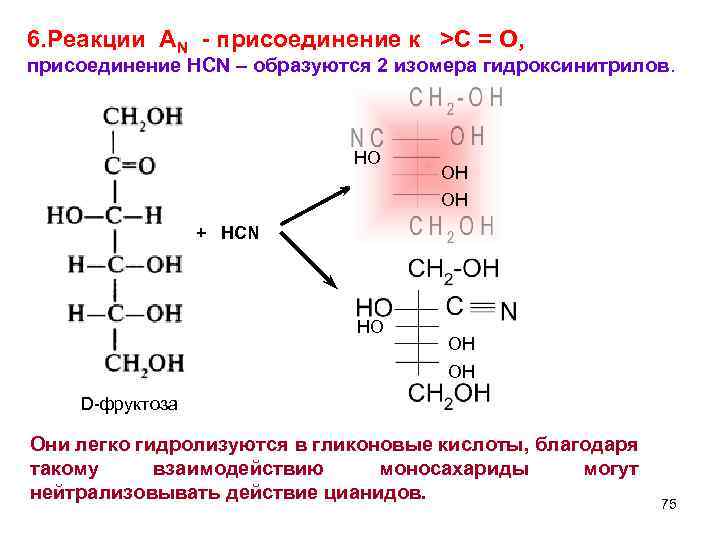
6. Реакции AN - присоединение к >C = O, присоединение HCN – образуются 2 изомера гидроксинитрилов. HO OH OH + HCN HO OH OH D-фруктоза Они легко гидролизуются в гликоновые кислоты, благодаря такому взаимодействию моносахариды могут нейтрализовывать действие цианидов. 75

7. Качественные реакции на Н > C = O (альдегидную группу) Ø образование озазонов при действии С 6 H 5 NH – NH 2 на > C = O Озазоны — окрашенные в желтый или оранжевый цвет кристаллы, 76 хорошо кристаллизуются и имеют четкие температуры плавления
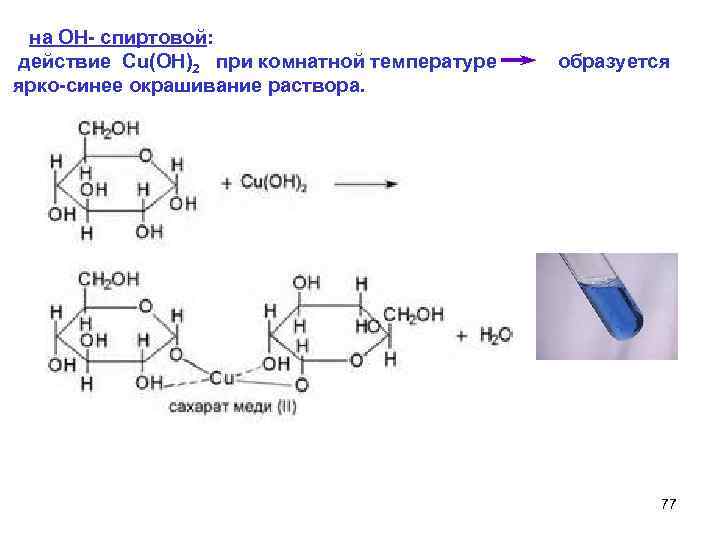
на ОН- спиртовой: действие Cu(OH)2 при комнатной температуре образуется ярко-синее окрашивание раствора. 77
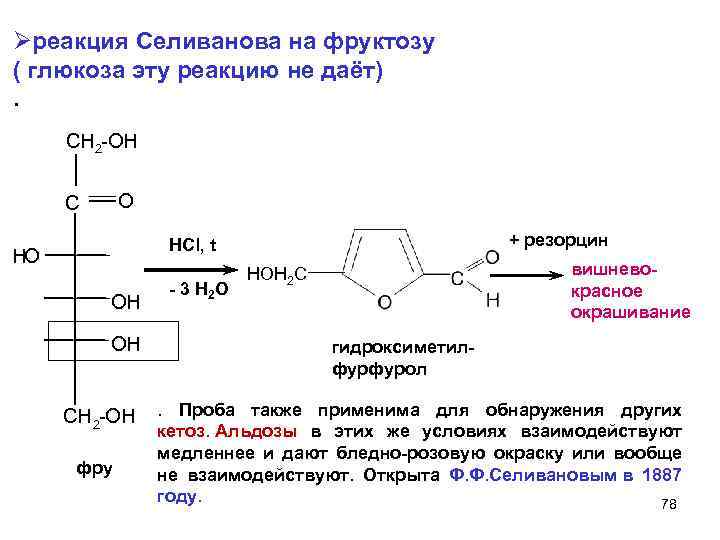
Øреакция Селиванова на фруктозу ( глюкоза эту реакцию не даёт). CH 2 -OН O C + резорцин HCl, t HO OH OH CH 2 -OH фру - 3 H 2 O вишневокрасное окрашивание HOH 2 C гидроксиметилфурфурол. Проба также применима для обнаружения других кетоз. Альдозы в этих же условиях взаимодействуют медленнее и дают бледно-розовую окраску или вообще не взаимодействуют. Открыта Ф. Ф. Селивановым в 1887 году. 78

Дисахариды 79
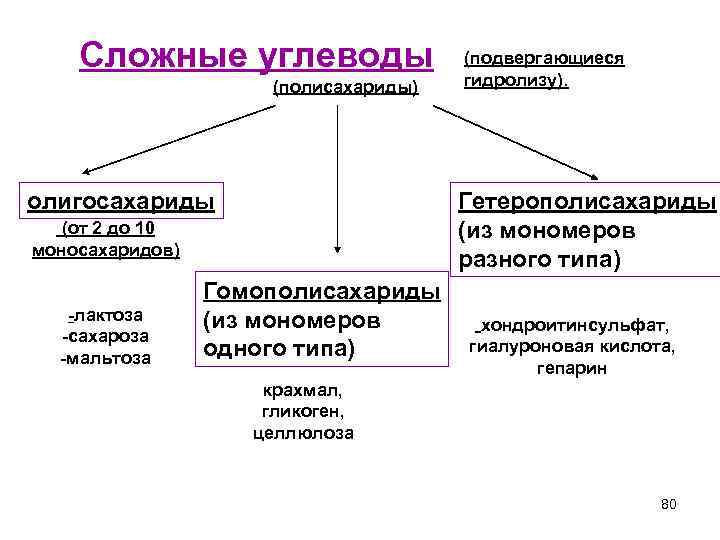
Сложные углеводы (полисахариды) олигосахариды Гетерополисахариды (из мономеров разного типа) (от 2 до 10 моносахаридов) -лактоза -сахароза -мальтоза (подвергающиеся гидролизу). Гомополисахариды (из мономеров одного типа) хондроитинсульфат, гиалуроновая кислота, гепарин крахмал, гликоген, целлюлоза 80
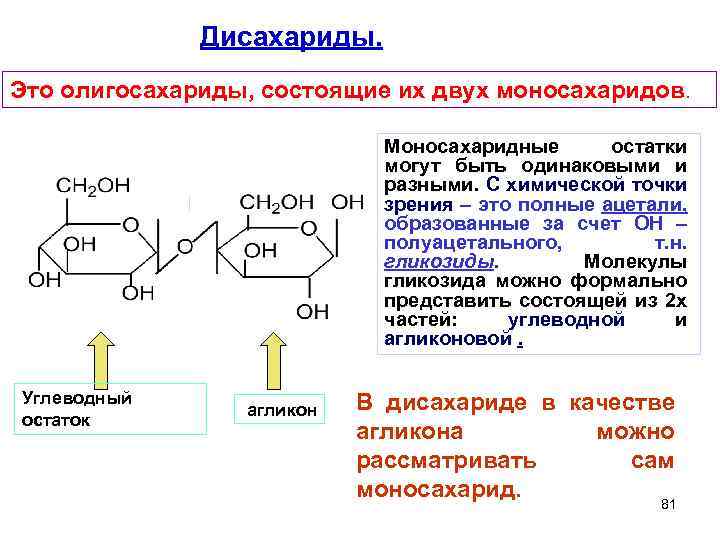
Дисахариды. Это олигосахариды, состоящие их двух моносахаридов. Моносахаридные остатки могут быть одинаковыми и разными. С химической точки зрения – это полные ацетали, образованные за счет ОН – полуацетального, т. н. гликозиды. Молекулы гликозида можно формально представить состоящей из 2 х частей: углеводной и агликоновой. Углеводный остаток агликон В дисахариде в качестве агликона можно рассматривать сам моносахарид. 81
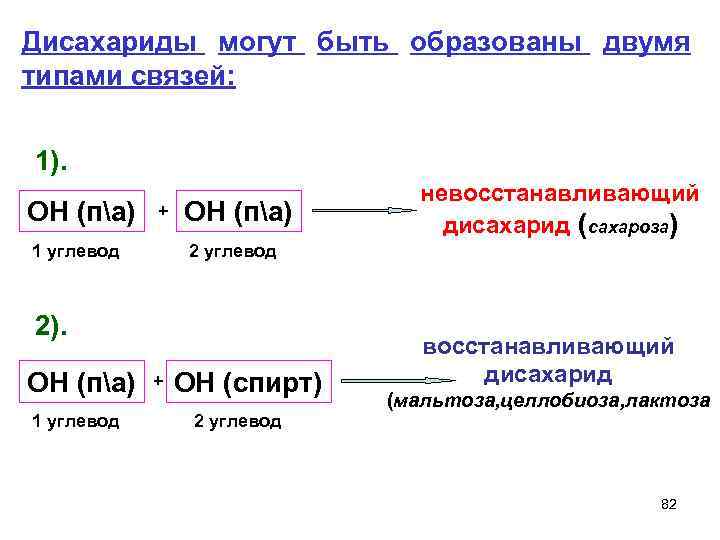
Дисахариды могут быть образованы двумя типами связей: 1). ОН (па) + 1 углевод ОН (па) 2 углевод 2). ОН (па) 1 углевод невосстанавливающий дисахарид (сахароза) + ОН (спирт) 2 углевод восстанавливающий дисахарид (мальтоза, целлобиоза, лактоза 82
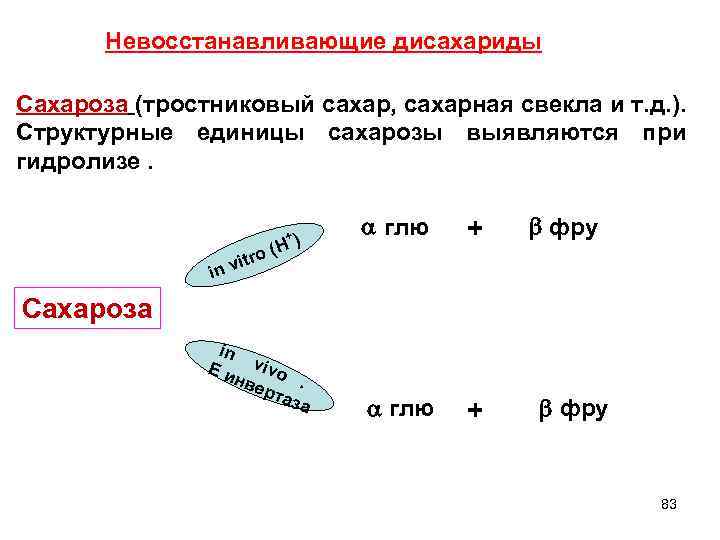
Невосстанавливающие дисахариды Сахароза (тростниковый сахар, сахарная свекла и т. д. ). Структурные единицы сахарозы выявляются при гидролизе. (H ro vit in +) глю + фру Сахароза in E vivo инв ерт . аза фру 83
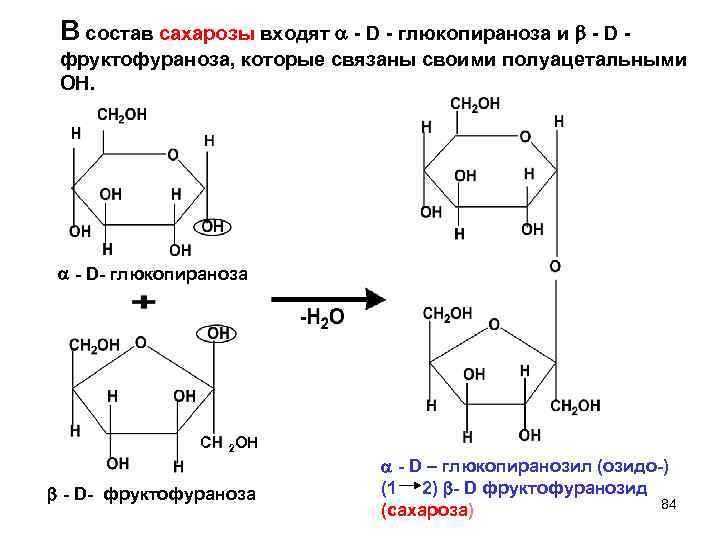
В состав сахарозы входят - D - глюкопираноза и - D - фруктофураноза, которые связаны своими полуацетальными ОН. - D- глюкопираноза С 2 ОН - D- фруктофураноза - D – глюкопиранозил (озидо-) (1 2) - D фруктофуранозид 84 (сахароза)

В названии невосстанавливающих дисахаридов отражено отсутствие полуацетальных ОН, суффикс оза заменен на озил (или озидо) для I углевода и озид для II. Сахароза – это озидо – озид. Правомерны оба названия: - D - фруктофуранозил - (2 1) - - D - глюкопиранозид. - D - глюкопиранозил - (1 2) - - D – фруктофуранозид. 85
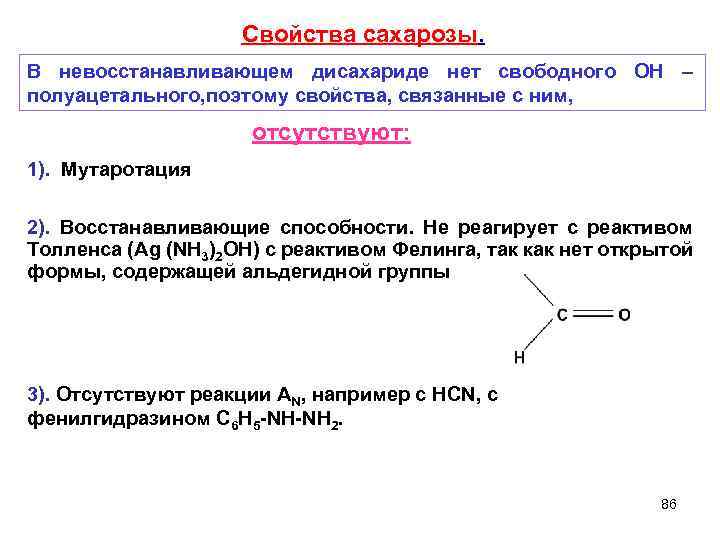
Свойства сахарозы. В невосстанавливающем дисахариде нет свободного ОН – полуацетального, поэтому свойства, связанные с ним, 1). Мутаротация отсутствуют: 2). Восстанавливающие способности. Не реагирует с реактивом Толленса (Ag (NH 3)2 OH) с реактивом Фелинга, так как нет открытой формы, содержащей альдегидной группы 3). Отсутствуют реакции AN, например с HCN, с фенилгидразином C 6 Н 5 -NH-NH 2. 86
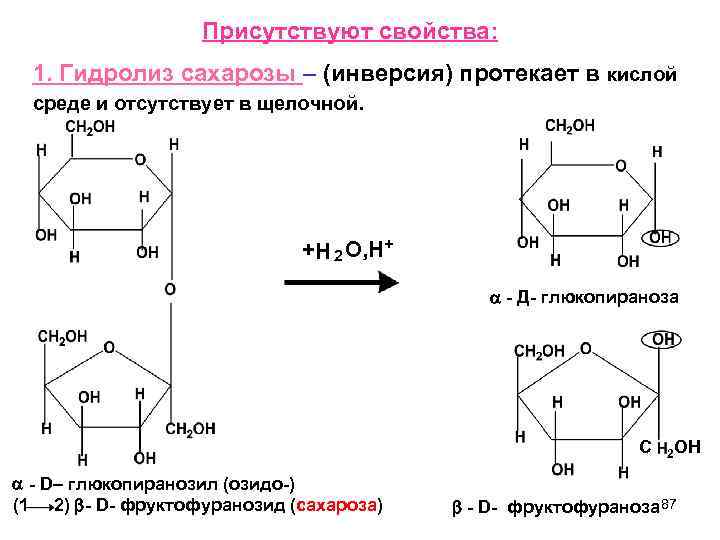
Присутствуют свойства: 1. Гидролиз сахарозы – (инверсия) протекает в кислой среде и отсутствует в щелочной. +H 2 O, H+ - Д- глюкопираноза С 2 ОН - D– глюкопиранозил (озидо-) (1 2) - D- фруктофуранозид (сахароза) - D- фруктофураноза 87

При гидролизе сахарозы в кислой образуются исходные моносахариды. среде Гидролиз сахарозы идет очень легко, даже в присутствии слабых кислот. Ход гидролиза можно проследить с помощью поляриметра, измеряя 20 (удельное вращение). Автоматический поляриметр Раствор сахарозы правовращающий (+), а при гидролизе образуется -D- глю (+) и -D- фру (-) – левовращающая. В результате будет преобладать левое вращение. 88

Поэтому процесс гидролиза иногда называется инверсией, а смесь образующихся глю и фру – инвертным сахаром. 89
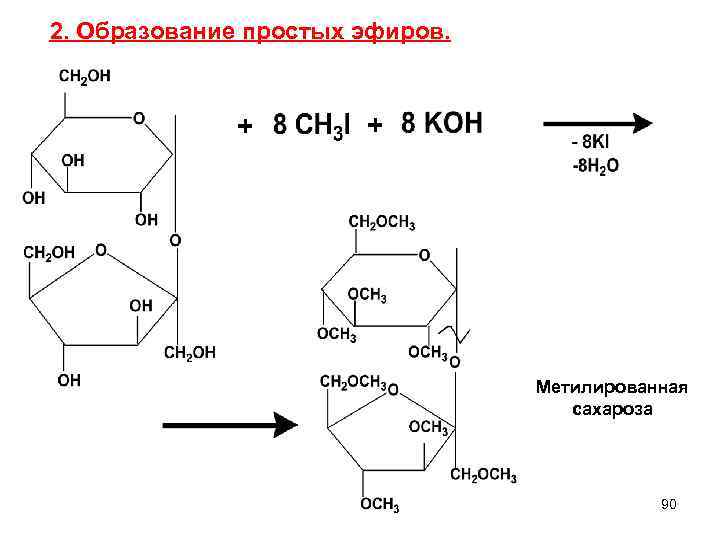
2. Образование простых эфиров. + + Метилированная сахароза 90
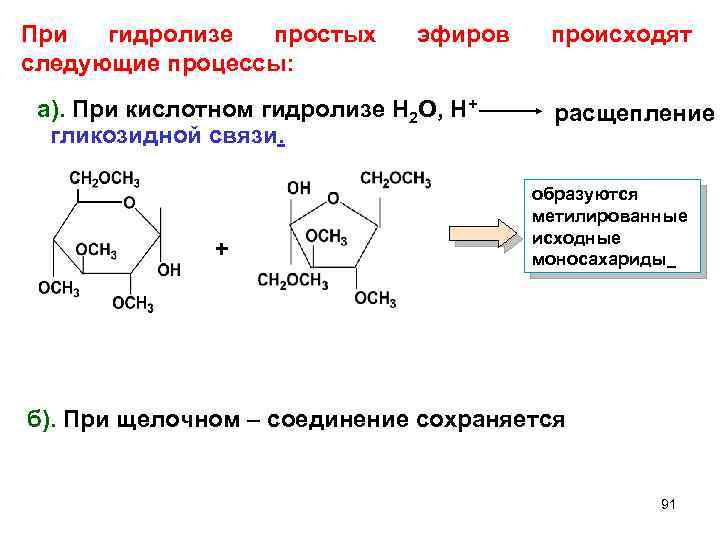
При гидролизе простых следующие процессы: эфиров а). При кислотном гидролизе Н 2 О, Н+ гликозидной связи. + происходят расщепление образуются метилированные исходные моносахариды б). При щелочном – соединение сохраняется 91
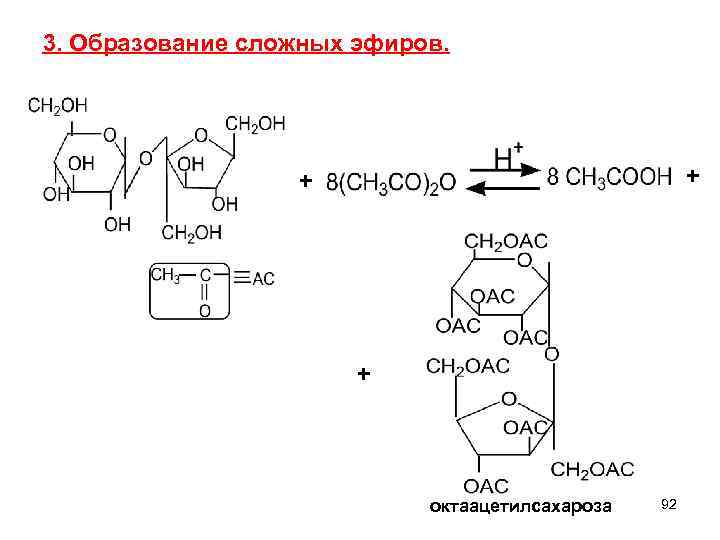
3. Образование сложных эфиров. + + + октaацетилсахароза 92
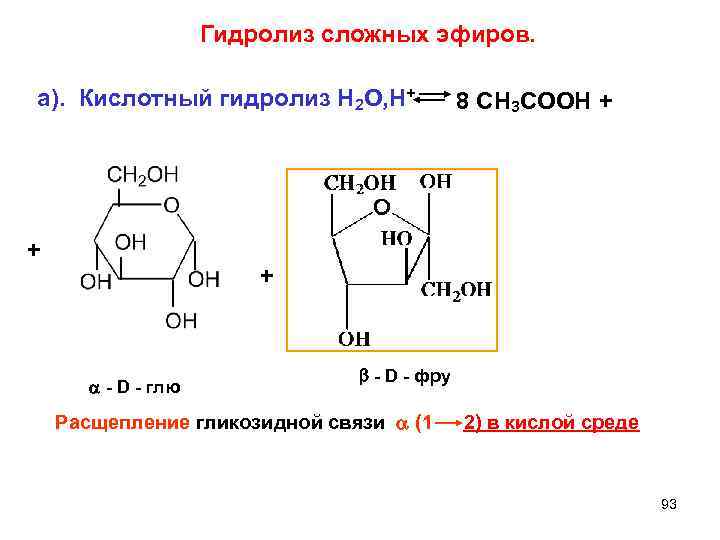
Гидролиз сложных эфиров. а). Кислотный гидролиз Н 2 О, Н+ + + - D - глю 8 СН 3 СООН + + - D - фру Расщепление гликозидной связи (1 2) в кислой среде 93
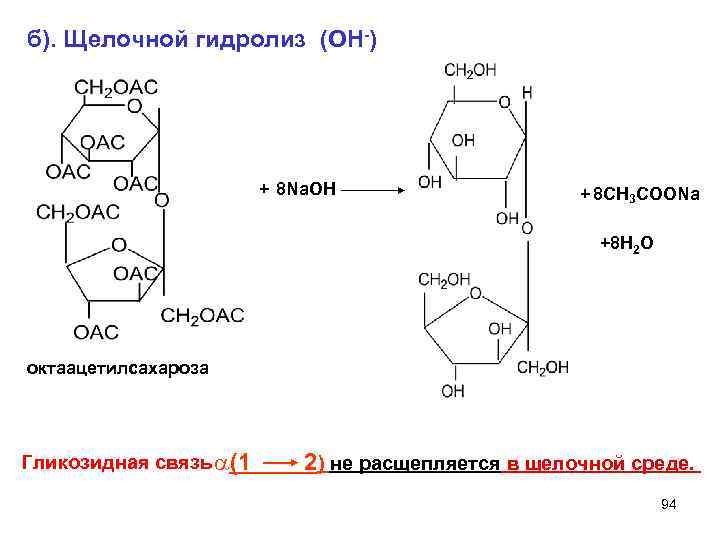
б). Щелочной гидролиз (ОН-) + 8 Na. ОН + 8 СН 3 СООNa +8 H 2 O октaацетилсахароза Гликозидная связь a(1 2) не расщепляется в щелочной среде. 94
![4. Жесткое окисление [O] трикарбоновая кислота – 3 СООН сахароза 95 4. Жесткое окисление [O] трикарбоновая кислота – 3 СООН сахароза 95](https://present5.com/presentation/200585563_454116983/image-95.jpg)
4. Жесткое окисление [O] трикарбоновая кислота – 3 СООН сахароза 95

Восстанавливающие дисахариды. образованы ОН(п/а) + ОН (спиртовой) 1 УВ 2 УВ -озил -оза 1). Лактоза. 2). Мальтоза. 3). Целлобиоза. Лактоза - молочный сахар. Образована - D- галактопиранозой и - ( ) - D - глюкопиранозой. 96
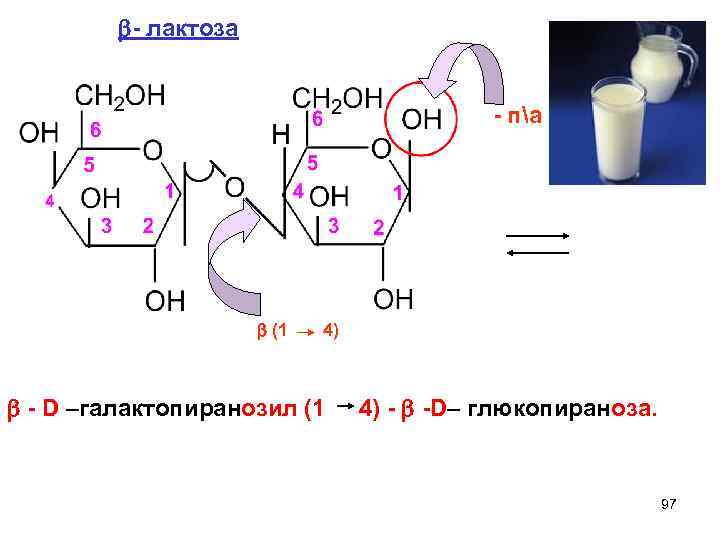
- лактоза - па (1 4) - D –галaктопиранозил (1 4) - -D– глюкопираноза. 97

- лактоза содержится в материнском молоке, является основным углеводом пищи для грудных детей; - лактоза ( - глю) – в коровьем. 98
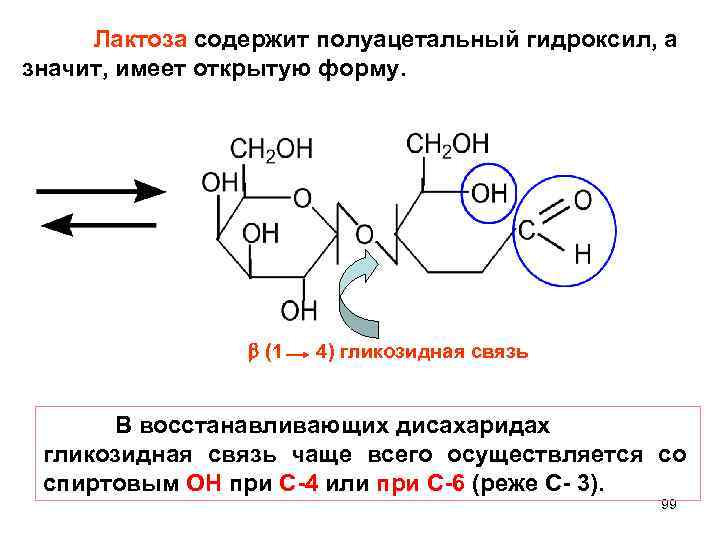
Лактоза содержит полуацетальный гидроксил, а значит, имеет открытую форму. (1 4) гликозидная связь В восстанавливающих дисахаридах гликозидная связь чаще всего осуществляется со спиртовым ОН при С-4 или при С-6 (реже C- 3). 99
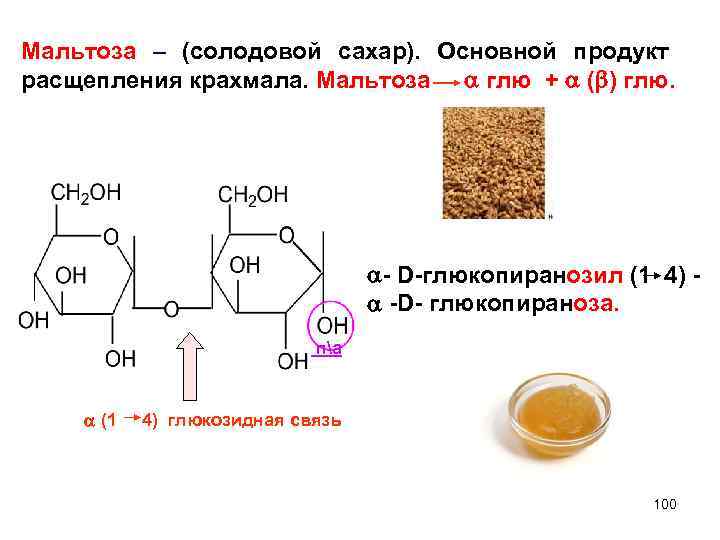
Мальтоза – (солодовой сахар). Основной продукт расщепления крахмала. Мальтоза глю + ( ) глю. - D-глюкопиранозил (1 4) - -D- глюкопираноза. па (1 4) глюкозидная связь 100

Мальтоза – структурная единица, биозный фрагмент крахмала и гликогена -гликозидная связь расположена aксиaльно и отвечает за клубкообразное строение фрагмента крахмала – амилозы. 101
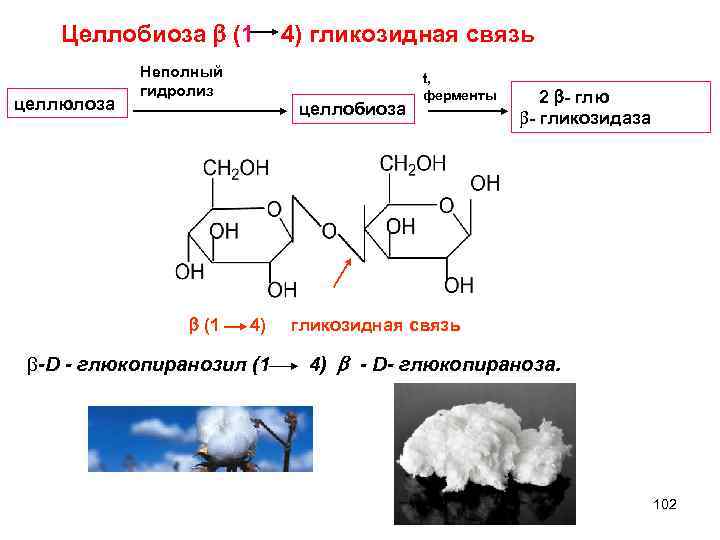
Целлобиоза (1 4) гликозидная связь целлюлоза Неполный гидролиз целлобиоза t, ферменты 2 - глю b- гликозидаза (1 4) гликозидная связь b-D - глюкопиранозил (1 4) - D- глюкопираноза. 102
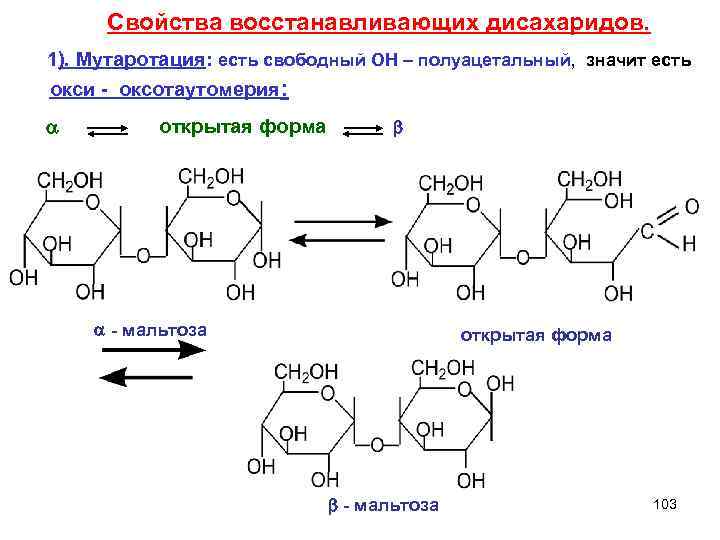
Свойства восстанaвливающих дисахаридов. 1). Мутаротация: есть свободный ОН – полуацетальный, значит есть окси - оксотаутомерия: открытая форма - мальтоза открытая форма - мальтоза 103
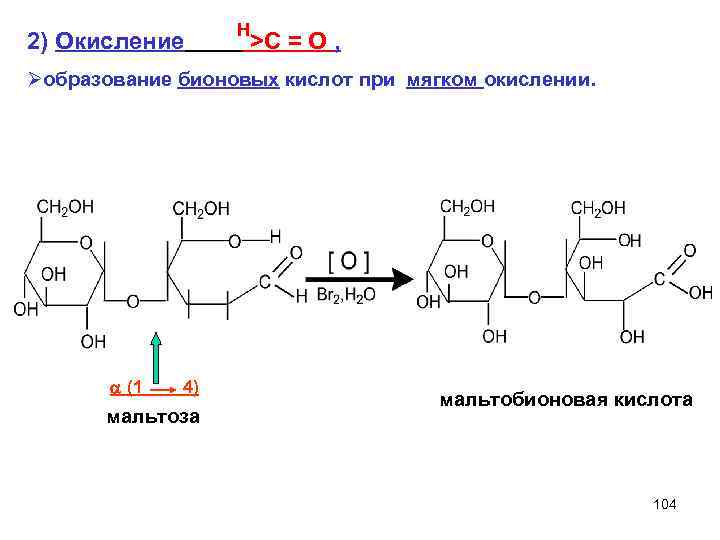
2) Окисление Н >C = O , Øобразование бионовых кислот при мягком окислении. (1 4) мальтоза мальтобионовая кислота 104
![ØЖесткое окисление [O] Свободная группа с защитой полуцетального гидроксила 105 ØЖесткое окисление [O] Свободная группа с защитой полуцетального гидроксила 105](https://present5.com/presentation/200585563_454116983/image-105.jpg)
ØЖесткое окисление [O] Свободная группа с защитой полуцетального гидроксила 105
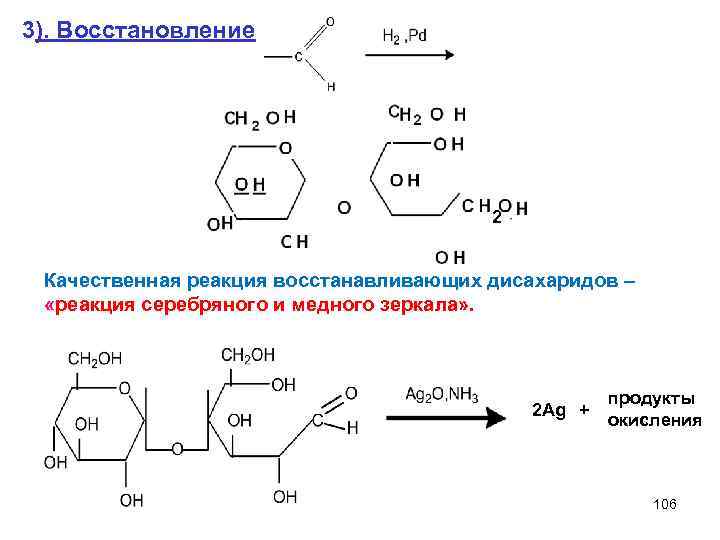
3). Восстановление 2 Качественная реакция восстанавливающих дисахаридов – «реакция серебряного и медного зеркала» . 2 Ag + продукты окисления 106
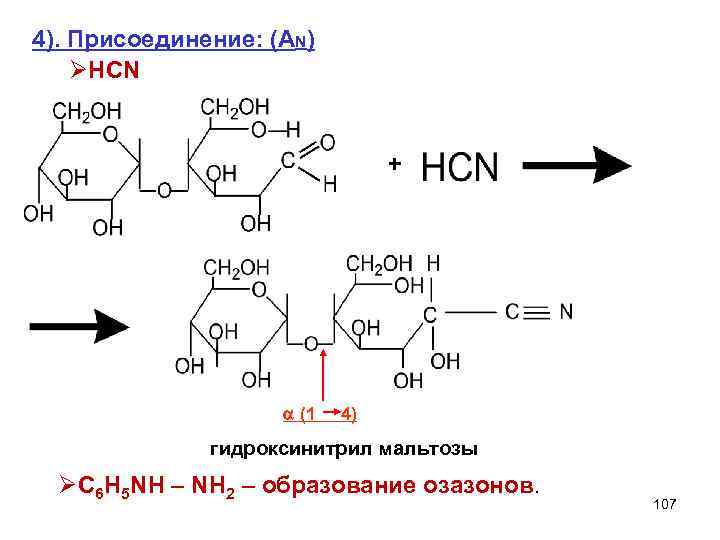
4). Присоединение: (AN) ØHCN + (1 4) гидроксинитрил мальтозы ØC 6 H 5 NH – NH 2 – образование озазонов. 107
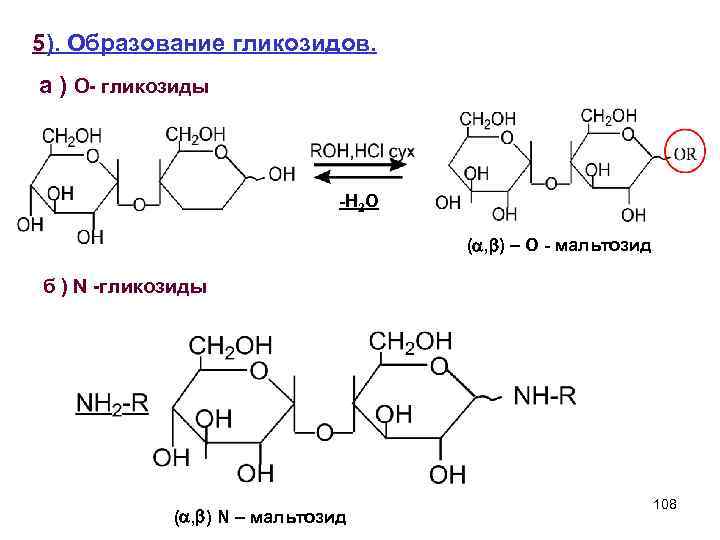
5). Образование гликозидов. а ) O- гликозиды -H 2 O ( , ) – О - мальтозид б ) N -гликозиды ( , ) N – мальтозид 108
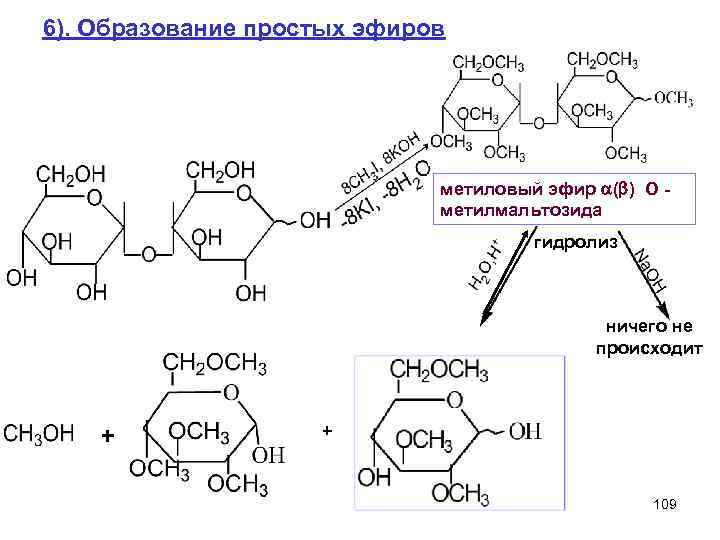
6). Образование простых эфиров метиловый эфир ( ) О - метилмальтозида гидролиз ничего не происходит + + 109
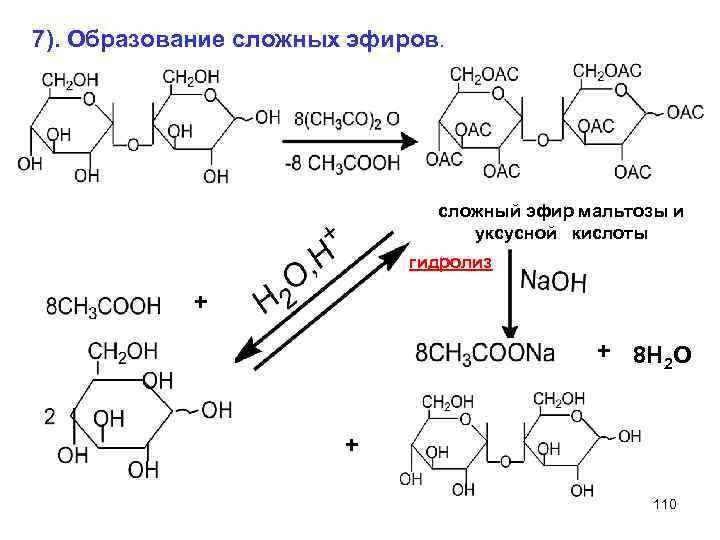
7). Образование сложных эфиров. сложный эфир мальтозы и уксусной кислоты гидролиз + + 8 H 2 O + 110

Физико-химические и химические методы исследования и идентификации углеводов Анализ органических соединений Выделенное и очищенное соединение идентифицируют путем сравнения его физических констант с аналогичными константами известных веществ. К таким константам относятся: 1. Температуры плавления и кипения 2. Плотность 3. Показатель преломления 4. Удельное вращение 5. Хроматографические и 6. Спектральные характеристики 111

Физико-химические и химические методы исследования и идентификации углеводов Качественный функциональный анализ Для установления строения органических соединений используют некоторые химические методы. 1. Для доказательства существования альдегидной группы используют её отличительную способность восстанавливать амммиачный раствор серебра (реактив Толленса) и щелочной раствор тартратного комплекса меди (II) (реактив Фелинга) : 2. Присутствие диольного рагмента определяют свежеосажденным гидроксидом меди (II) при комнатной температуре. 3. Присутствие енольного фрагмента подтверждается цветной реакцией с раствором хлорида железа (III). 112

Хроматографические методы исследования • Распределительная хроматография была впервые применена для разделения углеводов в 1949 г. С тех пор этот метод широко используется в препаративной химии углеводов. Область применения этого метода в химии углеводов обширна. • Тонкослойная хроматография (ТСХ) в том виде, в каком она известна сейчас впервые была описана Шталем 1958 г. , а в 1961 г. появилось первое сообщение о применении ТСХ для разделения углеводов. • Начиная с этого времени ТСХ широко используется для идентификации углеводов, в том числе незамещенных моно- и олигосахаридов и различных производных сахаров и сложных эфиров, циклических ацеталей и других производных. 113
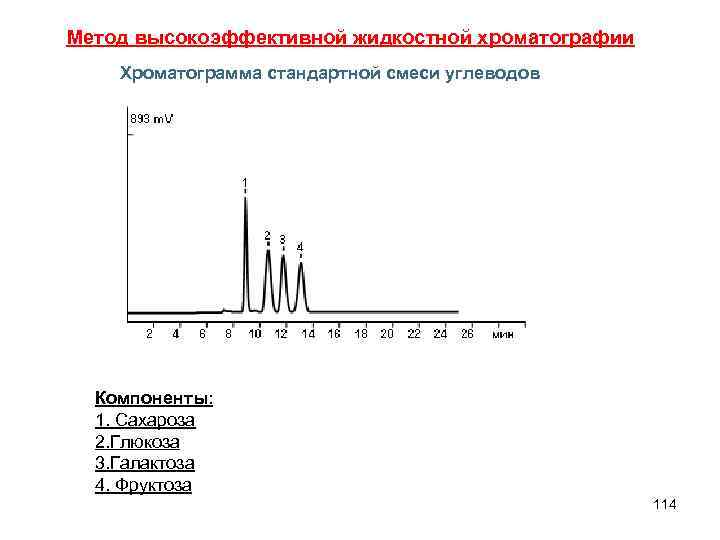
Метод высокоэффективной жидкостной хроматографии Хроматограмма стандартной смеси углеводов Компоненты: 1. Сахароза 2. Глюкоза 3. Галактоза 4. Фруктоза 114
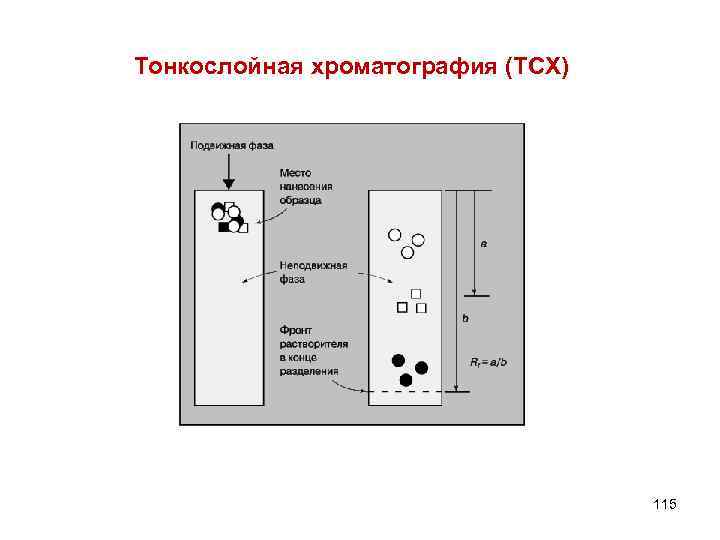
Тонкослойная хроматография (ТСХ) 115
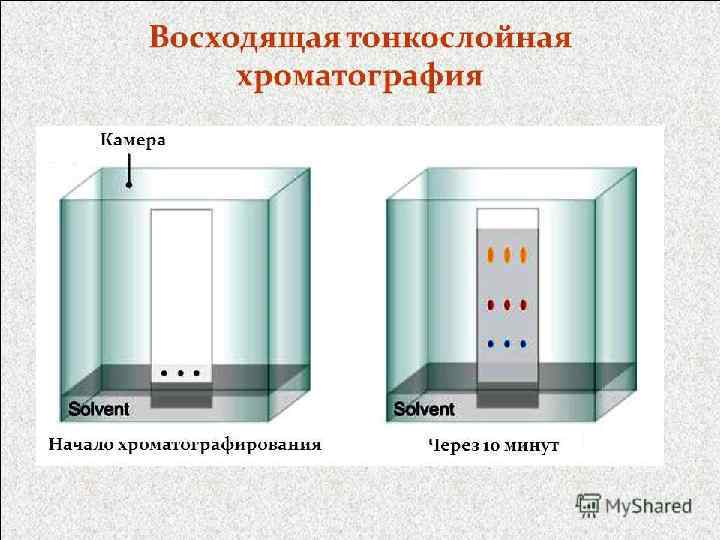
116
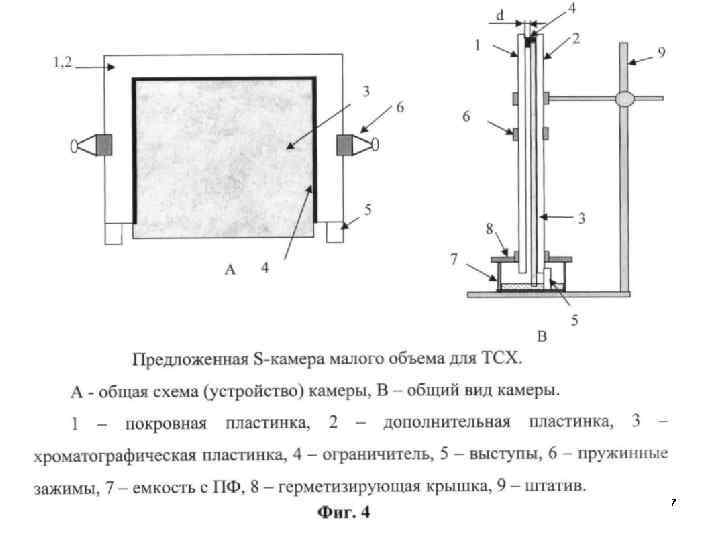
117

Хроматографические методы исследования Тонкослойная хроматография находит все большее применение для количественного определения углеводов. Этот метод чрезвычайно полезен при изучении кинетики реакций, исследовании их механизма и определении выхода продуктов, однако он применим лишь для анализа смесей, компоненты которых можно полностью разделить. Способы количественного определения делят на две большие группы: а) прямое определение (установление количества вещества непосредственно на пластинке); б) косвенное определение (элюирование пятен вещества с последующим анализом элюата физическими методами). 118

Спасибо за внимание! 119
lect_org_6-1.ppt