lect_org_1.ppt
- Количество слайдов: 132

Кафедра общей и медицинской химии Лекция № 1 Ароматические и гетероциклические соединения. Электронная спектроскопия 1
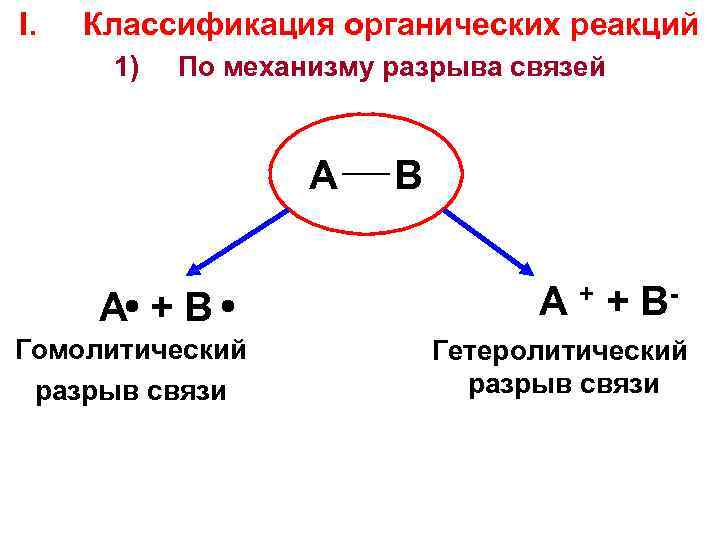
I. Классификация органических реакций 1) По механизму разрыва связей А В А + В Гомолитический разрыв связи А + + В- Гетеролитический разрыв связи 2
а) Радикальные реакции: ь гомолитический разрыв связи: А· + В· - свободные радикалы (R) - очень активные частицы, стремятся к образованию связей Н·, Cl·, O: , ·OH Условия: газовая фаза, свет, неполярный растворитель 3

Н. Н. Семенов (1896 -1986 г. ) ь Лауреат Нобелевской премии (1956 г. ) ь Создатель теории механизма свободнорадикальных(цепных) реакций 4

б) Ионные реакции: ь гетеролитический разрыв связи ь образуются положительные частицы- электрофилы Е ( ) (Н+, NO 2+, Br+, SO 3 и т. д. ) ь отрицательные частицы – нуклеофилы – Nu (H–, OH–, NH 2, H 2 O и т. д. ) Условия протекания ионных реакций: полярные растворители 5

в) синхронные реакции–разрыв старых и образование новых связей происходят одновременно. 6

2) По конечному результату: S: (реакции замещения, анл. Substitution) SR - алканы SE - арены SN - галогенпроизводные, спирты, карбоновые кислоты A: (реакции присоединения , англ. Addition) AR – алкены, алкины AE – алкены, алкины AN – альдегиды, кетоны E (реакции отщепления, англ. Elimination) OBР (окислительно-восстановительные) 7

3) По числу частиц, принимающих участие в элементарной стадии: - мономолекулярные (SN 1) - бимолекулярные (SN 2) 8

II. Электронные эффекты заместителей. Участок молекулы, где ē - плотность максимальная или минимальная является самым реакционноспособным. На реакционную способность влияют: ь электронные эффекты заместителей ь наличие сопряжения ь пространственные факторы 9

Электронные эффекты заместителей. Любой атом или группа атомов, замещающая H в исходном соединении, называется заместителем. Влияние заместителей определяется электронными эффектами: индуктивным (I) и мезомерным (M). 10
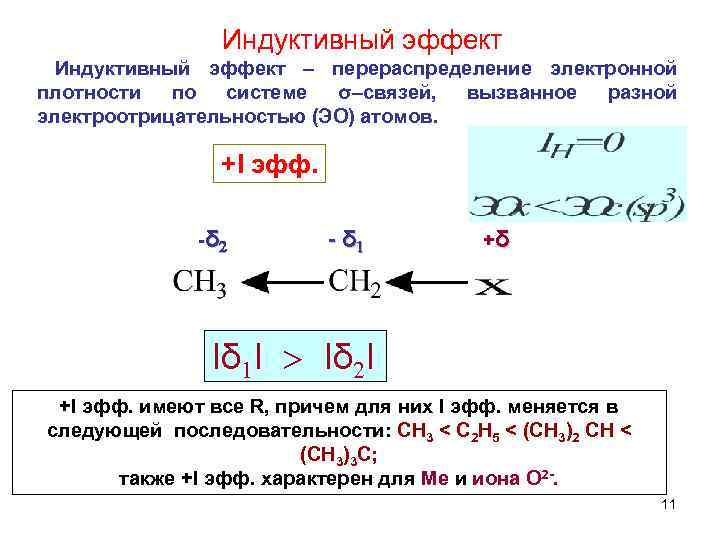
Индуктивный эффект – перераспределение электронной плотности по системе σ–связей, вызванное разной электроотрицательностью (ЭО) атомов. +I эфф. -δ 2 - δ 1 +δ Іδ 1І > Іδ 2І +I эфф. имеют все R, причем для них I эфф. меняется в следующей последовательности: CH 3 < C 2 H 5 < (CH 3)2 CH < (CH 3)3 C; также +I эфф. характерен для Мe и иона О 2 -. 11
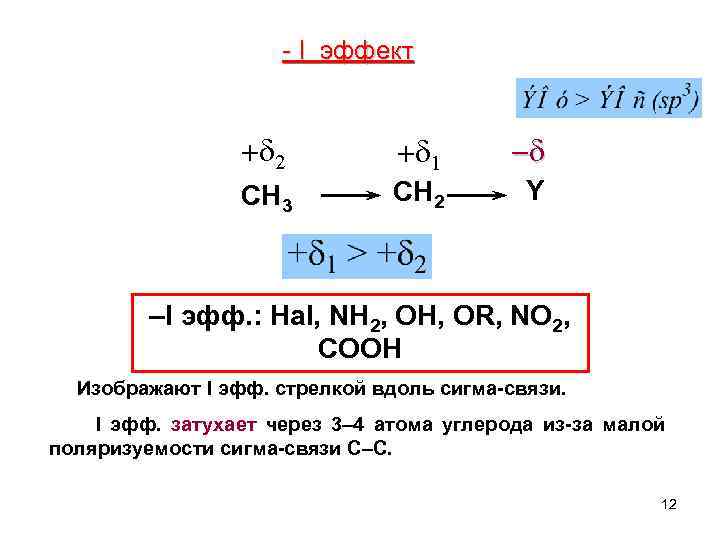
- I эффект + 2 + 1 - CH 3 CH 2 Y –I эфф. : Hal, NH 2, OH, OR, NO 2, COOH Изображают I эфф. стрелкой вдоль сигма-связи. I эфф. затухает через 3– 4 атома углерода из-за малой поляризуемости сигма-связи С–С. 12

МЕЗОМЕРНЫЙ ЭФФЕКТ (ЭФФЕКТ СОПРЯЖЕНИЯ) Мезомерный эффект (М) – перераспределение электронной плотности по системе p–связей. М эфф. , в отличие от I эфф. , возникает лишь там, где появляется сопряжение. Сопряжение – это выравнивание связей и зарядов в реальной молекуле по сравнению с идеальной. Сопряжение возникает в результате образования единого –делокализованного облака, принадлежащего более чем двум атомам. 13
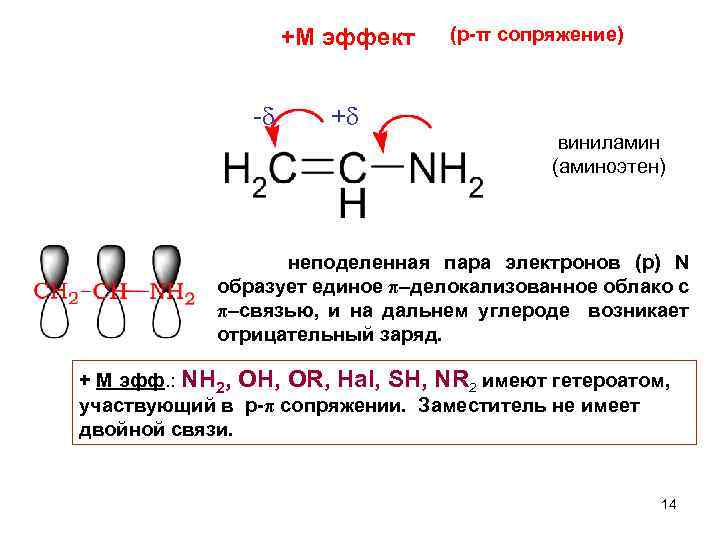
+М эффект - (p-π сопряжение) + виниламин (аминоэтен) неподеленная пара электронов (р) N образует единое π–делокализованное облако с π–связью, и на дальнем углероде возникает отрицательный заряд. + М эфф. : NH 2, OH, OR, Hal, SH, NR 2 имеют гетероатом, участвующий в p-π сопряжении. Заместитель не имеет двойной связи. 14
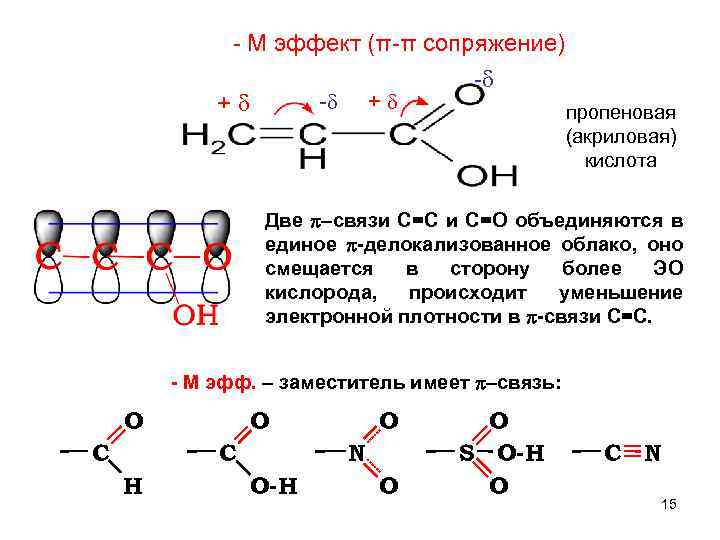
- М эффект (π-π сопряжение) - - + + пропеновая (акриловая) кислота Две p–связи С=С и С=О объединяются в единое p-делокализованное облако, оно смещается в сторону более ЭО кислорода, происходит уменьшение электронной плотности в p-связи С=С. - М эфф. – заместитель имеет p–связь: O C H O N O-H O O S O-H O C N 15
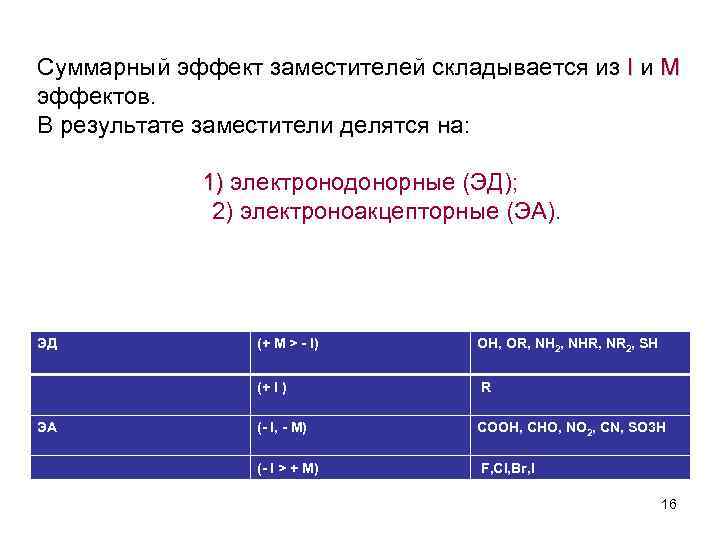
Суммарный эффект заместителей складывается из I и М эффектов. В результате заместители делятся на: 1) электронодонорные (ЭД); 1) 2) электроноакцепторные (ЭА). ЭД OH, OR, NH 2, NHR, NR 2, SH (+ I ) ЭА (+ М > - I) R (- I, - M) COOH, CHO, NO 2, CN, SO 3 Н (- I > + M) F, CI, Br, I 16

Сопряженные системы С открытой цепью сопряжения ь имеют начало и конец сопряжения ь Представители: - бутадиен-1, 3 - изопрен - циклопентадиен- (1, 3) - сорбиновая кислота - β-каротин С замкнутой цепью сопряжения ь циклическое сопряжение ь Представители - арены - гетероциклические соединения 17

Системы с открытой цепью сопряжения СОПРЯЖЕНИЕ – это выравнивание связи по энергии и по длине, вызванное образованием π –единого делокализованного облака. ЭНЕРГИЯ СОПРЯЖЕНИЯ – понижение энергии реальной молекулы, по сравнению с молекулами с изолированными связями. В результате сопряжения молекула становится более термодинамически устойчивой. NB! Чем больше энергия сопряжения, тем устойчивее молекула! 18

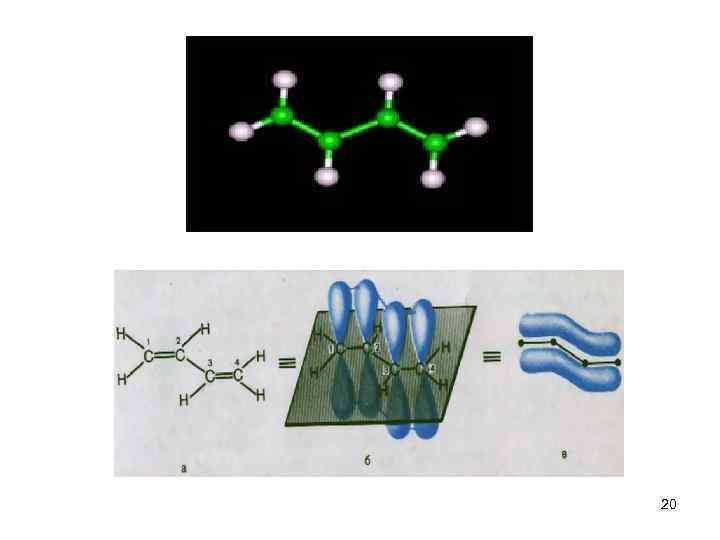
В сопряженных системах существует чередование двойной и одинарной связей: Если имеется начало и конец сопряжения – это открытая цепь сопряжения. бутадиен-1, 3: Е сопр. = 15 к. Дж/Моль 19
20
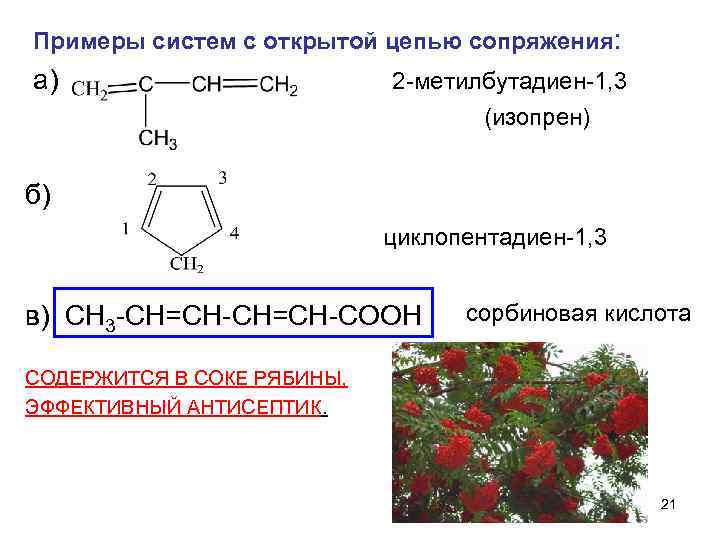
Примеры систем с открытой цепью сопряжения: а) 2 -метилбутадиен-1, 3 (изопрен) б) циклопентадиен-1, 3 в) CH 3 -CH=CH-COOH сорбиновая кислота СОДЕРЖИТСЯ В СОКЕ РЯБИНЫ, ЭФФЕКТИВНЫЙ АНТИСЕПТИК. 21

β–каротин – провитамин А, обуславливает окраску моркови, томатов, масла; имеет сопряженную систему из 11 двойных (= ) связей. В организме при его расщеплении образуется ретинол – витамин А – (5 =): витамин роста, понижает сопротивление к инфекционным заболеваниям; и ретиналь (6 =): отвечает за поглощение света в зрительном нерве. Чем длиннее цепь сопряжения, тем устойчивее молекула к внешним воздействиям! 22

ОСОБЕННОСТИ РЕАКЦИОННОЙ СПОСОБНОСТИ СОПРЯЖЕННЫХ СИСТЕМ С ОТКРЫТОЙ ЦЕПЬЮ СОПРЯЖЕНИЯ Химическое поведение молекулы обусловлено природой химической связи, распределением электронной плотности. NB! Особенности химической связи в сопряженных системах: 1) Образование π-делокализованного облака, единого для всей молекулы 2) Выравнивание длины связи 3) Легкая поляризуемость π-облака 23
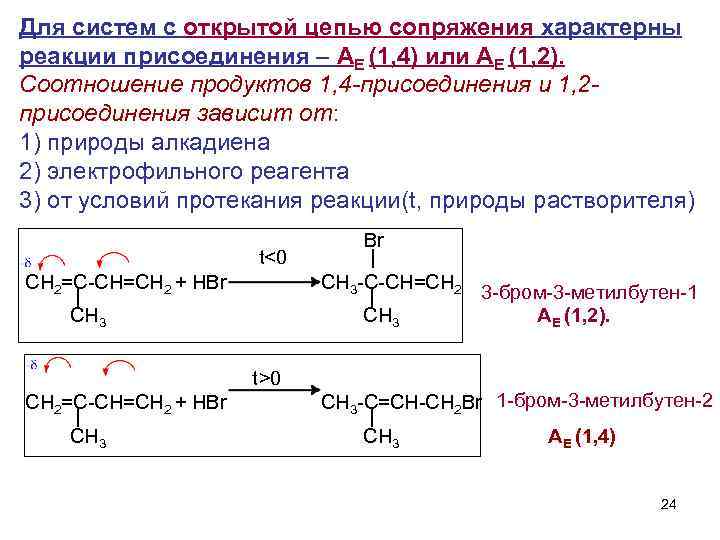
Для систем с открытой цепью сопряжения характерны реакции присоединения – АЕ (1, 4) или АЕ (1, 2). Соотношение продуктов 1, 4 -присоединения и 1, 2 присоединения зависит от: 1) природы алкадиена 2) электрофильного реагента 3) от условий протекания реакции(t, природы растворителя) Br t<0 | СH 2=C-CH=CH 2 + HBr СH 3 -C-CH=CH 2 3 -бром-3 -метилбутен-1 | CH 3 АЕ (1, 2). t>0 СH 2=C-CH=CH 2 + HBr СH 3 -C=CH-CH 2 Br 1 -бром-3 -метилбутен-2 | CH 3 АЕ (1, 4) 24
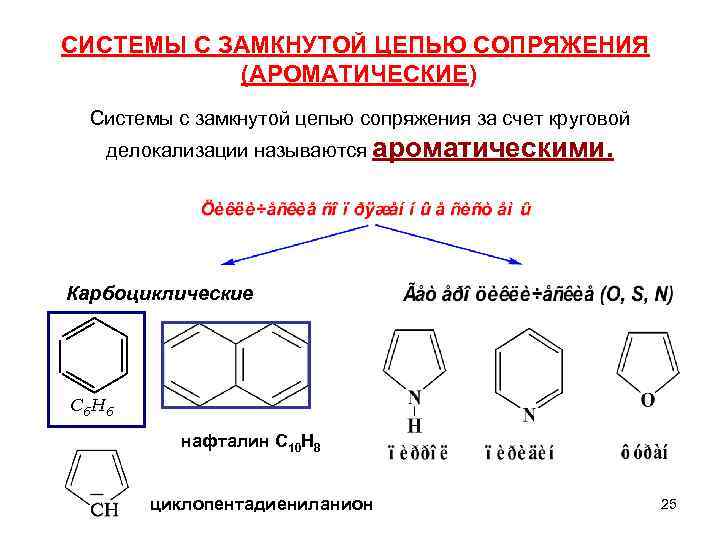
СИСТЕМЫ С ЗАМКНУТОЙ ЦЕПЬЮ СОПРЯЖЕНИЯ (АРОМАТИЧЕСКИЕ) Системы с замкнутой цепью сопряжения за счет круговой делокализации называются ароматическими. Карбоциклические C 6 H 6 нафталин C 10 H 8 циклопентадиениланион 25
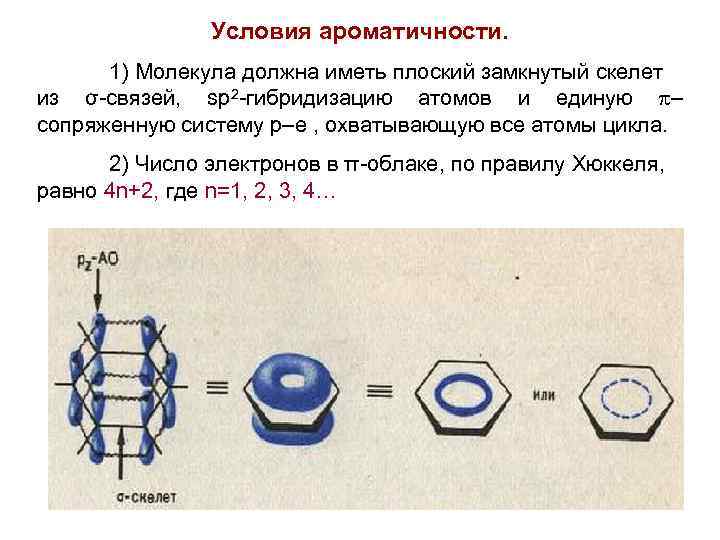
Условия ароматичности. 1) Молекула должна иметь плоский замкнутый скелет из σ-связей, sp 2 -гибридизацию атомов и единую – сопряженную систему р–е , охватывающую все атомы цикла. 2) Число электронов в π-облаке, по правилу Хюккеля, равно 4 n+2, где n=1, 2, 3, 4… 26

ХИМИЧЕСКИЕ СВОЙСТВА БЕНЗОЛА 27

Для ароматических УВ, характерны реакции, обусловленные замкнутой цепью сопряжения. ь Устойчивость к окислению (энергия сопряжения =150 к. Дж/моль) ; ь Способность к реакциям SЕ (сохраняющим ароматичность) ь Относительная устойчивость к реакциям присоединения А (жесткие условия). 28

Общая схема SE а) Образование электрофильной частицы под действием катализатора: б) Образование π-комплекса π–комплекс: нехимическое соединение, π–облако содержит 6 электронов, ароматический характер не нарушен. 29
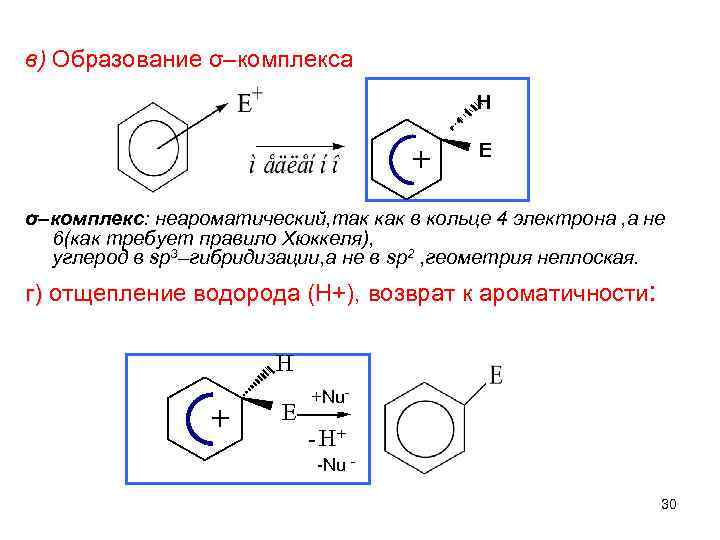
в) Образование σ–комплекса H + E σ–комплекс: неароматический, так как в кольце 4 электрона , а не 6(как требует правило Хюккеля), углерод в sp 3–гибридизации, а не в sp 2 , геометрия неплоская. г) отщепление водорода (Н+), возврат к ароматичности: г) H + E +Nu- - H+ -Nu 30

Химические реакции 1) Галогенирование: Реагенты: Cl 2, Br 2; катализаторы: Al. Cl 3, Fe. Br 3 2) Нитрование: Реагент: HNO 3 (конц. ); УСЛОВИЯ: H 2 SO 4 (конц. ) 3) Сульфирование: Реагент H 2 SO 4 конц. (SO 3) 4) Алкилирование – образование гомологов бензола (реакция Фриделя-Крафтса): Реагент R- Г (Г-CI, Br, I), катализатор Al. Cl 3, Fe. Cl 3, Fe. Br 3 5) Ацилирование - образование кетонов (реакция Фриделя. Крафтса) Реагент: RCOCl, ; катализаторы: Al. Cl 3, Fe. Br 3 31
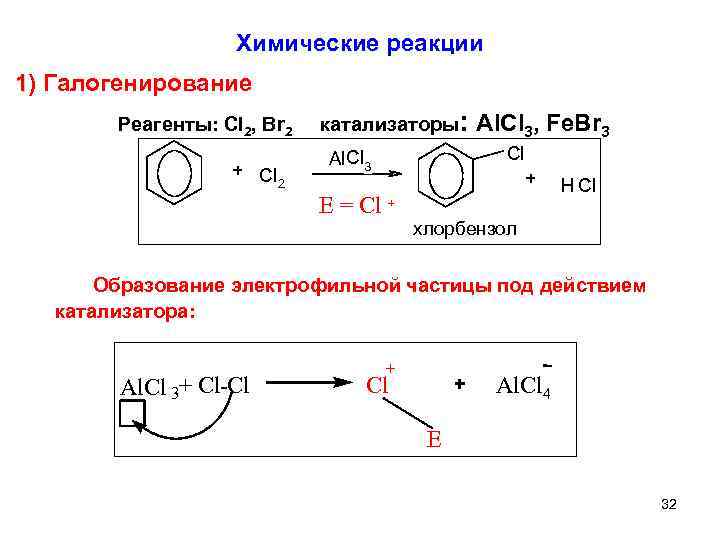
Химические реакции 1) Галогенирование Реагенты: Cl 2, Br 2 катализаторы: Al. Cl 3, Fe. Br 3 + Cl 2 Cl Al. Cl 3 E = Cl + H Cl + хлорбензол Образование электрофильной частицы под действием катализатора: Al. Cl 3+ Cl-Cl + Al. Cl 4 E 32
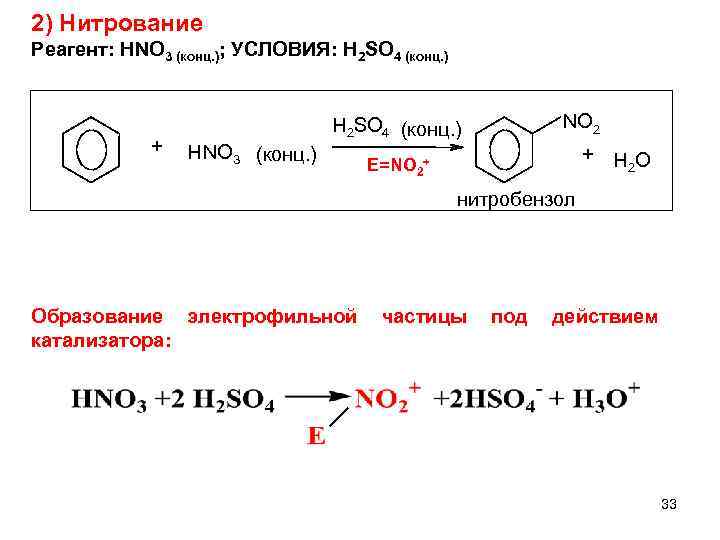
2) Нитрование Реагент: HNO 3 (конц. ); УСЛОВИЯ: H 2 SO 4 (конц. ) + H 2 SO 4 (конц. ) H NО 3 (конц. ) NО 2 + HО 2 E=NO 2+ нитробензол Образование электрофильной частицы под действием катализатора: 33
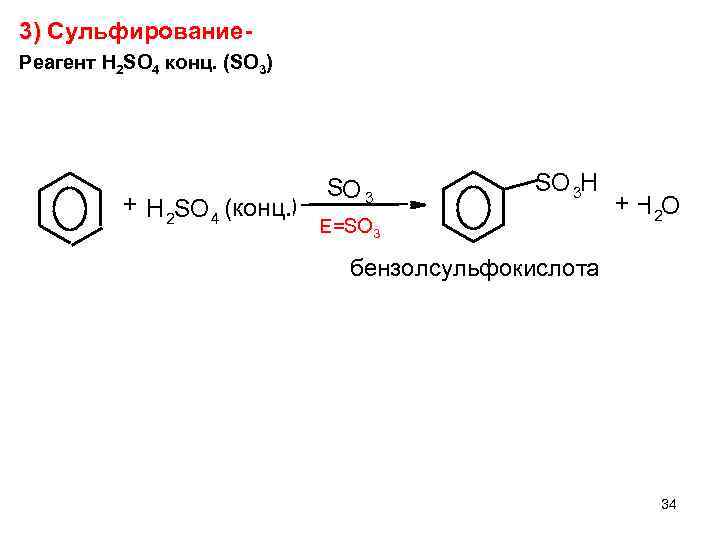
3) Сульфирование- 3) Реагент H 2 SO 4 конц. (SO 3) + H 2 SO 4 (конц. ) SО 3 SO 3 H E=SO 3 + H 2 О бензолсульфокислота 34
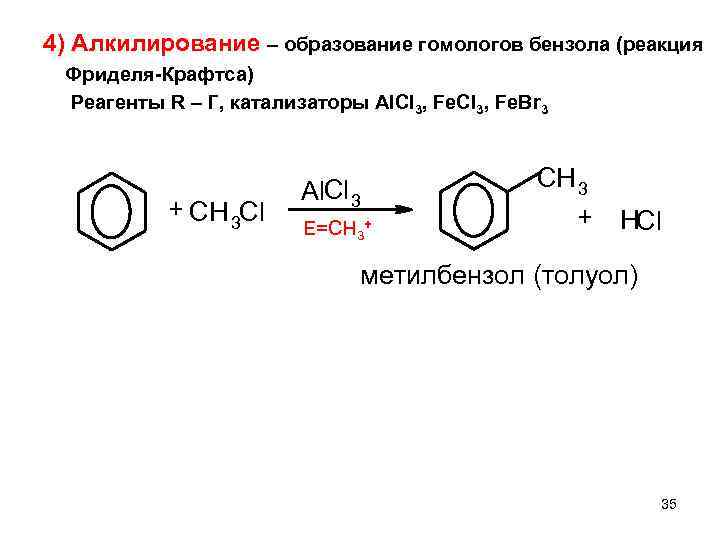
4) Алкилирование – образование гомологов бензола (реакция Фриделя-Крафтса) Реагенты R – Г, катализаторы Al. Cl 3, Fe. Br 3 + CH 3 Cl Al. Cl 3 E=CH 3+ CH 3 + HCl метилбензол (толуол) 35
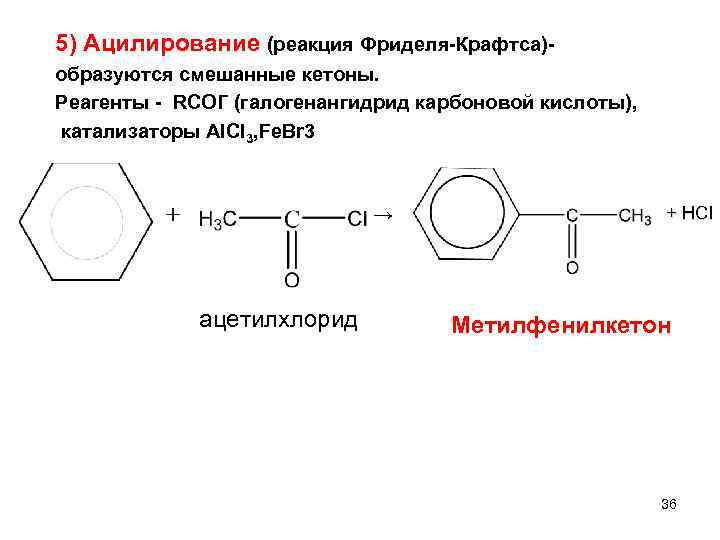
5) Ацилирование (реакция Фриделя-Крафтса)образуются смешанные кетоны. Реагенты - RCOГ (галогенангидрид карбоновой кислоты), катализаторы AICI 3, Fe. Br 3 → ацетилхлорид + HCI Метилфенилкетон 36

ПРАВИЛА ЗАМЕЩЕНИЯ В БЕНЗОЛЬНОМ КОЛЬЦЕ NB! 1. Первый заместитель встает в любое положение и влияет на распределение электронной плотности в кольце. 2. По влиянию на распределение электронной плотности заместители делятся на два рода. 37
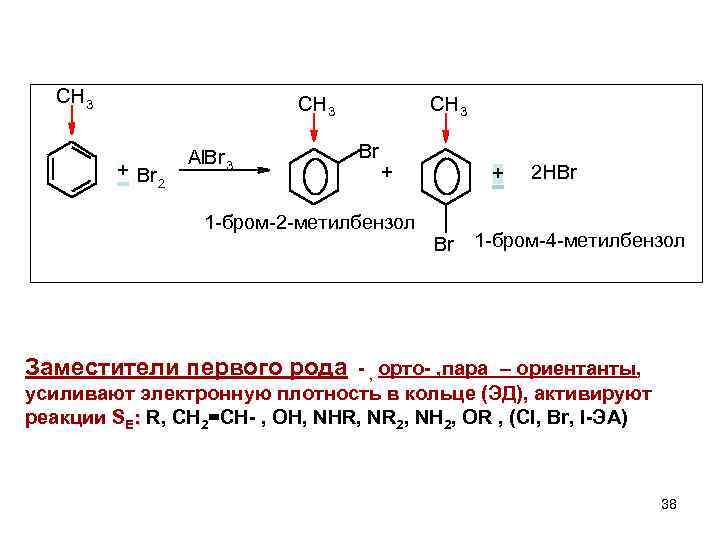
CH 3 + Br 2 Al. Br 3 CH 3 Br + 1 -бром-2 -метилбензол + Br 2 HBr 1 -бром-4 -метилбензол Заместители первого рода - , орто- , пара – ориентанты, усиливают электронную плотность в кольце (ЭД), активируют реакции SЕ: R, CH 2=CH- , OH, NHR, NR 2, NH 2, OR , (Cl, Br, I-ЭА) 38
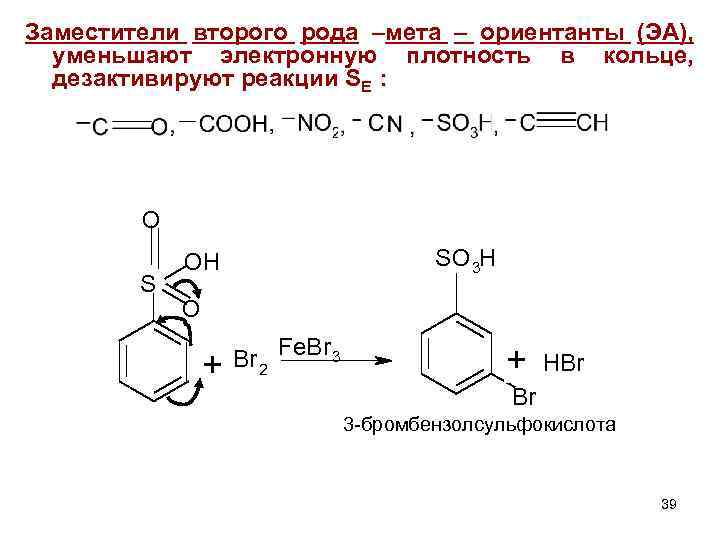
Заместители второго рода –мета – ориентанты (ЭА), уменьшают электронную плотность в кольце, дезактивируют реакции SE : O S O + SO 3 H OH Br 2 Fe. Br 3 + HBr Br 3 -бромбензолсульфокислота 39

ЛЕКАРСТВЕННЫЕ СРЕДСТВА НА ОСНОВЕ БЕНЗОЛА 40

Фенолокислоты — это ароматические кислоты, в молекуле которых одновременно с карбоксильной группой имеется фенольный гидроксил. Наибольшую физиологическую активность проявляет - о-гидроксибензойная, или салициловая, 2 -гидроксибензойная кислота (салициловая) 41
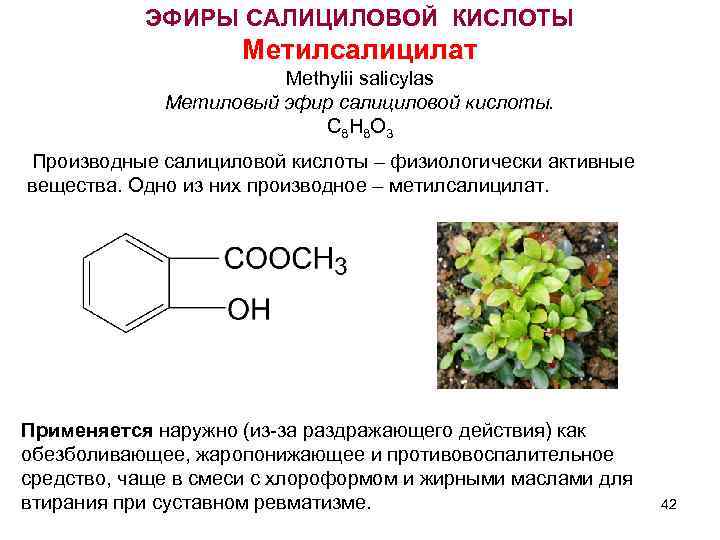
ЭФИРЫ САЛИЦИЛОВОЙ КИСЛОТЫ Метилсалицилат Methylii salicylas Метиловый эфир салициловой кислоты. С 8 Н 8 О 3 Производные салициловой кислоты – физиологически активные вещества. Одно из них производное – метилсалицилат. Применяется наружно (из-за раздражающего действия) как обезболивающее, жаропонижающее и противовоспалительное средство, чаще в смеси с хлороформом и жирными маслами для втирания при суставном ревматизме. 42
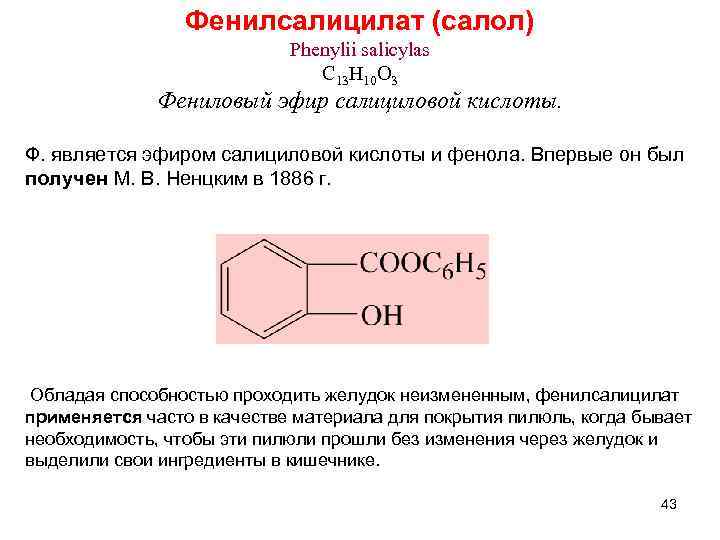
Фенилсалицилат (салол) Phenylii salicylas C 13 H 10 O 3 Фениловый эфир салициловой кислоты. Ф. является эфиром салициловой кислоты и фенола. Впервые он был получен М. В. Ненцким в 1886 г. Обладая способностью проходить желудок неизмененным, фенилсалицилат применяется часто в качестве материала для покрытия пилюль, когда бывает необходимость, чтобы эти пилюли прошли без изменения через желудок и выделили свои ингредиенты в кишечнике. 43
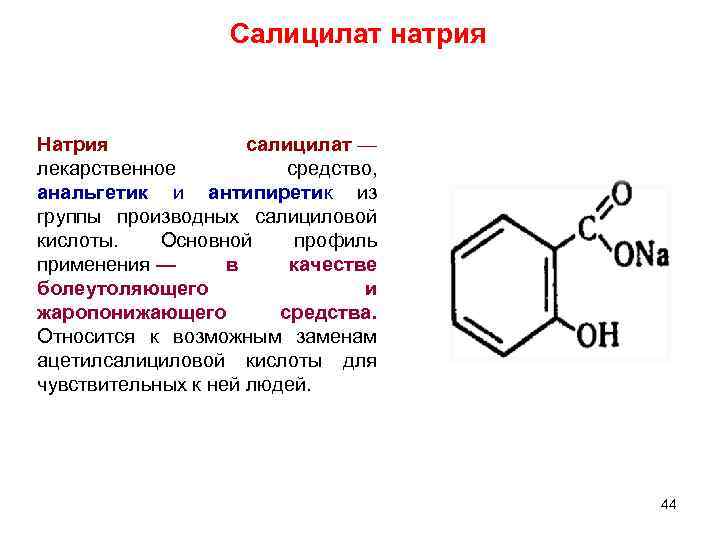
Салицилат натрия Натрия салицилат — лекарственное средство, анальгетик и антипиретик из группы производных салициловой кислоты. Основной профиль применения — в качестве болеутоляющего и жаропонижающего средства. Относится к возможным заменам ацетилсалициловой кислоты для чувствительных к ней людей. 44

Ацетилсалициловая кислота (аспирин) Acidum acetylsalicylicum C 9 H 8 O 4 2 -(ацетилокси)-бензойная кислота. Салициловая кислота впервые была получена путем окисления салицилового альдегида, содержавшегося в растении Таволге (род Spireae). Отсюда её первоначальное название – спировая кислота, с которым связано название аспирин ( «а» обозначает ацетил). Ацетилсалициловая кислота в природе не найдена. 45
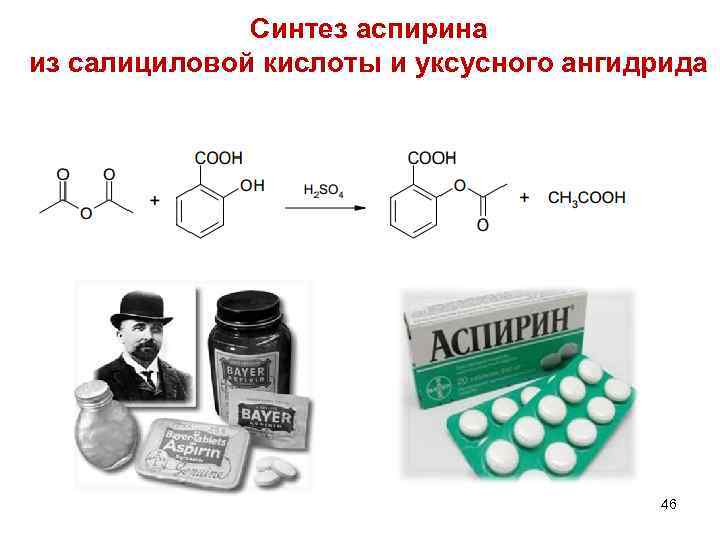
Синтез аспирина из салициловой кислоты и уксусного ангидрида 46
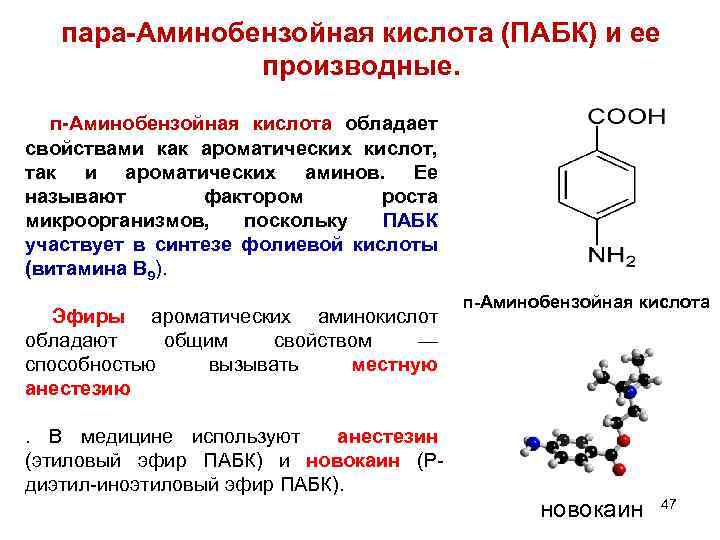
пара-Аминобензойная кислота (ПАБК) и ее производные. п-Аминобензойная кислота обладает свойствами как ароматических кислот, так и ароматических аминов. Ее называют фактором роста микроорганизмов, поскольку ПАБК участвует в синтезе фолиевой кислоты (витамина В 9). п-Аминобензойная кислота Эфиры ароматических аминокислот обладают общим свойством — способностью вызывать местную анестезию. В медицине используют анестезин (этиловый эфир ПАБК) и новокаин (Рдиэтил-иноэтиловый эфир ПАБК). новокаин 47
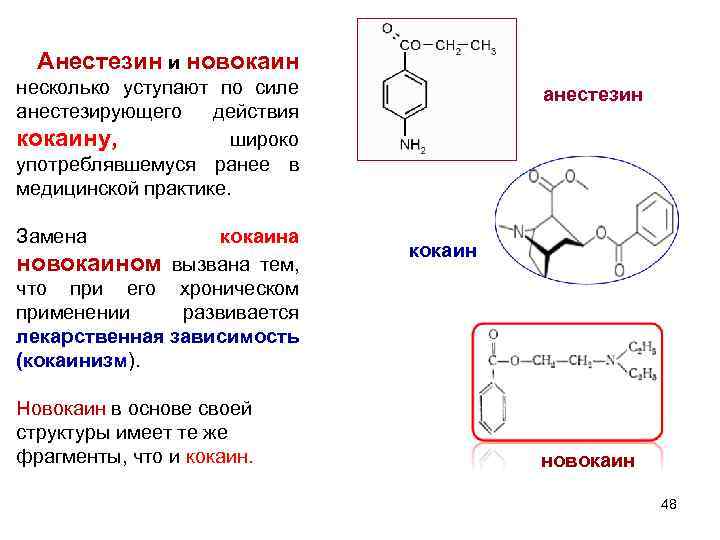
Анестезин и новокаин несколько уступают по силе анестезирующего действия кокаину, широко употреблявшемуся ранее в медицинской практике. Замена кокаина новокаином вызвана тем, что при его хроническом применении развивается лекарственная зависимость (кокаинизм). Новокаин в основе своей структуры имеет те же фрагменты, что и кокаин. анестезин кокаин новокаин 48
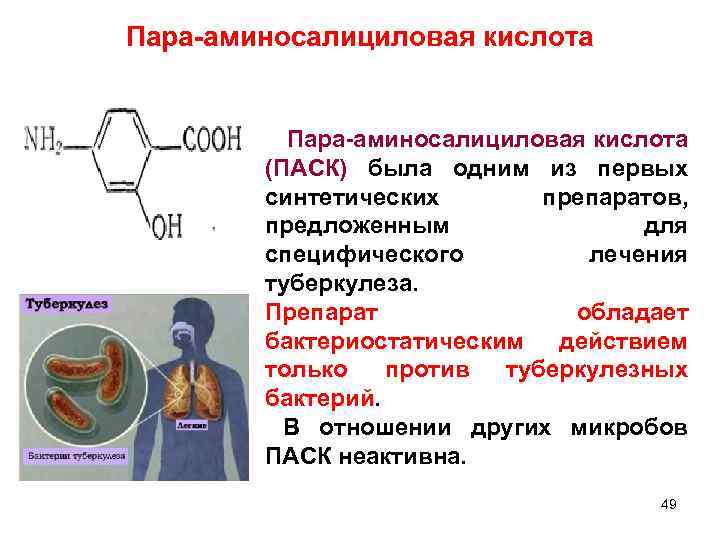
Пара-аминосалициловая кислота (ПАСК) была одним из первых синтетических препаратов, предложенным для специфического лечения туберкулеза. Препарат обладает бактериостатическим действием только против туберкулезных бактерий. В отношении других микробов ПАСК неактивна. 49
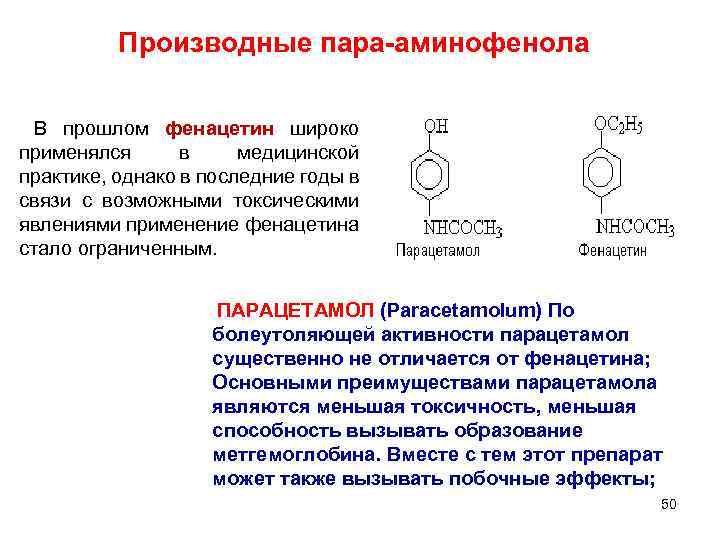
Производные пара-аминофенола В прошлом фенацетин широко применялся в медицинской практике, однако в последние годы в связи с возможными токсическими явлениями применение фенацетина стало ограниченным. ПАРАЦЕТАМОЛ (Paracetamolum) По болеутоляющей активности парацетамол существенно не отличается от фенацетина; Основными преимуществами парацетамола являются меньшая токсичность, меньшая способность вызывать образование метгемоглобина. Вместе с тем этот препарат может также вызывать побочные эффекты; 50

Анальгин (Метамизол натрия) лекарственное средство, анальгетик и антипиретик из группы пиразолонов. Синтезирован Людвигом Кнорром в 1920 году. Во многих странах изъят из оборота в связи с риском развития агранулоцитоза. При возникновении агранулоцитоза вероятность смертельного исхода оценивают примерно в 7 % — в случае доступности медицинской помощи 51
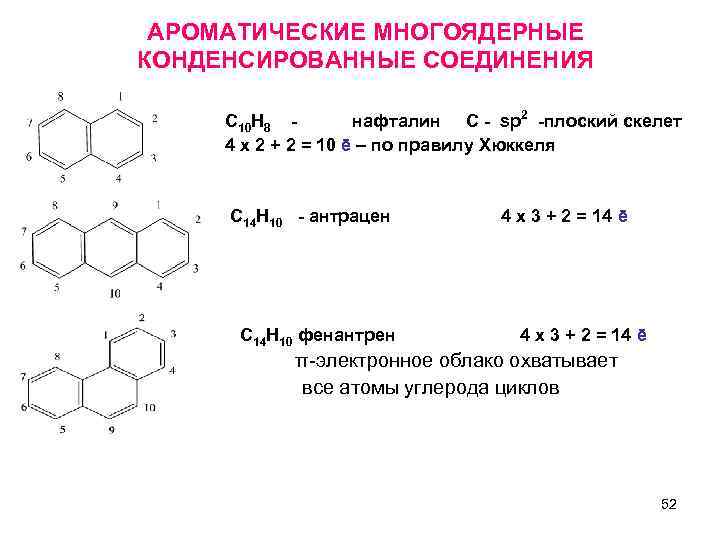
АРОМАТИЧЕСКИЕ МНОГОЯДЕРНЫЕ КОНДЕНСИРОВАННЫЕ СОЕДИНЕНИЯ С 10 Н 8 - нафталин С - sp 2 -плоский скелет 4 х 2 + 2 = 10 ē – по правилу Хюккеля С 14 Н 10 - антрацен 4 х 3 + 2 = 14 ē С 14 Н 10 фенантрен 4 х 3 + 2 = 14 ē π-электронное облако охватывает все атомы углерода циклов 52
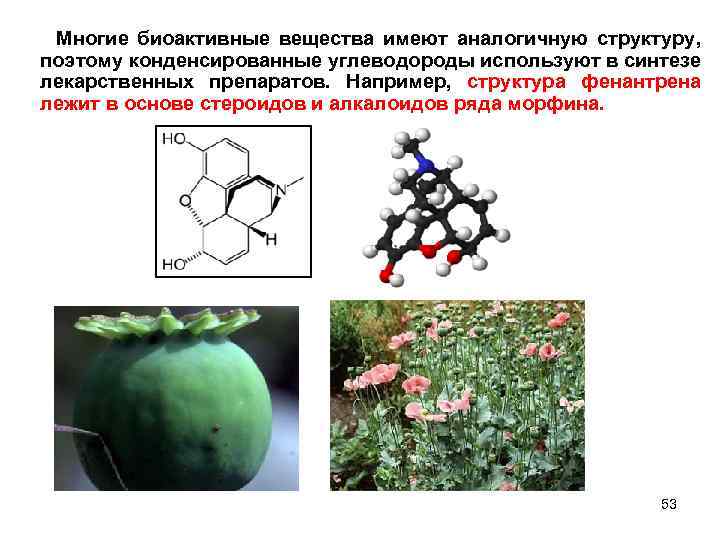
Многие биоактивные вещества имеют аналогичную структуру, поэтому конденсированные углеводороды используют в синтезе лекарственных препаратов. Например, структура фенантрена лежит в основе стероидов и алкалоидов ряда морфина. 53
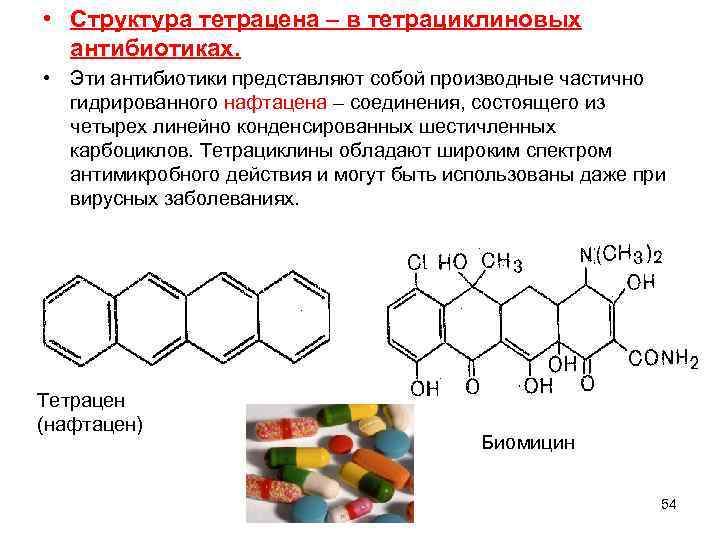
• Структура тетрацена – в тетрациклиновых антибиотиках. • Эти антибиотики представляют собой производные частично гидрированного нафтацена – соединения, состоящего из четырех линейно конденсированных шестичленных карбоциклов. Тетрациклины обладают широким спектром антимикробного действия и могут быть использованы даже при вирусных заболеваниях. Тетрацен (нафтацен) Биомицин 54
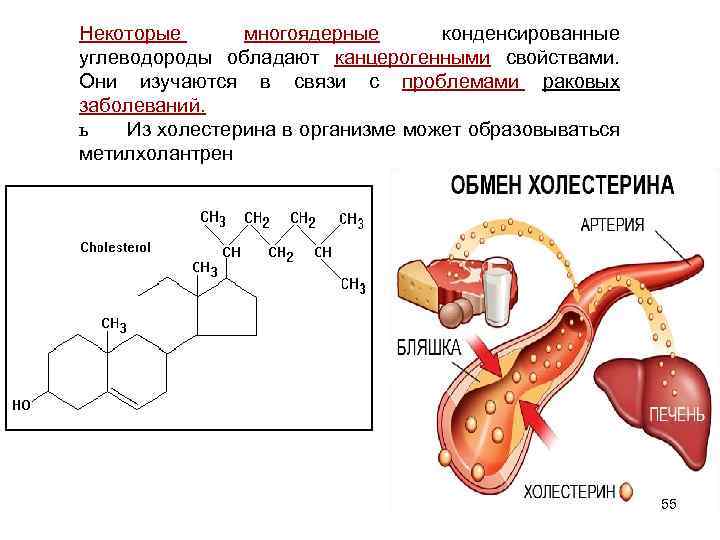
Некоторые многоядерные конденсированные углеводороды обладают канцерогенными свойствами. Они изучаются в связи с проблемами раковых заболеваний. ь Из холестерина в организме может образовываться метилхолантрен 55
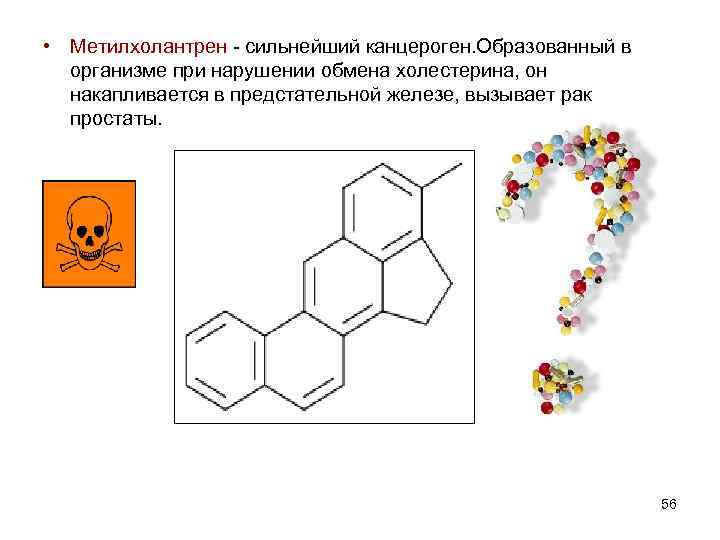
• Метилхолантрен - сильнейший канцероген. Образованный в организме при нарушении обмена холестерина, он накапливается в предстательной железе, вызывает рак простаты. 56
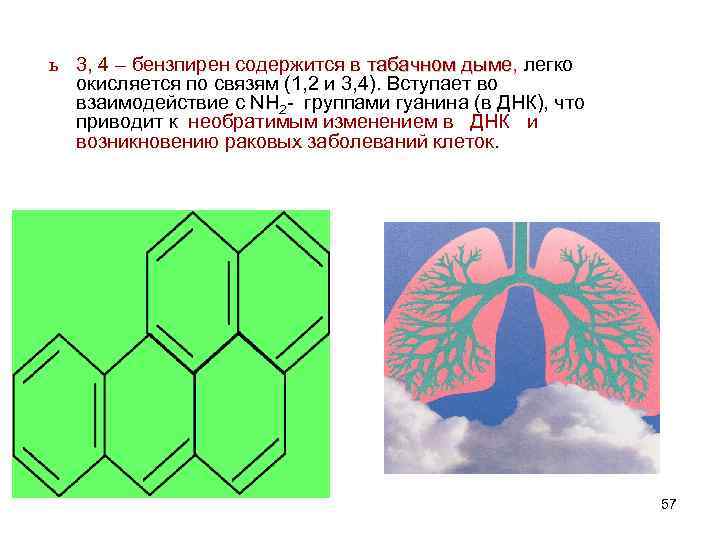
ь 3, 4 – бензпирен содержится в табачнoм дыме, легко м дыме окисляется по связям (1, 2 и 3, 4). Вступает во взаимодействие с NH 2 - группами гуанина (в ДНК), что приводит к необратимым изменением в ДНК и возникновению раковых заболеваний клеток. 57

Химические свойства конденсированных систем Химические свойства подобны свойствам бензола но, в связи с неполной выравненностью электронной плотности, имеют особенности: а) SЕ протекают легче, чем в бензоле б) достаточно активны в реакциях присоединения и окисления 58
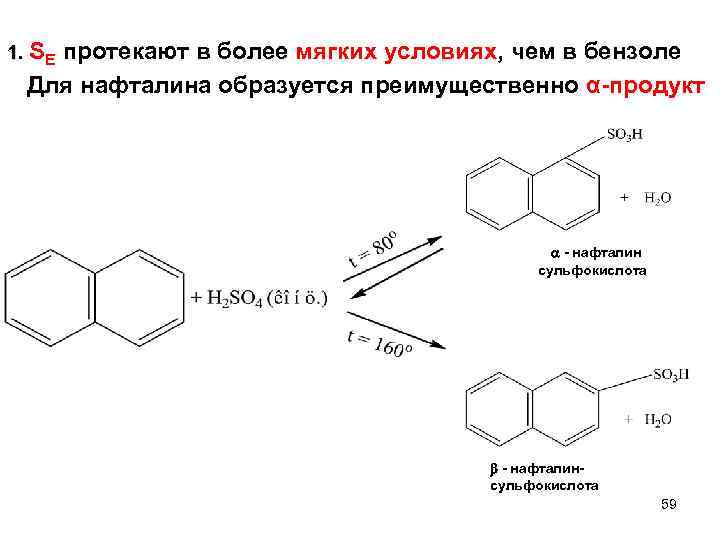
1. SЕ протекают в более мягких условиях, чем в бензоле Для нафталина образуется преимущественно α-продукт - нафталин сульфокислота - нафталин сульфокислота 59
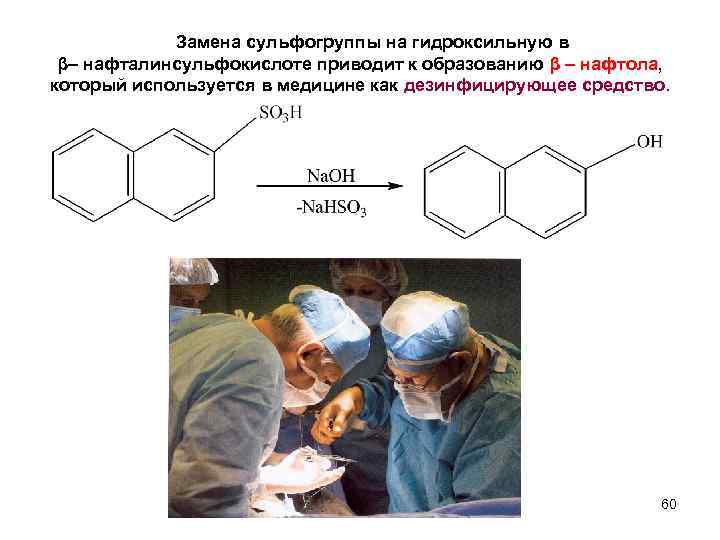
Замена сульфогруппы на гидроксильную в β– нафталинсульфокислоте приводит к образованию β – нафтола, – нафтола который используется в медицине как дезинфицирующее средство. 60
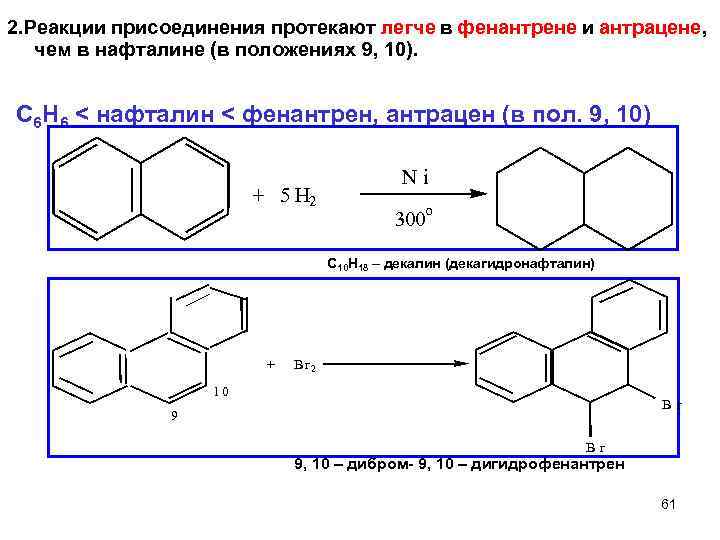
2. Реакции присоединения протекают легче в фенантрене и антрацене, чем в нафталине (в положениях 9, 10). C 6 H 6 < нафталин < фенантрен, антрацен (в пол. 9, 10) Ni + 5 H 2 o 300 C H – декалин (декагидронафталин) 10 + 18 Br 2 10 9 Br 9, 10 – дибром- 9, 10 – дигидрофенантрен 61
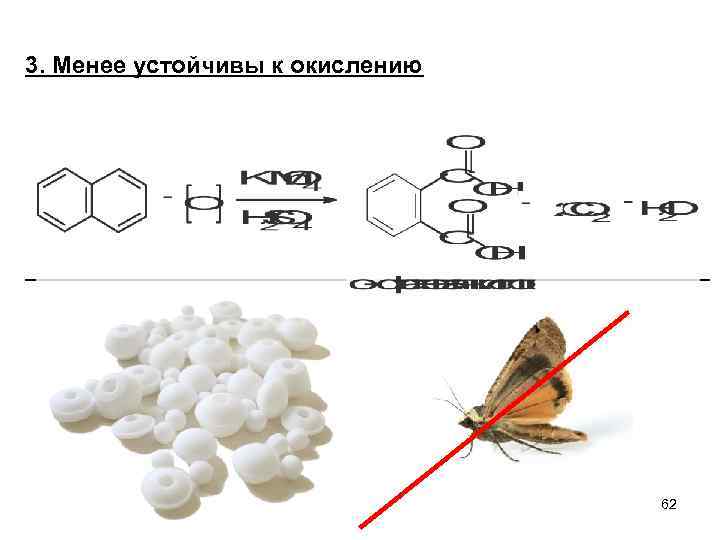
3. Менее устойчивы к окислению 62
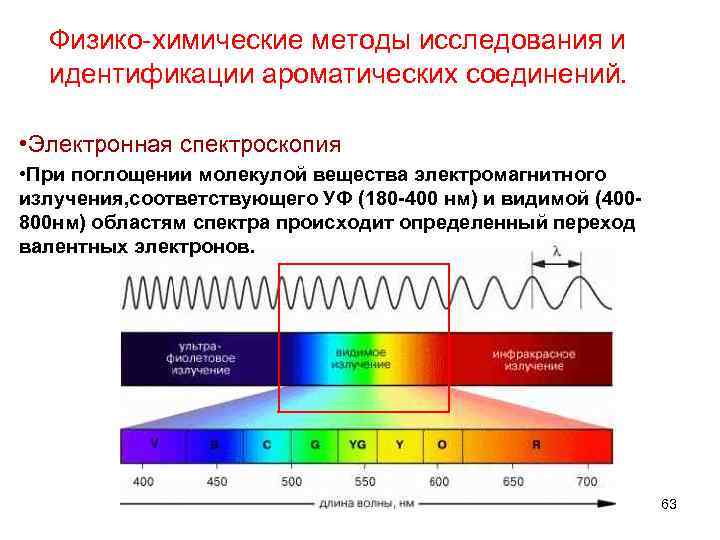
Физико-химические методы исследования и идентификации ароматических соединений. • Электронная спектроскопия • При поглощении молекулой вещества электромагнитного излучения, соответствующего УФ (180 -400 нм) и видимой (400800 нм) областям спектра происходит определенный переход валентных электронов. 63
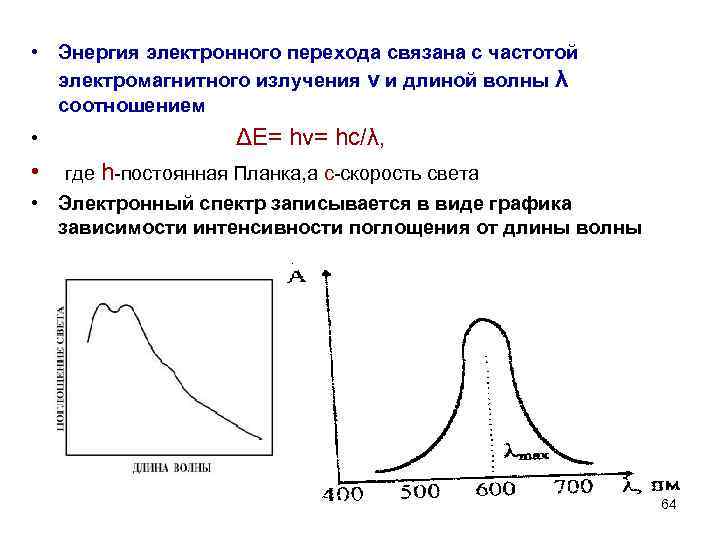
• Энергия электронного перехода связана с частотой электромагнитного излучения ν и длиной волны λ соотношением • ΔЕ= hν= hc/λ, • где h-постоянная Планка, а с-скорость света • Электронный спектр записывается в виде графика зависимости интенсивности поглощения от длины волны 64
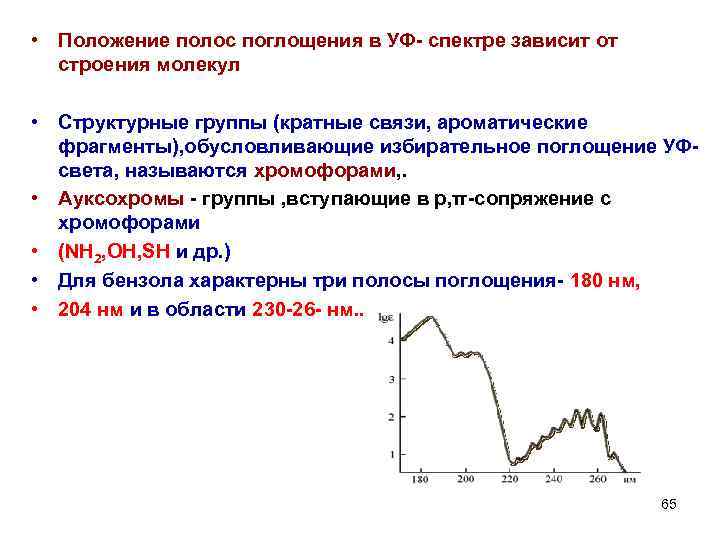
• Положение полос поглощения в УФ- спектре зависит от строения молекул • Структурные группы (кратные связи, ароматические фрагменты), обусловливающие избирательное поглощение УФсвета, называются хромофорами, . • Ауксохромы - группы , вступающие в р, π-сопряжение с хромофорами • (NH 2, OH, SH и др. ) • Для бензола характерны три полосы поглощения- 180 нм, • 204 нм и в области 230 -26 - нм. . 65
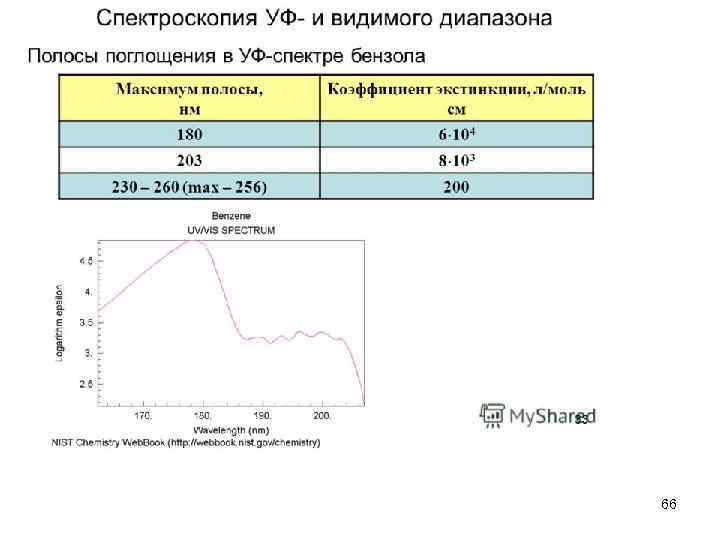
66
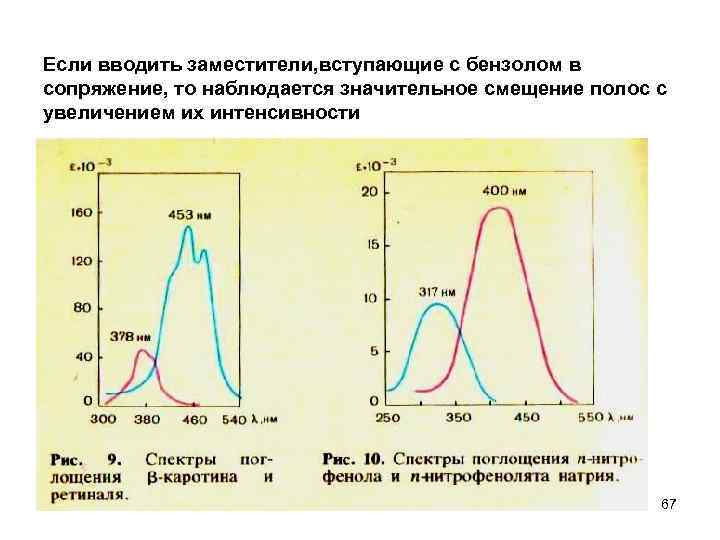
Если вводить заместители, вступающие с бензолом в сопряжение, то наблюдается значительное смещение полос с увеличением их интенсивности 67

• Применение метода электронной спектроскопии • Идентификация органических соединений-сравнение спектра исследуемого соединения со спектрами соединений известной структуры. • Изучение кинетики и контроль за ходом реакции. • Изучение пространственного строения. • Количественный анализ содержания действующих компонентов в составе лекарственной формы 68

Инфракрасная спектроскопия • ИК-спектроскопия является распространенным спектральным методом. • В этом виде спектроскопии установлены четкие эмпирические закономерности, связывающие структуру вещества с параметрами спектра. • Применение ИК-спектроскопии: • Идентификация и установление строения вещества. • Анализ смесей. • Кинетический контроль за ходом реакции. • Изучение внутри- и межмолекулярных взаимодействий. 69

• ИК-спектр возникает при поглощении веществом электромагнитного излучения с длиной волны от 2, 5 до 25 мкм (4000 -400 см-1 70

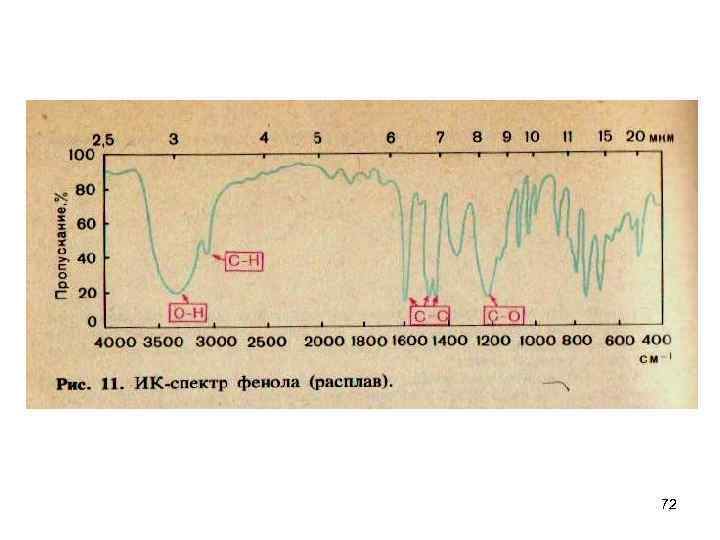
• . Поглощенная веществом энергия преобразуется главным образом в энергию колебания атомов, и молекула переходит в возбужденное колебательное состояние. • Молекула поглощает ИК-излучение с такими частотами, с какими колеблются отдельные связи в молекуле. • Некоторые группы атомов поглощают частоты в узком интервале частот независимо от строения остальной части молекулы. Это-характеристические частоты и группы. • CH, CH 2, CH 3, OH, NH 2, SH, и группы с кратной связью: CO, SO 2, NO, CN и др. • Они собраны в таблицы и используются при интерпретации ИК-спектров. • Интенсивность полос оценивается только качественно (сильная, средняя, слабая, переменная. ) 71
72
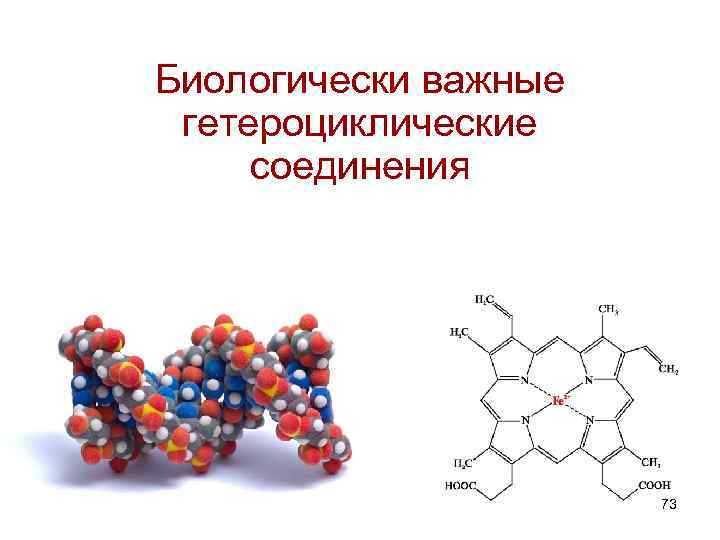
Биологически важные гетероциклические соединения 73
БИОЛОГИЧЕСКИ ВАЖНЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ Гетероциклическими называются циклические органические соединения, в состав цикла которых, помимо атомов углерода, входят один или несколько атомов других элементов (гетероатомов). 74
Гетероциклические соединения Пятичленные гетероциклы Шестичленные гетероциклы (π-избыточные) (π-недостаточные) ь С одним гетероатомом ь - С двумя гетероатомами 75
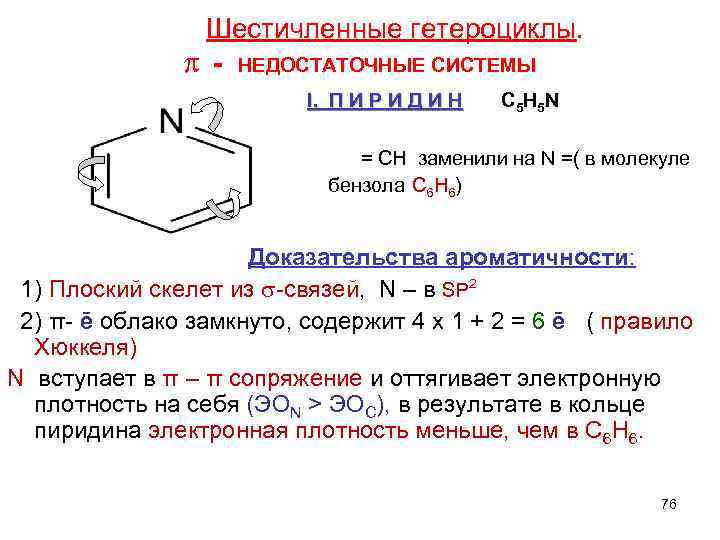
Шестичленные гетероциклы. π - НЕДОСТАТОЧНЫЕ СИСТЕМЫ . П И Р И Д И Н C 5 H 5 N I. П И Р И Д И Н = СН заменили на N =( в молекуле бензола С 6 Н 6) Доказательства ароматичности: 1) Плоский скелет из -связей, N – в SP 2 2) π- ē облако замкнуто, содержит 4 х 1 + 2 = 6 ē ( правило Хюккеля) N вступает в π – π сопряжение и оттягивает электронную плотность на себя (ЭОN > ЭОC), в результате в кольце пиридина электронная плотность меньше, чем в С 6 Н 6. 76
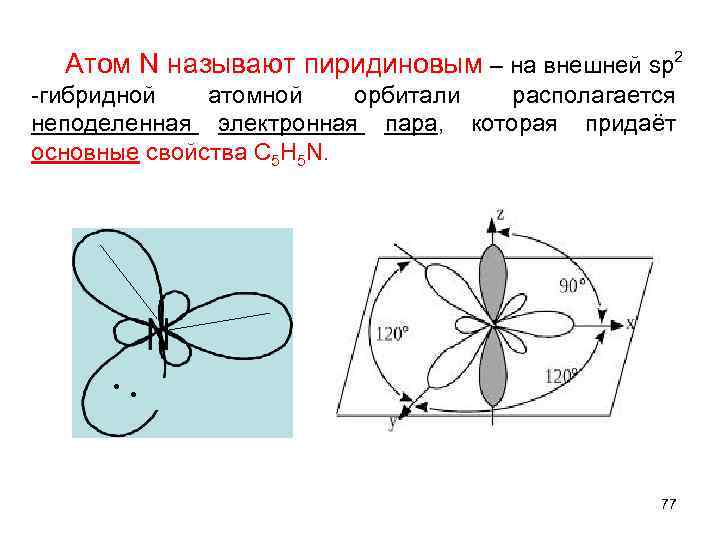
Атом N называют пиридиновым – на внешней sp 2 -гибридной атомной орбитали располагается неподеленная электронная пара, которая придаёт основные свойства С 5 Н 5 N. • • 77
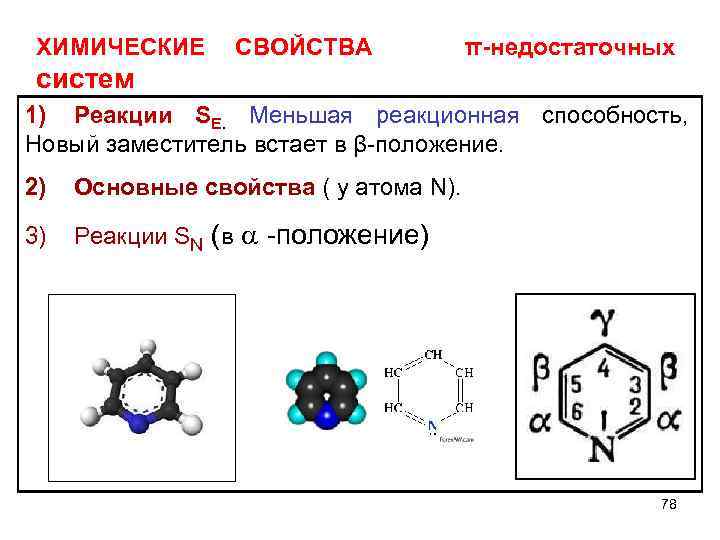
ХИМИЧЕСКИЕ СВОЙСТВА π-недостаточных систем 1) Реакции SЕ. Меньшая реакционная способность, Новый заместитель встает в β-положение. 2) Основные свойства ( у атома N). 3) Реакции SN (в -положение) 78
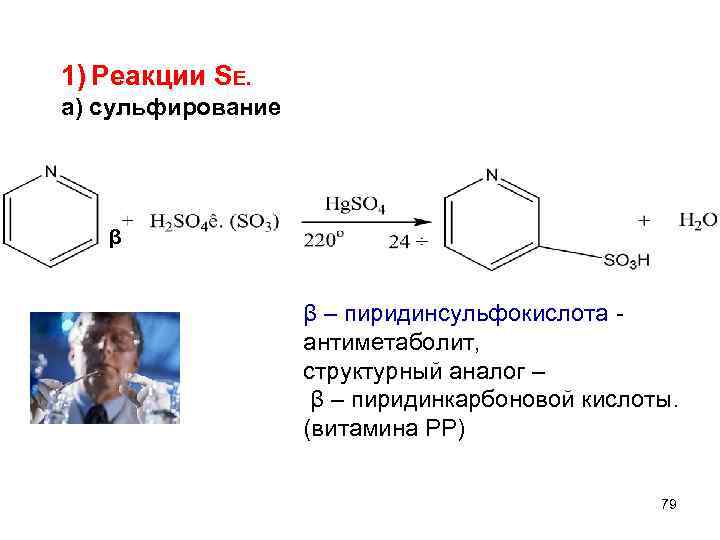
1) Реакции SЕ. а) сульфирование β β – пиридинсульфокислота антиметаболит, структурный аналог – β – пиридинкарбоновой кислоты. (витамина РР) 79
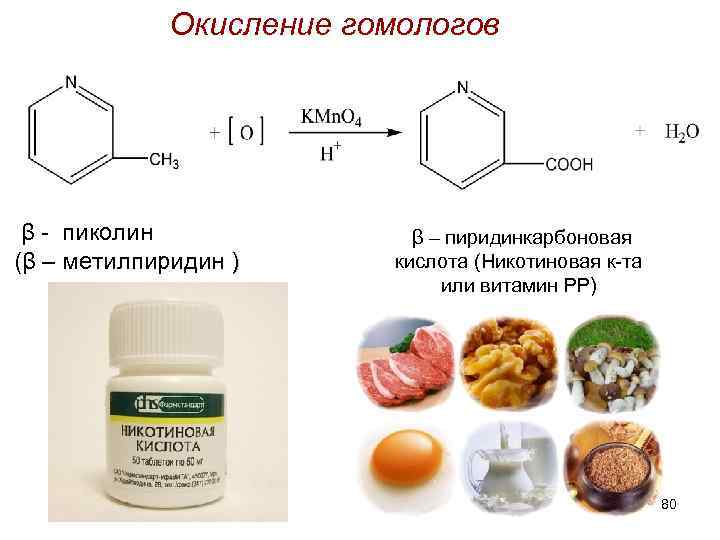
Окисление гомологов β - пиколин (β – метилпиридин ) β – пиридинкарбоновая кислота (Никотиновая к-та или витамин РР) 80
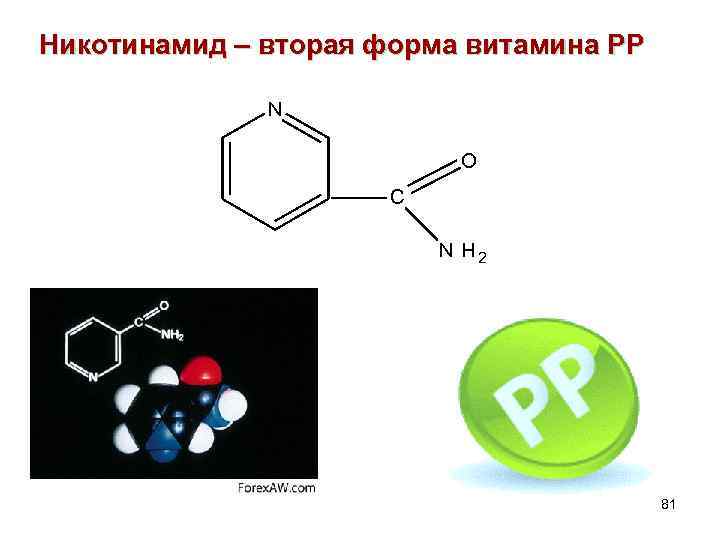
Никотинамид – вторая форма витамина PP N O C NH 2 81

• В организме свободная никотиновая кислота быстро превращается в амид никотиновой кислоты. • Избыток никотиновой кислоты и её амида выводится из организма с мочой в виде, главным образом, N- метилникотинамида и частично некоторых других их производных. CONH 2 N+ CH 3 N- метилникотинамид 82
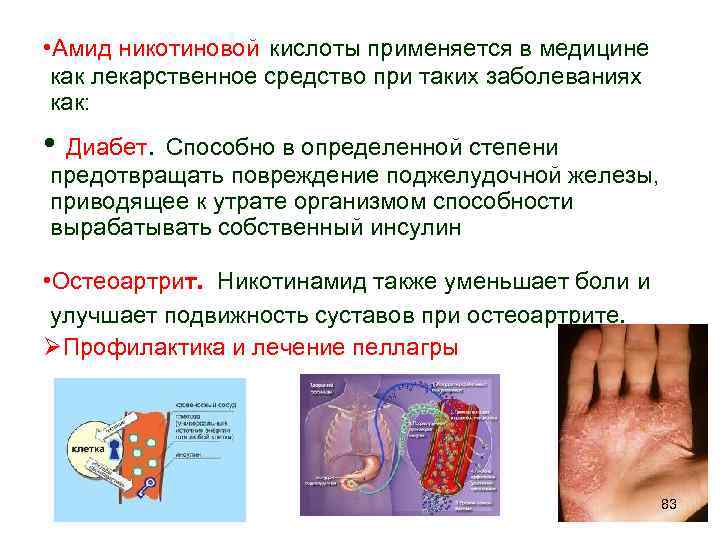
• Амид никотиновой кислоты применяется в медицине как лекарственное средство при таких заболеваниях как: • Диабет. Способно в определенной степени предотвращать повреждение поджелудочной железы, приводящее к утрате организмом способности вырабатывать собственный инсулин • Остеоартрит. Никотинамид также уменьшает боли и улучшает подвижность суставов при остеоартрите. ØПрофилактика и лечение пеллагры 83
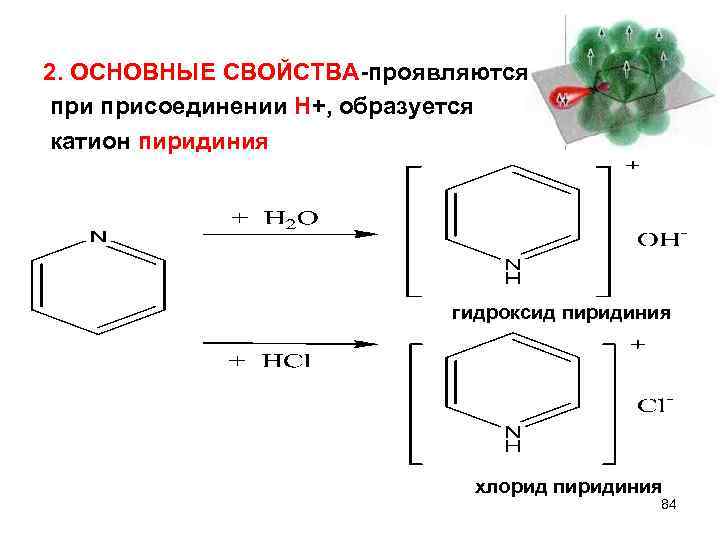
2. ОСНОВНЫЕ СВОЙСТВА-проявляются присоединении Н+, образуется катион пиридиния гидроксид пиридиния хлорид пиридиния 84
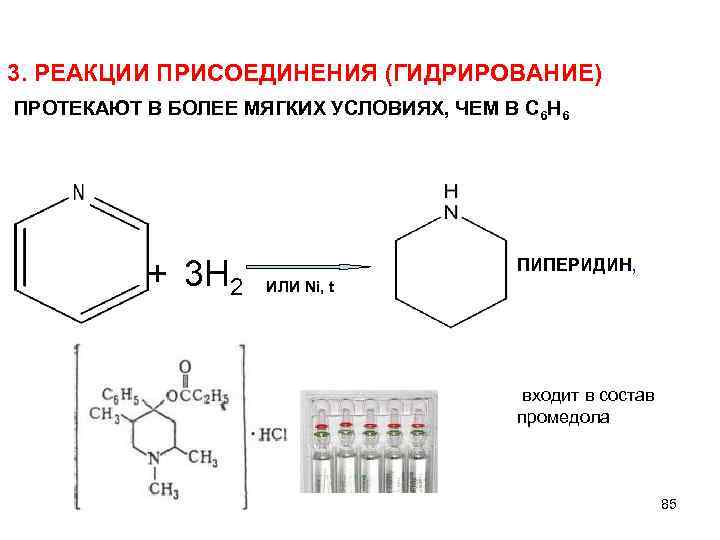
3. РЕАКЦИИ ПРИСОЕДИНЕНИЯ (ГИДРИРОВАНИЕ) ПРОТЕКАЮТ В БОЛЕЕ МЯГКИХ УСЛОВИЯХ, ЧЕМ В С 6 Н 6 Na + C 2 H 5 OH + 3 Н 2 ИЛИ Ni, t ПИПЕРИДИН, входит в состав промедола 85

пиперидин ь Встречается во многих алкалоидах: никотин, кониин ь Алкалоиды – гетероциклические азотсодержащие основания растительного происхождения, обладающие выраженным физиологическим действием 86

Кониин-производное пиперидина яд, выделенный из болиголова: этим веществом был отравлен Сократ 87
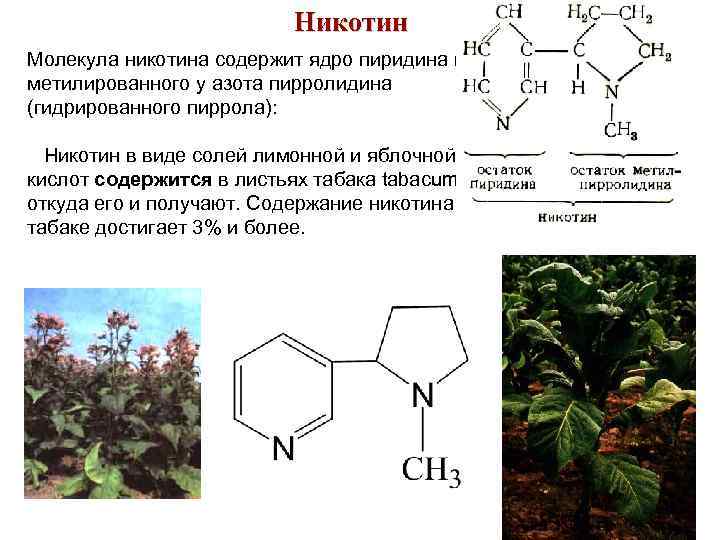
Никотин Молекула никотина содержит ядро пиридина и метилированного у азота пирролидина (гидрированного пиррола): Никотин в виде солей лимонной и яблочной кислот содержится в листьях табака tabacum, откуда его и получают. Содержание никотина в табаке достигает 3% и более. 88
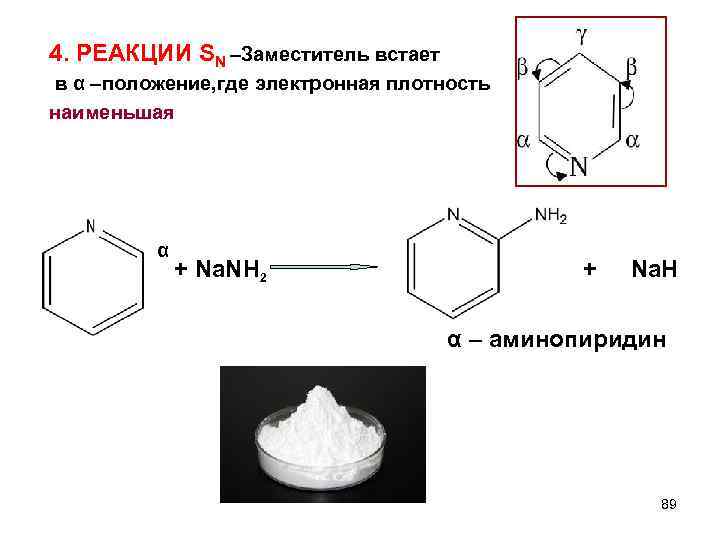
4. РЕАКЦИИ SN –Заместитель встает в α –положение, где электронная плотность наименьшая α + Na. NH 2 + Na. H α – аминопиридин 89
МЕДИКО-БИОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ ь ь ВДЫХАНИЕ ПАРОВ ПИРИДИНА МОЖЕТ ПРИВЕСТИ К ТЯЖЕЛОМУ ПОРАЖЕНИЮ НЕРВНОЙ СИСТЕМЫ ГОМОЛОГ ПИРИДИНА β – ПИКОЛИН ПРЕВРАЩАЕТСЯ В НИКОТИНОВУЮ КИСЛОТУ, НИКОТИНАМИД, КОТОРЫЕ ИЗВЕСТНЫ КАК ДВЕ ФОРМЫ ВИТАМИНА РР, ДИЭТИЛАМИД НИКОТИНОВОЙ КИСЛОТЫ – КОРДИАМИН – ЭФФЕКТИВНЫЙ СТИМУЛЯТОР ЦНС ПИПЕРИДИН ВХОДИТ В СОСТАВ ПРОМЕДОЛА, ВСТРЕЧАЕТСЯ ВО МНОГИХ алкалоидах. 90
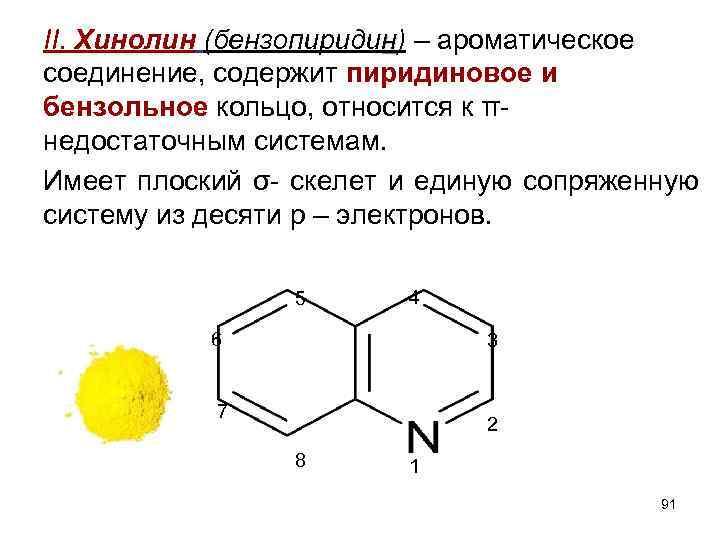
II. Хинолин (бензопиридин) – ароматическое соединение, содержит пиридиновое и бензольное кольцо, относится к πнедостаточным системам. Имеет плоский σ- скелет и единую сопряженную систему из десяти p – электронов. 5 4 6 3 7 2 8 1 91

ОСОБЕННОСТИ ХИМИЧЕСКОГО ПОВЕДЕНИЯ ХИНОЛИНА 1) В реакциях SE атаке подвергается бензольное кольцо (кольцо пиридина является π – недостаточным). Замещение протекает в положении 5 или 8. 2) В реакции SN может вступать только π – недостаточное пиридиновое кольцо (положения 2 и пиридиновое 4). 92
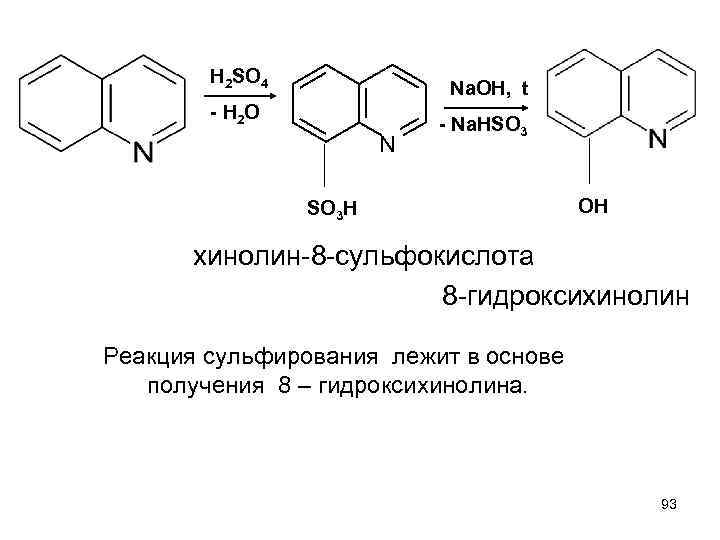
H 2 SO 4 Na. OH, t - H 2 O N - Na. HSO 3 SO 3 H OH хинолин-8 -сульфокислота 8 -гидроксихинолин Реакция сульфирования лежит в основе получения 8 – гидроксихинолина. 93
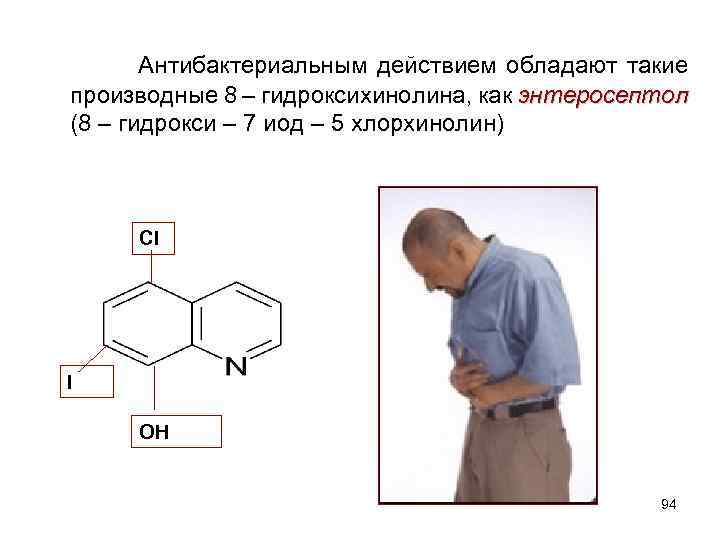
Антибактериальным действием обладают такие производные 8 – гидроксихинолина, как энтеросептол (8 – гидрокси – 7 иод – 5 хлорхинолин) Cl I OH 94
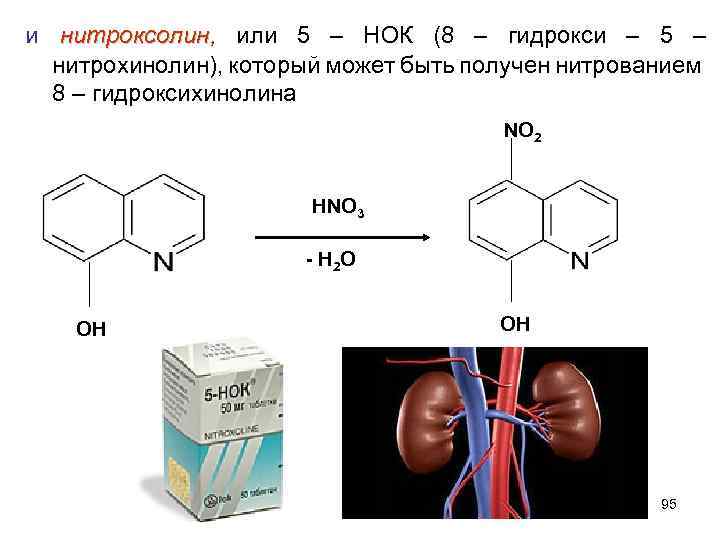
и нитроксолин, или 5 – НОК (8 – гидрокси – 5 – нитроксолин нитрохинолин), который может быть получен нитрованием 8 – гидроксихинолина NO 2 HNO 3 - H 2 O OH OH 95
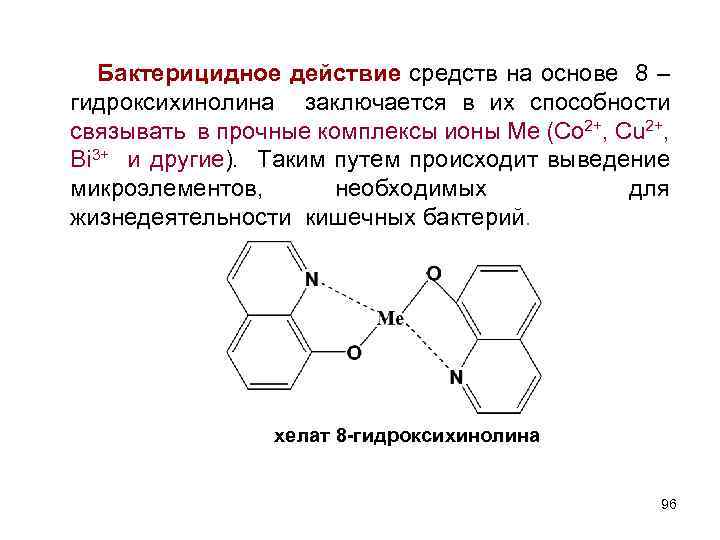
Бактерицидное действие средств на основе 8 – гидроксихинолина заключается в их способности связывать в прочные комплексы ионы Ме (Со 2+, Сu 2+, Bi 3+ и другие). Таким путем происходит выведение микроэлементов, необходимых для жизнедеятельности кишечных бактерий. хелат 8 -гидроксихинолина 96
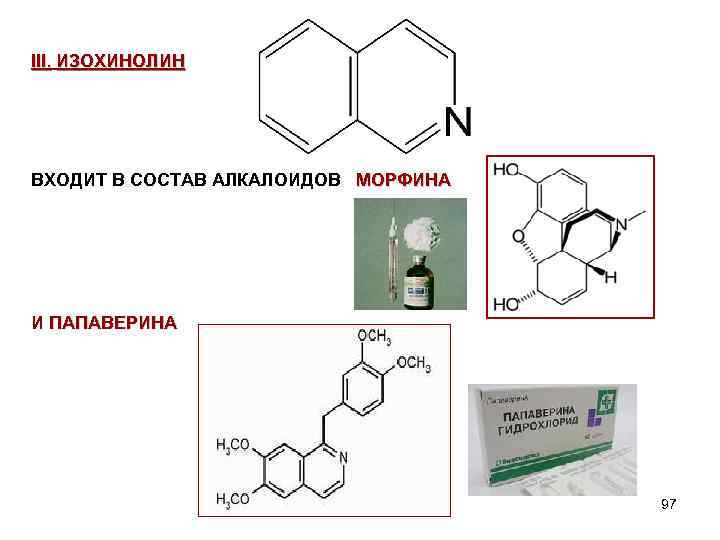
III. ИЗОХИНОЛИН ВХОДИТ В СОСТАВ АЛКАЛОИДОВ МОРФИНА И ПАПАВЕРИНА 97
Применяют морфин как болеутоляющее средство при травмах и сопровождающихся ощущениями. различных сильными заболеваниях, болевыми 98
А так же при подготовке к операции, при бессоннице, иногда при сильном кашле. 99
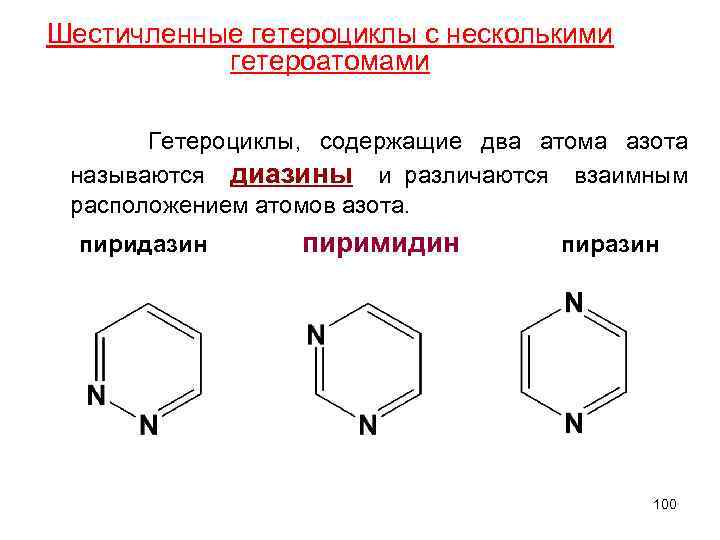
Шестичленные гетероциклы с несколькими гетероатомами Гетероциклы, содержащие два атома азота называются диазины и различаются взаимным расположением атомов азота. пиридазин пиримидин пиразин 100
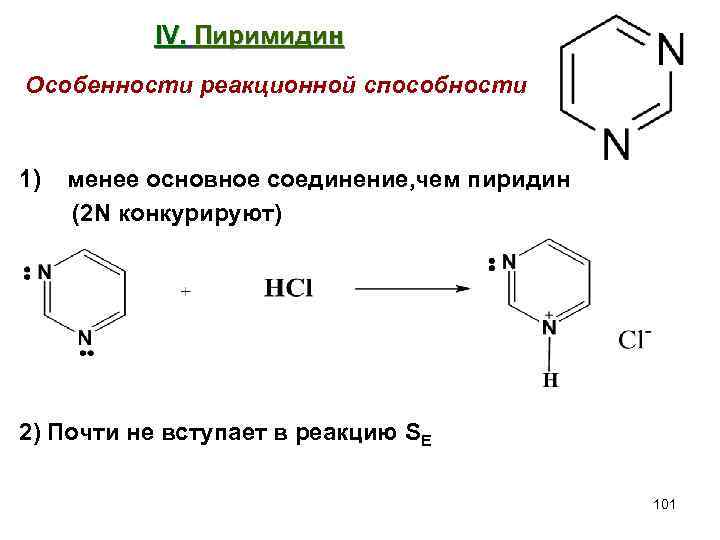
IV. Пиримидин Особенности реакционной способности 1) менее основное соединение, чем пиридин (2 N конкурируют) 2) Почти не вступает в реакцию SE 101
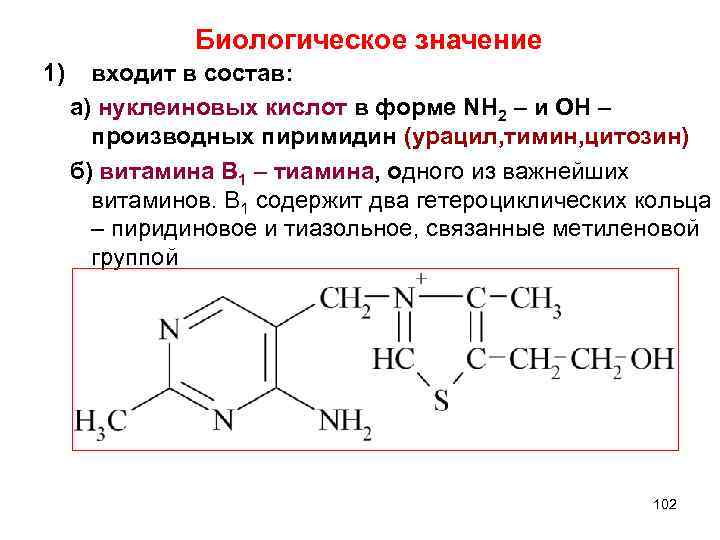
Биологическое значение 1) входит в состав: а) нуклеиновых кислот в форме NH 2 – и ОН – производных пиримидин (урацил, тимин, цитозин) б) витамина В 1 – тиамина, одного из важнейших витаминов. В 1 содержит два гетероциклических кольца – пиридиновое и тиазольное, связанные метиленовой группой 102
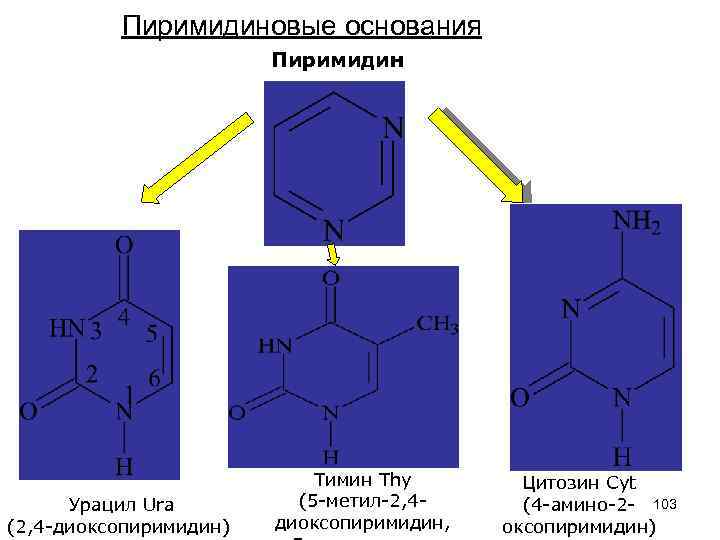
Пиримидиновые основания Пиримидин Урацил Ura (2, 4 -диоксопиримидин) Тимин Thy (5 -метил-2, 4 диоксопиримидин, Цитозин Cyt (4 -амино-2 - 103 оксопиримидин)
Свойства тиамина • Играет важную роль в метаболизме углеводов и жиров. • Незаменим для утилизации глюкозы Поддерживает работу сердца, нервной и пищеварительной систем. • Недостаток витамина в пище приводит к тяжелому заболеванию «бери-бери» 104

Источники витамина тиамина 0, 96 мкг 0, 48 мкг 0, 72 мкг 0, 51 мкг 105
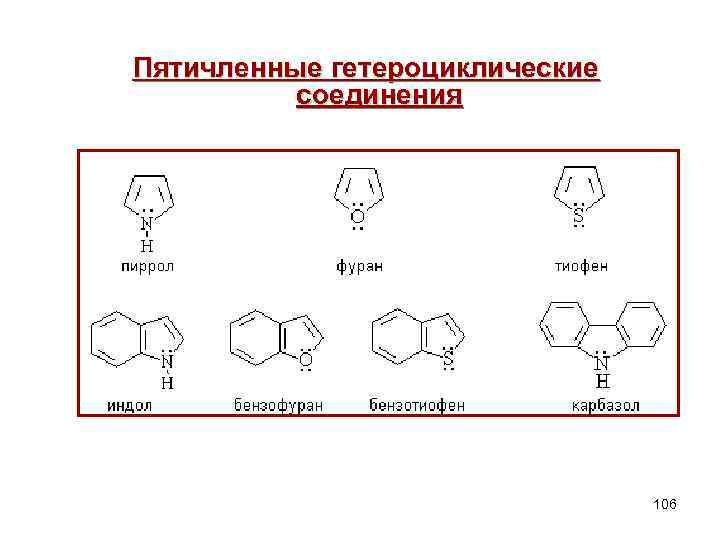
Пятичленные гетероциклические соединения 106
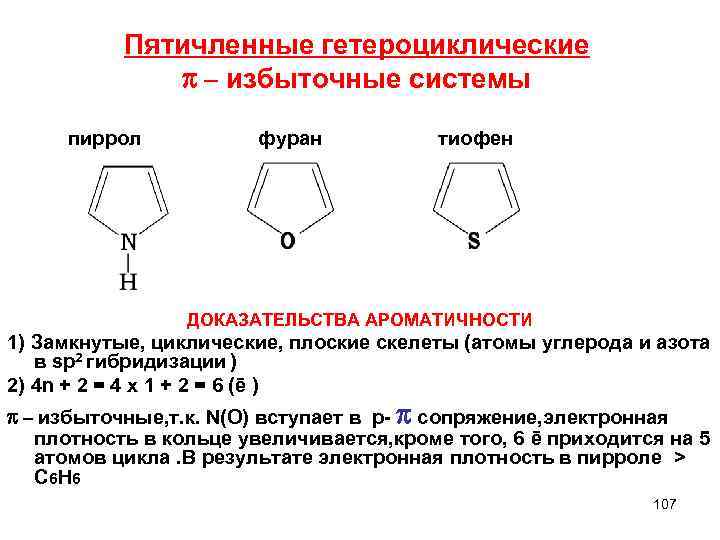
Пятичленные гетероциклические π – избыточные системы пиррол фуран тиофен ДОКАЗАТЕЛЬСТВА АРОМАТИЧНОСТИ 1) Замкнутые, циклические, плоские скелеты (атомы углерода и азота в sp 2 гибридизации ) 2) 4 n + 2 = 4 х 1 + 2 = 6 (ē ) π – избыточные, т. к. N(O) вступает в р- π сопряжение, электронная плотность в кольце увеличивается, кроме того, 6 ē приходится на 5 атомов цикла. В результате электронная плотность в пирроле > C 6 H 6 107
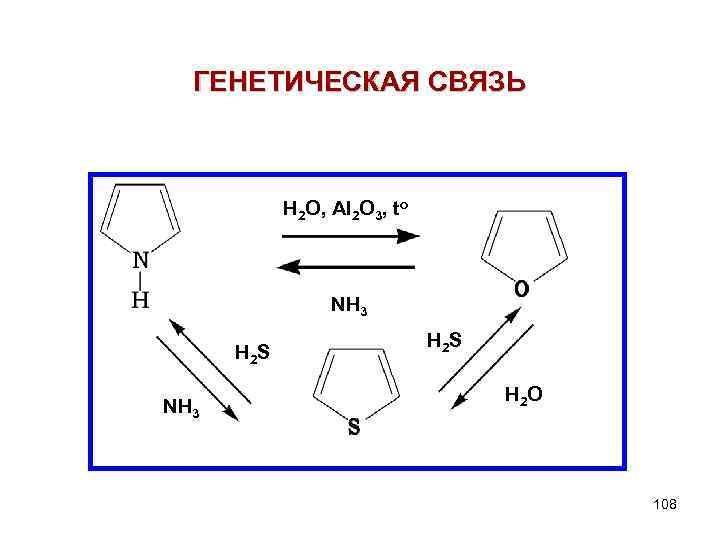
ГЕНЕТИЧЕСКАЯ СВЯЗЬ H 2 O, Al 2 O 3, to NH 3 H 2 S H 2 O 108
I. ФУРАН 109
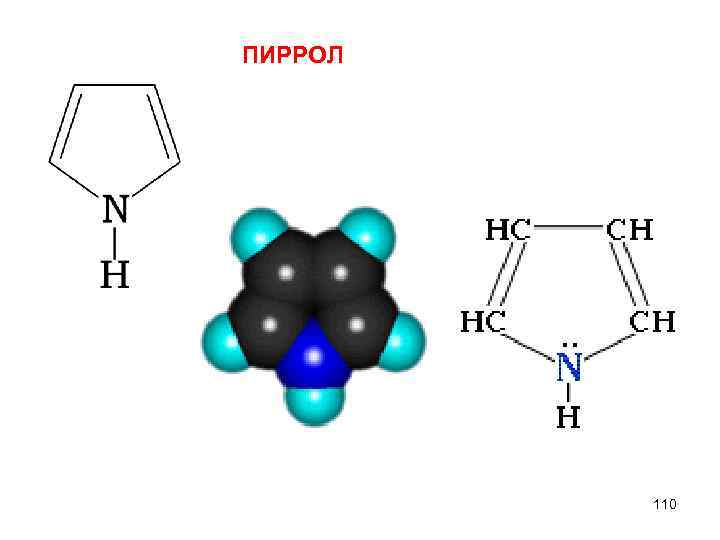
ПИРРОЛ 110
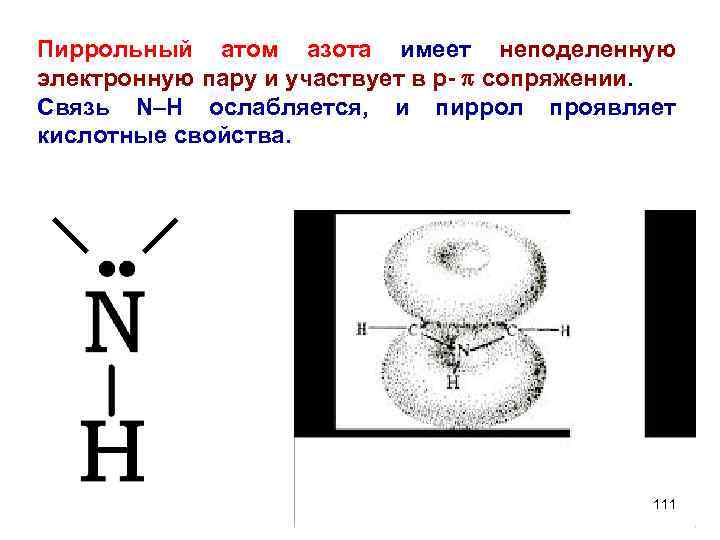
Пиррольный атом азота имеет неподеленную электронную пару и участвует в р- p сопряжении. Связь N–Н ослабляется, и пиррол проявляет кислотные свойства. 111

ХИМИЧЕСКИЕ СВОЙСТВА π-избыточных систем 1) Реакции SЕ. Большая реакционная способность, чем у С 6 Н 6, заместитель встает в α –положение, где сосредоточена большая электронная плотность а) алкилирование б) галогенирование в) ацилирование г) сульфирование д) нитрование 2) Слабокислые свойства-образование солей. 112
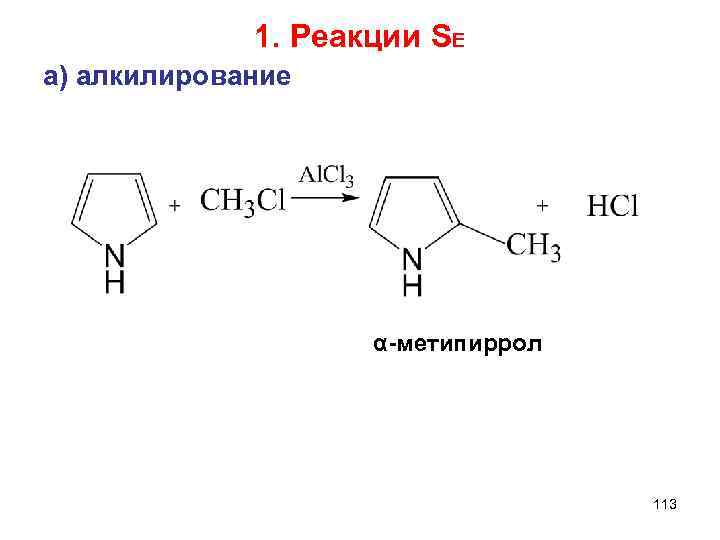
1. Реакции SE а) алкилирование α-метипиррол 113
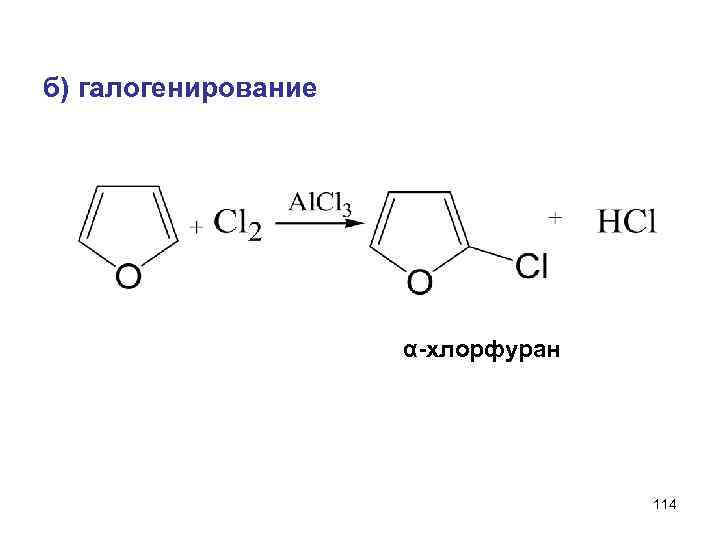
б) галогенирование α-хлорфуран 114

Пиррол и фуран обладают свойствами ацидофобности (т. е. разрушаются в кислой среде. Реагент не должен содержать Н+ ) Тиофен – более ароматичен, не боится кислоты. 115
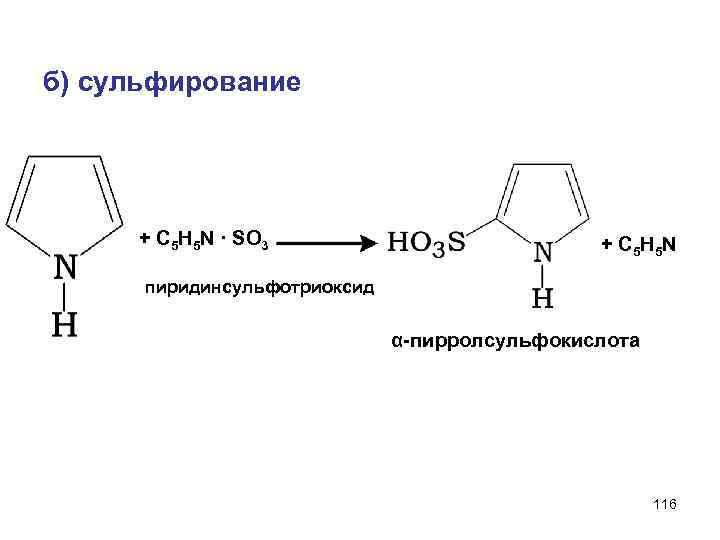
б) сульфирование + С 5 Н 5 N · SO 3 + С 5 H 5 N пиридинсульфотриоксид α-пирролсульфокислота 116
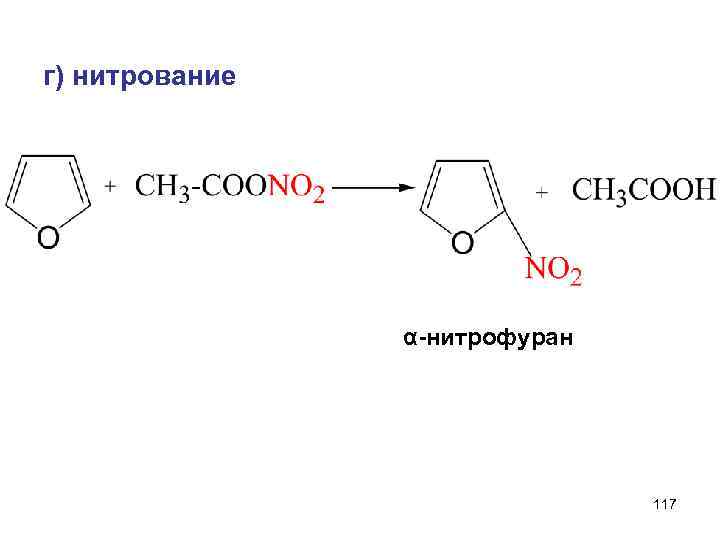
г) нитрование α-нитрофуран 117
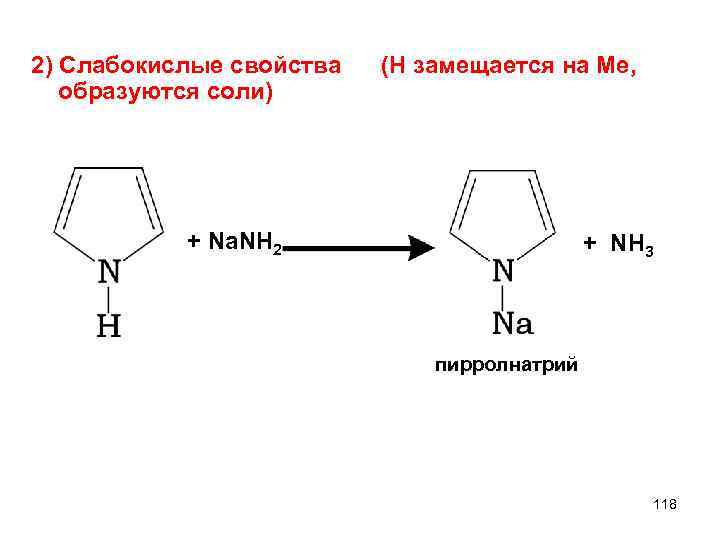
2) Слабокислые свойства (Н замещается на Ме, образуются соли) + Na. NH 2 + NH 3 пирролнатрий 118
![3) восстановление пиррола: 4[H] пирролидин Входит в состав лекарственных средств, некоторых алкалоидов, α-аминокислоты пролина. 3) восстановление пиррола: 4[H] пирролидин Входит в состав лекарственных средств, некоторых алкалоидов, α-аминокислоты пролина.](https://present5.com/presentation/321218603_437090666/image-119.jpg)
3) восстановление пиррола: 4[H] пирролидин Входит в состав лекарственных средств, некоторых алкалоидов, α-аминокислоты пролина. 119
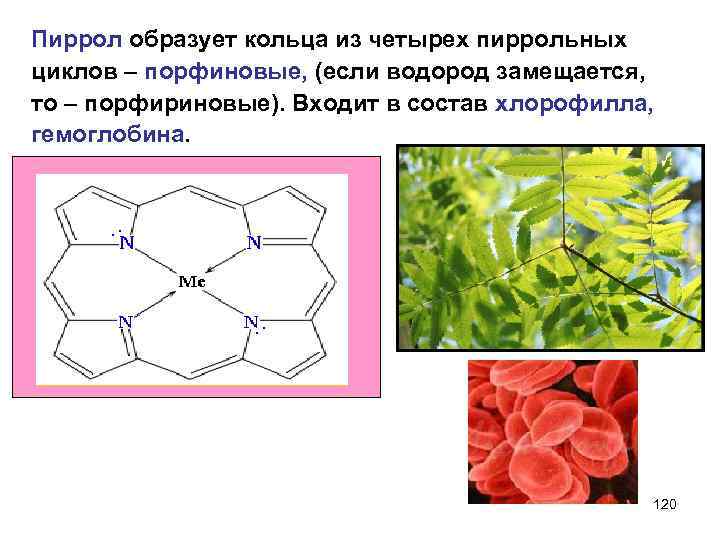
Пиррол образует кольца из четырех пиррольных циклов – порфиновые, (если водород замещается, то – порфириновые). Входит в состав хлорофилла, гемоглобина. 120
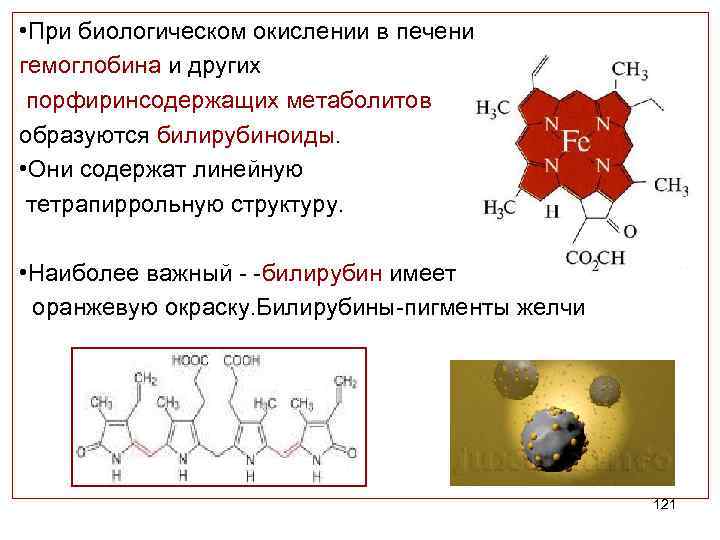
• При биологическом окислении в печени гемоглобина и других порфиринсодержащих метаболитов образуются билирубиноиды. • Они содержат линейную тетрапиррольную структуру. • Наиболее важный - -билирубин имеет оранжевую окраску. Билирубины-пигменты желчи 121
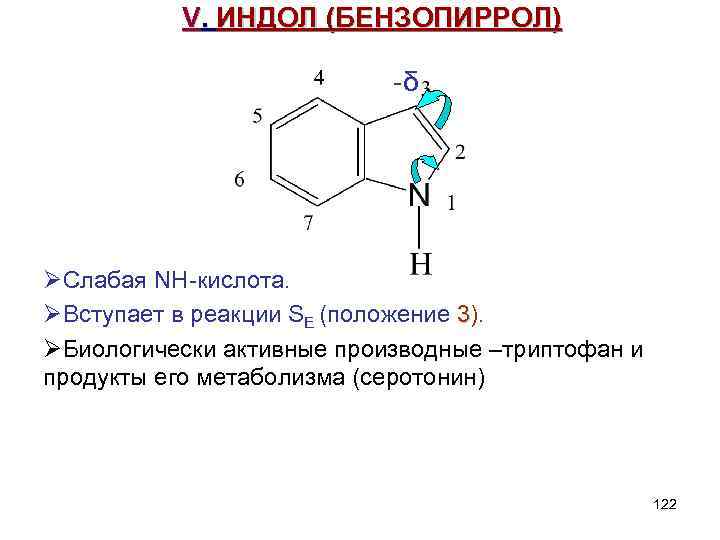
V. ИНДОЛ (БЕНЗОПИРРОЛ) -δ ØСлабая NH-кислота. ØВступает в реакции SE (положение 3). ØБиологически активные производные –триптофан и продукты его метаболизма (серотонин) 122

БИОЛОГИЧЕСКИ АКТИВНЫЕ ПРОИЗВОДНЫЕ ИНДОЛА Триптофан – α-амино-β-(β‘-индолил) пропионовая кислота. Входит в состав полипептидов растительных и животных организмов. Участвует в реакции гидроксилирования (получение 5 гидрокситриптофана, который подвергается декарбоксилированию с образованием 5 -гидрокситриптамина(серотонина). Серотонин является одним из нейромедиаторов головного мозга. Нарушение его нормального обмена ведет к шизофрении. Гормон удовольствия. 123
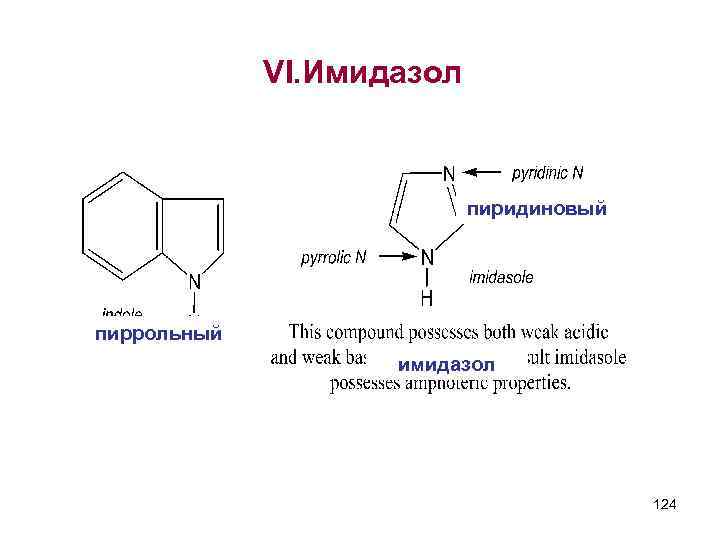
VI. Имидазол пиридиновый пиррольный имидазол 124

Имидазол-амфотерное соединение 1. Проявляет слабокислотные свойства за счет пиррольного N 2. Слабоосновные – за счет пиридинового N ь образует соли с сильными кислотами и щелочными металлами ь NH кислотная группа и –N= основная образуют межмолекулярные водородные связи 125

Биологически активные производные имидазола Гистидин - α-амино-β-(4(5)‘-имидазолиллил) пропионовая кислота. Входит в состав многих белков-глобина Участвует в ферментативных реакциях (кислотный и основной катализ) Гистамин – биогенный амин, продукт декарбоксилирования гистидина, имеет отношение к аллергическим реакциям организма 126
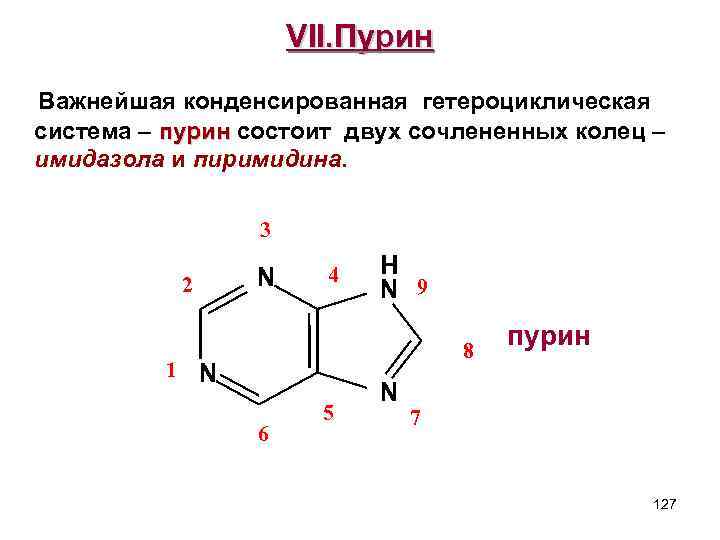
VII. Пурин Важнейшая конденсированная гетероциклическая система – пурин состоит двух сочлененных колец – пурин имидaзола и пиримидина. 3 H 2 N 9 N 4 пурин 8 1 N 6 5 N 7 127

Свойства пурина 1) Устойчив к действию окислителей 2) Хорошо растворяется в воде 3) Амфотерен, образует соли не только с сильными кислотами, но (благодаря наличию NH – группы) и со щелочными Ме. !Наиболее важны гидрокси – и аминопурины, принимающие активное участие в процессах жизнедеятельности. 128
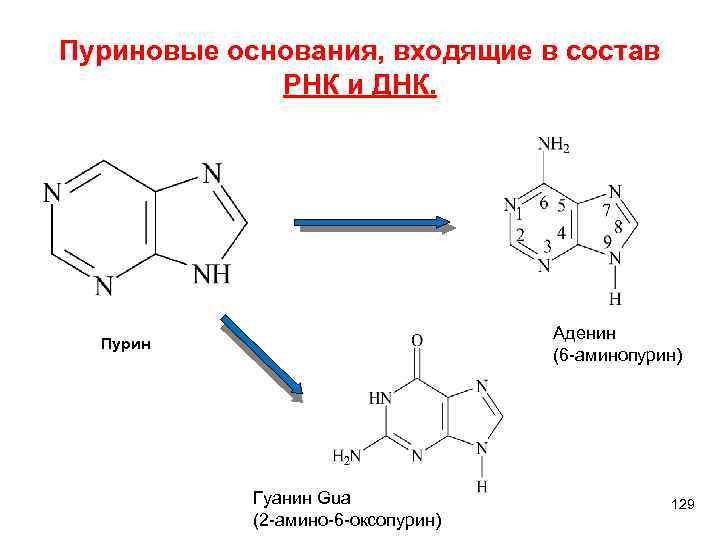
Пуриновые основания, входящие в состав РНК и ДНК. Аденин (6 -аминопурин) Пурин Гуанин Gua (2 -амино-6 -оксопурин) 129
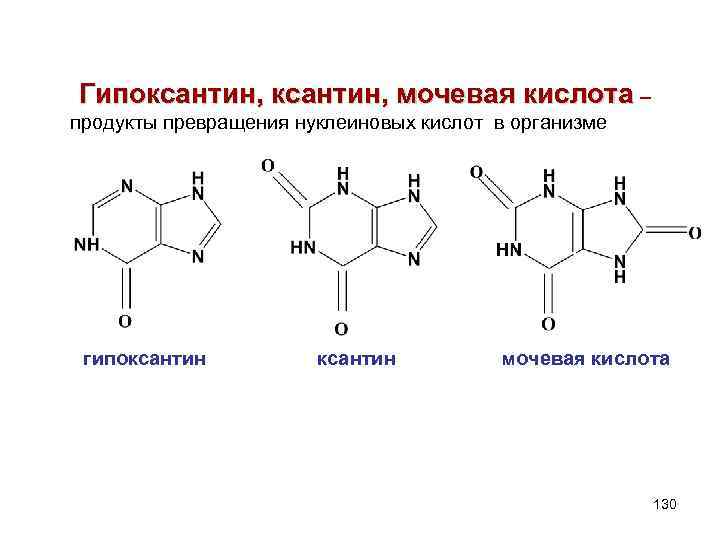
Гипоксантин, мочевая кислота – продукты превращения нуклеиновых кислот в организме гипоксантин мочевая кислота 130

К пуриновым алкалоидам относятся: теобромин кофеин теофиллин (какао) (чай, кофе) (чай) Эти алкалоиды оказывают возбуждающее действие на центральную нервную систему. 131

СПАСИБО ЗА ВНИМАНИЕ! 132
lect_org_1.ppt