Кафедра общей и медицинской химии «Гидролиз»


Кафедра общей и медицинской химии "Гидролиз" 1
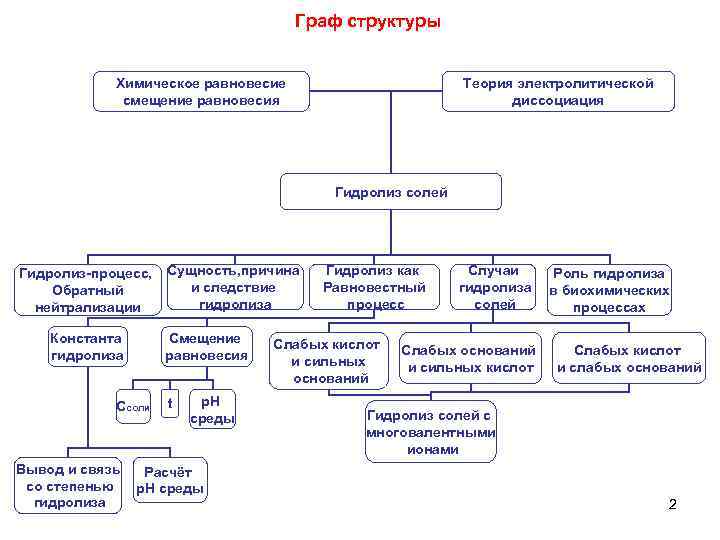
Граф структуры Химическое равновесие Теория электролитической смещение равновесия диссоциация Гидролиз солей Гидролиз-процесс, Сущность, причина Гидролиз как Случаи Роль гидролиза Обратный и следствие Равновестный гидролиза в биохимических нейтрализации гидролиза процесс солей процессах Константа Смещение Слабых кислот гидролиза равновесия Слабых оснований Слабых кислот и сильных кислот и слабых оснований оснований Ссоли t р. Н среды Гидролиз солей с многовалентными ионами Вывод и связь Расчёт со степенью р. Н среды гидролиза 2

В общем случае к гидролизу относятся процессы взаимодействия частей вещества с ионами Н+ и ОН– воды. 3

р. Н слезы 7. 6 - 7. 8 Na. Cl - ? ? ? 4

Гидролиз солей - процесс взаимодействия ионов соли с составными частями воды (Н+ и ОН–). Причина-образование малодиссоциированных соединений (слабых электролитов) Следствие – сдвиг равновесия диссоциации (ионизации) воды, который сопровождается изменением кислотности среды вследствие накопления Н+ или ОН– ионов. 5

Гидролиз – процесс: üобратимый ( ↔ ) üступенчатый üэндотермический (-Q), так как обратен реакции нейтрализации. Гидролиз идет по слабому компоненту соли! Кислотность определяет сильный компонент! Количественно гидролиз характеризуется константой гидролиза Кг и степенью гидролиза h. 6

Варианты гидролиза: 1. Соль образована одноосновной слабой кислотой и однокислотным сильным основанием ( Na С N, CH 3 COONa, Na. NO 2…) – среда щелочная Константа гидролиза Кг Так как [H 2 O] практически постоянна, 7

Связь Кг с ионным произведением воды и Кд Домножим числитель и знаменатель на [H+]: Значение Кг показывает, что в момент равновесия произведение концентраций исходных веществ примерно в миллиард раз больше, чем продуктов реакции, что говорит об относительно небольшой степени протекания гидролиза. 8
![Вывод степени гидролиза h [OH-]=[CH 3 COOH] Приравнивая формулы (1) и Вывод степени гидролиза h [OH-]=[CH 3 COOH] Приравнивая формулы (1) и](https://present5.com/presentation/3/-119053949_440680904.pdf-img/-119053949_440680904.pdf-9.jpg)
Вывод степени гидролиза h [OH-]=[CH 3 COOH] Приравнивая формулы (1) и (2), получим: 9
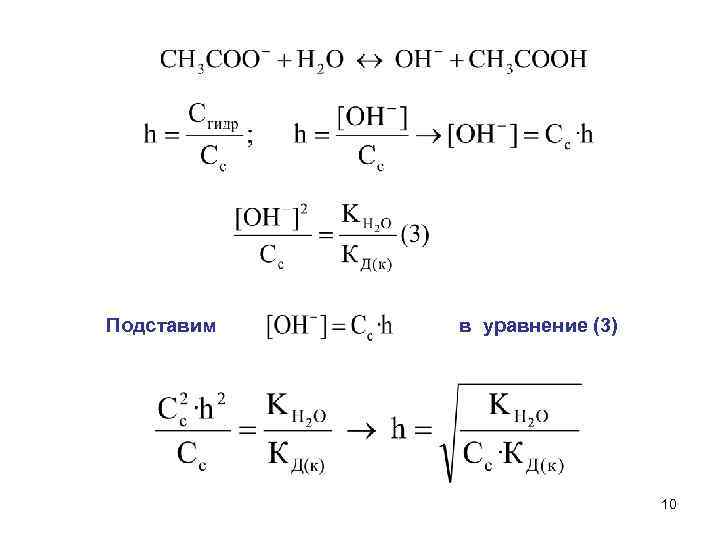
Подставим в уравнение (3) 10

Вывод формулы для расчёта p. H CH 3 COONa ( р. Н>7 ) 11
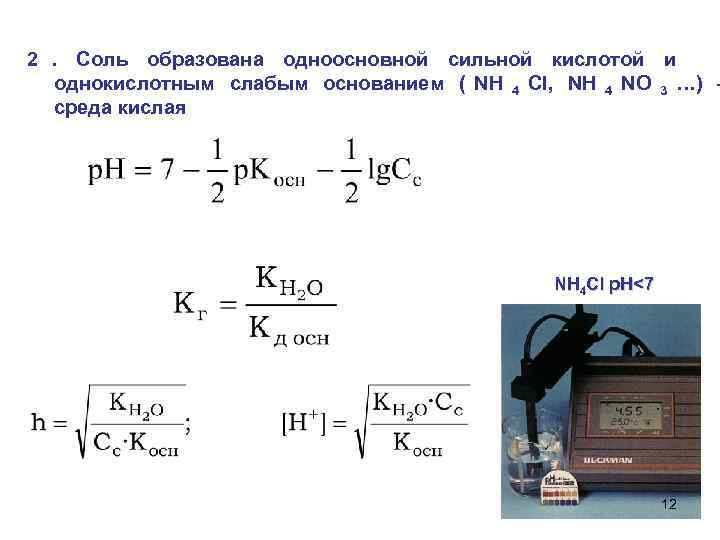
2. Соль образована одноосновной сильной кислотой и однокислотным слабым основанием ( NH 4 Cl, NH 4 NO 3 …) – среда кислая NH 4 Cl р. Н<7 12

3. Соль образована слабым однокислотным основанием и слабой одноосновной кислотой ( NH 4 CN, CH 3 COONH 4 …) среда ≈ нейтральная р. Н не зависит от концентрации соли, гидролиз проходит достаточно глубоко CH 3 COONН 4+ ( р. Н ≈ 7 ) 13

Гидролиз кислых солей Параллельно с гидролизом в растворах кислых солей протекает диссоциация кислотного остатка, поэтому при оценке значения р. Н необходимо сравнить константы гидролиза (Кг) и диссоциации кислоты по второй ступени (К 2): В данном случае намного меньше, чем следовательно, среда будет слабокислой. 14

Растворы кислых солей имеют различный характер среды: Na 2 HPO 4 - щелочная Na. H 2 PO 4 – кислая Раствор питьевой соды Na. HCO 3 имеет слабощелочную среду и используется в медицине для предотвращения ацидозов Расчет степени гидролиза концентрации ионов водорода и р. Н среды для кислых солей 15

Ступенчатый гидролиз В случае солей многоосновных кислот или многокислотных оснований процесс гидролиза протекает ступенчато 1 - я ступень: 2 -я ступень: Сравнение величин Кг 1 и Кг 2 показывает, что практически гидролиз протекает только по первой ступени. Cмещением равновесия вправо ( нагреванием и разбавлением раствора – согласно принципу Ле-Шателье) можно добиться в ряде 16 случаев реализации гидролиза по второй и даже по третьей ступени.

Смещение равновесия обратимого гидролиза 17

1. Влияние температуры: Так как реакция нейтрализации экзотермична (ΔHo = -56, 5 к. Дж/моль), то противоположный ей процесс гидролиза является эндотермическим. В соответствии с принципом Ле. Шателье с повышением температуры степень гидролиза растет. 18

2. Добавление кислот и щелочей. Если при обратимом гидролизе накапливаются ионы Н+, в соответствии с принципом Ле Шателье процесс подавляется при подкислении и усиливается при подщелачивании. При накапливании ионов ОН- гидролиз подавляется при подщелачивании и усиливается при добавлении кислот. 3. Разбавление раствора увеличивает степень гидролиза 19

Необратимый гидролиз Если какое-либо из образующихся в процессе гидролиза веществ накапливается в растворе в таких количествах, что станет возможным выделение его в осадок или улетучивание в виде газа, то гидролиз будет необратимым, что приведет к полному разложению соли водой: Соли, подвергающиеся необратимому гидролизу: 20

Роль гидролиза биоорганических соединений в процессах жизнедеятельности 1. Каждый из ферментов активен при строго определенных значениях р. Н: пепсин желудочного сока активен при р. Н 1, 5– 2, 0, каталаза крови – при р. Н 7, 0; тканевые кетапсины при реакции среды, близкой к нейтральной, катализируют синтез белка, а при кислой реакции расщепляют его. 2. Ионы водорода катализируют гидролиз сложных жиров, сахарозы. 21

3. Без ферментативного гидролиза невозможно усвоение пищевых продуктов (жиры, углеводы, белки) , так как всасываться в кишечнике способны только относительно небольшие молекулы. ü Жиры в желудочно-кишечном тракте расщепляются водой на более мелкие фрагменты. R 1—О—R 2 + H 2 O → R 1—ОН + R 2—ОН R 1, R 2 — фрагменты биоорганической молекулы ü Усвоение полисахаридов и дисахаридов становится возможным лишь после полного их гидролиза ферментами до моносахаридов. ü Белки гидролизуются до веществ, которые лишь потом могут усваиваться. 22

4. Гидролиз АТФ - источник энергии в организме Человек получает энергию как за счет многостадийного процесса окисления пищи — белков, жиров и углеводов, так и за счет гидролиза некоторых сложных эфиров, амидов, пептидов и гликозидов. Космические ракеты высотой с башню устремляются в небо за счет громадной энергии, что выделяется при сжигании водорода в чистом кислороде. Эта же энергия поддерживает жизнь и в клетках нашего тела. В них реакция окисления протекает поэтапно. Кроме того, сначала вместо тепловой и кинетической энергии наши клетки создают клеточное «топливо» — АТФ. 23
Образование АТФ в клетке происходит в митохондриях за счет энергии, выделяющейся при биологическом окислении. 24
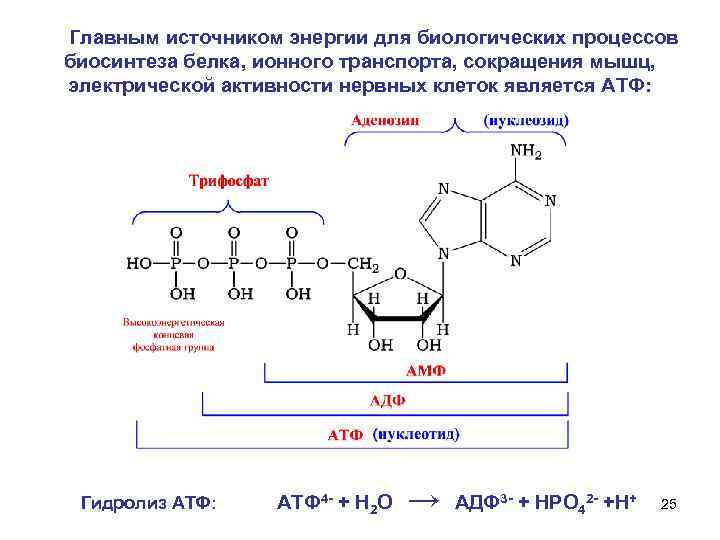
Главным источником энергии для биологических процессов биосинтеза белка, ионного транспорта, сокращения мышц, электрической активности нервных клеток является АТФ: Гидролиз АТФ: АТФ 4 - + Н 2 О → АДФ 3 - + НРО 42 - +Н+ 25
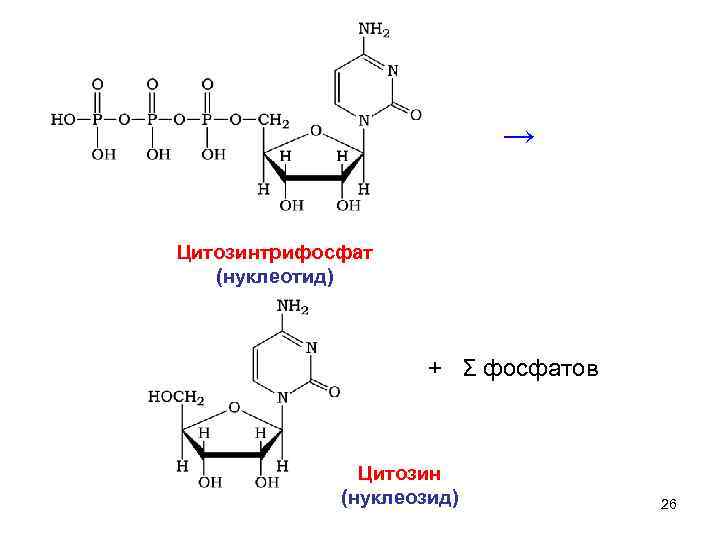
→ Цитозинтрифосфат (нуклеотид) + Σ фосфатов Цитозин (нуклеозид) 26
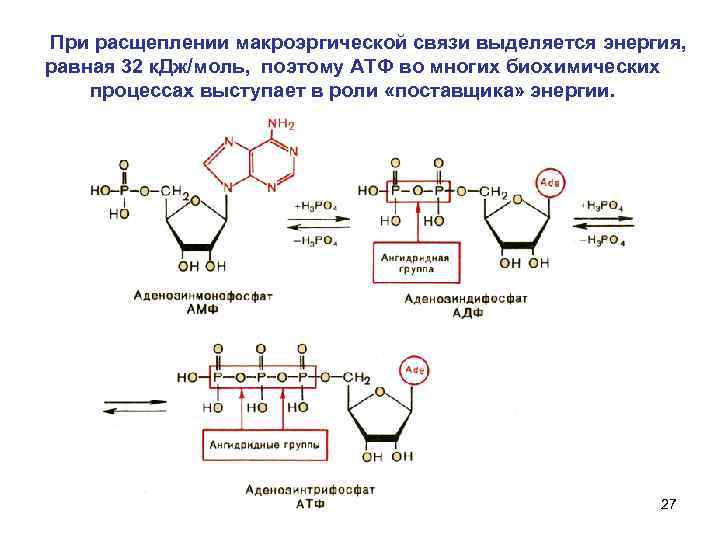
При расщеплении макроэргической связи выделяется энергия, равная 32 к. Дж/моль, поэтому АТФ во многих биохимических процессах выступает в роли «поставщика» энергии. 27

5. Гидролиз –один из важнейших путей метаболизма лекарственных препаратов и пищевых продуктов Процесс гидролиза может идти: ь В плазме крови ь На клеточных мембранах ь В цитоплазме клеток ь Во внутренних органеллах, в частности в лизосомах 28
Большинство лекарственных веществ метаболизируются в печени, располагающей для этого набором ферментных систем весьма большой мощности. Эти ферментные системы локализованы либо в митохондриях, либо в микросомах, либо в гиалоплазме. 29
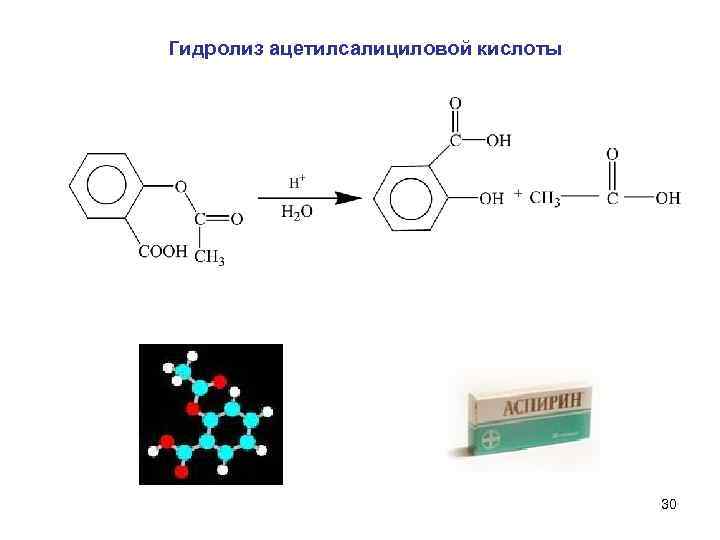
Гидролиз ацетилсалициловой кислоты 30
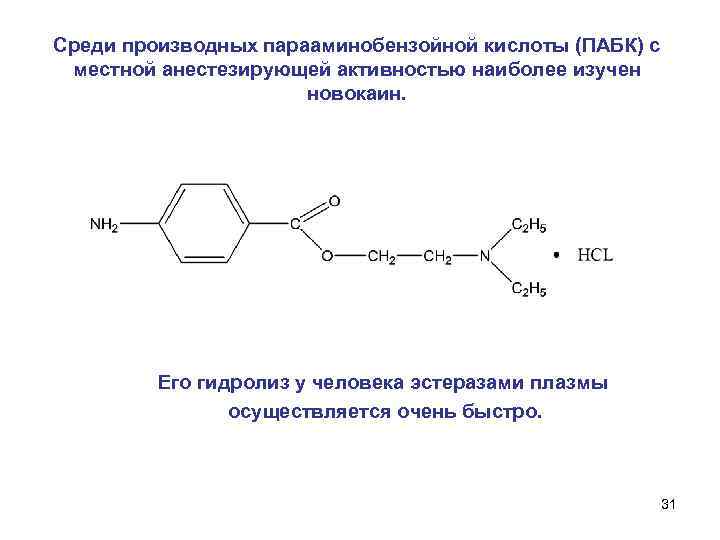
Среди производных парааминобензойной кислоты (ПАБК) с местной анестезирующей активностью наиболее изучен новокаин. Его гидролиз у человека эстеразами плазмы осуществляется очень быстро. 31
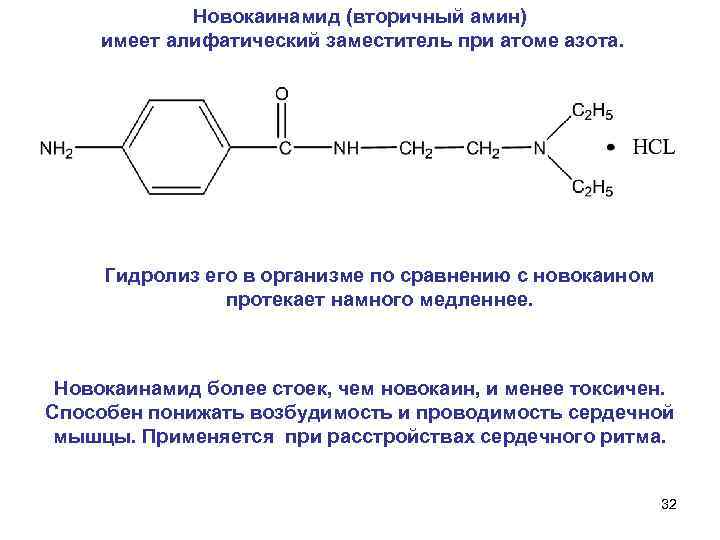
Новокаинамид (вторичный амин) имеет алифатический заместитель при атоме азота. Гидролиз его в организме по сравнению с новокаином протекает намного медленнее. Новокаинамид более стоек, чем новокаин, и менее токсичен. Способен понижать возбудимость и проводимость сердечной мышцы. Применяется при расстройствах сердечного ритма. 32
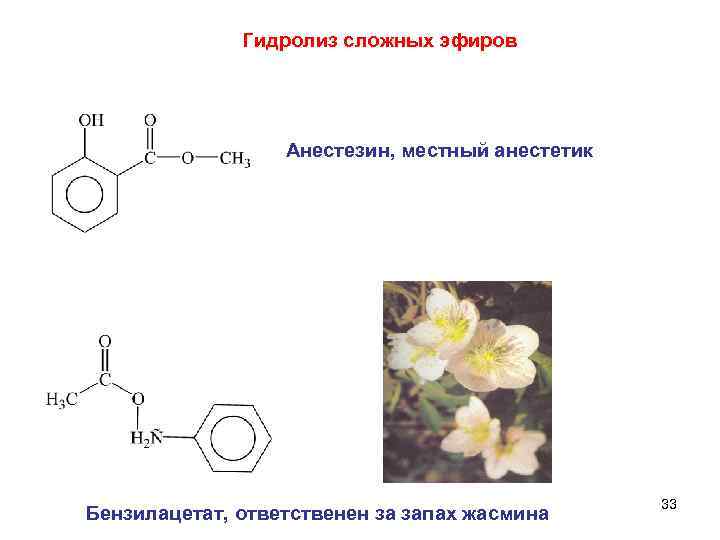
Гидролиз сложных эфиров Анестезин, местный анестетик 33 Бензилацетат, ответственен за запах жасмина

Тристеарин – компонент сала и некоторых твердых растительных жиров 34

Пентилацетат 35
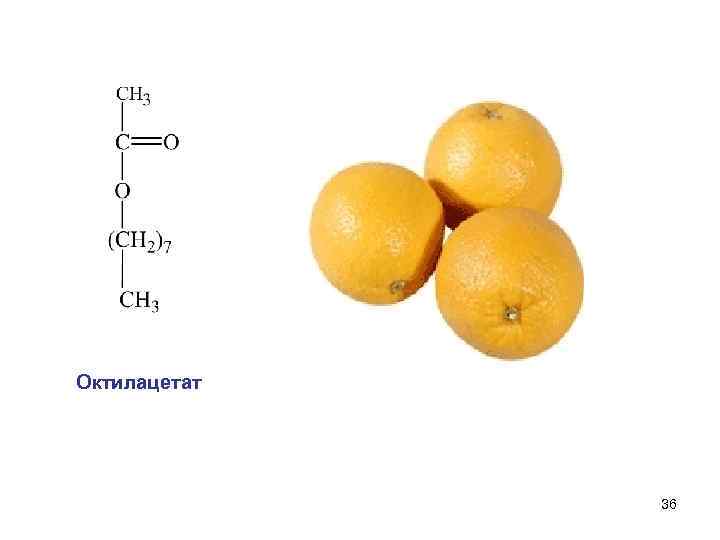
Октилацетат 36
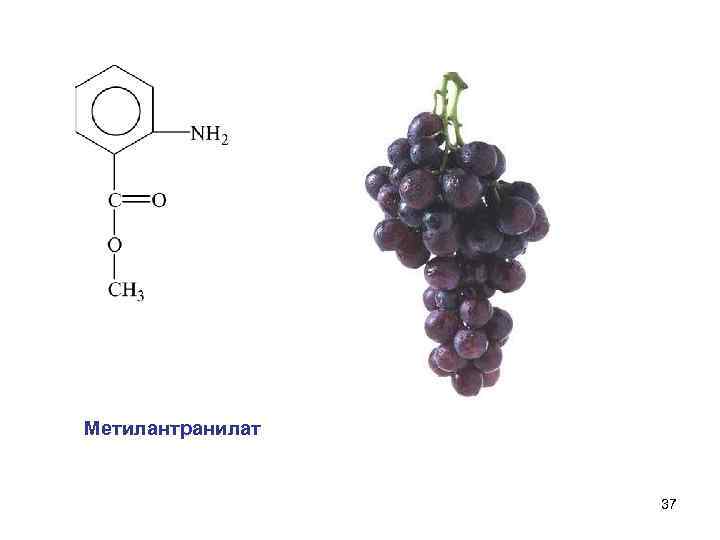
Метилантранилат 37
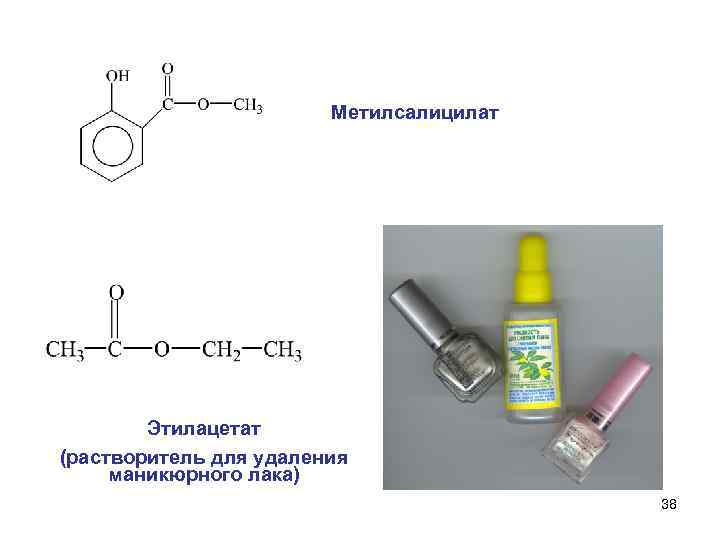
Метилсалицилат Этилацетат (растворитель для удаления маникюрного лака) 38

Этилбутанат Изопентилацетат 39
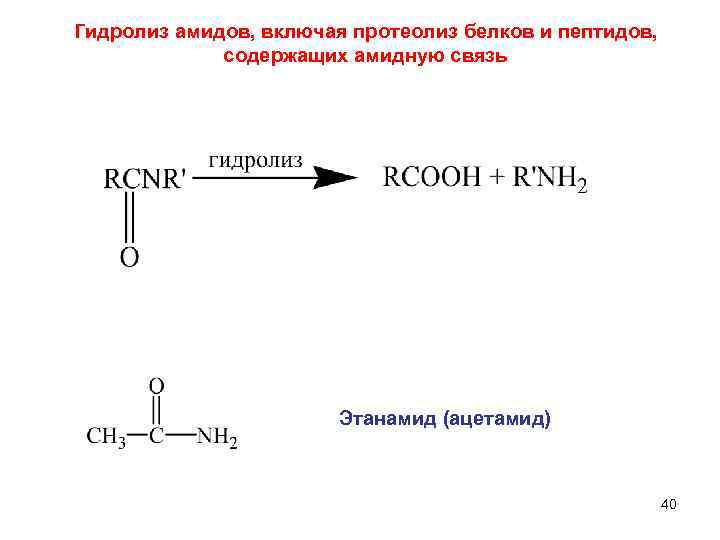
Гидролиз амидов, включая протеолиз белков и пептидов, содержащих амидную связь Этанамид (ацетамид) 40
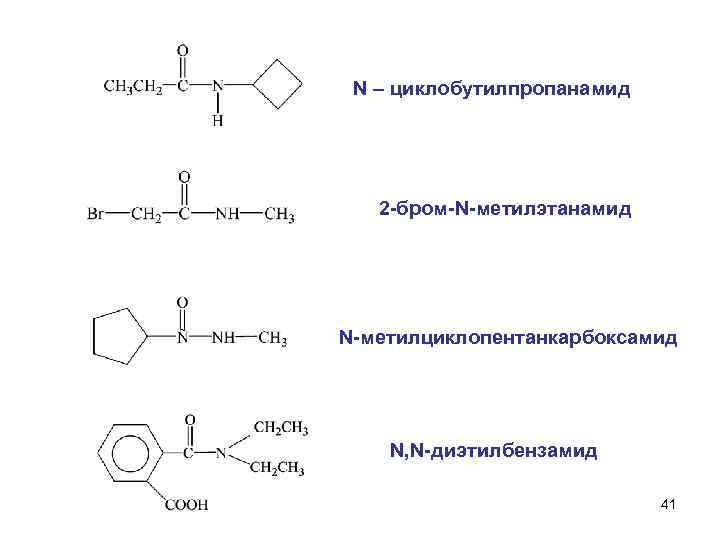
N – циклобутилпропанамид 2 -бром-N-метилэтанамид N-метилциклопентанкарбоксамид N, N-диэтилбензамид 41
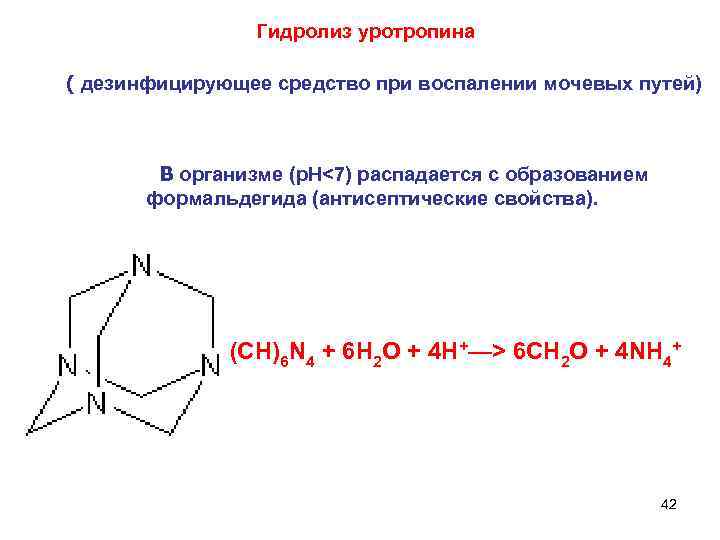
Гидролиз уротропина ( дезинфицирующее средство при воспалении мочевых путей) В организме (p. H<7) распадается с образованием формальдегида (антисептические свойства). (CH)6 N 4 + 6 Н 2 О + 4 H+—> 6 СН 2 О + 4 NH 4+ 42
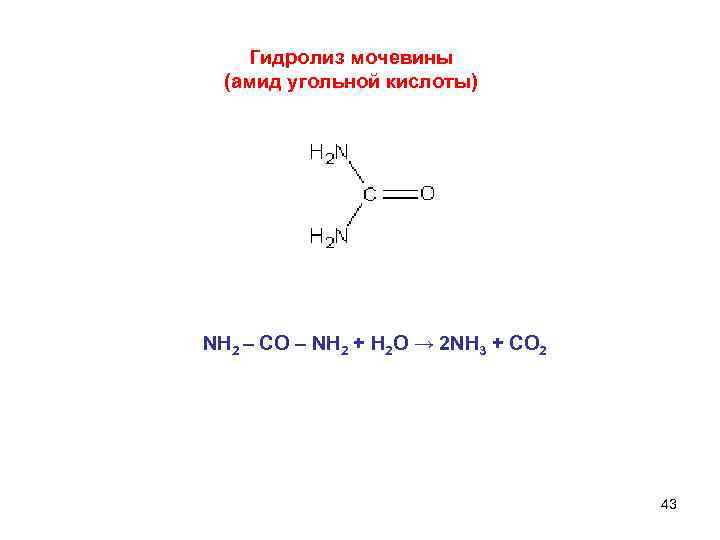
Гидролиз мочевины (амид угольной кислоты) NH 2 – CO – NH 2 + H 2 O → 2 NH 3 + CO 2 43
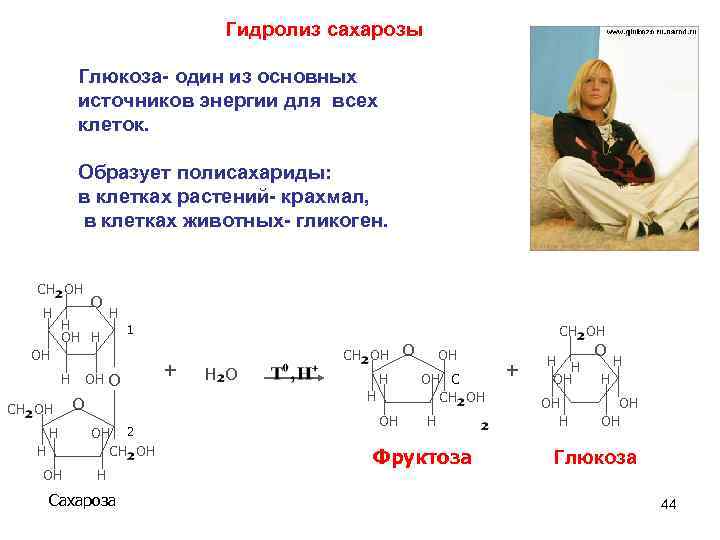
Гидролиз сахарозы Глюкоза- один из основных источников энергии для всех клеток. Образует полисахариды: в клетках растений- крахмал, в клетках животных- гликоген. + CH OH О H H 1 CH OH H OH CH OH О OH О H H H H OH О + H O H OH С + OH H CH OH О OH OH OH H OH 2 H CH OH Фруктоза Глюкоза OH H Сахароза 44

45

Спасибо за внимание! 46
03-2 Гидролиз.ppt
- Количество слайдов: 46

