Кафедра медицинской микробиологии Генетика бактерий












































































































genetika_bakteriy.pptx
- Размер: 36.8 Мб
- Автор:
- Количество слайдов: 186
Описание презентации Кафедра медицинской микробиологии Генетика бактерий по слайдам
 Кафедра медицинской микробиологии Генетика бактерий
Кафедра медицинской микробиологии Генетика бактерий
 • 1865 год • Открытие Г. Менделем (1822– 1884) факторов наследственности и разработка гибридологического метода, т. е. правил скрещивания организмов и учета признаков у их потомства.
• 1865 год • Открытие Г. Менделем (1822– 1884) факторов наследственности и разработка гибридологического метода, т. е. правил скрещивания организмов и учета признаков у их потомства.
 • 1900 год • Формальное рождение генетики как науки. Независимая публикация статей Г. де Фриза, К. Корренса и Э. Чермака с изложением основных законов наследования. «Переоткрыты» и стали известны широкой научной общественности исследования Г. Менделя.
• 1900 год • Формальное рождение генетики как науки. Независимая публикация статей Г. де Фриза, К. Корренса и Э. Чермака с изложением основных законов наследования. «Переоткрыты» и стали известны широкой научной общественности исследования Г. Менделя.
 • 1905 год • У. Бэтсон предлагает слово «генетика» (от греч. — порождать) для нового направления науки.
• 1905 год • У. Бэтсон предлагает слово «генетика» (от греч. — порождать) для нового направления науки.
 • 1910 год • Т. Г. Морган установил, что гены расположены в хромосомах в линейном порядке, образуя группы сцепления. Морган установил также закономерности наследования признаков, сцепленных с полом ( Нобелевская премия 1933 г. по физиологии и медицине за экспериментальное обоснование хромосомной теории наследственности). • А. Кёссель получил Нобелевскую премию по химии за установление того, что в состав ДНК входят четыре азотистых основания: аденин, гуанин, цитозин и тимин.
• 1910 год • Т. Г. Морган установил, что гены расположены в хромосомах в линейном порядке, образуя группы сцепления. Морган установил также закономерности наследования признаков, сцепленных с полом ( Нобелевская премия 1933 г. по физиологии и медицине за экспериментальное обоснование хромосомной теории наследственности). • А. Кёссель получил Нобелевскую премию по химии за установление того, что в состав ДНК входят четыре азотистых основания: аденин, гуанин, цитозин и тимин.
 • 1929– 1930 годы • А. С. Серебровский и Н. П. Дубинин впервые продемонстрировали сложную природу организации гена; первые реальные шаги на пути создания современного представления о тонкой структуре гена.
• 1929– 1930 годы • А. С. Серебровский и Н. П. Дубинин впервые продемонстрировали сложную природу организации гена; первые реальные шаги на пути создания современного представления о тонкой структуре гена.
 • 1940 год • Дж. Бидл и Э. Татум сформулировали теорию «один ген — один фермент» . (Нобелевская премия по физиологии и медицине за 1958 г. ).
• 1940 год • Дж. Бидл и Э. Татум сформулировали теорию «один ген — один фермент» . (Нобелевская премия по физиологии и медицине за 1958 г. ).
 • 1943 год • И. А. Рапопорт, Ш. Ауэрбах и Дж. Г. Робсон впервые показали индукцию мутаций химическими веществами.
• 1943 год • И. А. Рапопорт, Ш. Ауэрбах и Дж. Г. Робсон впервые показали индукцию мутаций химическими веществами.
 • 1944 год • О. Эвери, К. Маклеод и М. Маккарти установили, что «веществом гена» служит ДНК. Начало «эры ДНК» . • М. Дельбрюк, С. Лурия, А. Херши произвели пионерские исследования по генетике кишечной палочки и ее фагов, после чего эти объекты стали модельными для генетических исследований на многие десятилетия. (Нобелевская премия по физиологии и медицине за 1969 год за открытие цикла репродукции вирусов и развитие генетики бактерий и вирусов). • Л. А. Зильбер сформулировал вирусно-генетическую теорию рака.
• 1944 год • О. Эвери, К. Маклеод и М. Маккарти установили, что «веществом гена» служит ДНК. Начало «эры ДНК» . • М. Дельбрюк, С. Лурия, А. Херши произвели пионерские исследования по генетике кишечной палочки и ее фагов, после чего эти объекты стали модельными для генетических исследований на многие десятилетия. (Нобелевская премия по физиологии и медицине за 1969 год за открытие цикла репродукции вирусов и развитие генетики бактерий и вирусов). • Л. А. Зильбер сформулировал вирусно-генетическую теорию рака.

 • 1950 год • Э. Чаргафф сформулировал знаменитое «правило Чаргаффа» , которое гласит: в ДНК число нуклеотидов А равно числу Т, а число Г — числу Ц. • Б. Мак-Клинток показала существование перемещающихся генетических элементов. • С большим опозданием (только в 1983 г. ) она получила за это Нобелевскую премию в области физиологии и медицины.
• 1950 год • Э. Чаргафф сформулировал знаменитое «правило Чаргаффа» , которое гласит: в ДНК число нуклеотидов А равно числу Т, а число Г — числу Ц. • Б. Мак-Клинток показала существование перемещающихся генетических элементов. • С большим опозданием (только в 1983 г. ) она получила за это Нобелевскую премию в области физиологии и медицины.


 • 1951 год • Р. Франклин и М. Уилкинс получили первую рентгенограмму молекулы ДНК.
• 1951 год • Р. Франклин и М. Уилкинс получили первую рентгенограмму молекулы ДНК.


 • 1953 год • Ф. Крик и Дж. Уотсон, опираясь на результаты опытов генетиков и биохимиков и на данные рентгеноструктурного анализа, создали структурную модель ДНК в форме двойной спирали. В 1962 году им совместно с М. X. Ф. Уилкинсом присуждена Нобелевская премия по физиологии и медицине.
• 1953 год • Ф. Крик и Дж. Уотсон, опираясь на результаты опытов генетиков и биохимиков и на данные рентгеноструктурного анализа, создали структурную модель ДНК в форме двойной спирали. В 1962 году им совместно с М. X. Ф. Уилкинсом присуждена Нобелевская премия по физиологии и медицине.




 • 1958 • Ледерберг, Нобелевская премия за открытие генетической рекомбинации
• 1958 • Ледерберг, Нобелевская премия за открытие генетической рекомбинации
 • 1968 • Холли, Корана, Ниренберг • Расшифровка генетического кода и его роли в синтезе белка
• 1968 • Холли, Корана, Ниренберг • Расшифровка генетического кода и его роли в синтезе белка
 • 1972 год • В лаборатории Пола Берга получены первые рекомбинантные ДНК (Нобелевская премия по химии за 1980 г. вручена П. Бергу и Г. Бойеру). Заложены основы генной инженерии.
• 1972 год • В лаборатории Пола Берга получены первые рекомбинантные ДНК (Нобелевская премия по химии за 1980 г. вручена П. Бергу и Г. Бойеру). Заложены основы генной инженерии.
 • 1985 год • Создание К. Б. Мюллисом революционизирующей технологии — полимеразной цепной реакции, ПЦР — наиболее чувствительного до сих пор метода детектирования ДНК. Эта технология получила широкое распространение (Нобелевская премия по химии за 1993 г. ).
• 1985 год • Создание К. Б. Мюллисом революционизирующей технологии — полимеразной цепной реакции, ПЦР — наиболее чувствительного до сих пор метода детектирования ДНК. Эта технология получила широкое распространение (Нобелевская премия по химии за 1993 г. ).
 • 1983, Барбара Мак Клинток • Открытие транспозонов
• 1983, Барбара Мак Клинток • Открытие транспозонов
 • 1995 год • Определена полная последовательность генома первого самостоятельно существующего организма — бактерии Haemophilus influenzae (1 830 137 п. н. ). Становление геномики как самостоятельного раздела генетики.
• 1995 год • Определена полная последовательность генома первого самостоятельно существующего организма — бактерии Haemophilus influenzae (1 830 137 п. н. ). Становление геномики как самостоятельного раздела генетики.
 Нобелевские премии по генетике • 1933 — теория гена (Т. Морган); • 1946 — открытие мутагенного действия Ренгеновских лучей на дрозофилу (Г. Меллер); • 1957 — расшифровка структуры нуклеотидов и нуклеозидов (A. Тодд); • 1958 — достижения в общей генетике (Г. Бидл, Э. Татум, Дж. Ледерберг); • 1959 — проведение синтеза нуклеиновых кислот in vitro (С. Очоа, А. Корнберг); • 1962 — расшифровка структуры ДНК (Дж. Уотсон, Ф. Крик, М. Уилкинс); • 1965 — достижения в генетике микроорганизмов (Ф. Жакоб, Ж. Моно, А. Львофф); • 1966 — исследования онкогенных вирусов (П. Раус); • 1968 — открытие и интерпретация генетического кода и его роли в синтезе белков (Р. Холли, Х. Корана, М. Ниренберг); • 1969 — исследования по генетике вирусов (М. Дельбрюк, С. Луриа, А. Херши); • 1975 — исследования по онкогенным вирусам (Р. Дальбекко, Х. Темин, Д. Балтимор); • 1978 — использование рестрикционных ферментов для картирования генов • (В. Арбер, Х. Смит, О. Натанс); • 1980 — достижения в области иммуногенетики (Г. Снелл, Ж. Доссе, Б. Бенасерра); • • достижения в области искусственного манипулирования ДНК (П. Берг, У. Гилберт, Ф, Сэнджер); • 1983 — открытие подвижных генетических элементов (Б. Мак-Клинток); • 1985 — установление механизмов рецепции низкомолекулярных липопротеинов и генетической природы семейной гиперхолестеринемии (М. Браун, Дж. Гольдштейн); • 1986 — конструирование первого электронного микроскопа (Э. Рушка); • 1987 — выяснение генетических механизмов многообразия антител (С. Тонегава); • 1989 — исследования по онкогенам ретровирусов (Дж. Бишоп, Х. Вармус);
Нобелевские премии по генетике • 1933 — теория гена (Т. Морган); • 1946 — открытие мутагенного действия Ренгеновских лучей на дрозофилу (Г. Меллер); • 1957 — расшифровка структуры нуклеотидов и нуклеозидов (A. Тодд); • 1958 — достижения в общей генетике (Г. Бидл, Э. Татум, Дж. Ледерберг); • 1959 — проведение синтеза нуклеиновых кислот in vitro (С. Очоа, А. Корнберг); • 1962 — расшифровка структуры ДНК (Дж. Уотсон, Ф. Крик, М. Уилкинс); • 1965 — достижения в генетике микроорганизмов (Ф. Жакоб, Ж. Моно, А. Львофф); • 1966 — исследования онкогенных вирусов (П. Раус); • 1968 — открытие и интерпретация генетического кода и его роли в синтезе белков (Р. Холли, Х. Корана, М. Ниренберг); • 1969 — исследования по генетике вирусов (М. Дельбрюк, С. Луриа, А. Херши); • 1975 — исследования по онкогенным вирусам (Р. Дальбекко, Х. Темин, Д. Балтимор); • 1978 — использование рестрикционных ферментов для картирования генов • (В. Арбер, Х. Смит, О. Натанс); • 1980 — достижения в области иммуногенетики (Г. Снелл, Ж. Доссе, Б. Бенасерра); • • достижения в области искусственного манипулирования ДНК (П. Берг, У. Гилберт, Ф, Сэнджер); • 1983 — открытие подвижных генетических элементов (Б. Мак-Клинток); • 1985 — установление механизмов рецепции низкомолекулярных липопротеинов и генетической природы семейной гиперхолестеринемии (М. Браун, Дж. Гольдштейн); • 1986 — конструирование первого электронного микроскопа (Э. Рушка); • 1987 — выяснение генетических механизмов многообразия антител (С. Тонегава); • 1989 — исследования по онкогенам ретровирусов (Дж. Бишоп, Х. Вармус);
 План лекции Строение и функционирование генетического аппарата бактериальной клетки. Нуклеоид. ДНК. РНК. Внехромосомные и мобильные гены бактерий. Виды изменчивости бактерий. Мутации. Мутагены. Репарации. Мутанты. Рекомбинации: Трансформация. Трансдукция. Коньюгация. Генетика патогенности и лекарственной устойчивости. Применение методов генетики бактерий в медицине и микробиологии. Геномика.
План лекции Строение и функционирование генетического аппарата бактериальной клетки. Нуклеоид. ДНК. РНК. Внехромосомные и мобильные гены бактерий. Виды изменчивости бактерий. Мутации. Мутагены. Репарации. Мутанты. Рекомбинации: Трансформация. Трансдукция. Коньюгация. Генетика патогенности и лекарственной устойчивости. Применение методов генетики бактерий в медицине и микробиологии. Геномика.
 1. Строение и функционирование генетического аппарата бактериальной клетки. Нуклеоид. ДНК. РНК.
1. Строение и функционирование генетического аппарата бактериальной клетки. Нуклеоид. ДНК. РНК.

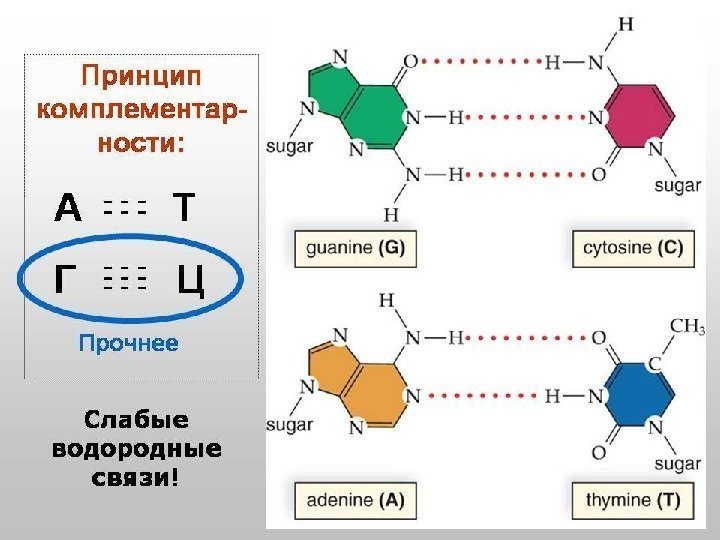
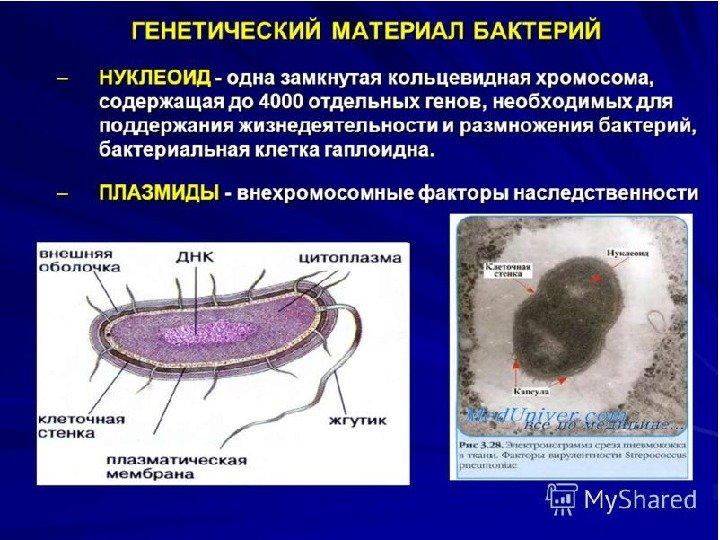
 Генетический материал бактерий представлен: 1. хромосомой ( одна, замкнутая в кольцо ) 2. внехромосомными элементами наследственности: . плазмидами. транспозонами . IS-элементами
Генетический материал бактерий представлен: 1. хромосомой ( одна, замкнутая в кольцо ) 2. внехромосомными элементами наследственности: . плазмидами. транспозонами . IS-элементами


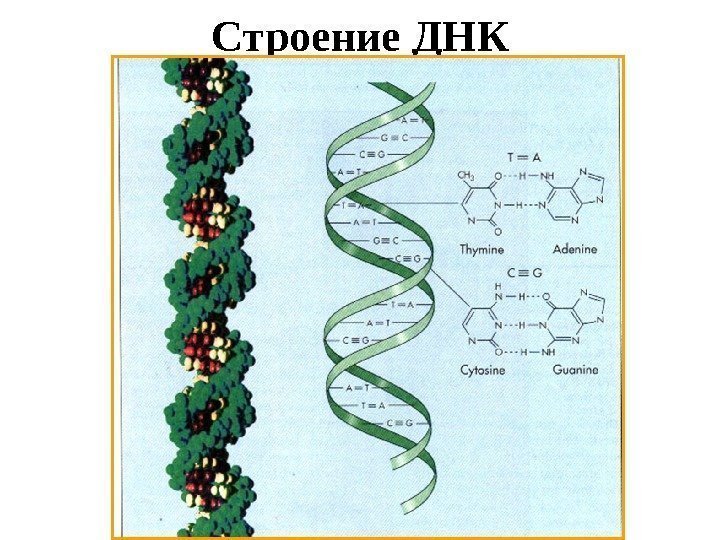
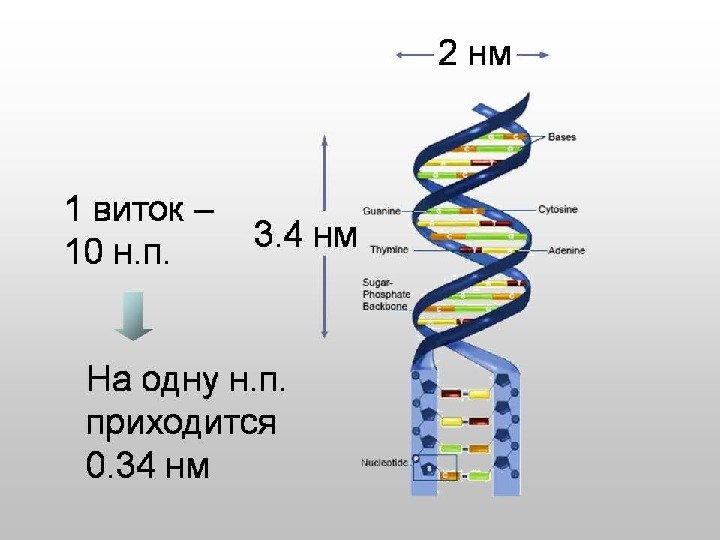
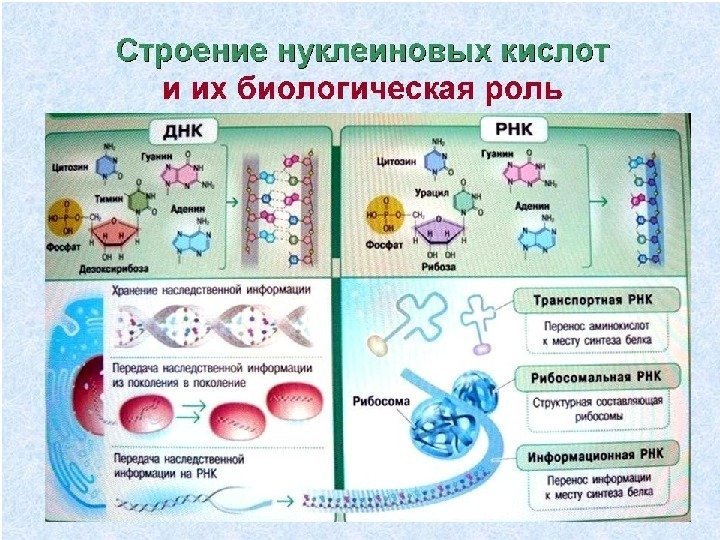
 Строение ДНК
Строение ДНК

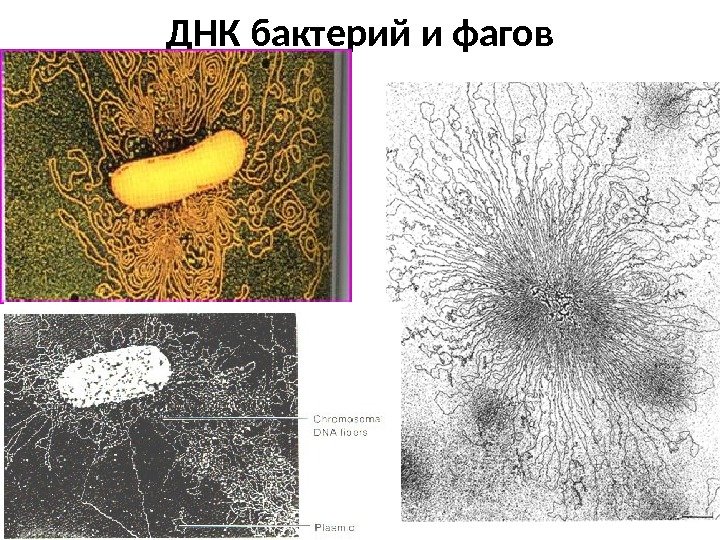
 ДНК бактерий и фагов
ДНК бактерий и фагов




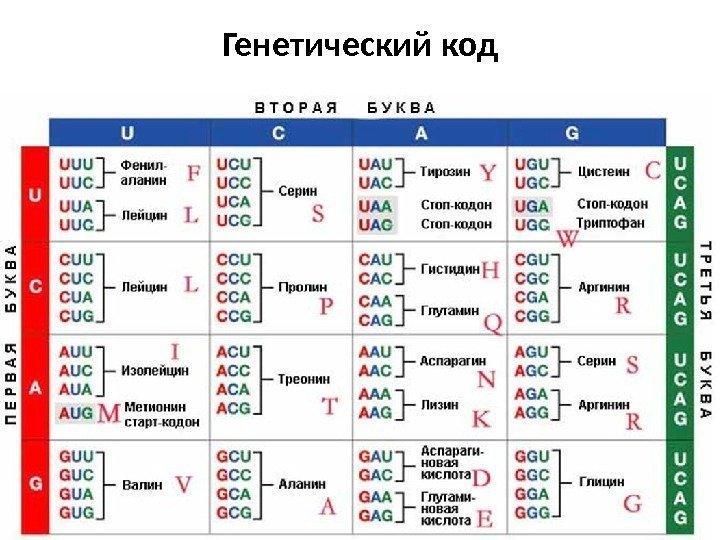
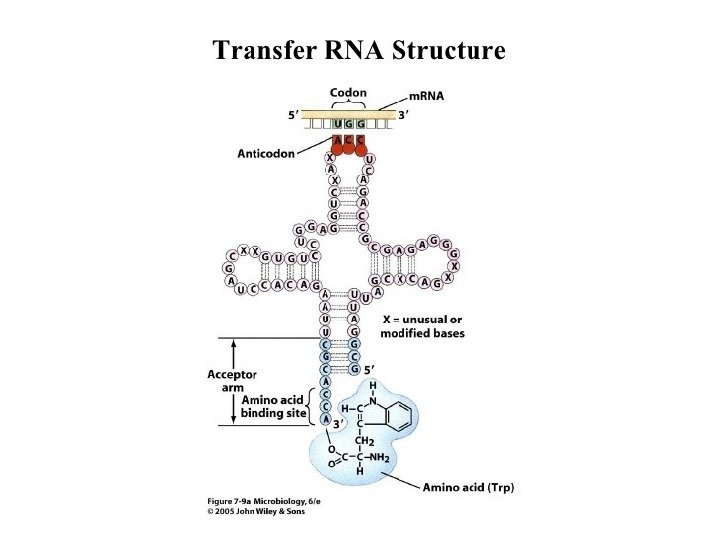
 Генетический код
Генетический код
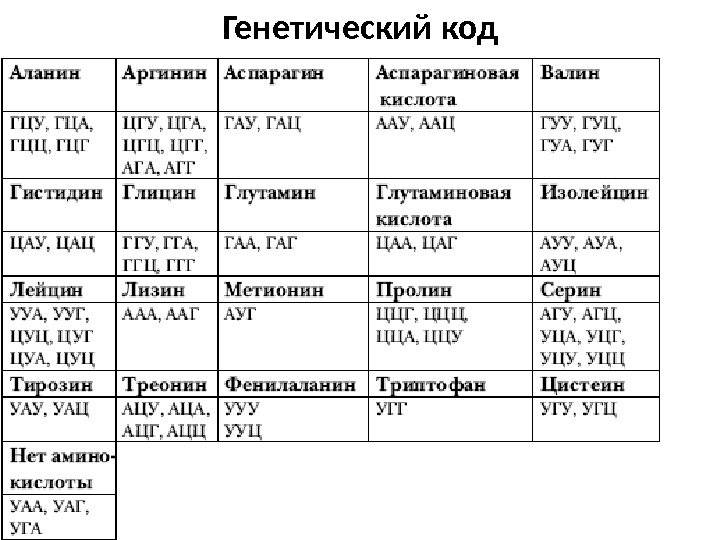
 Генетический код
Генетический код
 Единицы наследственного материала • Ген – функциональная единица наследственности Структурные гены(около 4000) Гены, кодирующие РНК(16 S, 5 S, 23 S + 20 тр. РНК) Регуляторные гены • Триплет (= кодон ) – смысловая единица, соответствующая аминокислоте • Нуклеотиды ( А, Г, Т, Ц) – основные структурные “буквы” генетического кода
Единицы наследственного материала • Ген – функциональная единица наследственности Структурные гены(около 4000) Гены, кодирующие РНК(16 S, 5 S, 23 S + 20 тр. РНК) Регуляторные гены • Триплет (= кодон ) – смысловая единица, соответствующая аминокислоте • Нуклеотиды ( А, Г, Т, Ц) – основные структурные “буквы” генетического кода
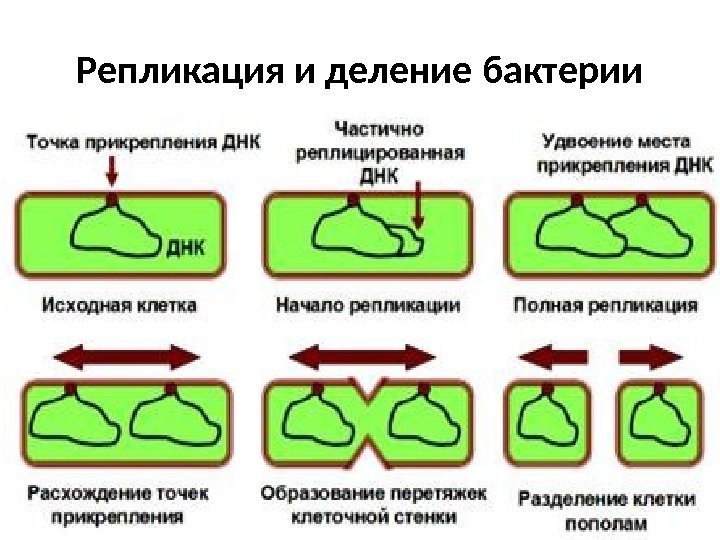
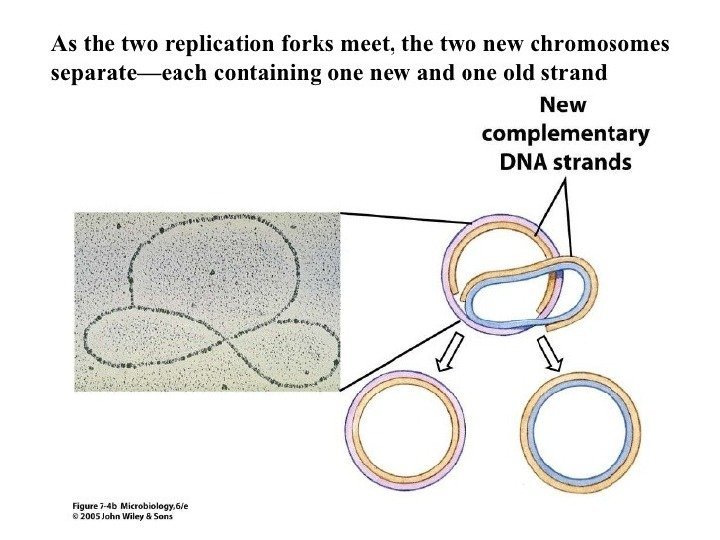
 Репликация и деление бактерии
Репликация и деление бактерии
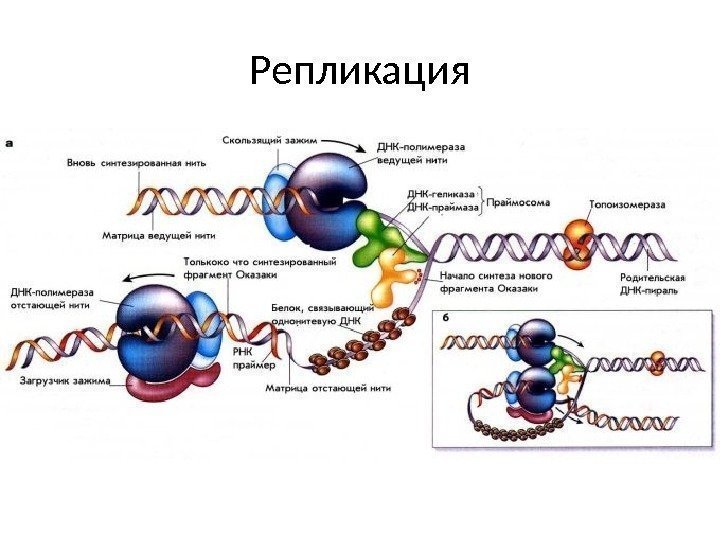
 Репликация
Репликация
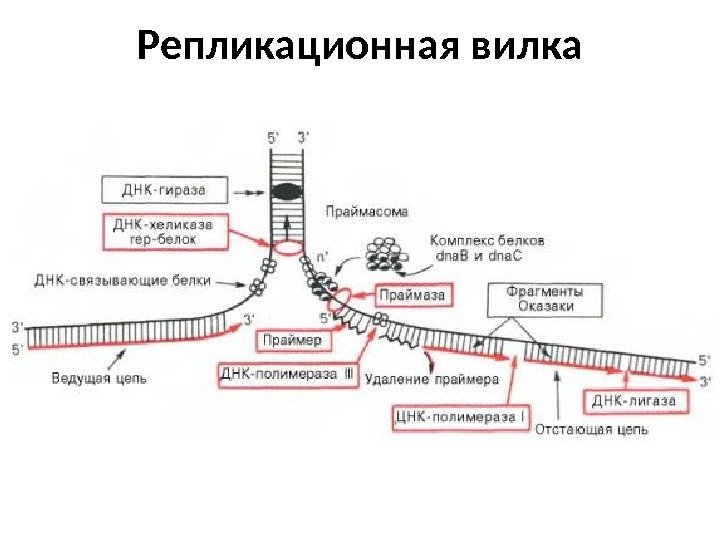
 Репликационная вилка
Репликационная вилка
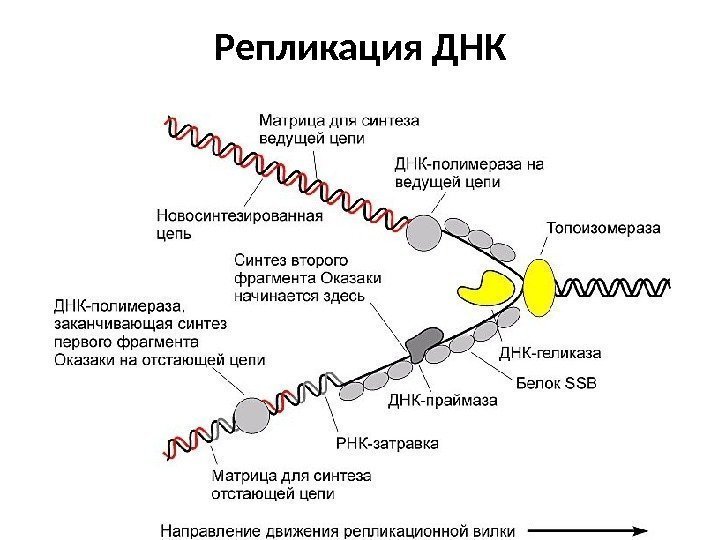
 Репликация ДНК
Репликация ДНК


 Х/т препараты, ингибирующие синтез нуклеиновых кислот (РНК и ДНК): • • А) ингибиторы синтеза предшественников НК • — сульфаниламиды • — триметоприм • В) ингибиторы репликации ДНК • фторхинолоны — ингибируют фермент ДНК-гиразу, что нарушает функцию ДНК и соответственно синтез РНК – ципрофлоксацин (ципробай) , норфлоксацин, офлоксацин. • нитроимидазолы • нитрофураны • С) ингибиторы РНК – полимеразы • группа анзамицинов – ингибируют фермент ДНК-зависимую РНК-полимеразу в результате чего происходит угнетение синтеза РНК – рифамицин и его полусинтетический аналог – рифампицин;
Х/т препараты, ингибирующие синтез нуклеиновых кислот (РНК и ДНК): • • А) ингибиторы синтеза предшественников НК • — сульфаниламиды • — триметоприм • В) ингибиторы репликации ДНК • фторхинолоны — ингибируют фермент ДНК-гиразу, что нарушает функцию ДНК и соответственно синтез РНК – ципрофлоксацин (ципробай) , норфлоксацин, офлоксацин. • нитроимидазолы • нитрофураны • С) ингибиторы РНК – полимеразы • группа анзамицинов – ингибируют фермент ДНК-зависимую РНК-полимеразу в результате чего происходит угнетение синтеза РНК – рифамицин и его полусинтетический аналог – рифампицин;
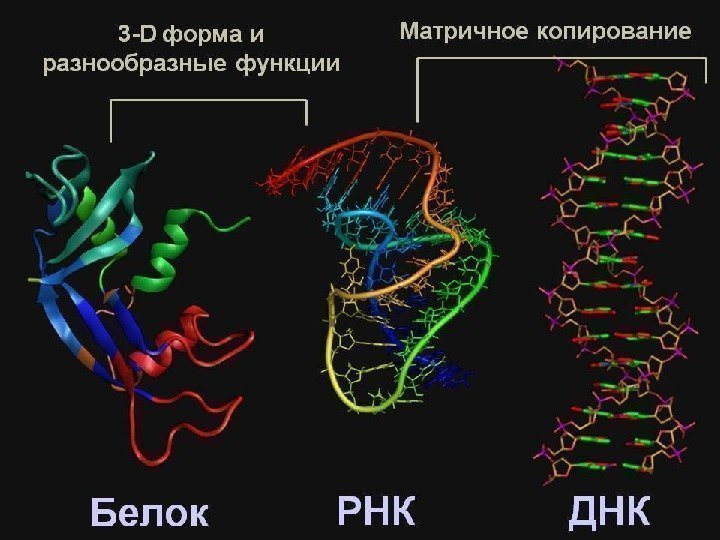
 Центральная догма генетики ДНК > РНК > белок (60 -е годы)
Центральная догма генетики ДНК > РНК > белок (60 -е годы)


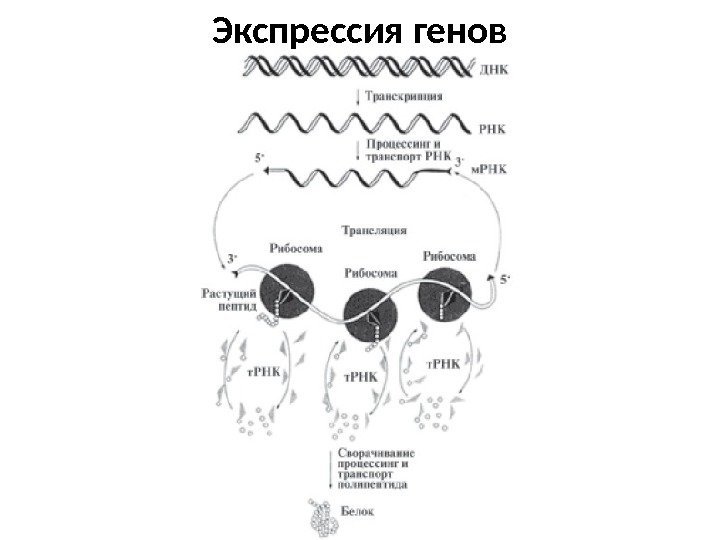
 Экспрессия генов
Экспрессия генов

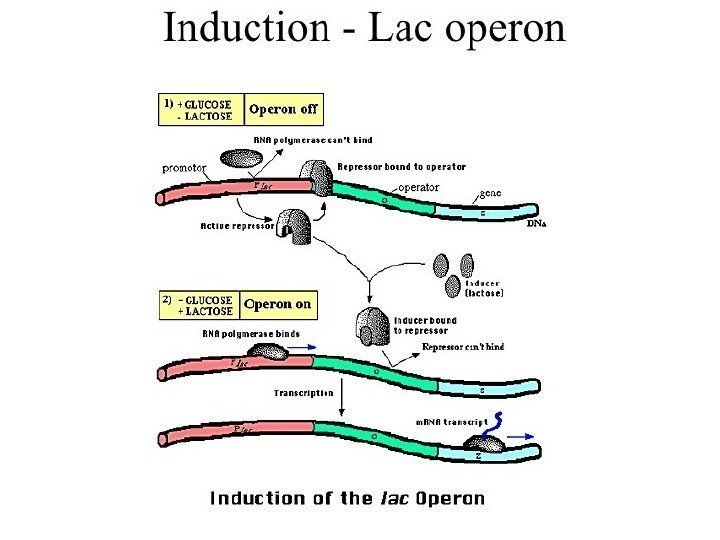
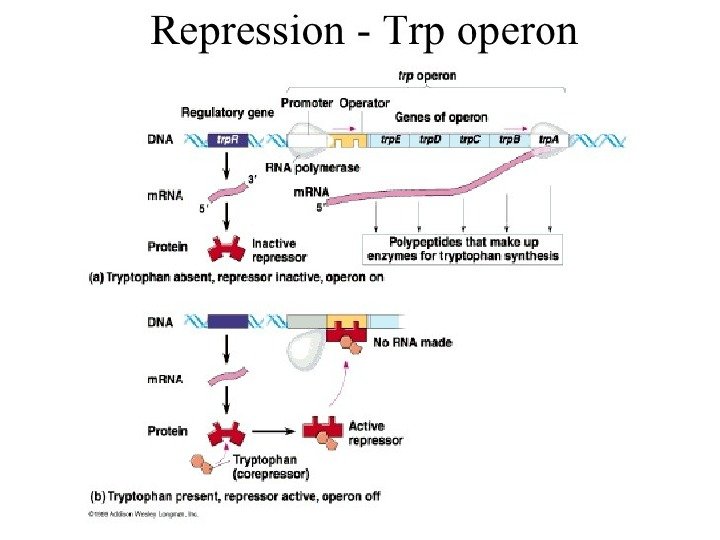
 Регуляция экспрессии генов • Не все гены постоянно работают и экспрессируются • Конститутивные гены постоянно экспрессируются и не регулируются • Катаболические и биосинтетические гены регулируются: – Включаются – Выключаются
Регуляция экспрессии генов • Не все гены постоянно работают и экспрессируются • Конститутивные гены постоянно экспрессируются и не регулируются • Катаболические и биосинтетические гены регулируются: – Включаются – Выключаются



 2. Внехромосомные и мобильные генетические элементы бактерий
2. Внехромосомные и мобильные генетические элементы бактерий
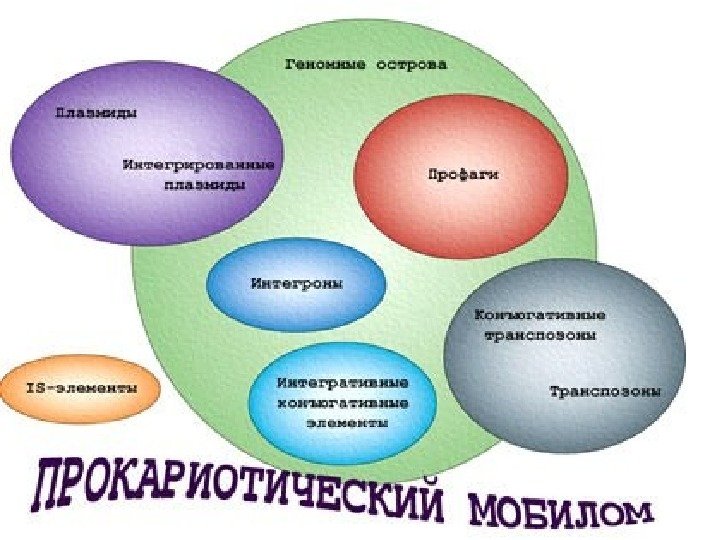
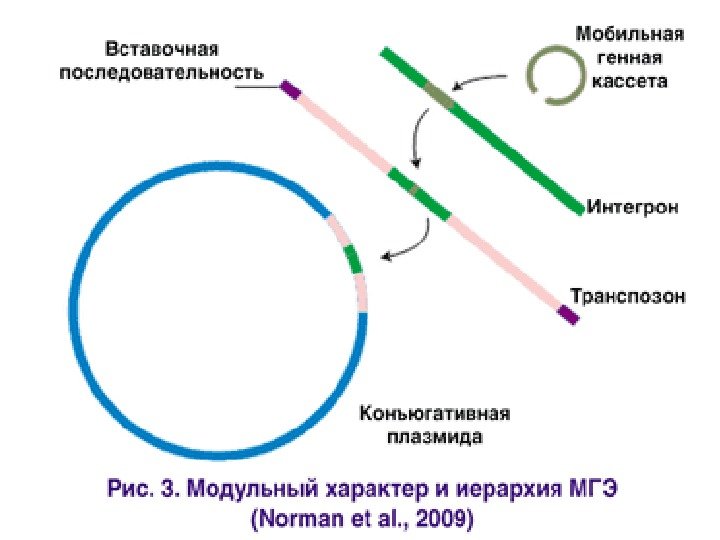
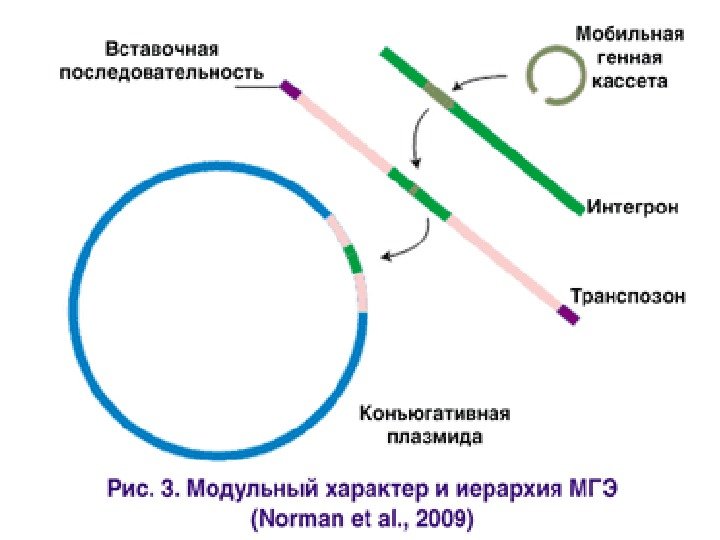
 Мобильные генетические элементы • Горизонтальный Генетический Перенос(ГГП) осуществляют мобильные генетические элементы (МГЭ) — чрезвычайно пёстрая группа «мигрантов» , в которую входят: • вирусы, плазмиды, транспозоны, интегроны, геномные острова, кластеры и кассеты генов. • Революционные темпы развития молекулярно-биологического инструментария и пополнения баз «прочитанных» нуклеотидных последовательностей способствовали открытию удивительного мира МГЭ, или мобилома.
Мобильные генетические элементы • Горизонтальный Генетический Перенос(ГГП) осуществляют мобильные генетические элементы (МГЭ) — чрезвычайно пёстрая группа «мигрантов» , в которую входят: • вирусы, плазмиды, транспозоны, интегроны, геномные острова, кластеры и кассеты генов. • Революционные темпы развития молекулярно-биологического инструментария и пополнения баз «прочитанных» нуклеотидных последовательностей способствовали открытию удивительного мира МГЭ, или мобилома.

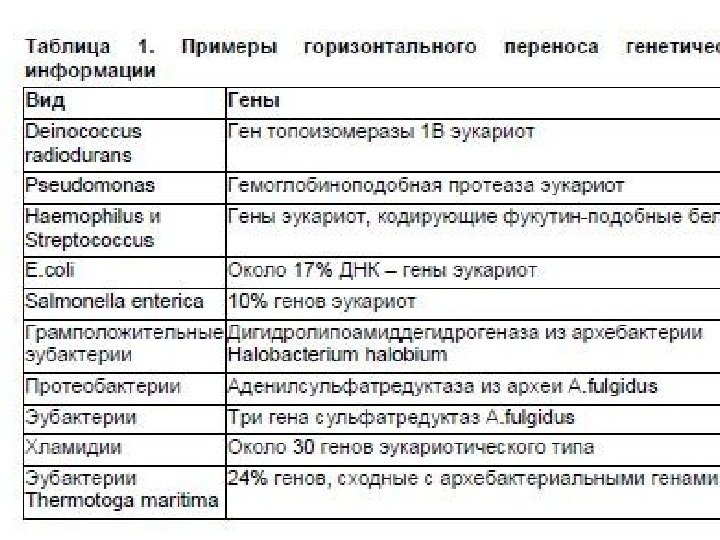
 Горизонтальный генетический перенос • ГГП может происходить внутри вирусов, прокариотических и эукариотических клеток • и даже между вирусов, прокариотических и эукариотически клеток • а также в пределах одной клетки. • В настоящее время ГГП признан одним из основных механизмов адаптивной эволюции.
Горизонтальный генетический перенос • ГГП может происходить внутри вирусов, прокариотических и эукариотических клеток • и даже между вирусов, прокариотических и эукариотически клеток • а также в пределах одной клетки. • В настоящее время ГГП признан одним из основных механизмов адаптивной эволюции.


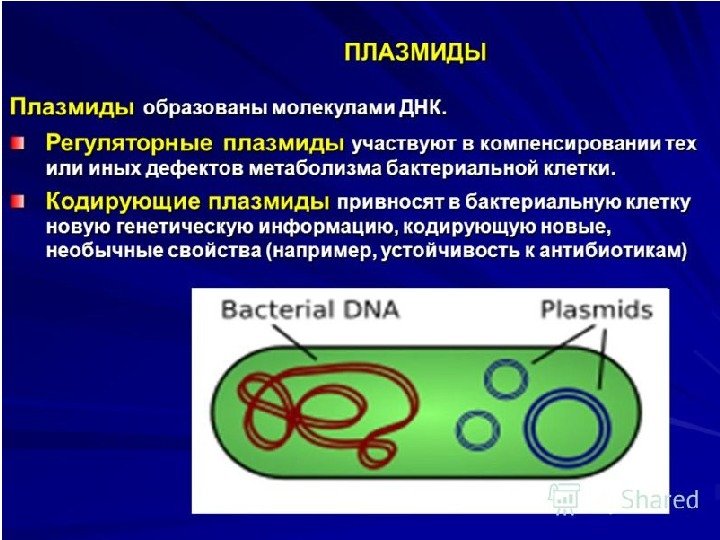
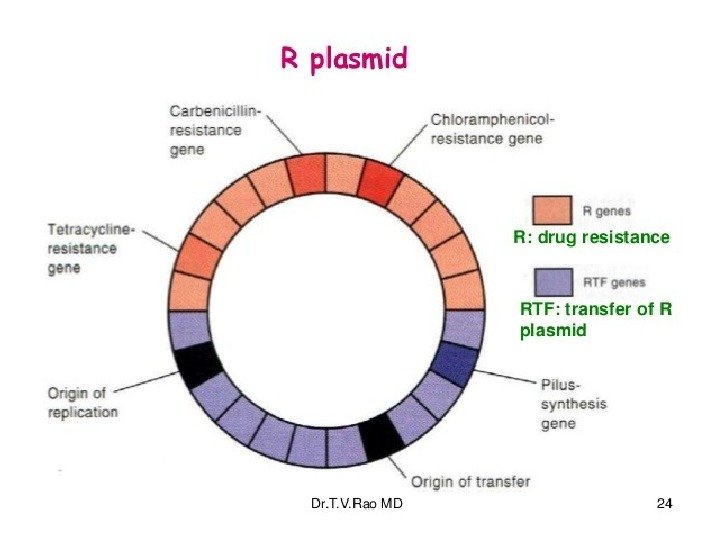
 Плазмиды Кольцевые молекулы ДНК молекулярной массой до 106 -108 Д с 1, 5 -400 тыс. пар оснований. Включают 4 -50 генов. Они могут существовать в цитоплазме в свободном состоянии или быть интегрированными с клеточной хромосомой. Тогда их называют эписомами. Плазмиды содержат в своем составе tra-оперон (transfer — перенос), который обеспечивает их способность к передаче, и гены, которые кодируют какой-то признак. Плазмиды называют трансмиссивными , если они самостоятельно передаются другим клеткам с помощью конъюгации, и нетрансмиссивными , когда не имеют собственного аппарата передачи, а переносятся вместе трансмиссивными или при трансдукції. Они могут существовать в клетке в нескольких копиях.
Плазмиды Кольцевые молекулы ДНК молекулярной массой до 106 -108 Д с 1, 5 -400 тыс. пар оснований. Включают 4 -50 генов. Они могут существовать в цитоплазме в свободном состоянии или быть интегрированными с клеточной хромосомой. Тогда их называют эписомами. Плазмиды содержат в своем составе tra-оперон (transfer — перенос), который обеспечивает их способность к передаче, и гены, которые кодируют какой-то признак. Плазмиды называют трансмиссивными , если они самостоятельно передаются другим клеткам с помощью конъюгации, и нетрансмиссивными , когда не имеют собственного аппарата передачи, а переносятся вместе трансмиссивными или при трансдукції. Они могут существовать в клетке в нескольких копиях.


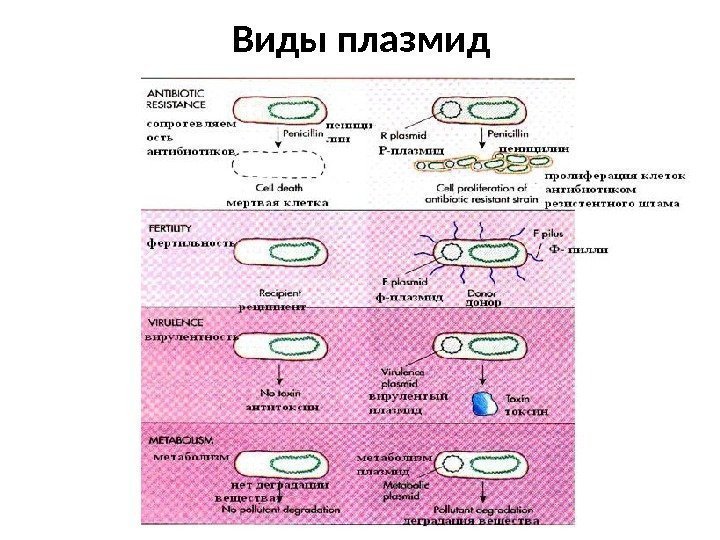
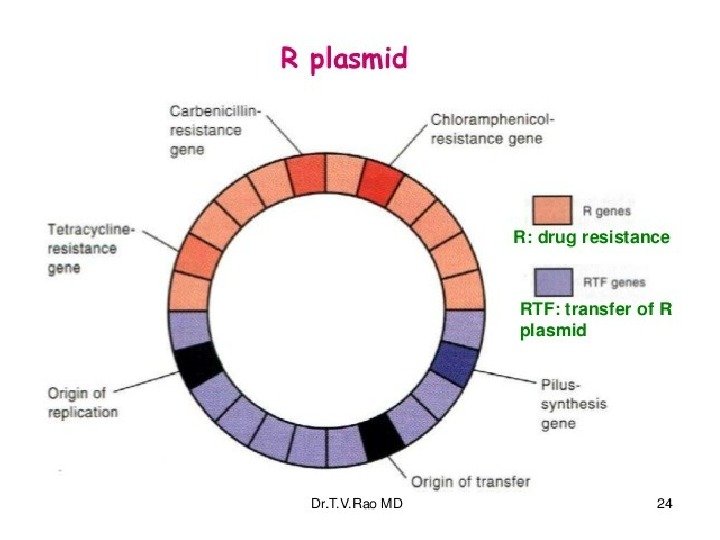
 Виды плазмид
Виды плазмид


 • Транспозиция обеспечивается ферментом – транспозазой. Ген, кодирующий этот фермент, входит в состав всех мобильных генетических элементов. • Транспозаза обладает эндонуклеазной и лигазной функцией: она разрезает ДНК по краям мобильного генетического элемента (эндонуклеазная функция) и сшивает его с разрывом ДНК в новом месте (лигазная функция). • В некоторых случаях транспозиция сопровождается удвоением мобильных генетических элементов и перемещением копии в другое место.
• Транспозиция обеспечивается ферментом – транспозазой. Ген, кодирующий этот фермент, входит в состав всех мобильных генетических элементов. • Транспозаза обладает эндонуклеазной и лигазной функцией: она разрезает ДНК по краям мобильного генетического элемента (эндонуклеазная функция) и сшивает его с разрывом ДНК в новом месте (лигазная функция). • В некоторых случаях транспозиция сопровождается удвоением мобильных генетических элементов и перемещением копии в другое место.
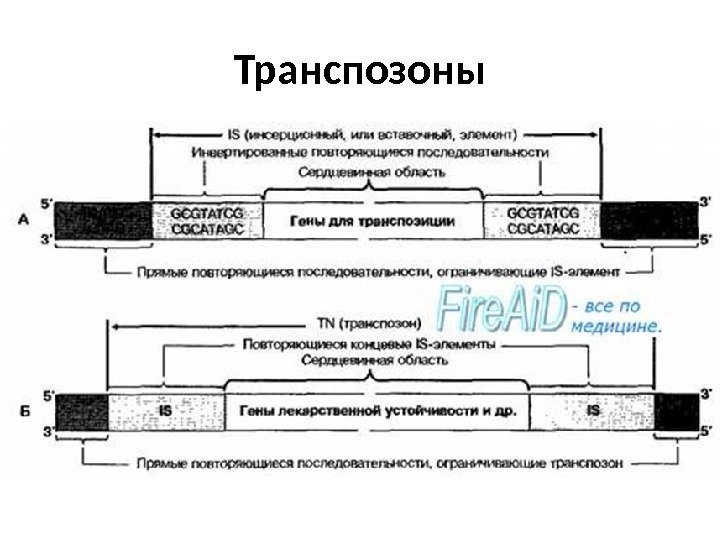
 Транспозоны
Транспозоны
 Перенос транспозонов • Перенос транспозонов осуществляется консервативным или репликативным механизмом. • Консервативный перенос происходит путем вырезания транспозона из одного участка и транспозицией в другой без увеличения количества копий, при этом участок ДНК, откуда вырезается транспозон, утрачивает свои функции. • При репликативном способе переноса синтезированная копия транспозона перемещается в новое место, при этом механизме увеличивается количество копий.
Перенос транспозонов • Перенос транспозонов осуществляется консервативным или репликативным механизмом. • Консервативный перенос происходит путем вырезания транспозона из одного участка и транспозицией в другой без увеличения количества копий, при этом участок ДНК, откуда вырезается транспозон, утрачивает свои функции. • При репликативном способе переноса синтезированная копия транспозона перемещается в новое место, при этом механизме увеличивается количество копий.
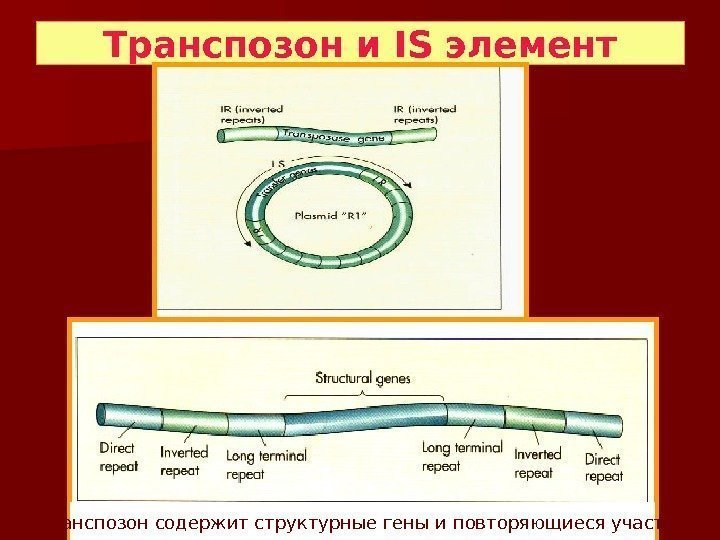
 Транспозон и IS элемент Транспозон содержит структурные гены и повторяющиеся участки
Транспозон и IS элемент Транспозон содержит структурные гены и повторяющиеся участки
 1. Регуляторная. 2. Кодирующая. 3. Индуцируют мутации. 4. Вызывают хромосомные аберрации. Функции транспозонов
1. Регуляторная. 2. Кодирующая. 3. Индуцируют мутации. 4. Вызывают хромосомные аберрации. Функции транспозонов
 1. Координирующая: взаимодействие транспозонов, плазмид, умеренных фагов между собой и хромосомой бактерии, обеспечивая их репликацию. 2. Регуляторная: вызывают инактива-цию генов, или служат промоторами (участки ДНК, которые регулируют экспрессию клеточных генов). 3. Индуцируют мутации по типу делеции или инверсии Функции IS-элементов
1. Координирующая: взаимодействие транспозонов, плазмид, умеренных фагов между собой и хромосомой бактерии, обеспечивая их репликацию. 2. Регуляторная: вызывают инактива-цию генов, или служат промоторами (участки ДНК, которые регулируют экспрессию клеточных генов). 3. Индуцируют мутации по типу делеции или инверсии Функции IS-элементов
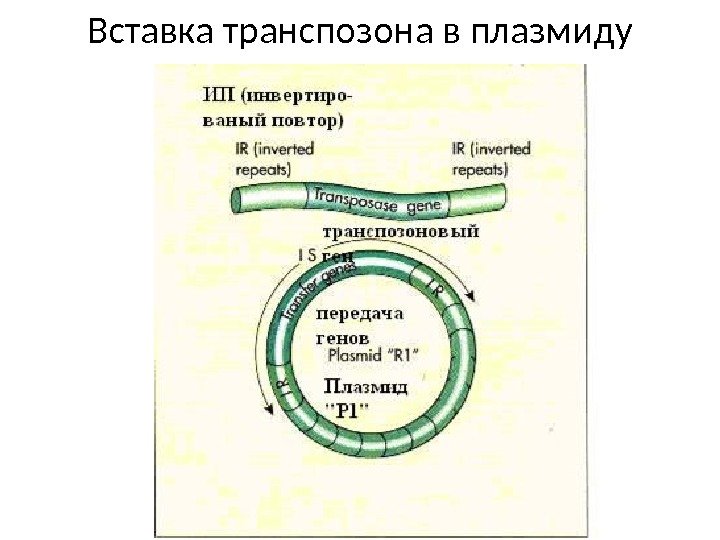
 Вставка транспозона в плазмиду
Вставка транспозона в плазмиду
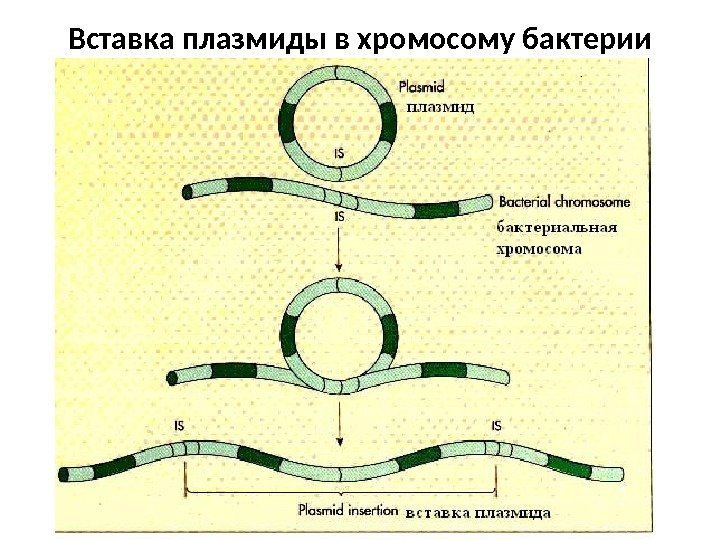
 Вставка плазмиды в хромосому бактерии
Вставка плазмиды в хромосому бактерии
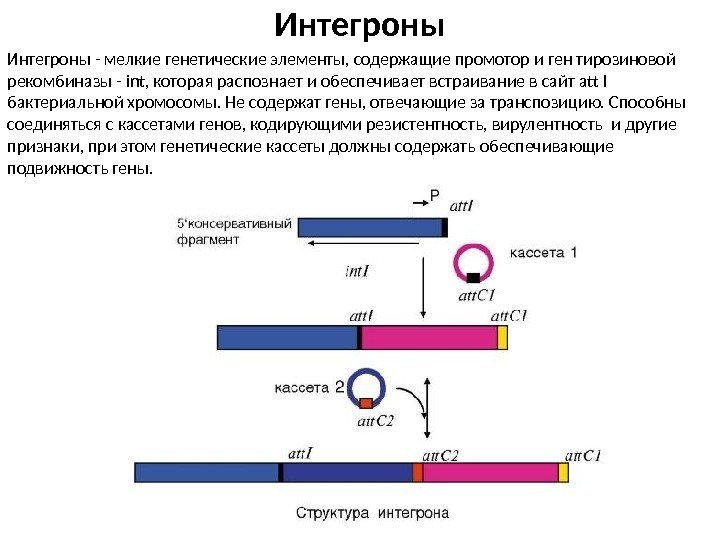
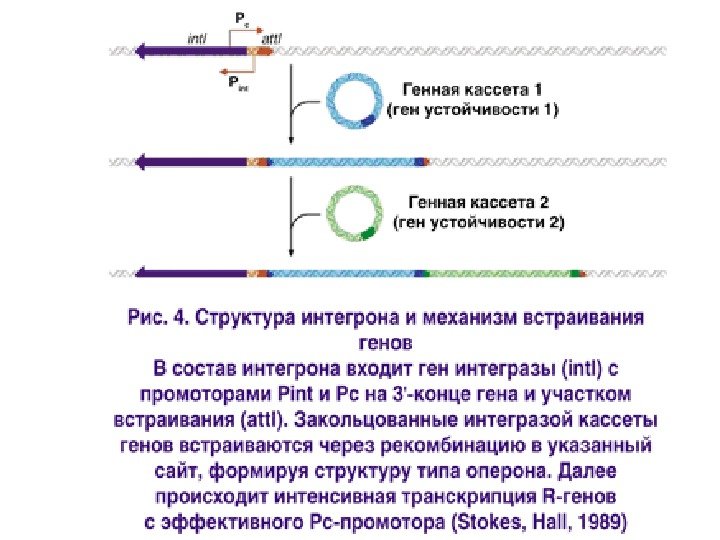
 Интегроны — мелкие генетические элементы, содержащие промотор и ген тирозиновой рекомбиназы — int, которая распознает и обеспечивает встраивание в сайт att I бактериальной хромосомы. Не содержат гены, отвечающие за транспозицию. Способны соединяться с кассетами генов, кодирующими резистентность, вирулентность и другие признаки, при этом генетические кассеты должны содержать обеспечивающие подвижность гены.
Интегроны — мелкие генетические элементы, содержащие промотор и ген тирозиновой рекомбиназы — int, которая распознает и обеспечивает встраивание в сайт att I бактериальной хромосомы. Не содержат гены, отвечающие за транспозицию. Способны соединяться с кассетами генов, кодирующими резистентность, вирулентность и другие признаки, при этом генетические кассеты должны содержать обеспечивающие подвижность гены.
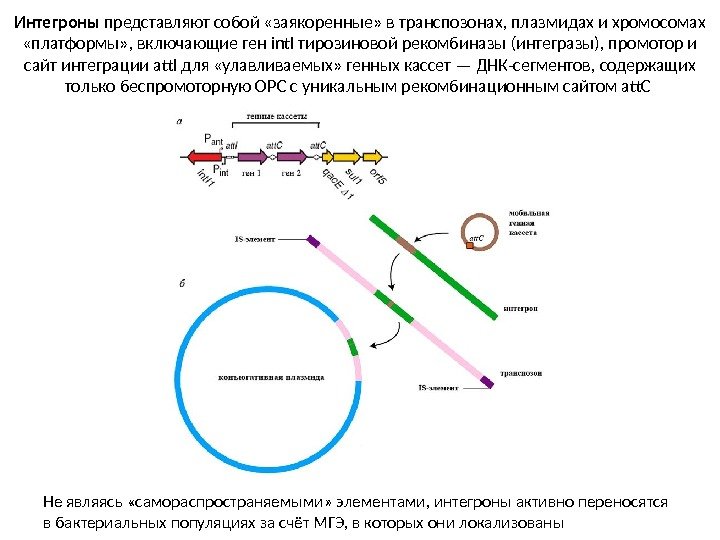
 Интегроны представляют собой «заякоренные» в транспозонах, плазмидах и хромосомах «платформы» , включающие ген int. I тирозиновой рекомбиназы (интегразы), промотор и сайт интеграции att. I для «улавливаемых» генных кассет — ДНК-сегментов, содержащих только беспромоторную ОРС с уникальным рекомбинационным сайтом att. C Не являясь «самораспространяемыми» элементами, интегроны активно переносятся в бактериальных популяциях за счёт МГЭ, в которых они локализованы
Интегроны представляют собой «заякоренные» в транспозонах, плазмидах и хромосомах «платформы» , включающие ген int. I тирозиновой рекомбиназы (интегразы), промотор и сайт интеграции att. I для «улавливаемых» генных кассет — ДНК-сегментов, содержащих только беспромоторную ОРС с уникальным рекомбинационным сайтом att. C Не являясь «самораспространяемыми» элементами, интегроны активно переносятся в бактериальных популяциях за счёт МГЭ, в которых они локализованы


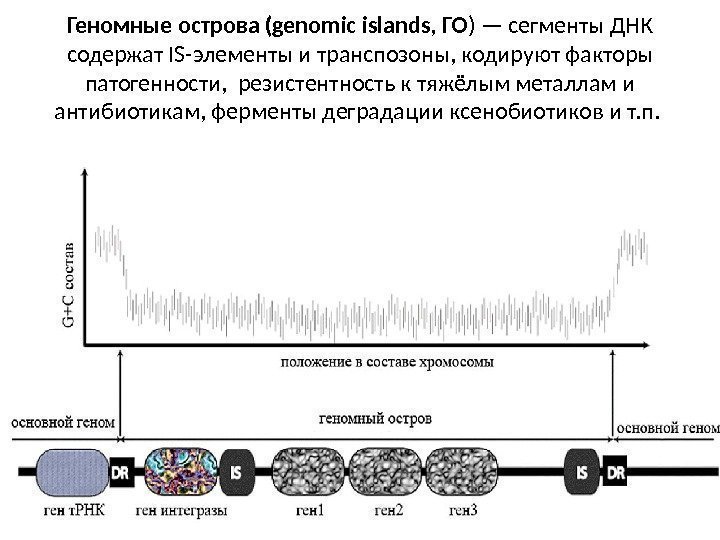
 Геномные острова (genomic islands, ГО ) — сегменты ДНК содержат IS-элементы и транспозоны, кодируют факторы патогенности, резистентность к тяжёлым металлам и антибиотикам, ферменты деградации ксенобиотиков и т. п.
Геномные острова (genomic islands, ГО ) — сегменты ДНК содержат IS-элементы и транспозоны, кодируют факторы патогенности, резистентность к тяжёлым металлам и антибиотикам, ферменты деградации ксенобиотиков и т. п.
 3. Виды изменчивости бактерий: ФЕНОТИПИЧЕСКАЯ(модификационная, адаптивная) – ИЗМЕНЕНИЕ ВНЕШНИХ ПРИЗНАКОВ И ХАРАКТЕРИСТИК , не затрагивающее геном. Механизм основан на регуляции оперонов. ГЕНОТИПИЧЕСКАЯ — изменение генов в результате мутаций и/или рекомбинаций. Имеет 2 варианта: -мутационная -рекомбинационная
3. Виды изменчивости бактерий: ФЕНОТИПИЧЕСКАЯ(модификационная, адаптивная) – ИЗМЕНЕНИЕ ВНЕШНИХ ПРИЗНАКОВ И ХАРАКТЕРИСТИК , не затрагивающее геном. Механизм основан на регуляции оперонов. ГЕНОТИПИЧЕСКАЯ — изменение генов в результате мутаций и/или рекомбинаций. Имеет 2 варианта: -мутационная -рекомбинационная
 Мутационная изменчивость • Мутации • Мутагены • Репарации • Мутанты
Мутационная изменчивость • Мутации • Мутагены • Репарации • Мутанты
 По происхождению: спонтанные индуцированные По локализации: нуклеоидные цитоплазматические По количеству генов, которые мутировали: генные хромосомные По величине: точковые. Мутации
По происхождению: спонтанные индуцированные По локализации: нуклеоидные цитоплазматические По количеству генов, которые мутировали: генные хромосомные По величине: точковые. Мутации
 Види плазмід делеция инсерция (вставка) замена: транзиция (пуриновая основа – на пуриновую, пиримидиновая – на пиримидиновую) трансверзия (пуриновая основа – на пиримидиновую и наоборот) Точковые мутации :
Види плазмід делеция инсерция (вставка) замена: транзиция (пуриновая основа – на пуриновую, пиримидиновая – на пиримидиновую) трансверзия (пуриновая основа – на пиримидиновую и наоборот) Точковые мутации :
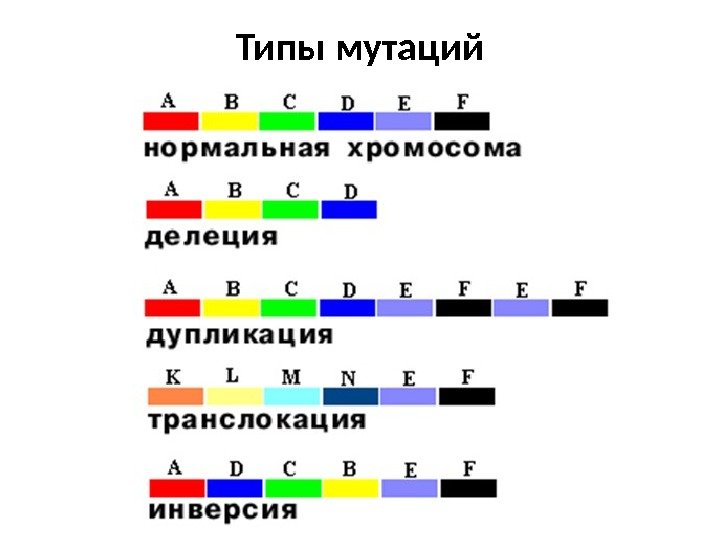
 Типы мутаций
Типы мутаций


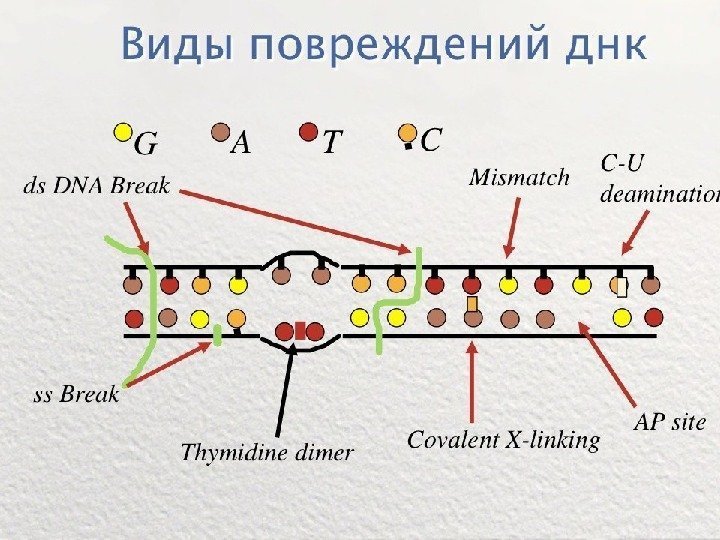
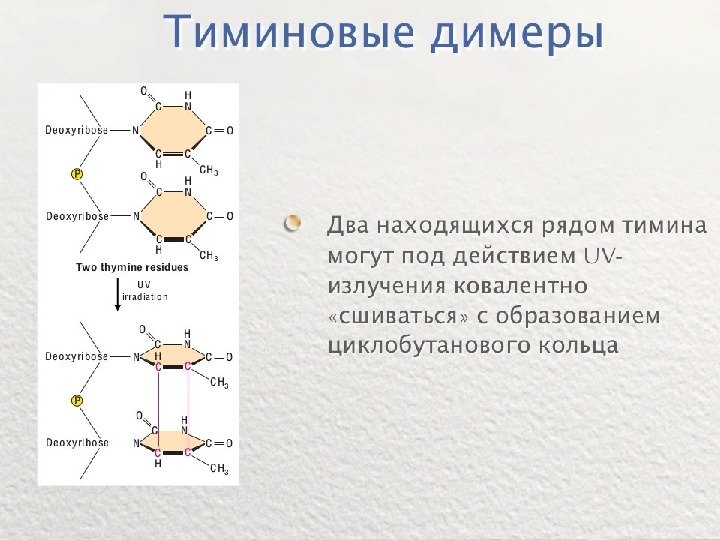
 Классификация мутагенов Физические: • 1. УФО (л-2600 А) –образуются димеры тимина, замена оснований • 2. Ионизирующее облучение (рентгеновское, гамма-лучи) Химические: • 1. Азотистая кислота (самый доступный и безопасный) • 2. N-нитрозометилмочевина – супермутаген, канцероген • 3. Этилметансульфонат • 4. Акридины • 5. Нитрозогуанидин • 6. Аналоги оснований (5 -бромурацил, 2 -аминопурин) • Ы 7. Лекарственные препараты (нитрофураны, некоторые антибиотики Биологические: вирусы , фаги, IS-элементы
Классификация мутагенов Физические: • 1. УФО (л-2600 А) –образуются димеры тимина, замена оснований • 2. Ионизирующее облучение (рентгеновское, гамма-лучи) Химические: • 1. Азотистая кислота (самый доступный и безопасный) • 2. N-нитрозометилмочевина – супермутаген, канцероген • 3. Этилметансульфонат • 4. Акридины • 5. Нитрозогуанидин • 6. Аналоги оснований (5 -бромурацил, 2 -аминопурин) • Ы 7. Лекарственные препараты (нитрофураны, некоторые антибиотики Биологические: вирусы , фаги, IS-элементы



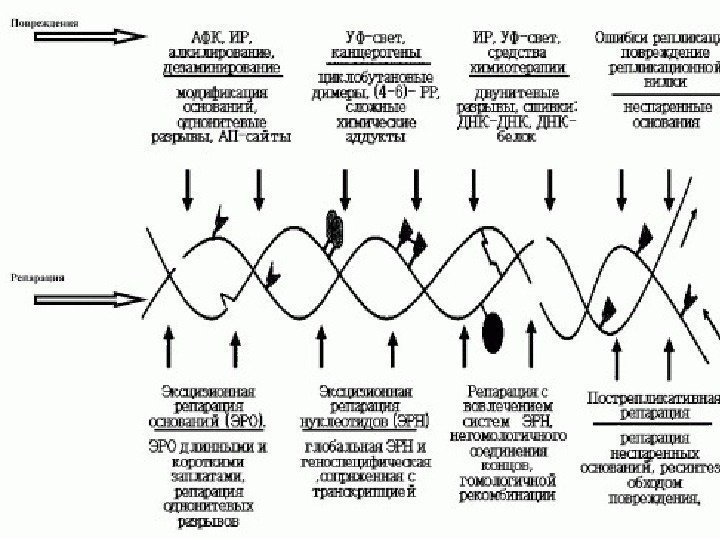
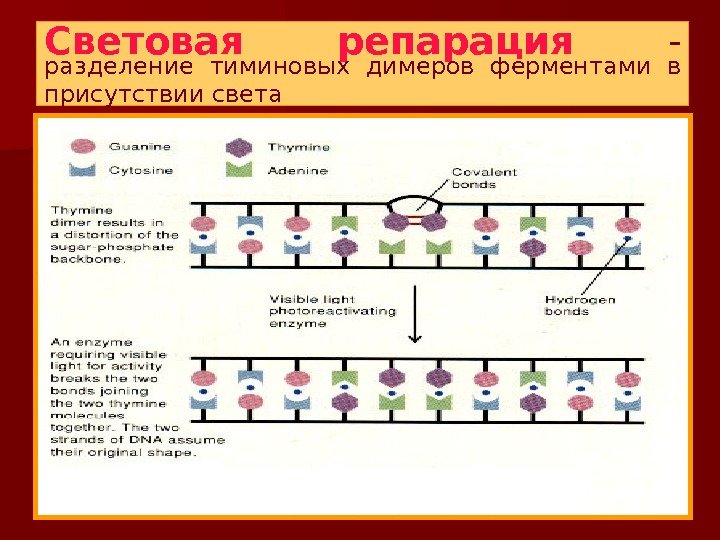
 Световая репарация — разделение тиминовых димеров ферментами в присутствии света
Световая репарация — разделение тиминовых димеров ферментами в присутствии света
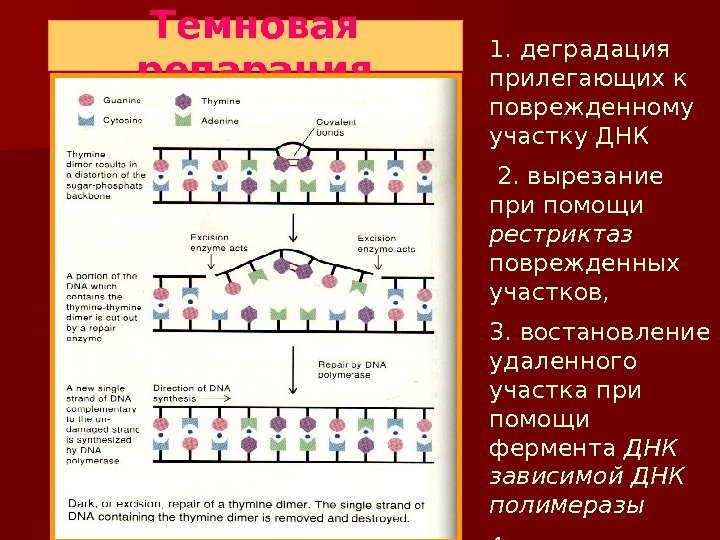
 Темновая репарация 1. деградация прилегающих к поврежденному участку ДНК 2. вырезание при помощи рестриктаз поврежденных участков, 3. востановление удаленного участка при помощи фермента ДНК зависимой ДНК полимеразы 4. сшивание ДНК- лигазами
Темновая репарация 1. деградация прилегающих к поврежденному участку ДНК 2. вырезание при помощи рестриктаз поврежденных участков, 3. востановление удаленного участка при помощи фермента ДНК зависимой ДНК полимеразы 4. сшивание ДНК- лигазами
 SOS — система репарации Реакция клетки на множественные повреждения с участием продуктов генов rec. A и lex. A. Участки с мутациями переводятся в неактивное состояние, а их роль исполняет неповрежденный участок ДНК.
SOS — система репарации Реакция клетки на множественные повреждения с участием продуктов генов rec. A и lex. A. Участки с мутациями переводятся в неактивное состояние, а их роль исполняет неповрежденный участок ДНК.
 Типы мутантов бактерий • Морфологические(L-формы, потеря жгутиков ) • Культуральные (S и R формы колоний) • Биохимические(ферментативные и ауксотрофные) • Устойчивые к х/т препаратам • Повышенная или сниженная вирулентность
Типы мутантов бактерий • Морфологические(L-формы, потеря жгутиков ) • Культуральные (S и R формы колоний) • Биохимические(ферментативные и ауксотрофные) • Устойчивые к х/т препаратам • Повышенная или сниженная вирулентность
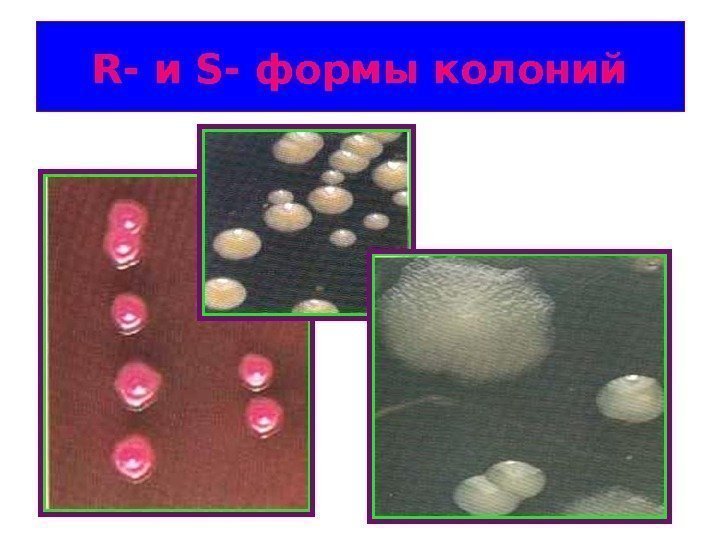
 R- и S- формы колоний
R- и S- формы колоний
 Свойства S-форм колоний микробов Клетки нормальной морфологии Диффузное помутнение бульона У подвижных видов есть жгутики У капсульных вариантов есть капсулы Биохимически более активны Полноценны в антигенном отношении У патогенных видов – вирулентны Выделяют в остром периоде заболевания Чувствительны к бактериофагам Менее чувствительны к фагоцитозу
Свойства S-форм колоний микробов Клетки нормальной морфологии Диффузное помутнение бульона У подвижных видов есть жгутики У капсульных вариантов есть капсулы Биохимически более активны Полноценны в антигенном отношении У патогенных видов – вирулентны Выделяют в остром периоде заболевания Чувствительны к бактериофагам Менее чувствительны к фагоцитозу
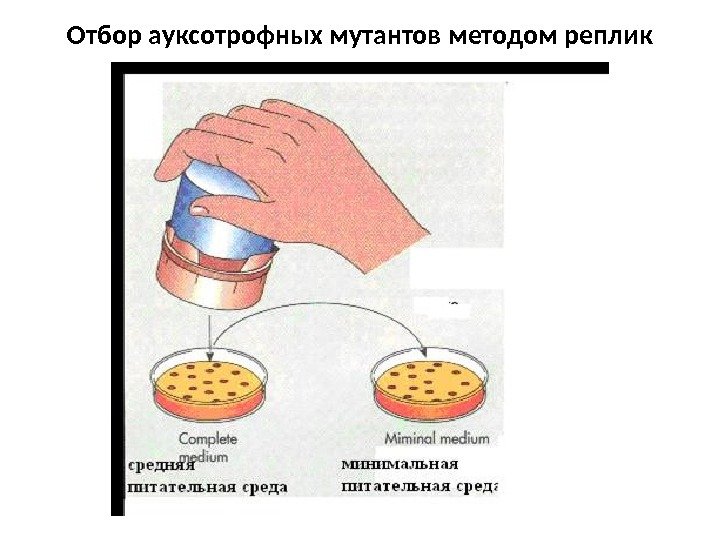
 Методы выявления мутантов По разнице скорости роста (посев на минимальную среду) Различная способность к выживанию Метод реплик Ледерберга
Методы выявления мутантов По разнице скорости роста (посев на минимальную среду) Различная способность к выживанию Метод реплик Ледерберга
 Отбор ауксотрофных мутантов методом реплик
Отбор ауксотрофных мутантов методом реплик
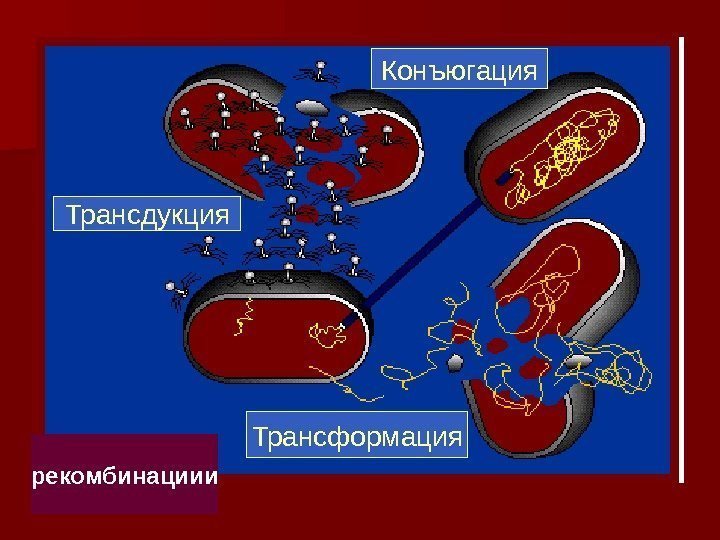
 Генетические рекомбинации Выделяют три основных вида генетических рекомбинаций : • трансформация • трансдукция • конъюгация
Генетические рекомбинации Выделяют три основных вида генетических рекомбинаций : • трансформация • трансдукция • конъюгация
 рекомбинациии Трансдукция Конъюгация Трансформация
рекомбинациии Трансдукция Конъюгация Трансформация
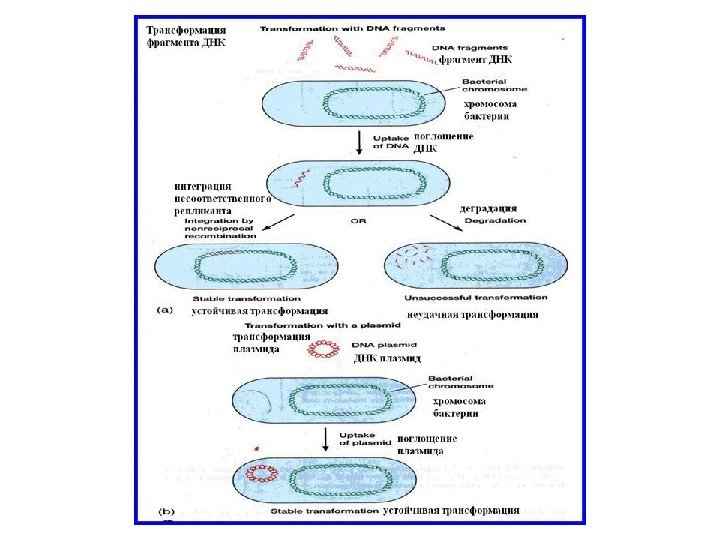
 Трансформация – передача генетического материала от донора реципиенту при помощи изолированной ДНК. Трансдукция – передача генетического материала от донора реципиенту при помощи бактериофага. Конъюгация — это передача генетического материала от бактерии-донора к бактерии-реципиенту путем непосредственного контакта.
Трансформация – передача генетического материала от донора реципиенту при помощи изолированной ДНК. Трансдукция – передача генетического материала от донора реципиенту при помощи бактериофага. Конъюгация — это передача генетического материала от бактерии-донора к бактерии-реципиенту путем непосредственного контакта.
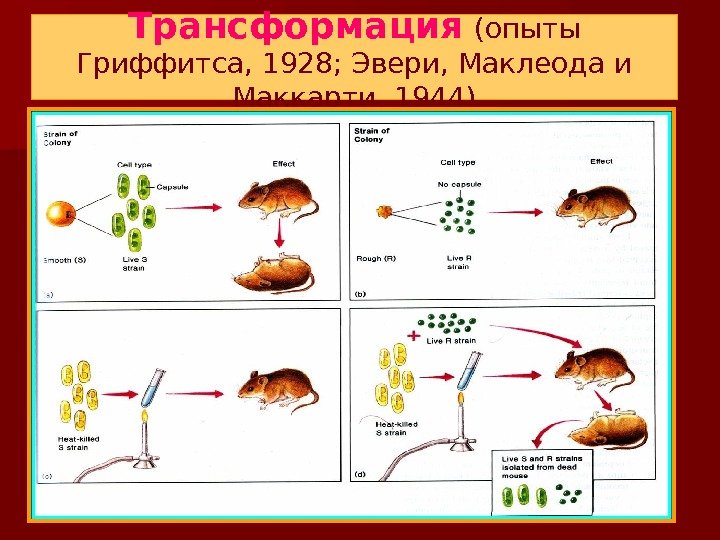
 Трансформация ( опыты Гриффитса, 1928; Эвери, Маклеода и Маккарти, 1944)
Трансформация ( опыты Гриффитса, 1928; Эвери, Маклеода и Маккарти, 1944)
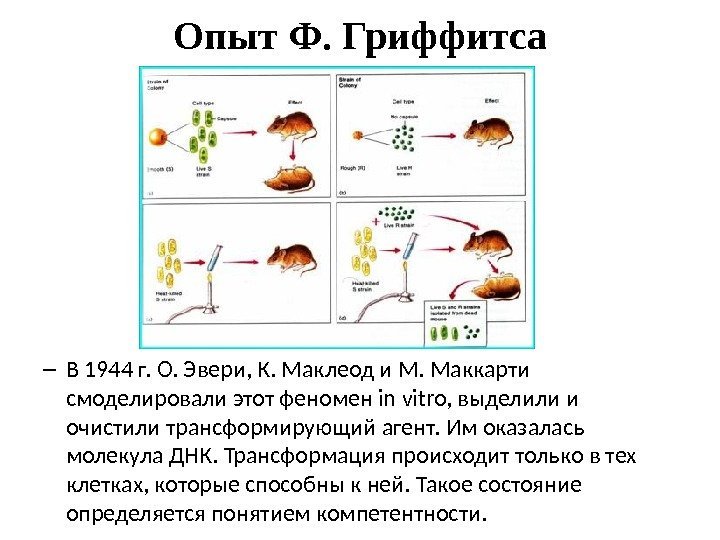
 Опыт Ф. Гриффитса – В 1944 г. О. Эвери, К. Маклеод и М. Маккарти смоделировали этот феномен in vitro, выделили и очистили трансформирующий агент. Им оказалась молекула ДНК. Трансформация происходит только в тех клетках, которые способны к ней. Такое состояние определяется понятием компетентности.
Опыт Ф. Гриффитса – В 1944 г. О. Эвери, К. Маклеод и М. Маккарти смоделировали этот феномен in vitro, выделили и очистили трансформирующий агент. Им оказалась молекула ДНК. Трансформация происходит только в тех клетках, которые способны к ней. Такое состояние определяется понятием компетентности.

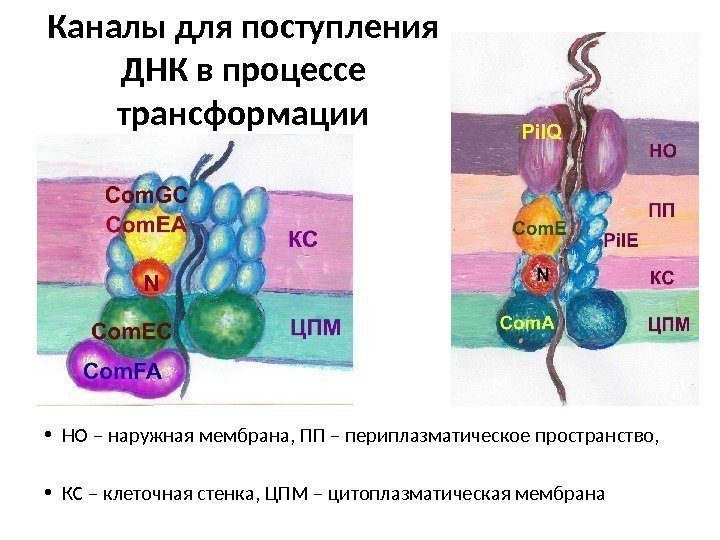
 Каналы для поступления ДНК в процессе трансформации • НО – наружная мембрана, ПП – периплазматическое пространство, • КС – клеточная стенка, ЦПМ – цитоплазматическая мембрана
Каналы для поступления ДНК в процессе трансформации • НО – наружная мембрана, ПП – периплазматическое пространство, • КС – клеточная стенка, ЦПМ – цитоплазматическая мембрана
 ТРАНСДУКЦИЯ (Циндер и Ледерберг, 1952) Виды: общая (генерализированная) специфическая абортивная Вызывают умеренные, дефектные фаги
ТРАНСДУКЦИЯ (Циндер и Ледерберг, 1952) Виды: общая (генерализированная) специфическая абортивная Вызывают умеренные, дефектные фаги
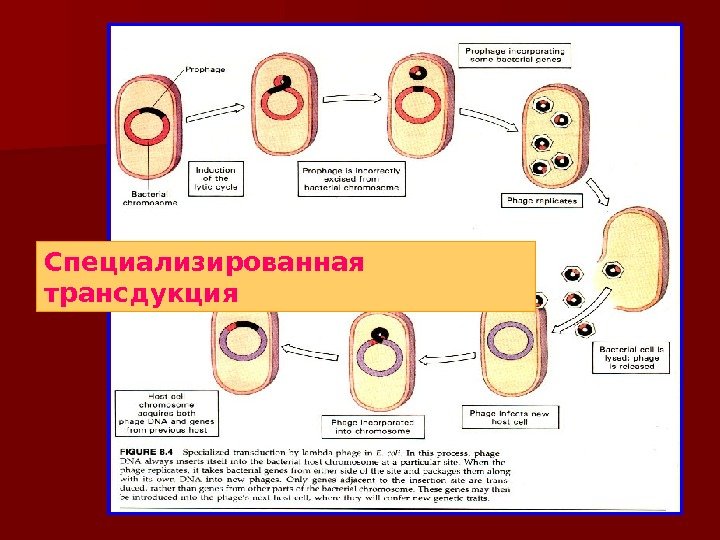
 Специализированная трансдукция
Специализированная трансдукция
 ОТЛИЧИЯ ТРАНСДУКЦИИ и ФАГОВОЙ КОНВЕРСИИ Трансдукция – перенос генов из клетки-донора в клетку-реципиент при помощи умеренного бактериофага Фаговая конверсия — э кспрeссия в клетке генома самого бактериофага (Corynebacterium diphtheriae, Clostridium botulinum, Staphylococcus spp. , Salmonella spp. )
ОТЛИЧИЯ ТРАНСДУКЦИИ и ФАГОВОЙ КОНВЕРСИИ Трансдукция – перенос генов из клетки-донора в клетку-реципиент при помощи умеренного бактериофага Фаговая конверсия — э кспрeссия в клетке генома самого бактериофага (Corynebacterium diphtheriae, Clostridium botulinum, Staphylococcus spp. , Salmonella spp. )


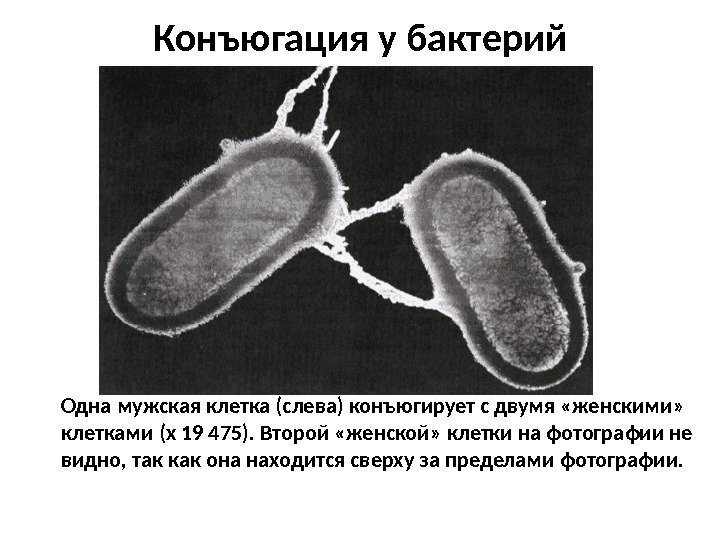
 Конъюгация у бактерий Одна мужская клетка (слева) конъюгирует с двумя «женскими» клетками (х 19 475). Второй «женской» клетки на фотографии не видно, так как она находится сверху за пределами фотографии.
Конъюгация у бактерий Одна мужская клетка (слева) конъюгирует с двумя «женскими» клетками (х 19 475). Второй «женской» клетки на фотографии не видно, так как она находится сверху за пределами фотографии.
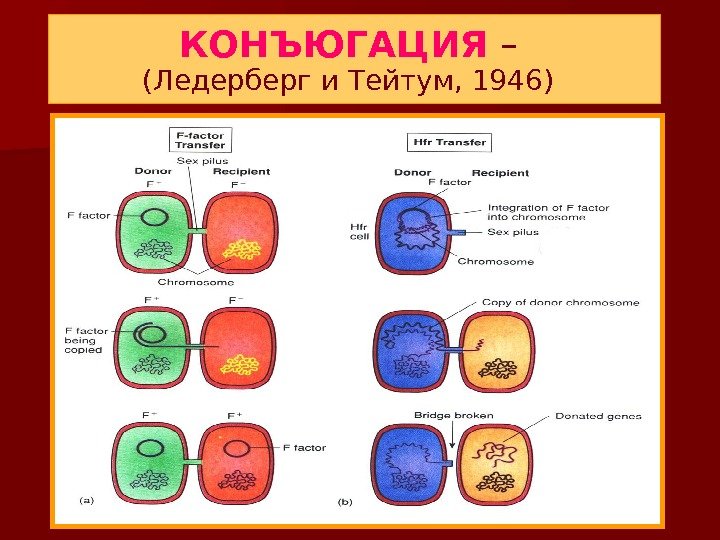
 КОНЪЮГАЦИЯ – (Ледерберг и Тейтум, 1946)
КОНЪЮГАЦИЯ – (Ледерберг и Тейтум, 1946)
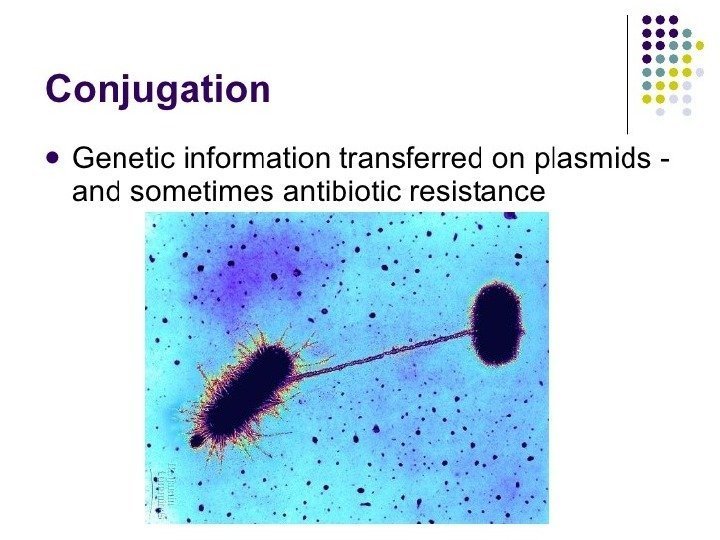
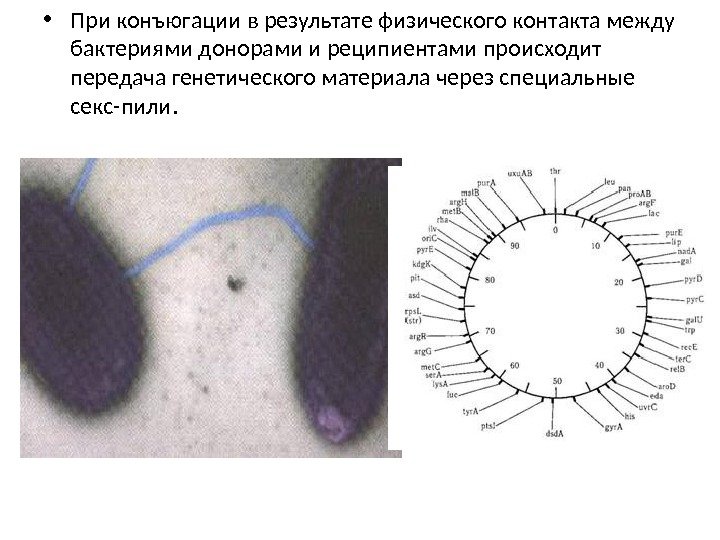
 • При конъюгации в результате физического контакта между бактериями донорами и реципиентами происходит передача генетического материала через специальные секс-пили.
• При конъюгации в результате физического контакта между бактериями донорами и реципиентами происходит передача генетического материала через специальные секс-пили.
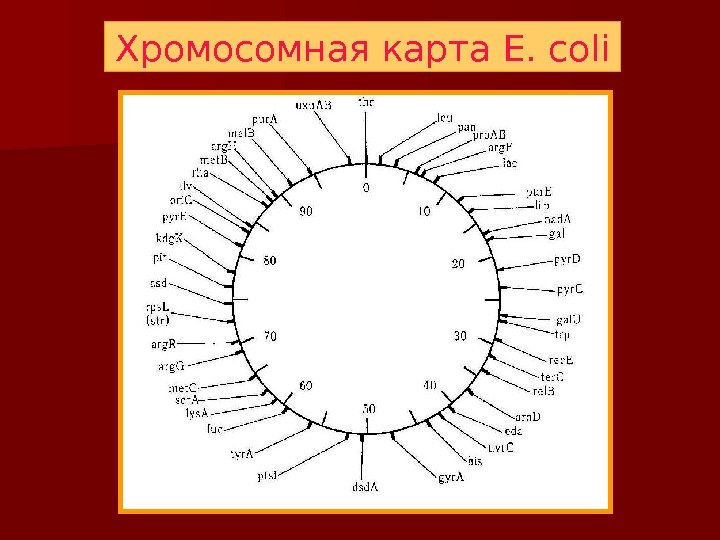
 Хромосомная карта E. coli
Хромосомная карта E. coli
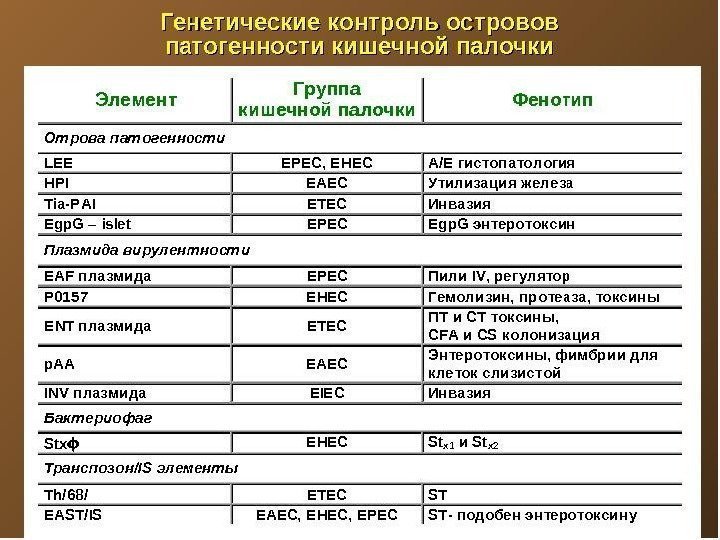
 Генетика патогенности
Генетика патогенности
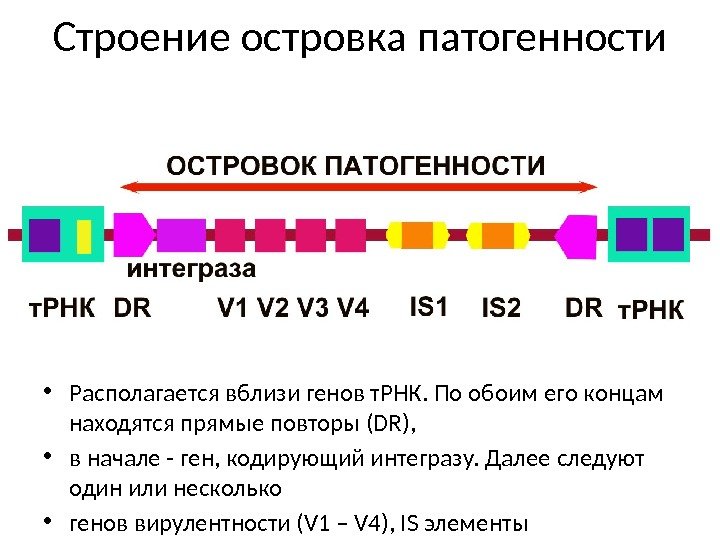
 Строение островка патогенности • Располагается вблизи генов т. РНК. По обоим его концам находятся прямые повторы (DR), • в начале — ген, кодирующий интегразу. Далее следуют один или несколько • генов вирулентности (V 1 – V 4), IS элементы
Строение островка патогенности • Располагается вблизи генов т. РНК. По обоим его концам находятся прямые повторы (DR), • в начале — ген, кодирующий интегразу. Далее следуют один или несколько • генов вирулентности (V 1 – V 4), IS элементы
 Островки патогенности – разновидность генетических островков, содержащих от одного до нескольких десятков генов, кодирующих факторы патогенности, и способных к одновременной горизонтальной внутривидовой и межвидовой передаче • Островки патогенности присутствуют только у вирулентных микроорганизмов в составе плазмид или бактериальной хромосомы, и отсутствуют у непатогенных штаммов того же или близкородственных видов. • Впервые ОП были описаны в 1980 г. у уропатогенных E. coli (UPEC) Йоргом Хакером и его коллегами из Вирцбургского университета, Германия. Они разработали концепцию «мозаичного» строения генома бактериальных патогенов, который включает относительно древние и стабильные участки ДНК и разбросанные среди них островки патогенности, приобретенные путем горизонтальной передачи. • Островки патогенности были найдены не только у E. coli, но и у широкого спектра патогенных бактерий. У грамположительных микроорганизмов роль островков патогенности играют генетические кассеты или кластеры генов.
Островки патогенности – разновидность генетических островков, содержащих от одного до нескольких десятков генов, кодирующих факторы патогенности, и способных к одновременной горизонтальной внутривидовой и межвидовой передаче • Островки патогенности присутствуют только у вирулентных микроорганизмов в составе плазмид или бактериальной хромосомы, и отсутствуют у непатогенных штаммов того же или близкородственных видов. • Впервые ОП были описаны в 1980 г. у уропатогенных E. coli (UPEC) Йоргом Хакером и его коллегами из Вирцбургского университета, Германия. Они разработали концепцию «мозаичного» строения генома бактериальных патогенов, который включает относительно древние и стабильные участки ДНК и разбросанные среди них островки патогенности, приобретенные путем горизонтальной передачи. • Островки патогенности были найдены не только у E. coli, но и у широкого спектра патогенных бактерий. У грамположительных микроорганизмов роль островков патогенности играют генетические кассеты или кластеры генов.

 Недавняя вспышка энтероколита в Европе, вызванная STEС (редкий энтероагрегативный С 227 -11 штамм Escherichia coli O 104: H 4, продуцирующий шига-токсин 2 -го типа), показала колоссальное значение горизонтального переноса детерминант патогенности при помощи конъюгативных плазмид. Даже незначительного количества попавших в пищеварительный тракт STEС оказывалось достаточно для запуска лавинообразного процесса обмена плазмидами между STEС и непатогенными E. coli кишечника, что приводило к продукции большого количества токсина и развитию тяжелого гемолитико-уремического синдрома. Гены, контролирующие синтез и высвобождение шига-токсина (stx. AB 2), находятся в области профага под контролем двух промоторов. Один из них, как оказалось, активируется ципрофлоксацином: добавление 25 нг/мл (рекомендованная терапевтическая концентрация в кишечнике) препарата в 80 раз повышает экспрессию данных генов (Rasko, 2011). Понятно, что лечение пациентов ципрофлоксацином резко отягощало течение болезни.
Недавняя вспышка энтероколита в Европе, вызванная STEС (редкий энтероагрегативный С 227 -11 штамм Escherichia coli O 104: H 4, продуцирующий шига-токсин 2 -го типа), показала колоссальное значение горизонтального переноса детерминант патогенности при помощи конъюгативных плазмид. Даже незначительного количества попавших в пищеварительный тракт STEС оказывалось достаточно для запуска лавинообразного процесса обмена плазмидами между STEС и непатогенными E. coli кишечника, что приводило к продукции большого количества токсина и развитию тяжелого гемолитико-уремического синдрома. Гены, контролирующие синтез и высвобождение шига-токсина (stx. AB 2), находятся в области профага под контролем двух промоторов. Один из них, как оказалось, активируется ципрофлоксацином: добавление 25 нг/мл (рекомендованная терапевтическая концентрация в кишечнике) препарата в 80 раз повышает экспрессию данных генов (Rasko, 2011). Понятно, что лечение пациентов ципрофлоксацином резко отягощало течение болезни.

 Детерминанты вирулентности, кодируемые ОП ОП могут содержать гены, детерминирующие признаки устойчивости к антибиотикам, адгезины, экзо- и эндотоксины, суперантигены, сидерофоры, секреторные системы. Детерминанты вирулентности, кодируемые ОП: • 1. Факторы адгезии и колонизации • Энтеропатогенные и энтерогеморрагические E. coli, вызывающие острые кишечные инфекции, имеют островок патогенности, кодирующий белок адгезии Tir-протеин встраивается в мембрану энтероцитов, взаимодействует с белком-интимином на поверхности энтеропатогенных и энтерогеморрагических E. coli, что приводит к адгезии возбудителей на энтероцитах. • 2. Факторы инвазии. ОП сальмонелл и шигелл кодируют инвазины, впрыскиваемые в клетку-мишень, в результате чего происходит перестройка цитоскелета с образованием пальцевидных выпячиваний на поверхности кишечного эпителия, которые смыкаются вокруг патогена с формированием эндосомы. • 3. Белки секреторных систем. Важной особенностью многих патогенных микроорганизмов является способность целенаправленно доставлять детерминанты вирулентности в клетку-мишень. Грамотрицательные патогены Salmonella spp. , E. coli, Bordetella pertussis, Pseudomonas aeruginosa, Helicobacter pylori, Brucella spp. , C hlamyophila psitaci, Legionella spp. , Yersinia pests имеют ОП, кодирующие системы секреции факторов патогенности I – V типов. • 4. Факторы, способствующие ускользанию от действия иммунной системы ивнутриклеточной бактерицидности. Шигеллы и листерии, находясь внутри клетки-хозяина в фагосоме, лизируют фагосомальную мембрану и поступают в цитоплазму, где становятся недоступными разрушению. Salmonella typhimurium, Mycobacterium tuberculosis, Chlamydia spp. , Legionella pneumophilia продуцируют белки, препятствующие слиянию лизосом с фагосомами, что предотвращает переваривание этих микроорганизмов. Белок Sip. B, кодируемый ОП-1 Salmonella spp. , вызывает апоптоз макрофагов. • 6. Систему сидерофоров. Способность конкурировать за питательные вещества является существенным аспектом патогенеза. Сидерофоры — белки, связывающие ионы железа и необходимые для его перемещения в бактериальную клетку. Ионы железа важны для проявления вирулентных свойств бактериями. Yersinia spp. синтезируют иерсинобактин, S. fexneri – аэробактин, S. typhimurium — Sit 1, S. pneumoniae — Рit 2.
Детерминанты вирулентности, кодируемые ОП ОП могут содержать гены, детерминирующие признаки устойчивости к антибиотикам, адгезины, экзо- и эндотоксины, суперантигены, сидерофоры, секреторные системы. Детерминанты вирулентности, кодируемые ОП: • 1. Факторы адгезии и колонизации • Энтеропатогенные и энтерогеморрагические E. coli, вызывающие острые кишечные инфекции, имеют островок патогенности, кодирующий белок адгезии Tir-протеин встраивается в мембрану энтероцитов, взаимодействует с белком-интимином на поверхности энтеропатогенных и энтерогеморрагических E. coli, что приводит к адгезии возбудителей на энтероцитах. • 2. Факторы инвазии. ОП сальмонелл и шигелл кодируют инвазины, впрыскиваемые в клетку-мишень, в результате чего происходит перестройка цитоскелета с образованием пальцевидных выпячиваний на поверхности кишечного эпителия, которые смыкаются вокруг патогена с формированием эндосомы. • 3. Белки секреторных систем. Важной особенностью многих патогенных микроорганизмов является способность целенаправленно доставлять детерминанты вирулентности в клетку-мишень. Грамотрицательные патогены Salmonella spp. , E. coli, Bordetella pertussis, Pseudomonas aeruginosa, Helicobacter pylori, Brucella spp. , C hlamyophila psitaci, Legionella spp. , Yersinia pests имеют ОП, кодирующие системы секреции факторов патогенности I – V типов. • 4. Факторы, способствующие ускользанию от действия иммунной системы ивнутриклеточной бактерицидности. Шигеллы и листерии, находясь внутри клетки-хозяина в фагосоме, лизируют фагосомальную мембрану и поступают в цитоплазму, где становятся недоступными разрушению. Salmonella typhimurium, Mycobacterium tuberculosis, Chlamydia spp. , Legionella pneumophilia продуцируют белки, препятствующие слиянию лизосом с фагосомами, что предотвращает переваривание этих микроорганизмов. Белок Sip. B, кодируемый ОП-1 Salmonella spp. , вызывает апоптоз макрофагов. • 6. Систему сидерофоров. Способность конкурировать за питательные вещества является существенным аспектом патогенеза. Сидерофоры — белки, связывающие ионы железа и необходимые для его перемещения в бактериальную клетку. Ионы железа важны для проявления вирулентных свойств бактериями. Yersinia spp. синтезируют иерсинобактин, S. fexneri – аэробактин, S. typhimurium — Sit 1, S. pneumoniae — Рit 2.
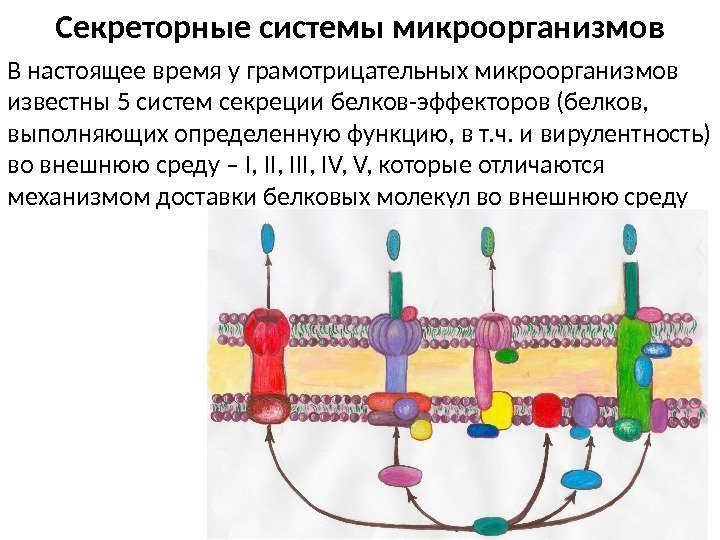
 Секреторные системы микроорганизмов В настоящее время у грамотрицательных микроорганизмов известны 5 систем секреции белков-эффекторов (белков, выполняющих определенную функцию, в т. ч. и вирулентность) во внешнюю среду – I, III, IV, V, которые отличаются механизмом доставки белковых молекул во внешнюю среду
Секреторные системы микроорганизмов В настоящее время у грамотрицательных микроорганизмов известны 5 систем секреции белков-эффекторов (белков, выполняющих определенную функцию, в т. ч. и вирулентность) во внешнюю среду – I, III, IV, V, которые отличаются механизмом доставки белковых молекул во внешнюю среду
 Сравнительная характеристика наиболее изученных секреторных систем I, III типов • Первый тип секреторной системы • E. coli секретирует -гемолизин, B. pertussis – аденилатциклазу, Pasteurella haemolytica – лейкоцидин, P. aeruginosa и Erwinia spp. – протеазы • Второй тип секреторной системы • Секретирует ферменты-токсины: Erwinia spp. – целлюлазу, P. aeruginosa – эластазу, экзотоксин А, фосфолипазу С, амилазу, протеазу • Третий тип секреторной системы • Shigella spp. секретирует белки Ipa B, Ipa. C, Ipg. D, Ipa. A, приводящие к перестройке цитоскелета и эндоцитозу шигелл в клетку-мишень. • Yersinia pestis секретируют Yop. B, Yop. H, препятствующие слиянию фагосом и лизосом, способствующие ускользанию от фагоцитоза и быстрому развитию септицемии
Сравнительная характеристика наиболее изученных секреторных систем I, III типов • Первый тип секреторной системы • E. coli секретирует -гемолизин, B. pertussis – аденилатциклазу, Pasteurella haemolytica – лейкоцидин, P. aeruginosa и Erwinia spp. – протеазы • Второй тип секреторной системы • Секретирует ферменты-токсины: Erwinia spp. – целлюлазу, P. aeruginosa – эластазу, экзотоксин А, фосфолипазу С, амилазу, протеазу • Третий тип секреторной системы • Shigella spp. секретирует белки Ipa B, Ipa. C, Ipg. D, Ipa. A, приводящие к перестройке цитоскелета и эндоцитозу шигелл в клетку-мишень. • Yersinia pestis секретируют Yop. B, Yop. H, препятствующие слиянию фагосом и лизосом, способствующие ускользанию от фагоцитоза и быстрому развитию септицемии
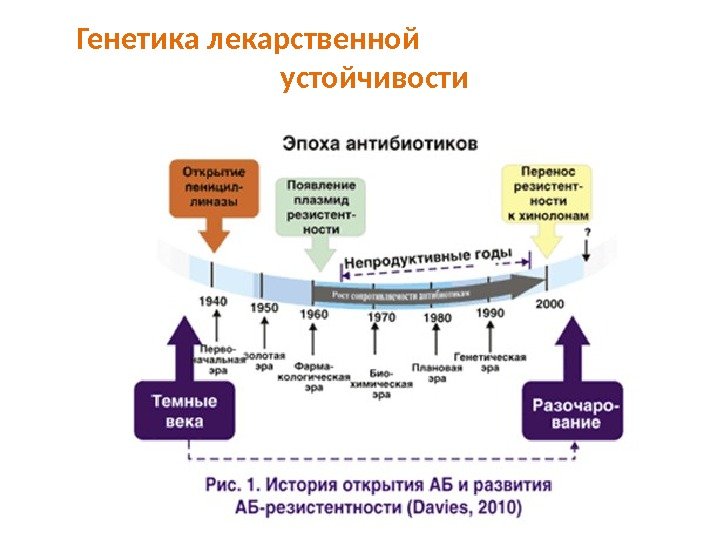
 Генетика лекарственной устойчивости
Генетика лекарственной устойчивости

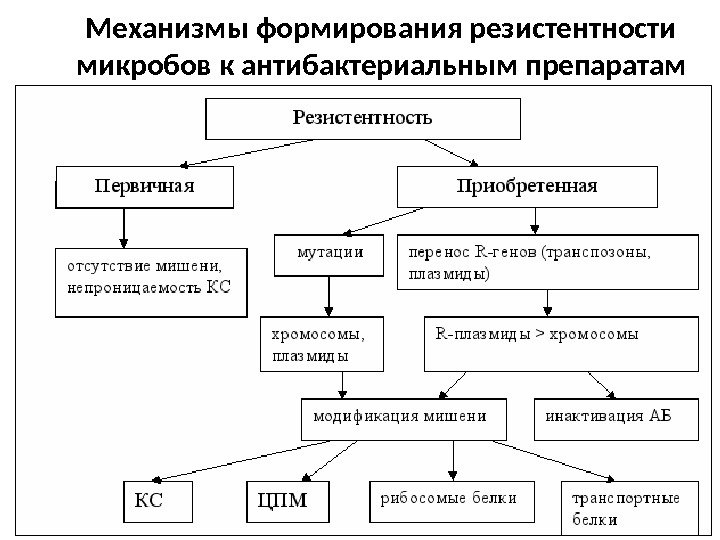
 Механизмы формирования резистентности микробов к антибактериальным препаратам
Механизмы формирования резистентности микробов к антибактериальным препаратам
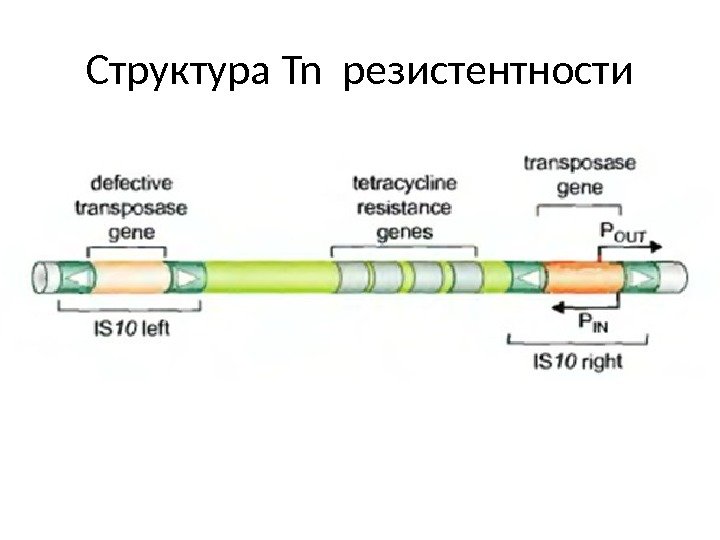
 Структура Tn резистентности
Структура Tn резистентности





 Супербактерии и суперрезистентность • Многие бактериальные патогены, ассоциированные с эпидемическими болезнями, эволюционировали в МЛР-формы. Среди них M. tuberculosis, возбудители нозокомиальных инфекций Acinetobacter baumanii, Burkholderia cepacia, Campylobacter jejuni, Citrobacter freundii, Clostridium difficile, Enterobacter spp. , Enterococcus faecium, Enterococcus faecalis, E. coli, Haemophilus infuenzae, Klebsiella pneumoniae, Proteus mirabilis, Pseudomonas aeruginosa, Salmonella spp. , Serrata spp. , S. aureus, S. epidermidis, Stenotrophomonas maltophilia, Streptococcus pneumoniae. • Термин «супербактерия» (superbug) относится к микробам, вызывающим инфекции с повышенным уровнем заболеваемости и смертности, обусловленным высокой устойчивостью к рекомендованным для их лечения АБ. Терапевтические возможности для заболеваний, вызванных этими бактериями, ограничены, а длительность и стоимость лечения увеличены.
Супербактерии и суперрезистентность • Многие бактериальные патогены, ассоциированные с эпидемическими болезнями, эволюционировали в МЛР-формы. Среди них M. tuberculosis, возбудители нозокомиальных инфекций Acinetobacter baumanii, Burkholderia cepacia, Campylobacter jejuni, Citrobacter freundii, Clostridium difficile, Enterobacter spp. , Enterococcus faecium, Enterococcus faecalis, E. coli, Haemophilus infuenzae, Klebsiella pneumoniae, Proteus mirabilis, Pseudomonas aeruginosa, Salmonella spp. , Serrata spp. , S. aureus, S. epidermidis, Stenotrophomonas maltophilia, Streptococcus pneumoniae. • Термин «супербактерия» (superbug) относится к микробам, вызывающим инфекции с повышенным уровнем заболеваемости и смертности, обусловленным высокой устойчивостью к рекомендованным для их лечения АБ. Терапевтические возможности для заболеваний, вызванных этими бактериями, ограничены, а длительность и стоимость лечения увеличены.
 MRSA • Одной из наиболее значимых супербактерий является бактерия S. aureus. Она тесно ассоциированна с человеком: ее носителями (назальными комменсалами) является не менее 30% популяции. S. aureus вызывает множество заболеваний и в последние годы считается главной причиной нозокомиальных инфекций. Применявшийся для лечения инфекций, вызванных S. aureus , пенициллин стал также первым модифицированным АБ, призванным игнорировать появление у стафилококков пенициллиназ (1959 г. , метициллин). Однако уже через 3 года появились устойчивые к метициллину штаммы (methicillin-resistant S. aureus , MRSA). • Недавно было установлено, что MRSA вышли за пределы больниц, превратившись в главный патоген окружающей среды с повышенной вирулентностью и трансмиссивными характеристиками (СА-MRSA). Последний сохранил гены MRSA и приобрел ряд новых, например ген, кодирующий цитотоксический лейкоцидин. В результате акроним MRSA теперь расшифровывается как multantbiotc-resistant S. aureus.
MRSA • Одной из наиболее значимых супербактерий является бактерия S. aureus. Она тесно ассоциированна с человеком: ее носителями (назальными комменсалами) является не менее 30% популяции. S. aureus вызывает множество заболеваний и в последние годы считается главной причиной нозокомиальных инфекций. Применявшийся для лечения инфекций, вызванных S. aureus , пенициллин стал также первым модифицированным АБ, призванным игнорировать появление у стафилококков пенициллиназ (1959 г. , метициллин). Однако уже через 3 года появились устойчивые к метициллину штаммы (methicillin-resistant S. aureus , MRSA). • Недавно было установлено, что MRSA вышли за пределы больниц, превратившись в главный патоген окружающей среды с повышенной вирулентностью и трансмиссивными характеристиками (СА-MRSA). Последний сохранил гены MRSA и приобрел ряд новых, например ген, кодирующий цитотоксический лейкоцидин. В результате акроним MRSA теперь расшифровывается как multantbiotc-resistant S. aureus.
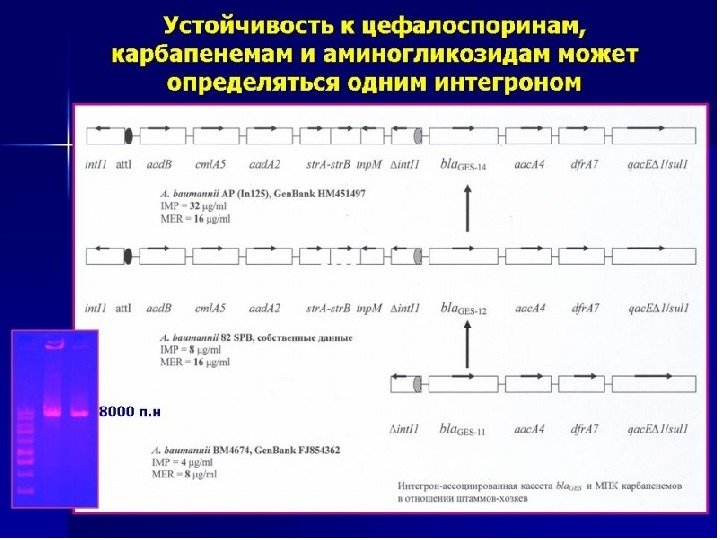
 Бактериальные фьючерсы У бактерий обнаружено огромное число кассет интегронов, которые не кодируют какие-либо известные в настоящее время детерминанты резистентности (Gillings et al. , 2008). Другими словами, бактерии разработали систему защиты от оружия, которого еще нет в природе.
Бактериальные фьючерсы У бактерий обнаружено огромное число кассет интегронов, которые не кодируют какие-либо известные в настоящее время детерминанты резистентности (Gillings et al. , 2008). Другими словами, бактерии разработали систему защиты от оружия, которого еще нет в природе.
 Бактериальные фьючерсы • Бактерии Escherichia coli, живущие на поверхности кожи представителей изолированных племен, оказались способными сопротивляться современным синтетическим антибиотикам. Это было показано в исследовании микробиома южноамериканского племени яномами, ранее не контактировавшего с внешним миром. С работой можно ознакомиться в журнале Science. • В 2008 году венесуэльский военный вертолет обнаружил изолированное поселение индейцев яномами, состоящее всего из 54 человек. Медицинская комиссия, отправившаяся к ним, получила разрешение взять образцы микрофлоры со слизистых, из кишечного материала, а также кожи предплечий 34 членов племени. • Секвенирование образцов показало, что микрофлора представителей племени оказалась самой многообразной из всех описанных, в том числе и в рамках проекта Человеческий Микробиом. Количество различных видов бактерий оказалось в два раза выше, чем у американцев, и превышает аналогичный показатель у других южноамериканских племен, контактировавших с цивилизованным обществом. Самым необычным результатом анализа стало то, что некоторые обнаруженные бактерии были устойчивы как к природным, так и к некоторым синтетическим антибиотикам. Авторы включили в список исследуемых препаратов как те, что действуют на ферменты синтеза клеточной стенки, (пенициллин, его синтетический аналог азтреонам) так и те, что мешают синтезу белка (хлорамфеникол, тетрациклин) и ДНК (ципрофлоксацин). Результаты показали, что наряду с устойчивостью к тетрациклину и пенициллину, бактерии оказались невосприимчивыми и к синтетическому азтреонаму, значительно отличающемся по строению от пенициллина. Однако к полностью синтетическому ципрофлоксацину, который не имеет аналогов в природе, устойчивых бактерий среди проанализированных образцов обнаружить не удалось (хотя вообще говоря они известны). По словам авторов, анализируемые штаммы оказались обладателями более 60 различных генов, которые могут включаться для борьбы с антибиотиками, в частности, около полудюжины генов, способных обеспечить защиту от синтетических препаратов.
Бактериальные фьючерсы • Бактерии Escherichia coli, живущие на поверхности кожи представителей изолированных племен, оказались способными сопротивляться современным синтетическим антибиотикам. Это было показано в исследовании микробиома южноамериканского племени яномами, ранее не контактировавшего с внешним миром. С работой можно ознакомиться в журнале Science. • В 2008 году венесуэльский военный вертолет обнаружил изолированное поселение индейцев яномами, состоящее всего из 54 человек. Медицинская комиссия, отправившаяся к ним, получила разрешение взять образцы микрофлоры со слизистых, из кишечного материала, а также кожи предплечий 34 членов племени. • Секвенирование образцов показало, что микрофлора представителей племени оказалась самой многообразной из всех описанных, в том числе и в рамках проекта Человеческий Микробиом. Количество различных видов бактерий оказалось в два раза выше, чем у американцев, и превышает аналогичный показатель у других южноамериканских племен, контактировавших с цивилизованным обществом. Самым необычным результатом анализа стало то, что некоторые обнаруженные бактерии были устойчивы как к природным, так и к некоторым синтетическим антибиотикам. Авторы включили в список исследуемых препаратов как те, что действуют на ферменты синтеза клеточной стенки, (пенициллин, его синтетический аналог азтреонам) так и те, что мешают синтезу белка (хлорамфеникол, тетрациклин) и ДНК (ципрофлоксацин). Результаты показали, что наряду с устойчивостью к тетрациклину и пенициллину, бактерии оказались невосприимчивыми и к синтетическому азтреонаму, значительно отличающемся по строению от пенициллина. Однако к полностью синтетическому ципрофлоксацину, который не имеет аналогов в природе, устойчивых бактерий среди проанализированных образцов обнаружить не удалось (хотя вообще говоря они известны). По словам авторов, анализируемые штаммы оказались обладателями более 60 различных генов, которые могут включаться для борьбы с антибиотиками, в частности, около полудюжины генов, способных обеспечить защиту от синтетических препаратов.
 Практическое значение генетики бактерий • Таксономия и эволюционный анализ • Определение мутагенности (тест Эймса) • Генетическая инженерия • Биотехнология • Идентификация бактерий в патологическом материале • Идентификация чистых культур возбудителей
Практическое значение генетики бактерий • Таксономия и эволюционный анализ • Определение мутагенности (тест Эймса) • Генетическая инженерия • Биотехнология • Идентификация бактерий в патологическом материале • Идентификация чистых культур возбудителей
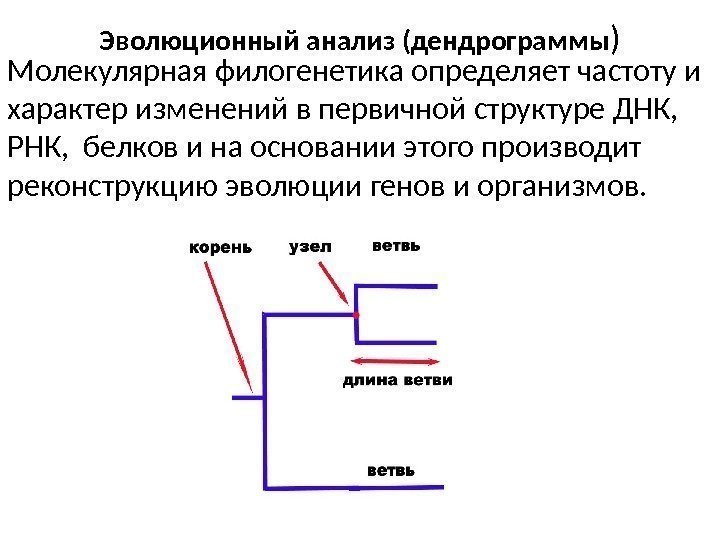
 Эволюционный анализ (дендрограммы ) Молекулярная филогенетика определяет частоту и характер изменений в первичной структуре ДНК, РНК, белков и на основании этого производит реконструкцию эволюции генов и организмов.
Эволюционный анализ (дендрограммы ) Молекулярная филогенетика определяет частоту и характер изменений в первичной структуре ДНК, РНК, белков и на основании этого производит реконструкцию эволюции генов и организмов.
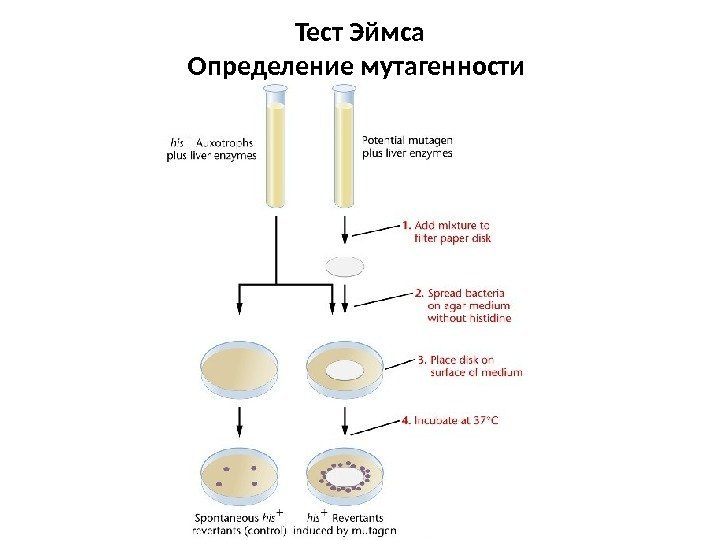
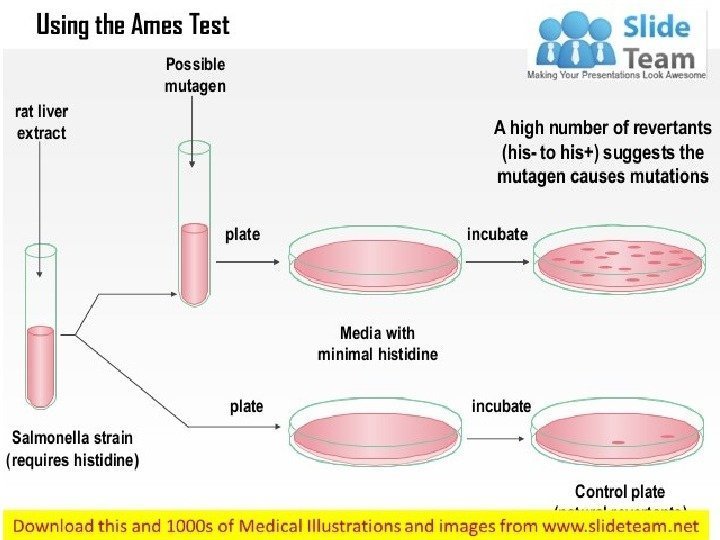
 Тест Эймса Определение мутагенности
Тест Эймса Определение мутагенности
 Брюс Эймс
Брюс Эймс

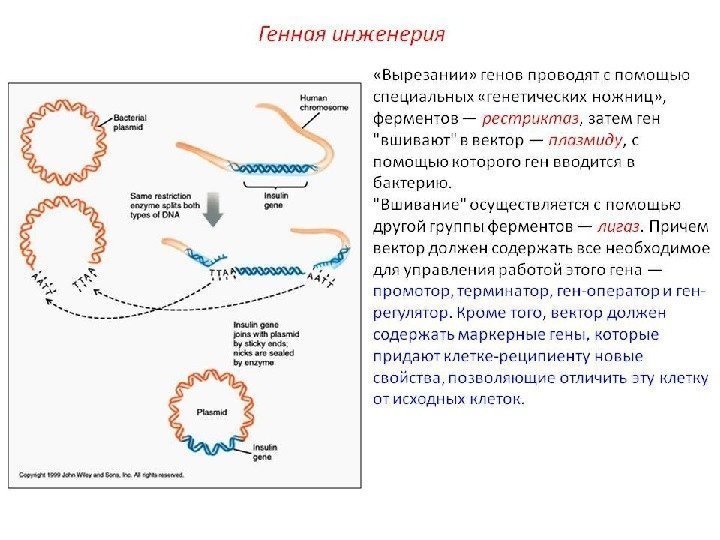
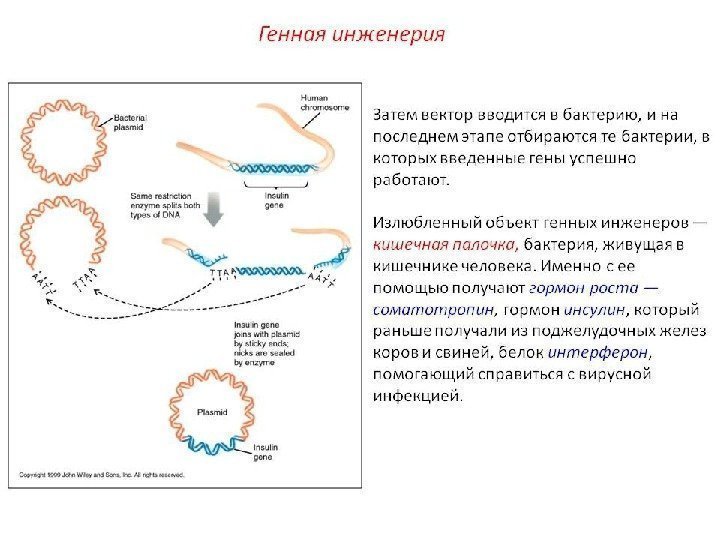
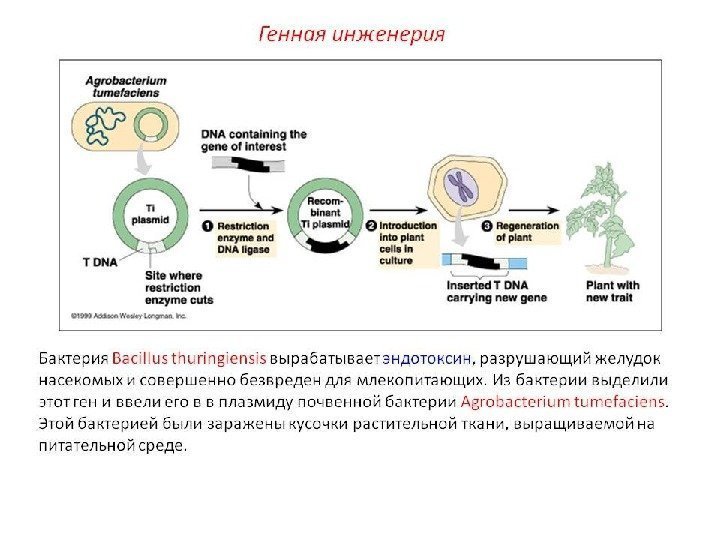
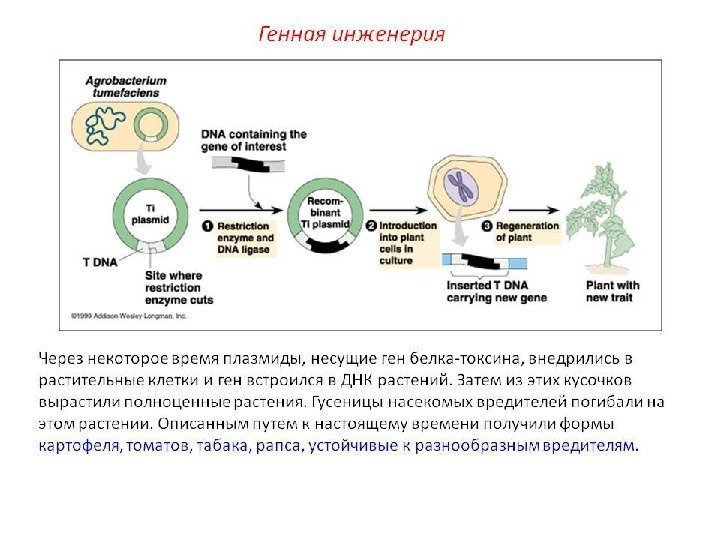
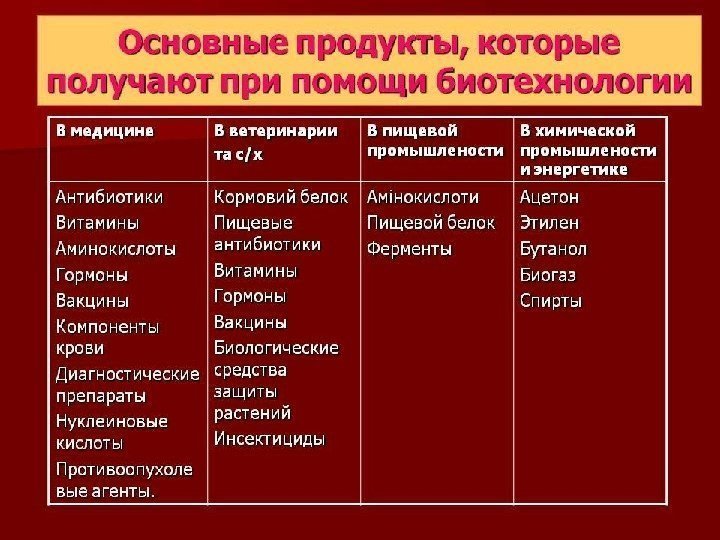
 Генетическая инженерия Генная инженерия – раздел генетики, позволяющий модифицировать генетический состав организма и конструировать организмы с новыми свойствами. Генетическая инженерия является основой биотехнологии и используют для получения: • Продуктов микробного синтеза: антибиотиков, ферментов, иммуномодуляторов (интерлейкинов); • Рекомбинантных и векторных вакцин ( «Энджерикс В» – генноинженерная вакцина против гепатита В); • Лекарственных рекомбинантных препаратов (инсулина, паратиреоидного гормона, гормона роста костей, активатора тканевого плазминогена, эритропоэтина, ); • Трансгенных животных и растений; • Микроорганизмов-деструкторов, разрушающих загрязнители окружающей среды; • Проведения генной терапии (введение нормально функционирующего гена).
Генетическая инженерия Генная инженерия – раздел генетики, позволяющий модифицировать генетический состав организма и конструировать организмы с новыми свойствами. Генетическая инженерия является основой биотехнологии и используют для получения: • Продуктов микробного синтеза: антибиотиков, ферментов, иммуномодуляторов (интерлейкинов); • Рекомбинантных и векторных вакцин ( «Энджерикс В» – генноинженерная вакцина против гепатита В); • Лекарственных рекомбинантных препаратов (инсулина, паратиреоидного гормона, гормона роста костей, активатора тканевого плазминогена, эритропоэтина, ); • Трансгенных животных и растений; • Микроорганизмов-деструкторов, разрушающих загрязнители окружающей среды; • Проведения генной терапии (введение нормально функционирующего гена).
 “ ИНСТРУМЕНТЫ» ДЛЯ ГЕННОЙ ИНЖЕНЕРИИ ФЕРМЕНТЫ (рестриктазы, лигазы, обратная транскриптаза) ВЕКТОРЫ (плазмиды, умеренные бактериофаги, космиды, транспозоны, вирусы)
“ ИНСТРУМЕНТЫ» ДЛЯ ГЕННОЙ ИНЖЕНЕРИИ ФЕРМЕНТЫ (рестриктазы, лигазы, обратная транскриптаза) ВЕКТОРЫ (плазмиды, умеренные бактериофаги, космиды, транспозоны, вирусы)




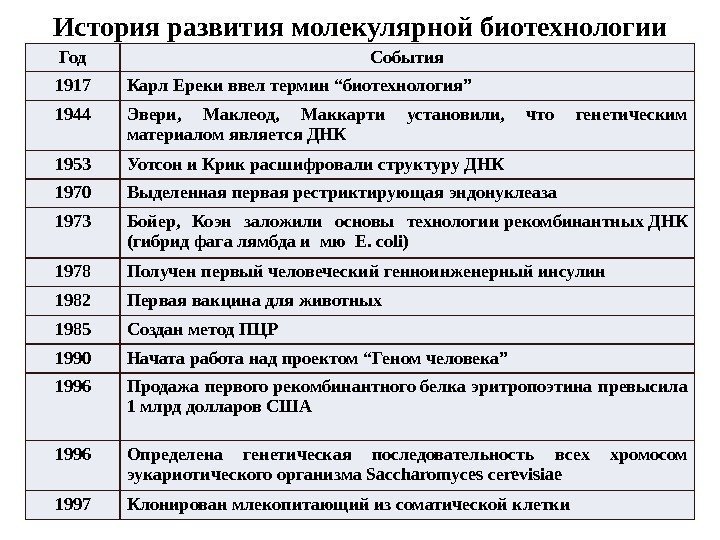
 История развития молекулярной биотехнологии Год События 1917 Карл Ереки ввел термин “биотехнология” 1944 Эвери, Маклеод, Маккарти установили, что генетическим материалом является ДНК 1953 Уотсон и Крик расшифровали структуру ДНК 1970 Выделенная первая рестриктирующая эндонуклеаза 1973 Бойер, Коэн заложили основы технологии рекомбинантных ДНК (гибрид фага лямбда и мю E. coli) 1978 Получен первый человеческий генноинженерный инсулин 1982 Первая вакцина для животных 1985 Создан метод ПЦР 1990 Начата работа над проектом “Геном человека” 1996 Продажа первого рекомбинантного белка эритропоэтина превысила 1 млрд долларов США 1996 Определена генетическая последовательность всех хромосом эукариотического организма Saccharomyces сеrevisiae 1997 Клонирован млекопитающий из соматической клетки
История развития молекулярной биотехнологии Год События 1917 Карл Ереки ввел термин “биотехнология” 1944 Эвери, Маклеод, Маккарти установили, что генетическим материалом является ДНК 1953 Уотсон и Крик расшифровали структуру ДНК 1970 Выделенная первая рестриктирующая эндонуклеаза 1973 Бойер, Коэн заложили основы технологии рекомбинантных ДНК (гибрид фага лямбда и мю E. coli) 1978 Получен первый человеческий генноинженерный инсулин 1982 Первая вакцина для животных 1985 Создан метод ПЦР 1990 Начата работа над проектом “Геном человека” 1996 Продажа первого рекомбинантного белка эритропоэтина превысила 1 млрд долларов США 1996 Определена генетическая последовательность всех хромосом эукариотического организма Saccharomyces сеrevisiae 1997 Клонирован млекопитающий из соматической клетки
 ПРОДУЦЕНТЫ, которые чаще всего используются в биотехнологии ЭУКАРИОТЫ – дрожжи, плесневые грибы, культуры клеток животных, людей и растений ПРОКАРИОТЫ – кишечная палочка, аэробные бациллы, псевдомонады, актиномицеты.
ПРОДУЦЕНТЫ, которые чаще всего используются в биотехнологии ЭУКАРИОТЫ – дрожжи, плесневые грибы, культуры клеток животных, людей и растений ПРОКАРИОТЫ – кишечная палочка, аэробные бациллы, псевдомонады, актиномицеты.
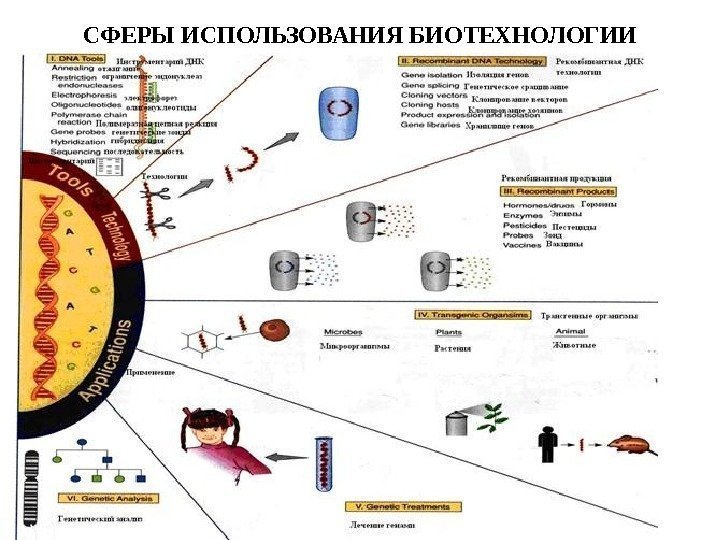
 СФЕРЫ ИСПОЛЬЗОВАНИЯ БИОТЕХНОЛОГИИ
СФЕРЫ ИСПОЛЬЗОВАНИЯ БИОТЕХНОЛОГИИ

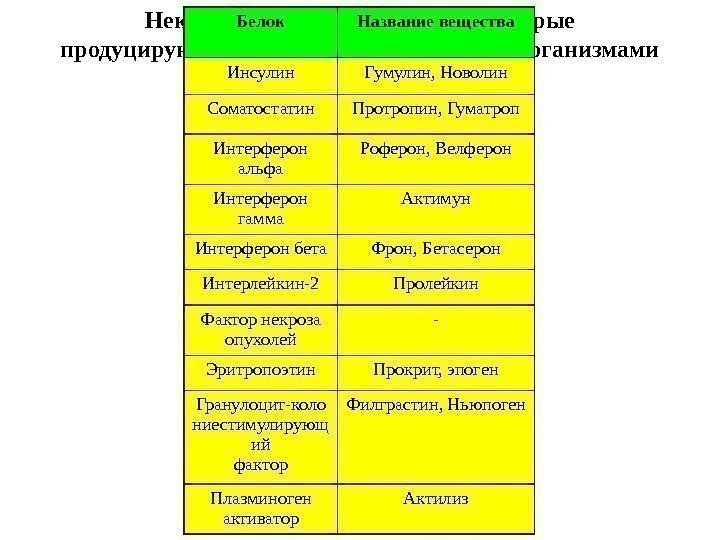
 Некоторые гормоны человека, которые продуцируются рекомбинантными микроорганизмами Белок Название вещества Инсулин Гумулин, Новолин Соматостатин Протропин, Гуматроп Интерферон альфа Роферон, Велферон Интерферон гамма Актимун Интерферон бета Фрон, Бетасерон Интерлейкин-2 Пролейкин Фактор некроза опухолей — Эритропоэтин Прокрит, эпоген Гранулоцит-коло ниестимулирующ ий фактор Филграстин, Ньюпоген Плазминоген активатор Актилиз
Некоторые гормоны человека, которые продуцируются рекомбинантными микроорганизмами Белок Название вещества Инсулин Гумулин, Новолин Соматостатин Протропин, Гуматроп Интерферон альфа Роферон, Велферон Интерферон гамма Актимун Интерферон бета Фрон, Бетасерон Интерлейкин-2 Пролейкин Фактор некроза опухолей — Эритропоэтин Прокрит, эпоген Гранулоцит-коло ниестимулирующ ий фактор Филграстин, Ньюпоген Плазминоген активатор Актилиз
 Применение молекулярно-генетических методов в диагностике инфекционных болезней Генетические методы применяются : • для обнаружения микроба в исследуемом материале без выделения чистой культуры • для идентификации чистой культуры • для определения таксономического положения нового микроба • для проведения внутривидового типирования.
Применение молекулярно-генетических методов в диагностике инфекционных болезней Генетические методы применяются : • для обнаружения микроба в исследуемом материале без выделения чистой культуры • для идентификации чистой культуры • для определения таксономического положения нового микроба • для проведения внутривидового типирования.
 1985 год Создание К. Б. Мюллисом революционизирующей технологии — полимеразной цепной реакции, ПЦР — наиболее чувствительного до сих пор метода детектирования ДНК. Эта технология получила широкое распространение (Нобелевская премия по химии за 1993 г. ).
1985 год Создание К. Б. Мюллисом революционизирующей технологии — полимеразной цепной реакции, ПЦР — наиболее чувствительного до сих пор метода детектирования ДНК. Эта технология получила широкое распространение (Нобелевская премия по химии за 1993 г. ).

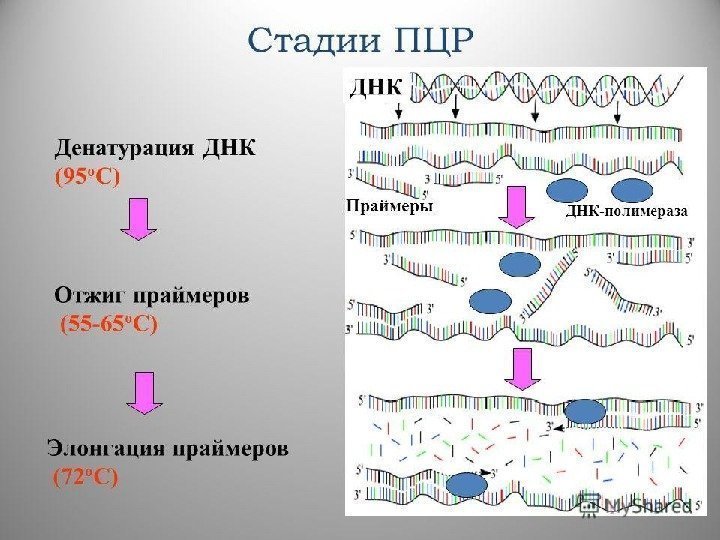
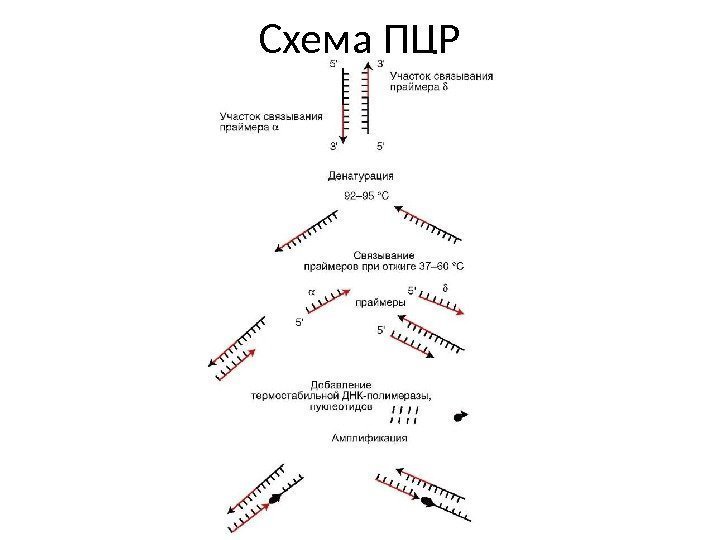
 Полимеразная цепная реакция • Полимеразная цепная реакция происходит в несколько этапов: 1) денатурация — образование из двуцепочечной ДНК одноцепочечной молекулы; 2) отжиг — ограничение амплифицируемого фрагмента путем присоединения прямого и обратного праймеров; 3) элонгация — полимеризация дочерних цепочек на ДНК-матрице. • Каждая из этих стадий протекает при определенной температуре. • Реакцию амплификации повторяют 20 -45 раз, предваряя ее дополнительной денатурацией и заканчивая дополнительной элонгацией.
Полимеразная цепная реакция • Полимеразная цепная реакция происходит в несколько этапов: 1) денатурация — образование из двуцепочечной ДНК одноцепочечной молекулы; 2) отжиг — ограничение амплифицируемого фрагмента путем присоединения прямого и обратного праймеров; 3) элонгация — полимеризация дочерних цепочек на ДНК-матрице. • Каждая из этих стадий протекает при определенной температуре. • Реакцию амплификации повторяют 20 -45 раз, предваряя ее дополнительной денатурацией и заканчивая дополнительной элонгацией.

 Схема ПЦР
Схема ПЦР
 Real-time ПЦР
Real-time ПЦР
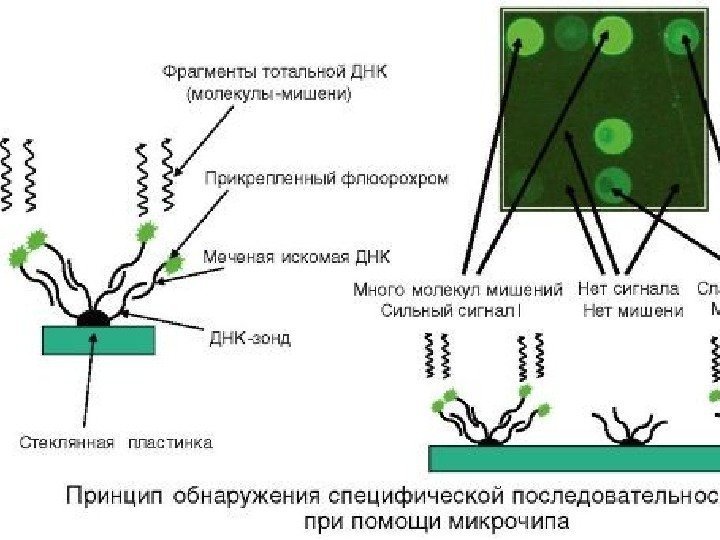
 Биочипы • Метод биочипов, основан на одновременном проведении большого количества (25 000 – 50 000) молекулярно-биологических реакций на микроносителях (чипах). • Биочип – это миниатюризированные подложки из стекла, нейлоновых и других материалов, на которых иммобилизованы десятки тысяч проб (ДНК, олигонукдеотидов, пептидов, клеток), при этом размер одной нанесенной пробы не превышает 200 – 300 микрон. • Метод используют в диагностике заболеваний, идентификации генов и изучении их экспрессии, сравнительном анализе геномов и протеомов. Метод позволяет идентифицировать: 1) нуклеиновые кислоты (эукариотическую и прокариотическую ДНК, продукты полимеразной цепной реакции, РНК, м. РНК); 2) белки (антитела/антигены, цитокины, ферменты, внутриклеточные белковые молекулы); 3) целые клетки (опухолевые).
Биочипы • Метод биочипов, основан на одновременном проведении большого количества (25 000 – 50 000) молекулярно-биологических реакций на микроносителях (чипах). • Биочип – это миниатюризированные подложки из стекла, нейлоновых и других материалов, на которых иммобилизованы десятки тысяч проб (ДНК, олигонукдеотидов, пептидов, клеток), при этом размер одной нанесенной пробы не превышает 200 – 300 микрон. • Метод используют в диагностике заболеваний, идентификации генов и изучении их экспрессии, сравнительном анализе геномов и протеомов. Метод позволяет идентифицировать: 1) нуклеиновые кислоты (эукариотическую и прокариотическую ДНК, продукты полимеразной цепной реакции, РНК, м. РНК); 2) белки (антитела/антигены, цитокины, ферменты, внутриклеточные белковые молекулы); 3) целые клетки (опухолевые).

 ДНК-микрочип (англ. DNA microarray) — технология, используемая в молекулярной биологии и медицине. • Современный ДНК-микрочип состоит из тысяч дезоксиолигонуклеотидов (зондов, или проб), сгруппированных в виде микроскопических точек и закреплённых на твёрдой подложке. Каждая точка содержит несколько пикомолей ДНК с определённой нуклеотидной последовательностью. Олигонуклеотиды ДНК-микрочипа могут быть короткими участками генов или других функциональных элементов ДНК и используются для гибридизации с к. ДНК или м. РНК (к. РНК). • Гибридизация зонда и мишени регистрируется и количественно характеризуется при помощи флюоресценции или хемилюминесценции , что позволяет определять относительное количество нуклеиновой кислоты с заданной последовательностью в образце. • В обычном ДНК-микрочипе зонды ковалентно прикрепляются к твёрдой поверхности — стеклянному или кремниевому чипу. Другие платформы, например, выпускаемые Illumina, используют микроскопические шарики вместо больших твёрдых поверхностей. • ДНК-микрочипы используют для анализа изменения экспрессии генов, выявления однонуклеотидных полиморфизмов, генотипирования или повторного секвенирования мутантных геномов. Микрочипы отличаются по конструкции, особенностям работы, точности, эффективности и стоимости. • Впервые набор различных ДНК, объединённых в чип, был использован в 1987 году для определения особенностей регуляции экспрессии генов интерферонами. Ранние ДНК-микрочипы были сделаны путём «раскапывания» микроколичеств к. ДНК на фильтровальную бумагу.
ДНК-микрочип (англ. DNA microarray) — технология, используемая в молекулярной биологии и медицине. • Современный ДНК-микрочип состоит из тысяч дезоксиолигонуклеотидов (зондов, или проб), сгруппированных в виде микроскопических точек и закреплённых на твёрдой подложке. Каждая точка содержит несколько пикомолей ДНК с определённой нуклеотидной последовательностью. Олигонуклеотиды ДНК-микрочипа могут быть короткими участками генов или других функциональных элементов ДНК и используются для гибридизации с к. ДНК или м. РНК (к. РНК). • Гибридизация зонда и мишени регистрируется и количественно характеризуется при помощи флюоресценции или хемилюминесценции , что позволяет определять относительное количество нуклеиновой кислоты с заданной последовательностью в образце. • В обычном ДНК-микрочипе зонды ковалентно прикрепляются к твёрдой поверхности — стеклянному или кремниевому чипу. Другие платформы, например, выпускаемые Illumina, используют микроскопические шарики вместо больших твёрдых поверхностей. • ДНК-микрочипы используют для анализа изменения экспрессии генов, выявления однонуклеотидных полиморфизмов, генотипирования или повторного секвенирования мутантных геномов. Микрочипы отличаются по конструкции, особенностям работы, точности, эффективности и стоимости. • Впервые набор различных ДНК, объединённых в чип, был использован в 1987 году для определения особенностей регуляции экспрессии генов интерферонами. Ранние ДНК-микрочипы были сделаны путём «раскапывания» микроколичеств к. ДНК на фильтровальную бумагу.



 Схема стратегии «дробовика» , используемая для секвенирования больших молекул ДНК
Схема стратегии «дробовика» , используемая для секвенирования больших молекул ДНК
 • Наличие в методе стадии молекулярного клонирования делает его достаточно трудоёмким. Кроме того, на 2016 год секвенирование по Сенгеру уже не применяется для определения последовательностей геномов. С другой стороны, методы секвенирования нового поколения позволяют получить последовательности геномов организмов, находящихся в образце среды, быстрее и без стадии молекулярного клонирования.
• Наличие в методе стадии молекулярного клонирования делает его достаточно трудоёмким. Кроме того, на 2016 год секвенирование по Сенгеру уже не применяется для определения последовательностей геномов. С другой стороны, методы секвенирования нового поколения позволяют получить последовательности геномов организмов, находящихся в образце среды, быстрее и без стадии молекулярного клонирования.
 Секвенаторы
Секвенаторы
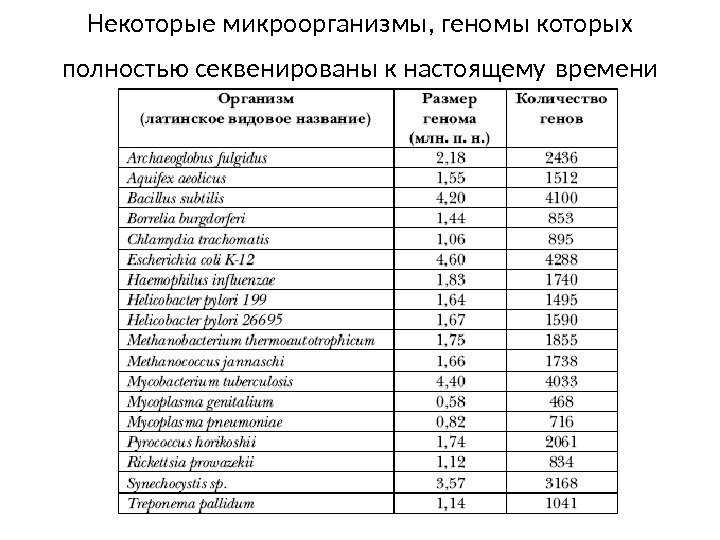
 Некоторые микроорганизмы, геномы которых полностью секвенированы к настоящему времени
Некоторые микроорганизмы, геномы которых полностью секвенированы к настоящему времени
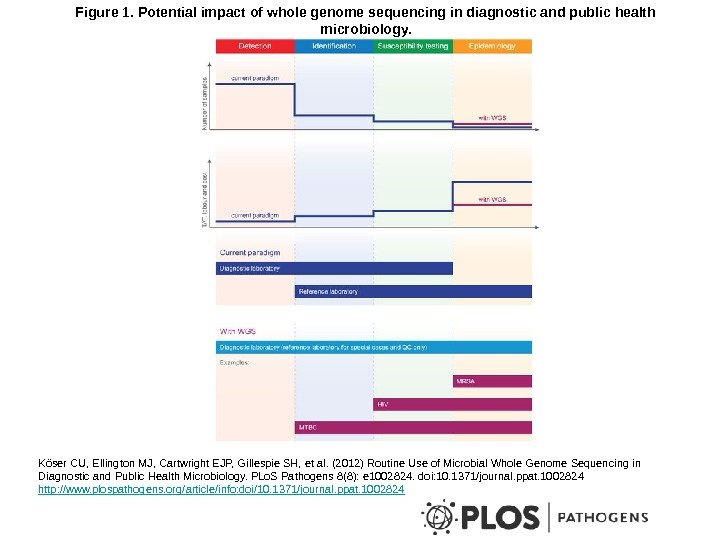
 Figure 1. Potential impact of whole genome sequencing in diagnostic and public health microbiology. Köser CU, Ellington MJ, Cartwright EJP, Gillespie SH, et al. (2012) Routine Use of Microbial Whole Genome Sequencing in Diagnostic and Public Health Microbiology. PLo. S Pathogens 8(8): e 1002824. doi: 10. 1371/journal. ppat. 1002824 http: //www. plospathogens. org/article/info: doi/10. 1371/journal. ppat.
Figure 1. Potential impact of whole genome sequencing in diagnostic and public health microbiology. Köser CU, Ellington MJ, Cartwright EJP, Gillespie SH, et al. (2012) Routine Use of Microbial Whole Genome Sequencing in Diagnostic and Public Health Microbiology. PLo. S Pathogens 8(8): e 1002824. doi: 10. 1371/journal. ppat. 1002824 http: //www. plospathogens. org/article/info: doi/10. 1371/journal. ppat.
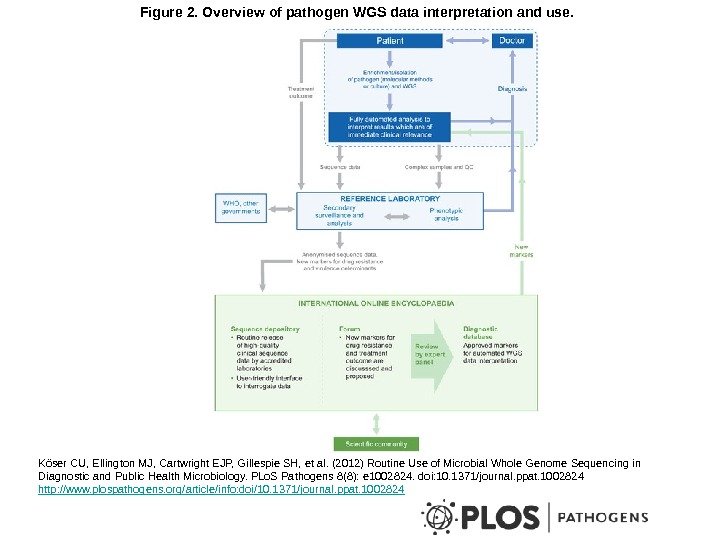
 Figure 2. Overview of pathogen WGS data interpretation and use. Köser CU, Ellington MJ, Cartwright EJP, Gillespie SH, et al. (2012) Routine Use of Microbial Whole Genome Sequencing in Diagnostic and Public Health Microbiology. PLo. S Pathogens 8(8): e 1002824. doi: 10. 1371/journal. ppat. 1002824 http: //www. plospathogens. org/article/info: doi/10. 1371/journal. ppat.
Figure 2. Overview of pathogen WGS data interpretation and use. Köser CU, Ellington MJ, Cartwright EJP, Gillespie SH, et al. (2012) Routine Use of Microbial Whole Genome Sequencing in Diagnostic and Public Health Microbiology. PLo. S Pathogens 8(8): e 1002824. doi: 10. 1371/journal. ppat. 1002824 http: //www. plospathogens. org/article/info: doi/10. 1371/journal. ppat.
 Геномика • Термин предложил в 1986 г. Томас Родерикк для обозначения дисциплины, занимающейся секвенированием и анализом геномов, составлением генетических карт организмов. • В настоящее время под термином «геномика» понимают новое направление генетики, изучающее геномы и отдельные гены организмов на индивидуальном и популяционных уровнях для установления взаимосвязи организмов и направления их эволюции. • Понятие геном следует отличать от понятия генотип. Генотип – это совокупность хромосомных генов, детерминирующих фенотипические признаки. Геном – это вся ДНК/РНК клетки или организма. • Развитие геномики начинается с началом глобального научного проекта «Геном человека» (1990 г. — ), в рамках которого в 1995 г. впервые секвенирован геном микроорганизма Haemophilus infuenzae , в 1996 г. – S. cerevisiae , в 2000 г. — геном человека. В настоящее время проводится секвенирование геномов 200 видов микроорганизмов, 60 из которых уже в стадии завершения. • В геномике выделяют : структурное и функциональное направления
Геномика • Термин предложил в 1986 г. Томас Родерикк для обозначения дисциплины, занимающейся секвенированием и анализом геномов, составлением генетических карт организмов. • В настоящее время под термином «геномика» понимают новое направление генетики, изучающее геномы и отдельные гены организмов на индивидуальном и популяционных уровнях для установления взаимосвязи организмов и направления их эволюции. • Понятие геном следует отличать от понятия генотип. Генотип – это совокупность хромосомных генов, детерминирующих фенотипические признаки. Геном – это вся ДНК/РНК клетки или организма. • Развитие геномики начинается с началом глобального научного проекта «Геном человека» (1990 г. — ), в рамках которого в 1995 г. впервые секвенирован геном микроорганизма Haemophilus infuenzae , в 1996 г. – S. cerevisiae , в 2000 г. — геном человека. В настоящее время проводится секвенирование геномов 200 видов микроорганизмов, 60 из которых уже в стадии завершения. • В геномике выделяют : структурное и функциональное направления
 Структурная геномика. • Определяет первичную структуру генома, границы генов и их организацию, структуру белков и других биомолекул клетки. • Описывает организацию генома и протеома в целом у различных организмов. • Использует методы картирования, секвенирования, рентгеноструктурного анализа, биоинформатики. • Биоинформатика – направление биологии, основанное на компьютерном анализе первичной, вторичной, третичной структуры молекул ДНК, РНК, белков. В этих целях разработаны компьютерные программы и созданы базы данных по составу геномов, протеомов организмов.
Структурная геномика. • Определяет первичную структуру генома, границы генов и их организацию, структуру белков и других биомолекул клетки. • Описывает организацию генома и протеома в целом у различных организмов. • Использует методы картирования, секвенирования, рентгеноструктурного анализа, биоинформатики. • Биоинформатика – направление биологии, основанное на компьютерном анализе первичной, вторичной, третичной структуры молекул ДНК, РНК, белков. В этих целях разработаны компьютерные программы и созданы базы данных по составу геномов, протеомов организмов.

 Функциональная геномика • изучает сетевые взаимодействия генов/белков. Функции генов могут быть установлены на основании изучения синтезируемых с них м. РНК, белков и образуемых метаболитов, поэтому в функциональной геномике выделяют следующие разделы: • 1) транскриптомика – раздел геномики, изучающий совокупность м. РНК клетки и изменения в них в зависимости от среды и стадии развития. • 2) протеомика — раздел геномики, изучающий совокупность всех белков клетки, их структуру и взаимодействие друг с другом в зависимости от микроокружения и стадии развития. • 3) метаболомика — раздел геномики, изучающий метаболиты (конечные продукты клеточных процессов) и изменения в их составе в разные фазы жизненного цикла и состояния микроокружения бактерий.
Функциональная геномика • изучает сетевые взаимодействия генов/белков. Функции генов могут быть установлены на основании изучения синтезируемых с них м. РНК, белков и образуемых метаболитов, поэтому в функциональной геномике выделяют следующие разделы: • 1) транскриптомика – раздел геномики, изучающий совокупность м. РНК клетки и изменения в них в зависимости от среды и стадии развития. • 2) протеомика — раздел геномики, изучающий совокупность всех белков клетки, их структуру и взаимодействие друг с другом в зависимости от микроокружения и стадии развития. • 3) метаболомика — раздел геномики, изучающий метаболиты (конечные продукты клеточных процессов) и изменения в их составе в разные фазы жизненного цикла и состояния микроокружения бактерий.
 Метаген мика оо • Метаген мика оо — раздел молекулярной генетики, в котором изучается генетический материал, полученный из образцов окружающей среды. Метагеномика изучает набор генов всех микроорганизмов, находящихся в образце среды, — метагеном. Метагеномный анализ позволяет определить видовое разнообразие исследуемого образца без необходимости выделения и культивирования микроорганизмов. • Основным преимуществом использования метагеномного подхода является учёт не только культивируемых микроорганизмов, но и некультивируемых. Оказалось, что такие организмы вносят основной вклад в видовое разнообразие сообществ. Метагеномика позволяет детально изучить разнообразие сообществ, а значит и выяснить механизмы их функционирования, определить метаболические взаимосвязи. • Широкое развитие метагеномики обусловлено распространением методов секвенирования нового поколения. Они позволяют получить последовательности практически всех генов каждого микроорганизма сообщества. • Термин «метагеномика» (англ. metagenomics) впервые был употреблён Джо Хандельсман, Джоном Кларди, Робертом Гудманом, Шоном Брэди (1998 г). Термин «метагеном» возник из идеи, что набор генов, собранных из окружающей среды, можно анализировать подобно тому, как анализируют цельные геномы. Кевин Чен и Лайор Пэтчер (исследователи из Университета Калифорнии, Беркли) определили метагеномику как «применение современных методов геномики без необходимости изолирования и лабораторного культивирования отдельных видов» .
Метаген мика оо • Метаген мика оо — раздел молекулярной генетики, в котором изучается генетический материал, полученный из образцов окружающей среды. Метагеномика изучает набор генов всех микроорганизмов, находящихся в образце среды, — метагеном. Метагеномный анализ позволяет определить видовое разнообразие исследуемого образца без необходимости выделения и культивирования микроорганизмов. • Основным преимуществом использования метагеномного подхода является учёт не только культивируемых микроорганизмов, но и некультивируемых. Оказалось, что такие организмы вносят основной вклад в видовое разнообразие сообществ. Метагеномика позволяет детально изучить разнообразие сообществ, а значит и выяснить механизмы их функционирования, определить метаболические взаимосвязи. • Широкое развитие метагеномики обусловлено распространением методов секвенирования нового поколения. Они позволяют получить последовательности практически всех генов каждого микроорганизма сообщества. • Термин «метагеномика» (англ. metagenomics) впервые был употреблён Джо Хандельсман, Джоном Кларди, Робертом Гудманом, Шоном Брэди (1998 г). Термин «метагеном» возник из идеи, что набор генов, собранных из окружающей среды, можно анализировать подобно тому, как анализируют цельные геномы. Кевин Чен и Лайор Пэтчер (исследователи из Университета Калифорнии, Беркли) определили метагеномику как «применение современных методов геномики без необходимости изолирования и лабораторного культивирования отдельных видов» .
 «Микробиом человека” (Human Microbiome Project) • Проект «Микробиом человека» (Human Microbiome Project), запущен в США в 2006 г. , с целью определить генетическую идентичность представителей микрофлоры, населя- ющей наш организм (полость рта, носа, кожу, кишечник) и проанализировать изменения микробного состава в зависимости от характера питания и возраста. • Цель проекта — расшифровка 900 полных геномов микробов, представленных одноклеточными простейшими, бактериями и археями, однако даже это количество, будет лишь малой толикой информации о всех микробах, живущих в человеческом теле, которые и составляют так называемый «МИКРОБИОМ». • Сообщества микроорганизмов или микрофлора, находятся в тесном взаимодействии с нашим организмом. Они могут способствовать нашей жизнедеятельности, либо вызвать заболевания. • Пять ключевых мест человеческого тела, а именно: кишечник, полость рта, дыхательные пути, кожные покровы и мочеполовая система, обильно населены различными видами микробов. В связи с этим они играют важную роль в поддержании иммунитета, обмена веществ, пищеварения и других функций. • Проект «Микробиом человека» является логическим развитием проекта «Геном человека», целью которого является полная расшифровка человеческого генома. Несмотря на то, что проект стартовал в 1990 году, а первый полный геном человека был опубликован в 2003 -м, этот проект до сих пор не завершен, так как нерасшифрованными остаются некоторые участки человеческой ДНК.
«Микробиом человека” (Human Microbiome Project) • Проект «Микробиом человека» (Human Microbiome Project), запущен в США в 2006 г. , с целью определить генетическую идентичность представителей микрофлоры, населя- ющей наш организм (полость рта, носа, кожу, кишечник) и проанализировать изменения микробного состава в зависимости от характера питания и возраста. • Цель проекта — расшифровка 900 полных геномов микробов, представленных одноклеточными простейшими, бактериями и археями, однако даже это количество, будет лишь малой толикой информации о всех микробах, живущих в человеческом теле, которые и составляют так называемый «МИКРОБИОМ». • Сообщества микроорганизмов или микрофлора, находятся в тесном взаимодействии с нашим организмом. Они могут способствовать нашей жизнедеятельности, либо вызвать заболевания. • Пять ключевых мест человеческого тела, а именно: кишечник, полость рта, дыхательные пути, кожные покровы и мочеполовая система, обильно населены различными видами микробов. В связи с этим они играют важную роль в поддержании иммунитета, обмена веществ, пищеварения и других функций. • Проект «Микробиом человека» является логическим развитием проекта «Геном человека», целью которого является полная расшифровка человеческого генома. Несмотря на то, что проект стартовал в 1990 году, а первый полный геном человека был опубликован в 2003 -м, этот проект до сих пор не завершен, так как нерасшифрованными остаются некоторые участки человеческой ДНК.
 «Микробиом человека” (Human Microbiome Project) • Консорциум американских ученых в 2012 г. опубликовал результаты пятилетней работы над проектом Национальных институтов здоровья «Микробиом человека» (Human Microbiome Project). В работе над проектом приняли участие около 200 ученых из 80 мультидисциплинарных исследовательских институтов с участием Российской Академии наук. Общая стоимость исследования составила 173 миллиона долларов. • Целью проекта было охарактеризовать все микробы, присутствующие в организме человека, для чего ученые взяли образцы тканей из 15 мест на теле 129 мужчин и из 18 мест у 113 женщин. Все добровольцы — здоровые люди в возрасте от 18 до 40 лет — предоставили по три образца слизистой с внутренней стороны щек, носа, кожи за ухом и локтевого сгиба, некоторых участков кожи, влагалища у женщин а также фекальные пробы. Исследования проводили в США, Европе, Китае, Японии. • По результатам генетического анализа биоматериала было установлено, что в человеческом организме обитает свыше 10 тысяч видов различных микробов. Как утверждают авторы исследования, такое разнообразие микробиома обеспечивает человека гораздо большим количеством генов, чем можно было представить. Так, если в геноме человека содержится 22 тысячи генов, кодирующих белки для регуляции метаболизма, микробиом добавляет еще около восьми миллионов уникальных бактериальных генов. • Ученые из Гарвардской школы общественного здоровья (Harvard T. H. Chan School of Public Health) под руководством Эрика Францосы (Eric Franzosa) пришли и к интересному выводу: микробиом каждого человека настолько уникален, что его можно было бы использовать вместо отпечатков пальцев для идентификации!
«Микробиом человека” (Human Microbiome Project) • Консорциум американских ученых в 2012 г. опубликовал результаты пятилетней работы над проектом Национальных институтов здоровья «Микробиом человека» (Human Microbiome Project). В работе над проектом приняли участие около 200 ученых из 80 мультидисциплинарных исследовательских институтов с участием Российской Академии наук. Общая стоимость исследования составила 173 миллиона долларов. • Целью проекта было охарактеризовать все микробы, присутствующие в организме человека, для чего ученые взяли образцы тканей из 15 мест на теле 129 мужчин и из 18 мест у 113 женщин. Все добровольцы — здоровые люди в возрасте от 18 до 40 лет — предоставили по три образца слизистой с внутренней стороны щек, носа, кожи за ухом и локтевого сгиба, некоторых участков кожи, влагалища у женщин а также фекальные пробы. Исследования проводили в США, Европе, Китае, Японии. • По результатам генетического анализа биоматериала было установлено, что в человеческом организме обитает свыше 10 тысяч видов различных микробов. Как утверждают авторы исследования, такое разнообразие микробиома обеспечивает человека гораздо большим количеством генов, чем можно было представить. Так, если в геноме человека содержится 22 тысячи генов, кодирующих белки для регуляции метаболизма, микробиом добавляет еще около восьми миллионов уникальных бактериальных генов. • Ученые из Гарвардской школы общественного здоровья (Harvard T. H. Chan School of Public Health) под руководством Эрика Францосы (Eric Franzosa) пришли и к интересному выводу: микробиом каждого человека настолько уникален, что его можно было бы использовать вместо отпечатков пальцев для идентификации!
 «Российский метагеномный проект» • В 2010 году начал работу «Российский метагеномный проект» (http: // metagenome. ru). • Российские медицинские, биологические и аналитические центры исследуют микробиоту желудочно-кишечного тракта, характерную для жителей различных территорий РФ, в норме и при патологиях — ее состав и возможный вклад в развитие заболеваний. • Российский микробиом имеет национальные черты, у сельского населения встречаются уникальные сообщества, не свойственные ни европейцам, ни американцам, ни китайцам, причем основу таких микробиот составляют бактерии, ассоциированные со здоровым кишечником. Некоторые образцы проявляют сходство с аборигенными, взятыми у гухибо и малавийцев. • Для России более характерно преобладание Faecalibacterium, Ruminococcus, Roseburia, для США— Bacteroides. Интересно, что западноевропейские образцы по этим показателям занимают промежуточное положение между Россией и США. Сейчас готовится к публикации научная статья российских ученых про эти открытия и другие особенности российской микробиоты.
«Российский метагеномный проект» • В 2010 году начал работу «Российский метагеномный проект» (http: // metagenome. ru). • Российские медицинские, биологические и аналитические центры исследуют микробиоту желудочно-кишечного тракта, характерную для жителей различных территорий РФ, в норме и при патологиях — ее состав и возможный вклад в развитие заболеваний. • Российский микробиом имеет национальные черты, у сельского населения встречаются уникальные сообщества, не свойственные ни европейцам, ни американцам, ни китайцам, причем основу таких микробиот составляют бактерии, ассоциированные со здоровым кишечником. Некоторые образцы проявляют сходство с аборигенными, взятыми у гухибо и малавийцев. • Для России более характерно преобладание Faecalibacterium, Ruminococcus, Roseburia, для США— Bacteroides. Интересно, что западноевропейские образцы по этим показателям занимают промежуточное положение между Россией и США. Сейчас готовится к публикации научная статья российских ученых про эти открытия и другие особенности российской микробиоты.
 Спасибо за внимание!
Спасибо за внимание!

