Лекция_1_Периодический закон.ppt
- Количество слайдов: 35

КАФЕДРА ФИЗИЧЕСКОЙ ХИМИИ СПб. ГЭТУ «ЛЭТИ» Курс ХИМИЯ Лектор: Альмяшев Вячеслав Исхакович Учебные материалы: http: //eltech. chemdm. ru/ Рекомендуемая литература: Лебедев О. А. Физическая химия. Конспект лекций. СПб. ГЭТУ "ЛЭТИ". 2006. 180 с. Коровин Н. В. Общая химия ВЕСЕННИЙ СЕМЕСТР 2015 -2016 УЧ. ГОД.

Общие понятия Химия – одна из важнейших областей естествознания, изучающих окружающий нас материальный мир во всем богатстве его форм и явлений Химия имеет дело с веществом – одной из форм материи, обладающих в отличие от полей массой покоя Современная химия – это наука, изучающая превращения веществ, сопровождающиеся изменением их состава и структуры Основные критерии химической формы движения материи, т. е. химического взаимодействия: пространственный масштаб событий 10 -8 – 10 -10 м температурный интервал 70 – 3000 K диапазон энергий ± (30 – 3000) к. Дж/моль

ОСНОВЫ СТРОЕНИЯ ВЕЩЕСТВА ПЕРИОДИЧЕСКИЙ ЗАКОН В СВЕТЕ УЧЕНИЯ О СТРОЕНИИ АТОМА Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово

Общие понятия Слово «элемент» (лат. elementum) использовалось с античности в смысле части чего-либо Химический элемент – базовое химическое понятие, отражающее химическую индивидуальность атомов в наиболее общем виде «Элементы – практически неразложимые тела, состоящие из сходных однородных (состоящих из первоматерии) корпускул, из которых составлены все сложные тела и на которые они могут быть разложены. Корпускулы могут различаться формой, размером, массой. Корпускулы, из которых образованы тела, остаются неизменными превращениях последних» Роберт Бойль. Химик-скептик. 1661 год Эмпирико-аналитическая концепция и первый в истории новой химии список химических элементов (таблицу простых тел), разделённых на несколько типов Антуан Лоран Лавуазье. Элементарный курс химии. 1789 год Атомно-молекулярная гипотеза. Химический элемент – отдельный вид атомов. Простые и сложные вещества состоят, соответственно, из атомов одного или различного видов. Атомный вес – важнейшее свойство элементов, определяющее его химическую природу Джон Дальтон. Новый курс химической философии. 1808 год «Химические элементы – материальные части простых или сложных тел, которые придают им известную совокупность физических и химических свойств» Дмитрий Иванович Менделеев. Середина XIX века
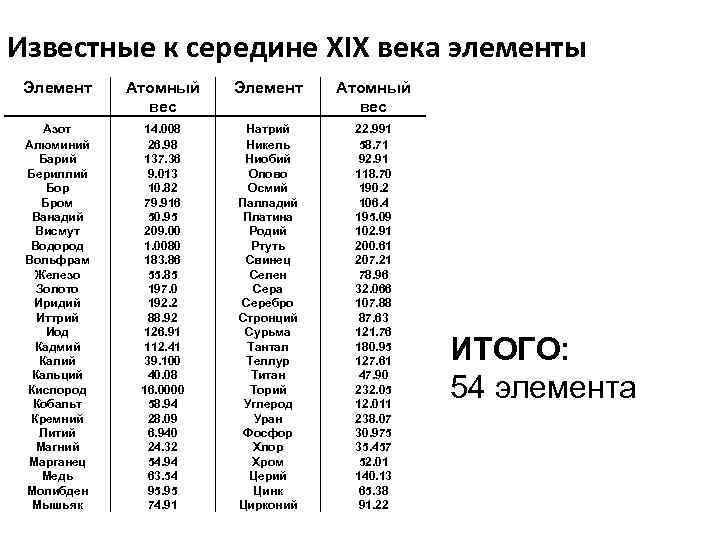
Известные к середине XIX века элементы Элемент Атомный вес Азот Алюминий Барий Бериллий Бор Бром Ванадий Висмут Водород Вольфрам Железо Золото Иридий Иттрий Иод Кадмий Кальций Кислород Кобальт Кремний Литий Магний Марганец Медь Молибден Мышьяк 14. 008 26. 98 137. 36 9. 013 10. 82 79. 916 50. 95 209. 00 1. 0080 183. 86 55. 85 197. 0 192. 2 88. 92 126. 91 112. 41 39. 100 40. 08 16. 0000 58. 94 28. 09 6. 940 24. 32 54. 94 63. 54 95. 95 74. 91 Натрий Никель Ниобий Олово Осмий Палладий Платина Родий Ртуть Свинец Селен Сера Серебро Стронций Сурьма Тантал Теллур Титан Торий Углерод Уран Фосфор Хлор Хром Церий Цинк Цирконий 22. 991 58. 71 92. 91 118. 70 190. 2 106. 4 195. 09 102. 91 200. 61 207. 21 78. 96 32. 066 107. 88 87. 63 121. 76 180. 95 127. 61 47. 90 232. 05 12. 011 238. 07 30. 975 35. 457 52. 01 140. 13 65. 38 91. 22 ИТОГО: 54 элемента

Приведение элементов в порядок Ø триады Дёберейнера (1829): Br – Cl – I, Ca – Sr – Ba, S – Se – Te Ø первый химический конгресс (1860 г. , Карлсруэ) Ø спираль де Шанкуртуа (1862) Ø октавы Ньюлендса (1864 - 1865) Ø таблицы Одлинга и Мейера (1870) Ø периодическая система Менделеева (1869) Ø коротко- и длиннопериодные варианты (всего ~ 700)
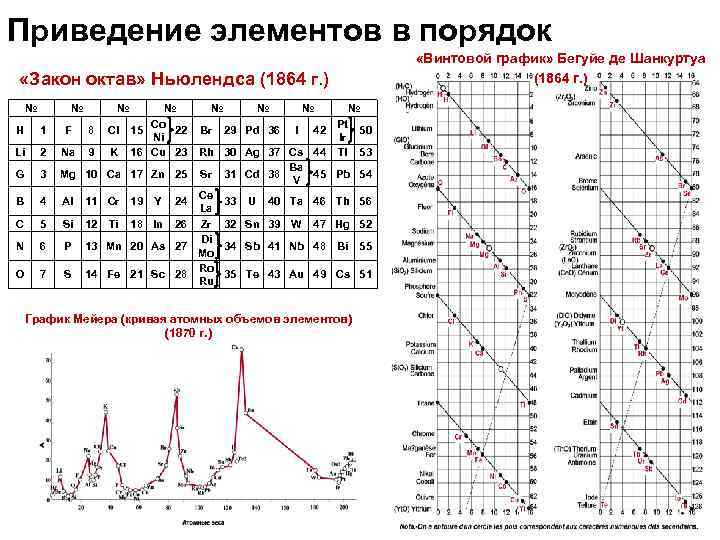
Приведение элементов в порядок «Винтовой график» Бегуйе де Шанкуртуа (1864 г. ) «Закон октав» Ньюлендса (1864 г. ) № № Co 15 22 Ni 16 Cu 23 H 1 F 8 Cl Li 2 Na 9 K G 3 Mg 10 Ca 17 Zn 25 B 4 Al 11 Cr 19 C 5 Si 12 N 6 P 13 Mn 20 As 27 O 7 S 14 Fe 21 Sc 28 Ti Y 24 18 In 26 № Br № 29 Pd 36 № I Rh 30 Ag 37 Cs Ba Sr 31 Cd 38 V Ce 33 U 40 Ta La Zr 32 Sn 39 W Di 34 Sb 41 Nb Mo Ro 35 Te 43 Au Ru 42 44 № Pt 50 Ir Tl 53 45 Pb 54 46 Th 56 47 Hg 52 48 Bi 55 49 Cs 51 График Мейера (кривая атомных объемов элементов) (1870 г. )
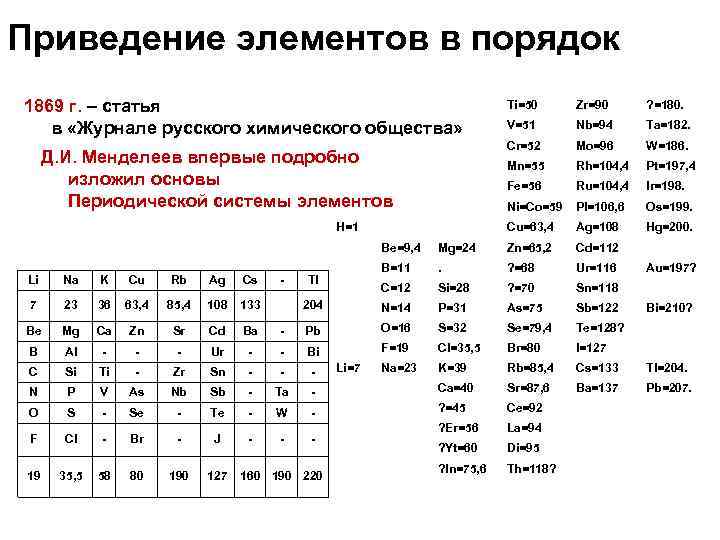
Приведение элементов в порядок 1869 г. – статья в «Журнале русского химического общества» ? =180. V=51 Nb=94 Ta=182. Mo=96 W=186. Mn=55 Rh=104, 4 Pt=197, 4 Fe=56 Ru=104, 4 Ir=198. Ni=Co=59 Pl=106, 6 Os=199. Cu=63, 4 H=1 Zr=90 Cr=52 Д. И. Менделеев впервые подробно изложил основы Периодической системы элементов Ti=50 Ag=108 Hg=200. Be=9, 4 Zn=65, 2 Cd=112 B=11 . ? =68 Ur=116 C=12 Si=28 ? =70 Sn=118 204 - Mg=24 N=14 P=31 As=75 Sb=122 Tl Au=197? Li Na K Cu Rb Ag Cs 7 23 36 63, 4 85, 4 108 133 Be Mg Ca Zn Sr Cd Ba - Pb O=16 S=32 Se=79, 4 Te=128? B Al - - - Ur - - Bi F=19 Cl=35, 5 Br=80 I=127 C Si Ti - Zr Sn - - - Na=23 K=39 Rb=85, 4 Cs=133 Tl=204. N P V As Nb Sb - Ta - Ca=40 Sr=87, 6 Ba=137 Pb=207. O S - Se - Te - W - ? =45 Ce=92 F Cl - Br - J - - - ? Er=56 La=94 ? Yt=60 Di=95 19 35, 5 58 80 190 127 ? In=75, 6 Th=118? 160 190 220 Li=7 Bi=210?

Периодический закон Д. И. Менделеева «Свойства простых тел, а так же формы и свойства соединений элементов находятся в прямой зависимости от атомных весов элементов»

Строение атома Атом – мельчайшая неделимая частица вещества В 1911 г. – планетарная модель V век до нашей эры … Размещение электронов на стационарных орбитах было очень важным шагом в понимании строения атома… противоречие с классической механикой: …при движении электрона по орбите он должен был терять потенциальную энергию и в конце концов "упасть" на ядро и атом должен был Э. Резерфорд прекратить свое существование… Демокрит В 1913 г. – постулаты Бора • электрон двигается по стационарным орбитам вокруг ядра • при нормальных условиях не поглощает и не испускает энергию Н. Бор 1920 -е годы – Л. де Бройль, В. Гейзенберг, Э. Шредингер, П. Дирак

Строение атома Атом – сложная электромагнитная система, включающая элементарные частицы – нуклоны (протоны, нейтроны) и электроны 10 -11 -10 -10, м Частица Символ Масса, а. е. м. Масса, г Заряд, e Протон Нейтрон Электрон Позитрон 1 p 1. 0073 1. 0087 0. 00055 1. 67· 10 -24 9. 1· 10 -28 +1 0 -1 +1 0 n ee+ Ядро (протоны и нейтроны) – определяют массу атома, заряд ядра и радиоактивные свойства 10 -15, м Электроны – определяют химические свойства Химический элемент – совокупность атомов с одинаковым зарядом ядра (числом протонов, числом электронов), совпадающим с порядковым (атомным) номером в таблице Менделеева Изотопы – разновидности атомов одного и того же химического элемента, различающиеся массовыми числами, но имеющие одинаковый заряд ядра Устойчивость атомного Легкие элементы: ~ 1 ядра: «число нейтронов/число протонов» Тяжелые элементы: ~ 1. 6

Квантово-механическая модель атома 1924 г. …волновые и корпускулярные свойства квантовой частицы фундаментальным образом взаимосвязаны… Л. де Бройль 1927 г. Принцип неопределенности В. Гейзенберг

Квантово-механическая модель атома Уравнение Шрёдингера (сферической стоячей волны) Э. Шрёдингер Величина, пропорциональная вероятности нахождения электрона в некотором объеме, окружающем точку с координатами x, y, z Электронная плотность Область пространства, в которой вероятность нахождения электрона составляет не менее 95%, называется атомной орбиталью, которая характеризуется определенной формой и расстоянием от ядра Состояние электрона в атоме полностью определяется четырьмя квантовыми числами, три из которых (n, l, ml) характеризуют электронную орбиталь, а четвертое (ms) – собственный момент электрона

Квантовые числа Квантовое число Принимаемые значения Характеризуемое свойство Главное (n) 1, 2, 3, …, ∞ Энергия (E) электронного уровня. Среднее расстояние от ядра n=∞ - отсутствует взаимодействие с ядром. E = 0 Орбитальное (l) 0, 1, …, (n-1) Всего n значений для данного n Орбитальный момент количества движения – форма орбитали Обычно используются буквенные символы: l: 0 1 2 3 4 spdfg Магнитное (ml) -l, …, 0, …, +l Всего 2 l+1 значение для данного l Ориентация момента количества движения – расположение орбитали в пространстве При помещении в магнитное поле орбитали с разными ml имеют разную энергию Спиновое (ms) ± 1/2 Не зависит от свойств орбитали Ориентация собственного магнитного момента электрона Обозначают ↑ или ↓ Примечание
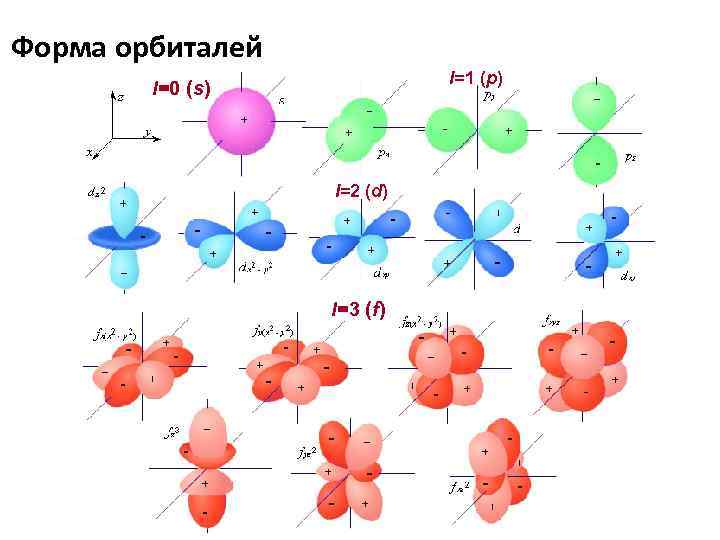
Форма орбиталей l=1 (p) l=0 (s) l=2 (d) l=3 (f)

Основные принципы заполнения орбиталей электронами Zэфф. – заряд, действующий на электрон внешнего уровня. Этот заряд меньше, чем истинный заряд ядра, т. к. внутренние электроны экранируют внешние 1. 2. В многоэлектронном атоме подуровни имеют различную энергию. Для одноэлектронного приближения их распределение по энергиям показано далее… Зависимость энергии орбитали от заряда ядра носит сложный немонотонный характер

Распределение орбиталей водородоподобного атома по энергиям E n=∞ n=6 n=5 6 s 5 s n=4 4 s n=3 5 p 3 d 3 p 2 p 2 s 1 s 4 d 4 p 3 s n=2 n=1 4 f

Основные принципы заполнения орбиталей электронами 1. Принцип наименьшей энергии В многоэлектронном атоме стабильной является такая конфигурация, для которой достигается минимум полной энергии. В первую очередь заполняются орбитали с наименьшей энергией, т. е. выполняется последовательность: 1 s<2 s<2 p<3 s<3 p<4 s<3 d<4 p<5 s<4 d<5 p<6 s<4 f<5 d<6 p<7 s<6 d<5 f Энергия орбиталей увеличивается в порядке возрастания суммы квантовых чисел n+l, а при одинаковой сумме этих чисел – в порядке возрастания главного квантового числа (Правило Клечковского)

Основные принципы заполнения орбиталей электронами 2. Принцип запрета Паули В атоме не существует двух электронов, состояние которых описывается одинаковым набором квантовых чисел (n, l, ms) Следовательно на одной орбитали (она характеризуется тремя квантовыми числами (n, l, ml) может находится не более двух электронов с разными значениями спинового квантового ↑ ↓) числа ( и 3. Правило Хунда В пределах одного подуровня (т. е. на орбиталях с одним и тем же значением l) электроны распределяются так, чтобы суммарный спин (Σms) был максимален
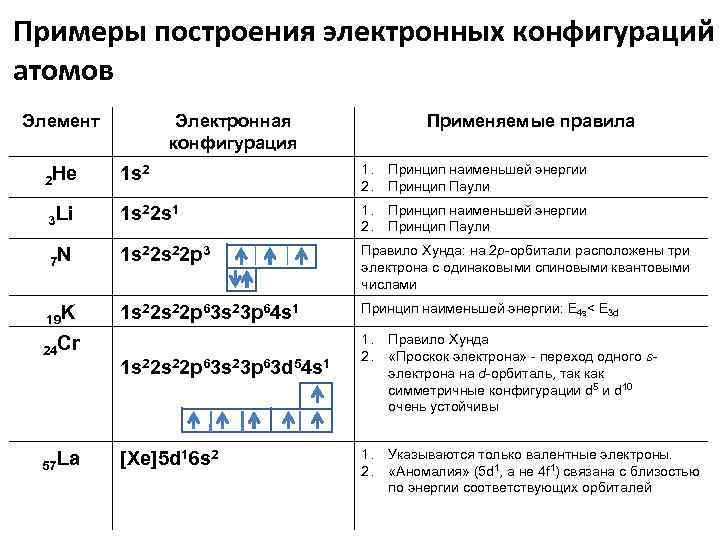
Примеры построения электронных конфигураций атомов Элемент Электронная конфигурация Применяемые правила 2 He 1 s 2 1. 2. Принцип наименьшей энергии Принцип Паули 3 Li 1 s 22 s 1 1. 2. Принцип наименьшей энергии Принцип Паули 7 N 1 s 22 p 3 Правило Хунда: на 2 p-орбитали расположены три электрона с одинаковыми спиновыми квантовыми числами 19 K 1 s 22 p 63 s 23 p 64 s 1 Принцип наименьшей энергии: E 4 s< E 3 d 24 Cr 57 La 1 s 22 p 63 s 23 p 63 d 54 s 1 [Xe]5 d 16 s 2 1. 2. Правило Хунда «Проскок электрона» - переход одного sэлектрона на d-орбиталь, так как симметричные конфигурации d 5 и d 10 очень устойчивы 1. 2. Указываются только валентные электроны. «Аномалия» (5 d 1, а не 4 f 1) связана с близостью по энергии соответствующих орбиталей

Основные характеристики атомов • Размер атома • Энергетические характеристики, включая потенциал ионизации и сродство к электрону • Спектральные характеристики (спектры испускания и поглощения) • Магнитные свойства
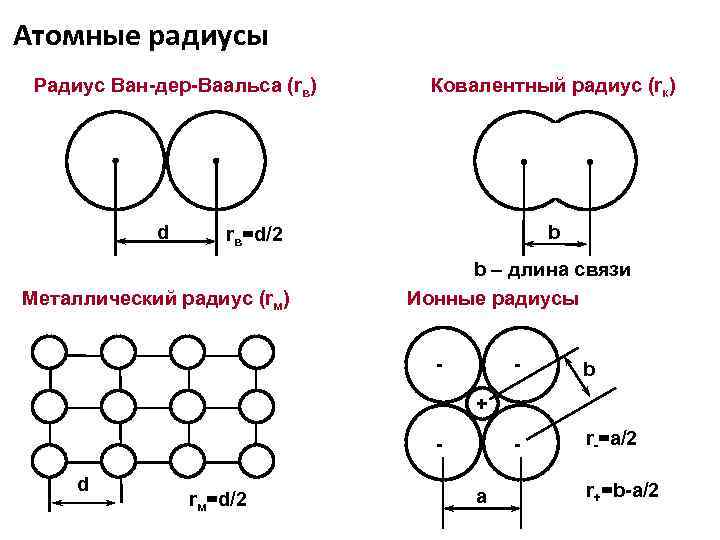
Атомные радиусы Радиус Ван-дер-Ваальса (rв) d Ковалентный радиус (rк) b rв=d/2 Металлический радиус (rм) b – длина связи Ионные радиусы - - b - r-=a/2 + d rм=d/2 a r+=b-a/2

Потенциал ионизации Минимальная энергия, которую необходимо затратить для удаления электрона из атома, находящегося в основном состоянии X → X++ e. I 1< I 2< I 3… <In - ПЕРВЫЙ ПОТЕНЦИАЛ ИОНИЗАЦИИ (I 1) Сродство к электрону Способность атома присоединять электрон с образованием отрицательно заряженного иона количественно характеризуется изменением энтальпии (энергии) процесса X + e- →X- СРОДСТВО К ЭЛЕКТРОНУ(A 1) A 1<A 2< A 3… <An Электроотрицательность по Малликену

Магнитный момент μэфф – эффективный магнитный момент Z<30 – основной вклад: собственный магнитный момент электрона – суммарный спин атома Т. к. в суммарный спин атома вклад вносят только неспаренные электроны (n), то Z>>30 – основной вклад: спин-орбитальное взаимодействие μэфф =0 (атом или ион, все электроны которого спарены) ДИАМАГНЕТИК μэфф ≠ 0 (атом или ион, имеющий неспаренные электроны) ПАРАМАГНЕТИК

Периодический закон Д. И. Менделеева Ti=50 Zr=90 ? =180. V=51 Nb=94 Ta=182. 204 Cr=52 Mo=96 W=186. - Pb Mn=55 Rh=104, 4 Pt=197, 4 - - Bi Fe=56 Ru=104, 4 Ir=198. Sn - - - Ni=Co=59 Pl=106, 6 Os=199. Nb Sb - Ta - Cu=63, 4 Ag=108 Hg=200. Se - Te - W - - Br - J - - - 58 80 190 127 Li Na K Cu Rb Ag Cs 7 23 36 63, 4 85, 4 108 133 Be Mg Ca Zn Sr Cd Ba B Al - - - Ur C Si Ti - Zr N P V As O S - F Cl 19 35, 5 - Tl H=1 Be=9, 4 Cd=112 . ? =68 Ur=116 C=12 Si=28 ? =70 Sn=118 N=14 P=31 As=75 Sb=122 O=16 S=32 Se=79, 4 Te=128? F=19 Li=7 Zn=65, 2 B=11 160 190 220 Mg=24 Cl=35, 5 Br=80 I=127 Na=23 K=39 Rb=85, 4 Cs=133 Tl=204. Ca=40 Sr=87, 6 Ba=137 Pb=207. ? =45 Ce=92 ? Er=56 La=94 ? Yt=60 Di=95 ? In=75, 6 Th=118? «Свойства простых тел, а так же формы и свойства соединений элементов находятся в прямой зависимости от атомных весов элементов» 1869 г. – статья в журнале Русского Химического общества» Au=197? Bi=210?

Периодический закон Д. И. Менделеева «Свойства простых тел, а так же формы и свойства соединений элементов находятся в прямой зависимости от атомных весов элементов» 1869 г. – статья в «Журнале русского химического общества» «Свойства простых веществ, а так же формы и свойства соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов» современная формулировка, отражающая влияние строения атома на его химическую индивидуальность

Периодическая система элементов Периодичность свойств ↕ Периодичность заселения электронных уровней Элементы – полные электронные аналоги – сходство во всех степенях окисления Элементы – неполные электронные аналоги – сходство не во всех степенях окисления
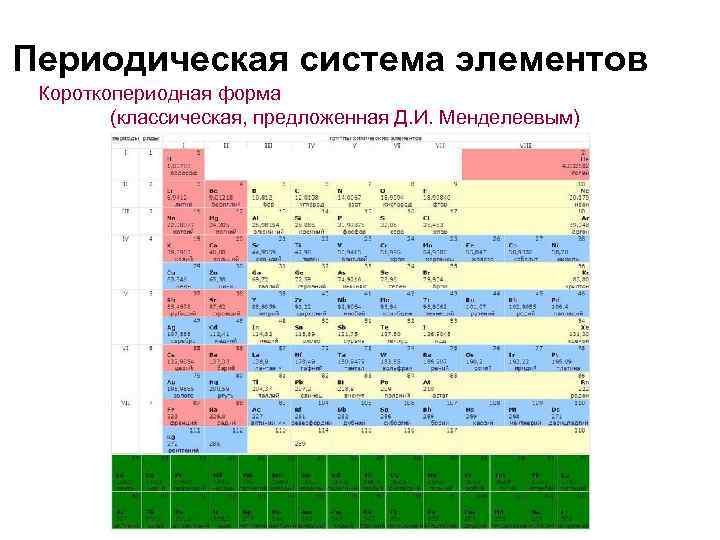
Периодическая система элементов Короткопериодная форма (классическая, предложенная Д. И. Менделеевым)
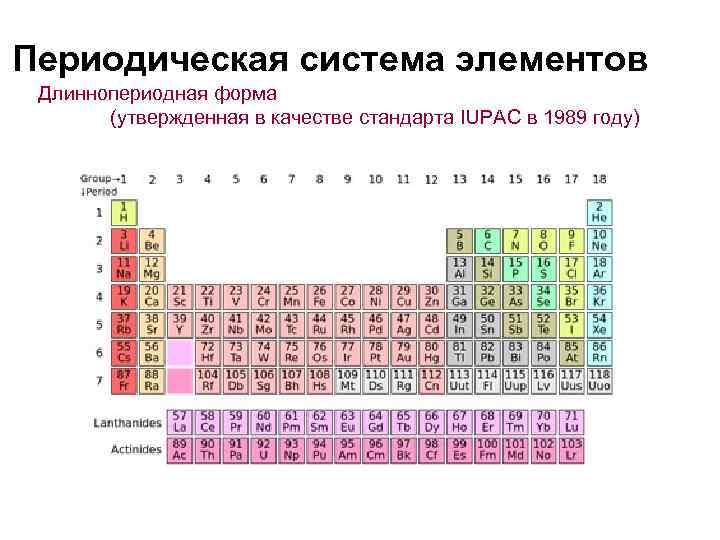
Периодическая система элементов Длиннопериодная форма (утвержденная в качестве стандарта IUPAC в 1989 году)
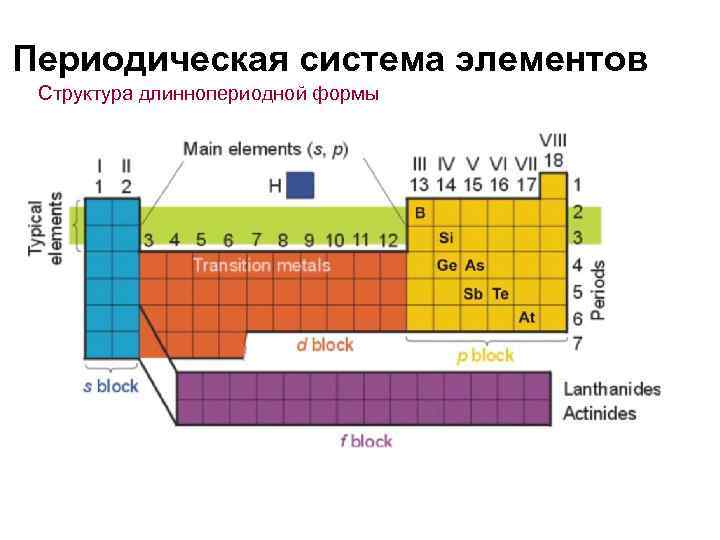
Периодическая система элементов Структура длиннопериодной формы
![Периодическая система элементов I A: Li, Na, K, Rb, Cs, Fr 1 [ ] Периодическая система элементов I A: Li, Na, K, Rb, Cs, Fr 1 [ ]](https://present5.com/presentation/3/-97575656_437392574.pdf-img/-97575656_437392574.pdf-31.jpg)
Периодическая система элементов I A: Li, Na, K, Rb, Cs, Fr 1 [ ] ns 1 щелочные металлы H – особый элемент 1 s 1 II A: Be, Mg, Ca, Sr, Ba, Ra 2 [ ] ns 2 щелочноземельные металлы H+ HIII A: B, Al, Ga, In, Tl 13 [ ] ns 2 np 1 IV A: C, Si, Ge, Sn, Pb, Fl 14 [ ] ns 2 np 2 V A: N, P, As, Sb, Bi 15 [ ] ns 2 np 3 пниктогены VI A: O, S, Se, Te, Po, Lv 16 [ ] ns 2 np 4 халькогены VII A: F, Cl, Br, I, At 17 [ ] ns 2 np 5 галогены O: He, Ne, Ar, Kr, Xe, Rn 18 1 s 2 [ ] ns 2 np 6 инертные газы 3→ 12 3 d – элементы (Sc → Zn) 4 d – элементы (Y → Cd) 5 d – элементы (La → Hg) 6 d – элементы (Ac, Th, Lr → Cn) 4 f – элементы (Ce → Lu) 5 f – элементы (Pa → No)
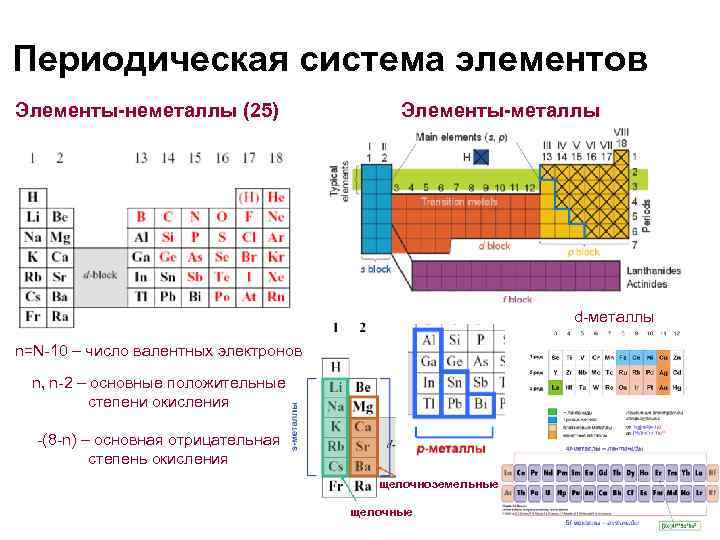
Периодическая система элементов Элементы-неметаллы (25) Элементы-металлы d-металлы n=N-10 – число валентных электронов n, n-2 – основные положительные степени окисления -(8 -n) – основная отрицательная степень окисления щелочноземельные щелочные
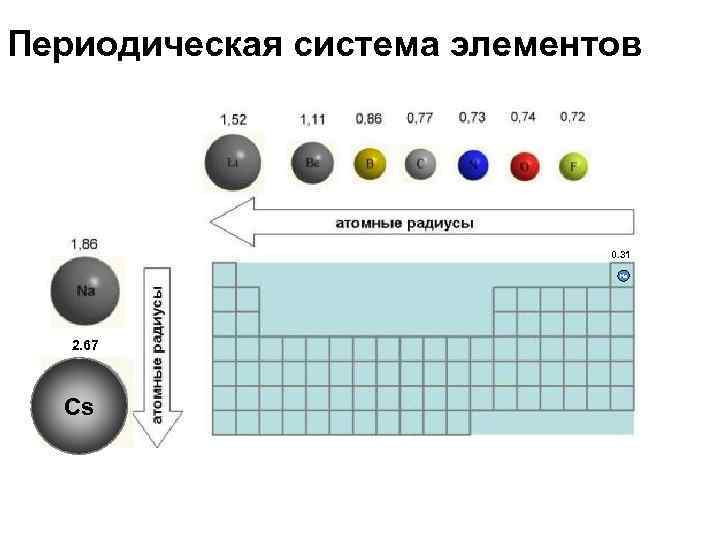
Периодическая система элементов 0. 31 He 2. 67 Cs
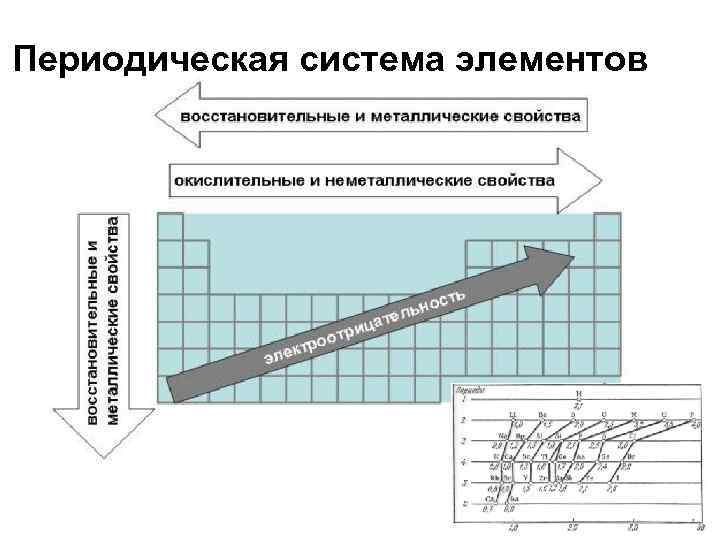
Периодическая система элементов

Периодическая система элементов А дальше?
Лекция_1_Периодический закон.ppt