ФАРМХИМИЯ реакции подлинности Л.В.ppt
- Количество слайдов: 48
 КАФЕДРА ФАРМАЦЕВТИЧЕСКОЙ ХИМИИ РЕАКЦИИ ПОДЛИННОСТИ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ. 1
КАФЕДРА ФАРМАЦЕВТИЧЕСКОЙ ХИМИИ РЕАКЦИИ ПОДЛИННОСТИ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ. 1
 K + KCl, KBr, KJ, CH 3 COOK, бензилпенициллина K соль и т. д. 1. Реакция с виннокаменной кислотой: + K + + CH 3 COONa на холоду, потирание стеклянной палочкой +H белый мелкокристл осадок 2. Окрашивание пламени в фиолетовый цвет. 2
K + KCl, KBr, KJ, CH 3 COOK, бензилпенициллина K соль и т. д. 1. Реакция с виннокаменной кислотой: + K + + CH 3 COONa на холоду, потирание стеклянной палочкой +H белый мелкокристл осадок 2. Окрашивание пламени в фиолетовый цвет. 2
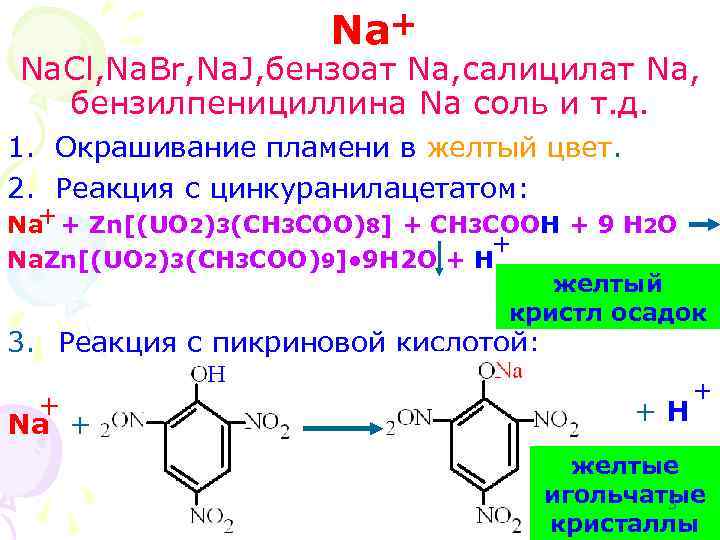 Na+ Na. Cl, Na. Br, Na. J, бензоат Na, салицилат Na, бензилпенициллина Na соль и т. д. 1. Окрашивание пламени в желтый цвет. 2. Реакция с цинкуранилацетатом: + Na + Zn[(UO 2)3(CH 3 COO)8] + CH 3 COOH + 9 H 2 O + Na. Zn[(UO 2)3(CH 3 COO)9]● 9 H 2 O + H желтый кристл осадок 3. Реакция с пикриновой кислотой: + Na + +H + желтые игольчатые 3 кристаллы
Na+ Na. Cl, Na. Br, Na. J, бензоат Na, салицилат Na, бензилпенициллина Na соль и т. д. 1. Окрашивание пламени в желтый цвет. 2. Реакция с цинкуранилацетатом: + Na + Zn[(UO 2)3(CH 3 COO)8] + CH 3 COOH + 9 H 2 O + Na. Zn[(UO 2)3(CH 3 COO)9]● 9 H 2 O + H желтый кристл осадок 3. Реакция с пикриновой кислотой: + Na + +H + желтые игольчатые 3 кристаллы
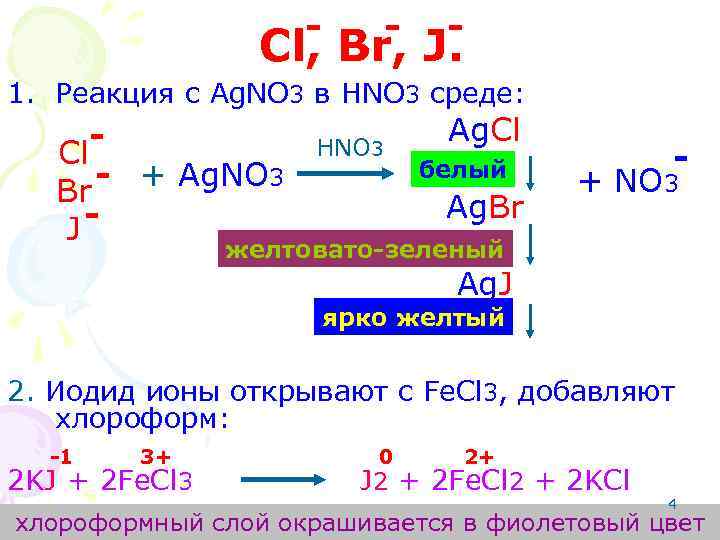 - - - Cl, Br, J. 1. Реакция с Ag. NO 3 в HNO 3 среде: Cl - + Ag. NO 3 Br J HNO 3 Ag. Cl белый Ag. Br - + NO 3 желтовато-зеленый Ag. J ярко желтый 2. Иодид ионы открывают с Fe. Cl 3, добавляют хлороформ: -1 3+ 2 KJ + 2 Fe. Cl 3 0 2+ J 2 + 2 Fe. Cl 2 + 2 KCl 4 хлороформный слой окрашивается в фиолетовый цвет
- - - Cl, Br, J. 1. Реакция с Ag. NO 3 в HNO 3 среде: Cl - + Ag. NO 3 Br J HNO 3 Ag. Cl белый Ag. Br - + NO 3 желтовато-зеленый Ag. J ярко желтый 2. Иодид ионы открывают с Fe. Cl 3, добавляют хлороформ: -1 3+ 2 KJ + 2 Fe. Cl 3 0 2+ J 2 + 2 Fe. Cl 2 + 2 KCl 4 хлороформный слой окрашивается в фиолетовый цвет
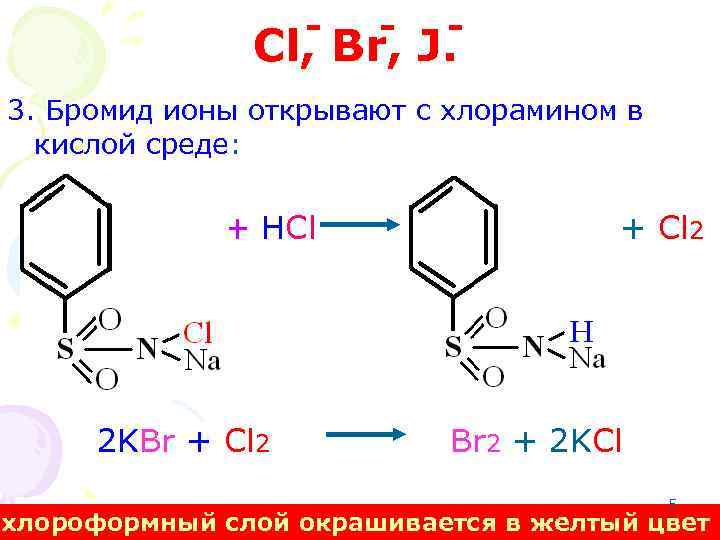 - - - Cl, Br, J. 3. Бромид ионы открывают с хлорамином в кислой среде: + HCl 2 KBr + Cl 2 Br 2 + 2 KCl 5 хлороформный слой окрашивается в желтый цвет
- - - Cl, Br, J. 3. Бромид ионы открывают с хлорамином в кислой среде: + HCl 2 KBr + Cl 2 Br 2 + 2 KCl 5 хлороформный слой окрашивается в желтый цвет
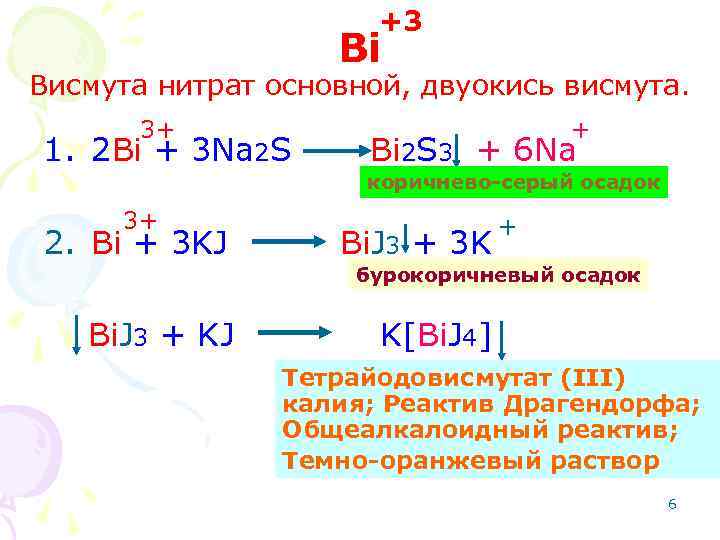 +3 Bi Висмута нитрат основной, двуокись висмута. 3+ 1. 2 Bi + 3 Na 2 S + Bi 2 S 3 + 6 Na коричнево-серый осадок 3+ 2. Bi + 3 KJ Bi. J 3 + 3 K + бурокоричневый осадок Bi. J 3 + KJ K[Bi. J 4] Тетрайодовисмутат (III) калия; Реактив Драгендорфа; Общеалкалоидный реактив; Темно-оранжевый раствор 6
+3 Bi Висмута нитрат основной, двуокись висмута. 3+ 1. 2 Bi + 3 Na 2 S + Bi 2 S 3 + 6 Na коричнево-серый осадок 3+ 2. Bi + 3 KJ Bi. J 3 + 3 K + бурокоричневый осадок Bi. J 3 + KJ K[Bi. J 4] Тетрайодовисмутат (III) калия; Реактив Драгендорфа; Общеалкалоидный реактив; Темно-оранжевый раствор 6
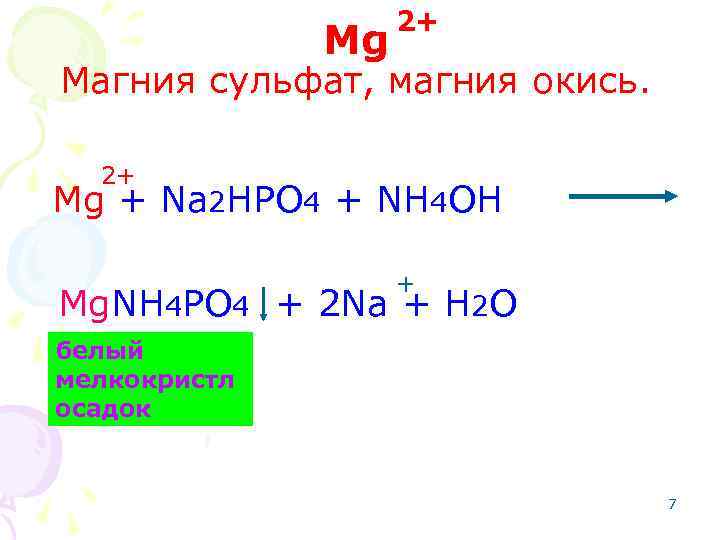 Mg 2+ Магния сульфат, магния окись. 2+ Mg + Na 2 HPO 4 + NH 4 OH + Mg. NH 4 PO 4 + 2 Na + H 2 O белый мелкокристл осадок 7
Mg 2+ Магния сульфат, магния окись. 2+ Mg + Na 2 HPO 4 + NH 4 OH + Mg. NH 4 PO 4 + 2 Na + H 2 O белый мелкокристл осадок 7
 2+ Zn Цинка окись, цинка сульфат. 2+ 1. Zn + Na 2 S + Zn. S + 2 Na белый осадок 2. Реакция с гексацианоферратом (II) калия (желтая кровяная соль): 2+ 3 Zn + 2 K 4[Fe(CN)6] + Zn 3 K 2[Fe(CN)6]2 + 6 K студенистый белый осадок 3. Zn. O при нагревании желтеет , при охлаждении белеет. 8
2+ Zn Цинка окись, цинка сульфат. 2+ 1. Zn + Na 2 S + Zn. S + 2 Na белый осадок 2. Реакция с гексацианоферратом (II) калия (желтая кровяная соль): 2+ 3 Zn + 2 K 4[Fe(CN)6] + Zn 3 K 2[Fe(CN)6]2 + 6 K студенистый белый осадок 3. Zn. O при нагревании желтеет , при охлаждении белеет. 8
![Ag. NO 3 1. Ag. NO 3 +2 NH 4 OH [Ag(NH 3)2]NO 3 Ag. NO 3 1. Ag. NO 3 +2 NH 4 OH [Ag(NH 3)2]NO 3](https://present5.com/presentation/3/136509829_437200460.pdf-img/136509829_437200460.pdf-9.jpg) Ag. NO 3 1. Ag. NO 3 +2 NH 4 OH [Ag(NH 3)2]NO 3 +2 H 2 O аммиачный раствор нитрата серебра 0 +H 2 Ot C серебристый осадок 2. Ag. NO 3 + HCl Ag. Cl + HNO 3 белый творожистый осадок 9
Ag. NO 3 1. Ag. NO 3 +2 NH 4 OH [Ag(NH 3)2]NO 3 +2 H 2 O аммиачный раствор нитрата серебра 0 +H 2 Ot C серебристый осадок 2. Ag. NO 3 + HCl Ag. Cl + HNO 3 белый творожистый осадок 9
![Cu. SO 4 1. Cu. SO 4 + 4 NH 4 OH [Cu(NH 3)4]SO Cu. SO 4 1. Cu. SO 4 + 4 NH 4 OH [Cu(NH 3)4]SO](https://present5.com/presentation/3/136509829_437200460.pdf-img/136509829_437200460.pdf-10.jpg) Cu. SO 4 1. Cu. SO 4 + 4 NH 4 OH [Cu(NH 3)4]SO 4 + 4 H 2 O комлексное соединение синего цвета 10
Cu. SO 4 1. Cu. SO 4 + 4 NH 4 OH [Cu(NH 3)4]SO 4 + 4 H 2 O комлексное соединение синего цвета 10
 Fe 2+ Fe. SO 4, ферроцерон. Реакция с гексацианоферратом(III) калия 3 Fe. SO 4 + 2 K 3[Fe(CN)6] Fe 3[Fe(CN)6]2 + 3 K 2 SO 4 осадок турнбулевого синего 11
Fe 2+ Fe. SO 4, ферроцерон. Реакция с гексацианоферратом(III) калия 3 Fe. SO 4 + 2 K 3[Fe(CN)6] Fe 3[Fe(CN)6]2 + 3 K 2 SO 4 осадок турнбулевого синего 11
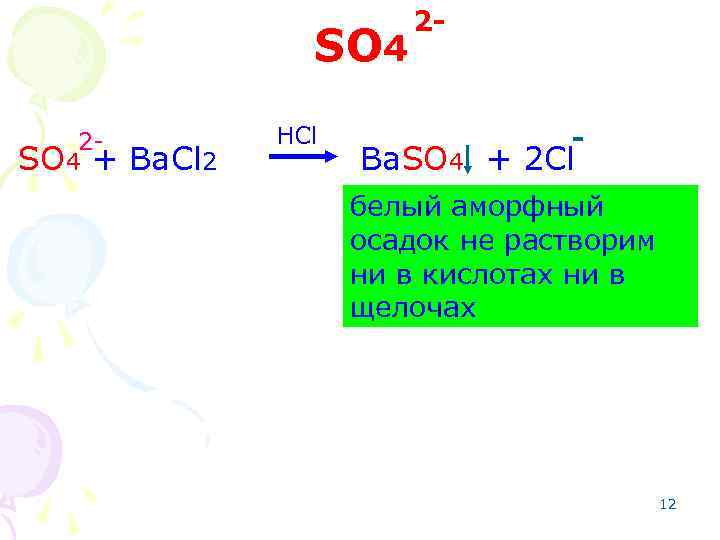 SO 4 2 SO 4 + Ba. Cl 2 HCl 2 - - Ba. SO 4 + 2 Cl белый аморфный осадок не растворим ни в кислотах ни в щелочах 12
SO 4 2 SO 4 + Ba. Cl 2 HCl 2 - - Ba. SO 4 + 2 Cl белый аморфный осадок не растворим ни в кислотах ни в щелочах 12
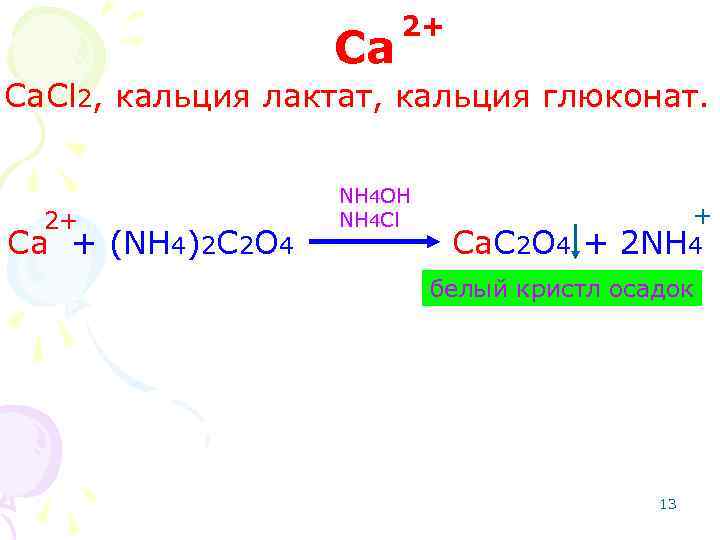 Ca 2+ Ca. Cl 2, кальция лактат, кальция глюконат. 2+ Ca + (NH 4)2 C 2 O 4 NH 4 OH NH 4 Cl Ca. C 2 O 4 + + 2 NH 4 белый кристл осадок 13
Ca 2+ Ca. Cl 2, кальция лактат, кальция глюконат. 2+ Ca + (NH 4)2 C 2 O 4 NH 4 OH NH 4 Cl Ca. C 2 O 4 + + 2 NH 4 белый кристл осадок 13
 Ba. SO 4 для рентгеноскопии. Он не растворим ни в воде, ни в кислотах, ни в щелочах. Чтобы определить его подлинность поступают следующим образом: его помещают в пробирку, добавляют Na 2 CO 3 и кипятят: t 0 Ba. SO 4 + Na 2 CO 3 Ba. CO 3 + Na 2 SO 4 Затем охлаждают, фильтруют и в фильтрате определяют: 2 SO 4 + Ba. Cl 2 Ba. SO 4 + 2 Cl На фильтре осадок Ba. CO 3 растворяют в разведенной HCl: H 2 SO 4 Ba. CO 3 + HCl H 2 O + CO 2 + Ba. Cl 2 K 2 Cr 2 O 4 Ba. Cr. O 4 кирпично 14 -красный
Ba. SO 4 для рентгеноскопии. Он не растворим ни в воде, ни в кислотах, ни в щелочах. Чтобы определить его подлинность поступают следующим образом: его помещают в пробирку, добавляют Na 2 CO 3 и кипятят: t 0 Ba. SO 4 + Na 2 CO 3 Ba. CO 3 + Na 2 SO 4 Затем охлаждают, фильтруют и в фильтрате определяют: 2 SO 4 + Ba. Cl 2 Ba. SO 4 + 2 Cl На фильтре осадок Ba. CO 3 растворяют в разведенной HCl: H 2 SO 4 Ba. CO 3 + HCl H 2 O + CO 2 + Ba. Cl 2 K 2 Cr 2 O 4 Ba. Cr. O 4 кирпично 14 -красный
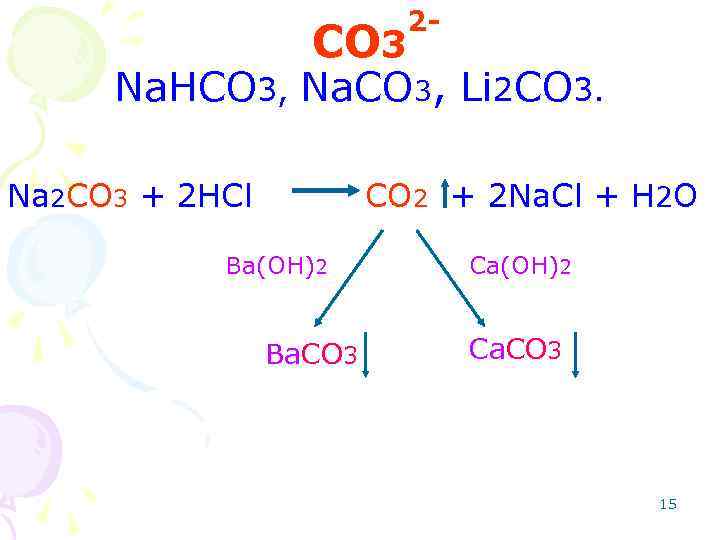 2 - CO 3 Na. HCO 3, Na. CO 3, Li 2 CO 3. Na 2 CO 3 + 2 HCl CO 2 + 2 Na. Cl + H 2 O Ba(OH)2 Ba. CO 3 Ca(OH)2 Ca. CO 3 15
2 - CO 3 Na. HCO 3, Na. CO 3, Li 2 CO 3. Na 2 CO 3 + 2 HCl CO 2 + 2 Na. Cl + H 2 O Ba(OH)2 Ba. CO 3 Ca(OH)2 Ca. CO 3 15
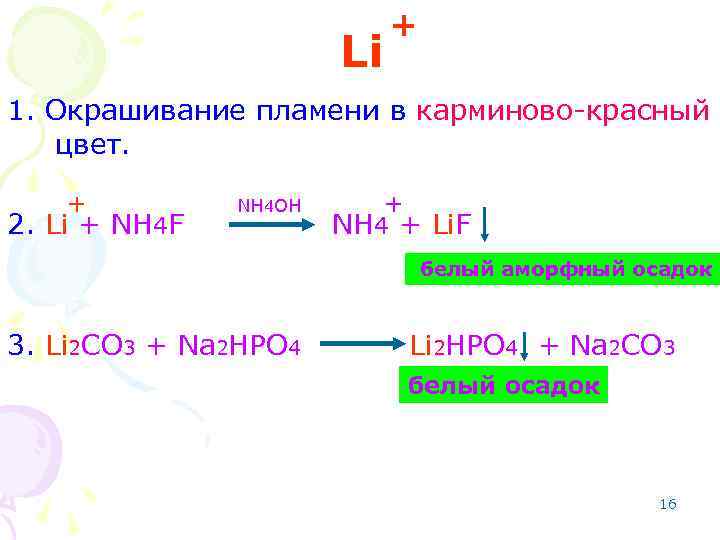 Li + 1. Окрашивание пламени в карминово-красный цвет. + 2. Li + NH 4 F NH 4 OH + NH 4 + Li. F белый аморфный осадок 3. Li 2 CO 3 + Na 2 HPO 4 Li 2 HPO 4 + Na 2 CO 3 белый осадок 16
Li + 1. Окрашивание пламени в карминово-красный цвет. + 2. Li + NH 4 F NH 4 OH + NH 4 + Li. F белый аморфный осадок 3. Li 2 CO 3 + Na 2 HPO 4 Li 2 HPO 4 + Na 2 CO 3 белый осадок 16
 BO 3 3 - Борная кислота, тетраборат натрия. 1. Реакция с куркумовой бумагой. Химизм смотри учебник В. Г. Беликов, 2003 год, стр. 189. 2. Образование борноэтилового эфира: OH B OH OH + 3 HO-H 5 C 2 H 2 SO 4 (k) -3 H 2 O B OC 2 H 5 горит зеленым пламенем 17
BO 3 3 - Борная кислота, тетраборат натрия. 1. Реакция с куркумовой бумагой. Химизм смотри учебник В. Г. Беликов, 2003 год, стр. 189. 2. Образование борноэтилового эфира: OH B OH OH + 3 HO-H 5 C 2 H 2 SO 4 (k) -3 H 2 O B OC 2 H 5 горит зеленым пламенем 17
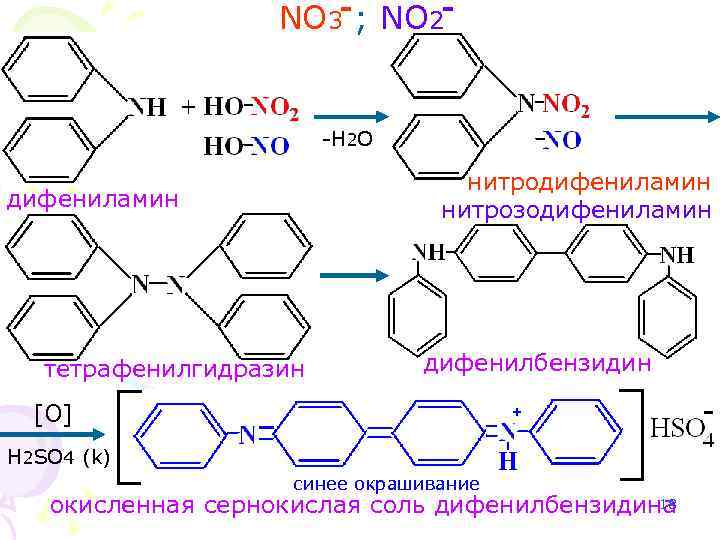 NO 3 - ; NO 2 - -H 2 O нитродифениламин нитрозодифениламин тетрафенилгидразин дифенилбензидин [O] H 2 SO 4 (k) синее окрашивание 18 окисленная сернокислая соль дифенилбензидина
NO 3 - ; NO 2 - -H 2 O нитродифениламин нитрозодифениламин тетрафенилгидразин дифенилбензидин [O] H 2 SO 4 (k) синее окрашивание 18 окисленная сернокислая соль дифенилбензидина
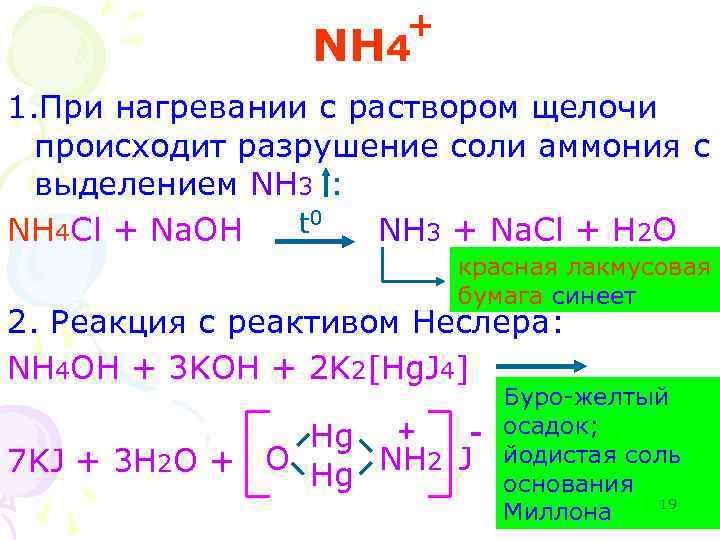 + NH 4 1. При нагревании с раствором щелочи происходит разрушение соли аммония с выделением NH 3 : t 0 NH 4 Cl + Na. OH NH 3 + Na. Cl + H 2 O красная лакмусовая бумага синеет 2. Реакция с реактивом Неслера: NH 4 OH + 3 KOH + 2 K 2[Hg. J 4] Hg 7 KJ + 3 H 2 O + O Hg Буро-желтый + - осадок; NH 2 J йодистая соль основания 19 Миллона
+ NH 4 1. При нагревании с раствором щелочи происходит разрушение соли аммония с выделением NH 3 : t 0 NH 4 Cl + Na. OH NH 3 + Na. Cl + H 2 O красная лакмусовая бумага синеет 2. Реакция с реактивом Неслера: NH 4 OH + 3 KOH + 2 K 2[Hg. J 4] Hg 7 KJ + 3 H 2 O + O Hg Буро-желтый + - осадок; NH 2 J йодистая соль основания 19 Миллона
 ОРГАНИЧЕСКИЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА Особенности анализа галогенпроизводных (этилхлорид, фторэтан, хлороформ, йодоформ). 20
ОРГАНИЧЕСКИЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА Особенности анализа галогенпроизводных (этилхлорид, фторэтан, хлороформ, йодоформ). 20
 1. Галоген связан ковалентной связью, проводят процесс минерализации с целью перевода галогена в ионогенное состояние. 2. Если лекарственные вещества содержат хлор, бром , то их переводят в ионогенное состояние путем нагревания с крепким раствором гидроксида натрия (30%) или сухим карбонатом натрия. Для определения фтора препарат нагревают с металлическим натрием (жесткая минерализация). 3. Если лекарственные вещества содержат йод, то минерализацию проводят с концентрированными серной или азотной кислотами при нагревании. При 2 этом выделяется фиолетовые пары йода. 1
1. Галоген связан ковалентной связью, проводят процесс минерализации с целью перевода галогена в ионогенное состояние. 2. Если лекарственные вещества содержат хлор, бром , то их переводят в ионогенное состояние путем нагревания с крепким раствором гидроксида натрия (30%) или сухим карбонатом натрия. Для определения фтора препарат нагревают с металлическим натрием (жесткая минерализация). 3. Если лекарственные вещества содержат йод, то минерализацию проводят с концентрированными серной или азотной кислотами при нагревании. При 2 этом выделяется фиолетовые пары йода. 1
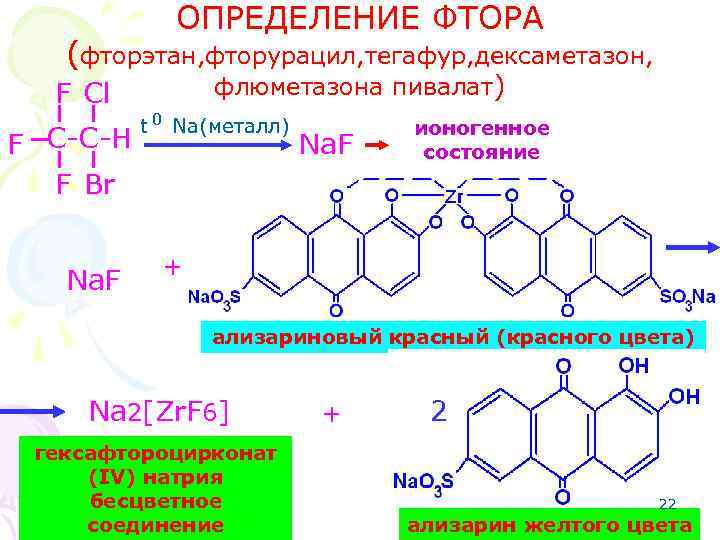 ОПРЕДЕЛЕНИЕ ФТОРА (фторэтан, фторурацил, тегафур, дексаметазон, флюметазона пивалат) F Cl F C-C-H F Br Na. F t 0 Na(металл) Na. F ионогенное состояние + ализариновый красный (красного цвета) Na 2[Zr. F 6] гексафтороцирконат (IV) натрия бесцветное соединение + 2 22 ализарин желтого цвета
ОПРЕДЕЛЕНИЕ ФТОРА (фторэтан, фторурацил, тегафур, дексаметазон, флюметазона пивалат) F Cl F C-C-H F Br Na. F t 0 Na(металл) Na. F ионогенное состояние + ализариновый красный (красного цвета) Na 2[Zr. F 6] гексафтороцирконат (IV) натрия бесцветное соединение + 2 22 ализарин желтого цвета
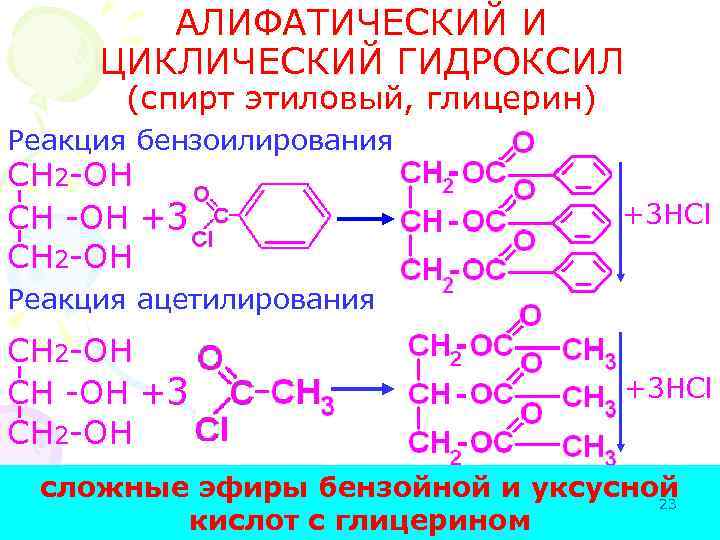 АЛИФАТИЧЕСКИЙ И ЦИКЛИЧЕСКИЙ ГИДРОКСИЛ (спирт этиловый, глицерин) Реакция бензоилирования CH 2 -OH CH -OH +3 CH 2 -OH +3 HCl Реакция ацетилирования CH 2 -OH CH -OH +3 CH 2 -OH +3 HCl сложные эфиры бензойной и уксусной 23 кислот с глицерином
АЛИФАТИЧЕСКИЙ И ЦИКЛИЧЕСКИЙ ГИДРОКСИЛ (спирт этиловый, глицерин) Реакция бензоилирования CH 2 -OH CH -OH +3 CH 2 -OH +3 HCl Реакция ацетилирования CH 2 -OH CH -OH +3 CH 2 -OH +3 HCl сложные эфиры бензойной и уксусной 23 кислот с глицерином
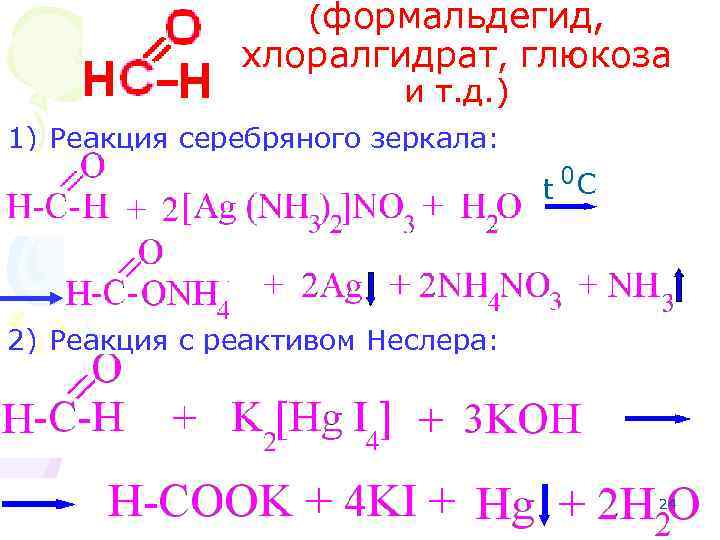 (формальдегид, хлоралгидрат, глюкоза и т. д. ) 1) Реакция серебряного зеркала: t 0 C 2) Реакция с реактивом Неслера: 24
(формальдегид, хлоралгидрат, глюкоза и т. д. ) 1) Реакция серебряного зеркала: t 0 C 2) Реакция с реактивом Неслера: 24
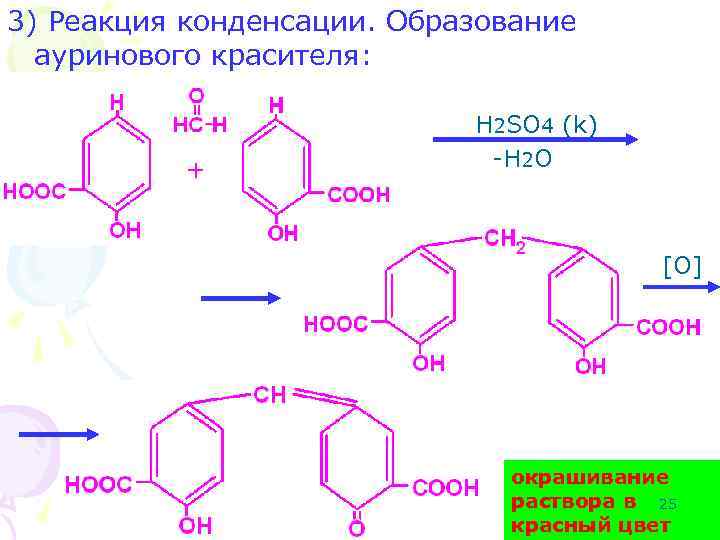 3) Реакция конденсации. Образование ауринового красителя: + H 2 SO 4 (k) -H 2 O [O] окрашивание раствора в 25 красный цвет
3) Реакция конденсации. Образование ауринового красителя: + H 2 SO 4 (k) -H 2 O [O] окрашивание раствора в 25 красный цвет
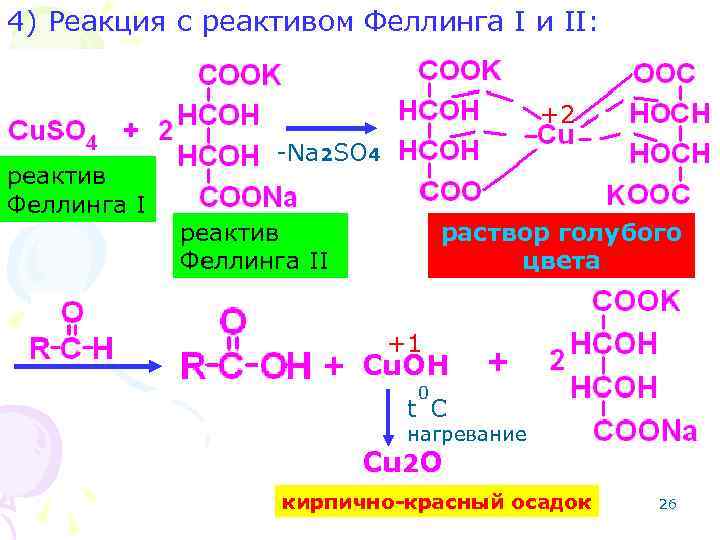 4) Реакция с реактивом Феллинга I и II: +2 реактив Феллинга I -Na 2 SO 4 реактив Феллинга II раствор голубого цвета +1 + Cu. OH + 0 t C нагревание Cu 2 O кирпично-красный осадок 26
4) Реакция с реактивом Феллинга I и II: +2 реактив Феллинга I -Na 2 SO 4 реактив Феллинга II раствор голубого цвета +1 + Cu. OH + 0 t C нагревание Cu 2 O кирпично-красный осадок 26
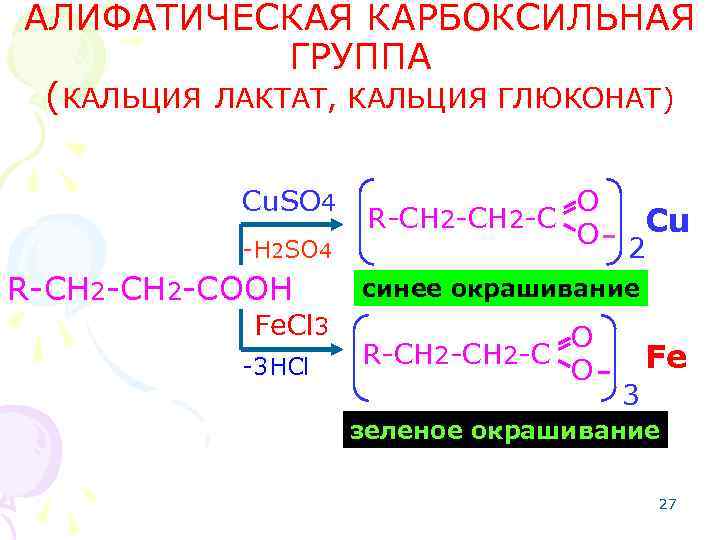 АЛИФАТИЧЕСКАЯ КАРБОКСИЛЬНАЯ ГРУППА (КАЛЬЦИЯ ЛАКТАТ, КАЛЬЦИЯ ГЛЮКОНАТ) Cu. SO 4 -H 2 SO 4 R-CH 2 -COOH Fe. Cl 3 -3 HCl O R-CH 2 -C O Cu 2 синее окрашивание O R-CH 2 -C O Fe 3 зеленое окрашивание 27
АЛИФАТИЧЕСКАЯ КАРБОКСИЛЬНАЯ ГРУППА (КАЛЬЦИЯ ЛАКТАТ, КАЛЬЦИЯ ГЛЮКОНАТ) Cu. SO 4 -H 2 SO 4 R-CH 2 -COOH Fe. Cl 3 -3 HCl O R-CH 2 -C O Cu 2 синее окрашивание O R-CH 2 -C O Fe 3 зеленое окрашивание 27
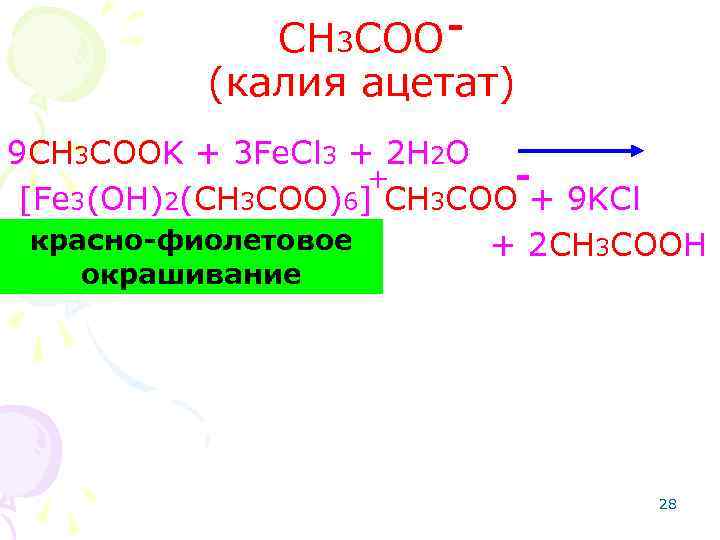 СH 3 COO (калия ацетат) 9 CH 3 COOK + 3 Fe. Cl 3 + 2 H 2 O + [Fe 3(OH)2(CH 3 COO)6] CH 3 COO + 9 KCl красно-фиолетовое + 2 CH 3 COOH окрашивание 28
СH 3 COO (калия ацетат) 9 CH 3 COOK + 3 Fe. Cl 3 + 2 H 2 O + [Fe 3(OH)2(CH 3 COO)6] CH 3 COO + 9 KCl красно-фиолетовое + 2 CH 3 COOH окрашивание 28
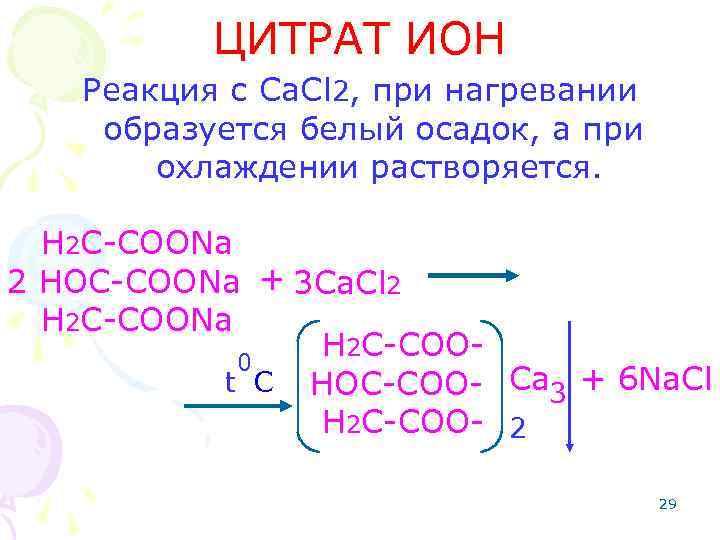 ЦИТРАТ ИОН Реакция с Ca. Cl 2, при нагревании образуется белый осадок, а при охлаждении растворяется. H 2 C-COONa 2 HOC-COONa + 3 Ca. Cl 2 H 2 C-COONa H 2 C-COO 0 t C HOC-COO- Ca 3 + 6 Na. Cl H 2 C-COO- 2 29
ЦИТРАТ ИОН Реакция с Ca. Cl 2, при нагревании образуется белый осадок, а при охлаждении растворяется. H 2 C-COONa 2 HOC-COONa + 3 Ca. Cl 2 H 2 C-COONa H 2 C-COO 0 t C HOC-COO- Ca 3 + 6 Na. Cl H 2 C-COO- 2 29
 АЛИФАТИЧЕСКАЯ АМИНОГРУППА Реакция с нингидрином сине-фиолетовое окрашивание. 30
АЛИФАТИЧЕСКАЯ АМИНОГРУППА Реакция с нингидрином сине-фиолетовое окрашивание. 30
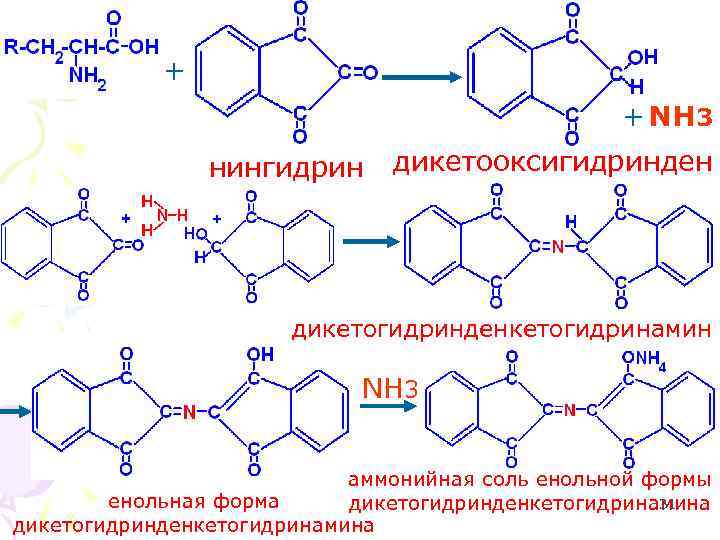 + + NH 3 нингидрин дикетооксигидринден дикетогидринденкетогидринамин NH 3 аммонийная соль енольной формы енольная форма 31 дикетогидринденкетогидринамина
+ + NH 3 нингидрин дикетооксигидринден дикетогидринденкетогидринамин NH 3 аммонийная соль енольной формы енольная форма 31 дикетогидринденкетогидринамина
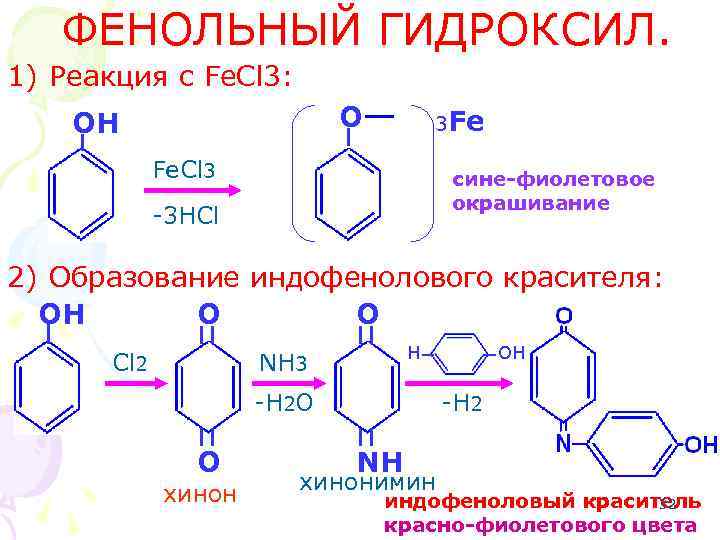 ФЕНОЛЬНЫЙ ГИДРОКСИЛ. 1) Реакция с Fe. Cl 3: O OH 3 Fe Fe. Cl 3 сине-фиолетовое окрашивание -3 HCl 2) Образование индофенолового красителя: OH O O Cl 2 H NH 3 -H 2 O O хинон OH -H 2 NH хинонимин индофеноловый краситель 32 красно-фиолетового цвета
ФЕНОЛЬНЫЙ ГИДРОКСИЛ. 1) Реакция с Fe. Cl 3: O OH 3 Fe Fe. Cl 3 сине-фиолетовое окрашивание -3 HCl 2) Образование индофенолового красителя: OH O O Cl 2 H NH 3 -H 2 O O хинон OH -H 2 NH хинонимин индофеноловый краситель 32 красно-фиолетового цвета
 АРОМАТИЧЕСКОЕ КОЛЬЦО. Реакции электрофильного замещения. Это реакции бромирования, йодирования, нитрования. Фенольный гидроксил - ориентант I рода, направляет последующие заместители в орто и пара положения. 33
АРОМАТИЧЕСКОЕ КОЛЬЦО. Реакции электрофильного замещения. Это реакции бромирования, йодирования, нитрования. Фенольный гидроксил - ориентант I рода, направляет последующие заместители в орто и пара положения. 33
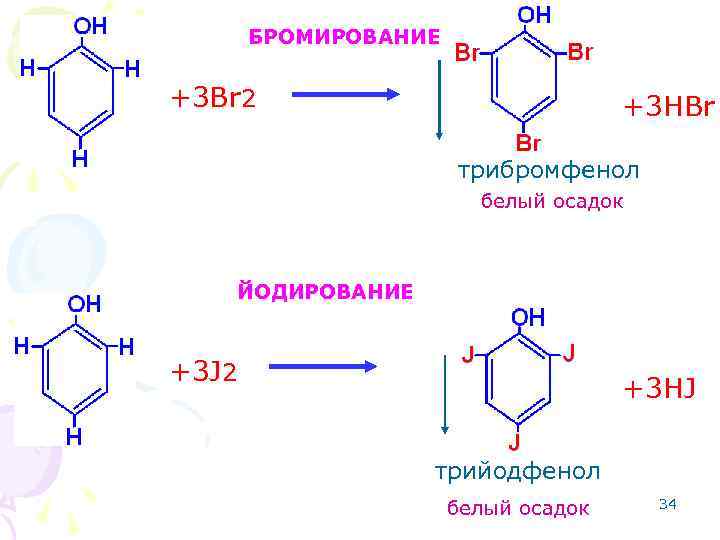 БРОМИРОВАНИЕ +3 Br 2 +3 HBr трибромфенол белый осадок ЙОДИРОВАНИЕ +3 J 2 +3 HJ трийодфенол белый осадок 34
БРОМИРОВАНИЕ +3 Br 2 +3 HBr трибромфенол белый осадок ЙОДИРОВАНИЕ +3 J 2 +3 HJ трийодфенол белый осадок 34
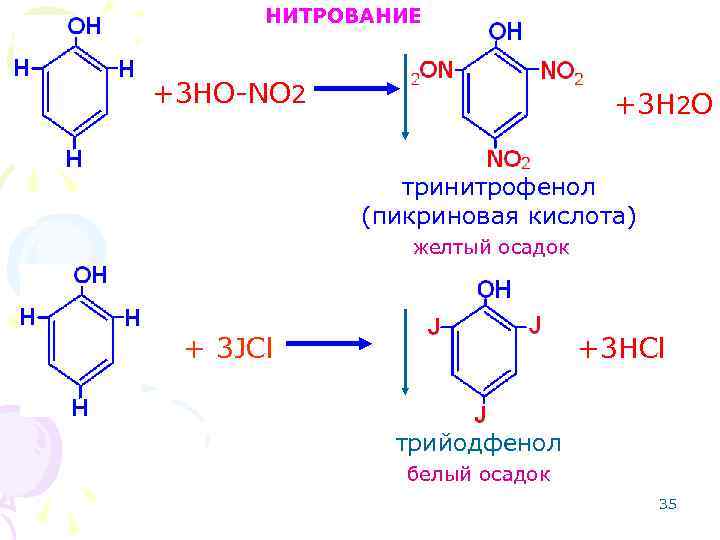 НИТРОВАНИЕ +3 HO-NO 2 +3 H 2 O тринитрофенол (пикриновая кислота) желтый осадок + 3 JCl +3 HCl трийодфенол белый осадок 35
НИТРОВАНИЕ +3 HO-NO 2 +3 H 2 O тринитрофенол (пикриновая кислота) желтый осадок + 3 JCl +3 HCl трийодфенол белый осадок 35
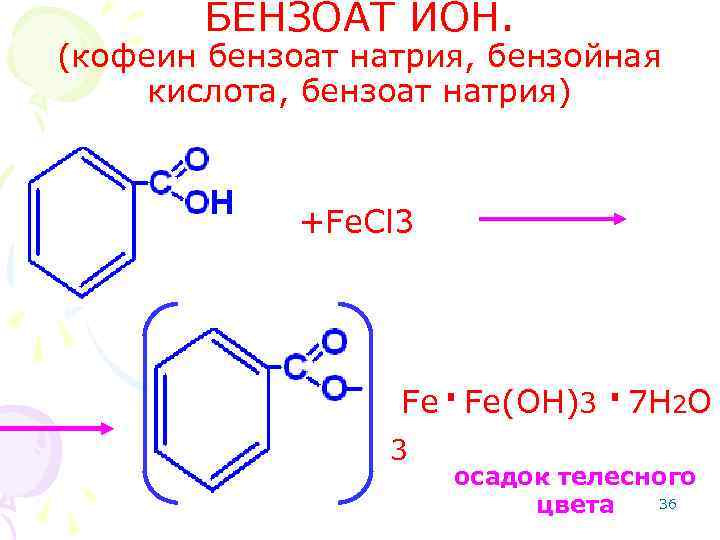 БЕНЗОАТ ИОН. (кофеин бензоат натрия, бензойная кислота, бензоат натрия) +Fe. Cl 3 . . Fe Fe(OH)3 7 H 2 O 3 осадок телесного 36 цвета
БЕНЗОАТ ИОН. (кофеин бензоат натрия, бензойная кислота, бензоат натрия) +Fe. Cl 3 . . Fe Fe(OH)3 7 H 2 O 3 осадок телесного 36 цвета
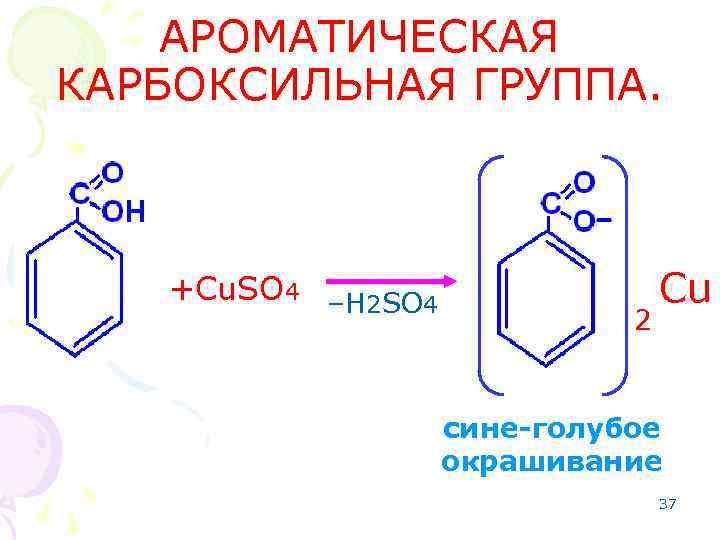 АРОМАТИЧЕСКАЯ КАРБОКСИЛЬНАЯ ГРУППА. +Cu. SO 4 –H 2 SO 4 2 Cu сине-голубое окрашивание 37
АРОМАТИЧЕСКАЯ КАРБОКСИЛЬНАЯ ГРУППА. +Cu. SO 4 –H 2 SO 4 2 Cu сине-голубое окрашивание 37
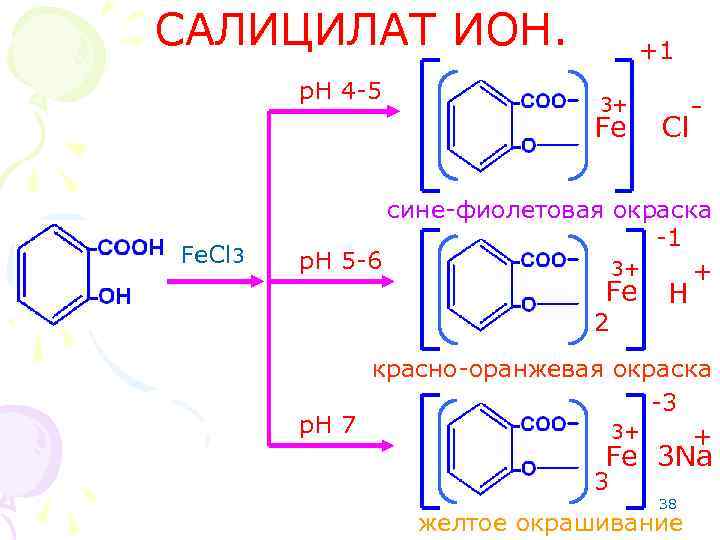 САЛИЦИЛАТ ИОН. p. H 4 -5 +1 3+ Fe Fe. Cl 3 Cl - сине-фиолетовая окраска -1 p. H 5 -6 3+ + Fe 2 H красно-оранжевая окраска -3 p. H 7 3+ + Fe 3 Na 3 38 желтое окрашивание
САЛИЦИЛАТ ИОН. p. H 4 -5 +1 3+ Fe Fe. Cl 3 Cl - сине-фиолетовая окраска -1 p. H 5 -6 3+ + Fe 2 H красно-оранжевая окраска -3 p. H 7 3+ + Fe 3 Na 3 38 желтое окрашивание
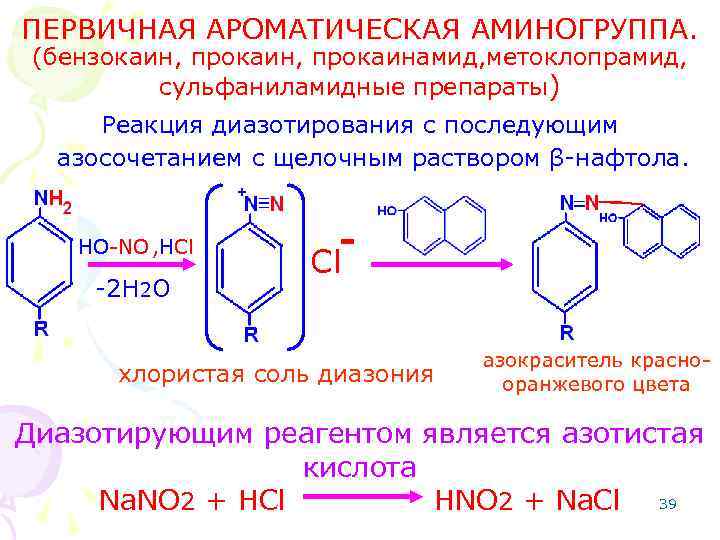 ПЕРВИЧНАЯ АРОМАТИЧЕСКАЯ АМИНОГРУППА. (бензокаин, прокаинамид, метоклопрамид, сульфаниламидные препараты) Реакция диазотирования с последующим азосочетанием с щелочным раствором β-нафтола. HO-NO , HCl -2 H 2 O - Cl хлористая соль диазония азокраситель краснооранжевого цвета Диазотирующим реагентом является азотистая кислота Na. NO 2 + HCl HNO 2 + Na. Cl 39
ПЕРВИЧНАЯ АРОМАТИЧЕСКАЯ АМИНОГРУППА. (бензокаин, прокаинамид, метоклопрамид, сульфаниламидные препараты) Реакция диазотирования с последующим азосочетанием с щелочным раствором β-нафтола. HO-NO , HCl -2 H 2 O - Cl хлористая соль диазония азокраситель краснооранжевого цвета Диазотирующим реагентом является азотистая кислота Na. NO 2 + HCl HNO 2 + Na. Cl 39
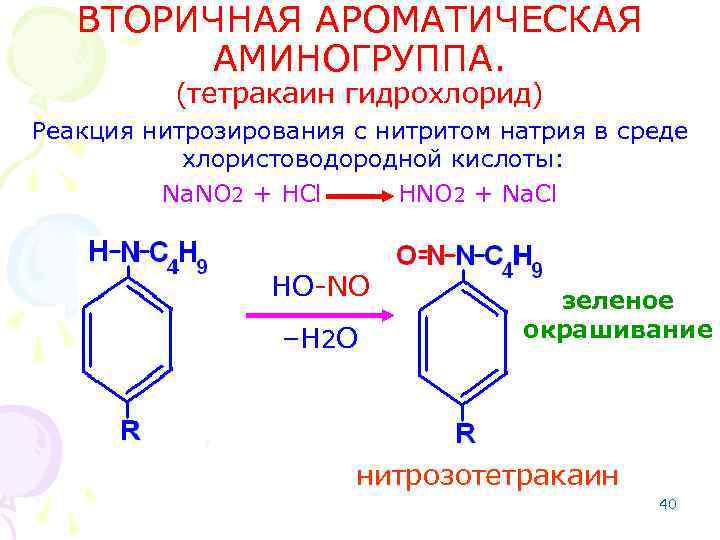 ВТОРИЧНАЯ АРОМАТИЧЕСКАЯ АМИНОГРУППА. (тетракаин гидрохлорид) Реакция нитрозирования с нитритом натрия в среде хлористоводородной кислоты: Na. NO 2 + HCl HNO 2 + Na. Cl HO-NO –H 2 O зеленое окрашивание нитрозотетракаин 40
ВТОРИЧНАЯ АРОМАТИЧЕСКАЯ АМИНОГРУППА. (тетракаин гидрохлорид) Реакция нитрозирования с нитритом натрия в среде хлористоводородной кислоты: Na. NO 2 + HCl HNO 2 + Na. Cl HO-NO –H 2 O зеленое окрашивание нитрозотетракаин 40
 СЛОЖНО-ЭФИРНАЯ ГРУППА (бензокаин, прокаин, тетракаин и т. д. ) Реакция со щелочным раствором гидроксиламина при нагревании образуется гидроксамовая кислота, которая с хлоридом железа (III) дает красно-фиолетовое окрашивание, а сульфатом меди (II) дает зеленое окрашивание. 41
СЛОЖНО-ЭФИРНАЯ ГРУППА (бензокаин, прокаин, тетракаин и т. д. ) Реакция со щелочным раствором гидроксиламина при нагревании образуется гидроксамовая кислота, которая с хлоридом железа (III) дает красно-фиолетовое окрашивание, а сульфатом меди (II) дает зеленое окрашивание. 41
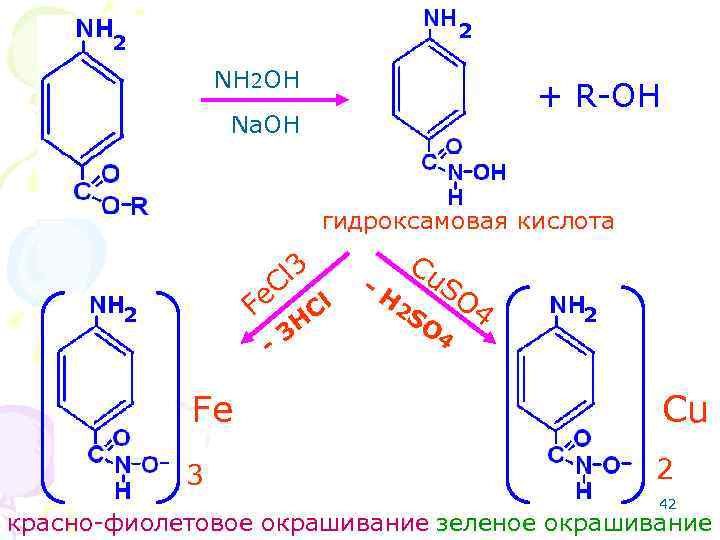 2 2 NH 2 OH + R-OH Na. OH гидроксамовая кислота l 3 C Fe 2 - 3 H Cl -H Cu 2 S SO O 4 4 2 Fe Cu 3 2 42 красно-фиолетовое окрашивание зеленое окрашивание
2 2 NH 2 OH + R-OH Na. OH гидроксамовая кислота l 3 C Fe 2 - 3 H Cl -H Cu 2 S SO O 4 4 2 Fe Cu 3 2 42 красно-фиолетовое окрашивание зеленое окрашивание
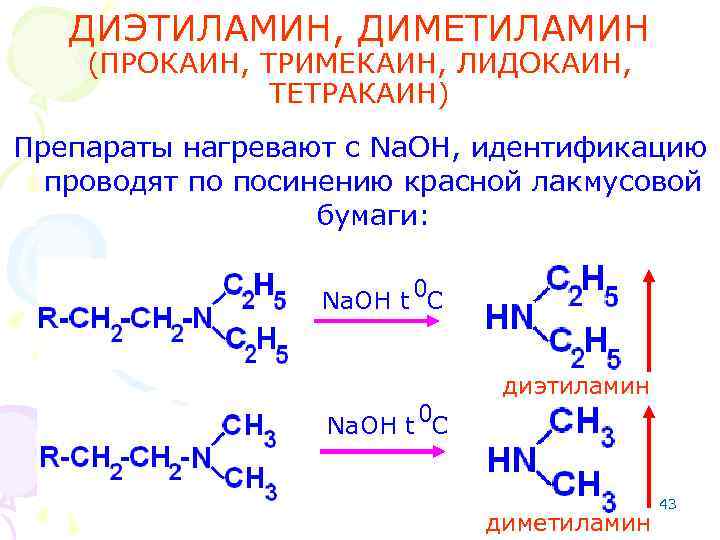 ДИЭТИЛАМИН, ДИМЕТИЛАМИН (ПРОКАИН, ТРИМЕКАИН, ЛИДОКАИН, ТЕТРАКАИН) Препараты нагревают с Na. OH, идентификацию проводят по посинению красной лакмусовой бумаги: Na. OH t 0 C диэтиламин диметиламин 43
ДИЭТИЛАМИН, ДИМЕТИЛАМИН (ПРОКАИН, ТРИМЕКАИН, ЛИДОКАИН, ТЕТРАКАИН) Препараты нагревают с Na. OH, идентификацию проводят по посинению красной лакмусовой бумаги: Na. OH t 0 C диэтиламин диметиламин 43
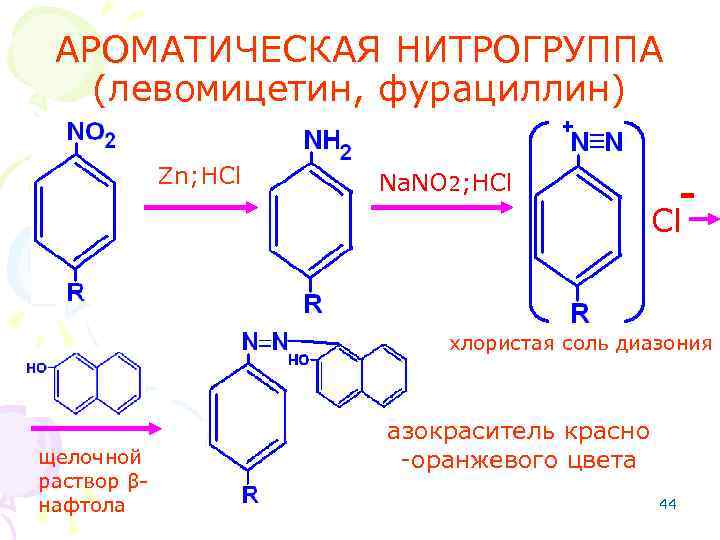 АРОМАТИЧЕСКАЯ НИТРОГРУППА (левомицетин, фурациллин) Zn; HCl Na. NO 2; HCl - Cl хлористая соль диазония щелочной раствор βнафтола азокраситель красно -оранжевого цвета 44
АРОМАТИЧЕСКАЯ НИТРОГРУППА (левомицетин, фурациллин) Zn; HCl Na. NO 2; HCl - Cl хлористая соль диазония щелочной раствор βнафтола азокраситель красно -оранжевого цвета 44
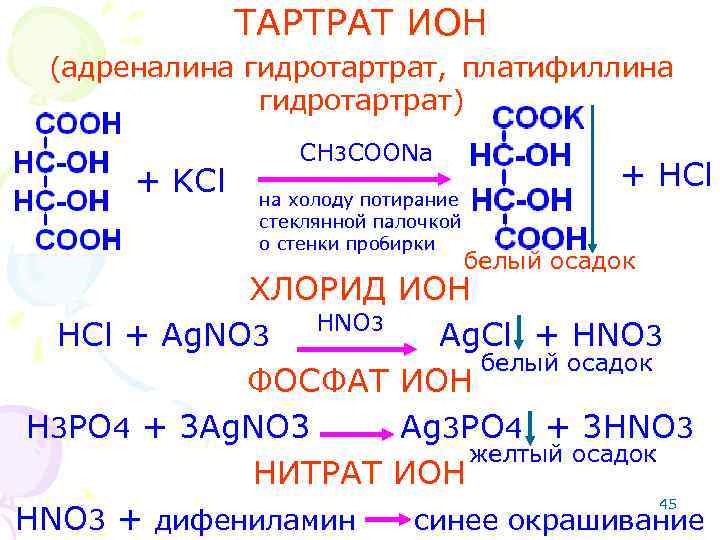 ТАРТРАТ ИОН (адреналина гидротартрат, платифиллина гидротартрат) + KCl CH 3 COONa на холоду потирание стеклянной палочкой о стенки пробирки + HCl белый осадок ХЛОРИД ИОН HNO 3 HCl + Ag. NO 3 Ag. Cl + HNO 3 белый осадок ФОСФАТ ИОН H 3 PO 4 + 3 Ag. NO 3 Ag 3 PO 4 + 3 HNO 3 желтый осадок НИТРАТ ИОН 45 HNO 3 + дифениламин синее окрашивание
ТАРТРАТ ИОН (адреналина гидротартрат, платифиллина гидротартрат) + KCl CH 3 COONa на холоду потирание стеклянной палочкой о стенки пробирки + HCl белый осадок ХЛОРИД ИОН HNO 3 HCl + Ag. NO 3 Ag. Cl + HNO 3 белый осадок ФОСФАТ ИОН H 3 PO 4 + 3 Ag. NO 3 Ag 3 PO 4 + 3 HNO 3 желтый осадок НИТРАТ ИОН 45 HNO 3 + дифениламин синее окрашивание
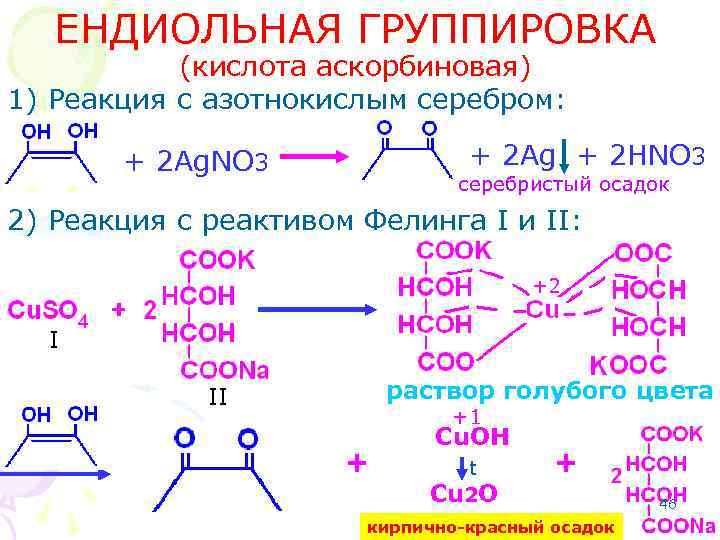 ЕНДИОЛЬНАЯ ГРУППИРОВКА (кислота аскорбиновая) 1) Реакция с азотнокислым серебром: + 2 Ag + 2 HNO 3 + 2 Ag. NO 3 серебристый осадок 2) Реакция с реактивом Фелинга I и II: +2 I раствор голубого цвета II +1 + Cu. OH t Cu 2 O + кирпично-красный осадок 46
ЕНДИОЛЬНАЯ ГРУППИРОВКА (кислота аскорбиновая) 1) Реакция с азотнокислым серебром: + 2 Ag + 2 HNO 3 + 2 Ag. NO 3 серебристый осадок 2) Реакция с реактивом Фелинга I и II: +2 I раствор голубого цвета II +1 + Cu. OH t Cu 2 O + кирпично-красный осадок 46
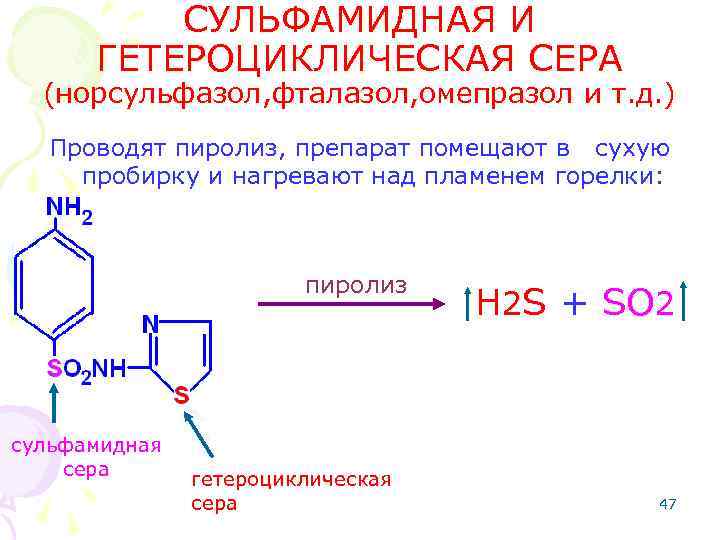 СУЛЬФАМИДНАЯ И ГЕТЕРОЦИКЛИЧЕСКАЯ СЕРА (норсульфазол, фталазол, омепразол и т. д. ) Проводят пиролиз, препарат помещают в сухую пробирку и нагревают над пламенем горелки: пиролиз сульфамидная сера гетероциклическая сера H 2 S + SO 2 47
СУЛЬФАМИДНАЯ И ГЕТЕРОЦИКЛИЧЕСКАЯ СЕРА (норсульфазол, фталазол, омепразол и т. д. ) Проводят пиролиз, препарат помещают в сухую пробирку и нагревают над пламенем горелки: пиролиз сульфамидная сера гетероциклическая сера H 2 S + SO 2 47
 ГЕТЕРОЦИКЛИЧЕСКАЯ СЕРА Пробирку закрывают бумагой, смоченной ацетатом свинца бумага чернеет H 2 S + Pb(CH 3 COO)2 Pb. S + 2 CH 3 COOH черный осадок СУЛЬФАМИДНАЯ СЕРА Пробирку закрывают бумагой, пропитанной йодатом калия и крахмалом бумага синеет от выделения свободного йода 5 SO 2 + 2 KJO 3 K 2 SO 4 + 4 SO 3 + J 2 48
ГЕТЕРОЦИКЛИЧЕСКАЯ СЕРА Пробирку закрывают бумагой, смоченной ацетатом свинца бумага чернеет H 2 S + Pb(CH 3 COO)2 Pb. S + 2 CH 3 COOH черный осадок СУЛЬФАМИДНАЯ СЕРА Пробирку закрывают бумагой, пропитанной йодатом калия и крахмалом бумага синеет от выделения свободного йода 5 SO 2 + 2 KJO 3 K 2 SO 4 + 4 SO 3 + J 2 48


