Кафедра фармацевтической и токсикологической химии





































![Натрия иодида [131 I] раствор ЕР Характеристика. Натрия иодида [131 I] раствор ЕР Характеристика.](https://present5.com/presentation/3/4124508_135243320.pdf-img/4124508_135243320.pdf-39.jpg)
![Натрия иодида [131 I] раствор ЕР Радионуклидная чистота. Регистрируют Натрия иодида [131 I] раствор ЕР Радионуклидная чистота. Регистрируют](https://present5.com/presentation/3/4124508_135243320.pdf-img/4124508_135243320.pdf-40.jpg)

![Натрия йодида [131 I] раствор ЕФ Радиохимическую чистоту Натрия йодида [131 I] раствор ЕФ Радиохимическую чистоту](https://present5.com/presentation/3/4124508_135243320.pdf-img/4124508_135243320.pdf-42.jpg)

![Натрия иодида [131 I] раствор ЕФ Натрия иодида [131 I] раствор ЕФ](https://present5.com/presentation/3/4124508_135243320.pdf-img/4124508_135243320.pdf-45.jpg)





























2012радиофарм преп_сокр. гомеопат.ppt
- Количество слайдов: 76
 Кафедра фармацевтической и токсикологической химии Лекция «Радиофармацевтические препараты» 21. 11. 2012 Богословская О. А. 1
Кафедра фармацевтической и токсикологической химии Лекция «Радиофармацевтические препараты» 21. 11. 2012 Богословская О. А. 1
 Масса протона 1, 0073 а. е. м. (атомные единицы массы). Заряд протона +1, Масса нейтрона 1, 0087 а. е. м. Заряд нейтрона 0 Согласно протонно-нейтронной теории строения ядра: В атоме Z протонов, где Z-порядковый номер элемента, (A-Z) = N нейтронов, 24 А-массовое число 51, 99 Cr Так, атом хрома содержит 52 -24=28 нейтронов 2
Масса протона 1, 0073 а. е. м. (атомные единицы массы). Заряд протона +1, Масса нейтрона 1, 0087 а. е. м. Заряд нейтрона 0 Согласно протонно-нейтронной теории строения ядра: В атоме Z протонов, где Z-порядковый номер элемента, (A-Z) = N нейтронов, 24 А-массовое число 51, 99 Cr Так, атом хрома содержит 52 -24=28 нейтронов 2
 Ядро атома водорода состоит из одного протона. - протий 11 Н. протий 1 1 Н + нейтрон образуется атом дейтерия 21 Н, дейтерий 21 Н + нейтрон – атом трития 31 Н. Все эти атомы имеют один заряд , но разные массы. Подобные разновидности одного вида атомов называется изотопами. Внизу- порядковый номер; вверху- число протонов и 3 нейтронов (масса)
Ядро атома водорода состоит из одного протона. - протий 11 Н. протий 1 1 Н + нейтрон образуется атом дейтерия 21 Н, дейтерий 21 Н + нейтрон – атом трития 31 Н. Все эти атомы имеют один заряд , но разные массы. Подобные разновидности одного вида атомов называется изотопами. Внизу- порядковый номер; вверху- число протонов и 3 нейтронов (масса)
 Изотопами называются атомы химических элементов , обладающие одинаковым числом протонов, но различным числом нейтронов : - одинаковый заряд ядра - одинаковые химические свойства - разную массу У водорода - 3 изотопа У углерода – 5 изотопов У технеция (Тс) – 16 изотопов Каждый изотоп характеризуется : -массовым числом 16 О; 8 -порядковым номером кислород имеет изотопы с массовыми числами 16, 17, 18: 16 О; 17 О; 18 О 4 8 8
Изотопами называются атомы химических элементов , обладающие одинаковым числом протонов, но различным числом нейтронов : - одинаковый заряд ядра - одинаковые химические свойства - разную массу У водорода - 3 изотопа У углерода – 5 изотопов У технеция (Тс) – 16 изотопов Каждый изотоп характеризуется : -массовым числом 16 О; 8 -порядковым номером кислород имеет изотопы с массовыми числами 16, 17, 18: 16 О; 17 О; 18 О 4 8 8
 А томная масса элемента = среднему значению из масс всех его природных изотопов с учетом их распространенности. Так, природный хлор состоит из 77, 4% изотопа с массовым числом 35 и из 22, 6% изотопа с массовым числом 37. Средняя атомная масса хлора = 35 х0, 774 + 37 х0, 226 = 35, 45. Изотопы имеют те же названия и символы, что и сами элементы. (Исключение -водород) 5
А томная масса элемента = среднему значению из масс всех его природных изотопов с учетом их распространенности. Так, природный хлор состоит из 77, 4% изотопа с массовым числом 35 и из 22, 6% изотопа с массовым числом 37. Средняя атомная масса хлора = 35 х0, 774 + 37 х0, 226 = 35, 45. Изотопы имеют те же названия и символы, что и сами элементы. (Исключение -водород) 5
 В начале 1896 г. Беккерель обнаружил, что фотографические пластинки в темноте под действием невидимых лучей, испускаемых ураном, засветились. Загадочное излучение стало известно как «лучи Беккереля» . Анри БЕККЕРЕЛЬ В 1903 г. ему, вместе с (Becquerel) супругами Кюри, была вручена Нобелевская премия по физике. (15. XII. 1852 - 25. VIII. 1908) 6
В начале 1896 г. Беккерель обнаружил, что фотографические пластинки в темноте под действием невидимых лучей, испускаемых ураном, засветились. Загадочное излучение стало известно как «лучи Беккереля» . Анри БЕККЕРЕЛЬ В 1903 г. ему, вместе с (Becquerel) супругами Кюри, была вручена Нобелевская премия по физике. (15. XII. 1852 - 25. VIII. 1908) 6
 Ученица Беккереля, Мари Кюри открыла, что торий также испускает лучи Беккереля, и переименовала их в радиоактивность. (от лат. radio — испускают лучи), а элементы, Мари Кюри (1867 -1934) испускающие лучи Беккереля, — радиоактивными элементами. Открыли два новых Пьер радиоактивных элемента - Кюри полоний (названный в честь (1859 - 1906) Польши) и радий. 7
Ученица Беккереля, Мари Кюри открыла, что торий также испускает лучи Беккереля, и переименовала их в радиоактивность. (от лат. radio — испускают лучи), а элементы, Мари Кюри (1867 -1934) испускающие лучи Беккереля, — радиоактивными элементами. Открыли два новых Пьер радиоактивных элемента - Кюри полоний (названный в честь (1859 - 1906) Польши) и радий. 7
 При явлении радиоактивности происходит превращение малоустойчивого изотопа одного химического элемента в другой. 226 88 Ra = 22286 Rn + 42 He. При этом соблюдаются законы сохранения массы и заряда: сумма масс и сумма зарядов в левой части уравнения равна сумме масс и зарядов в правой части уравнения. сумма масс: 226=222+4; сумма зарядов 88=86+2. Д ля всех химических элементов могут быть получены радиоактивные изотопы. Их известно 8 около 1500.
При явлении радиоактивности происходит превращение малоустойчивого изотопа одного химического элемента в другой. 226 88 Ra = 22286 Rn + 42 He. При этом соблюдаются законы сохранения массы и заряда: сумма масс и сумма зарядов в левой части уравнения равна сумме масс и зарядов в правой части уравнения. сумма масс: 226=222+4; сумма зарядов 88=86+2. Д ля всех химических элементов могут быть получены радиоактивные изотопы. Их известно 8 около 1500.
 Элементы, состоящие только из радиоактивных изотопов, называются радиоактивными. Это элементы с порядковыми номерами 43 (технеций Тс), 61 (прометий Рm) и 84 -107. Нестабильные изотопы называются радионуклидами Стабильных (нерадиоактивных изотопов) известно около 300. Из них состоит большинство химических элементов ПС. Однако, у некоторых элементов наряду со стабильными имеются и долгоживущие радиоактивные изотопы. Это 4019 К, 8737 Rb и др. 9
Элементы, состоящие только из радиоактивных изотопов, называются радиоактивными. Это элементы с порядковыми номерами 43 (технеций Тс), 61 (прометий Рm) и 84 -107. Нестабильные изотопы называются радионуклидами Стабильных (нерадиоактивных изотопов) известно около 300. Из них состоит большинство химических элементов ПС. Однако, у некоторых элементов наряду со стабильными имеются и долгоживущие радиоактивные изотопы. Это 4019 К, 8737 Rb и др. 9
 Различают три вида радиоактивных лучей, резко отличающихся друг от друга по природе: , и -лучи. 1. Альфа-частицы - поток положительно заряженных частиц. -частица – это ядро гелия, заряд -частицы равен 2+, а масса 4. 226 Ra = 222 Rn + 4 He 88 86 2 2. -лучи - поток электронов, поток электронов A X → A Y + β- + γ, Z Z+1 10
Различают три вида радиоактивных лучей, резко отличающихся друг от друга по природе: , и -лучи. 1. Альфа-частицы - поток положительно заряженных частиц. -частица – это ядро гелия, заряд -частицы равен 2+, а масса 4. 226 Ra = 222 Rn + 4 He 88 86 2 2. -лучи - поток электронов, поток электронов A X → A Y + β- + γ, Z Z+1 10
 3. Гамма-излучение – электромагнитное излучение, всегда сопутствует альфа- распаду и бета-превращениям. Чистая эмиссия гамма-лучей - технеций 99 m (99 m. Tc), (время полураспада 6. 0 часов). 99 m 99 43 Tc —> 43 Tc + γ (0. 14 Me. V) 99 Tc (время полураспада (2. 13 x 105 лет) ) 11
3. Гамма-излучение – электромагнитное излучение, всегда сопутствует альфа- распаду и бета-превращениям. Чистая эмиссия гамма-лучей - технеций 99 m (99 m. Tc), (время полураспада 6. 0 часов). 99 m 99 43 Tc —> 43 Tc + γ (0. 14 Me. V) 99 Tc (время полураспада (2. 13 x 105 лет) ) 11
 Закон смещения Содди-Фаянса обобщает явления природной радиоактивности: природной радиоактивности • -При испускании элементом альфа-частицы (Не 2+) порядковый номер, образовавшегося элемента уменьшается на две единицы, а массовое число – на четыре; новый элемент располагается в ПС на два места левее исходного; 23892 U 23490 Th • -При испускании -частицы порядковый номер, -частицы образовавшегося элемента увеличивается на единицу. Происходит превращение нейтрона в протон с испусканием электрона: 10 n 1 р + 0 е. 1 -1 • Масса элемента не меняется; новый элемент - в ПСЭ на одно место правее исходного; 90 Th 91 Pa. 234 12
Закон смещения Содди-Фаянса обобщает явления природной радиоактивности: природной радиоактивности • -При испускании элементом альфа-частицы (Не 2+) порядковый номер, образовавшегося элемента уменьшается на две единицы, а массовое число – на четыре; новый элемент располагается в ПС на два места левее исходного; 23892 U 23490 Th • -При испускании -частицы порядковый номер, -частицы образовавшегося элемента увеличивается на единицу. Происходит превращение нейтрона в протон с испусканием электрона: 10 n 1 р + 0 е. 1 -1 • Масса элемента не меняется; новый элемент - в ПСЭ на одно место правее исходного; 90 Th 91 Pa. 234 12
 • -При испускании элементом - излучения не изменяется ни заряд, излучения ни масса. • Закон смещения определил место изотопов элементов в ПС. 13
• -При испускании элементом - излучения не изменяется ни заряд, излучения ни масса. • Закон смещения определил место изотопов элементов в ПС. 13
 1. Независимо от природы радиоактивного излучения радиоактивный распад элемента происходит по основному закону радиоактивного распада: - (d. N/dτ) = λN, § где N - число ядер нуклида, § Т - время § -( d. N/dτ ) – скорость распада радионуклида ; d. N разница между последующим и предыдущим значением величины N, § т. к. N уменьшается в данном процессе – идет распад нуклида, то d. N <0, отрицательная величина. § λ – постоянная распада ( радиоактивная постоянная ) для данного нуклида. λ показывает , какая часть общего количества радиоактивного вещества распадается в единицу времени. 14
1. Независимо от природы радиоактивного излучения радиоактивный распад элемента происходит по основному закону радиоактивного распада: - (d. N/dτ) = λN, § где N - число ядер нуклида, § Т - время § -( d. N/dτ ) – скорость распада радионуклида ; d. N разница между последующим и предыдущим значением величины N, § т. к. N уменьшается в данном процессе – идет распад нуклида, то d. N <0, отрицательная величина. § λ – постоянная распада ( радиоактивная постоянная ) для данного нуклида. λ показывает , какая часть общего количества радиоактивного вещества распадается в единицу времени. 14
 2. Скорость процессов радиоактивных превращений характеризуется периодом полураспада (τ1/2) - время, в течение которого , число радиоактивных ядер уменьшается вдвое. λ τ1/2= ln 2 = 0. 692 Чем меньше τ1/2, тем менее устойчиво ядро, тем интенсивнее протекает распад. 15
2. Скорость процессов радиоактивных превращений характеризуется периодом полураспада (τ1/2) - время, в течение которого , число радиоактивных ядер уменьшается вдвое. λ τ1/2= ln 2 = 0. 692 Чем меньше τ1/2, тем менее устойчиво ядро, тем интенсивнее протекает распад. 15
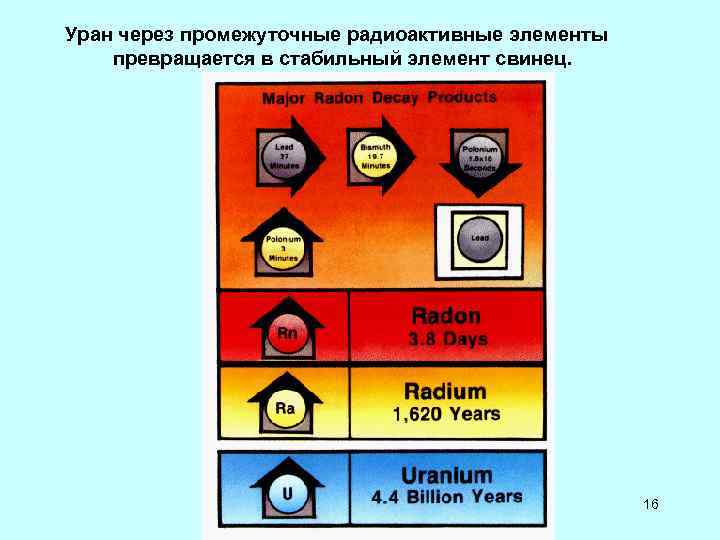
 Уран через промежуточные радиоактивные элементы превращается в стабильный элемент свинец. 16
Уран через промежуточные радиоактивные элементы превращается в стабильный элемент свинец. 16
 Разные виды излучений обладают разной проникающей способностью, поэтому они оказывают неодинаковое воздействие на ткани живого организма. Глубина проникновения ионизирующего излучения зависит: - От природы излучения, заряда, массы и энергии составляющих его частиц, -От состава и плотности облучаемого вещества 17
Разные виды излучений обладают разной проникающей способностью, поэтому они оказывают неодинаковое воздействие на ткани живого организма. Глубина проникновения ионизирующего излучения зависит: - От природы излучения, заряда, массы и энергии составляющих его частиц, -От состава и плотности облучаемого вещества 17
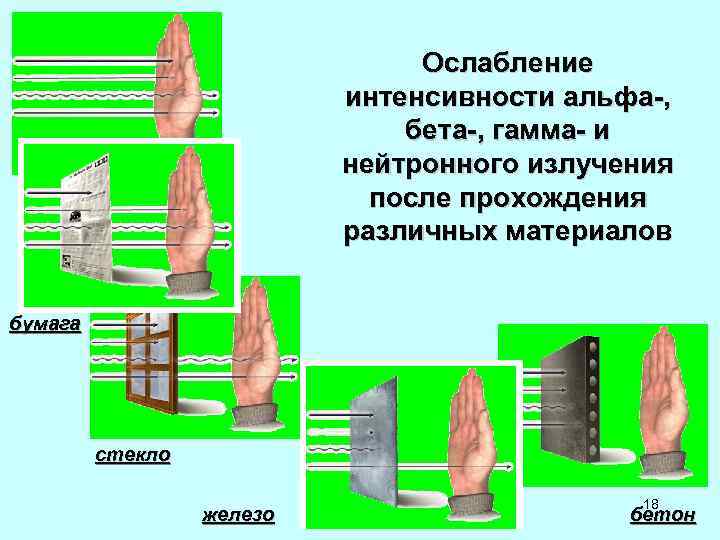
 Ослабление интенсивности альфа-, бета-, гамма- и нейтронного излучения после прохождения различных материалов бумага стекло 18 железо бетон
Ослабление интенсивности альфа-, бета-, гамма- и нейтронного излучения после прохождения различных материалов бумага стекло 18 железо бетон
 • Пробег альфа-частиц в воздухе не превышает нескольких сантиметров. Альфа-частицы поглощаются резиновыми перчатками, одеждой, стенками стеклянной ампулы и т. п. • Пробег бета-частиц в воздухе в зависимости от их энергии составляет величину от сантиметров до нескольких метров. Для защиты от бета-излучения применяют материалы с малым атомным номером, например, специальные экраны из плексигласа, контейнеры из алюминия и пластмасс и т. п. • Для защиты от тормозного излучения (фотонное ионизирующее излучение)– вторичного излучения, возникающего при прохождении бета-частиц через вещество применяют комбинированную защиту: Ø внутренний слой (со стороны источника) делается из вещества с малым атомным номером для поглощения бета-излучения, Ø внешний слой– из вещества с большим атомным 19 номером для ослабления тормозного излучения.
• Пробег альфа-частиц в воздухе не превышает нескольких сантиметров. Альфа-частицы поглощаются резиновыми перчатками, одеждой, стенками стеклянной ампулы и т. п. • Пробег бета-частиц в воздухе в зависимости от их энергии составляет величину от сантиметров до нескольких метров. Для защиты от бета-излучения применяют материалы с малым атомным номером, например, специальные экраны из плексигласа, контейнеры из алюминия и пластмасс и т. п. • Для защиты от тормозного излучения (фотонное ионизирующее излучение)– вторичного излучения, возникающего при прохождении бета-частиц через вещество применяют комбинированную защиту: Ø внутренний слой (со стороны источника) делается из вещества с малым атомным номером для поглощения бета-излучения, Ø внешний слой– из вещества с большим атомным 19 номером для ослабления тормозного излучения.
 • Гамма-излучение в отличие от альфа- и бета- излучения не характеризуется определенным пробегом в веществе – оно поглощается по мере прохождения через вещество по экспоненциальному закону. • Наиболее эффективно поглощают гамма-излучение вещества с большим атомным номером, например свинец. • Гамма-излучение определенной энергии можно характеризовать толщиной слоя половинного ослабления (полутолщина ослабления) в веществе. ослабления (полутолщина ослабления) Это та толщина защитного материала, которая ослабляет первоначальную интенсивность излучения в 2 раза. Например, через защитный материал, толщина которого равна 7 слоям половинного ослабления (полутолщинам), проходит менее 1% излучения незащищенного источника. • Защита от гамма-излучения радиоактивных препаратов достигается не только применением поглощающих экранов, но также и путем увеличения 20 расстояния от препарата.
• Гамма-излучение в отличие от альфа- и бета- излучения не характеризуется определенным пробегом в веществе – оно поглощается по мере прохождения через вещество по экспоненциальному закону. • Наиболее эффективно поглощают гамма-излучение вещества с большим атомным номером, например свинец. • Гамма-излучение определенной энергии можно характеризовать толщиной слоя половинного ослабления (полутолщина ослабления) в веществе. ослабления (полутолщина ослабления) Это та толщина защитного материала, которая ослабляет первоначальную интенсивность излучения в 2 раза. Например, через защитный материал, толщина которого равна 7 слоям половинного ослабления (полутолщинам), проходит менее 1% излучения незащищенного источника. • Защита от гамма-излучения радиоактивных препаратов достигается не только применением поглощающих экранов, но также и путем увеличения 20 расстояния от препарата.
 Радиофармацевтический препарат ( Radiopharmaceutical ) – лекарственны препарат, который в готовой для использования форме содержит один или несколько радионуклидов (радиоактивных изотопов) и разрешен для введения человеку с диагностической или лечебной целью. . 21
Радиофармацевтический препарат ( Radiopharmaceutical ) – лекарственны препарат, который в готовой для использования форме содержит один или несколько радионуклидов (радиоактивных изотопов) и разрешен для введения человеку с диагностической или лечебной целью. . 21
 Используют радиофармацевтические препараты по двум направлениям. 1. Гамма лучи эффективно не взаимодействуют с лучи химическими группами. Это приводит к меньшим химическим повреждениям, чем для α- или β- частиц. Поэтому γ-излучатели обычно используются при диагностике. 2. α- и β-частицы в результате реакций с -частицы близлежащими химическими группами имеют короткий пробег, поэтому α- и β-излучатели используется в радиотерапии главным образом для лечения злокачественных новообразований 22
Используют радиофармацевтические препараты по двум направлениям. 1. Гамма лучи эффективно не взаимодействуют с лучи химическими группами. Это приводит к меньшим химическим повреждениям, чем для α- или β- частиц. Поэтому γ-излучатели обычно используются при диагностике. 2. α- и β-частицы в результате реакций с -частицы близлежащими химическими группами имеют короткий пробег, поэтому α- и β-излучатели используется в радиотерапии главным образом для лечения злокачественных новообразований 22
 Эффективность радиопрепаратов определяется: периодом полураспада, интенсивностью излучения, видом излучения способностью селективно депонироваться в больном органе. Основные радиоизотопы, используемые в медицине: К-43 (бета, гамма) – 22 ч, Ga-57 (гамма) – 78 ч, Ru-97 (гамма) – 69 ч, Tc-99 m* (гамма) – 6 ч, I-123 (гамма) – 13 ч, I-131 (бета, гамма) – 8 дн, Re-186 (бета, гамма) – 89 ч, Pb-212 (альфа, бета, гамма) – 1 ч. 23
Эффективность радиопрепаратов определяется: периодом полураспада, интенсивностью излучения, видом излучения способностью селективно депонироваться в больном органе. Основные радиоизотопы, используемые в медицине: К-43 (бета, гамма) – 22 ч, Ga-57 (гамма) – 78 ч, Ru-97 (гамма) – 69 ч, Tc-99 m* (гамма) – 6 ч, I-123 (гамма) – 13 ч, I-131 (бета, гамма) – 8 дн, Re-186 (бета, гамма) – 89 ч, Pb-212 (альфа, бета, гамма) – 1 ч. 23
 Критерии выбора радиоизотопа для изготовления радиофармацевтических препаратов. 1. Радиоизотоп должен иметь время распада не слишком короткое, чтобы радионуклид мог быть синтезирован и транспортироваться, но и достаточно короткое (идеально менее 8 дней), чтобы интенсивность радиоизлучения была высокой. λ τ1/2= ln 2 2. Для диагностических целей полезно, если уровни эмиссии уменьшаются в течение нескольких дней, чтобы в случае необходимости повторить обработку. 3. Радиоизотоп должен селективно восприниматься органами или опухолями. Требуется тщательное нацеливание на выбранный орган или опухоль. 24
Критерии выбора радиоизотопа для изготовления радиофармацевтических препаратов. 1. Радиоизотоп должен иметь время распада не слишком короткое, чтобы радионуклид мог быть синтезирован и транспортироваться, но и достаточно короткое (идеально менее 8 дней), чтобы интенсивность радиоизлучения была высокой. λ τ1/2= ln 2 2. Для диагностических целей полезно, если уровни эмиссии уменьшаются в течение нескольких дней, чтобы в случае необходимости повторить обработку. 3. Радиоизотоп должен селективно восприниматься органами или опухолями. Требуется тщательное нацеливание на выбранный орган или опухоль. 24
 I. Е диницы измерения , используемые п характеристике радиофармацевтических препаратов. А). Единицей измерения радиоактивности в СИ является беккерель (Бк). ). 1 Бк – активность радионуклида в источнике , в котором за 1 секунду происходит один акт распада. Широко используются кратные единицы : к. Бк ( килобеккерель -10 Бк , МБк ( мегабекерель - 10 6 Бк ) и 3 ) ГБк (гигабекерель - 109 Бк). В ГФXI использованы внесистемные единицы : кюри (Кu). ГФ ХII: Кюри – устаревшая единица активности (Ки), 1 (Ки), Кu – активность радионуклида в источнике, в котором за 1 секунду происходит 3, 7 • 1010 актов распада, т. е. I. 1 Кu = 3, 7 • 1010 Бк. 25
I. Е диницы измерения , используемые п характеристике радиофармацевтических препаратов. А). Единицей измерения радиоактивности в СИ является беккерель (Бк). ). 1 Бк – активность радионуклида в источнике , в котором за 1 секунду происходит один акт распада. Широко используются кратные единицы : к. Бк ( килобеккерель -10 Бк , МБк ( мегабекерель - 10 6 Бк ) и 3 ) ГБк (гигабекерель - 109 Бк). В ГФXI использованы внесистемные единицы : кюри (Кu). ГФ ХII: Кюри – устаревшая единица активности (Ки), 1 (Ки), Кu – активность радионуклида в источнике, в котором за 1 секунду происходит 3, 7 • 1010 актов распада, т. е. I. 1 Кu = 3, 7 • 1010 Бк. 25
 Б). Единицей измерения энергии ионизирующего излучения в СИ является джоуль (Дж). Энергию радиоактивного излучения отдельных частиц обычно измеряют в мегаэлектронвольтах (Мэ. В); 1 Мэ. В = 1, 6. 10 -13 Дж = 0, 16 п. Дж (пико. Джоулей; пико - 10 -12). 26
Б). Единицей измерения энергии ионизирующего излучения в СИ является джоуль (Дж). Энергию радиоактивного излучения отдельных частиц обычно измеряют в мегаэлектронвольтах (Мэ. В); 1 Мэ. В = 1, 6. 10 -13 Дж = 0, 16 п. Дж (пико. Джоулей; пико - 10 -12). 26
 Радиофармацевтические препараты поступают в лечебно-диагностические учреждения: 1. в виде готовых к применению форм, 2. в виде наборов для приготовления. Готовые фармацевтические препараты: • Изотонический раствор Na. I-131, • Гиппуран-I-131, • Иодокапс. 27
Радиофармацевтические препараты поступают в лечебно-диагностические учреждения: 1. в виде готовых к применению форм, 2. в виде наборов для приготовления. Готовые фармацевтические препараты: • Изотонический раствор Na. I-131, • Гиппуран-I-131, • Иодокапс. 27
 Наборы для приготовления радиофармацевтических препаратов Р адиофармацевтический препарат готовится в лаборатории из набора реагентов и радиоактивной метки непосредственно перед использованием. В качестве метки чаще всего применяют короткоживущий радионуклид технеция 99 м. Тс. Макротех , Пертехнетат , Технефор Технемаг, Пирфотех. 28
Наборы для приготовления радиофармацевтических препаратов Р адиофармацевтический препарат готовится в лаборатории из набора реагентов и радиоактивной метки непосредственно перед использованием. В качестве метки чаще всего применяют короткоживущий радионуклид технеция 99 м. Тс. Макротех , Пертехнетат , Технефор Технемаг, Пирфотех. 28
 Перечень основных разделов ФС и ФСП на радиофармацевтический препарат • Препараты, поставляемые в клинические учреждения в готовой для использования форме (ГФ XII): • состав, описание, подлинность, р. Н, объемная активность, радионуклидные примеси, радиохимическая чистота (радиохимические примеси), химические примеси, компоненты, бактериальные эндотоксины или пирогенность*, стерильность, упаковка*, маркировка, транспортирование*, хранение*, срок годности, меры предосторожности. 29
Перечень основных разделов ФС и ФСП на радиофармацевтический препарат • Препараты, поставляемые в клинические учреждения в готовой для использования форме (ГФ XII): • состав, описание, подлинность, р. Н, объемная активность, радионуклидные примеси, радиохимическая чистота (радиохимические примеси), химические примеси, компоненты, бактериальные эндотоксины или пирогенность*, стерильность, упаковка*, маркировка, транспортирование*, хранение*, срок годности, меры предосторожности. 29
 • Активность, молярная (Activity, molar) – Активность, молярная для определенного изотопа: активность соединения (A), отнесенная к его количеству в молях (n). Am = A/n. • Активность объемная (Activity, Активность объемная concentration, Volume activity) – отношение активности (A) радионуклида в препарате (образце) к объему (V) препарата (образца). АV = A/V. • Активность, удельная (Activity, specific) – Активность, удельная для определенного изотопа или смеси изотопов: активность вещества (A), отнесенная к его массе (m). a = A/m. 30
• Активность, молярная (Activity, molar) – Активность, молярная для определенного изотопа: активность соединения (A), отнесенная к его количеству в молях (n). Am = A/n. • Активность объемная (Activity, Активность объемная concentration, Volume activity) – отношение активности (A) радионуклида в препарате (образце) к объему (V) препарата (образца). АV = A/V. • Активность, удельная (Activity, specific) – Активность, удельная для определенного изотопа или смеси изотопов: активность вещества (A), отнесенная к его массе (m). a = A/m. 30
 • Радионуклидная чистота (Radionuclidic purity) чистота препарата – отношение активности основного радионуклида к общей активности препарата, выраженное в процентах, не является постоянной характеристикой данного препарата, а изменяется с течением времени. • Радионуклидные примеси (Radionuclidic impurities) – примеси других радиоактивных нуклидов (как того же, так и других элементов). • Количество радионуклидных примесей - отношением примесей активности примесей к активности основного нуклида (на определенную дату и, при необходимости, время), выраженное в процентах. • Дочерние радионуклиды, образующиеся в результате Дочерние радионуклиды, радиоактивного распада материнского (основного) радионуклида, не считаются радионуклидными примесями: например, ксенон-131 m не рассматривается как радионуклидная примесь к йоду-131. 31
• Радионуклидная чистота (Radionuclidic purity) чистота препарата – отношение активности основного радионуклида к общей активности препарата, выраженное в процентах, не является постоянной характеристикой данного препарата, а изменяется с течением времени. • Радионуклидные примеси (Radionuclidic impurities) – примеси других радиоактивных нуклидов (как того же, так и других элементов). • Количество радионуклидных примесей - отношением примесей активности примесей к активности основного нуклида (на определенную дату и, при необходимости, время), выраженное в процентах. • Дочерние радионуклиды, образующиеся в результате Дочерние радионуклиды, радиоактивного распада материнского (основного) радионуклида, не считаются радионуклидными примесями: например, ксенон-131 m не рассматривается как радионуклидная примесь к йоду-131. 31
 Анализ радионуклидной чистоты включает три этапа: · 1. обнаружение радионуклидных примесей - Примеси обнаруживают путем измерения энергии бетта - и гамма-излучений и периодов полураспада для анализируемого препарата и выделенных из него отдельных примесей. Аппаратура : радиометрические установки с бета- и гамма-счетчиками, спектрометры. Конкретные методики анализа на отдельные радионуклидные примеси приводят в соответствующих частных ФС или ФСП. 32
Анализ радионуклидной чистоты включает три этапа: · 1. обнаружение радионуклидных примесей - Примеси обнаруживают путем измерения энергии бетта - и гамма-излучений и периодов полураспада для анализируемого препарата и выделенных из него отдельных примесей. Аппаратура : радиометрические установки с бета- и гамма-счетчиками, спектрометры. Конкретные методики анализа на отдельные радионуклидные примеси приводят в соответствующих частных ФС или ФСП. 32
 · 2. идентификация радионуклидных примесей - с помощью справочных таблиц идентифицируют примеси по периодам полураспада , энергии и интенсивности излучения. М етодики анализа н отдельные радионуклидные примеси приведены в соответствующих ФС. - Детальный анализ радионуклидной чистоты производится только предприятием-изготовителем. · 3. определение активности радионуклидных примесей. Активность обнаруженной примеси приводится в процентах по отношению к активности основного радионуклида в препарате на определенную дату. 33.
· 2. идентификация радионуклидных примесей - с помощью справочных таблиц идентифицируют примеси по периодам полураспада , энергии и интенсивности излучения. М етодики анализа н отдельные радионуклидные примеси приведены в соответствующих ФС. - Детальный анализ радионуклидной чистоты производится только предприятием-изготовителем. · 3. определение активности радионуклидных примесей. Активность обнаруженной примеси приводится в процентах по отношению к активности основного радионуклида в препарате на определенную дату. 33.
 • Радионуклидные примеси, активность примеси которых составляет не более 0, 01% от не более 0, 01% активности основного радионуклида в течение всего срока годности, в частных ФСП не приводят, но указание о пределе суммарной примеси в фармакопейной статье обязательно. • Когда примесь не обнаружена, должен Когда примесь не обнаружена быть указан нижний предел обнаружения примененным методом анализа. 34
• Радионуклидные примеси, активность примеси которых составляет не более 0, 01% от не более 0, 01% активности основного радионуклида в течение всего срока годности, в частных ФСП не приводят, но указание о пределе суммарной примеси в фармакопейной статье обязательно. • Когда примесь не обнаружена, должен Когда примесь не обнаружена быть указан нижний предел обнаружения примененным методом анализа. 34
 • Контроль препарата на содержание Контроль радионуклидных примесей не выполняют, не выполняют если: Ø имеется НД (ФС, ТУ, СТП) на имеется НД радиоактивное исходное сырье, радиоактивное исходное сырье применяемое для получения препарата, и в этом документе указано содержание радионуклидных примесей; Ø анализ не может быть выполнен в анализ не может быть выполнен течение срока годности препарата. 35
• Контроль препарата на содержание Контроль радионуклидных примесей не выполняют, не выполняют если: Ø имеется НД (ФС, ТУ, СТП) на имеется НД радиоактивное исходное сырье, радиоактивное исходное сырье применяемое для получения препарата, и в этом документе указано содержание радионуклидных примесей; Ø анализ не может быть выполнен в анализ не может быть выполнен течение срока годности препарата. 35
 Радионуклидная чистота РФП в течение срока годности должна быть, как правило, не ниже 99, 5%, т. е. допустимая величина примесей других радиоактивных нуклидов не должна превышать 0, 5%. Например, в препарате «Раствор индия (111 In) хлорида» обнаружены примесные радионуклиды: 110 In, 114 In и 65 Zn. Радионуклидная чистота препарата характеризуется радиоактивностью этих примесных радионуклидов, которая составляет 3 КБк на 1 МБк, т. е. 0, 3%. 36
Радионуклидная чистота РФП в течение срока годности должна быть, как правило, не ниже 99, 5%, т. е. допустимая величина примесей других радиоактивных нуклидов не должна превышать 0, 5%. Например, в препарате «Раствор индия (111 In) хлорида» обнаружены примесные радионуклиды: 110 In, 114 In и 65 Zn. Радионуклидная чистота препарата характеризуется радиоактивностью этих примесных радионуклидов, которая составляет 3 КБк на 1 МБк, т. е. 0, 3%. 36
 Радиохимическая чистота (Radiochemical purity) Радиохимическая чистота – отношение активности радионуклида, который присутствует в препарате в устойчивой химической форме основного вещества, к общей активности радионуклида в этом препарате, выраженное в процентах. Радиохимические примеси (Radiochemical Радиохимические примеси impurities) – примеси химических соединений, отличных от основного вещества, составляющего препарат, но содержащих тот же радионуклид. Величину радиохимических примесей, т. е. активность содержащегося в них радионуклида, выражают в процентах к общей активности радионуклида в препарате. 37
Радиохимическая чистота (Radiochemical purity) Радиохимическая чистота – отношение активности радионуклида, который присутствует в препарате в устойчивой химической форме основного вещества, к общей активности радионуклида в этом препарате, выраженное в процентах. Радиохимические примеси (Radiochemical Радиохимические примеси impurities) – примеси химических соединений, отличных от основного вещества, составляющего препарат, но содержащих тот же радионуклид. Величину радиохимических примесей, т. е. активность содержащегося в них радионуклида, выражают в процентах к общей активности радионуклида в препарате. 37
 Радиохимические примеси могут образовываться в результате: Ø - производства радионуклида Ø - последующих химических операций; Ø - химических изменений в результате хранения. 38
Радиохимические примеси могут образовываться в результате: Ø - производства радионуклида Ø - последующих химических операций; Ø - химических изменений в результате хранения. 38
![> Натрия иодида [131 I] раствор ЕР Характеристика. > Натрия иодида [131 I] раствор ЕР Характеристика.](https://present5.com/presentation/3/4124508_135243320.pdf-img/4124508_135243320.pdf-39.jpg) Натрия иодида [131 I] раствор ЕР Характеристика. Прозрачный , бесцветный раствор. Время полураспада =8, 04 дней Испускает бетта- и гамма-излучение. 39
Натрия иодида [131 I] раствор ЕР Характеристика. Прозрачный , бесцветный раствор. Время полураспада =8, 04 дней Испускает бетта- и гамма-излучение. 39
![>Натрия иодида [131 I] раствор ЕР Радионуклидная чистота. Регистрируют >Натрия иодида [131 I] раствор ЕР Радионуклидная чистота. Регистрируют](https://present5.com/presentation/3/4124508_135243320.pdf-img/4124508_135243320.pdf-40.jpg) Натрия иодида [131 I] раствор ЕР Радионуклидная чистота. Регистрируют спектр излучения на специальной аппаратуре. Спектр должен соответствовать спектру -излучения стандартного образца «Йод-131» . Определяют относительное содержание йода-131, йода-133, йода-135 и другие присутствующие радионуклидные примеси. Время полураспада йода-133 =20, 8 часов и он имеет характерные линии поглощения с энергией 0, 53 и 0, 875 Мэв. Время полураспада йода-135 =6, 55 часов и он имеет характерные линии поглощения с энергией 0, 527 и 1, 260 Мэв. Не менее 99, 9% общей радиоактивности обусловлено йодом-131 и менее чем 0, 1% общей радиоактивности приходится на йод-133, йод-135 и др. радионуклидные 40 примеси.
Натрия иодида [131 I] раствор ЕР Радионуклидная чистота. Регистрируют спектр излучения на специальной аппаратуре. Спектр должен соответствовать спектру -излучения стандартного образца «Йод-131» . Определяют относительное содержание йода-131, йода-133, йода-135 и другие присутствующие радионуклидные примеси. Время полураспада йода-133 =20, 8 часов и он имеет характерные линии поглощения с энергией 0, 53 и 0, 875 Мэв. Время полураспада йода-135 =6, 55 часов и он имеет характерные линии поглощения с энергией 0, 527 и 1, 260 Мэв. Не менее 99, 9% общей радиоактивности обусловлено йодом-131 и менее чем 0, 1% общей радиоактивности приходится на йод-133, йод-135 и др. радионуклидные 40 примеси.
 • Подлинность. • А. Регистрируют спектр -излучения на специальной аппаратуре. Спектр должен соответствовать спектру -излучения стандартного образца «Йод-131» , который имеет характерную линию поглощения с энергией 0, 365 Мэв. • В. Исследуют хроматограммы препарата на радиохимическую чистоту. • С. Метод получения изотопа Йод-131 – радиоактивный изотоп йода, и может быть получен нейтронной бомбордировкой теллурия или выделен из продуктов расщепления урана 41
• Подлинность. • А. Регистрируют спектр -излучения на специальной аппаратуре. Спектр должен соответствовать спектру -излучения стандартного образца «Йод-131» , который имеет характерную линию поглощения с энергией 0, 365 Мэв. • В. Исследуют хроматограммы препарата на радиохимическую чистоту. • С. Метод получения изотопа Йод-131 – радиоактивный изотоп йода, и может быть получен нейтронной бомбордировкой теллурия или выделен из продуктов расщепления урана 41
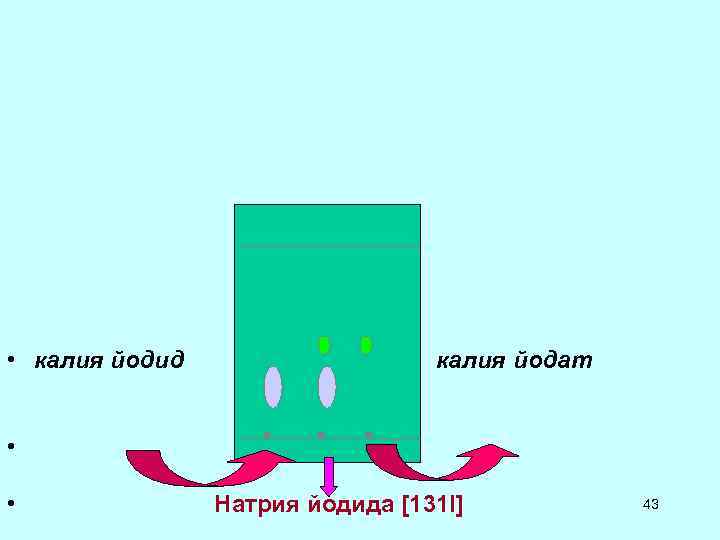
![> Натрия йодида [131 I] раствор ЕФ Радиохимическую чистоту > Натрия йодида [131 I] раствор ЕФ Радиохимическую чистоту](https://present5.com/presentation/3/4124508_135243320.pdf-img/4124508_135243320.pdf-42.jpg) Натрия йодида [131 I] раствор ЕФ Радиохимическую чистоту исследуют с помощью бумажной хроматографии. Тестовый раствор Эталонный раствор (а). 1% р-р калия йодида в воде Эталонный раствор (в). 2 % р-р калия йодата в воде На старт наносят 20 l тестового раствора, 10 эталонного раствора (а) и 10 l эталонного раствора (в). Определяют распределение радиоактивности. На хроматограмме с тест-раствором н е менее 95% всей радиоактивности приходится на пятно йодидов. 42
Натрия йодида [131 I] раствор ЕФ Радиохимическую чистоту исследуют с помощью бумажной хроматографии. Тестовый раствор Эталонный раствор (а). 1% р-р калия йодида в воде Эталонный раствор (в). 2 % р-р калия йодата в воде На старт наносят 20 l тестового раствора, 10 эталонного раствора (а) и 10 l эталонного раствора (в). Определяют распределение радиоактивности. На хроматограмме с тест-раствором н е менее 95% всей радиоактивности приходится на пятно йодидов. 42
 • калия йодид калия йодат • • Натрия йодида [131 I] 43
• калия йодид калия йодат • • Натрия йодида [131 I] 43
 Для количественного анализа: определяют удельную активность препарата по сравнению с эталоном. 44
Для количественного анализа: определяют удельную активность препарата по сравнению с эталоном. 44
![> Натрия иодида [131 I] раствор ЕФ > Натрия иодида [131 I] раствор ЕФ](https://present5.com/presentation/3/4124508_135243320.pdf-img/4124508_135243320.pdf-45.jpg) Натрия иодида [131 I] раствор ЕФ Удельная радиоактивность ЛП Метод приготовления препарата таков, что удельная радиоактивность составляет не менее 185 ГБк (GBq) йода-131 на миллиграмм иодида на дату указанную на этикетке. Радиоактивность препарата Радиоактивность раствора составляет не менее 90% и не более 110% радиоактивности йода-131, на дату указанную на этикетке. Применение Для диагностики функционального состояния шитовидной железы и с терапевтической целью. 45 Препарат выпускается для внутривенного введения.
Натрия иодида [131 I] раствор ЕФ Удельная радиоактивность ЛП Метод приготовления препарата таков, что удельная радиоактивность составляет не менее 185 ГБк (GBq) йода-131 на миллиграмм иодида на дату указанную на этикетке. Радиоактивность препарата Радиоактивность раствора составляет не менее 90% и не более 110% радиоактивности йода-131, на дату указанную на этикетке. Применение Для диагностики функционального состояния шитовидной железы и с терапевтической целью. 45 Препарат выпускается для внутривенного введения.
 ФОРМА ВЫПУСКА И ХРАНЕНИЕ РФП Растворы фармакопейных радиоактивных препаратов выпускают: § во флаконах, § Флаконы закрыты резиновыми пробками с металлическими колпаками, § Флаконы упакованы в защитные контейнеры. Ø На этикетке первичной упаковки (флакона ) со знаком . радиационной опасности указывают: Øназвание препарата, Øлекарственную форму, Øактивность (для капсул или драже активность каждой единицы) на установленную дату (и время) поставки, Ø номер серии, Øсрок годности. 46
ФОРМА ВЫПУСКА И ХРАНЕНИЕ РФП Растворы фармакопейных радиоактивных препаратов выпускают: § во флаконах, § Флаконы закрыты резиновыми пробками с металлическими колпаками, § Флаконы упакованы в защитные контейнеры. Ø На этикетке первичной упаковки (флакона ) со знаком . радиационной опасности указывают: Øназвание препарата, Øлекарственную форму, Øактивность (для капсул или драже активность каждой единицы) на установленную дату (и время) поставки, Ø номер серии, Øсрок годности. 46
 • На этикетке вторичной упаковки (комплект На этикетке вторичной упаковки упаковочный транспортный) со знаком радиационной опасности указывают: Ø наименование производителя, Ø товарный знак производителя Ø адрес Ø название препарата, Ø лекарственную форму, Ø состав, Ø активность на установленную дату (и время) поставки, Ø номер серии, Ø «стерильно» Ø срок годности, Ø условия хранения, Ø тип и номер контейнера, Ø транспортную категорию Ø номер регистрационного удостоверения Ø штрих-код. 47
• На этикетке вторичной упаковки (комплект На этикетке вторичной упаковки упаковочный транспортный) со знаком радиационной опасности указывают: Ø наименование производителя, Ø товарный знак производителя Ø адрес Ø название препарата, Ø лекарственную форму, Ø состав, Ø активность на установленную дату (и время) поставки, Ø номер серии, Ø «стерильно» Ø срок годности, Ø условия хранения, Ø тип и номер контейнера, Ø транспортную категорию Ø номер регистрационного удостоверения Ø штрих-код. 47
 • РФП хранят в соответствии: Ø «Основными санитарными правилами обеспечения радиационной безопасности» (ОСПОРБ-99)(в специальных шкафах для радиоактивных веществ) Ø специальными требованиями, если таковые предусмотрены ФС (ФСП) на конкретные препараты. • Условия хранения должны обеспечивать снижение мощности дозы излучения до допустимого уровня. 48
• РФП хранят в соответствии: Ø «Основными санитарными правилами обеспечения радиационной безопасности» (ОСПОРБ-99)(в специальных шкафах для радиоактивных веществ) Ø специальными требованиями, если таковые предусмотрены ФС (ФСП) на конкретные препараты. • Условия хранения должны обеспечивать снижение мощности дозы излучения до допустимого уровня. 48
 • Срок годности радиофармацевтического препарата препарата (Storage time of Radiopharmaceutical) – время, в течение которого радиофармацевтический препарат удовлетворяет требованиям фармакопейной статьи (фармакопейной статьи предприятия). • Ультракороткоживущий радионуклид – радионуклид с периодом полураспада до 2 часов. 49
• Срок годности радиофармацевтического препарата препарата (Storage time of Radiopharmaceutical) – время, в течение которого радиофармацевтический препарат удовлетворяет требованиям фармакопейной статьи (фармакопейной статьи предприятия). • Ультракороткоживущий радионуклид – радионуклид с периодом полураспада до 2 часов. 49
 Срок годности РФП определяется следующими факторами: Ø Стабильностью химического и радиохимического состава; Ø Уменьшением активности с течением времени по закону радиоактиного распада; Ø Возрастанием относительного состава долгоживущих радионуклидных примесей, имеющие периоды полураспада больше, чем у основного радионуклида Ø Срок хранения приводится в ФС. 50
Срок годности РФП определяется следующими факторами: Ø Стабильностью химического и радиохимического состава; Ø Уменьшением активности с течением времени по закону радиоактиного распада; Ø Возрастанием относительного состава долгоживущих радионуклидных примесей, имеющие периоды полураспада больше, чем у основного радионуклида Ø Срок хранения приводится в ФС. 50
 Из организма радиоактивные препараты выводятся постепенно через желудочно- кишечный тракт (до 90%) или через почки (до 10%), значительно реже через слизистую оболочку рта, кожу, потовые и молочные железы. 51
Из организма радиоактивные препараты выводятся постепенно через желудочно- кишечный тракт (до 90%) или через почки (до 10%), значительно реже через слизистую оболочку рта, кожу, потовые и молочные железы. 51
 Гомеопатические лекарственные средства неорганической природы 52
Гомеопатические лекарственные средства неорганической природы 52
 • Основатель гомеопатии -немецкий ученый и врач Христиан Самуэль Ганеман (1755 - 1843). • 1796 – год рождения гомеопатии. • Метод гомеопатии разрешен в >30 стран: В Индии 50% врачей применяют гомеопатическую систему лечения, в Англии – 45%, во Франции -32%, в Германии – 25%. 53
• Основатель гомеопатии -немецкий ученый и врач Христиан Самуэль Ганеман (1755 - 1843). • 1796 – год рождения гомеопатии. • Метод гомеопатии разрешен в >30 стран: В Индии 50% врачей применяют гомеопатическую систему лечения, в Англии – 45%, во Франции -32%, в Германии – 25%. 53
 основные принципы и правила гомеопатии • 1. Испытания на здоровых людях: испытываемое вещество, из которого впоследствии с помощью гомеопатических фармацевтических технологий может быть изготовлено гомеопатическое лекарство, вводится в субтоксических дозах и вызывает дозах временное (хотя и не опасное) расстройство здоровья. 54
основные принципы и правила гомеопатии • 1. Испытания на здоровых людях: испытываемое вещество, из которого впоследствии с помощью гомеопатических фармацевтических технологий может быть изготовлено гомеопатическое лекарство, вводится в субтоксических дозах и вызывает дозах временное (хотя и не опасное) расстройство здоровья. 54
 2. Принцип подобия • Основным принципом гомеопатии является «Закон подобия» «Similia Similibus curantur» . • Ганеман предложил осуществлять подбор ЛС, сопоставляя признаки отравления большими дозами ЛС с симптомами болезни. • Отсюда произошло название гомеопатия: homois – подобный, pathos- болезнь. 55
2. Принцип подобия • Основным принципом гомеопатии является «Закон подобия» «Similia Similibus curantur» . • Ганеман предложил осуществлять подбор ЛС, сопоставляя признаки отравления большими дозами ЛС с симптомами болезни. • Отсюда произошло название гомеопатия: homois – подобный, pathos- болезнь. 55
 3. Принцип потенцирования и приготовление гомеопатических лекарств 56
3. Принцип потенцирования и приготовление гомеопатических лекарств 56
 57
57
 58
58
 • С. Ганеман разработал и применил новый принцип – потенцирование (динамизация) гомеопатических лекарств в процессе их приготовления • Сущность принципа: поэтапное снижение концентрации исходного гомеопатического концентрации вещества в носителе – в растворе, матричной настойке или порошке – (в 10 или 100 раз на каждом этапе, ). • Одновременно на каждом этапе изготовляемое ЛВ подвергается процессу потенцирования (динамизации) – интенсивно встряхивается или растирается в течение определенного времени. 59
• С. Ганеман разработал и применил новый принцип – потенцирование (динамизация) гомеопатических лекарств в процессе их приготовления • Сущность принципа: поэтапное снижение концентрации исходного гомеопатического концентрации вещества в носителе – в растворе, матричной настойке или порошке – (в 10 или 100 раз на каждом этапе, ). • Одновременно на каждом этапе изготовляемое ЛВ подвергается процессу потенцирования (динамизации) – интенсивно встряхивается или растирается в течение определенного времени. 59
 • в гомеопатии применяются лекарства, концентрации которых по сравнению с исходной настойкой составляют от 10 -3 до 10 -400 • Для характеристики гомеопатических лекарств применяется термин разведение (потенция). • Цифровое обозначение количества операций разбавления исходного вещества определяет потенцию гомеопатического лекарства. 60
• в гомеопатии применяются лекарства, концентрации которых по сравнению с исходной настойкой составляют от 10 -3 до 10 -400 • Для характеристики гомеопатических лекарств применяется термин разведение (потенция). • Цифровое обозначение количества операций разбавления исходного вещества определяет потенцию гомеопатического лекарства. 60
 • буква D, или «Х» указывает на использование , или «Х десятичной шкалы разведений • D 3 показывает, что в процессе изготовления из исходной субстанции (матричной настойки) ЛС прошло три этапа, на каждом из которых подвергалось потенцированию и разведению в 10 раз • Обозначение 12, С 12, или СН 12 показывает, 12, С 12, или СН 12 что в процессе изготовления лекарство прошло двенадцать этапов, на каждом из которых подвергалось потенцированию и разведению в 100 раз • Пятидесятитысячная шкала обозначается буквами LМ или Q. Самая высокая потенция LМ 30 • • корсаковская шкала – К. 61
• буква D, или «Х» указывает на использование , или «Х десятичной шкалы разведений • D 3 показывает, что в процессе изготовления из исходной субстанции (матричной настойки) ЛС прошло три этапа, на каждом из которых подвергалось потенцированию и разведению в 10 раз • Обозначение 12, С 12, или СН 12 показывает, 12, С 12, или СН 12 что в процессе изготовления лекарство прошло двенадцать этапов, на каждом из которых подвергалось потенцированию и разведению в 100 раз • Пятидесятитысячная шкала обозначается буквами LМ или Q. Самая высокая потенция LМ 30 • • корсаковская шкала – К. 61
 Критерии выбора потенции: ØНизкие - при заболеваниях органов; Øсредние - при функциональных расстройствах; Øвысокие - при психических симтомах • Если ЛВ в непотенцированном виде – незначительно терапевтически активны, то – низкая потенция. Токсические ЛВ – в высокой потенции • Низкие потенции – при вялых вегетативных реакциях, высокие – при аллергических реакциях и вегетативной дисфункции 62
Критерии выбора потенции: ØНизкие - при заболеваниях органов; Øсредние - при функциональных расстройствах; Øвысокие - при психических симтомах • Если ЛВ в непотенцированном виде – незначительно терапевтически активны, то – низкая потенция. Токсические ЛВ – в высокой потенции • Низкие потенции – при вялых вегетативных реакциях, высокие – при аллергических реакциях и вегетативной дисфункции 62
 Адреналин • Большая доза: Д 6 –спазм сосудов • Немая доза: Д 7 -Д 32 – отсутствие эффекта • Малая доза Д 33 – расширение сосудов 63
Адреналин • Большая доза: Д 6 –спазм сосудов • Немая доза: Д 7 -Д 32 – отсутствие эффекта • Малая доза Д 33 – расширение сосудов 63
 4. Выбор и назначение гомеопатического лекарства • Реперторизация – метод выбора гомеопатического монопрепарата путем аналитического сравнения комплекса симптомов больного с лекарственным патогенезом с помощью реперториума по специальной схеме. • Реперториум в гомеопатии – это справочник симптомов по «Материи Медика» . 64
4. Выбор и назначение гомеопатического лекарства • Реперторизация – метод выбора гомеопатического монопрепарата путем аналитического сравнения комплекса симптомов больного с лекарственным патогенезом с помощью реперториума по специальной схеме. • Реперториум в гомеопатии – это справочник симптомов по «Материи Медика» . 64
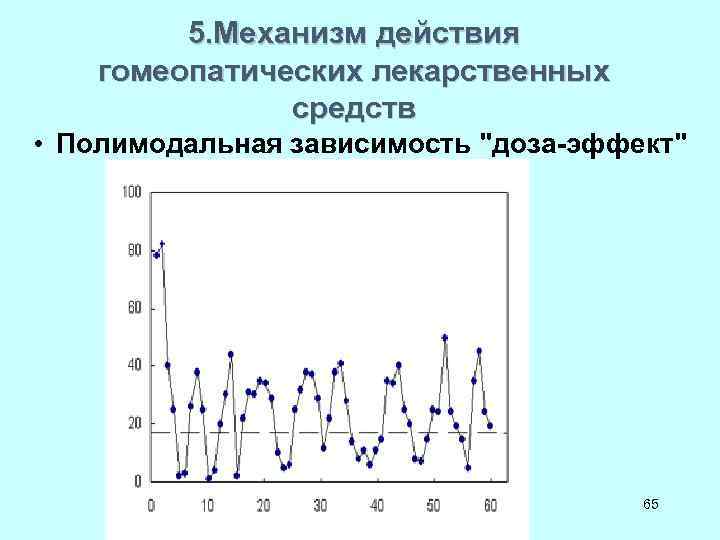
 5. Механизм действия гомеопатических лекарственных средств • Полимодальная зависимость "доза-эффект" 65
5. Механизм действия гомеопатических лекарственных средств • Полимодальная зависимость "доза-эффект" 65
 • Эффект действия ЛС сохраняется в процессе последовательных разведений и перемешивании, и отсутствует в противном случае. • доказана разница в действии на активность цитохромоксидазы митохондрий между гомеопатически приготовленными Mercurius phosphoricus в потенциях D 6, D 8, D 12, D 15 и фосфорнокислой ртути в разведения х 10 -6, 10 -8, 10 -12, 10 -15. 66
• Эффект действия ЛС сохраняется в процессе последовательных разведений и перемешивании, и отсутствует в противном случае. • доказана разница в действии на активность цитохромоксидазы митохондрий между гомеопатически приготовленными Mercurius phosphoricus в потенциях D 6, D 8, D 12, D 15 и фосфорнокислой ртути в разведения х 10 -6, 10 -8, 10 -12, 10 -15. 66
 • «Natrium chloratum» • Рекомендуемая доза – С 3, С 6 или С 12. • Приготовление 1 -ой сотенной тритурации С 1: 0, 1 г вещества растирают с 9, 9 г молочного сахара. • С 1= 10 -2 содержит 0, 1 г Na. Cl составляет 0, 0017 М = 17 х10 -4 М вещества. • Разведение С 12 соответствует 10 -24. Содержание исходного вещества в С 12 тритурации составит 17 х10 -4 х10 -24: 10 -2 =17 х10 - 26 моль. • 1 моль содержит 6, 02 х1023 частиц. Следовательно, в 12 -ом сотенном растирании будет содержаться: 6, 02 х1023 х 17 х10 -26=102 х10 -3 = 0, 1 частиц. 67
• «Natrium chloratum» • Рекомендуемая доза – С 3, С 6 или С 12. • Приготовление 1 -ой сотенной тритурации С 1: 0, 1 г вещества растирают с 9, 9 г молочного сахара. • С 1= 10 -2 содержит 0, 1 г Na. Cl составляет 0, 0017 М = 17 х10 -4 М вещества. • Разведение С 12 соответствует 10 -24. Содержание исходного вещества в С 12 тритурации составит 17 х10 -4 х10 -24: 10 -2 =17 х10 - 26 моль. • 1 моль содержит 6, 02 х1023 частиц. Следовательно, в 12 -ом сотенном растирании будет содержаться: 6, 02 х1023 х 17 х10 -26=102 х10 -3 = 0, 1 частиц. 67
 При изготовлении ЛП для получения последующего разведения, массу расчитывают по формулам: А=Б: 100 В=Б-А А-масса предыдущего разведения Б-масса изготовленного ЛП В- масса вспомогательного в-ва 68
При изготовлении ЛП для получения последующего разведения, массу расчитывают по формулам: А=Б: 100 В=Б-А А-масса предыдущего разведения Б-масса изготовленного ЛП В- масса вспомогательного в-ва 68
 ЗАДАЧИ • Студент изготовил вручную 300 г внутриаптечной заготовки Baruta carbonica C 3, взяв 3, 0 г бария карбоната в разведении С 2 и 297 г сахара молочного. Правильно ли взяты навески? (Тритурация гомеопатическая – твердая ЛФ в виде порошка, состоящая из смеси ЛВ со вспомогательными веществами). • 69
ЗАДАЧИ • Студент изготовил вручную 300 г внутриаптечной заготовки Baruta carbonica C 3, взяв 3, 0 г бария карбоната в разведении С 2 и 297 г сахара молочного. Правильно ли взяты навески? (Тритурация гомеопатическая – твердая ЛФ в виде порошка, состоящая из смеси ЛВ со вспомогательными веществами). • 69
 • Да: • Baruta carbonica C 2 = 300: 100=3 г 70
• Да: • Baruta carbonica C 2 = 300: 100=3 г 70
 • Студент изготовил с помощью механического смесителя внутриаптечную заготовку тритурацию Cuprum metallicum D 3, взяв 0, 2 г меди металлической в разведении D 2 и 199, 8 г сахара молочного. Правильно ли взяты навески, если нужно было получить 200 г тритурации Cuprum metallicum. (Тритурация гомеопатическая – твердая ЛФ в виде порошка, состоящая из смеси ЛВ со вспомогательными веществами). • 71
• Студент изготовил с помощью механического смесителя внутриаптечную заготовку тритурацию Cuprum metallicum D 3, взяв 0, 2 г меди металлической в разведении D 2 и 199, 8 г сахара молочного. Правильно ли взяты навески, если нужно было получить 200 г тритурации Cuprum metallicum. (Тритурация гомеопатическая – твердая ЛФ в виде порошка, состоящая из смеси ЛВ со вспомогательными веществами). • 71
 • Нет. Масса Cuprum metallicum D 2 = 200: 10=20 грамм + 180, 0 г сахара молочного 72
• Нет. Масса Cuprum metallicum D 2 = 200: 10=20 грамм + 180, 0 г сахара молочного 72
 • Студент приготовил внутриаптечную заготовку Bismuthum subnitricum (Висмута нитрат основной) C 6, используя висмута нитрат основной в качестве основного компонента и сахар молочный, как вспомогательное вещество. Определите сколько молекул висмута нитрата основного содержится в 10 г данной тритурации. Известно, что для приготовления тритурации С 1 взяли 0, 1 г висмута нитрата основного и 9, 9 г сахара молочного. 73
• Студент приготовил внутриаптечную заготовку Bismuthum subnitricum (Висмута нитрат основной) C 6, используя висмута нитрат основной в качестве основного компонента и сахар молочный, как вспомогательное вещество. Определите сколько молекул висмута нитрата основного содержится в 10 г данной тритурации. Известно, что для приготовления тритурации С 1 взяли 0, 1 г висмута нитрата основного и 9, 9 г сахара молочного. 73
 • Приготовление 1 -ой сотенной тритурации С 1: 0, 1 г вещества растирают с 9, 9 г молочного сахара. • М м Bi. ONO 3 = 209+64+14=277 1 М – 277 г Х - 0, 1 г Х=3, 6 х10 -4 М • В С 1= 10 -2 Bismuthum subnitricum содержится = 3, 6 х10 -4 М вещества. • Разведение С 6 соответствует 10 -12. Содержание исходного вещества в С 6 тритурации составит 3, 6 х10 -4 х10 -12: 10 -2=3, 6 х 10 -14 моль. • 1 моль содержит 6, 02 х1023 частиц. Следовательно, в 6 -ом сотенном растирании будет содержаться: • 6, 02 х1023 х 3, 6 х 10 -14=2, 167 х1010 молекул. 74
• Приготовление 1 -ой сотенной тритурации С 1: 0, 1 г вещества растирают с 9, 9 г молочного сахара. • М м Bi. ONO 3 = 209+64+14=277 1 М – 277 г Х - 0, 1 г Х=3, 6 х10 -4 М • В С 1= 10 -2 Bismuthum subnitricum содержится = 3, 6 х10 -4 М вещества. • Разведение С 6 соответствует 10 -12. Содержание исходного вещества в С 6 тритурации составит 3, 6 х10 -4 х10 -12: 10 -2=3, 6 х 10 -14 моль. • 1 моль содержит 6, 02 х1023 частиц. Следовательно, в 6 -ом сотенном растирании будет содержаться: • 6, 02 х1023 х 3, 6 х 10 -14=2, 167 х1010 молекул. 74
 Контроль качества лекарственных средств, используемых в гомеопатии в различных лекарственных формах • Специфическая черта контроля качества ГЛС - постадийность. 1. ЛС, содержащие БАВ в разведениях до С 2 (10 -4), контролируют по тем же показателям, что и аллопатические лекарственные средства. • 2. ЛС, содержащие БАВ в С 3 (10 -6), контролируют, после проведения концентрирования БАВ в пробах. 75
Контроль качества лекарственных средств, используемых в гомеопатии в различных лекарственных формах • Специфическая черта контроля качества ГЛС - постадийность. 1. ЛС, содержащие БАВ в разведениях до С 2 (10 -4), контролируют по тем же показателям, что и аллопатические лекарственные средства. • 2. ЛС, содержащие БАВ в С 3 (10 -6), контролируют, после проведения концентрирования БАВ в пробах. 75
 • 3. ЛС, содержащие БАВ в разведениях от С 4 (10 -8) до С 6 (10 -12), контролируют путем установления подлинности БАВ в пробе, адекватной суточному приему, а в отдельных случаях – прописанной на курс лечения. • 4. ЛС, содержащие БАВ в разведениях свыше С 6 (10 -12) контролируют путем строгого соблюдения технологии и составления акта загрузки всех ингредиентов при получении лекарственной формы. 76
• 3. ЛС, содержащие БАВ в разведениях от С 4 (10 -8) до С 6 (10 -12), контролируют путем установления подлинности БАВ в пробе, адекватной суточному приему, а в отдельных случаях – прописанной на курс лечения. • 4. ЛС, содержащие БАВ в разведениях свыше С 6 (10 -12) контролируют путем строгого соблюдения технологии и составления акта загрузки всех ингредиентов при получении лекарственной формы. 76

