Кафедра фармацевтической и токсикологической химии



































































оконч. V гр. Лекция III группа2012.ppt
- Количество слайдов: 76
 Кафедра фармацевтической и токсикологической химии Лекция № 6 «Лекарственные средства производные р- элементов V гр. ПСЭ» (продолжение) доц. Богословская О. А. 18. 10. 2012
Кафедра фармацевтической и токсикологической химии Лекция № 6 «Лекарственные средства производные р- элементов V гр. ПСЭ» (продолжение) доц. Богословская О. А. 18. 10. 2012
 Висмута нитрат основный Ø Висмута субнитрат Bismuthi subnitras Bi. O(NO 3) • Н 2 О Мr 305, 0 Описание Ø Аморфный или микрокристаллический порошок белого цвета, без запаха. Ø Практически не растворим в воде и спирте. Легко растворим в минеральных кислотах (азотная, соляная). 2
Висмута нитрат основный Ø Висмута субнитрат Bismuthi subnitras Bi. O(NO 3) • Н 2 О Мr 305, 0 Описание Ø Аморфный или микрокристаллический порошок белого цвета, без запаха. Ø Практически не растворим в воде и спирте. Легко растворим в минеральных кислотах (азотная, соляная). 2
 Определение подлинности n 1. При прокаливании препарата образуется желто-оранжевый оксид висмута Bi 2 O 3 и выделяются красно-бурые пары диоксида азота (IV): 4 Bi. ONO 3 2 Bi 2 O 3 + 4 NO 2 + O 2 3
Определение подлинности n 1. При прокаливании препарата образуется желто-оранжевый оксид висмута Bi 2 O 3 и выделяются красно-бурые пары диоксида азота (IV): 4 Bi. ONO 3 2 Bi 2 O 3 + 4 NO 2 + O 2 3
 Общие реакции подлинности на ион висмута Bi 3+ • 2. Сульфиды щелочных металлов дают с растворами солей висмута темно- коричневый осадок сульфида висмута. Реакция идет в кислой среде – для перевода препарата в ионное состояние - висмутил 2 Bi. ONO 3 + 3 Na 2 S + 4 HCI 2 Bi 2 S 3 + + 2 Na. NO 3 + 4 Na. CI + 2 H 2 O Сульфид висмута растворяется в концентрированной азотной кислоте. • Эта реакция позволяет обнаружить висмут в количестве 10 мкг/л (1: 100000). 4
Общие реакции подлинности на ион висмута Bi 3+ • 2. Сульфиды щелочных металлов дают с растворами солей висмута темно- коричневый осадок сульфида висмута. Реакция идет в кислой среде – для перевода препарата в ионное состояние - висмутил 2 Bi. ONO 3 + 3 Na 2 S + 4 HCI 2 Bi 2 S 3 + + 2 Na. NO 3 + 4 Na. CI + 2 H 2 O Сульфид висмута растворяется в концентрированной азотной кислоте. • Эта реакция позволяет обнаружить висмут в количестве 10 мкг/л (1: 100000). 4
 n 3. Реакция с йодидом калия. При добавлении к концентрированному подкисленному раствору препарата раствора йодида калия выделяется бурый осадок йодида висмута, который растворяется в избытке реактива с образованием калия тетрайодовисмутата(III), окрашенного в темно-оранжевый цвет: Bi(NO 3)3 + 3 KI Bi. I 3 + 3 KNO 3 Bi. I 3 + KI K[Bi. I 4] раствор йодида калия вначале добавляют по каплям 5
n 3. Реакция с йодидом калия. При добавлении к концентрированному подкисленному раствору препарата раствора йодида калия выделяется бурый осадок йодида висмута, который растворяется в избытке реактива с образованием калия тетрайодовисмутата(III), окрашенного в темно-оранжевый цвет: Bi(NO 3)3 + 3 KI Bi. I 3 + 3 KNO 3 Bi. I 3 + KI K[Bi. I 4] раствор йодида калия вначале добавляют по каплям 5
 Подлинность (ВР): Ø А. с калия йодида. Ø B. Даёт реакцию (б) на висмут (Общие реакции). Ø С. Даёт реакцию на нитраты. Ø D. р. Н раствора 5% раствора, содержащего 10% азотной кислоты и 22% аммиака, ≤ 2. 0 6
Подлинность (ВР): Ø А. с калия йодида. Ø B. Даёт реакцию (б) на висмут (Общие реакции). Ø С. Даёт реакцию на нитраты. Ø D. р. Н раствора 5% раствора, содержащего 10% азотной кислоты и 22% аммиака, ≤ 2. 0 6
 Оценка чистоты (ГФ) Недопустимые примеси: Недопустимые примеси Ø медь, Ø свинец, Ø соли аммония, Ø сульфаты, Ø мышьяк и теллур. Допустимые примеси Ø хлориды, Ø соли щелочных и щелочноземельных металлов, Ø карбонаты, Ø серебро. 7
Оценка чистоты (ГФ) Недопустимые примеси: Недопустимые примеси Ø медь, Ø свинец, Ø соли аммония, Ø сульфаты, Ø мышьяк и теллур. Допустимые примеси Ø хлориды, Ø соли щелочных и щелочноземельных металлов, Ø карбонаты, Ø серебро. 7
 Оценка чистоты n Недопустимые примеси n Для обнаружения меди, свинца и сульфатов препарат растворяют в азотной кислоте, осаждают основные соли висмута, образовавшиеся в результате гидролиза при разбавлении и нагревании раствора. n Для обнаружения меди в фильтрат добавляют аммиак. В присутствии меди фильтрат должен окрашиваться в ультрамариновый цвет, в результате образования аммиаката меди. 2 Cu 2+ + 4 NH 3. H 2 O 2[Сu(NН 3)4]2+ + 4 H 2 O комплекс ультрамаринового цвета 8
Оценка чистоты n Недопустимые примеси n Для обнаружения меди, свинца и сульфатов препарат растворяют в азотной кислоте, осаждают основные соли висмута, образовавшиеся в результате гидролиза при разбавлении и нагревании раствора. n Для обнаружения меди в фильтрат добавляют аммиак. В присутствии меди фильтрат должен окрашиваться в ультрамариновый цвет, в результате образования аммиаката меди. 2 Cu 2+ + 4 NH 3. H 2 O 2[Сu(NН 3)4]2+ + 4 H 2 O комплекс ультрамаринового цвета 8
 n Для обнаружения свинца в этот же фильтрат добавляют разведенной серной кислоты. Образуется сульфат свинца и появляется белый осадок или муть (Pb. SO 4). n Для обнаружения сульфатов в этот же фильтрат добавляют нитрат бария. Раствор должен оставаться прозрачным. 9
n Для обнаружения свинца в этот же фильтрат добавляют разведенной серной кислоты. Образуется сульфат свинца и появляется белый осадок или муть (Pb. SO 4). n Для обнаружения сульфатов в этот же фильтрат добавляют нитрат бария. Раствор должен оставаться прозрачным. 9
 n Определение мышьяка и теллура проводят по методу Буго и Тиле. Мышьяк и теллур восстанавливают до элементных форм. В качестве восстановителя используют гипофосфит натрия: 2 Na(H 2 P+1 O 2) + Na 2 Te. O 3 Te + 2 Na 2(HP+3 O 3) + H 2 O n При этом теллур дает черное окрашивание, а мышьяк – бурое, за счет выделения элементных форм. n Соли аммония не должны обнаруживаться по запаху при кипячении 1 г препарата в 5 мл раствора натрия гидроксида. 10
n Определение мышьяка и теллура проводят по методу Буго и Тиле. Мышьяк и теллур восстанавливают до элементных форм. В качестве восстановителя используют гипофосфит натрия: 2 Na(H 2 P+1 O 2) + Na 2 Te. O 3 Te + 2 Na 2(HP+3 O 3) + H 2 O n При этом теллур дает черное окрашивание, а мышьяк – бурое, за счет выделения элементных форм. n Соли аммония не должны обнаруживаться по запаху при кипячении 1 г препарата в 5 мл раствора натрия гидроксида. 10
 n Соли щелочных и щелочно-земельных металлов : препарат растворяют в соляной кислоте, пропускают сероводород до полного осаждения висмута (сульфид висмута), фильтруют. Фильтрат выпаривают досуха и остаток прокаливают до постоянной массы. Остаток оксидов и неразлагаюшихся солей не должен превышать 0, 5 %. 11
n Соли щелочных и щелочно-земельных металлов : препарат растворяют в соляной кислоте, пропускают сероводород до полного осаждения висмута (сульфид висмута), фильтруют. Фильтрат выпаривают досуха и остаток прокаливают до постоянной массы. Остаток оксидов и неразлагаюшихся солей не должен превышать 0, 5 %. 11
 Ø Содержание карбонатов не должно превышать количества, которое Содержание карбонатов можно обнаружить по выделению углекислого газа, если на 1 г препарата подействовать 3 мл азотной кислоты. Ø Определение хлоридов –эталонный метод Определение хлоридов Ø Определение серебра –эталонный метод. Определение серебра Приготовление эталона описано в ФС 12
Ø Содержание карбонатов не должно превышать количества, которое Содержание карбонатов можно обнаружить по выделению углекислого газа, если на 1 г препарата подействовать 3 мл азотной кислоты. Ø Определение хлоридов –эталонный метод Определение хлоридов Ø Определение серебра –эталонный метод. Определение серебра Приготовление эталона описано в ФС 12
 Оценка чистоты (ЕР) Допустимые примеси Ø медь, Ø свинец, Ø Вещества, осаждаемые аммиаком, Ø хлориды, Ø серебро. 13
Оценка чистоты (ЕР) Допустимые примеси Ø медь, Ø свинец, Ø Вещества, осаждаемые аммиаком, Ø хлориды, Ø серебро. 13
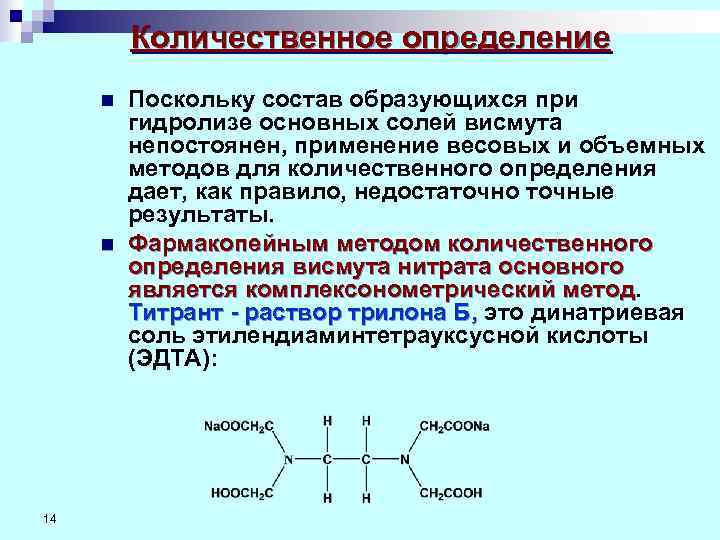
 Количественное определение n Поскольку состав образующихся при гидролизе основных солей висмута непостоянен, применение весовых и объемных методов для количественного определения дает, как правило, недостаточно точные результаты. n Фармакопейным методом количественного определения висмута нитрата основного является комплексонометрический метод Титрант - раствор трилона Б, это динатриевая Титрант - раствор трилона Б, соль этилендиаминтетрауксусной кислоты (ЭДТА): 14
Количественное определение n Поскольку состав образующихся при гидролизе основных солей висмута непостоянен, применение весовых и объемных методов для количественного определения дает, как правило, недостаточно точные результаты. n Фармакопейным методом количественного определения висмута нитрата основного является комплексонометрический метод Титрант - раствор трилона Б, это динатриевая Титрант - раствор трилона Б, соль этилендиаминтетрауксусной кислоты (ЭДТА): 14
 Ø ЭДТА является шестидентатным лигандом, так как содержит 4 карбоксильные группы и два атома азота, имеющие каждый по неподеленной паре электронов. Хелаты ЭДТА с ионами металлов называют комплексонатами. Ø ЭДТА- четырехосновная кислота и обозначается H 4 Y Ø ЭДТА как титрант реагирует с ионами металла в соотношении 1: 1 независимо от зарядов катиона, при этом происходит выделение двух ионов водорода: Bi 3+ + H 2 Y 2 - → Bi. Y- + 2 H+. Ø Для связывания ионов водорода в анализируемый раствор добавляют аммиачный буфер или щелочь. Если определение проводят в кислой среде, то ионы водорода не связываются. Ø В качестве индикаторов используют металлоиндикаторы (органические красители, образующие с ионами титруемого металла интенсивно окрашенные комплексы, цвет которых 15 отличается от окраски свободного индикатора).
Ø ЭДТА является шестидентатным лигандом, так как содержит 4 карбоксильные группы и два атома азота, имеющие каждый по неподеленной паре электронов. Хелаты ЭДТА с ионами металлов называют комплексонатами. Ø ЭДТА- четырехосновная кислота и обозначается H 4 Y Ø ЭДТА как титрант реагирует с ионами металла в соотношении 1: 1 независимо от зарядов катиона, при этом происходит выделение двух ионов водорода: Bi 3+ + H 2 Y 2 - → Bi. Y- + 2 H+. Ø Для связывания ионов водорода в анализируемый раствор добавляют аммиачный буфер или щелочь. Если определение проводят в кислой среде, то ионы водорода не связываются. Ø В качестве индикаторов используют металлоиндикаторы (органические красители, образующие с ионами титруемого металла интенсивно окрашенные комплексы, цвет которых 15 отличается от окраски свободного индикатора).
 Принцип комплексонометрического титрования Ø К исследуемому раствору, содержащему определенный катион, при строго определенном значении р. Н прибавляют небольшое количество соответствующего индикатора (менее 1%). Ø Если индикатор –шестиосновная кислота (ксиленовый оранжевый): Н 6 Ind=3 H+ + Н 3 Ind 3 - (в свободном виде - желтого цвета) В результате образуется хорошо растворимое в воде окрашенное комплексное соединение индикатора с металлом. Bi 3+ + Н 3 Ind 3 - = Bi. Н 3 Ind 3 - Bi Ø Комплекс индикатора с ионом металла достаточно устойчив, но в 10 раз менее устойчив, чем комплекс металла с ЭДТА (изменение окраски индикатора должно быть четким, контрастным и быстрым). 16
Принцип комплексонометрического титрования Ø К исследуемому раствору, содержащему определенный катион, при строго определенном значении р. Н прибавляют небольшое количество соответствующего индикатора (менее 1%). Ø Если индикатор –шестиосновная кислота (ксиленовый оранжевый): Н 6 Ind=3 H+ + Н 3 Ind 3 - (в свободном виде - желтого цвета) В результате образуется хорошо растворимое в воде окрашенное комплексное соединение индикатора с металлом. Bi 3+ + Н 3 Ind 3 - = Bi. Н 3 Ind 3 - Bi Ø Комплекс индикатора с ионом металла достаточно устойчив, но в 10 раз менее устойчив, чем комплекс металла с ЭДТА (изменение окраски индикатора должно быть четким, контрастным и быстрым). 16
 Ø Проводят титрование раствором трилона Б свободных ионов металла. Более 99% ионов металла находится в свободном виде и в ходе титрования связывается комплексоном (Трилоном Б) в бесцветный растворимый комплекс ЭДТА с металлом. Bi 3+ + H 2 Y 2 - → Bi. Y- + 2 H+. n В процессе титрования титрант трилон Б (Na 2 ЭДТА) связывает ионы висмута, образовавшиеся при растворении препарата в азотной кислоте, в комплексное соединение: Na 2 ЭДТА + Bi(NO 3)3 Na[Bi. ЭДТА]+2 HNO 3+Na. NO 3 17
Ø Проводят титрование раствором трилона Б свободных ионов металла. Более 99% ионов металла находится в свободном виде и в ходе титрования связывается комплексоном (Трилоном Б) в бесцветный растворимый комплекс ЭДТА с металлом. Bi 3+ + H 2 Y 2 - → Bi. Y- + 2 H+. n В процессе титрования титрант трилон Б (Na 2 ЭДТА) связывает ионы висмута, образовавшиеся при растворении препарата в азотной кислоте, в комплексное соединение: Na 2 ЭДТА + Bi(NO 3)3 Na[Bi. ЭДТА]+2 HNO 3+Na. NO 3 17
 Ø В точке эквивалентности: происходит В точке эквивалентности: разрушение комплекса металл-индикатор, образование более устойчивого комплекса металла – ЭДТА и свободного индикатора. Bi. Н 3 Ind 3 - + H 2 Y 2 - → Bi. Y- + 3 H+ +Ind 3 - Bi + Ø При этом выделяется свободный индикатор, который окрашивает раствор в другой цвет, присущий свободному индикатору при данном значении р. Н. 18
Ø В точке эквивалентности: происходит В точке эквивалентности: разрушение комплекса металл-индикатор, образование более устойчивого комплекса металла – ЭДТА и свободного индикатора. Bi. Н 3 Ind 3 - + H 2 Y 2 - → Bi. Y- + 3 H+ +Ind 3 - Bi + Ø При этом выделяется свободный индикатор, который окрашивает раствор в другой цвет, присущий свободному индикатору при данном значении р. Н. 18
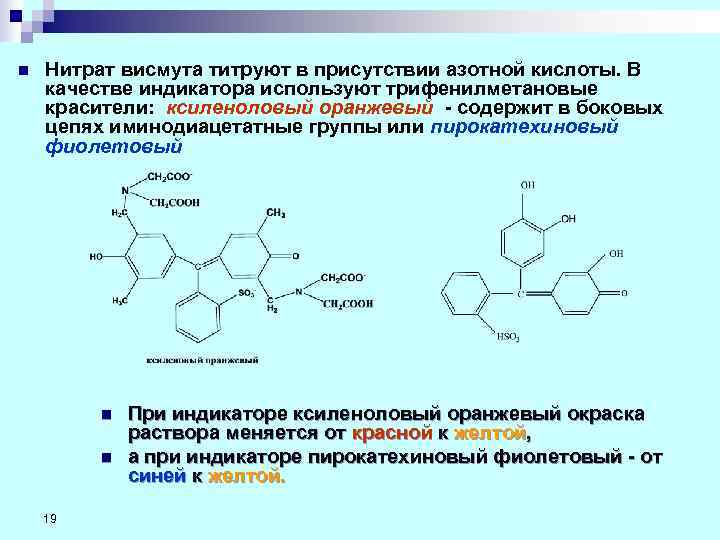
 n Нитрат висмута титруют в присутствии азотной кислоты. В качестве индикатора используют трифенилметановые красители: ксиленоловый оранжевый - cодержит в боковых цепях иминодиацетатные группы или пирокатехиновый фиолетовый n При индикаторе ксиленоловый оранжевый окраска раствора меняется от красной к желтой, n а при индикаторе пирокатехиновый фиолетовый - от синей к желтой. 19
n Нитрат висмута титруют в присутствии азотной кислоты. В качестве индикатора используют трифенилметановые красители: ксиленоловый оранжевый - cодержит в боковых цепях иминодиацетатные группы или пирокатехиновый фиолетовый n При индикаторе ксиленоловый оранжевый окраска раствора меняется от красной к желтой, n а при индикаторе пирокатехиновый фиолетовый - от синей к желтой. 19
 Применение Ø Вяжущее, адсорбирующее, антацидное, противомикробное и противовоспалительное средство. Применяют при желудочно-кишечных заболеваниях. Ø Выпускается в порошке и таблетках по 0, 25 и 0, 5 г. Входит в состав комбинированных антацидных препаратов (таблетки «Викалин» , «Викаир» и др. ). Ø Применяют также наружно в виде мази и присыпки при воспалительных заболеваниях кожи и слизистых оболочек. В терапии вместо Bi(NO 3)3 следует применять (Bi. O)2 CO 3, поскольку нитрат восстанавливается кишечными микробами до нитрита. Последний может вызывать отравления, ошибочно принимаемые за отравления висмутом. 20
Применение Ø Вяжущее, адсорбирующее, антацидное, противомикробное и противовоспалительное средство. Применяют при желудочно-кишечных заболеваниях. Ø Выпускается в порошке и таблетках по 0, 25 и 0, 5 г. Входит в состав комбинированных антацидных препаратов (таблетки «Викалин» , «Викаир» и др. ). Ø Применяют также наружно в виде мази и присыпки при воспалительных заболеваниях кожи и слизистых оболочек. В терапии вместо Bi(NO 3)3 следует применять (Bi. O)2 CO 3, поскольку нитрат восстанавливается кишечными микробами до нитрита. Последний может вызывать отравления, ошибочно принимаемые за отравления висмутом. 20
 Хранение В хорошо закрытых банках в сухом, защищенном от света месте без доступа воздуха. 21
Хранение В хорошо закрытых банках в сухом, защищенном от света месте без доступа воздуха. 21
 «Лекарственные средства на основе p -элементов III группы» B, Al, Ga, In, Tl (бор, алюминий, галлий, индий, таллий)
«Лекарственные средства на основе p -элементов III группы» B, Al, Ga, In, Tl (бор, алюминий, галлий, индий, таллий)
 Атомы р-элементов III группы n На внешнем электронном слое содержат три валентных электрона. Поэтому бор, алюминий, галлий и индий в своих соединениях имеют степень окисления +III. n С ростом порядкового номера внутри подгруппы металлические свойства элементов усиливаются: Ø бор имеет ярко выраженный неметаллический характер, Ø алюминий, галлий и индий – металлы с амфотерными свойствами, Ø таллий - выраженые металлические свойства. n Наиболее широко в качестве лекарственных средств используются соединения бора и алюминия. 23
Атомы р-элементов III группы n На внешнем электронном слое содержат три валентных электрона. Поэтому бор, алюминий, галлий и индий в своих соединениях имеют степень окисления +III. n С ростом порядкового номера внутри подгруппы металлические свойства элементов усиливаются: Ø бор имеет ярко выраженный неметаллический характер, Ø алюминий, галлий и индий – металлы с амфотерными свойствами, Ø таллий - выраженые металлические свойства. n Наиболее широко в качестве лекарственных средств используются соединения бора и алюминия. 23
 Лекарственные средства на основе р- элементов III группы: борная кислота (Н 3 ВО 3), тетраборат натрия (Na 2 B 4 O 7. 10 Н 2 О), гидроксид алюминия (Al(OH)3), фосфат алюминия (Al. PO 4). 24
Лекарственные средства на основе р- элементов III группы: борная кислота (Н 3 ВО 3), тетраборат натрия (Na 2 B 4 O 7. 10 Н 2 О), гидроксид алюминия (Al(OH)3), фосфат алюминия (Al. PO 4). 24
 Биологическое значение р-элементов III группы ØГаллий Поступает в организм с пищей и содержится в тканях в количестве 0, 01 -0, 06 мкг/г. Галлиий присутствует в железах внутренней секреции, в частности, в гипофизе. «Депо» галлия в организме - костная ткань и печень.
Биологическое значение р-элементов III группы ØГаллий Поступает в организм с пищей и содержится в тканях в количестве 0, 01 -0, 06 мкг/г. Галлиий присутствует в железах внутренней секреции, в частности, в гипофизе. «Депо» галлия в организме - костная ткань и печень.
 Ø У животных, при отравлении галлием, наблюдается поражение нервной системы, сопровождающееся морфологическими изменениями в печени и почках. Наблюдаются значительные колебания в содержании калия и натрия в сыворотке крови, повреждения слизистых оболочек желудочно-кишечного тракта. Ø В медицине нитрат галлия используется при лечении гиперкальциемии у онкологических больных. Ø Радиоизотоп галлия применяют в диагностике и лечении опухолевых заболеваний. В USP-24 приведены фармакопейная статья на инъекционный раствор галлия цитрат 67 Ga. 26
Ø У животных, при отравлении галлием, наблюдается поражение нервной системы, сопровождающееся морфологическими изменениями в печени и почках. Наблюдаются значительные колебания в содержании калия и натрия в сыворотке крови, повреждения слизистых оболочек желудочно-кишечного тракта. Ø В медицине нитрат галлия используется при лечении гиперкальциемии у онкологических больных. Ø Радиоизотоп галлия применяют в диагностике и лечении опухолевых заболеваний. В USP-24 приведены фармакопейная статья на инъекционный раствор галлия цитрат 67 Ga. 26
 Ø Индий- очень мягкий серебристо-белый металл. Индий не обнаружен в составе каких- либо жизненно важных соединений. Считают, что препараты индия могут стимулировать метаболизм. Ø В USP-24 приведены фармакопейная статья на инъекционный раствор индия хлорида, на основе радиоактивного изотопа 111 In. 27
Ø Индий- очень мягкий серебристо-белый металл. Индий не обнаружен в составе каких- либо жизненно важных соединений. Считают, что препараты индия могут стимулировать метаболизм. Ø В USP-24 приведены фармакопейная статья на инъекционный раствор индия хлорида, на основе радиоактивного изотопа 111 In. 27
 Ø Таллий — белый металл с голубоватым оттенком. Как сам таллий, так и его соединения высокотоксичны. Симптомы отравления — поражение нервной системы, почек, желудка, выпадение волос. ПДК в воде для таллия 0, 0001 мг/м 3, в атмосферном воздухе 0, 004 мг/м 3. Смертельная для человека доза таллия составляет 600 мг. Ø В качестве антидота используется берлинская лазурь. Ø Соединения таллия в медицине не применяются из-за своей токсичности. Предполагают, что ион таллия замещает в метаболических процессах ион К+, так как их ионные радиусы близки по величине. Ион таллия, может прочно связываться с тиоловыми группами, нарушая функционирование ряда ферментов. 28
Ø Таллий — белый металл с голубоватым оттенком. Как сам таллий, так и его соединения высокотоксичны. Симптомы отравления — поражение нервной системы, почек, желудка, выпадение волос. ПДК в воде для таллия 0, 0001 мг/м 3, в атмосферном воздухе 0, 004 мг/м 3. Смертельная для человека доза таллия составляет 600 мг. Ø В качестве антидота используется берлинская лазурь. Ø Соединения таллия в медицине не применяются из-за своей токсичности. Предполагают, что ион таллия замещает в метаболических процессах ион К+, так как их ионные радиусы близки по величине. Ион таллия, может прочно связываться с тиоловыми группами, нарушая функционирование ряда ферментов. 28
 Ø Бор относится к эссенциальным микроэлементам. Ø Содержание в организме человека составляет 20 мг. Ø Участвует в углеводном, жировом обменах, в окислительно-восстановительных процессах организма. Ø Предполагают, что бор участвует в кальциевом обмене, т. к. содержание его в паращитовидной железе – основном органе регуляции кальциевого обмена в организме - высокое. Ø Бор снижает токсичность мышьяка при их совместном применении. 29
Ø Бор относится к эссенциальным микроэлементам. Ø Содержание в организме человека составляет 20 мг. Ø Участвует в углеводном, жировом обменах, в окислительно-восстановительных процессах организма. Ø Предполагают, что бор участвует в кальциевом обмене, т. к. содержание его в паращитовидной железе – основном органе регуляции кальциевого обмена в организме - высокое. Ø Бор снижает токсичность мышьяка при их совместном применении. 29
 Ø Верхний предел среднесуточной, безопасной дозы бора для человека - 13 мг. Ø Токсическая доза для человека: 4 г. Летальная доза бора для человека не определена. Ø При острой интоксикации соединениями бора (бурой, борной кислотой) наблюдается рвота и другие диспепсические расстройства, а также шок. Ø При вдыхании газообразных соединений бора могут развиться судороги, мышечные боли, психические нарушения, диплопия. Описано такое эндемическое заболевание, как борный энтерит, которое встречается на Южном Урале и на севере Казахстана. Ø Хроническое перенасыщение бором приводит к выпадению волос, полиморфной сухой эритеме и анемии, которые проходят при нормализации уровня бора в диете. 30
Ø Верхний предел среднесуточной, безопасной дозы бора для человека - 13 мг. Ø Токсическая доза для человека: 4 г. Летальная доза бора для человека не определена. Ø При острой интоксикации соединениями бора (бурой, борной кислотой) наблюдается рвота и другие диспепсические расстройства, а также шок. Ø При вдыхании газообразных соединений бора могут развиться судороги, мышечные боли, психические нарушения, диплопия. Описано такое эндемическое заболевание, как борный энтерит, которое встречается на Южном Урале и на севере Казахстана. Ø Хроническое перенасыщение бором приводит к выпадению волос, полиморфной сухой эритеме и анемии, которые проходят при нормализации уровня бора в диете. 30
 Ø Преимущественно бор накапливается в щитовидной и паращитовидной железах, костной ткани, а также почках, селезенке и сердце. Ø Суточное поступление в организм колеблется от 0, 35 мг до 41 мг в сутки. Для питьевых вод, которые применяются ежедневно, рекомендована предельно допустимая концентрация бора 0, 5 мг/л (по санитарно- эпидемиологическим нормам). 31
Ø Преимущественно бор накапливается в щитовидной и паращитовидной железах, костной ткани, а также почках, селезенке и сердце. Ø Суточное поступление в организм колеблется от 0, 35 мг до 41 мг в сутки. Для питьевых вод, которые применяются ежедневно, рекомендована предельно допустимая концентрация бора 0, 5 мг/л (по санитарно- эпидемиологическим нормам). 31
 Ø Бор имеет тенденцию к накоплению в растениях (особенно в овощах и фруктах): присутствует в яблоках (245 мкг%), грушах (135 мкг%), винограде (365 мкг%), моркови (200 мкг%), орехах (мкг% - это величина, показывающая содержание вещества в микрограммах в 100 граммах продукта). Ø В природных водах бор находится в виде ионов борных кислот. Ø В маломинерализованных подземных водах содержание бора составляет, как правило десятки- сотни мкг/дм 3 , однако в минерализованных щелочных водах его концентрация может достигать единиц и даже десятков мг/л, что делает такую воду потенциально небезопасной для питьевого применения. 32
Ø Бор имеет тенденцию к накоплению в растениях (особенно в овощах и фруктах): присутствует в яблоках (245 мкг%), грушах (135 мкг%), винограде (365 мкг%), моркови (200 мкг%), орехах (мкг% - это величина, показывающая содержание вещества в микрограммах в 100 граммах продукта). Ø В природных водах бор находится в виде ионов борных кислот. Ø В маломинерализованных подземных водах содержание бора составляет, как правило десятки- сотни мкг/дм 3 , однако в минерализованных щелочных водах его концентрация может достигать единиц и даже десятков мг/л, что делает такую воду потенциально небезопасной для питьевого применения. 32
 БОР: растпространение в природе Ø Бор в природе встречается в виде кислородных соединений, входит в состав борной кислоты. Ø В свободном виде известны две разновидности борной кислоты: v метаборная - НВО 2 v ортоборная - Н 3 ВО 3. Ø Полиборные кислоты Н 3 m -2 n В m О 3 m - n в свободном виде не выделены, но известны их соли, например двузамещенный тетраборат натрия или бура - Na 2 B 4 O 7 (m=4, n=5). Ø В большинстве соединений бор трехвалентен. Но присутствие свободной р -орбитали у атома бора делает возможным образование химической связи по донорно-акцепторному типу, что приводит к увеличению валентности до четырех. 33
БОР: растпространение в природе Ø Бор в природе встречается в виде кислородных соединений, входит в состав борной кислоты. Ø В свободном виде известны две разновидности борной кислоты: v метаборная - НВО 2 v ортоборная - Н 3 ВО 3. Ø Полиборные кислоты Н 3 m -2 n В m О 3 m - n в свободном виде не выделены, но известны их соли, например двузамещенный тетраборат натрия или бура - Na 2 B 4 O 7 (m=4, n=5). Ø В большинстве соединений бор трехвалентен. Но присутствие свободной р -орбитали у атома бора делает возможным образование химической связи по донорно-акцепторному типу, что приводит к увеличению валентности до четырех. 33
 Кислота борная Acidum boricum Н 3 ВО 3 М. м. 61. 8 Ø Получение. Из буры (Na 2 B 4 O 7. 10 H 2 O - Natrii tetraboras). Горячий раствор тетрабората натрия обрабатывают минеральной кислотой, затем раствор охлаждают, а выделившиеся кристаллы борной кислоты перекристаллизовывают из воды: Na 2 B 4 O 7 + Н 2 SО 4 + 5 Н 2 О Na 2 SO 4 + 4 Н 3 ВО 3 Ø Описание. Бесцветные блестящие чешуйчатые Описание. кристаллы, жирные на ощупь (водородные связи образуют слоистую структуру) или мелкий белый кристаллический порошок без запаха (вид Н 3 ВО 3 зависит от технологии получения). Ø В холодной воде растворима (1: 25), легко растворима в горячей воде(1: 4). Растворима в спирте (1: 25) (1: 16 – BP), легко растворима в глицерине (1: 7) (1: 4 – BP). 34
Кислота борная Acidum boricum Н 3 ВО 3 М. м. 61. 8 Ø Получение. Из буры (Na 2 B 4 O 7. 10 H 2 O - Natrii tetraboras). Горячий раствор тетрабората натрия обрабатывают минеральной кислотой, затем раствор охлаждают, а выделившиеся кристаллы борной кислоты перекристаллизовывают из воды: Na 2 B 4 O 7 + Н 2 SО 4 + 5 Н 2 О Na 2 SO 4 + 4 Н 3 ВО 3 Ø Описание. Бесцветные блестящие чешуйчатые Описание. кристаллы, жирные на ощупь (водородные связи образуют слоистую структуру) или мелкий белый кристаллический порошок без запаха (вид Н 3 ВО 3 зависит от технологии получения). Ø В холодной воде растворима (1: 25), легко растворима в горячей воде(1: 4). Растворима в спирте (1: 25) (1: 16 – BP), легко растворима в глицерине (1: 7) (1: 4 – BP). 34
 Ø При длительном нагревании до 100°С борная кислота теряет часть воды и переходит в метаборную кислоту. При более сильном нагревании борная кислота превращается в тетраборную кислоту Н 2 B 4 О 7 и, наконец, пройдя стадию стекловидной сплавленной массы, теряет всю воду и превращается в борный ангидрид (оксид бора В 2 О 3). - Н 2 О Н 3 ВО 3 → НВО 2 → Н 2 B 4 О 7 → 2 В 2 О 3 При растворении в воде все эти соединения снова переходят в борную кислоту 35
Ø При длительном нагревании до 100°С борная кислота теряет часть воды и переходит в метаборную кислоту. При более сильном нагревании борная кислота превращается в тетраборную кислоту Н 2 B 4 О 7 и, наконец, пройдя стадию стекловидной сплавленной массы, теряет всю воду и превращается в борный ангидрид (оксид бора В 2 О 3). - Н 2 О Н 3 ВО 3 → НВО 2 → Н 2 B 4 О 7 → 2 В 2 О 3 При растворении в воде все эти соединения снова переходят в борную кислоту 35
 Ø Борная кислота – относится к очень слабым, трехосновным кислотам Ø Константы ионизации равны: Ка 1 = 5, 8 10 -10, Ка 2 = 2 10– 13, Ка 3 = 2 10 – 14. Прочных солей борная кислота не образует (Тетраборат натрия является солью тетраборной кислоты). Ø Растворы борной кислоты имеют р. Н от 3. 8 до 4. 8 (слабо-кислая). В отличие от других кислот протолитические свойства борной кислоты связаны не с отщеплением протона, а присоединением гидроксид- ионов: Н 3 ВО 3 + Н 2 О [B(OH)4]- + H+ 36
Ø Борная кислота – относится к очень слабым, трехосновным кислотам Ø Константы ионизации равны: Ка 1 = 5, 8 10 -10, Ка 2 = 2 10– 13, Ка 3 = 2 10 – 14. Прочных солей борная кислота не образует (Тетраборат натрия является солью тетраборной кислоты). Ø Растворы борной кислоты имеют р. Н от 3. 8 до 4. 8 (слабо-кислая). В отличие от других кислот протолитические свойства борной кислоты связаны не с отщеплением протона, а присоединением гидроксид- ионов: Н 3 ВО 3 + Н 2 О [B(OH)4]- + H+ 36
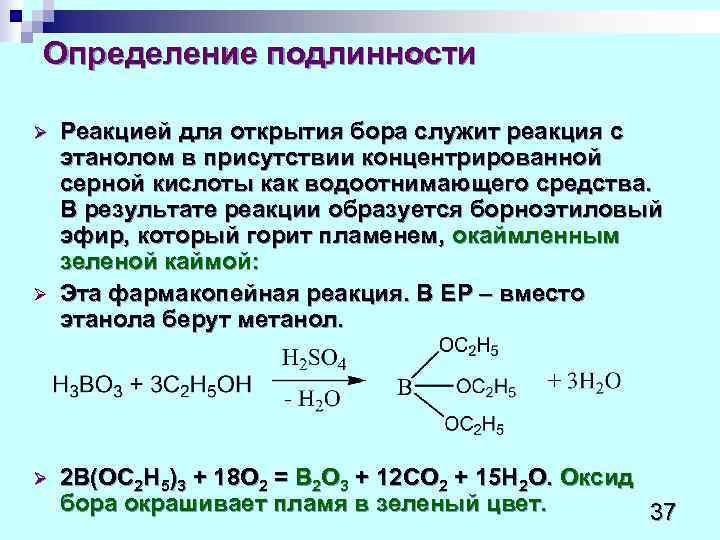
 Определение подлинности Ø Реакцией для открытия бора служит реакция с этанолом в присутствии концентрированной серной кислоты как водоотнимающего средства. В результате реакции образуется борноэтиловый эфир, который горит пламенем, окаймленным зеленой каймой: Ø Эта фармакопейная реакция. В ЕP – вместо этанола берут метанол. Ø 2 В(ОС 2 Н 5)3 + 18 О 2 = В 2 О 3 + 12 СО 2 + 15 Н 2 О. Оксид бора окрашивает пламя в зеленый цвет. 37
Определение подлинности Ø Реакцией для открытия бора служит реакция с этанолом в присутствии концентрированной серной кислоты как водоотнимающего средства. В результате реакции образуется борноэтиловый эфир, который горит пламенем, окаймленным зеленой каймой: Ø Эта фармакопейная реакция. В ЕP – вместо этанола берут метанол. Ø 2 В(ОС 2 Н 5)3 + 18 О 2 = В 2 О 3 + 12 СО 2 + 15 Н 2 О. Оксид бора окрашивает пламя в зеленый цвет. 37
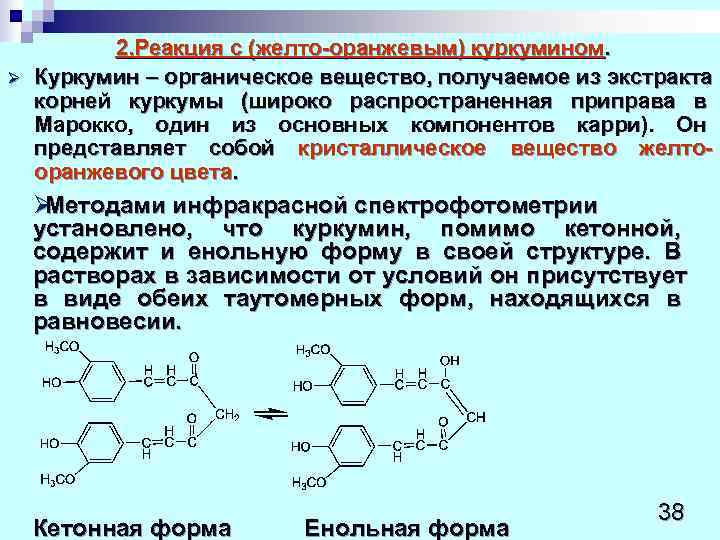
 2. Реакция с (желто-оранжевым) куркумином. Ø Куркумин – органическое вещество, получаемое из экстракта корней куркумы (широко распространенная приправа в Марокко, один из основных компонентов карри). Он представляет собой кристаллическое вещество желто- оранжевого цвета. ØМетодами инфракрасной спектрофотометрии установлено, что куркумин, помимо кетонной, содержит и енольную форму в своей структуре. В растворах в зависимости от условий он присутствует в виде обеих таутомерных форм, находящихся в равновесии. 38 Кетонная форма Енольная форма
2. Реакция с (желто-оранжевым) куркумином. Ø Куркумин – органическое вещество, получаемое из экстракта корней куркумы (широко распространенная приправа в Марокко, один из основных компонентов карри). Он представляет собой кристаллическое вещество желто- оранжевого цвета. ØМетодами инфракрасной спектрофотометрии установлено, что куркумин, помимо кетонной, содержит и енольную форму в своей структуре. В растворах в зависимости от условий он присутствует в виде обеих таутомерных форм, находящихся в равновесии. 38 Кетонная форма Енольная форма
 Ø Для реакции применяется куркумовая бумага: фильтровальная бумага, пропитанную спиртовой настойкой куркумина, а затем высушенная в помещении, не содержащем паров кислот и аммиака. Ø Исследуемый раствор борной кислоты (1: 50) наносят на куркумовую бумагу, одновременно добавляют несколько капель хлороводородной кислоты. Ø При высушивании, в зависимости от концентрации борной кислоты, появляется розовый или буровато- красный цвет. Это образуется розоцианин. цвет. Это образуется Ø Если бумагу смочить раствором аммиака, окраска переходит в зеленовато-черную , а при очень разбавленных растворах – фиолетовую
Ø Для реакции применяется куркумовая бумага: фильтровальная бумага, пропитанную спиртовой настойкой куркумина, а затем высушенная в помещении, не содержащем паров кислот и аммиака. Ø Исследуемый раствор борной кислоты (1: 50) наносят на куркумовую бумагу, одновременно добавляют несколько капель хлороводородной кислоты. Ø При высушивании, в зависимости от концентрации борной кислоты, появляется розовый или буровато- красный цвет. Это образуется розоцианин. цвет. Это образуется Ø Если бумагу смочить раствором аммиака, окраска переходит в зеленовато-черную , а при очень разбавленных растворах – фиолетовую
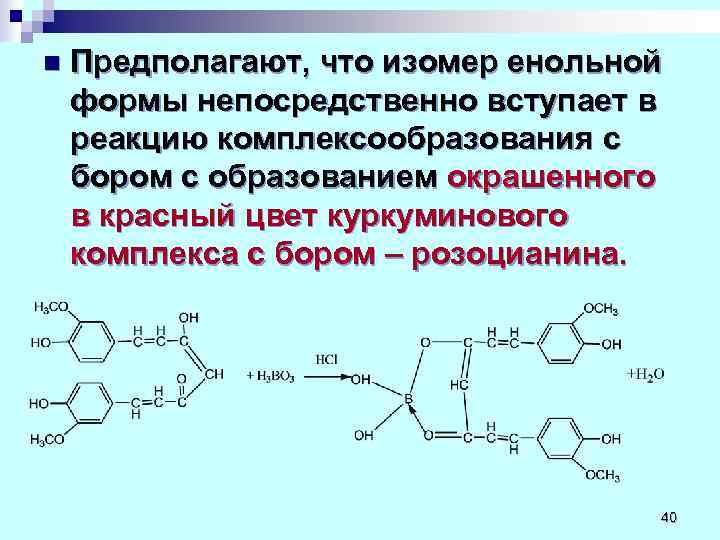
 n Предполагают, что изомер енольной формы непосредственно вступает в реакцию комплексообразования с бором с образованием окрашенного в красный цвет куркуминового комплекса с бором – розоцианина. 40
n Предполагают, что изомер енольной формы непосредственно вступает в реакцию комплексообразования с бором с образованием окрашенного в красный цвет куркуминового комплекса с бором – розоцианина. 40
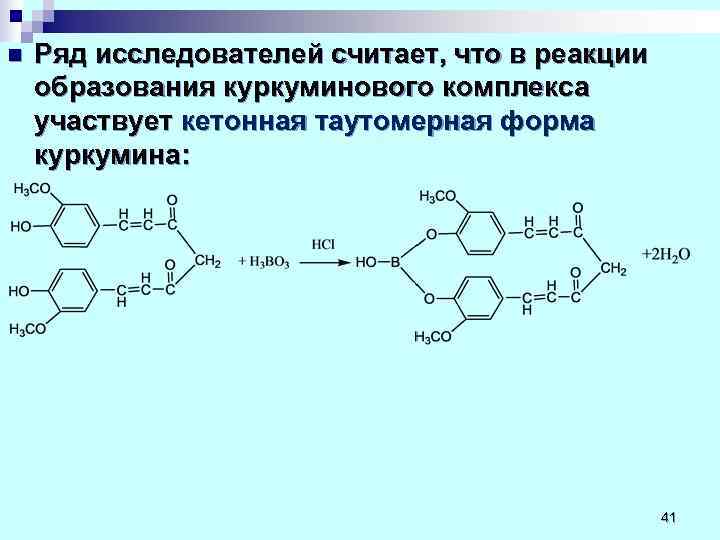
 n Ряд исследователей считает, что в реакции образования куркуминового комплекса участвует кетонная таутомерная форма куркумина: 41
n Ряд исследователей считает, что в реакции образования куркуминового комплекса участвует кетонная таутомерная форма куркумина: 41
 Определению бора с куркумином мешают: Ø железо, Ø молибден, Ø вольфрам, Ø берилий, Ø висмут, Ø мышьяк и ряд других элементов, которые в тех же условиях реагируют с куркумином с образованием окрашенных комплексов. Кроме того, этой реакции мешают и окислители, окисляющие куркумин. 42
Определению бора с куркумином мешают: Ø железо, Ø молибден, Ø вольфрам, Ø берилий, Ø висмут, Ø мышьяк и ряд других элементов, которые в тех же условиях реагируют с куркумином с образованием окрашенных комплексов. Кроме того, этой реакции мешают и окислители, окисляющие куркумин. 42
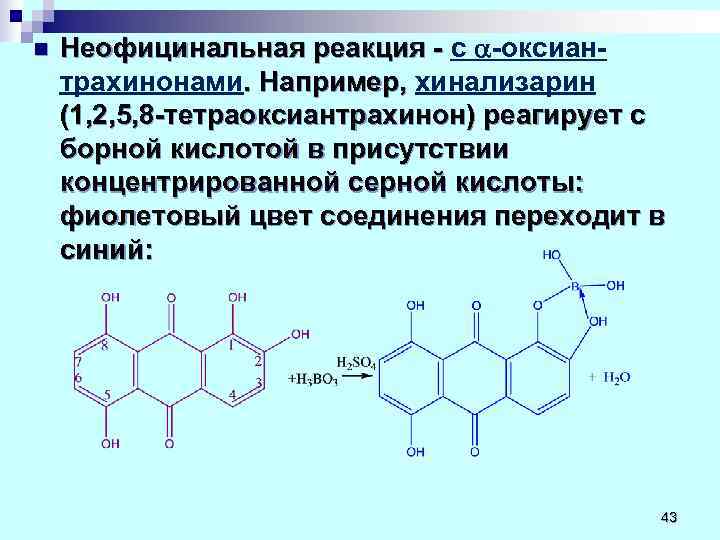
 n Неофицинальная реакция - с -оксиан- Неофицинальная реакция - трахинонами. Например, хинализарин . Например, (1, 2, 5, 8 -тетраоксиантрахинон) реагирует с 1, 2, 5, 8 -тетраоксиантрахинон) борной кислотой в присутствии концентрированной серной кислоты: фиолетовый цвет соединения переходит в синий: 43
n Неофицинальная реакция - с -оксиан- Неофицинальная реакция - трахинонами. Например, хинализарин . Например, (1, 2, 5, 8 -тетраоксиантрахинон) реагирует с 1, 2, 5, 8 -тетраоксиантрахинон) борной кислотой в присутствии концентрированной серной кислоты: фиолетовый цвет соединения переходит в синий: 43
 Ø Е P помимо реакции с метанолом, включает тест на кислоту с индикаторами метиловым красным (оранжевая или красная окраска) или бромтимоловым голубым (желтая окраска). Методика определения: 3, 3% раствор борной кислоты, объемом 100 мл, должен иметь кислую реакцию. Ø Эта процедура необходима для отличия борной кислоты от другого препарата бора – буры: водный раствор буры имеет щелочную реакцию. 44
Ø Е P помимо реакции с метанолом, включает тест на кислоту с индикаторами метиловым красным (оранжевая или красная окраска) или бромтимоловым голубым (желтая окраска). Методика определения: 3, 3% раствор борной кислоты, объемом 100 мл, должен иметь кислую реакцию. Ø Эта процедура необходима для отличия борной кислоты от другого препарата бора – буры: водный раствор буры имеет щелочную реакцию. 44
 Оценка чистоты Ø ГФ: Недопустимыми примесями в препарате являются минеральные кислоты. К 10 г препарата добавляют 50 мл воды, отфильтровывают выделившуюся борную кислоту, 1 мл фильтрата разводят в 10 мл воды, прибавлют к раствору препарата 1 капли метилового оранжевого. Раствор не должен окрашиваться в розовый или оранжевый цвет (интервал перехода окраски индикатора – р. Н 3, 1 -4, 0). ЕР: р. Н = 3. 8 - 4. 8 Ø ЕР: Борная кислота должна полностью растворяться в горячей воде: 3, 3 г растворяют в 80 мл кипящей в горячей воде: воды, охлаждают и доводят до 100 мл – раствор прозрачный и бесцветный Ø ЕР: В спирте: раствор, 1 г чистой борной кислоты в 10 мл кипящего спирта, должен быть бесцветным и его опалесценция не должна превышать опалесценцию эталонного раствора II. 45
Оценка чистоты Ø ГФ: Недопустимыми примесями в препарате являются минеральные кислоты. К 10 г препарата добавляют 50 мл воды, отфильтровывают выделившуюся борную кислоту, 1 мл фильтрата разводят в 10 мл воды, прибавлют к раствору препарата 1 капли метилового оранжевого. Раствор не должен окрашиваться в розовый или оранжевый цвет (интервал перехода окраски индикатора – р. Н 3, 1 -4, 0). ЕР: р. Н = 3. 8 - 4. 8 Ø ЕР: Борная кислота должна полностью растворяться в горячей воде: 3, 3 г растворяют в 80 мл кипящей в горячей воде: воды, охлаждают и доводят до 100 мл – раствор прозрачный и бесцветный Ø ЕР: В спирте: раствор, 1 г чистой борной кислоты в 10 мл кипящего спирта, должен быть бесцветным и его опалесценция не должна превышать опалесценцию эталонного раствора II. 45
 Ø ЕР: Недопустимые примеси: Органические вещества обнаруживают при постепенном нагревании: не должно происходить потемнения препарата до слабого покраснения. Ø ЕР: Сульфаты. 450 мкг/мл (ррm). Ø ЕР: Тяжелые металлы. 15 мкг/мл (ррm). 46
Ø ЕР: Недопустимые примеси: Органические вещества обнаруживают при постепенном нагревании: не должно происходить потемнения препарата до слабого покраснения. Ø ЕР: Сульфаты. 450 мкг/мл (ррm). Ø ЕР: Тяжелые металлы. 15 мкг/мл (ррm). 46
 Количественное определение Метод нейтрализации. Титрование щелочью комплексных соединений борной кислоты с многоатомными спиртами или сахарами. (борная кислота - очень слабая (р. Ка 1 = 9, 24), поэтому прямое титрование ее щелочью невозможно). Ø точка эквивалентности при титровании щелочью находится в области значений р. Н, где трудно подобрать индикатор с заметным переходом окраски. Ø при действии щелочей на борную кислоту образуются соли не ортоборной кислоты Н 3 ВО 3, а тетрабораты и метаборной НВО 2 кислоты. При титровании борной кислоты щелочью, образующаяся соль метаборной кислоты гидролизуется: 2 Na. BO 2 + 4 Н 2 О 2 Н 3 ВО 3 + 2 Na. OH Ø В результате гидролиза щелочная реакция раствора достигается значительно ранее достижения эквивалентной точки. 47
Количественное определение Метод нейтрализации. Титрование щелочью комплексных соединений борной кислоты с многоатомными спиртами или сахарами. (борная кислота - очень слабая (р. Ка 1 = 9, 24), поэтому прямое титрование ее щелочью невозможно). Ø точка эквивалентности при титровании щелочью находится в области значений р. Н, где трудно подобрать индикатор с заметным переходом окраски. Ø при действии щелочей на борную кислоту образуются соли не ортоборной кислоты Н 3 ВО 3, а тетрабораты и метаборной НВО 2 кислоты. При титровании борной кислоты щелочью, образующаяся соль метаборной кислоты гидролизуется: 2 Na. BO 2 + 4 Н 2 О 2 Н 3 ВО 3 + 2 Na. OH Ø В результате гидролиза щелочная реакция раствора достигается значительно ранее достижения эквивалентной точки. 47
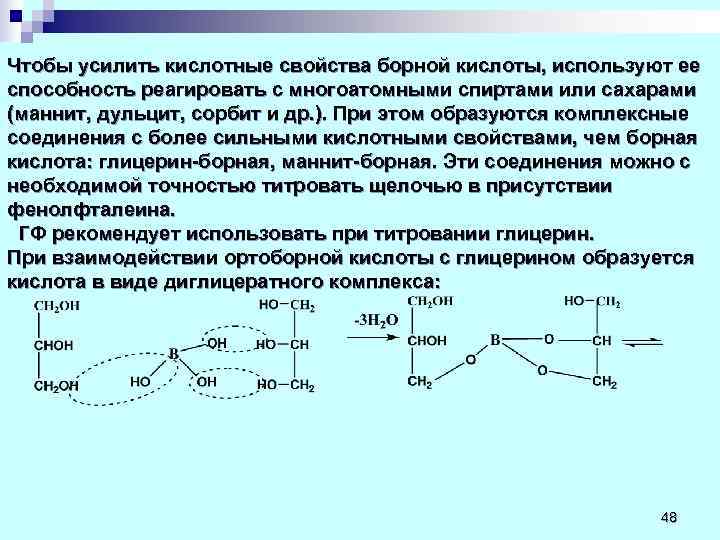
 Чтобы усилить кислотные свойства борной кислоты, используют ее способность реагировать с многоатомными спиртами или сахарами (маннит, дульцит, сорбит и др. ). При этом образуются комплексные соединения с более сильными кислотными свойствами, чем борная кислота: глицерин-борная, маннит-борная. Эти соединения можно с необходимой точностью титровать щелочью в присутствии фенолфталеина. ГФ рекомендует использовать при титровании глицерин. При взаимодействии ортоборной кислоты с глицерином образуется кислота в виде диглицератного комплекса: 48
Чтобы усилить кислотные свойства борной кислоты, используют ее способность реагировать с многоатомными спиртами или сахарами (маннит, дульцит, сорбит и др. ). При этом образуются комплексные соединения с более сильными кислотными свойствами, чем борная кислота: глицерин-борная, маннит-борная. Эти соединения можно с необходимой точностью титровать щелочью в присутствии фенолфталеина. ГФ рекомендует использовать при титровании глицерин. При взаимодействии ортоборной кислоты с глицерином образуется кислота в виде диглицератного комплекса: 48
 Условия 1. Глицерин предварительно необходимо нейтрализовать щелочью по фенолфталеину, так как он имеет слабокислую реакцию среды, поскольку является многоатомным спиртом. 2. Чтобы избежать распада образующейся комплексной кислоты и сместить равновесие вправо, в конце титрования в реакционную смесь добавляют порцию глицерина. 3. В конце титрования, при добавлении в реакционную смесь порции глицерина, розовая окраска фенолфталеина не должна исчезнуть. Исчезновение окраски свидетельствует о смещении равновесия влево (гидролиз диглицерата бора). В этом случае необходимо добавить новую порцию глицерина и продолжить титрование. 4. Вода для растворения навески борной кислоты и раствор гидроксида натрия не должны содержать СО 2 (прокипятить). Угольная кислота, как более сильная кислота может вытеснять борную кислоту из ее солей. 5. Борную кислоту следует титровать при комнатной температуре, так как при температуре выше 50°С комплекс борной кислоты с глицерином начинает разрушаться. 6. Точку эквивалентности можно определить потенциометрически. 50
Условия 1. Глицерин предварительно необходимо нейтрализовать щелочью по фенолфталеину, так как он имеет слабокислую реакцию среды, поскольку является многоатомным спиртом. 2. Чтобы избежать распада образующейся комплексной кислоты и сместить равновесие вправо, в конце титрования в реакционную смесь добавляют порцию глицерина. 3. В конце титрования, при добавлении в реакционную смесь порции глицерина, розовая окраска фенолфталеина не должна исчезнуть. Исчезновение окраски свидетельствует о смещении равновесия влево (гидролиз диглицерата бора). В этом случае необходимо добавить новую порцию глицерина и продолжить титрование. 4. Вода для растворения навески борной кислоты и раствор гидроксида натрия не должны содержать СО 2 (прокипятить). Угольная кислота, как более сильная кислота может вытеснять борную кислоту из ее солей. 5. Борную кислоту следует титровать при комнатной температуре, так как при температуре выше 50°С комплекс борной кислоты с глицерином начинает разрушаться. 6. Точку эквивалентности можно определить потенциометрически. 50
 ПРИМЕНЕНИЕ: Антисептическое средство. Ø При местном применении (в виде 5 % мази) оказывает антипедикулезное действие. Ø Ранее использовалась в качестве антисептического средства у взрослых и детей. В связи с выявленными побочными явлениями, внесены ограничения к ее применению. Ø Применяют в виде 2 % водного раствора для промывания конъюнктивального мешка при конъюнктивитах; Ø 3 % растворы - для примочек при мокнущей экземе, дерматитах. Ø Спиртовыми растворы 0, 5 %, 1 %, 2 % и 3 % - в виде капель с при остром и хроническом отите Ø 10 % раствор в глицерине применяют для смазывания пораженных участков кожи при опрелостях, кольпитах. 51
ПРИМЕНЕНИЕ: Антисептическое средство. Ø При местном применении (в виде 5 % мази) оказывает антипедикулезное действие. Ø Ранее использовалась в качестве антисептического средства у взрослых и детей. В связи с выявленными побочными явлениями, внесены ограничения к ее применению. Ø Применяют в виде 2 % водного раствора для промывания конъюнктивального мешка при конъюнктивитах; Ø 3 % растворы - для примочек при мокнущей экземе, дерматитах. Ø Спиртовыми растворы 0, 5 %, 1 %, 2 % и 3 % - в виде капель с при остром и хроническом отите Ø 10 % раствор в глицерине применяют для смазывания пораженных участков кожи при опрелостях, кольпитах. 51
 Борная кислота входит в состав ЛС: 1. Линимент борно-цинковый (Linimentum Boro-zincatum). 2. Паста борно-цинко-нафталанная 3. Паста Теймурова (Pasta Teimurovi). 4. Мазь борная (Unguentum Acidi borici 5%) 5. Мазь солидоловая (по прописи Н. Ф. Рыбакова) (Unguentum Solidoli). Обладает кератолитическим эффектом. Применяют для лечения псориаза. Хранение: в прохладном, защищенном от света месте. 52
Борная кислота входит в состав ЛС: 1. Линимент борно-цинковый (Linimentum Boro-zincatum). 2. Паста борно-цинко-нафталанная 3. Паста Теймурова (Pasta Teimurovi). 4. Мазь борная (Unguentum Acidi borici 5%) 5. Мазь солидоловая (по прописи Н. Ф. Рыбакова) (Unguentum Solidoli). Обладает кератолитическим эффектом. Применяют для лечения псориаза. Хранение: в прохладном, защищенном от света месте. 52
 Натрия тетраборат Natrii tetraboras Бура Borax Na 2 B 4 O 7. 10 Н 2 О М. м. 381, 4 Ø В свободном состоянии тетраборат натрия в природе встречается в виде минерала тинкала (в кристаллах которого атомы бора и кислорода чередуются, образуя цепь, содержащую 4 атома бора). Ø Получение ¨ Для медицинских целей буру чаще всего получают из борокальцитов или борной кислоты при действии водного горячего раствора карбоната натрия: Са. В 4 О 7 + Na 2 CO 3 Ca. CO 3 + Na 2 B 4 O 7 4 Н 3 ВО 3 + Na 2 CO 3 Na 2 B 4 O 7 + CO 2 + 6 Н 2 О ¨ Образующийся кристаллогидрат Na 2 B 4 O 7. 10 Н 2 О при прокаливании теряет всю воду и превращается в безводную соль. 53.
Натрия тетраборат Natrii tetraboras Бура Borax Na 2 B 4 O 7. 10 Н 2 О М. м. 381, 4 Ø В свободном состоянии тетраборат натрия в природе встречается в виде минерала тинкала (в кристаллах которого атомы бора и кислорода чередуются, образуя цепь, содержащую 4 атома бора). Ø Получение ¨ Для медицинских целей буру чаще всего получают из борокальцитов или борной кислоты при действии водного горячего раствора карбоната натрия: Са. В 4 О 7 + Na 2 CO 3 Ca. CO 3 + Na 2 B 4 O 7 4 Н 3 ВО 3 + Na 2 CO 3 Na 2 B 4 O 7 + CO 2 + 6 Н 2 О ¨ Образующийся кристаллогидрат Na 2 B 4 O 7. 10 Н 2 О при прокаливании теряет всю воду и превращается в безводную соль. 53.
 Ø Описание. v Бесцветные, прозрачные, легко выветривающиеся кристаллы или белый кристаллический порошок. v Бура растворима в воде (1: 20), v Очень легко растворима в горячей воде (1: 0, 6). v Легко растворяется в глицерине (1: 1), v Очень мало растворима в спирте (1: 2000) 54
Ø Описание. v Бесцветные, прозрачные, легко выветривающиеся кристаллы или белый кристаллический порошок. v Бура растворима в воде (1: 20), v Очень легко растворима в горячей воде (1: 0, 6). v Легко растворяется в глицерине (1: 1), v Очень мало растворима в спирте (1: 2000) 54
 Определение подлинности Ø ГФ: Бура вступает во все реакции, характерные для борной кислоты. В присутствии концентрированной серной кислоты образует эфиры с метанолом, этанолом, глицерином, фенолами. Образующиеся эфиры, сгорая, окрашивают пламя в зеленый цвет. Ø ЕР: с метанолом Na 2 B 4 О 7 + H 2 SO 4 + 5 H 2 O 4 Н 3 ВО 3 + 2 Na 2 SO 4 Ø(ГФ) Образование розоцианинов с куркумином. Ø(ГФ, ЕР) Реакции на ион натрия. 55
Определение подлинности Ø ГФ: Бура вступает во все реакции, характерные для борной кислоты. В присутствии концентрированной серной кислоты образует эфиры с метанолом, этанолом, глицерином, фенолами. Образующиеся эфиры, сгорая, окрашивают пламя в зеленый цвет. Ø ЕР: с метанолом Na 2 B 4 О 7 + H 2 SO 4 + 5 H 2 O 4 Н 3 ВО 3 + 2 Na 2 SO 4 Ø(ГФ) Образование розоцианинов с куркумином. Ø(ГФ, ЕР) Реакции на ион натрия. 55
 n ЕР : (р. Н среды от 9, 0 до 9, 6) n ГФ: водный раствор буры (отличие от борной кислоты) имеет щелочную реакцию вследствие гидролиза буры с образованием натрия метабората и дальнейшего гидролиза последнего. При прибавлении фенолфталеина, раствор окрашивается в красно-фиолетовый цвет. 2 Na 2 В 4 О 7 + 6 Н 2 О 4 Н 3 ВО 3 + 4 Na. ВО 2 Na. ВО 2 + 2 НОН Н 3 ВО 3 + Na. ОН (реакция среды – щелочная по фенолфталеину) n При добавлении глицерина (85%), окраска исчезает, поскольку образующийся глицератный комплекс борной кислоты, представляет собой кислоту: Соляная кислота вытесняет из горячего раствора буры борную кислоту, которая при охлаждении раствора выпадает в осадок: 56 Na 2 B 4 О 7 + 5 H 2 O+2 HCl 4 Н 3 ВО 3 + 2 Na. Cl
n ЕР : (р. Н среды от 9, 0 до 9, 6) n ГФ: водный раствор буры (отличие от борной кислоты) имеет щелочную реакцию вследствие гидролиза буры с образованием натрия метабората и дальнейшего гидролиза последнего. При прибавлении фенолфталеина, раствор окрашивается в красно-фиолетовый цвет. 2 Na 2 В 4 О 7 + 6 Н 2 О 4 Н 3 ВО 3 + 4 Na. ВО 2 Na. ВО 2 + 2 НОН Н 3 ВО 3 + Na. ОН (реакция среды – щелочная по фенолфталеину) n При добавлении глицерина (85%), окраска исчезает, поскольку образующийся глицератный комплекс борной кислоты, представляет собой кислоту: Соляная кислота вытесняет из горячего раствора буры борную кислоту, которая при охлаждении раствора выпадает в осадок: 56 Na 2 B 4 О 7 + 5 H 2 O+2 HCl 4 Н 3 ВО 3 + 2 Na. Cl
 Ø Оценка чистоты Ø Недопустимой примесью по ГФ являются карбонаты. Определяются по выделению диоксида углерода прибавлении к раствору препарата (1: 50) хлороводородной кислоты. Ø Количественное определение Проводят методом нейтрализации. Ø ГФ: Титрант - хлороводородная кислота. Ø Индикатор - метиловый оранжевый (титруют до розовато-оранжевого окрашивания). Na 2 B 4 O 7 + 2 HCI + 5 H 2 O 4 B(OH)3 + 2 Na. CI (М 1/ z = ½ ) Индикатор изменяет окраску от избыточной капли хлороводородной кислоты. Ø ЕР при количественном определении буры, как и в случае борной кислоты, использует образование комплексной кислоты с маннитолом и последующее ее титрование раствором щелочи в присутствии 57 фенолфталеина.
Ø Оценка чистоты Ø Недопустимой примесью по ГФ являются карбонаты. Определяются по выделению диоксида углерода прибавлении к раствору препарата (1: 50) хлороводородной кислоты. Ø Количественное определение Проводят методом нейтрализации. Ø ГФ: Титрант - хлороводородная кислота. Ø Индикатор - метиловый оранжевый (титруют до розовато-оранжевого окрашивания). Na 2 B 4 O 7 + 2 HCI + 5 H 2 O 4 B(OH)3 + 2 Na. CI (М 1/ z = ½ ) Индикатор изменяет окраску от избыточной капли хлороводородной кислоты. Ø ЕР при количественном определении буры, как и в случае борной кислоты, использует образование комплексной кислоты с маннитолом и последующее ее титрование раствором щелочи в присутствии 57 фенолфталеина.
 Ø ГФ регламентирует содержание буры в ГФ регламентирует препарате не менее 99, 5 % (ВР - 99. 0 %) и не более 103, 0 %. Допустимое увеличение содержания основного вещества выше 100% связано с возможной потерей кристаллизационной воды. Ø Применение. Бура применяется как антисептик в виде 1 -2% растворов для полосканий, промываний, ингаляций при воспалительных процессах верхних дыхательных путей. Ø Хранить препарат следует в хорошо закупоренных банках в прохладном месте, чтобы исключить потерю (выветривание) воды. 58
Ø ГФ регламентирует содержание буры в ГФ регламентирует препарате не менее 99, 5 % (ВР - 99. 0 %) и не более 103, 0 %. Допустимое увеличение содержания основного вещества выше 100% связано с возможной потерей кристаллизационной воды. Ø Применение. Бура применяется как антисептик в виде 1 -2% растворов для полосканий, промываний, ингаляций при воспалительных процессах верхних дыхательных путей. Ø Хранить препарат следует в хорошо закупоренных банках в прохладном месте, чтобы исключить потерю (выветривание) воды. 58
 Ø Алюминий – Мягкий лёгкий металл серебристо-белого цвета. Микроэлемент, содержание в организме не превышает 50 мг. Суточное потребление алюминия человеком составляет 5 -50 мг. В желудочно-кишечном тракте человека всасывается 2 - 4% поступившего алюминия, причем лучше усваиваются растворимые соли, такие как Al. Cl 3. Ø Растительные продукты содержат в 50 -100 раз больше алюминия, чем продукты животного происхождения. Ø При горячей обработке пищевых продуктов или выпечке хлеба, за счет использования алюминиевой посуды, происходит загрязнение пищи алюминием. Ø Питьевая вода: содержание алюминия составляет 2 -4 мг/л. 59
Ø Алюминий – Мягкий лёгкий металл серебристо-белого цвета. Микроэлемент, содержание в организме не превышает 50 мг. Суточное потребление алюминия человеком составляет 5 -50 мг. В желудочно-кишечном тракте человека всасывается 2 - 4% поступившего алюминия, причем лучше усваиваются растворимые соли, такие как Al. Cl 3. Ø Растительные продукты содержат в 50 -100 раз больше алюминия, чем продукты животного происхождения. Ø При горячей обработке пищевых продуктов или выпечке хлеба, за счет использования алюминиевой посуды, происходит загрязнение пищи алюминием. Ø Питьевая вода: содержание алюминия составляет 2 -4 мг/л. 59
 Источники, которые могут содержать излишки алюминия: Ø чай, Ø морковь, Ø некоторые травы Ø плавленые сыры, Ø лекарственные вещества, Ø антациды, Ø дезодоранты, Ø бумажные полотенца, Ø продукты, контактирующие с алюминиевой фольгой.
Источники, которые могут содержать излишки алюминия: Ø чай, Ø морковь, Ø некоторые травы Ø плавленые сыры, Ø лекарственные вещества, Ø антациды, Ø дезодоранты, Ø бумажные полотенца, Ø продукты, контактирующие с алюминиевой фольгой.
 Ø Алюминий влияет на ферментативные процессы. Предполагают, что он замещает ионы магния и кальция в активных центрах, так как ионные радиусы и энергии ионизации этих атомов близки по значениям. Ø Отличается незначительным токсическим действием, но многие растворимые в воде неорганические соединения алюминия сохраняются в растворённом состоянии длительное время и могут оказывать вредное воздействие на человека и теплокровных животных через питьевую воду. Ø Действует на нервную систему (накапливается в нервной ткани, приводя к тяжёлым расстройствам функции ЦНС). 61
Ø Алюминий влияет на ферментативные процессы. Предполагают, что он замещает ионы магния и кальция в активных центрах, так как ионные радиусы и энергии ионизации этих атомов близки по значениям. Ø Отличается незначительным токсическим действием, но многие растворимые в воде неорганические соединения алюминия сохраняются в растворённом состоянии длительное время и могут оказывать вредное воздействие на человека и теплокровных животных через питьевую воду. Ø Действует на нервную систему (накапливается в нервной ткани, приводя к тяжёлым расстройствам функции ЦНС). 61
 Алюминий и его соединения Алюминия гидроксид Alumini hydroxydum Al(OH)3. Ø Получение Осаждение из горячего раствора сульфата алюминия 10% раствором аммиака. Al 2(SO 4)3 + 6 NH 3. Н 2 O 2 Al(OH)3 + 3(NH 4)2 SO 4 После отделения раствора, осадок промывают горячей водой до полного удаления сульфат-ионов и высушивают, вначале при температуре 400, а затем - при 1000 С. Ø Описание Аморфный рыхлый белый порошок, в воде практически нерастворим, в воде образует гель. Растворим при нагревании в разбавленных кислотах и растворах едких щелочей, т. е. гидроксид алюминия является амфотерным соединением: Al(OH)3 + 3 HCI AICI 3 + 3 H 2 O Al(OH)3 + Na. OH Na[AI(OH)4] 62
Алюминий и его соединения Алюминия гидроксид Alumini hydroxydum Al(OH)3. Ø Получение Осаждение из горячего раствора сульфата алюминия 10% раствором аммиака. Al 2(SO 4)3 + 6 NH 3. Н 2 O 2 Al(OH)3 + 3(NH 4)2 SO 4 После отделения раствора, осадок промывают горячей водой до полного удаления сульфат-ионов и высушивают, вначале при температуре 400, а затем - при 1000 С. Ø Описание Аморфный рыхлый белый порошок, в воде практически нерастворим, в воде образует гель. Растворим при нагревании в разбавленных кислотах и растворах едких щелочей, т. е. гидроксид алюминия является амфотерным соединением: Al(OH)3 + 3 HCI AICI 3 + 3 H 2 O Al(OH)3 + Na. OH Na[AI(OH)4] 62
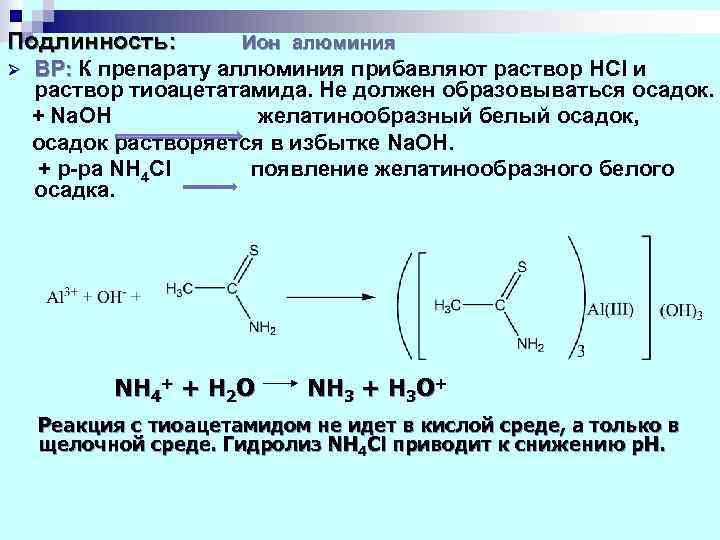
 Подлинность: Ион алюминия Ø ВР: К препарату аллюминия прибавляют раствор HCl и ВР: раствор тиоацетатамида. Не должен образовываться осадок. + Na. OH желатинообразный белый осадок, осадок растворяется в избытке Na. OH. + р-ра NH 4 Cl появление желатинообразного белого осадка. NH 4+ + H 2 O NH 3 + H 3 O+ Реакция с тиоацетамидом не идет в кислой среде, а только в щелочной среде. Гидролиз NH 4 Cl приводит к снижению p. H.
Подлинность: Ион алюминия Ø ВР: К препарату аллюминия прибавляют раствор HCl и ВР: раствор тиоацетатамида. Не должен образовываться осадок. + Na. OH желатинообразный белый осадок, осадок растворяется в избытке Na. OH. + р-ра NH 4 Cl появление желатинообразного белого осадка. NH 4+ + H 2 O NH 3 + H 3 O+ Реакция с тиоацетамидом не идет в кислой среде, а только в щелочной среде. Гидролиз NH 4 Cl приводит к снижению p. H.
 Ø ГФ: При прокаливании препарата, предварительно смоченного раствором нитрата кобальта, образуется плав, окрашенный в синий цвет, вследствие образования алюмината кобальта Сo(Al. O 2)2 - тенарова синь: 2 Al(OH)3 Al 2 O 3 + 3 H 2 O 2 Co(NO 3)2 2 Co. O + 4 NO 2 + O 2 Al 2 O 3 + Co. O Co(Al. O 2)2 Неофицинальные реакции: Ø 1. Гидроксид алюминия растворяют при нагревании в растворе Na. OH. К прозрачному р-ру добавляют NH 4 Cl. Образуется белый студенистый осадок Al(OH)3 (при добавлении к щелочному раствору гидроксида алюминия хлорида аммония, р. Н раствора понижается и гидроксид алюминия выпадет в осадок). Al(OH)3 + Na. OH Na[AI(OH)4] 2[Al(OH)4 ] - + NH 4+ Al 2 O 3. H 2 О + NH 3 Ø комлпесообразования с ализарином образуется ализаринат алюминия красного цвета; Ø с 8 -оксихинолином образуется белое комплексное соединение, выпадающее в осадок Ø с алюминоном образуется соединение в виде красного осадка.
Ø ГФ: При прокаливании препарата, предварительно смоченного раствором нитрата кобальта, образуется плав, окрашенный в синий цвет, вследствие образования алюмината кобальта Сo(Al. O 2)2 - тенарова синь: 2 Al(OH)3 Al 2 O 3 + 3 H 2 O 2 Co(NO 3)2 2 Co. O + 4 NO 2 + O 2 Al 2 O 3 + Co. O Co(Al. O 2)2 Неофицинальные реакции: Ø 1. Гидроксид алюминия растворяют при нагревании в растворе Na. OH. К прозрачному р-ру добавляют NH 4 Cl. Образуется белый студенистый осадок Al(OH)3 (при добавлении к щелочному раствору гидроксида алюминия хлорида аммония, р. Н раствора понижается и гидроксид алюминия выпадет в осадок). Al(OH)3 + Na. OH Na[AI(OH)4] 2[Al(OH)4 ] - + NH 4+ Al 2 O 3. H 2 О + NH 3 Ø комлпесообразования с ализарином образуется ализаринат алюминия красного цвета; Ø с 8 -оксихинолином образуется белое комплексное соединение, выпадающее в осадок Ø с алюминоном образуется соединение в виде красного осадка.
 Оценка чистоты Ø ГФ: Допустимые примеси: карбонаты хлориды, железо, сульфаты, тяжелые металлы, мышьяк. Ø ЕP: Допустимые примеси: хлориды, сульфаты, тяжелые металлы, мышьяк. Ø ЕP: Микробиологическое загрязнение. Общее количество аэробных колоний не должно быть более чем 103 микроорганизмов на грамм. 65
Оценка чистоты Ø ГФ: Допустимые примеси: карбонаты хлориды, железо, сульфаты, тяжелые металлы, мышьяк. Ø ЕP: Допустимые примеси: хлориды, сульфаты, тяжелые металлы, мышьяк. Ø ЕP: Микробиологическое загрязнение. Общее количество аэробных колоний не должно быть более чем 103 микроорганизмов на грамм. 65
 ЕР: Нейтрализующая способность. Ø Диспергируйте 0, 5 г препарата в 100 мл воды, нагрейте, добавьте 100 мл 0, 1 М хлороводородной кислоты, предварительно нагретой до 37 градусов; Ø Измерить р. Н раствора через 10, 15, и 20 минут: должно быть не менее 1, 8; 2, 3 и 3, 0 соответственно и далее во времени – не выше 4, 5. Ø Добавьте 10 мл 0, 5 М хлороводородной кислоты, предварительно нагретой, через 1 час титруйте 0, 1 М раствором натрия гидроксида до р. Н 3, 5. Должно потребоваться не более чем 35 мл 0, 1 М раствора натрия гидроксида.
ЕР: Нейтрализующая способность. Ø Диспергируйте 0, 5 г препарата в 100 мл воды, нагрейте, добавьте 100 мл 0, 1 М хлороводородной кислоты, предварительно нагретой до 37 градусов; Ø Измерить р. Н раствора через 10, 15, и 20 минут: должно быть не менее 1, 8; 2, 3 и 3, 0 соответственно и далее во времени – не выше 4, 5. Ø Добавьте 10 мл 0, 5 М хлороводородной кислоты, предварительно нагретой, через 1 час титруйте 0, 1 М раствором натрия гидроксида до р. Н 3, 5. Должно потребоваться не более чем 35 мл 0, 1 М раствора натрия гидроксида.
 Количественное определение Ø ГФ не приводит количественного определение данного препарата. Ø 1. ЕР – комплексонометрическое определение (Метод обратного титрования). Применяется, когда проведение прямого титрования затруднено из-за медленного протекания реакции образования комплексоната или невозможности подбора индикатора. Ø Методика. К 20 мл раствора препарата добавляют 25 мл 0, 1 М ЭДТА и 10 мл смеси эквивалентный объемов растворов ацетата аммония и уксусной кислоты. Кипятят 2 мин. , охлаждают и прибавляют 50 мл абсолютного этанола и 3 мл свежеприготовленного 0, 025% раствора дитизона в абсолютном спирте. Ø Титрант – цинка сульфат 67 Ø 1 мл 0, 1 М ЭДТА эквивалентен 5, 098 мг алюминия.
Количественное определение Ø ГФ не приводит количественного определение данного препарата. Ø 1. ЕР – комплексонометрическое определение (Метод обратного титрования). Применяется, когда проведение прямого титрования затруднено из-за медленного протекания реакции образования комплексоната или невозможности подбора индикатора. Ø Методика. К 20 мл раствора препарата добавляют 25 мл 0, 1 М ЭДТА и 10 мл смеси эквивалентный объемов растворов ацетата аммония и уксусной кислоты. Кипятят 2 мин. , охлаждают и прибавляют 50 мл абсолютного этанола и 3 мл свежеприготовленного 0, 025% раствора дитизона в абсолютном спирте. Ø Титрант – цинка сульфат 67 Ø 1 мл 0, 1 М ЭДТА эквивалентен 5, 098 мг алюминия.
 n Прибавление избытка ЭДТА в раствор приводит к образованию комплексоната Al. Y- Al 3+ + H 2 Y 2 -(изб)= Al. Y- + 2 H+ n Индикатор – дитизон (дифенилтиокарбазон) – С 6 Н 5 -N=N- С(S)NНNН-С 6 Н 5 (2 -фенилгидразид ( фенилазотиомуравьиной к-ты). Присутствует в свободной форме HInd 2 - (зеленовато-голубая окраска) n При титровании избыточных анионов H 2 Y 2 - раствором При титровании избыточных анионов цинка сульфата образуется комплексонат цинка H 2 Y 2 - + Zn 2+ = Zn. Y 2 - + 2 H+ n В точке эквивалентности все анионы H 2 Y 2 - оттитрованы, анионы поэтому избыточная капля титранта приводит к образованию красновато-фиолетового комплекса дитизоната цинка Zn. Ind- HInd 2 - + Zn 2+ = Zn. Ind- + H+
n Прибавление избытка ЭДТА в раствор приводит к образованию комплексоната Al. Y- Al 3+ + H 2 Y 2 -(изб)= Al. Y- + 2 H+ n Индикатор – дитизон (дифенилтиокарбазон) – С 6 Н 5 -N=N- С(S)NНNН-С 6 Н 5 (2 -фенилгидразид ( фенилазотиомуравьиной к-ты). Присутствует в свободной форме HInd 2 - (зеленовато-голубая окраска) n При титровании избыточных анионов H 2 Y 2 - раствором При титровании избыточных анионов цинка сульфата образуется комплексонат цинка H 2 Y 2 - + Zn 2+ = Zn. Y 2 - + 2 H+ n В точке эквивалентности все анионы H 2 Y 2 - оттитрованы, анионы поэтому избыточная капля титранта приводит к образованию красновато-фиолетового комплекса дитизоната цинка Zn. Ind- HInd 2 - + Zn 2+ = Zn. Ind- + H+
 Ø 2. Гравиметрический метод: прокаливание, охлаждении и взвешивание образовавшегося оксида алюминия: t 2 Al(OH)3 Al 2 О 3 + 3 H 2 O
Ø 2. Гравиметрический метод: прокаливание, охлаждении и взвешивание образовавшегося оксида алюминия: t 2 Al(OH)3 Al 2 О 3 + 3 H 2 O
 Применение n Антацидное средство. Антацидное действие Антацидное средство основано на нейтрализации HCl (1 г препарата нейтрализует 250 мл 0, 1 моль/л раствора HCl): Al(OH)3 + 3 HCl Al. Cl 3 + 3 H 2 O n Значение р. Н желудочного сока постепенно повышается до 3, 5 -4, 5 и остается на этом уровне в течение нескольких часов. n Обладает также адсорбирующими и обволакивающими свойствами. n В содержимом кишечника катион алюминия гидролизуется с образованием малорастворимых и невсасывающихся основных солей или гидроксида: Al. Cl 3 + 2 H 2 O Al(OH)2 Cl + 2 HCl n Кроме того в кишечнике возможно образование малорастворимого фосфата: Al 3+ + PO 43 - Al. PO 4 70
Применение n Антацидное средство. Антацидное действие Антацидное средство основано на нейтрализации HCl (1 г препарата нейтрализует 250 мл 0, 1 моль/л раствора HCl): Al(OH)3 + 3 HCl Al. Cl 3 + 3 H 2 O n Значение р. Н желудочного сока постепенно повышается до 3, 5 -4, 5 и остается на этом уровне в течение нескольких часов. n Обладает также адсорбирующими и обволакивающими свойствами. n В содержимом кишечника катион алюминия гидролизуется с образованием малорастворимых и невсасывающихся основных солей или гидроксида: Al. Cl 3 + 2 H 2 O Al(OH)2 Cl + 2 HCl n Кроме того в кишечнике возможно образование малорастворимого фосфата: Al 3+ + PO 43 - Al. PO 4 70
 n В последнее время применяют ряд комбинированных готовых лекарственных препаратов: n Альмагель (Almagel) – гель, 5 мл которого содержат ) 4, 75 мл геля гидроокиси алюминия и 0, 1 г магния окиси с добавлением D-сорбита. n Альмагель А содержит дополительно 0. 1 г анестезина. Применяют, если язвенная болезнь желудка или двенадцатиперстной кишки сопровождаются тошнотой, рвотой, болезненостью. n Маалокс (Maalox) – комбинированный препарат в виде таблеток, содержащих по 0, 4 г алюминия гидроокиси и гидроокиси магния, или суспензии, содержащей в 100 мл по 3, 49 г алюминия гидроокиси и 3, 99 г магния гидроокиси. n Гастал (Gastal) – таблетки, содержащие 0, 45 г алюминия гидроокиси в комбинации с магния карбонатом и магния окисью (0, 3 г). n Хранение. Хранить в темном месте в хорошо закрытых банках.
n В последнее время применяют ряд комбинированных готовых лекарственных препаратов: n Альмагель (Almagel) – гель, 5 мл которого содержат ) 4, 75 мл геля гидроокиси алюминия и 0, 1 г магния окиси с добавлением D-сорбита. n Альмагель А содержит дополительно 0. 1 г анестезина. Применяют, если язвенная болезнь желудка или двенадцатиперстной кишки сопровождаются тошнотой, рвотой, болезненостью. n Маалокс (Maalox) – комбинированный препарат в виде таблеток, содержащих по 0, 4 г алюминия гидроокиси и гидроокиси магния, или суспензии, содержащей в 100 мл по 3, 49 г алюминия гидроокиси и 3, 99 г магния гидроокиси. n Гастал (Gastal) – таблетки, содержащие 0, 45 г алюминия гидроокиси в комбинации с магния карбонатом и магния окисью (0, 3 г). n Хранение. Хранить в темном месте в хорошо закрытых банках.
 Алюминия фосфат Aluminii phosphatum Gel Al. PO 4 122, 0 n Получение реакция взаимодействия сульфата алюминия с эквивалентным количеством фосфата натрия. При этом раствор должен иметь р. Н 4, 0 -4, 5: Al 2(SO 4)3 + 2 Nа 3 РО 4 + n. Н 2 O 2 Al. PO 4. n. Н 2 O + 3 Nа 2 SO 4 n Описание Белый рыхлый аморфный порошок. Практически не растворим в воде и в спирте. Растворим в разведенных минеральных кислотах. 72
Алюминия фосфат Aluminii phosphatum Gel Al. PO 4 122, 0 n Получение реакция взаимодействия сульфата алюминия с эквивалентным количеством фосфата натрия. При этом раствор должен иметь р. Н 4, 0 -4, 5: Al 2(SO 4)3 + 2 Nа 3 РО 4 + n. Н 2 O 2 Al. PO 4. n. Н 2 O + 3 Nа 2 SO 4 n Описание Белый рыхлый аморфный порошок. Практически не растворим в воде и в спирте. Растворим в разведенных минеральных кислотах. 72
 Подлинность (по ЕР) Ø Препарат растворяют в хлороводородной кислоте, а далее – реакция на ион алюминия (c тиоацетатамидом). Ø Препарат растворяют в азотной кислоте, а далее – характерная реакция на фосфаты. Растворы фосфатов в разведенной азотной кислоте при взаимодействии с молибдатом аммония (NH 4)3 Mo. O 4 при нагревании окрашиваются в желтый цвет, затем образуется желтый кристаллический осадок фосфомолибдата аммония: Ø Осадок растворяется в азотной кислоте, растворах щелочей и аммиака, в присутствии большого количества фосфат-ионов ( с образованием желтого раствора) 73
Подлинность (по ЕР) Ø Препарат растворяют в хлороводородной кислоте, а далее – реакция на ион алюминия (c тиоацетатамидом). Ø Препарат растворяют в азотной кислоте, а далее – характерная реакция на фосфаты. Растворы фосфатов в разведенной азотной кислоте при взаимодействии с молибдатом аммония (NH 4)3 Mo. O 4 при нагревании окрашиваются в желтый цвет, затем образуется желтый кристаллический осадок фосфомолибдата аммония: Ø Осадок растворяется в азотной кислоте, растворах щелочей и аммиака, в присутствии большого количества фосфат-ионов ( с образованием желтого раствора) 73
 Оценка чистоты Допустимые примеси: v хлориды (500 ррм), v сульфаты (0, 2%), v тяжелые металлы (10 ррм), v мышьяк (1 ррм). v растворимые фосфаты (не более 0, 5% РО 43 - )- с (не более аммония молибдатом). Измеряют абсорбцию испытуемого раствора и эталонного раствора при 400 нм. v Растворимые соли алюминия (10 ррм): к 16 г ЛС добавляем 50 мл воды, кипятим 5 мин. , отмываем, центрифугируем. Титруем ЭДТА. v Микробиологическое загрязнение. Общее количество . Общее количество аэробных колоний не должно быть более чем 103 микроорганизмов на грамм.
Оценка чистоты Допустимые примеси: v хлориды (500 ррм), v сульфаты (0, 2%), v тяжелые металлы (10 ррм), v мышьяк (1 ррм). v растворимые фосфаты (не более 0, 5% РО 43 - )- с (не более аммония молибдатом). Измеряют абсорбцию испытуемого раствора и эталонного раствора при 400 нм. v Растворимые соли алюминия (10 ррм): к 16 г ЛС добавляем 50 мл воды, кипятим 5 мин. , отмываем, центрифугируем. Титруем ЭДТА. v Микробиологическое загрязнение. Общее количество . Общее количество аэробных колоний не должно быть более чем 103 микроорганизмов на грамм.
 n р. Н = 6. 0 -8. 0 n Способность нейтрализовывать кислоты: 2 г ЛC Способность нейтрализовывать кислоты растворить в 30 мл 0, 1 М HCl при 37 о. С. Через 15 мин. р. Н= 2. 0 -2. 5 р. Н= n Остаток при прокаливании при 500 о. С 19 -23% n Микробиологическое загрязнение. Общее количество аэробных колоний не должно быть более чем 103 микроорганизмов на грамм. n Перекиси (150 ррм). Определения проводят с (150 ррм). диванадием пентоксидом V 2 O 5, который в степени окисления +5 проявляют свойства окислителей ( по окраске не превосходит эталонный раствор)
n р. Н = 6. 0 -8. 0 n Способность нейтрализовывать кислоты: 2 г ЛC Способность нейтрализовывать кислоты растворить в 30 мл 0, 1 М HCl при 37 о. С. Через 15 мин. р. Н= 2. 0 -2. 5 р. Н= n Остаток при прокаливании при 500 о. С 19 -23% n Микробиологическое загрязнение. Общее количество аэробных колоний не должно быть более чем 103 микроорганизмов на грамм. n Перекиси (150 ррм). Определения проводят с (150 ррм). диванадием пентоксидом V 2 O 5, который в степени окисления +5 проявляют свойства окислителей ( по окраске не превосходит эталонный раствор)
 Ø ЕР – комплексонометрическое определение (Метод обратного титрования). Ø Методика. К 50 мл раствора препарата (0. 3 г ЛС) добавляют 10 мл 0, 1 М ЭДТА и 30 мл смеси эквивалентный объемов растворов ацетата аммония и уксусной кислоты. Кипятят 3 мин. , охлаждают и прибавляют 25 мл абсолютного этанола и титруют. Ø Титрант – цинка сульфат Ø Точка эквивалентности – потенциометрически. Ø 1 мл 0, 1 М цинка сульфата эквивалентен 12, 2 мг алюминия фосфата. Ø Содержание Al. PO 4 19 -21%
Ø ЕР – комплексонометрическое определение (Метод обратного титрования). Ø Методика. К 50 мл раствора препарата (0. 3 г ЛС) добавляют 10 мл 0, 1 М ЭДТА и 30 мл смеси эквивалентный объемов растворов ацетата аммония и уксусной кислоты. Кипятят 3 мин. , охлаждают и прибавляют 25 мл абсолютного этанола и титруют. Ø Титрант – цинка сульфат Ø Точка эквивалентности – потенциометрически. Ø 1 мл 0, 1 М цинка сульфата эквивалентен 12, 2 мг алюминия фосфата. Ø Содержание Al. PO 4 19 -21%
 Ø Применение. Как антацидное средство при язвенной болезни, гастритах, диспепсии. Ø Хранение. В хорошо закрытых банках, в сухом прохлодном месте. Ø Фосфалюгель (Fosfalugel). Препарат содержит около 23% алюминия фосфата, а также гель пектинов (растительных полисахаридов) и агара (полисахаридного препарата, содержащего 50 -80% агарозы – линейного полисахарида). Ø Гефал (Gefal) – содержит фосфат алюминия в виде суспезии (наполнители – сахар, нипагин, нипазол) белого цвета, сладковатого вкуса, с запахом ароматических добавок. Выпускают в полиэтиленовых флаконах по 250 г. 77
Ø Применение. Как антацидное средство при язвенной болезни, гастритах, диспепсии. Ø Хранение. В хорошо закрытых банках, в сухом прохлодном месте. Ø Фосфалюгель (Fosfalugel). Препарат содержит около 23% алюминия фосфата, а также гель пектинов (растительных полисахаридов) и агара (полисахаридного препарата, содержащего 50 -80% агарозы – линейного полисахарида). Ø Гефал (Gefal) – содержит фосфат алюминия в виде суспезии (наполнители – сахар, нипагин, нипазол) белого цвета, сладковатого вкуса, с запахом ароматических добавок. Выпускают в полиэтиленовых флаконах по 250 г. 77

