Кафедра биоорганической химии БГМУ Тема лекции 4:


Кафедра биоорганической химии БГМУ Тема лекции 4: Общие закономерности реакционной способности органических соединений

Академик Н. Н. Семенов n Химический процесс – то главное и основное, что отличает физику от химии и делает вторую более интересной наукой (из нобелевской лекции) Автор теории цепных свободно- радикальных процессов

Активированный комплекс — Органическая реакция — процесс, при состояние реагирующих веществ, при котором химическая система из состояния старые связи еще не котором с одним вещественным разорвались, а новые — не составом переходит в состояние с другим вещественным составом образовались

Химический процесс n Совокупность всех элементарных стадий через которые протекает химическая реакция с указанием условий ее проведения, характера разрыва ковалентной связи, характера образующихся промежуточных продуктов и скоростей отдельных стадий называется химическим процессом

Скорость лимитирующая стадия И механизм реакции n Самая медленная стадия в химическом процессе называется скорость лимитирующей, так она определяет скорость выхода конечного продукта Механизм реакции определяется характером разрыва ковалентной связи, характером реагента и образующегося промежуточного продукта на самой медленной, скорость лимитирующей стадии химического процесса

Классификация органическихучетом По направлению реакций с реакций конечного результата: р. замещения Substitution - S р. присоединения Addition -A р. отщепления Elimination -E р. перегруппировки Isomerisation -I
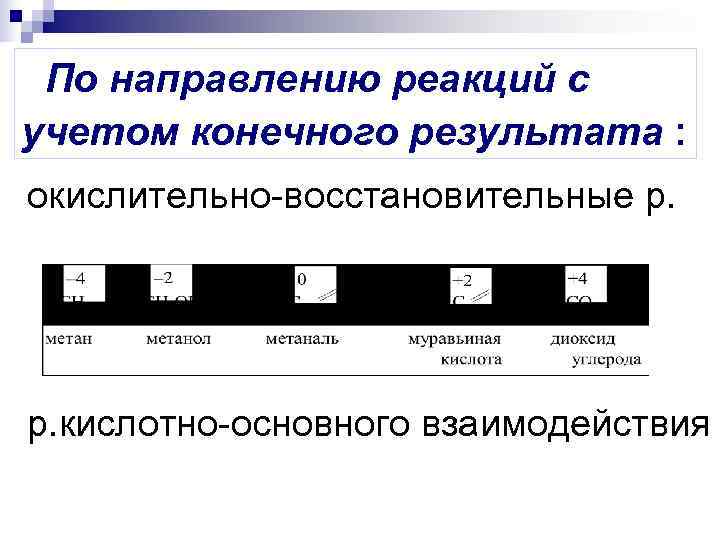
По направлению реакций с учетом конечного результата : окислительно-восстановительные р. р. кислотно-основного взаимодействия

По характеру изменений связей в субстрате и реагенте n радикальные n ионные n согласованные Диеновый синтез Дильса-Альдера

Радикальные реакции Гомолитический разрыв связи n свободные радикалы: sp 2 -гибридизация плоскостное строение

Свободный радикал n Свободный радикал – атом, группировка атомов или молекула , имеющие на одном из атомов свободный неспаренный электрон и обладающие повышенной реакционной способностью

Признаки радикальных реакций 1. гомолитически разрывается неполярная ков. связь 2. реакции протекают в газовой фазе или в неполярных растворителях 3. инициируются физическими (излучения, tº), а также химическими факторами (R-O-O-R, Fe 2+)

Признаки радикальных реакций 4. чувствительны к действию акцепторов электронов (фенолы, тиолы) 5. являются цепными самоускоряющимися рекциями Стадии радикальных реакций: 1. инициирование радикалов 2. рост цепи 3. обрыв цепи

Радикальные реакции n SR n AR n окисление n. SR - для алканов, циклоалканов (кроме малых циклов) n. AR - для малых циклов
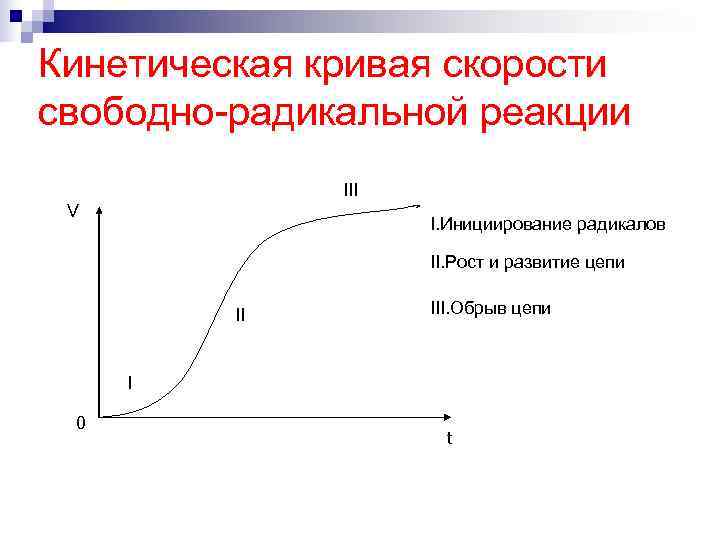
Кинетическая кривая скорости свободно-радикальной реакции III V I. Инициирование радикалов II. Рост и развитие цепи III. Обрыв цепи I 0 t
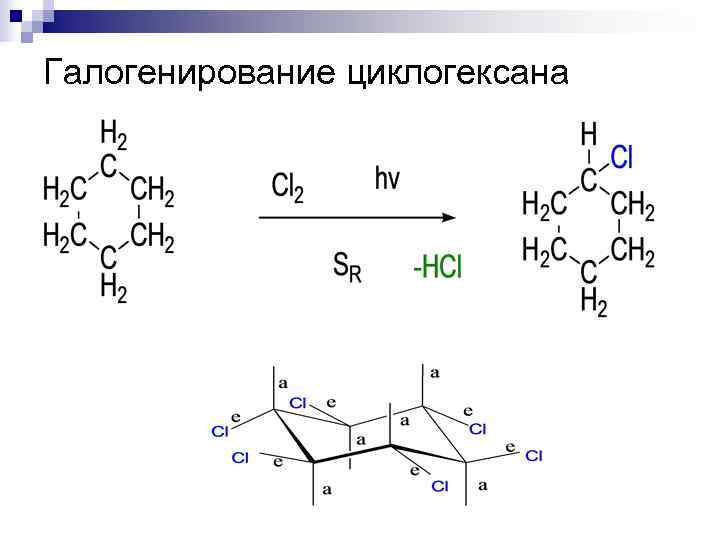
Галогенирование циклогексана
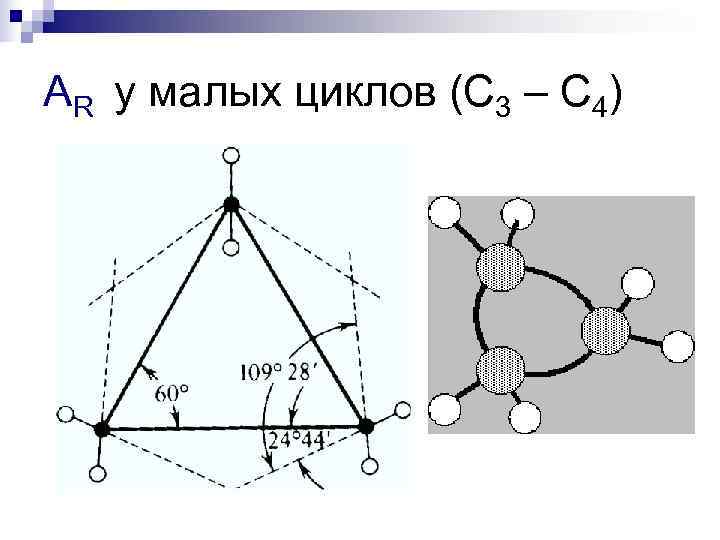
AR у малых циклов (С 3 – С 4)
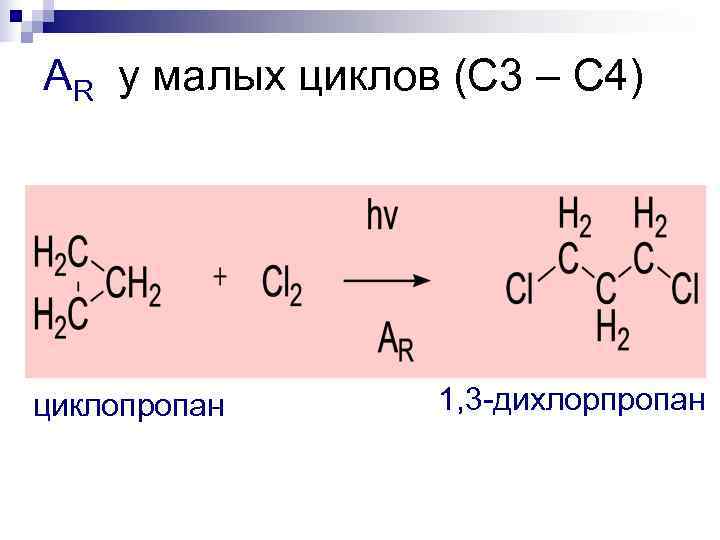
AR у малых циклов (С 3 – С 4) циклопропан 1, 3 -дихлорпропан
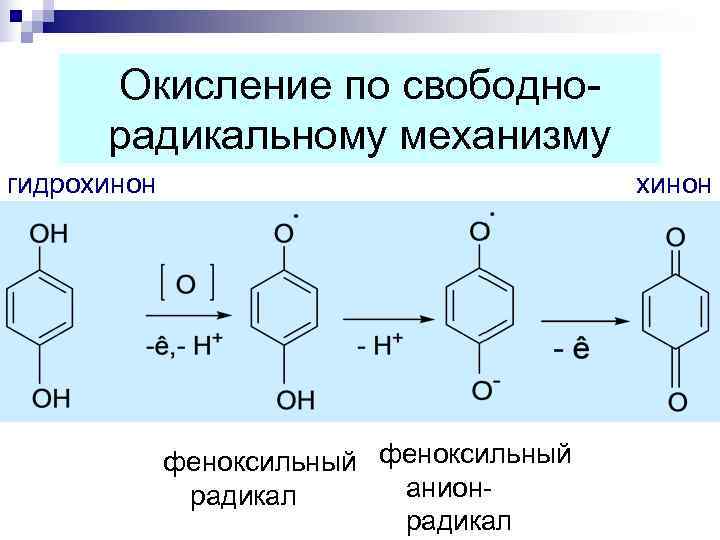
Окисление по свободно- радикальному механизму гидрохинон хинон феноксильный радикал анион- радикал
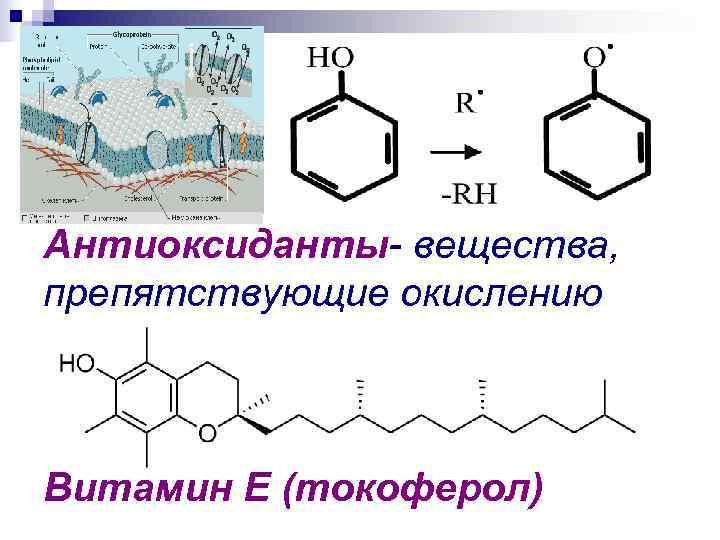
Антиоксиданты- вещества, препятствующие окислению Витамин Е (токоферол)
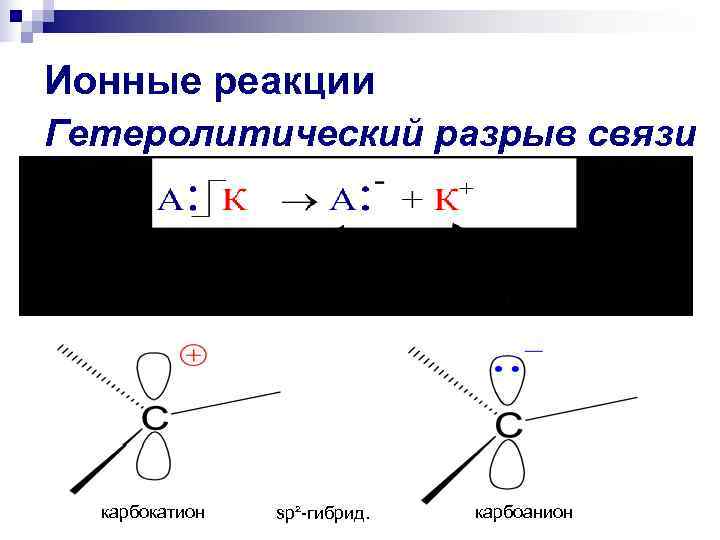
Ионные реакции Гетеролитический разрыв связи карбокатион sp²-гибрид. карбоанион

Реагенты: Нуклеофильные реагенты Nu а) отрицательно заряженные ионы : Н : Вr¯ : ОН¯ : OR¯ : SН¯ : SR¯ б) молекулы, имеющие свободную неподеленную пару электронов . . . . HOH ROH RNH 2 RSH

Реагенты: Электрофильные Е а) положительно заряженные ионы Н+ Br+ Н 3 С + Н 5 С 2+ б) молекулы с частичным положительным зарядом на одном из атомов

Признаки ионных реакций 1. гетеролитически разрывается полярная или легко поляризующаяся ковалентная связь 2. такие реакции протекают в полярных растворителях 3. катализируются кислотами или основаниями 4. являются реакциями I или II порядка

AE- реакции электрофильного присоединения Алкены Алкадиены Арены (в особых условиях)
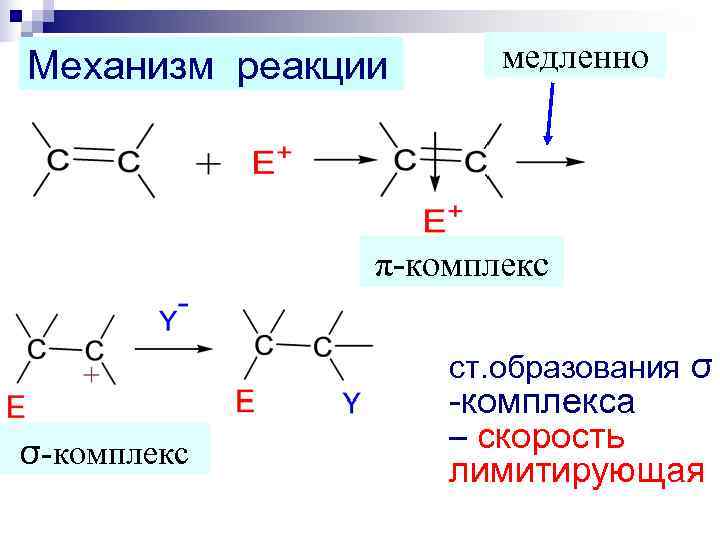
Механизм реакции медленно π-комплекс ст. образования σ -комплекса σ-комплекс – скорость лимитирующая

Реакции АЕ у алкенов n По механизму АЕ протекают реакции: n С бромной водой (Br 2) –качеств. реакция на двойную связь; n Реакция гидрохлорирования (с НCl); n Реакция гидратации (с Н 2 О):
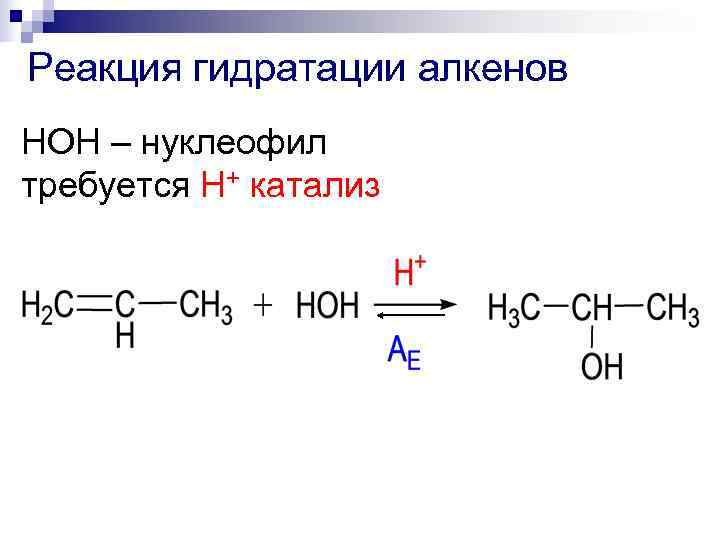
Реакция гидратации алкенов НОН – нуклеофил требуется Н+ катализ
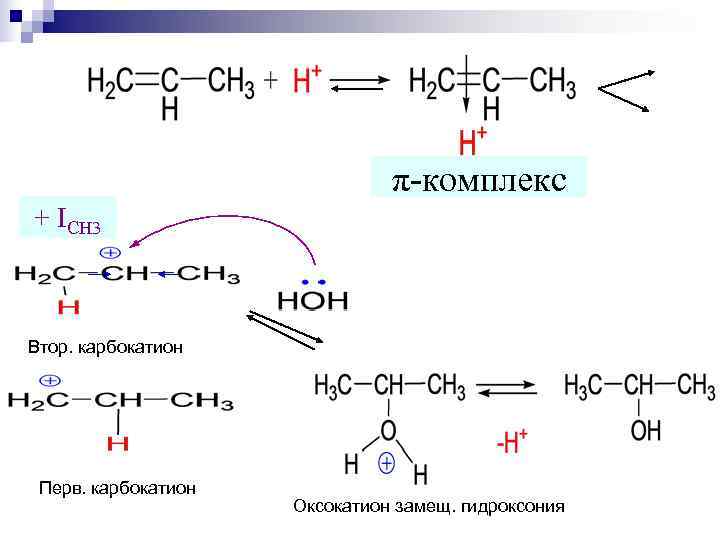
π-комплекс + ICH 3 Втор. карбокатион Перв. карбокатион Оксокатион замещ. гидроксония
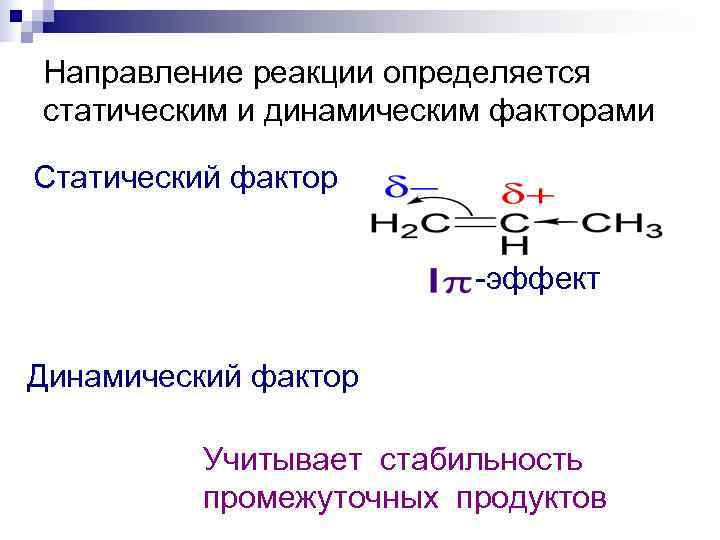
Направление реакции определяется статическим и динамическим факторами Статический фактор -эффект Динамический фактор Учитывает стабильность промежуточных продуктов

Правило Марковникова в современной интерпретации: направление присоединения реагентов типа НХ к непредельным соединениям определяется относительной устойчивостью образующихся карбокатионов

Реакции электрофильного замещения у аренов SE
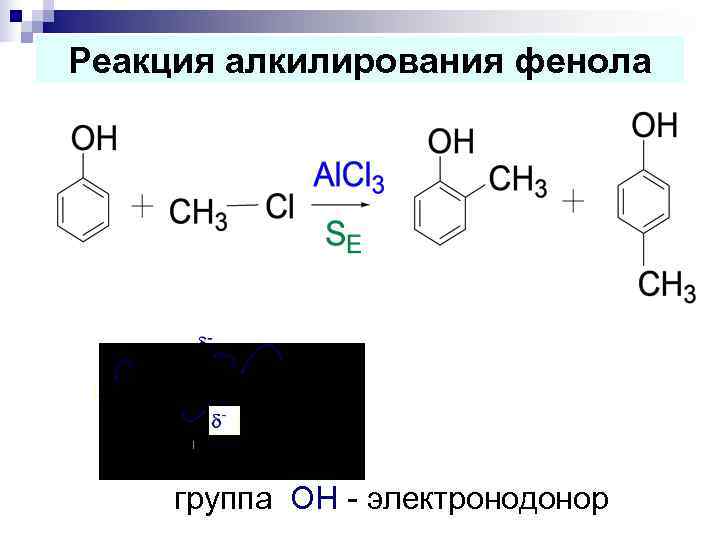
Реакция алкилирования фенола группа ОН - электронодонор
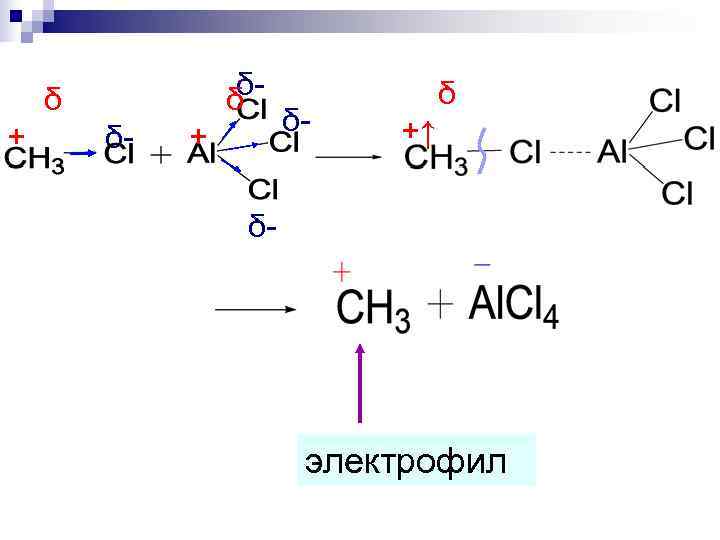
δ δδ- δ- +↑ + δ- + δ- электрофил
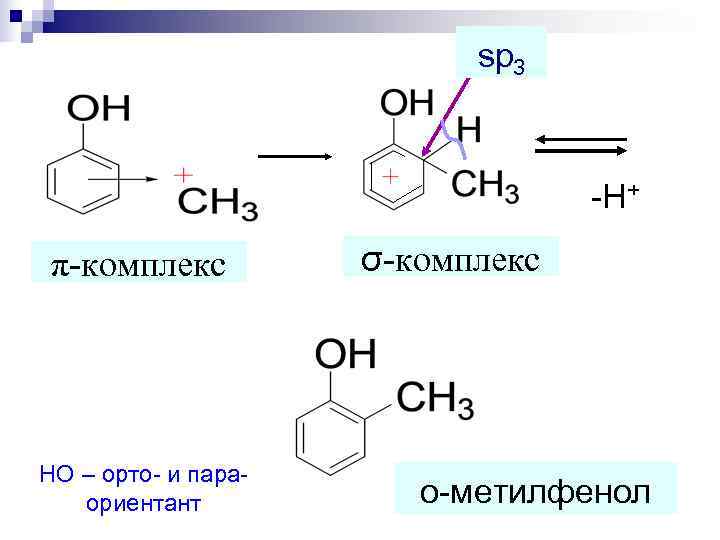
sp 3 -H+ π-комплекс σ-комплекс НО – орто- и пара- ориентант о-метилфенол
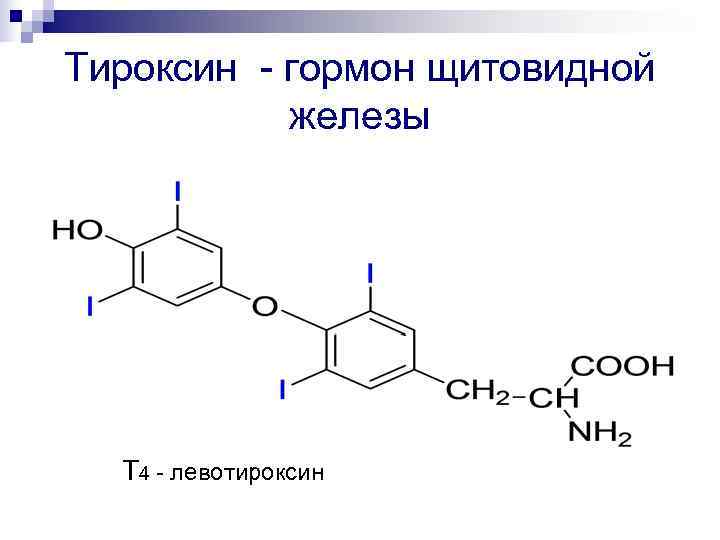
Тироксин - гормон щитовидной железы Т 4 - левотироксин

-I CHO , - М CHO электроноакцептор Мета - ориентант
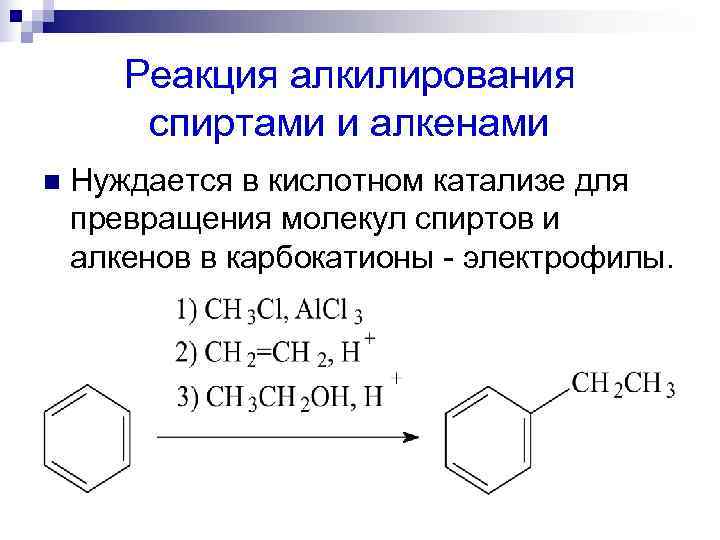
Реакция алкилирования спиртами и алкенами n Нуждается в кислотном катализе для превращения молекул спиртов и алкенов в карбокатионы - электрофилы.

Окисление по боковой цепи Реакция окисления :
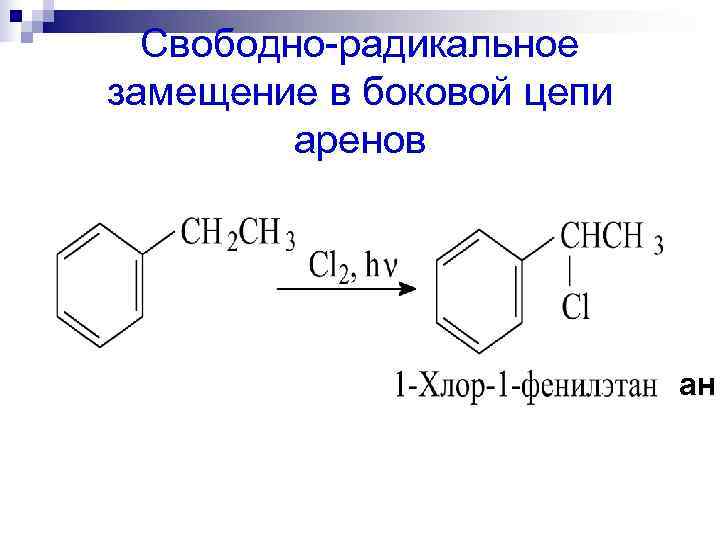
Свободно-радикальное замещение в боковой цепи аренов ан
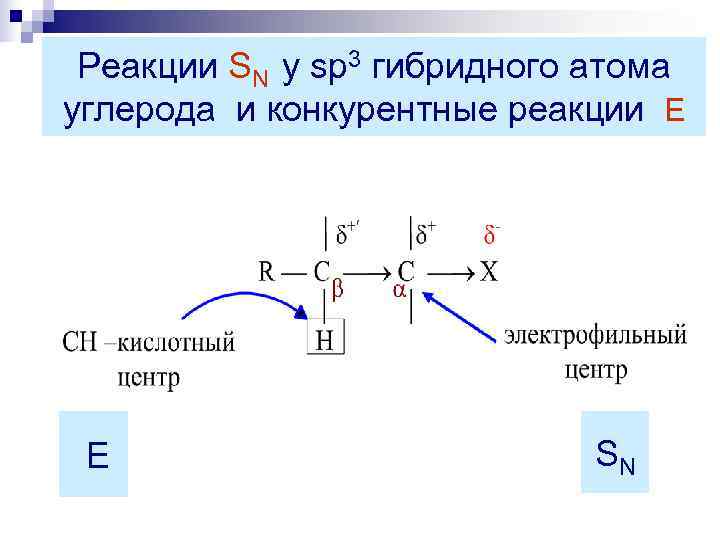
Реакции SN у sp 3 гибридного атома углерода и конкурентные реакции E E SN
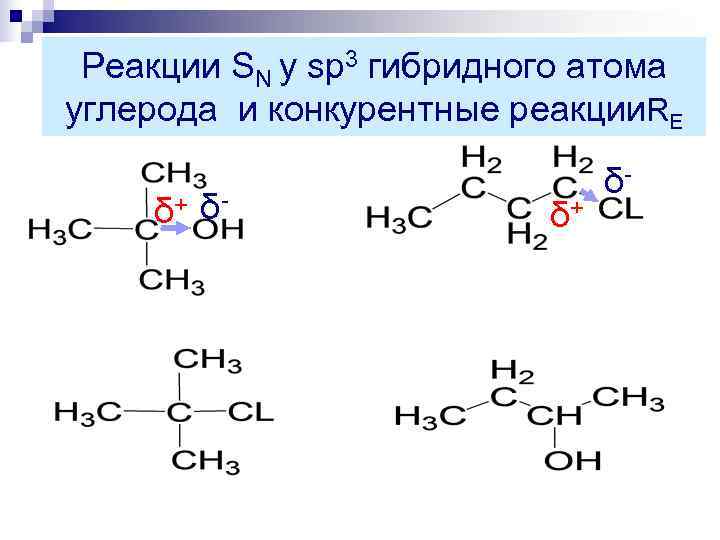
Реакции SN у sp 3 гибридного атома углерода и конкурентные реакции. RE δ- δ+ δ- δ+

В зависимости от строения субстрата: мономолекулярные SN 1 E 1 бимолекулярные SN 2 E 2
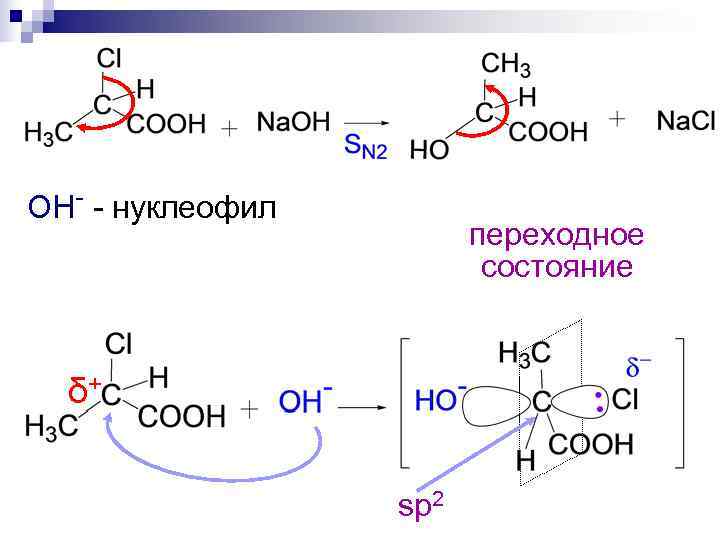
OH- - нуклеофил переходное состояние δ+ sp 2
![обращение конфигурации V = K [ГА] · [Nu] обращение конфигурации V = K [ГА] · [Nu]](https://present5.com/presentation/3/17146331_106329712.pdf-img/17146331_106329712.pdf-44.jpg)
обращение конфигурации V = K [ГА] · [Nu]
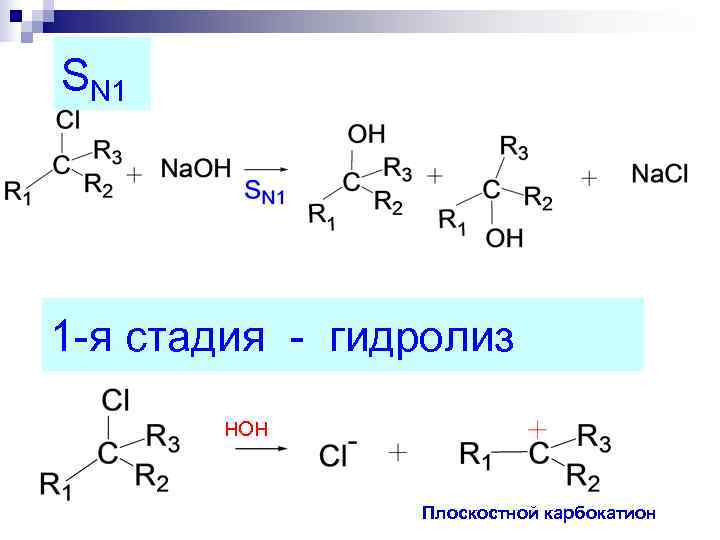
SN 1 1 -я стадия - гидролиз НОН Плоскостной карбокатион
![плоскостное строение V = K [ГА] образуется рацемат плоскостное строение V = K [ГА] образуется рацемат](https://present5.com/presentation/3/17146331_106329712.pdf-img/17146331_106329712.pdf-46.jpg)
плоскостное строение V = K [ГА] образуется рацемат

Конкурентные реакции элиминирования → СН 3 – СН = СН 2 алкен
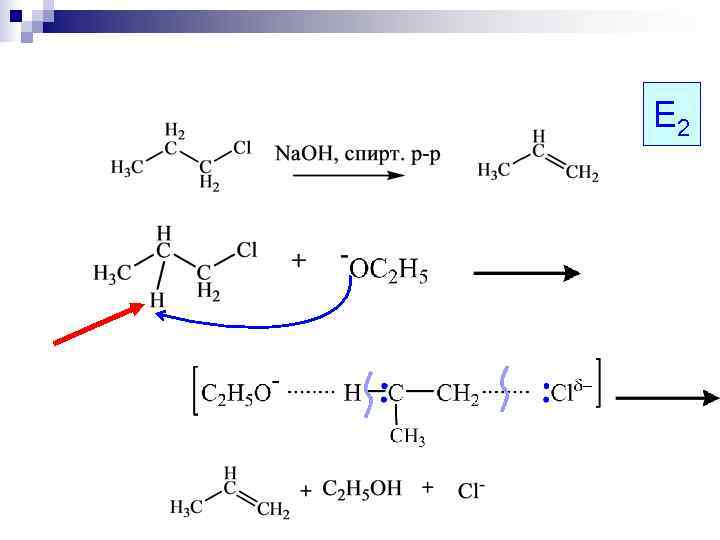
Е 2
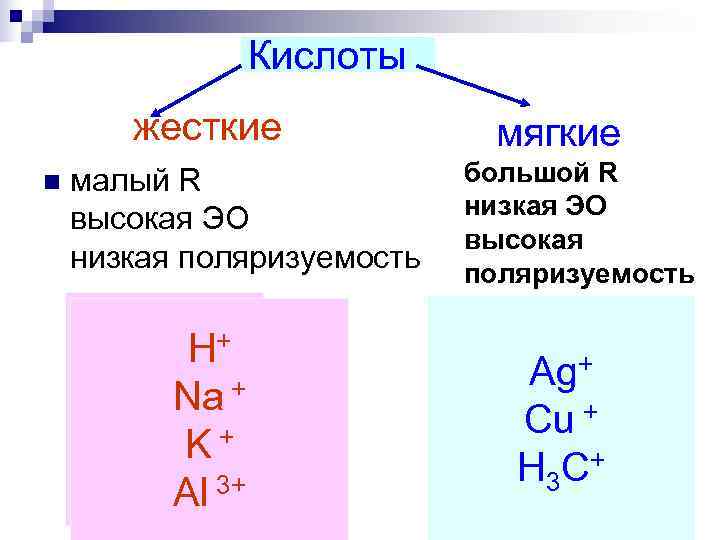
Кислоты жесткие мягкие n малый R большой R высокая ЭО низкая ЭО высокая низкая поляризуемость H+ Ag+ Na + Cu + K+ H 3 C + Al 3+
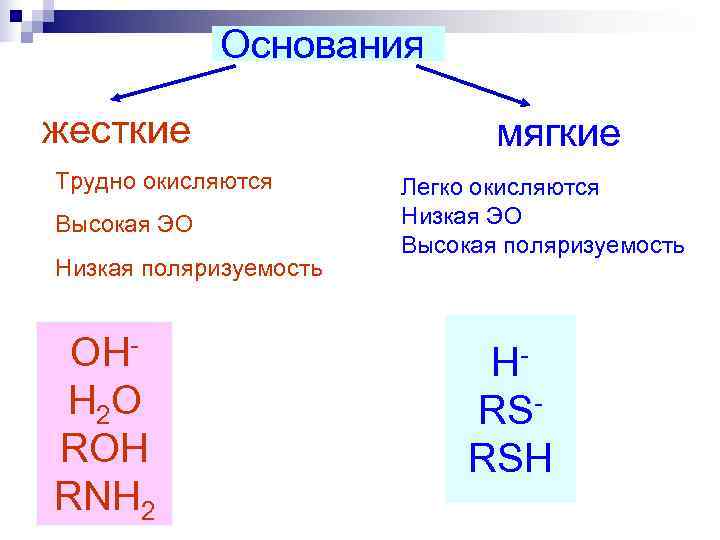
Основания жесткие мягкие Трудно окисляются Легко окисляются Высокая ЭО Низкая ЭО Высокая поляризуемость Низкая поляризуемость OH- H- H 2 O RS- ROH RSH RNH 2
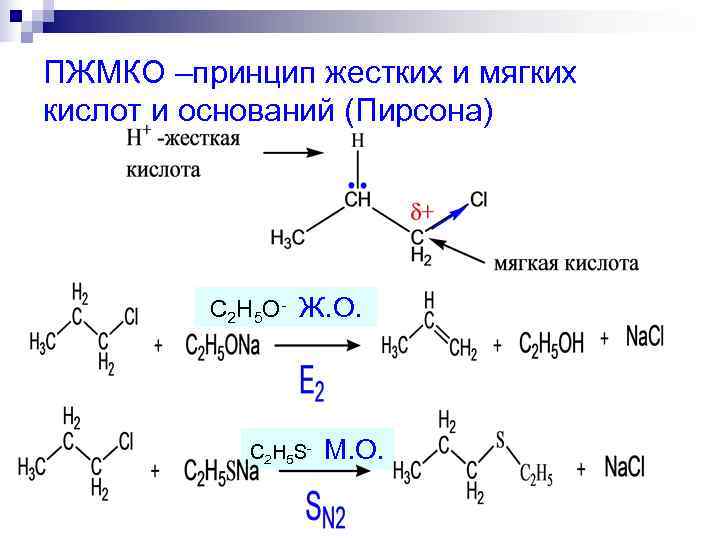
ПЖМКО –принцип жестких и мягких кислот и оснований (Пирсона) С 2 Н 5 О- Ж. О. С 2 Н 5 S - M. О.
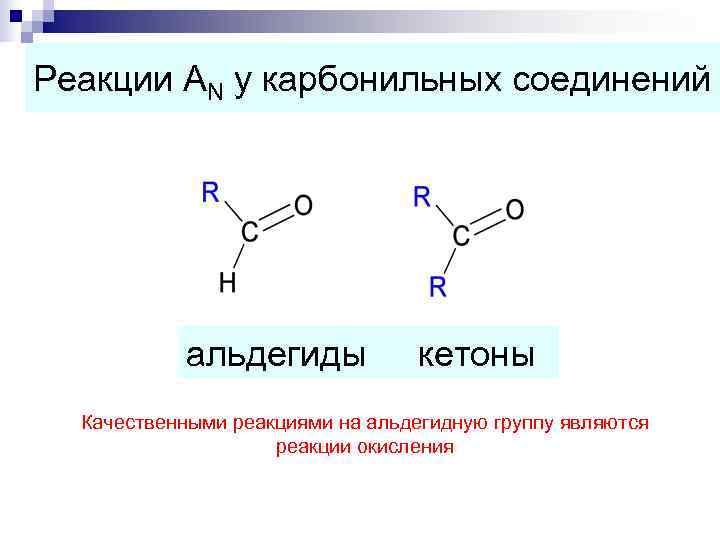
Реакции АN у карбонильных соединений альдегиды кетоны Качественными реакциями на альдегидную группу являются реакции окисления

AN – нуклеофильное присоединение

Типичные АN реакции карбонильных соединений n Присоединение воды; n Присоединение спиртов; n Присоединение аминов; n Реакции восстановления; n Реакция альдольной конденсации.
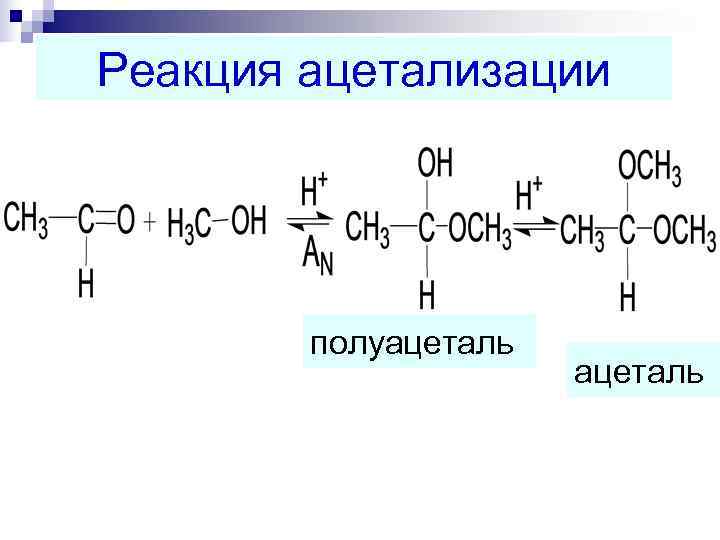
Реакция ацетализации полуацеталь ацеталь
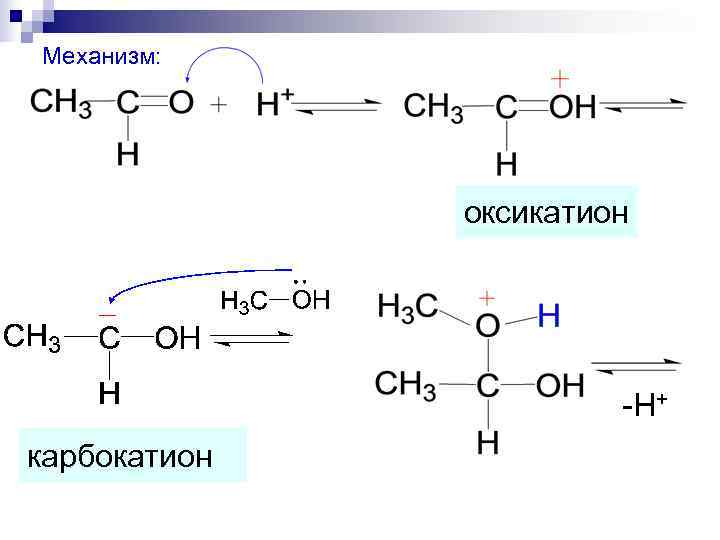
Механизм: оксикатион -H+ карбокатион
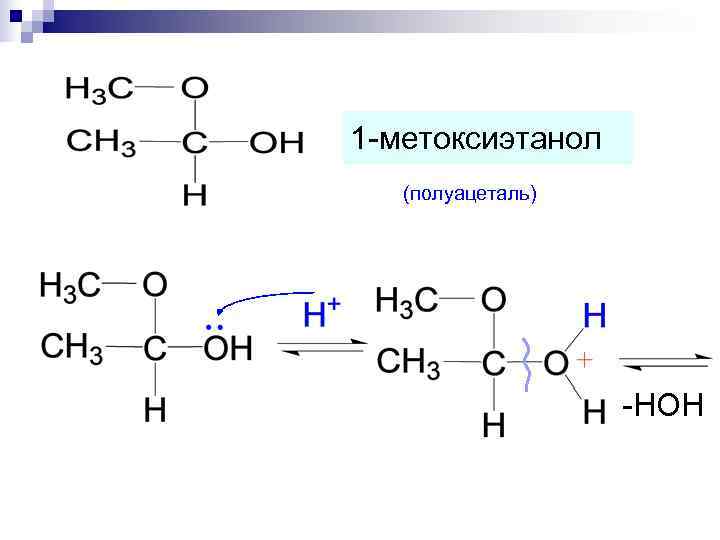
1 -метоксиэтанол (полуацеталь) -HOH
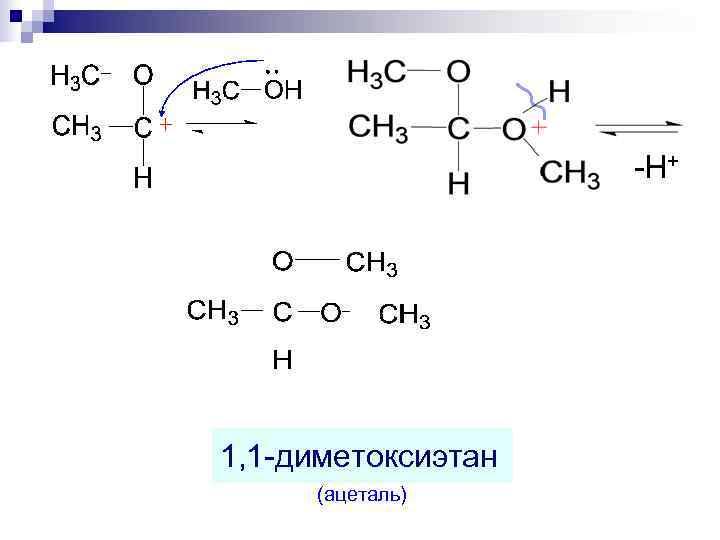
-H+ 1, 1 -диметоксиэтан (ацеталь)
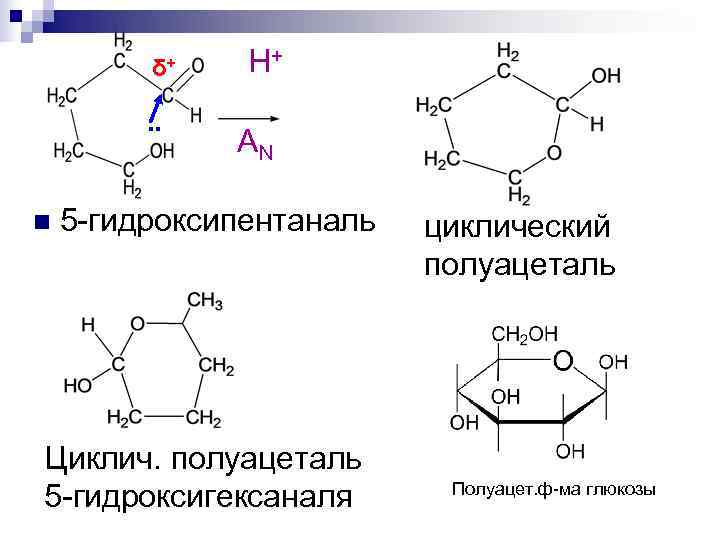
δ+ Н+ . . AN n 5 -гидроксипентаналь циклический полуацеталь Циклич. полуацеталь 5 -гидроксигексаналя Полуацет. ф-ма глюкозы
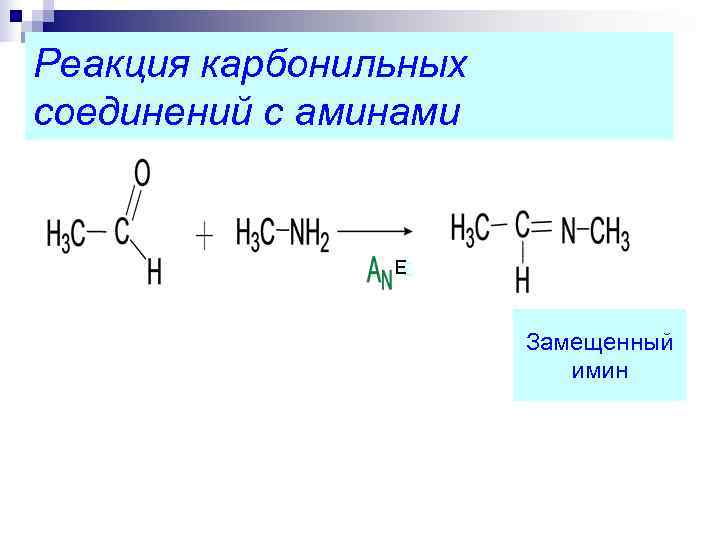
Реакция карбонильных соединений с аминами ЕЕ Замещенный имин
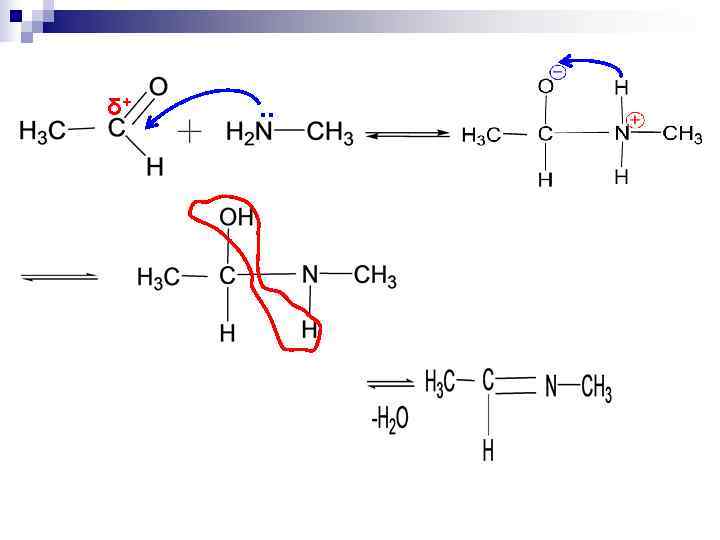
δ+ . .

РЕАКЦИИ ВОССТАНОВЛЕНИЯ + Гидриды лития или бора спирт In vivo донором гидрид иона (Н¯) служит НАДН

Формалин – 40% р-р формальдегида в воде -используется для консервирования анатомических препаратов -как дезинфицирующее средство -вызывает денатурацию белков за счет взаимодействия с NH 2 -группами
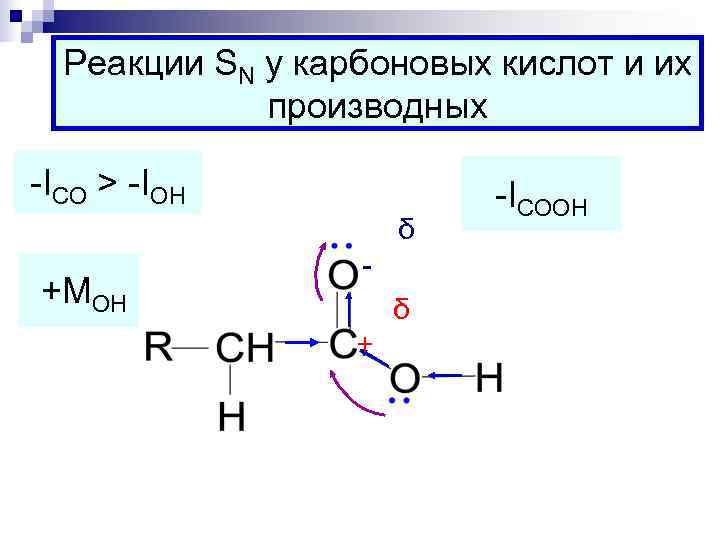
Реакции SN у карбоновых кислот и их производных -ICO > -IOH -ICOOH δ - +MOH δ +
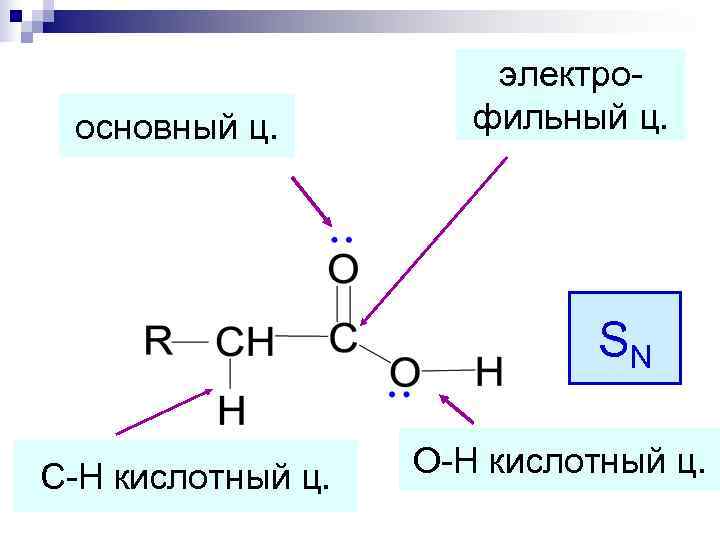
электро- основный ц. фильный ц. SN С-Н кислотный ц. О-Н кислотный ц.
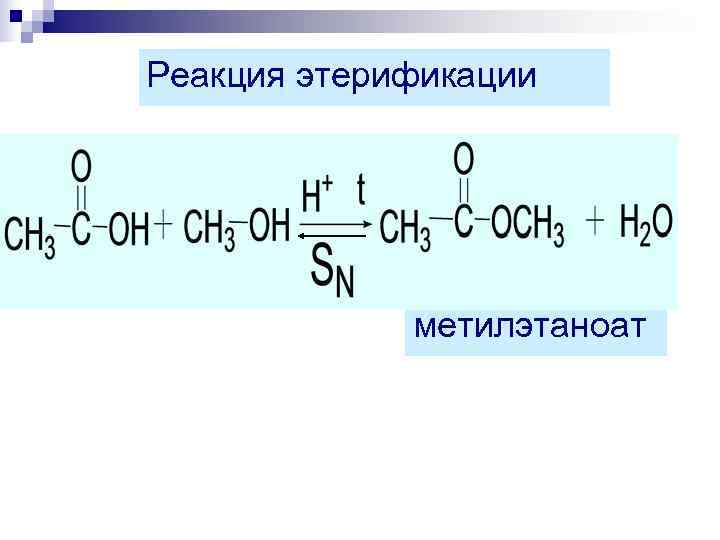
Реакция этерификации метилэтаноат
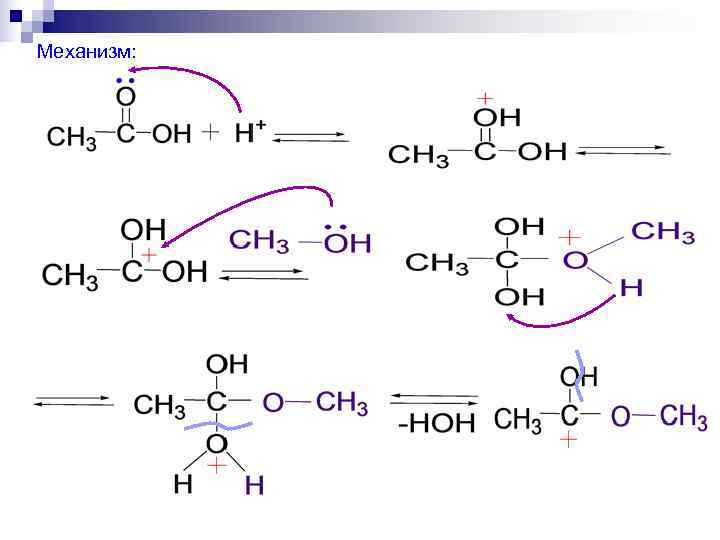
Механизм:
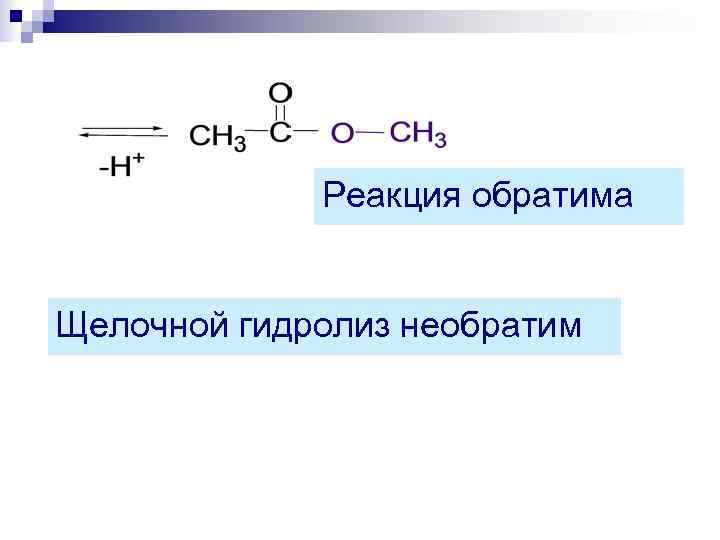
Реакция обратима Щелочной гидролиз необратим
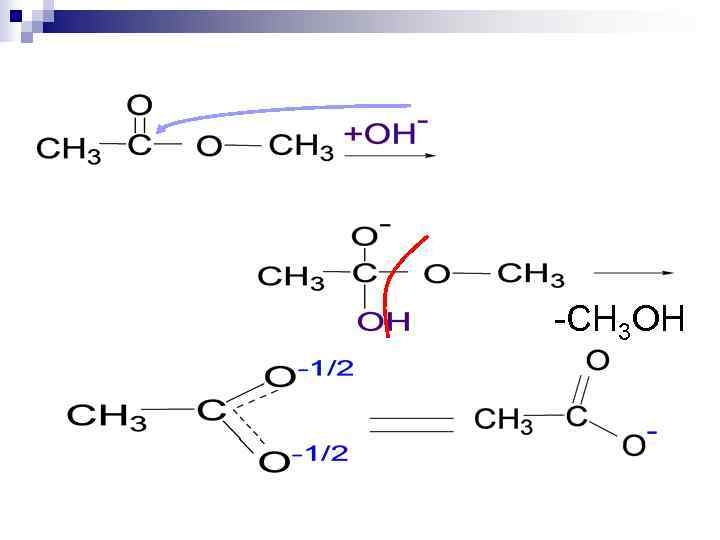
-СН 3 ОН
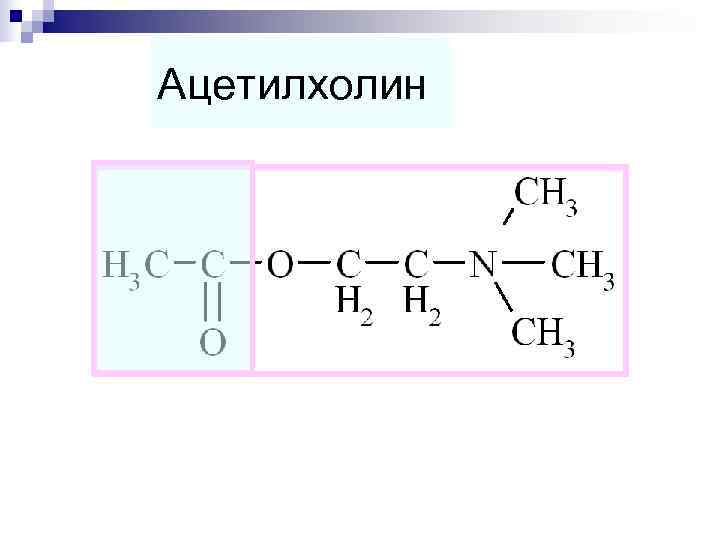
Ацетилхолин

Реакции ацилирования n Реакции получения сложных эфиров при действии на спирты ацилирующих агентов: галоидацил ангидрид сложный эфир Амид к-ты кислота (снижение реакционной способности в SN-реакциях) Сl- > OR ¯ > - Nн 2¯ анион галогена ацилат-ион алкоксид-ион амид-ион (уменьшение стабильности уходящего аниона)
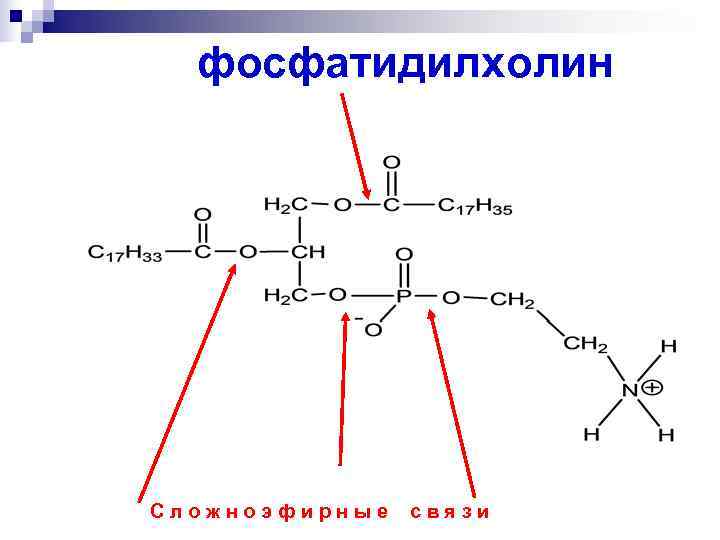
фосфатидилхолин Сложноэфирные связи

БЛАГОДАРЮ ЗА ВНИМАНИЕ !
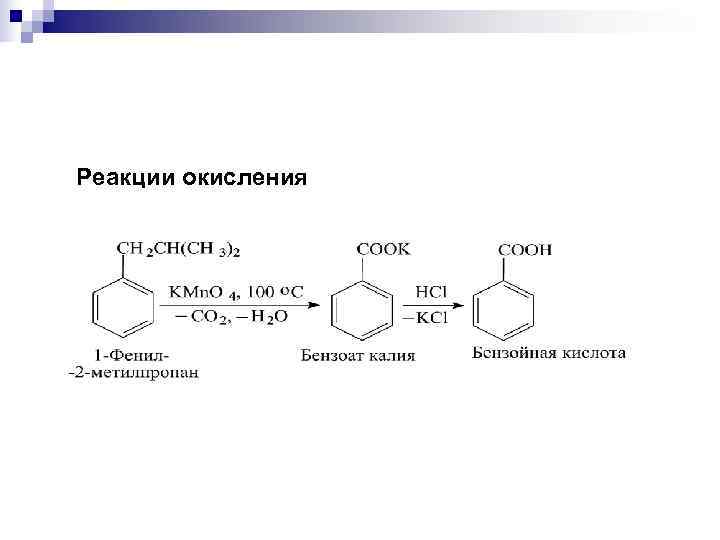
Реакции окисления
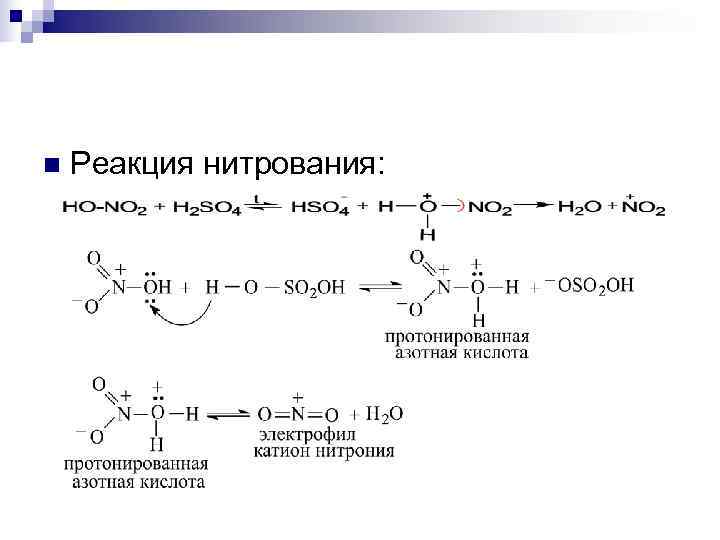
n Реакция нитрования:
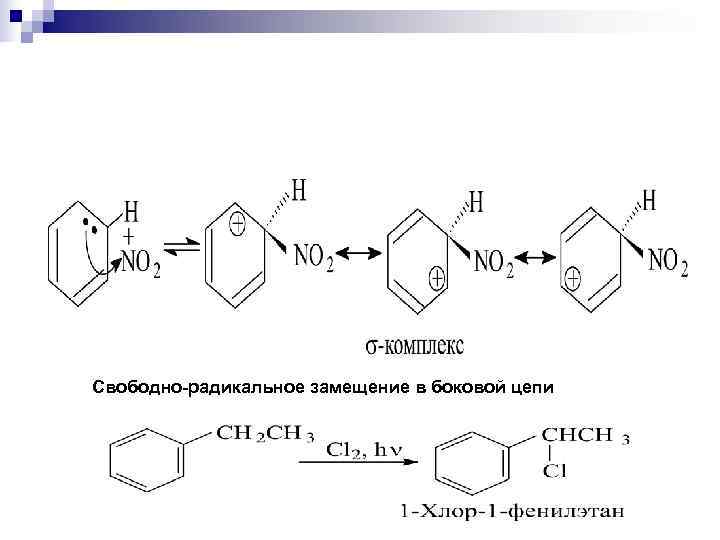
Свободно-радикальное замещение в боковой цепи
механизмы реакций1.ppt
- Количество слайдов: 76

