Лекция 6 РеакцСоедОднойОдновалентФункцБОХ _ЛЕЧ.ppt
- Количество слайдов: 54

Кафедра биологической химии с курсами медицинской, фармакологической и токсикологической химии Тема: Реакционная способность соединений с одной одновалентной функцией Лекция № 6 для студентов 1 курса, обучающихся по специальности 060101 -Лечебное дело Лектор: к. б. н. доцент Оловянникова Раиса Яковлевна Красноярск, 2011 1

Кафедра биологической химии с курсами медицинской, фармакологической и токсикологической химии Тема: Реакционная способность соединений с одной одновалентной функцией Лекция № 6 для студентов 1 курса, обучающихся по специальности 060103 -Педиатрия Лектор: к. б. н. доцент Оловянникова Раиса Яковлевна Красноярск, 2011 2

Цель лекции На основе знаний электронного строения атомов и химических связей в органических молекулах, их реакционных центров сформировать знания: üО кислотности и основности как одном из видов взаимодействия между большинством молекул и как основной движущей силе определенного этапа реакции üО закономерностях химического поведения соединений типа С-Х, где Х – одновалентная функция (Hal, ОН, ОR, SH, SR, NH 2) 3

План 1. Актуальность темы 2. Классы органических соединений с одновалентной функцией типа С→Х 3. Кислоты и основания Бренстеда, их классификация, сравнительная сила. 4. Другие реакционные центры соединений типа С→Х и реакции с их участием (написание схем и механизмов). 5. Выводы 4

Актуальность темы • Большинство видов взаимодействий между органическими молекулами можно рассматривать как кислотно-основные • Эти взаимодействия играют огромную роль в катализе органических реакций • Знание кислотности и основности позволяет по-новому понять природу некоторых связей, например, водородных. 5

Актуальность темы • Через реакции у тетрагонального атома углерода осуществляется взаимосвязь между различными классами соединений типа С-Х, а также между соединениями этого типа и алкенами. • Спиртовые, тиольные и аминогруппы содержатся во многих биологически активных веществах (в том числе, лекарственных), 6

Актуальность темы а также энергетических и информационных субстратах и метаболитах организма. • Функционирование спиртовых, тиольных и аминогрупп лежит в основе процессов жизнедеятельности. • Изучение данной темы поможет нам понять, как это возможно, для чего служат функциональные группы лекарственных веществ и метаболитов организма. 7

Классы органических соединений с одновалентной функцией типа С→Х Группа Х • Hal (Cl, Br, I) • ОН • ОR • SH • SR • NH 2, NHR, NR 2 • • Классы соединений Галогенопроизводные Спирты Простые эфиры Тиолы Сульфиды Амины 8
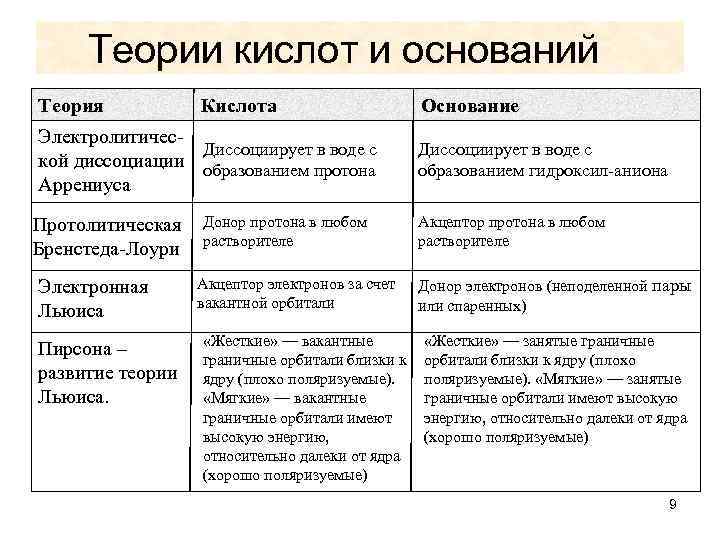
Теории кислот и оснований Теория Кислота Электролитичес. Диссоциирует в воде с кой диссоциации образованием протона Аррениуса Протолитическая Бренстеда-Лоури Электронная Льюиса Пирсона – развитие теории Льюиса. Донор протона в любом растворителе Акцептор электронов за счет вакантной орбитали «Жесткие» — вакантные граничные орбитали близки к ядру (плохо поляризуемые). «Мягкие» — вакантные граничные орбитали имеют высокую энергию, относительно далеки от ядра (хорошо поляризуемые) Основание Диссоциирует в воде с образованием гидроксил-аниона Акцептор протона в любом растворителе Донор электронов (неподеленной пары или спаренных) «Жесткие» — занятые граничные орбитали близки к ядру (плохо поляризуемые). «Мягкие» — занятые граничные орбитали имеют высокую энергию, относительно далеки от ядра (хорошо поляризуемые) 9

Кислотно-основное взаимодействие по Бренстеду Сопряженная к/о пара +ВН/ В ‥ • АН + В ⇆ − А + + ВН Сопряженная к/о пара АН/А− • Две формы одного и того же соединения, отличающиеся на один протон, называются сопряженной кислотно-основной парой. • Силовой характеристикой сопряженной кислотноосновной пары является р. Ка (р. КВН+) • Чем меньше р. Ка (р. КВН+), тем сильнее кислота и слабее сопряженное ей основание. 10
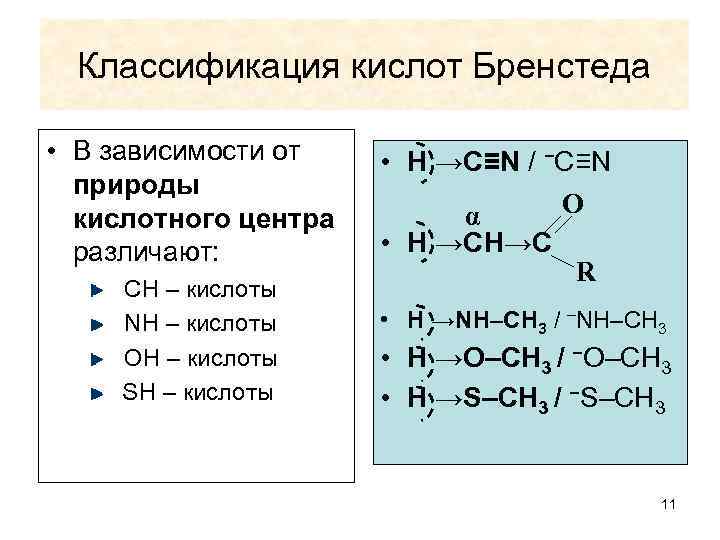
Классификация кислот Бренстеда • В зависимости от природы кислотного центра различают: СН – кислоты NН – кислоты OH – кислоты SН – кислоты • H →C≡N / −C≡N O α • H →CH→C R • H →NH–CH 3 / –NH–CH 3 • H →O–CH 3 / −O–CH 3 • H →S–CH 3 / −S–CH 3 11
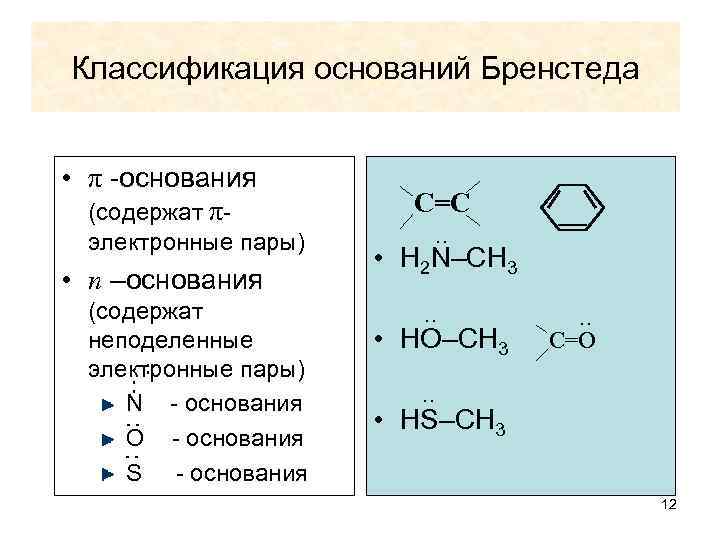
Классификация оснований Бренстеда • π -основания (содержат πэлектронные пары) • n –основания ︰ ︰ (содержат неподеленные ︰ электронные пары) ︰ N - основания O - основания S - основания С=С ‥ • H 2 N–CH 3 ‥ • HO–CH 3 ‥ С=O ‥ • HS–CH 3 12

• • • HCl / Cl− HCOOH / HCOO− C 6 H 5 COOH / C 6 H 5 COO− C 6 H 5 OH / C 6 H 5 O− HOH / HO− C 2 H 5 OH / C 2 H 5 O− p. K a -7, 0 3, 7 4, 2 10, 0 15, 7 18, 0 Увеличивается сила кислот, уменьшается сила сопряженных им оснований Примеры сопряженных кислотноосновных пар АН/А– 13

• • • + ‥ RSH 2 / RSH ‥ + Ar. OH 2 / Ar. OH ‥ + ROH 2 / ROH ‥ + H 3 O / H 2 O ‥ + NH 4 / NH 3 ‥ + CH 3 NH 3 / CH 3 NH 2 + p. KBH - 7, 0 - 6, 0 - 2, 0 - 1, 7 9, 2 10, 6 Увеличивается сила кислот Примеры сопряженных кислотно. . основных пар ВН+/В Сильной кислоте соответствует слабое сопряженное основание и наоборот. 14
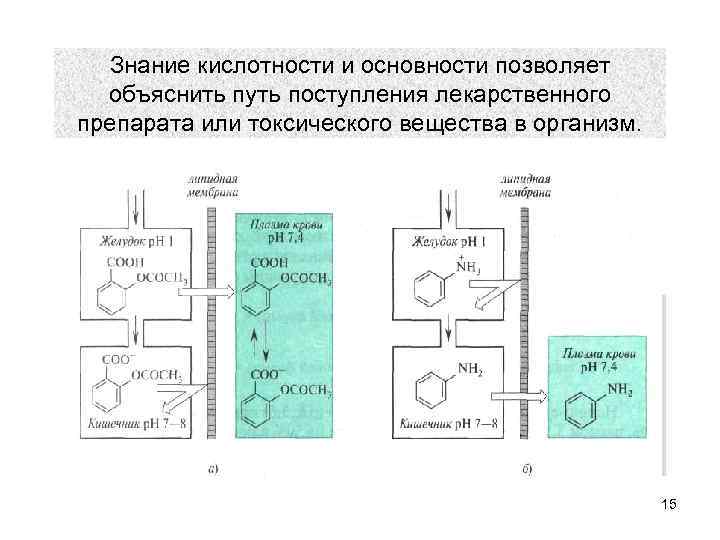
Знание кислотности и основности позволяет объяснить путь поступления лекарственного препарата или токсического вещества в организм. 15

Качественная оценка сравнения силы кислот вида АН • Сила кислот • Стабильность сопряженных анионов • Делокализация заряда Чем стабильнее сопряженный анион, тем сильнее кислота Чем больше делокализован заряд, тем стабильнее анион ü Природа атома в активном центре ü ü (его электроотрицательность и поляризуемость) Участие активного центра в сопряжении Участие АЦ в образовании водородной связи Природа заместителя у активного центра Природа растворителя Факторы делокализации заряда 16

Природа атома в активном центре • Для атомов, стоящих в одном периоде, большее значение имеет электроотрицательность, которая растет слева направо: С < N < O • В этом же ряду будет увеличиваться делокализация заряда: С− < N − < O −, а значит и стабильность соответствующих анионов. 17

Природа атома в активном центре (продолжение) • Для атомов, стоящих в одной группе, большее значение имеет поляризуемость, которая растет сверху вниз: O < S • В этом же ряду будет увеличиваться делокализация заряда: O − < S − , а значит и стабильность соответствующих анионов. • Отсюда вывод: SH-кислоты сильнее ОНкислот, а ОН-кислоты сильнее NH-кислот. 18

Задачи • Расположить в ряд по усилению кислотности метанол, метантиол, метиламин. Решение CH 3 OH/ CH 3 O− CH 3 SH/ CH 3 S− CH 3 NH 2/ CH 3 NH− Сопряженные кислотно-основные пары • Стабильность сопряженных анионов будет увеличиваться в ряду: ЭО П Факторы делокализации CH 3 NH− < CH 3 O− < CH 3 S− • В этом же ряду усиливается и кислотность: CH 3 NH 2 < CH 3 OН < CH 3 SН 19
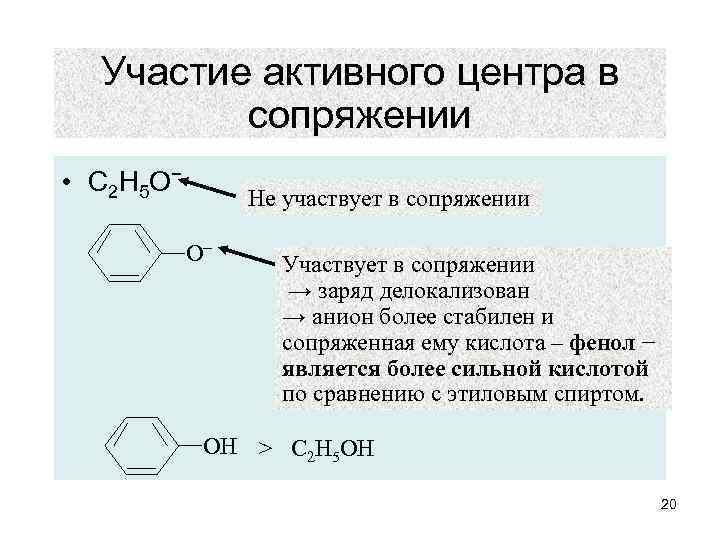
Участие активного центра в сопряжении • С 2 Н 5 О − Не участвует в сопряжении О− Участвует в сопряжении → заряд делокализован → анион более стабилен и сопряженная ему кислота – фенол − является более сильной кислотой по сравнению с этиловым спиртом. ОН > С 2 Н 5 ОН 20
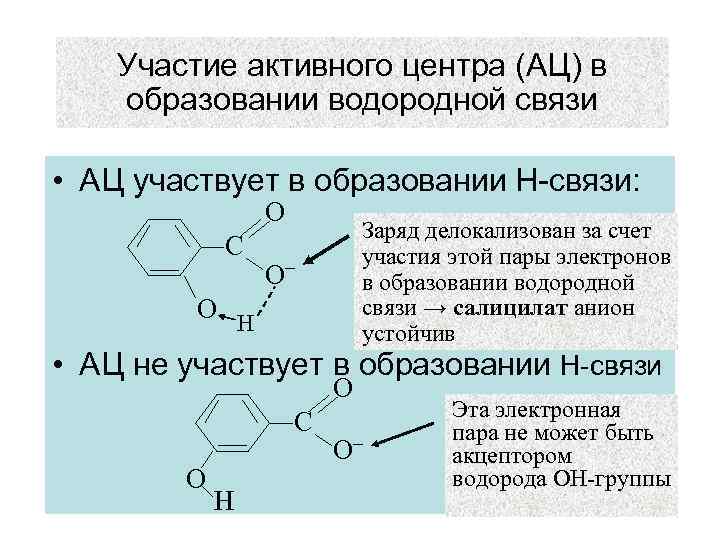
Участие активного центра (АЦ) в образовании водородной связи • АЦ участвует в образовании Н-связи: О С Заряд делокализован за счет участия этой пары электронов в образовании водородной связи → салицилат анион устойчив О− О Н • АЦ не участвует в образовании Н-связи О С О Н О− Эта электронная пара не может быть акцептором водорода ОН-группы 21

Природа заместителя у активного центра • Электроноакцепторные заместители у активного центра усиливают делокализацию заряда и тем самым стабилизируют анион. • Электронодонорные заместители, наоборот, способствуют локализации заряда и дестабилизируют анион. 22
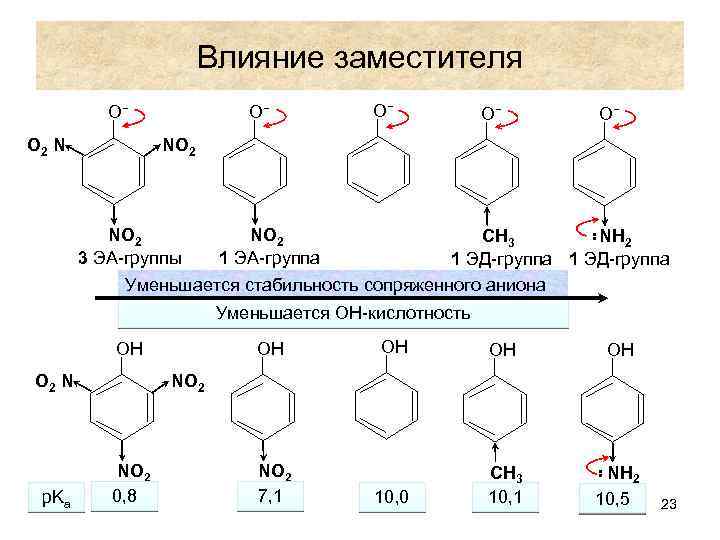
Влияние заместителя О− О 2 N О− О− NО 2 3 ЭА-группы NО 2 1 ЭА-группа ∙∙ СН 3 NН 2 1 ЭД-группа Уменьшается стабильность сопряженного аниона Уменьшается ОН-кислотность ОН О 2 N ОН ОН ОН 10, 0 СН 3 10, 1 NН 2 10, 5 NО 2 0, 8 NО 2 7, 1 ∙∙ p. Ka ОН 23

Природа растворителя • Полярный сольватирующий растворитель способствует гашению (делокализации) заряда аниона и тем самым стабилизирует анион. Поэтому, чем лучше сольватируется анион, тем он более стабилен. СН 3–О− > СН 3–СН–О− > СН 3–С–О− СН 3 Уменьшается сольватируемость аниона и делокализация заряда 24

Качественная оценка сравнения силы ‥ оснований вида В • Принцип: силу оснований Бренстеда принято оценивать по локализации электронной пары в активном центре. • Чем больше локализована электронная пара, тем сильнее основание. • Факторы локализации те же, что и делокализации, только действуют в противоположном направлении. 25
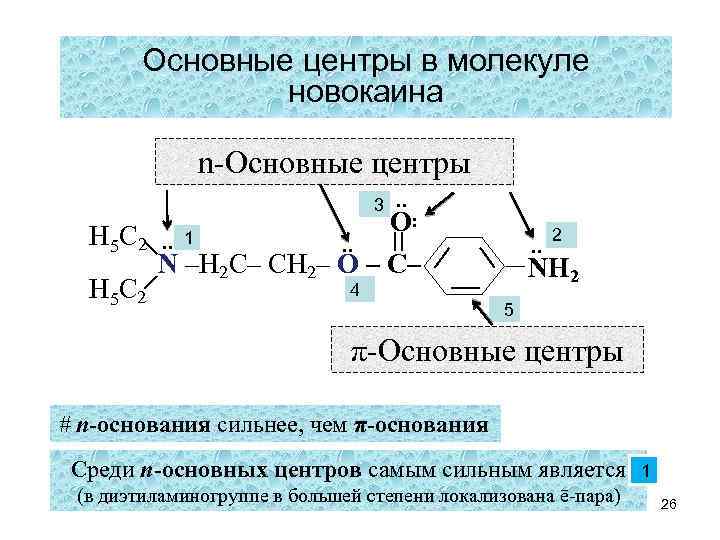
Основные центры в молекуле новокаина n-Основные центры 3 . . О Н 5 С 2. . 1. . N –Н 2 С– СН 2– О – С– 4 Н 5 С 2 . . 2 NH 2 5 π-Основные центры # n-основания сильнее, чем π-основания Среди n-основных центров самым сильным является (в диэтиламиногруппе в большей степени локализована ē-пара) 1 26
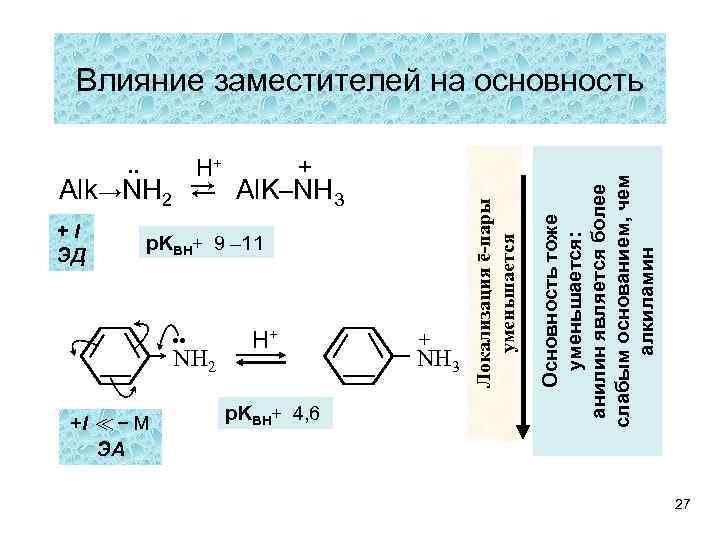
. . Alk→NH 2 ⇄ Al. K–NH 3 +I ЭД H+ p. KBH+ 9 – 11 . . NH 2 +I ≪- M ЭА H+ + Основность тоже уменьшается: анилин является более слабым основанием, чем алкиламин p. KBH+ 4, 6 NH 3 + Локализация ē-пары уменьшается Влияние заместителей на основность 27
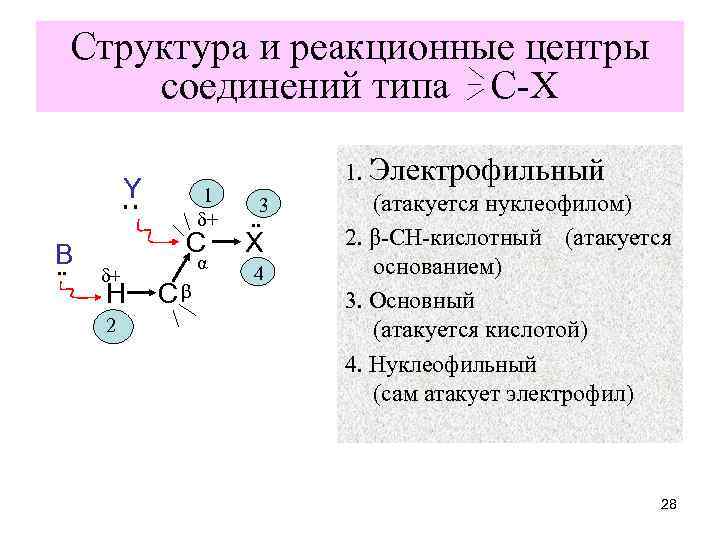
Структура и реакционные центры соединений типа С-Х Y ︰ 1 δ+ B. . С δ+ H 2 α Сβ 3. . Х 4 1. Электрофильный (атакуется нуклеофилом) 2. β-СН-кислотный (атакуется основанием) 3. Основный (атакуется кислотой) 4. Нуклеофильный (сам атакует электрофил) 28

Общие принципы химического поведения – два варианта. . I. Группа Х покидает Сδ+ самопроизвольно (до. . атаки Y). Тогда скорость реакции будет зависеть от концентрации только одного субстрата, и реакция называется мономолекулярной (не зависит от концентрации реагента) 29

. . 2. Группа Х уходит под давлением. . а) со стороны нуклеофильной группы Y по Сδ+ (и будет реакция SN) или . . б) со стороны основания В по β-СН-кислотному центру (и будет реакция элиминирования). В каждом случае скорость реакции зависит от концентраций двух веществ (субстрата и реагента) Такие реакции называется бимолекулярными 30

Мономолекулярные реакции протекают при наличии следующих признаков: v Связь С → Х легко ионизируется (в полярном растворителе с легко поляризуемой группой. . – Х). При этом образуются карбокатион и Х (или Х) ︰ v Образующиеся карбокатион и группа Х – устойчивы (например, третичные субстраты: алкилгалогениды или алкилониевые соли дадут третичн. КК) С С – С → Cl С С + С – С → ОН 2 НSO 4− С 31

Другие условия для мономолекулярных реакций (продолжаем) v. Высокие температуры (все связи хорошо рвутся). . v Атакующая группа Y – слабый нуклеофил или слабое основание (например, Cl− в водном растворе гидратирован, и его заряд за счет этого будет делокализован, частица неактивна) 32
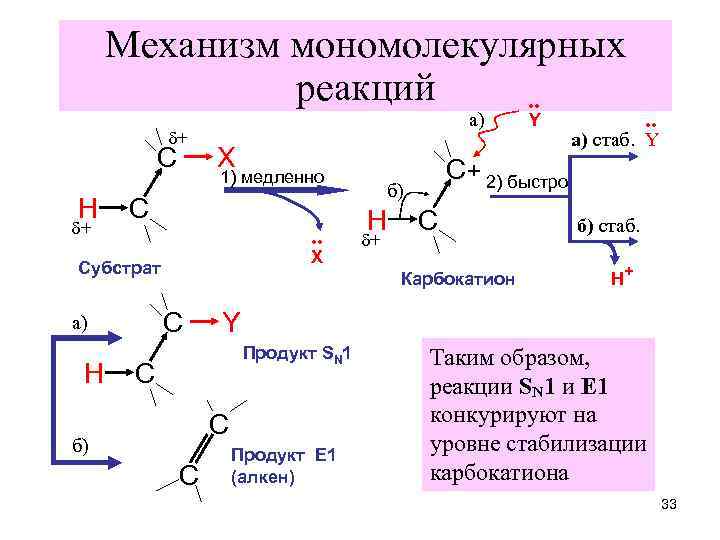
Механизм мономолекулярных реакций. . δ+ С H δ+ а) Х 1) медленно С . . Х Субстрат H б) H δ+ С+ 2) быстро С Карбокатион С а) б) . . а) стаб. Y б) стаб. Н+ Y Продукт SN 1 С С С Y Продукт Е 1 (алкен) Таким образом, реакции SN 1 и E 1 конкурируют на уровне стабилизации карбокатиона 33
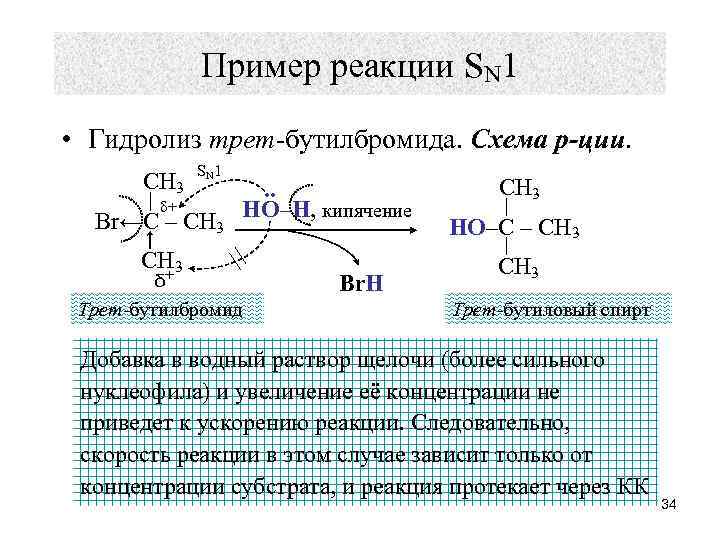
Пример реакции SN 1 • Гидролиз трет-бутилбромида. Схема р-ции. CH 3 S N 1 δ+ Br←C – CH 3 + δ Трет-бутилбромид . . HO–H, кипячение Br. H CH 3 HO–C – CH 3 Трет-бутиловый спирт Добавка в водный раствор щелочи (более сильного нуклеофила) и увеличение её концентрации не приведет к ускорению реакции. Следовательно, скорость реакции в этом случае зависит только от концентрации субстрата, и реакция протекает через КК 34
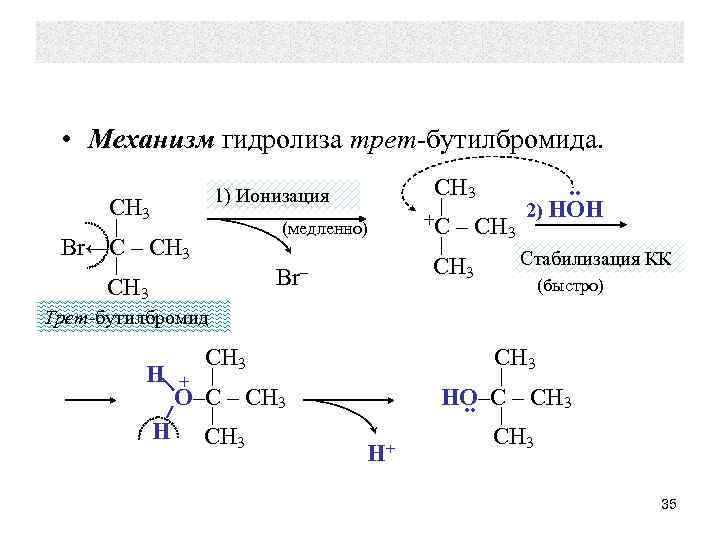
• Механизм гидролиза трет-бутилбромида. CH 3 1) Ионизация CH 3 (медленно) Br←C – CH 3 Br– CH 3 +C . . 2) НОН Стабилизация КК (быстро) Трет-бутилбромид H H CH 3 + О–C – CH 3 H+ НО–C – CH 3. . CH 3 35
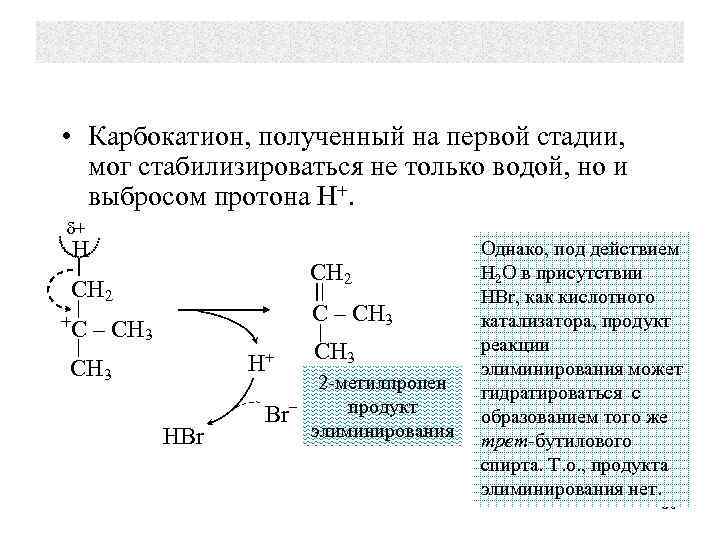
• Карбокатион, полученный на первой стадии, мог стабилизироваться не только водой, но и выбросом протона Н+. δ+ H CH 2 +C C – CH 3 H+ CH 3 HBr Br– CH 3 2 -метилпропен продукт элиминирования Однако, под действием Н 2 О в присутствии НBr, как кислотного катализатора, продукт реакции элиминирования может гидратироваться с образованием того же трет-бутилового спирта. Т. о. , продукта элиминирования нет. 36
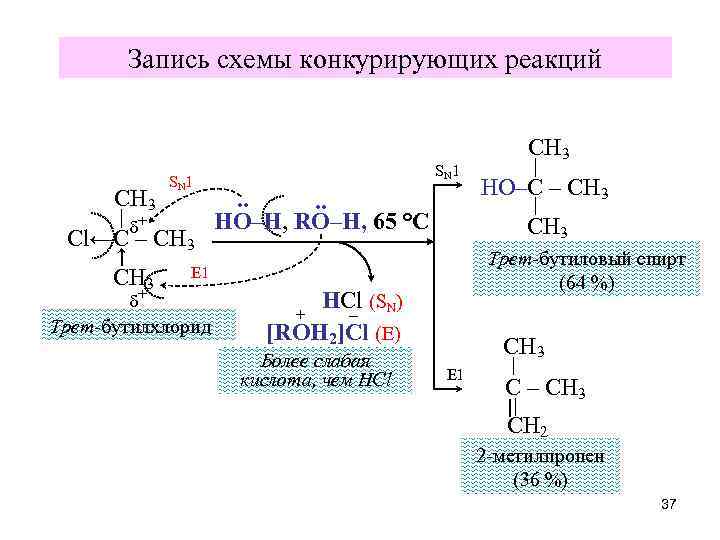
Запись схемы конкурирующих реакций CH 3 S N 1 δ+ Cl←C – CH 3 S N 1 . . HO–H, RO–H, 65 °C Трет-бутилхлорид HO–C – CH 3 Трет-бутиловый спирт (64 %) Е 1 δ+ CH 3 HCl (SN) – [ROH 2]Cl (Е) + Более слабая кислота, чем НCl CH 3 Е 1 C – CH 3 CH 2 2 -метилпропен (36 %) 37
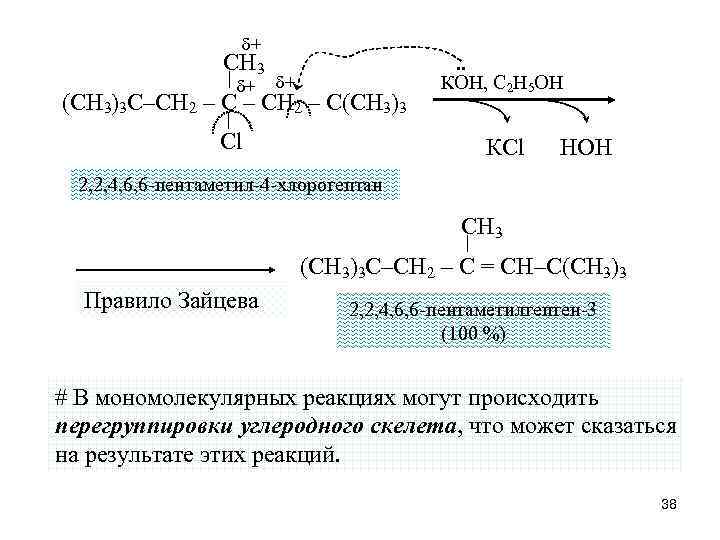
δ+ CН 3 δ+ δ+ (СН 3)3 С–СН 2 – С(СН 3)3 Cl . . КOH, С 2 Н 5 ОН КCl НОН 2, 2, 4, 6, 6 -пентаметил-4 -хлорогептан CН 3 (СН 3)3 С–СН 2 – С = СН–С(СН 3)3 Правило Зайцева 2, 2, 4, 6, 6 -пентаметилгептен-3 (100 %) # В мономолекулярных реакциях могут происходить перегруппировки углеродного скелета, что может сказаться на результате этих реакций. 38

Бимолекулярные реакции имеют место тогда, когда отсутствуют признаки для мономолекулярных, т. е. v Связь С → Х плохо ионизируется (в неполярном растворителе с трудно поляризуемой группой Х). R –CH 2 -Cl ‥ v Карбокатион и (или) группа Х – неустойчивы (у первичных субстратов: алкилгалогенидов + или алкилониевых солей) [R –CH 2 –OH 2] HSO 4 v При низких температурах (когда все связи плохо рвутся). . v Атакующая группа Y –сильный нуклеофил или сильное основание (например, алкоксид-анион) 39
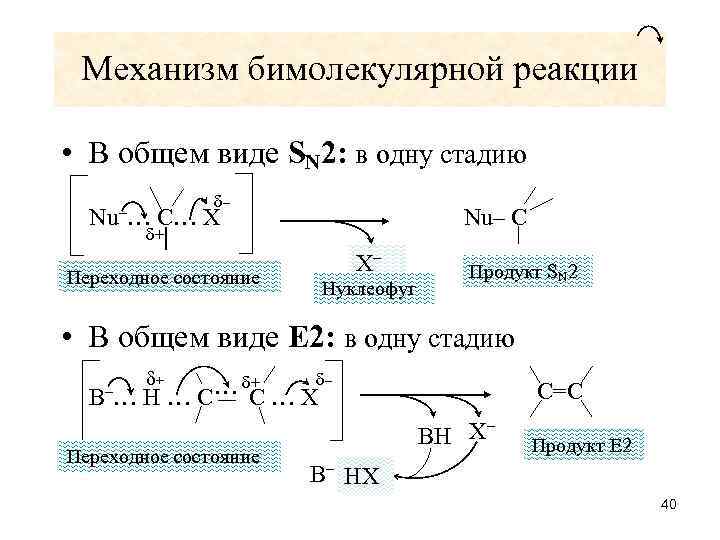
Механизм бимолекулярной реакции • В общем виде SN 2: в одну стадию Nu–… δ– C… X Nu– C δ+ Переходное состояние Х– Нуклеофуг Продукт SN 2 • В общем виде Е 2: в одну стадию В –… δ+ + … δС … Хδ– Н…С Переходное состояние С=С Х– ВН Продукт Е 2 В– НХ 40

• Легкость протекания реакций SN 2 обусловлена относительной стабильностью уходящей группы (нуклеофуга) – и входящей (нуклеофила). • Для осуществления реакции SN 2 необходимо, чтобы уходящая нуклеофильная группа (нуклеофуг) была стабильнее входящей. 41

Реакции SN 2 у Сsp 3 • Примером реакции SN 2 у Сsp 3 может служить взаимодействие алкилгалогенидов с алкоксидами, приводящее к образованию простых эфиров. • Схема реакции SN 2: δ+ СН 3 – СН 2→ Br + + – Na. OCH 2 – CH 3 НОС 3 Н 7 + – Na. Br СН 3 – СН 2 – ОСН 2 – СН 3 Здесь устойчивость Вr– > C 3 H 7 O– В обратном направлении реакция будет невозможна 42
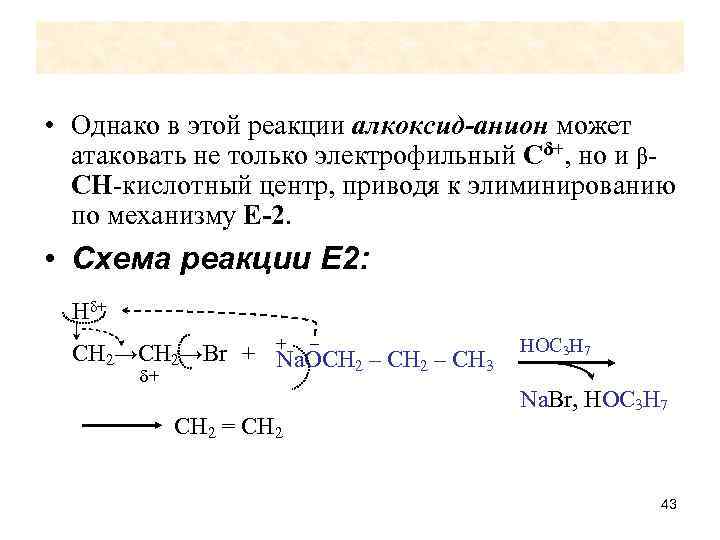
• Однако в этой реакции алкоксид-анион может атаковать не только электрофильный Сδ+, но и βСН-кислотный центр, приводя к элиминированию по механизму Е-2. • Схема реакции Е 2: Нδ+ – СН 2→Br + + Na. OCH 2 – CH 3 δ+ СН 2 = СН 2 НОС 3 Н 7 Na. Br, НОС 3 Н 7 43
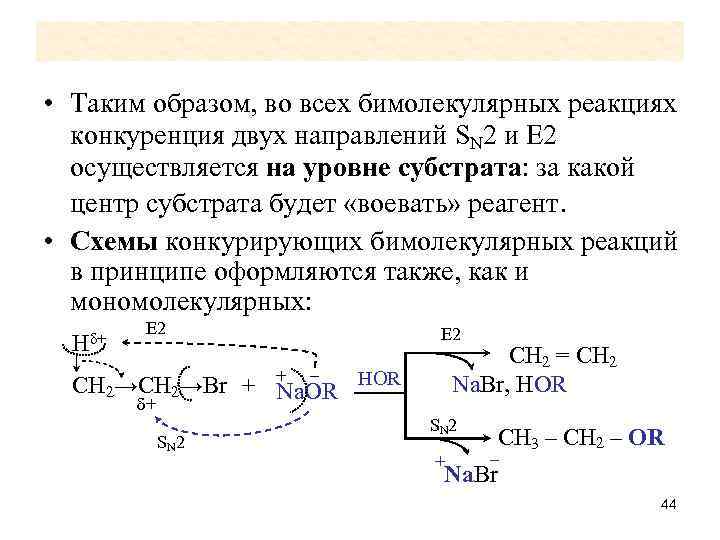
• Таким образом, во всех бимолекулярных реакциях конкуренция двух направлений SN 2 и Е 2 осуществляется на уровне субстрата: за какой центр субстрата будет «воевать» реагент. • Схемы конкурирующих бимолекулярных реакций в принципе оформляются также, как и мономолекулярных: Нδ+ E 2 СН 2 = СН 2 Na. Br, НОR – НОR СН 2→Br + + Na. OR δ+ SN 2 + СН 3 – СН 2 – ОR – Na. Br 44

Хорошие уходящие группы • Хорошими уходящими группами являются: Ø Cl-, Br-, IØ N≡N Ø группы, стабилизированные сопряжением -О– СН=СН, -О–С Н , −OSO R 6 5 2 Эти группы уходят под натиском любых нуклеофилов и сильных оснований без использования каких-либо особых приемов. 45

Плохие уходящие группы • Плохими уходящими группами являются: Ø -ОН, -ОR Ø -NH 2, -NHR, -NR 2 Их удается вывести из субстратов только при использовании катализаторов (Н+, Zn. Cl 2), которые превращают плохие уходящие группы в хорошие. SH, SR группы не удается вытеснить в обычных условиях из-за прочности связи C–S. 46

Подвижность ОН групп в реакциях SN у спиртов – на ЛЗ • Проба Лукаса. Суть: действуют НСl на спирты в присутствии кислоты Льюиса Zn. Cl 2. Это позволяет различать первичные, вторичные и третичные спирты. • У третичных спиртов нуклеофильная ОН группа легче замещается на Сl–, чем у вторичных спиртов (в первом случае реакция протекает моментально, а во втором случае продукт обнаружится только через 5 минут). У первичных спиртов эта реакция не идет без нагревания. 47

Подвижность ОН групп в реакциях Е у спиртов • Реакции элиминирования у первичных, вторичных и третичных спиртов протекают в присутствии Н 2 SO 4 конц, но у третичных спиртов они протекают в более мягких условиях (меньше температура, меньше концентрация кислоты), чем у вторичных и первичных. • Серная кислота необходима для превращения плохой уходящей группы ОН в хорошую НОН и используется как водоотнимающее средство. 48
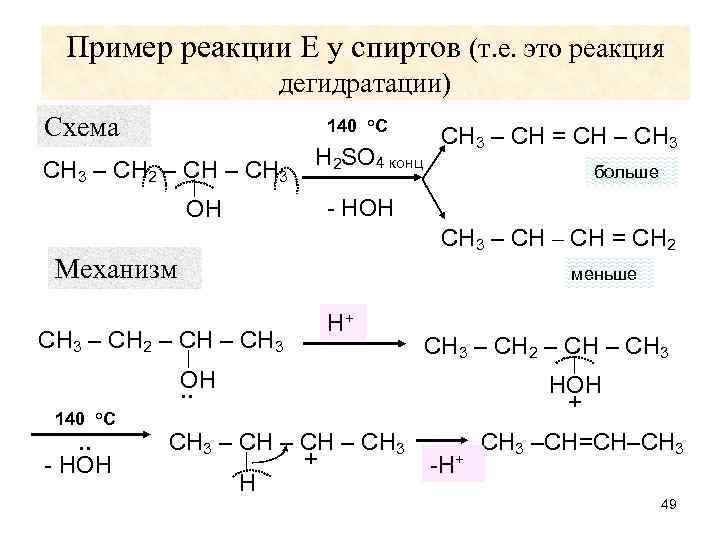
Пример реакции Е у спиртов (т. е. это реакция дегидратации) Схема 140 °С СН 3 – СН 2 – СН 3 ОН Н 2 SO 4 конц СН 3 – СН = СН – СН 3 больше - НОН СН 3 – СН = СН 2 Механизм меньше СН 3 – СН 2 – СН 3 Н+ СН 3 – СН 2 – СН 3 ОН. . 140 °С . . - НОН СН 3 – СН 3 + Н НОН + -Н+ СН 3 –СН=СН–СН 3 49

Выбор направления и механизма реакции Выбор преимущественного направления реакции (SN или Е) у Сsp 3 в спиртах и их механизм определяются не только строением спирта и реагента, но и: • Соотношением спирта и Н 2 SO 4. – При избытке спирта образуется простой эфир по механизму SN 2 (у перв. спиртов) или по механизму SN 1 (у трет. спиртов). – При избытке Н 2 SO 4 конц. произойдет дегидратация спирта с образованием алкена по механизму Е 1 • Температурой. Высокие температуры также способствуют дегидратации спирта (даже первичного при 170 °С) с образованием алкена по механизму Е 1. 50

Основные выводы • Соединения типа С–Х могут проявлять кислотные, основные и нуклеофильные свойства • Соединения типа С–Х могут вступать в реакции нуклеофильного замещения и элиминирования. • Механизм и направление реакций зависит от природы субстрата и реагента, температуры, природы растворителя. 51

Литература Основная: • Слесарев В. И. – Химия: Основы химии живого: Учебник для вузов. – 3 -е изд. , испр. – СПб: Химиздат. – 2007. – 784 с. • Тюкавкина Н. А. , Бауков Ю. И. – Биоорганическая химия : Учебник. – М. : ДРОФА. – 2006. – С. 100 – 115, , 149 – 159, 167 – 181. 52

Литература дополнительная: • Грандберг И. И. – Органическая химия: Учеб. Для студ. вузов, обучающихся по агроном. спец. – 5 -е изд. – М. : Дрофа, 2002. – 672 с. • Пузаков С. А. – Химия: Учебник, 2 -е изд. испр. и доп. М. : ГЭОТАР-Медиа Медицина, - 2006. – 630 с. 53

Литература электронные ресурсы: • Электронная библиотека Т. 12. Органическая химия. /гл. ред. М. А. Пальцев. -М. : Русский врач, 2005 • Электронная библиотека Colibris • Электронный каталог Крас ГМУ • Ресурсы Интернет 54
Лекция 6 РеакцСоедОднойОдновалентФункцБОХ _ЛЕЧ.ppt