Щелочные.Ме.pptx
- Количество слайдов: 58
 Кадета: Гофман С
Кадета: Гофман С
 Лирическое отступление Применение щелочных металлов в жизни homo sapiens
Лирическое отступление Применение щелочных металлов в жизни homo sapiens

 Металл (название происходит от лат. metallum — шахта) — группа элементов, обладающая характерными металлическими свойствами, такими как: высокая тепло- и электропроводность положительный температурный коэффициент сопротивления высокая пластичность и др.
Металл (название происходит от лат. metallum — шахта) — группа элементов, обладающая характерными металлическими свойствами, такими как: высокая тепло- и электропроводность положительный температурный коэффициент сопротивления высокая пластичность и др.

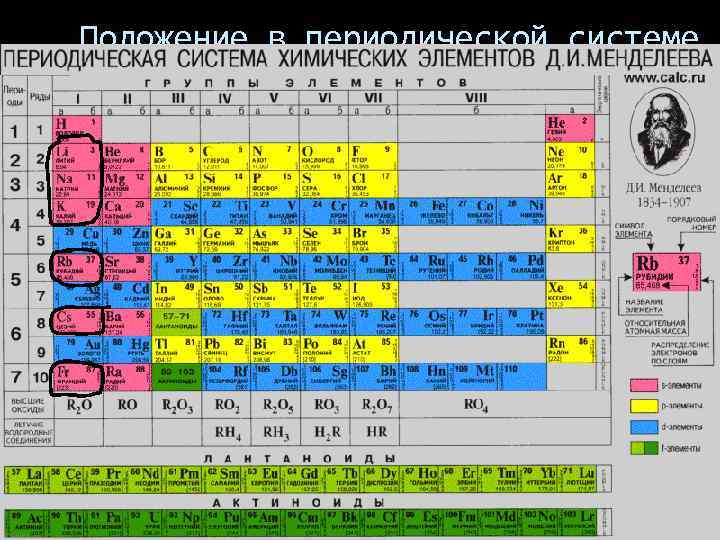 Положение в периодической системе химических элементов Д. И. Менделеева
Положение в периодической системе химических элементов Д. И. Менделеева

 Щелочные металлы — элементы главной подгруппы I группы Периодической системы химических элементов Д. И. Менделеева: литий Li, натрий Na, калий K, рубидий Rb, цезий Cs и франций Fr.
Щелочные металлы — элементы главной подгруппы I группы Периодической системы химических элементов Д. И. Менделеева: литий Li, натрий Na, калий K, рубидий Rb, цезий Cs и франций Fr.
 Эти металлы получили название щелочных, потому что большинство их соединений растворимо в воде. По-славянски «выщелачивать» означает «растворять» , это и определило название данной группы металлов.
Эти металлы получили название щелочных, потому что большинство их соединений растворимо в воде. По-славянски «выщелачивать» означает «растворять» , это и определило название данной группы металлов.
 При растворении щелочных металлов в воде образуются растворимые гидроксиды, называемые щёлочами. Здесь они представлены в твердом агрегатном состоянии Гидроксида лития Li. OH Гидроксид калия KOH Гидроксид натрия Na. OH
При растворении щелочных металлов в воде образуются растворимые гидроксиды, называемые щёлочами. Здесь они представлены в твердом агрегатном состоянии Гидроксида лития Li. OH Гидроксид калия KOH Гидроксид натрия Na. OH
 Литий История и происхождение названия Литий был открыт в 1817 году шведским химиком А. Арфведсоном сначала в минерале петалите, а затем в сподумене и в лепидолите. Металлический литий впервые получил Хамфри Дэви в 1825 году. Своё название литий получил из-за того, что был обнаружен в «камнях» . Первоначально назывался «литион» , современное название было предложено Берцелиусом.
Литий История и происхождение названия Литий был открыт в 1817 году шведским химиком А. Арфведсоном сначала в минерале петалите, а затем в сподумене и в лепидолите. Металлический литий впервые получил Хамфри Дэви в 1825 году. Своё название литий получил из-за того, что был обнаружен в «камнях» . Первоначально назывался «литион» , современное название было предложено Берцелиусом.

 Литий элемент главной подгруппы первой группы, второго периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 3. Физические свойства Литий Цвет Серебристо-белый Блеск Имеет характерный металлический блеск Плотность 0, 534 г/см³ Теплопроводность 84, 8 Вт/(м·K) Температура плавления 2, 89 к. Дж/моль
Литий элемент главной подгруппы первой группы, второго периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 3. Физические свойства Литий Цвет Серебристо-белый Блеск Имеет характерный металлический блеск Плотность 0, 534 г/см³ Теплопроводность 84, 8 Вт/(м·K) Температура плавления 2, 89 к. Дж/моль
 Химические свойства Щелочной металл, неустойчив на воздухе. Литий является наименее активным щелочным металлом, с сухим воздухом (и даже с сухим кислородом) при комнатной температуре практически не реагирует. Спокойно, без взрыва и возгорания, реагирует с водой, образуя Li. OH и H 2 По состоянию на конец 2007 − начало 2008 года цены на металлический литий 99 % составляют 63 долларов за 1 кг.
Химические свойства Щелочной металл, неустойчив на воздухе. Литий является наименее активным щелочным металлом, с сухим воздухом (и даже с сухим кислородом) при комнатной температуре практически не реагирует. Спокойно, без взрыва и возгорания, реагирует с водой, образуя Li. OH и H 2 По состоянию на конец 2007 − начало 2008 года цены на металлический литий 99 % составляют 63 долларов за 1 кг.
 Натрий История и происхождение названия Название «натрий» (natrium) происходит от арабского натрун (по-гречески — nitron) и первоначально относилось к природной соде. Сам элемент ранее именовался содием (лат. Sodium). Натрий использовался с давних времён. Природную соду(натрон) древние египтяне использовали для бальзамирования, отбеливания холста, при варке пищи, изготовлении красок и глазурей. Натрий впервые был получен английским химиком Хемфри Дэви в 1807 году электролизом твердого Na. OH.
Натрий История и происхождение названия Название «натрий» (natrium) происходит от арабского натрун (по-гречески — nitron) и первоначально относилось к природной соде. Сам элемент ранее именовался содием (лат. Sodium). Натрий использовался с давних времён. Природную соду(натрон) древние египтяне использовали для бальзамирования, отбеливания холста, при варке пищи, изготовлении красок и глазурей. Натрий впервые был получен английским химиком Хемфри Дэви в 1807 году электролизом твердого Na. OH.
 Внешний вид простого вещества Порошок натрия
Внешний вид простого вещества Порошок натрия
 НАТРИЙ — ЭЛЕМЕНТ ГЛАВНОЙ ПОДГРУППЫ I ГРУППЫ, III ПЕРИОДА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА, С АТОМНЫМ НОМЕРОМ 11. Физические свойства Натрий Цвет серебристо-белый Блеск Характерный металлический Плотность 0, 971 г/см³ Температура плавления 2, 64 к. Дж/моль Теплопроводность 142, 0 Вт/(м·K)
НАТРИЙ — ЭЛЕМЕНТ ГЛАВНОЙ ПОДГРУППЫ I ГРУППЫ, III ПЕРИОДА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА, С АТОМНЫМ НОМЕРОМ 11. Физические свойства Натрий Цвет серебристо-белый Блеск Характерный металлический Плотность 0, 971 г/см³ Температура плавления 2, 64 к. Дж/моль Теплопроводность 142, 0 Вт/(м·K)
 Щелочной металл, на воздухе легко окисляется. Для защиты от кислорода воздуха металлический натрий хранят под слоем керосина. Натрий менее активный чем литий, поэтому с азотом реагирует только при нагревании: 2 Na + 3 N 2=2 Na. N 3 При большом избытке кислорода образуется пероксид натрия 2 Na + O 2 = Na 2 O 2
Щелочной металл, на воздухе легко окисляется. Для защиты от кислорода воздуха металлический натрий хранят под слоем керосина. Натрий менее активный чем литий, поэтому с азотом реагирует только при нагревании: 2 Na + 3 N 2=2 Na. N 3 При большом избытке кислорода образуется пероксид натрия 2 Na + O 2 = Na 2 O 2
 Интервью натрия =) Незримо бываю я в вашей тарелке, Я в соли и в соде, а сам я – металл. И жёлтым окрашу я пламя горелки, Когда попадёт туда соли кристалл. Я – Натрий, металл щелочной и активный, В воде я взорвусь, запылаю огнем! И хоть я опасный и нравом противный, Я мягок и режусь обычным ножом!
Интервью натрия =) Незримо бываю я в вашей тарелке, Я в соли и в соде, а сам я – металл. И жёлтым окрашу я пламя горелки, Когда попадёт туда соли кристалл. Я – Натрий, металл щелочной и активный, В воде я взорвусь, запылаю огнем! И хоть я опасный и нравом противный, Я мягок и режусь обычным ножом!
 Калий История и происхождение названия В 1807 году английский химик Дэви электролизом расплава едкого калия (KOH) выделил калий и назвал его «потассий» (это название до сих пор употребительно в английском, французском, испанском, португальском и польском языках). В 1809 году Л. В. Гильберт предложил название «калий» (лат. kalium, от араб. аль -кали — поташ).
Калий История и происхождение названия В 1807 году английский химик Дэви электролизом расплава едкого калия (KOH) выделил калий и назвал его «потассий» (это название до сих пор употребительно в английском, французском, испанском, португальском и польском языках). В 1809 году Л. В. Гильберт предложил название «калий» (лат. kalium, от араб. аль -кали — поташ).

 Калий химический элемент I группы периодической системы Менделеева; атомный номер 19, атомная масса 39, 098 Физические свойства Калий Цвет Серебристо-белый Блеск Имеет характерный металлический блеск Плотность 0, 856 г/см³ Теплопроводность 79, 0 Вт/(м·K) Температура плавления 102, 5 к. Дж/моль
Калий химический элемент I группы периодической системы Менделеева; атомный номер 19, атомная масса 39, 098 Физические свойства Калий Цвет Серебристо-белый Блеск Имеет характерный металлический блеск Плотность 0, 856 г/см³ Теплопроводность 79, 0 Вт/(м·K) Температура плавления 102, 5 к. Дж/моль
 Калий проявляет типичные металлические свойства и очень химически активен, является сильным восстановителем. Хранить его необходимо под слоем бензина или керосина.
Калий проявляет типичные металлические свойства и очень химически активен, является сильным восстановителем. Хранить его необходимо под слоем бензина или керосина.
 Взаимодействие с водородом Взаимодействие с кислородом Взаимодействие с водой, кислотами НО. . Это Друзья мои, далеко не всё и наш журнал не резиновый и не позволяет вместить все хим. св-ва калия и др. щелочных металлов.
Взаимодействие с водородом Взаимодействие с кислородом Взаимодействие с водой, кислотами НО. . Это Друзья мои, далеко не всё и наш журнал не резиновый и не позволяет вместить все хим. св-ва калия и др. щелочных металлов.
 Калий, как и другие щелочные металлы, получают электролизом расплавленных хлоридов или щелочей. Чаще проводят электролиз расправленных щелочей с добавкой к ним соды или поташа.
Калий, как и другие щелочные металлы, получают электролизом расплавленных хлоридов или щелочей. Чаще проводят электролиз расправленных щелочей с добавкой к ним соды или поташа.
 Цезий История открытия Цезий был открыт в 1860 году немецкими учёными Р. В. Бунзеном и Г. Р. Кирхгофом в водах Дюрхгеймского минерального источника в Германии методом оптической спектроскопии, тем самым, став первым элементом, открытым при помощи спектрального анализа. В чистом виде цезий впервые был выделен в 1882 году шведским химиком К. Сеттербергом при электролизе расплава смеси цианида цезия и бария.
Цезий История открытия Цезий был открыт в 1860 году немецкими учёными Р. В. Бунзеном и Г. Р. Кирхгофом в водах Дюрхгеймского минерального источника в Германии методом оптической спектроскопии, тем самым, став первым элементом, открытым при помощи спектрального анализа. В чистом виде цезий впервые был выделен в 1882 году шведским химиком К. Сеттербергом при электролизе расплава смеси цианида цезия и бария.

 элемент Це зий лемент главной подгруппы первой э периодической системы группы шестого периода периодической системы химических элементов Д. И. Менделеева, Д. И. Менделеева атомный номер 55. Обозначается символом Cs Физические свойства Цезий Цвет серебристо-жёлтый похожий на золото Блеск Характерный металлический Плотность 1, 873 г/см³ Теплопроводность 35, 9 Вт/(м·K) Температура плавления 2, 09 к. Дж/моль
элемент Це зий лемент главной подгруппы первой э периодической системы группы шестого периода периодической системы химических элементов Д. И. Менделеева, Д. И. Менделеева атомный номер 55. Обозначается символом Cs Физические свойства Цезий Цвет серебристо-жёлтый похожий на золото Блеск Характерный металлический Плотность 1, 873 г/см³ Теплопроводность 35, 9 Вт/(м·K) Температура плавления 2, 09 к. Дж/моль
 Цезий является наиболее химически активным металлом. Вступает в реакцию с кислородом О 2 , образуя Cs. O 2. Цезий вступает в реакцию со льдом , простыми спиртами, галогенидами тяжёлых металлов, кислотами, сухим льдом (взаимодействие протекает с сильным взрывом).
Цезий является наиболее химически активным металлом. Вступает в реакцию с кислородом О 2 , образуя Cs. O 2. Цезий вступает в реакцию со льдом , простыми спиртами, галогенидами тяжёлых металлов, кислотами, сухим льдом (взаимодействие протекает с сильным взрывом).
 Методы получения При промышленном получении цезий в виде соединений извлекается из минерала поллуцита. Это делается хлоридным или сульфатным вскрытием. Существует несколько лабораторных методов получения цезия. Он может быть получен: нагревом в вакууме смеси хромата или дихромата цезия с цирконием; разложением азида цезия в вакууме; нагревом смеси хлорида цезия и специально подготовленного кальция
Методы получения При промышленном получении цезий в виде соединений извлекается из минерала поллуцита. Это делается хлоридным или сульфатным вскрытием. Существует несколько лабораторных методов получения цезия. Он может быть получен: нагревом в вакууме смеси хромата или дихромата цезия с цирконием; разложением азида цезия в вакууме; нагревом смеси хлорида цезия и специально подготовленного кальция
 Рубидий История открытия В 1861 году немецкие учёные Роберт Вильгельм Бунзен и Густав Роберт Кирхгоф, изучая с помощью спектрального анализа природные алюмосиликаты, обнаружили в них новый элемент, впоследствии названный рубидием по цвету наиболее сильных линий спектра.
Рубидий История открытия В 1861 году немецкие учёные Роберт Вильгельм Бунзен и Густав Роберт Кирхгоф, изучая с помощью спектрального анализа природные алюмосиликаты, обнаружили в них новый элемент, впоследствии названный рубидием по цвету наиболее сильных линий спектра.
 Вид простого вещества.
Вид простого вещества.
 элемент периодической системы химических элементов Д. И. Менделеева атомным номером Физические свойства Рубидий Цвет серебристо-белый металл Блеск Характерный металлический Плотность 1, 532 г/cм³ Теплопроводность 58, 2 Вт/(м·K) Температура плавления 312, 2 K
элемент периодической системы химических элементов Д. И. Менделеева атомным номером Физические свойства Рубидий Цвет серебристо-белый металл Блеск Характерный металлический Плотность 1, 532 г/cм³ Теплопроводность 58, 2 Вт/(м·K) Температура плавления 312, 2 K
 Щелочной металл, крайне неустойчив на воздухе (реагирует с воздухом в присутствии следов воды с воспламенением). Образует все виды солей — большей частью легкорастворимые.
Щелочной металл, крайне неустойчив на воздухе (реагирует с воздухом в присутствии следов воды с воспламенением). Образует все виды солей — большей частью легкорастворимые.
 Большую часть добываемого рубидия получают как побочный продукт при производстве лития из лепидолита. После выделения лития в виде карбоната или гидроксида рубидий осаждают из маточных растворов. Смесь разделяют многократной перекристаллизацией. Можно извлекать рубидий и из технологических растворов, образующихся при получении глинозёма из нефелина.
Большую часть добываемого рубидия получают как побочный продукт при производстве лития из лепидолита. После выделения лития в виде карбоната или гидроксида рубидий осаждают из маточных растворов. Смесь разделяют многократной перекристаллизацией. Можно извлекать рубидий и из технологических растворов, образующихся при получении глинозёма из нефелина.
 Франций История открытия Этот элемент был предсказан Д. И. Менделеевым (как Эка-цезий), и был открыт (по его радиоактивности) в 1939 г. Маргаритой Пере, сотрудницей Института радия в Париже. Она же дала ему в 1964 г. название в честь своей родины — Франции.
Франций История открытия Этот элемент был предсказан Д. И. Менделеевым (как Эка-цезий), и был открыт (по его радиоактивности) в 1939 г. Маргаритой Пере, сотрудницей Института радия в Париже. Она же дала ему в 1964 г. название в честь своей родины — Франции.
 Фра нций — элемент главной подгруппы первой группы седьмого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 87. Обозначается символом Fr. Радиоактивный щелочной металл, обладающий высокой химической активностью.
Фра нций — элемент главной подгруппы первой группы седьмого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 87. Обозначается символом Fr. Радиоактивный щелочной металл, обладающий высокой химической активностью.
 Физические свойства Франций Цвет Не имеет, т. к. радиоактивный щелочной металл Блеск Характерный Плотность 1, 87 г/см³ Температура плавления ~ 2 к. Дж/моль Теплопроводность n/a Вт/(м·K)
Физические свойства Франций Цвет Не имеет, т. к. радиоактивный щелочной металл Блеск Характерный Плотность 1, 87 г/см³ Температура плавления ~ 2 к. Дж/моль Теплопроводность n/a Вт/(м·K)
 • Франций похож по свойствам на цезий. Всегда сокристаллизуется с его соединениями. Так как в распоряжении исследователей имеются лишь мельчайшие образцы, содержащие не более 10− 7 г франция, то сведения о его свойствах известны с достаточно большой погрешностью, однако они все время уточняются. Методы получения Микроскопические количества франция-223 и франция-224 могут быть химически выделены из минералов урана и тория. Другие изотопы франция получают искусственным путём с помощью ядерных реакций.
• Франций похож по свойствам на цезий. Всегда сокристаллизуется с его соединениями. Так как в распоряжении исследователей имеются лишь мельчайшие образцы, содержащие не более 10− 7 г франция, то сведения о его свойствах известны с достаточно большой погрешностью, однако они все время уточняются. Методы получения Микроскопические количества франция-223 и франция-224 могут быть химически выделены из минералов урана и тория. Другие изотопы франция получают искусственным путём с помощью ядерных реакций.
 Лирическое отступление
Лирическое отступление


 Zzz…водоро д …гелий…
Zzz…водоро д …гелий…


 Применение щелочных металлов в жизни homo sapiens
Применение щелочных металлов в жизни homo sapiens
 Литий используется при производстве литиевых аккумуляторов, такие аккумуляторы применяются в кардиостимуляторах.
Литий используется при производстве литиевых аккумуляторов, такие аккумуляторы применяются в кардиостимуляторах.
 Пары натрия используются в люминесцентных светильниках. Натрий используется при производстве калия, титана, циркония и тантала, а также тетраэтилсвинца – добавки, улучшающей детонационные свойства бензина. Натрий служит катализатором в производстве каучука.
Пары натрия используются в люминесцентных светильниках. Натрий используется при производстве калия, титана, циркония и тантала, а также тетраэтилсвинца – добавки, улучшающей детонационные свойства бензина. Натрий служит катализатором в производстве каучука.
 Расплавы натрия и калия используются в качестве теплоносителей в атомных реакторах и в авиационных двигателях. Авиационный двигатель
Расплавы натрия и калия используются в качестве теплоносителей в атомных реакторах и в авиационных двигателях. Авиационный двигатель
 Гидроксид калия применяется для получения жидкого мыла и стекла. Гидроксид натрия используется для производства бумаги, искусственных тканей, мыла, очистки нефтепроводов, в производстве искусственного волокна и в щелочных аккумуляторах.
Гидроксид калия применяется для получения жидкого мыла и стекла. Гидроксид натрия используется для производства бумаги, искусственных тканей, мыла, очистки нефтепроводов, в производстве искусственного волокна и в щелочных аккумуляторах.
 Нитрат калия – комплексное минеральное удобрение, применяется для производства черного пороха и фейерверков. Цезий нашел применение в фотоэлементах.
Нитрат калия – комплексное минеральное удобрение, применяется для производства черного пороха и фейерверков. Цезий нашел применение в фотоэлементах.

 По содержанию в организме человека натрий (0, 08%) и калий (0, 23%) относятся к макроэлементам, остальные – литий (10 -4%), рубидий (10 -5 %) и цезий (10 -4%) – микроэлементам. Щелочные металлы в виде различных соединений входят в состав тканей животных и человека. Натрий и калий – жизненно необходимые элементы, постоянно содержатся в организме, участвуют в обмене веществ. Литий, рубидий, цезий – также постоянно содержатся в организме, однако физиологическая и биохимическая роль их мало выяснена.
По содержанию в организме человека натрий (0, 08%) и калий (0, 23%) относятся к макроэлементам, остальные – литий (10 -4%), рубидий (10 -5 %) и цезий (10 -4%) – микроэлементам. Щелочные металлы в виде различных соединений входят в состав тканей животных и человека. Натрий и калий – жизненно необходимые элементы, постоянно содержатся в организме, участвуют в обмене веществ. Литий, рубидий, цезий – также постоянно содержатся в организме, однако физиологическая и биохимическая роль их мало выяснена.
 В организме человека… Совместно с калием натрий выполняет следующие функции: Создание условий для возникновения мембранного потенциала и мышечных сокращений. Поддержание осмотической концентрации крови. Поддержание кислотно-щелочного баланса. Нормализация водного баланса. Обеспечение мембранного транспорта. Активация многих энзимов. Рекомендуемая доза натрия составляет для детей от 600 до 1700 миллиграмм, для взрослых от 1200 до 2300 миллиграмм.
В организме человека… Совместно с калием натрий выполняет следующие функции: Создание условий для возникновения мембранного потенциала и мышечных сокращений. Поддержание осмотической концентрации крови. Поддержание кислотно-щелочного баланса. Нормализация водного баланса. Обеспечение мембранного транспорта. Активация многих энзимов. Рекомендуемая доза натрия составляет для детей от 600 до 1700 миллиграмм, для взрослых от 1200 до 2300 миллиграмм.
 Калий — важнейший биогенный элемент, особенно в растительном мире. При недостатке калия в почве растения развиваются очень плохо, уменьшается урожай, поэтому около 90 % добываемых солей калия используют в качестве удобрений.
Калий — важнейший биогенный элемент, особенно в растительном мире. При недостатке калия в почве растения развиваются очень плохо, уменьшается урожай, поэтому около 90 % добываемых солей калия используют в качестве удобрений.
 Щелочные металлы играют ОГРОМНУЮ роль в жизни человека, как в производстве, так и в организме.
Щелочные металлы играют ОГРОМНУЮ роль в жизни человека, как в производстве, так и в организме.



