1 Качественный анализ.ppt
- Количество слайдов: 21

Качественный анализ Часть 1 Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016

Техника безопасности Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016

Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016

Что такое качественный анализ? Качественный анализ – это идентификация (обнаружение) компонентов анализируемых веществ и материалов и оценка их количества Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016

Аналитическая реакция - это реакция, которая сопровождается каким-либо внешним эффектом (образование или растворение осадка, выделение газа, изменение окраски раствора и т. д. ), позволяющим сделать вывод о наличии или отсутствии соответствующих ионов или молекул в анализируемом веществе Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016

Реакции ионного обмена Ba. Cl 2 + Na 2 SO 4 = Ba. SO 4↓ + 2 Na. Cl Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016
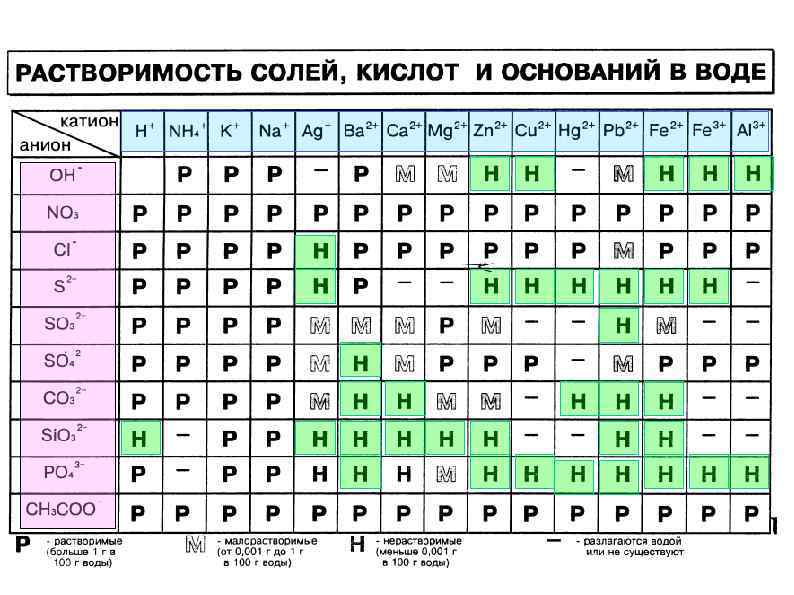
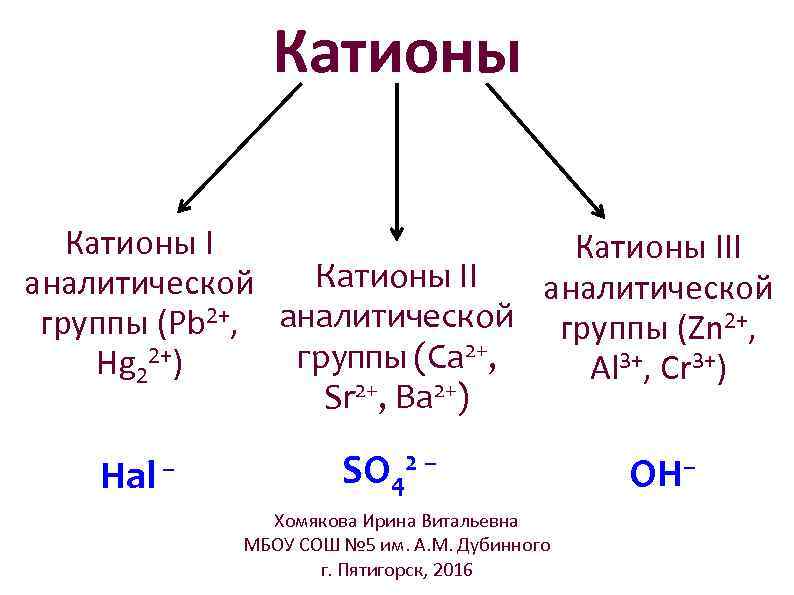
Катионы II аналитической группы (Pb 2+, аналитической группы (Zn 2+, 2+) группы (Ca 2+, Hg 2 Al 3+, Cr 3+) Sr 2+, Ba 2+) Hal – SO 42 – Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016 OH–
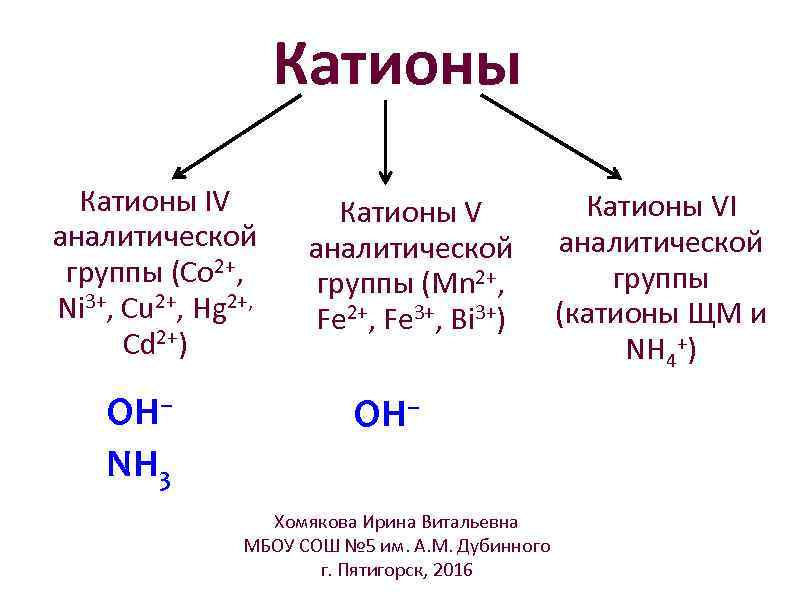
Катионы IV аналитической группы (Co 2+, Ni 3+, Cu 2+, Hg 2+, Cd 2+) OH– NH 3 Катионы V аналитической группы (Mn 2+, Fe 3+, Bi 3+) OH– Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016 Катионы VI аналитической группы (катионы ЩМ и NH 4+)

Pb 2+ + 2 Cl- = Pb. Cl 2 Hg 22+ + 2 Cl- = Hg 2 Cl 2 Качественная реакция на Pb 2+ + 2 I– = Pb. I 2↓ 2+ Pb 1. К анализируемому раствору добавить р-р Na. I или KI 2. Если выпал золотистый осадок, то в анализируемом растворе был Pb 2+ Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016

Pb 2+ + 2 Cl- = Pb. Cl 2 Hg 22+ + 2 Cl- = Hg 2 Cl 2 Качественная реакция на 2+ Ba 1. К анализируемому раствору добавить р-р Na 2 SO 4 (K 2 SO 4) 2. Если выпал белый осадок, то в анализируемом растворе был Ba 2+ + SO 42– = Ba. SO 4↓ Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016

Как распознать 2+? Cu Cu 2+ + 2 NH 3·H 2 O + SO 42 - = Cu 2(OH)2 SO 4 + 2 NH 4+ Cu 2(OH)2 SO 4 + 4 NH 3·H 2 O = [Cu(NH 3)4]2+ + SO 42 - + 2 OH- + 4 H 2 O 1. 2. 3. К анализируемому раствору добавить р-р Na. OH или KOH Если выпал голубой осадок, то к нему добавить водный NH 3 Если р-р стал синий, то в нем есть Cu 2+ Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016

Как распознать 2+? Ni Ni 2+ + 2 NH 3·H 2 O = Ni(OH)2 + 2 NH 4+ Ni(OH)2 + 6 NH 3·H 2 O = [Ni(NH 3)6]2+ + 2 OH 1. К анализируемому раствору добавить избыток NH 3 (водн) 2. Если р-р стал фиолетовый, то в нем есть Ni 2+ Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016

Соединения никеля Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016

Как распознать Способ 1 1. К анализируемому раствору добавить р-р Na. OH или KOH 2. Если выпал бурый осадок, то в анализируемом растворе был Fe 3+ + 3 OH– = Fe(OH)3↓ бурый Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016 3+? Fe

Как распознать 3+? Fe Способ 2 1. К анализируемому раствору добавить р-р KSCN 2. Если раствор стал ярко красным, то в нем есть Fe 3+ + 3 SCN– = Fe(SCN)3 красный Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016

Как распознать 4+? NH 1. К анализируемому раствору добавить избыток водного раствора Na. OH или KOH 2. Нагреть полученный раствор 3. Если появился запах аммиака, то в исходном растворе был NH 4+ NH 4 + + – OH = NH 3↑ + H 2 O Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016

Индикаторы Кислая среда H+: водные растворы кислот Щелочная среда ОH–: водные растворы щелочей Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016
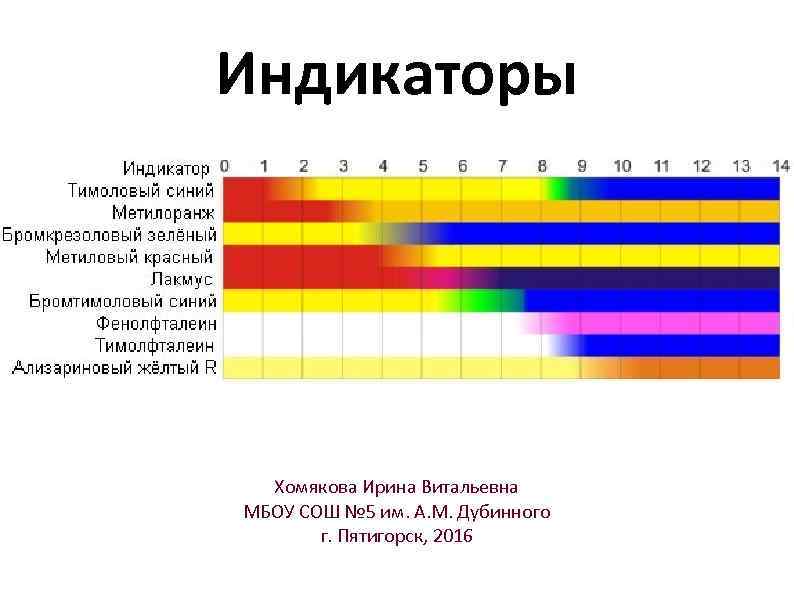
Индикаторы Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016

Метилоранж Фенолфталеин p. H > 7 p. H < 7 p. H > 7

Кислоты Щелочи HCl (соляная) Na. OH (гидроксид натрия) H 2 SO 4 (серная) HNO 3 (азотная) H 3 PO 4 (ортофосфорная) CH 3 COOH (уксусная) KOH (гидроксид калия) Хомякова Ирина Витальевна МБОУ СОШ № 5 им. А. М. Дубинного г. Пятигорск, 2016
1 Качественный анализ.ppt