КАЧЕСТВЕННЫЕ РЕАКЦИИ НА ФУНКЦИОНАЛЬНЫЕ ГРУППЫ














14 Лек.Качественные реакции на функ. группы.ppt
- Количество слайдов: 28
 КАЧЕСТВЕННЫЕ РЕАКЦИИ НА ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
КАЧЕСТВЕННЫЕ РЕАКЦИИ НА ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
 Функциональная группа – это атом или группа атомов неуглеводородного характера, которые определяют принад - лежность соединения к определённому классу. Функциональные группы обуславливают: Øсвойства веществ; Øхарактер реакций идентификации; Øметодов количественного определения.
Функциональная группа – это атом или группа атомов неуглеводородного характера, которые определяют принад - лежность соединения к определённому классу. Функциональные группы обуславливают: Øсвойства веществ; Øхарактер реакций идентификации; Øметодов количественного определения.
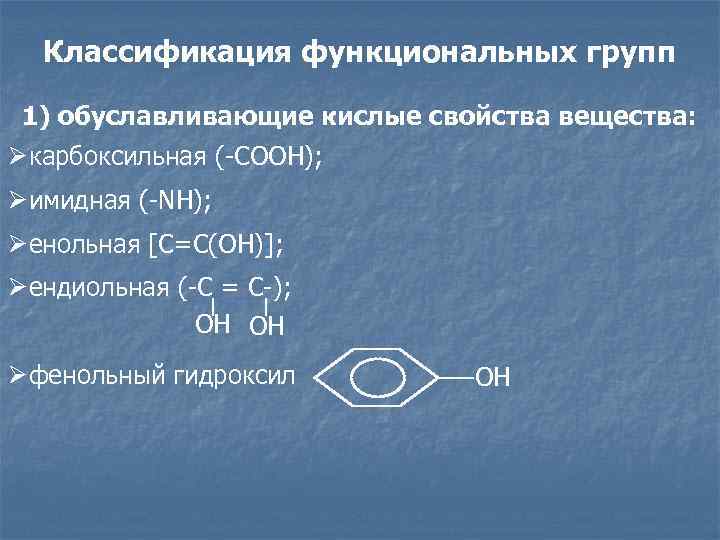
 Классификация функциональных групп 1) обуславливающие кислые свойства вещества: Øкарбоксильная (-СООН); Øимидная (-NH); Øенольная [C=C(OH)]; Øендиольная (-С = С-); ОН ОН Øфенольный гидроксил ОН
Классификация функциональных групп 1) обуславливающие кислые свойства вещества: Øкарбоксильная (-СООН); Øимидная (-NH); Øенольная [C=C(OH)]; Øендиольная (-С = С-); ОН ОН Øфенольный гидроксил ОН
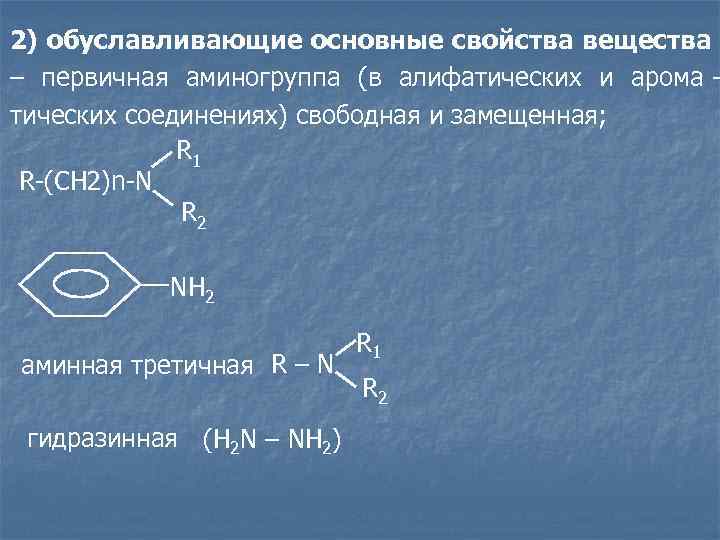
 2) обуславливающие основные свойства вещества – первичная аминогруппа (в алифатических и арома - тических соединениях) свободная и замещенная; R 1 R-(CH 2)n-N R 2 NH 2 R 1 аминная третичная R – N R 2 гидразинная (H 2 N – NH 2)
2) обуславливающие основные свойства вещества – первичная аминогруппа (в алифатических и арома - тических соединениях) свободная и замещенная; R 1 R-(CH 2)n-N R 2 NH 2 R 1 аминная третичная R – N R 2 гидразинная (H 2 N – NH 2)
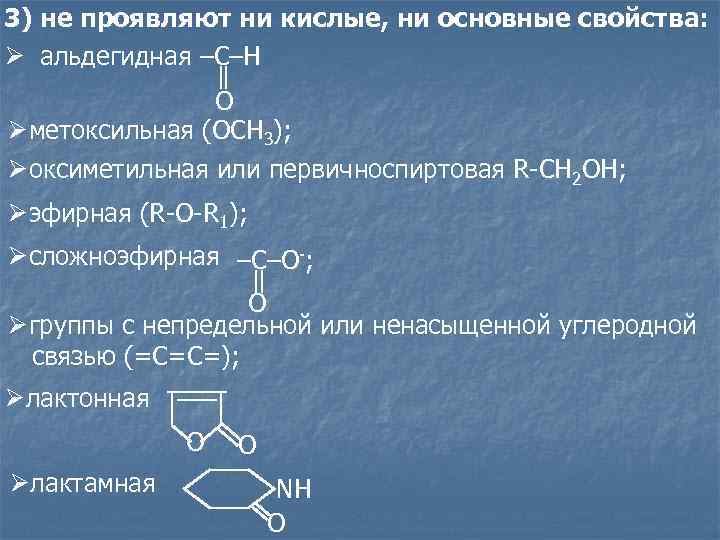
 3) не проявляют ни кислые, ни основные свойства: Ø aльдегидная –C–H O Øметоксильная (ОСН 3); Øоксиметильная или первичноспиртовая R-CH 2 OH; Øэфирная (R-O-R 1); Øсложноэфирная –C–O-; O Øгруппы с непредельной или ненасыщенной углеродной связью (=С=С=); Øлактонная O O Øлактамная NH O
3) не проявляют ни кислые, ни основные свойства: Ø aльдегидная –C–H O Øметоксильная (ОСН 3); Øоксиметильная или первичноспиртовая R-CH 2 OH; Øэфирная (R-O-R 1); Øсложноэфирная –C–O-; O Øгруппы с непредельной или ненасыщенной углеродной связью (=С=С=); Øлактонная O O Øлактамная NH O
 КАЧЕСТВЕННЫЕ РЕАКЦИИ НА ФУНКЦИОНАЛЬНЫЕ ГРУППЫ I. Гидроксильная группа – спиртовая (одно- атомные спирты). Образование сложного эфира: H 2 SO 4 конц. C 2 H 5 OH + CH 3 COOH C 2 H 5 О – CH 3 + H 2 O этилацетат с характерным запахом Образование йодоформа: C 2 H 5 OH + 6 Na. OH + 4 J 2 → CHJ 3↓ + HCOONa + 5 Na. J + 5 H 2 O жёлтый осадок, характерный запах
КАЧЕСТВЕННЫЕ РЕАКЦИИ НА ФУНКЦИОНАЛЬНЫЕ ГРУППЫ I. Гидроксильная группа – спиртовая (одно- атомные спирты). Образование сложного эфира: H 2 SO 4 конц. C 2 H 5 OH + CH 3 COOH C 2 H 5 О – CH 3 + H 2 O этилацетат с характерным запахом Образование йодоформа: C 2 H 5 OH + 6 Na. OH + 4 J 2 → CHJ 3↓ + HCOONa + 5 Na. J + 5 H 2 O жёлтый осадок, характерный запах
 II. Гидроксильная группа – фенольная. Лекарственные средства, содержащие фено- льную группу: Øсалициловая кислота; Øацетилсалициловая кислота; Øсалицилат натрия; Øрезорцин; Øадреналин; Øпиридоксин; Øморфин. C 6 H 5 OH + Fe. Cl 3 C 6 H 5 OFe. Cl 2 + HCl
II. Гидроксильная группа – фенольная. Лекарственные средства, содержащие фено- льную группу: Øсалициловая кислота; Øацетилсалициловая кислота; Øсалицилат натрия; Øрезорцин; Øадреналин; Øпиридоксин; Øморфин. C 6 H 5 OH + Fe. Cl 3 C 6 H 5 OFe. Cl 2 + HCl
 III. Карбонильная группа – альдегидная. Лекарственные средства: Øглюкоза; Øраствор формальдегида. Реакция «серебряного зеркала» Ag. NO 3 + 3 NH 4 OH → [Ag(NH 3)2]OH + NH 4 NO 3 + 2 Н 2 О t 2[Ag(NH 3)2]OH + R–C–H → 2 Ag↓ + R –C– OH + 4 NH 3↑+ H 2 O серый осадок O или «зеркало» O
III. Карбонильная группа – альдегидная. Лекарственные средства: Øглюкоза; Øраствор формальдегида. Реакция «серебряного зеркала» Ag. NO 3 + 3 NH 4 OH → [Ag(NH 3)2]OH + NH 4 NO 3 + 2 Н 2 О t 2[Ag(NH 3)2]OH + R–C–H → 2 Ag↓ + R –C– OH + 4 NH 3↑+ H 2 O серый осадок O или «зеркало» O
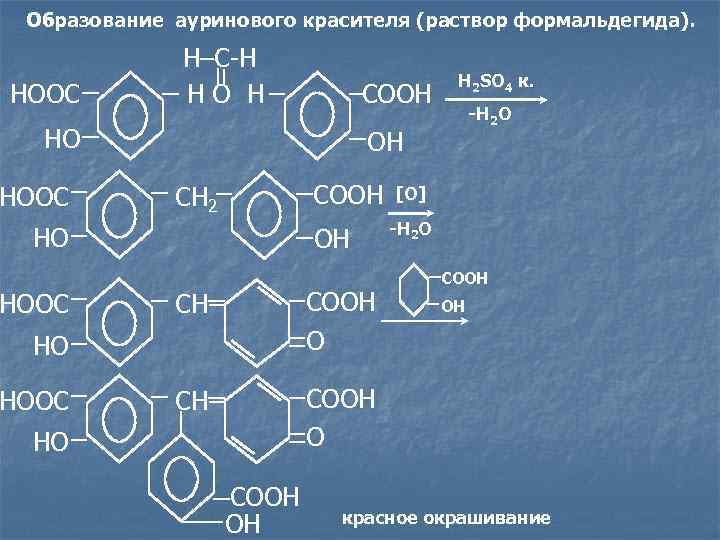
 Образование ауринового красителя (раствор формальдегида). H–C-H H 2 SO 4 к. HOOC HO H COOH -H 2 O HO OH HOOC CH 2 COOH [O] -H 2 O HO OH COOH HOOC CH COOH HO O HOOC CH COOH HO COOH красное окрашивание OH
Образование ауринового красителя (раствор формальдегида). H–C-H H 2 SO 4 к. HOOC HO H COOH -H 2 O HO OH HOOC CH 2 COOH [O] -H 2 O HO OH COOH HOOC CH COOH HO O HOOC CH COOH HO COOH красное окрашивание OH
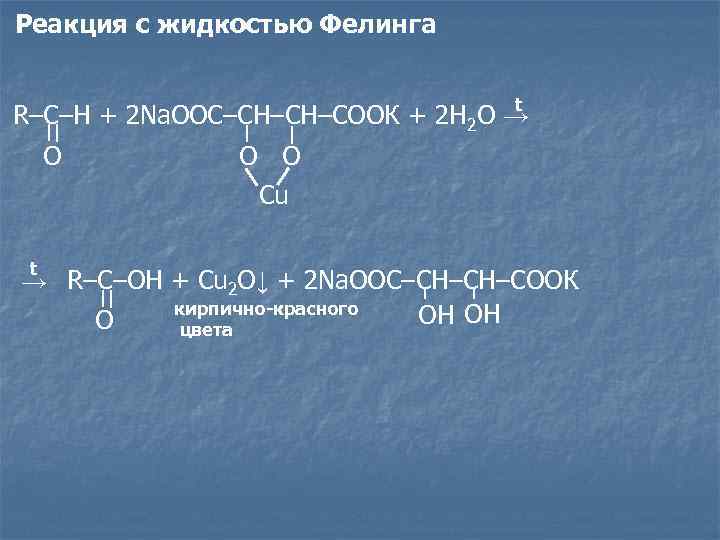
 Реакция с жидкостью Фелинга t R–C–H + 2 Na. OOC–CH–CH–COOК + 2 H 2 O → O O O Cu t → R–C–OH + Cu 2 O↓ + 2 Na. OOC–CH–CH–COOК кирпично-красного O цвета OH OH
Реакция с жидкостью Фелинга t R–C–H + 2 Na. OOC–CH–CH–COOК + 2 H 2 O → O O O Cu t → R–C–OH + Cu 2 O↓ + 2 Na. OOC–CH–CH–COOК кирпично-красного O цвета OH OH
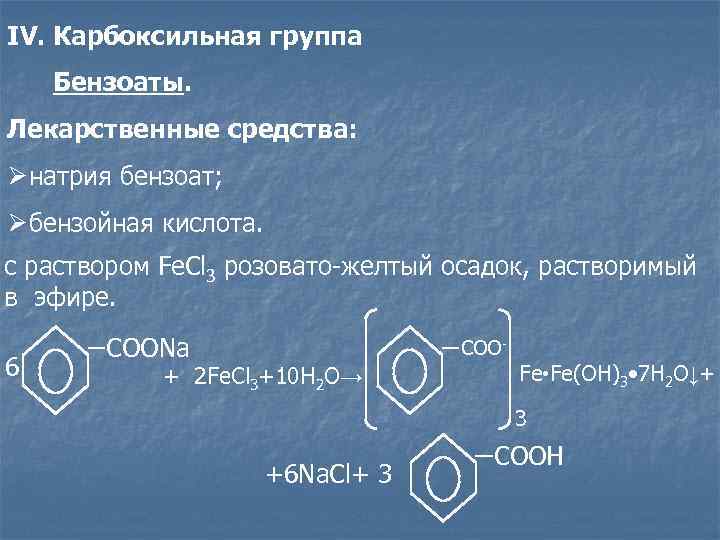
 IV. Карбоксильная группа Бензоаты. Лекарственные средства: Øнатрия бензоат; Øбензойная кислота. c раствором Fe. Cl 3 розовато-желтый осадок, растворимый в эфире. COONa COO- 6 + 2 Fe. Cl 3+10 H 2 O→ Fe • Fe(OH)3 • 7 H 2 O↓+ 3 COOH +6 Na. Cl+ 3
IV. Карбоксильная группа Бензоаты. Лекарственные средства: Øнатрия бензоат; Øбензойная кислота. c раствором Fe. Cl 3 розовато-желтый осадок, растворимый в эфире. COONa COO- 6 + 2 Fe. Cl 3+10 H 2 O→ Fe • Fe(OH)3 • 7 H 2 O↓+ 3 COOH +6 Na. Cl+ 3
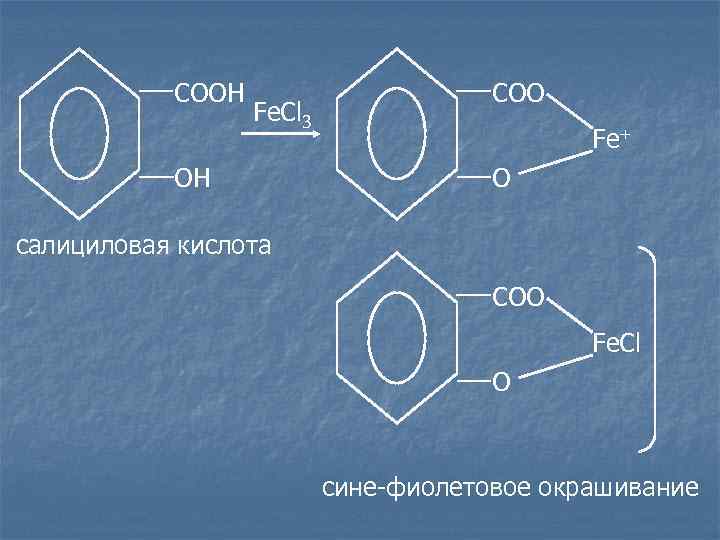
 Салицилаты. Лекарственные средства: Øсалициловая кислота; Øнатрия салицилат. c раствором Fe. Cl 3 появляется сине-фиолетовое или красное окрашивание, сохраняется в присутствии разведенной уксусной кислоты, исчезает прибавлении хлороводородной кислоты.
Салицилаты. Лекарственные средства: Øсалициловая кислота; Øнатрия салицилат. c раствором Fe. Cl 3 появляется сине-фиолетовое или красное окрашивание, сохраняется в присутствии разведенной уксусной кислоты, исчезает прибавлении хлороводородной кислоты.
 COOН COO Fe. Cl 3 Fe+ OН O салициловая кислота COO Fe. Cl O сине-фиолетовое окрашивание
COOН COO Fe. Cl 3 Fe+ OН O салициловая кислота COO Fe. Cl O сине-фиолетовое окрашивание
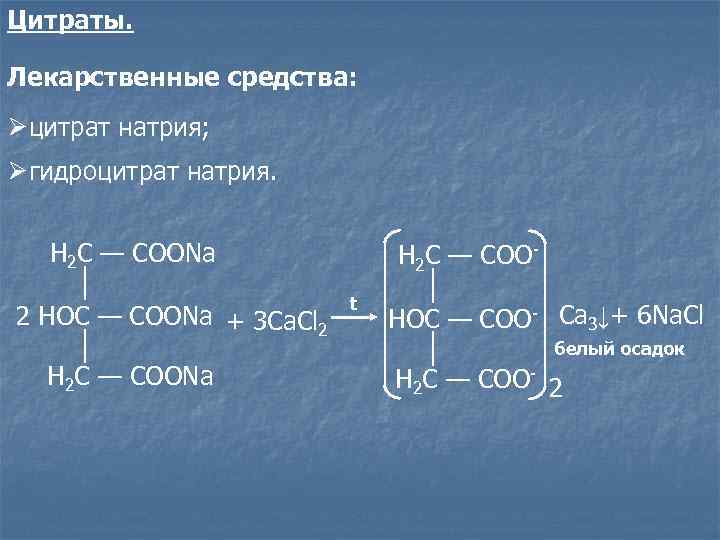
 Цитраты. Лекарственные средства: Øцитрат натрия; Øгидроцитрат натрия. Н 2 С — СООNa Н 2 С — СОО- t 2 НOС — СООNa + 3 Ca. Cl 2 НOС — СОО- Ca 3↓+ 6 Na. Cl белый осадок Н 2 С — СООNa Н 2 С — СОО- 2
Цитраты. Лекарственные средства: Øцитрат натрия; Øгидроцитрат натрия. Н 2 С — СООNa Н 2 С — СОО- t 2 НOС — СООNa + 3 Ca. Cl 2 НOС — СОО- Ca 3↓+ 6 Na. Cl белый осадок Н 2 С — СООNa Н 2 С — СОО- 2
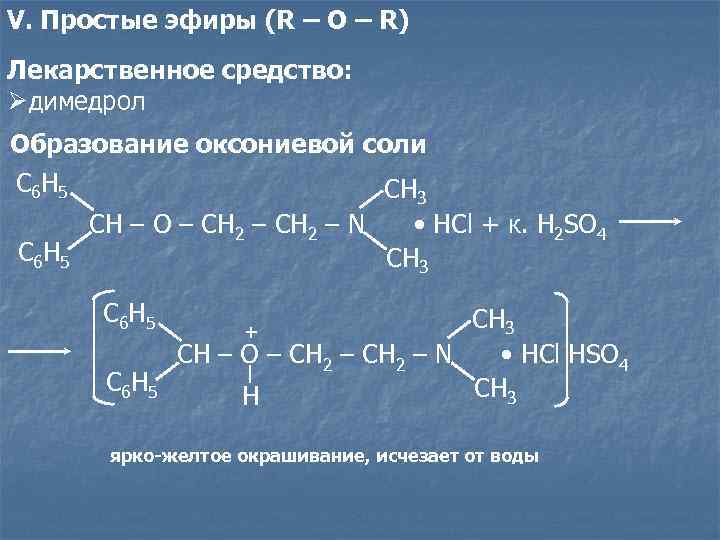
 V. Простые эфиры (R – O – R) Лекарственное средство: Øдимедрол Образование оксониевой соли C 6 H 5 CH 3 CH – O – CH 2 – N • HСl + к. H 2 SO 4 C 6 H 5 CH 3 + CH – O – CH 2 – N • HСl HSO 4 C 6 H 5 CH 3 H ярко-желтое окрашивание, исчезает от воды
V. Простые эфиры (R – O – R) Лекарственное средство: Øдимедрол Образование оксониевой соли C 6 H 5 CH 3 CH – O – CH 2 – N • HСl + к. H 2 SO 4 C 6 H 5 CH 3 + CH – O – CH 2 – N • HСl HSO 4 C 6 H 5 CH 3 H ярко-желтое окрашивание, исчезает от воды
 VI. Амины ароматические первичные (R – NH 2) Лекарственные средства: Øанестезин; Øновокаин; Øстрептоцид; Øнорсульфазол; Øсульфацил натрия; Øнатрия пара-аминосалицилат.
VI. Амины ароматические первичные (R – NH 2) Лекарственные средства: Øанестезин; Øновокаин; Øстрептоцид; Øнорсульфазол; Øсульфацил натрия; Øнатрия пара-аминосалицилат.
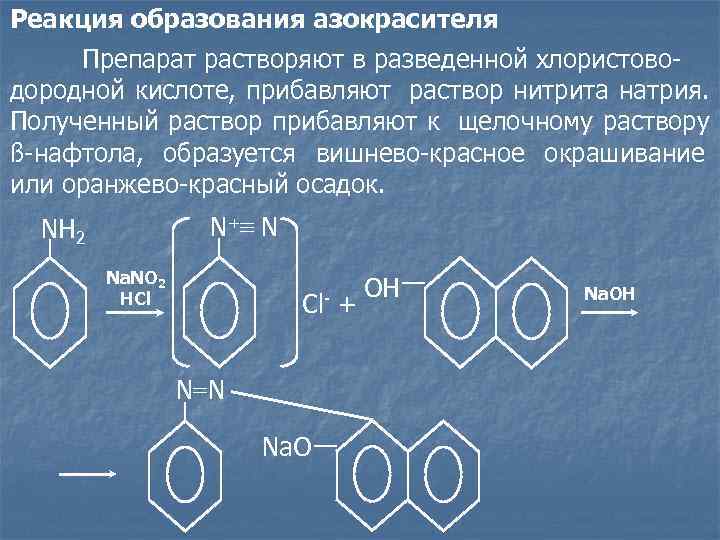
 Реакция образования азокрасителя Препарат растворяют в разведенной хлористово- дородной кислоте, прибавляют раствор нитрита натрия. Полученный раствор прибавляют к щелочному раствору ß-нафтола, образуется вишнево-красное окрашивание или оранжево-красный осадок. NH 2 N +≡ N Na. NO 2 ОН Na. OH HCl Cl- + N=N Na. O
Реакция образования азокрасителя Препарат растворяют в разведенной хлористово- дородной кислоте, прибавляют раствор нитрита натрия. Полученный раствор прибавляют к щелочному раствору ß-нафтола, образуется вишнево-красное окрашивание или оранжево-красный осадок. NH 2 N +≡ N Na. NO 2 ОН Na. OH HCl Cl- + N=N Na. O
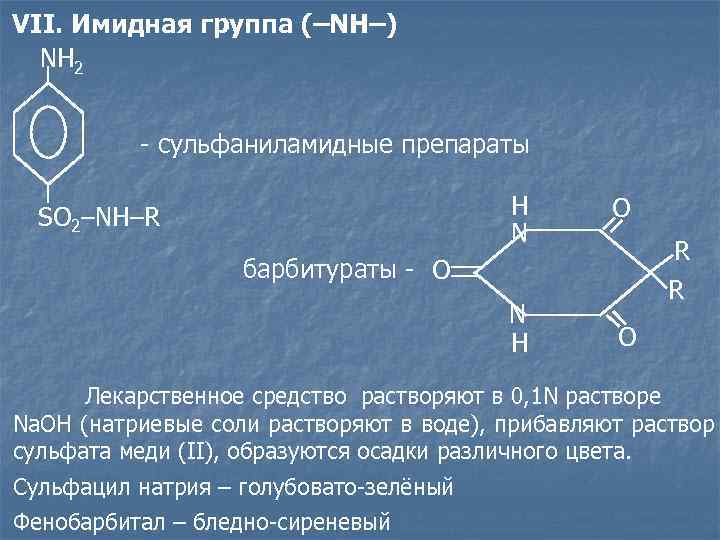
 VII. Имидная группа (–NH–) NH 2 - сульфаниламидные препараты SO 2–NH–R H O N R барбитураты - O R N H O Лекарственное средство растворяют в 0, 1 N растворе Na. OH (натриевые соли растворяют в воде), прибавляют раствор сульфата меди (II), образуются осадки различного цвета. Сульфацил натрия – голубовато-зелёный Фенобарбитал – бледно-сиреневый
VII. Имидная группа (–NH–) NH 2 - сульфаниламидные препараты SO 2–NH–R H O N R барбитураты - O R N H O Лекарственное средство растворяют в 0, 1 N растворе Na. OH (натриевые соли растворяют в воде), прибавляют раствор сульфата меди (II), образуются осадки различного цвета. Сульфацил натрия – голубовато-зелёный Фенобарбитал – бледно-сиреневый
 МЕТОД НЕВОДНОГО ТИТРОВАНИЯ Классификация растворителей 1) Амфитропные или амфотерные: H 2 O, CH 3 OH, C 2 H 5 OH и другие. Эти растворители играют роль основания по отношению к кислотам и роль кислоты по отношению к основаниям. 2) Протогенные или кислотные: HF, H 2 SO 4, HCOOH, CH 3 COOH и другие вещества кислотного характера. Молекулы протогенных растворителей склонны отдавать свои протоны и превращаться в основания: HF + C 2 H 5 OH → C 2 H 5 OH 2+ + F-
МЕТОД НЕВОДНОГО ТИТРОВАНИЯ Классификация растворителей 1) Амфитропные или амфотерные: H 2 O, CH 3 OH, C 2 H 5 OH и другие. Эти растворители играют роль основания по отношению к кислотам и роль кислоты по отношению к основаниям. 2) Протогенные или кислотные: HF, H 2 SO 4, HCOOH, CH 3 COOH и другие вещества кислотного характера. Молекулы протогенных растворителей склонны отдавать свои протоны и превращаться в основания: HF + C 2 H 5 OH → C 2 H 5 OH 2+ + F-
 3) Протофильные или основные: NH 3 , H 2 N - NH 2 , H 2 N ( CH 2 ) 2 NH 2 , HCO вещества основного характера. Молекулы протофильных растворителей отличаются большим сродством к протону и поэтому легко присое - диняют протоны: HCON(CH 3)2 + CH 3 COOH [HCONH(CH 3)2]+ + СН 3 СОО- 4) Апротонные или апротные: C 2 H 6 , C 6 H 12 , CCl 4 и другие вещества нейт характера, молекулы которых не способны ни отдавать, ни присоединять протоны, т. к. молекулы апротонных растворителей не диссоциированы.
3) Протофильные или основные: NH 3 , H 2 N - NH 2 , H 2 N ( CH 2 ) 2 NH 2 , HCO вещества основного характера. Молекулы протофильных растворителей отличаются большим сродством к протону и поэтому легко присое - диняют протоны: HCON(CH 3)2 + CH 3 COOH [HCONH(CH 3)2]+ + СН 3 СОО- 4) Апротонные или апротные: C 2 H 6 , C 6 H 12 , CCl 4 и другие вещества нейт характера, молекулы которых не способны ни отдавать, ни присоединять протоны, т. к. молекулы апротонных растворителей не диссоциированы.
 Преимущество метода кислотно- основного титрования в неводных средах состоит и в том, что он позволяет определять соли органических оснований или кислот по физиологически активной части молекулы.
Преимущество метода кислотно- основного титрования в неводных средах состоит и в том, что он позволяет определять соли органических оснований или кислот по физиологически активной части молекулы.
 ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ОСНОВАНИЙ И ИХ СОЛЕЙ. HCl. O 4 + CH 3 COOH → Cl. O 4 - + CH 3 COOH 2+ кислота основание ион ацетония Ацетат-ионы, обуславливающие в безводной уксусной кислоте щелочность раствора, нейтрализуются ионами ацетония, обуславливающими в том же растворителе кислотность раствора: CH 3 COO- + CH 3 COOH 2+ → 2 CH 3 COOH
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ОСНОВАНИЙ И ИХ СОЛЕЙ. HCl. O 4 + CH 3 COOH → Cl. O 4 - + CH 3 COOH 2+ кислота основание ион ацетония Ацетат-ионы, обуславливающие в безводной уксусной кислоте щелочность раствора, нейтрализуются ионами ацетония, обуславливающими в том же растворителе кислотность раствора: CH 3 COO- + CH 3 COOH 2+ → 2 CH 3 COOH
 Реакция нейтрализации сопровождается образо- ванием молекул того растворителя, в среде которого протекает данная реакция. 1) HCl. O 4 + 2 CH 3 COOH → 2 CH 3 COOH 2 + + 2 Cl. O 4 - ацетоний СН 3 CH 3 COOH 2) 2 R – N – CH 3 · HCl + Hg(CH 3 COO)2 СН 3 2 R – N+ – CH 3 COO- + Hg. Сl 2 Н+ ацетат димедрола
Реакция нейтрализации сопровождается образо- ванием молекул того растворителя, в среде которого протекает данная реакция. 1) HCl. O 4 + 2 CH 3 COOH → 2 CH 3 COOH 2 + + 2 Cl. O 4 - ацетоний СН 3 CH 3 COOH 2) 2 R – N – CH 3 · HCl + Hg(CH 3 COO)2 СН 3 2 R – N+ – CH 3 COO- + Hg. Сl 2 Н+ ацетат димедрола
 СН 3 3) 2 R – N+ – CH 3 COO- + 2 CH 3 COOH 2+ Н+ СН 3 2 R – N+ – CH 3 + 4 CH 3 COOH Н СН 3 4) 2 R – N+ – CH 3 + 2 Cl. O 4 - → 2 R – N+ – CH 3 Cl. O 4 - Н перхлорат
СН 3 3) 2 R – N+ – CH 3 COO- + 2 CH 3 COOH 2+ Н+ СН 3 2 R – N+ – CH 3 + 4 CH 3 COOH Н СН 3 4) 2 R – N+ – CH 3 + 2 Cl. O 4 - → 2 R – N+ – CH 3 Cl. O 4 - Н перхлорат
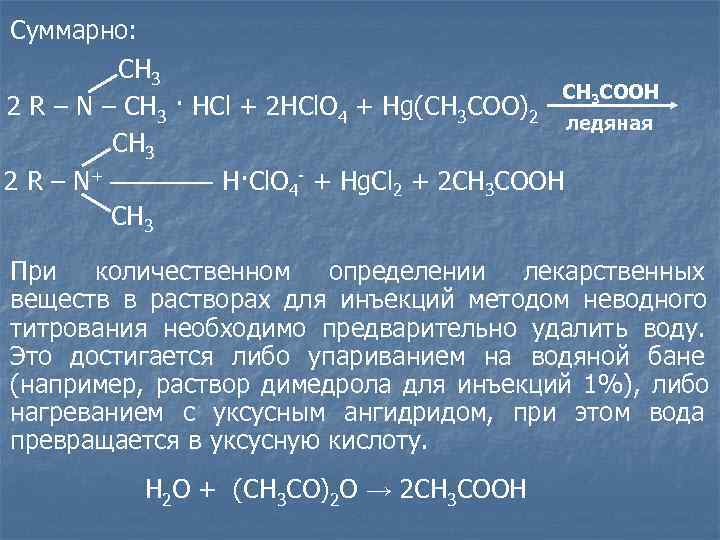
 Суммарно: СН 3 CH 3 COOH 2 R – N – CH 3 · HCl + 2 HCl. O 4 + Hg(CH 3 COO)2 ледяная СН 3 2 R – N+ H·Cl. O 4 - + Hg. Cl 2 + 2 CH 3 COOH СН 3 При количественном определении лекарственных веществ в растворах для инъекций методом неводного титрования необходимо предварительно удалить воду. Это достигается либо упариванием на водяной бане (например, раствор димедрола для инъекций 1%), либо нагреванием с уксусным ангидридом, при этом вода превращается в уксусную кислоту. Н 2 О + (СН 3 СО)2 О → 2 СН 3 СООН
Суммарно: СН 3 CH 3 COOH 2 R – N – CH 3 · HCl + 2 HCl. O 4 + Hg(CH 3 COO)2 ледяная СН 3 2 R – N+ H·Cl. O 4 - + Hg. Cl 2 + 2 CH 3 COOH СН 3 При количественном определении лекарственных веществ в растворах для инъекций методом неводного титрования необходимо предварительно удалить воду. Это достигается либо упариванием на водяной бане (например, раствор димедрола для инъекций 1%), либо нагреванием с уксусным ангидридом, при этом вода превращается в уксусную кислоту. Н 2 О + (СН 3 СО)2 О → 2 СН 3 СООН
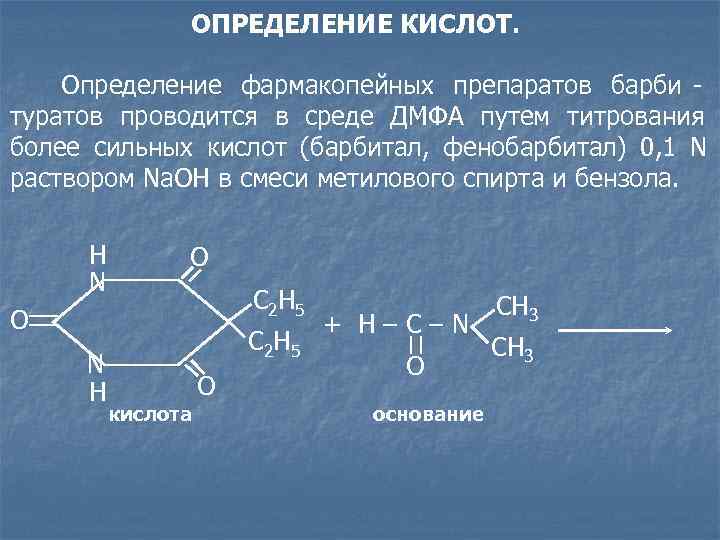
 ОПРЕДЕЛЕНИЕ КИСЛОТ. Определение фармакопейных препаратов барби - туратов проводится в среде ДМФА путем титрования более сильных кислот (барбитал, фенобарбитал) 0, 1 N раствором Na. OH в смеси метилового спирта и бензола. H O N С 2 Н 5 СН 3 O + H–C–N С 2 Н 5 СН 3 N O H O кислота основание
ОПРЕДЕЛЕНИЕ КИСЛОТ. Определение фармакопейных препаратов барби - туратов проводится в среде ДМФА путем титрования более сильных кислот (барбитал, фенобарбитал) 0, 1 N раствором Na. OH в смеси метилового спирта и бензола. H O N С 2 Н 5 СН 3 O + H–C–N С 2 Н 5 СН 3 N O H O кислота основание
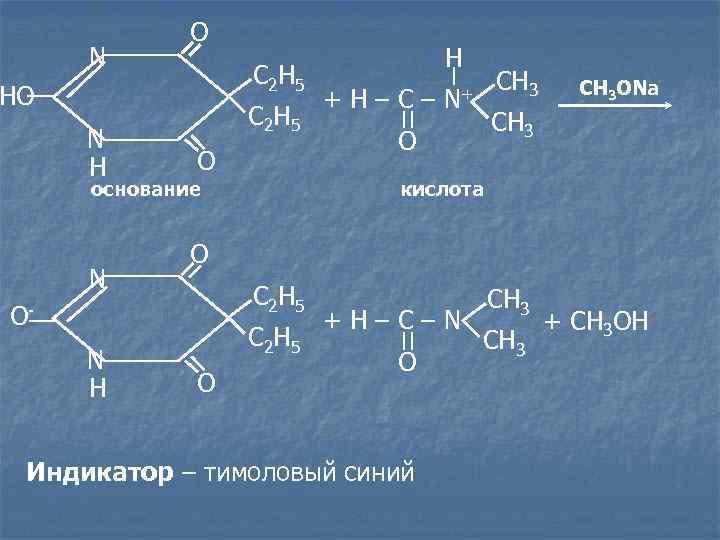
 O N H С 2 Н 5 СН 3 CH 3 ONa HO +H–C– N+ С 2 Н 5 СН 3 N O H O основание кислота O N С 2 Н 5 СН 3 O- +H–C–N + CH 3 OH С 2 Н 5 СН 3 N O H O Индикатор – тимоловый синий
O N H С 2 Н 5 СН 3 CH 3 ONa HO +H–C– N+ С 2 Н 5 СН 3 N O H O основание кислота O N С 2 Н 5 СН 3 O- +H–C–N + CH 3 OH С 2 Н 5 СН 3 N O H O Индикатор – тимоловый синий
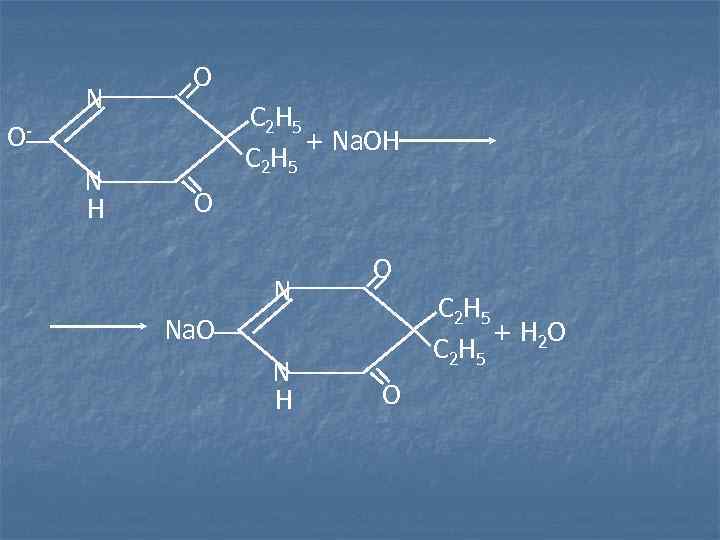
 O N С 2 Н 5 O- + Na. OH С 2 Н 5 N H O N С 2 Н 5 Na. O + H 2 O С 2 Н 5 N H O
O N С 2 Н 5 O- + Na. OH С 2 Н 5 N H O N С 2 Н 5 Na. O + H 2 O С 2 Н 5 N H O

