 КАЧЕСТВЕННЫЕ РЕАКЦИИ КАТИОНЫ
КАЧЕСТВЕННЫЕ РЕАКЦИИ КАТИОНЫ
 • + Na. Cl + Ag осадок белого цвета, нерастворимый в кислотах • +K 2 Cr 2 O 7 красно-бурое окрашивание или осадок, растворимый в кислотах • +Na 2 S черный осадок, нерастворимый в кислотах • + Na. OH коричневый осадок, растворимый в кислотах
• + Na. Cl + Ag осадок белого цвета, нерастворимый в кислотах • +K 2 Cr 2 O 7 красно-бурое окрашивание или осадок, растворимый в кислотах • +Na 2 S черный осадок, нерастворимый в кислотах • + Na. OH коричневый осадок, растворимый в кислотах
 2+ Рb • + KI осадок желтого цвета • + NH 3 или карбонат аммония белый осадок, нерастворимый в избытке осадителя • +Na 2 HP 04 белый осадок, легко растворимый в азотной кислотеи щелочах • + Na 2 S черный осадок, нерастворимый в кислотах
2+ Рb • + KI осадок желтого цвета • + NH 3 или карбонат аммония белый осадок, нерастворимый в избытке осадителя • +Na 2 HP 04 белый осадок, легко растворимый в азотной кислотеи щелочах • + Na 2 S черный осадок, нерастворимый в кислотах
 2+ Рb • +Na 2 S 04 белый осадок, нерастворимый в кислотах, но растворимый в щелочи и в ацетате аммония • +K 2 Cr 2 O 7 или K 2 Cr. O 4 осадок желтого цвета нерастворимый в уксусной кислоте, но растворимый в щелочи • + Na 2 S 203 белый осадок, растворимый в избытке осадителя. При кипячении выпадает черный осадок
2+ Рb • +Na 2 S 04 белый осадок, нерастворимый в кислотах, но растворимый в щелочи и в ацетате аммония • +K 2 Cr 2 O 7 или K 2 Cr. O 4 осадок желтого цвета нерастворимый в уксусной кислоте, но растворимый в щелочи • + Na 2 S 203 белый осадок, растворимый в избытке осадителя. При кипячении выпадает черный осадок
 2+ Ва • + Н 2 С 2 О 4 осадок белого цвета • +Na 2 СОз осадок белого цвета • +K 2 Cr 2 O 7 или K 2 Cr. O 4 осадок белого цвета нерастворимый в уксусной к
2+ Ва • + Н 2 С 2 О 4 осадок белого цвета • +Na 2 СОз осадок белого цвета • +K 2 Cr 2 O 7 или K 2 Cr. O 4 осадок белого цвета нерастворимый в уксусной к
 2+ Са + Н 2 С 2 О 4 осадок белого цвета +Na 2 СОз осадок белого цвета
2+ Са + Н 2 С 2 О 4 осадок белого цвета +Na 2 СОз осадок белого цвета
 Mg 2+ • +Na. OH бледно-розовый осадок, постепенно буреющий на воздухе • +Na 2 СОз белый осадок, пузырьки газа • + (NН 4)2 СОЗ белый осадок образуется только при кипячении или после длительного стояния. Прибавление избытка реагента и этанола к холодному концентрированному раствору соли магния вызывает полное осаждение магния. Осадок не образуется, если (NН 4)2 СОЗ прибавлять к горячему разбавленному раствору магниевой
Mg 2+ • +Na. OH бледно-розовый осадок, постепенно буреющий на воздухе • +Na 2 СОз белый осадок, пузырьки газа • + (NН 4)2 СОЗ белый осадок образуется только при кипячении или после длительного стояния. Прибавление избытка реагента и этанола к холодному концентрированному раствору соли магния вызывает полное осаждение магния. Осадок не образуется, если (NН 4)2 СОЗ прибавлять к горячему разбавленному раствору магниевой
 2+ Sn • + Na. OH белый студенистый осадок Sn 2++2 OH-=Sn(OH)2 • + NH 3 или карбонат аммония белый осадок, незначительно растворимый в избытке осадителя Sn 2++CO 32 -=Ca. CO 3
2+ Sn • + Na. OH белый студенистый осадок Sn 2++2 OH-=Sn(OH)2 • + NH 3 или карбонат аммония белый осадок, незначительно растворимый в избытке осадителя Sn 2++CO 32 -=Ca. CO 3
 2+ Sn • + Na 2 S+ 2 -3 капли HCL S 2 -+ Sn 2+=Sn. S шоколадно-коричневый осадок, нерастворимый в кислоте • + Zn H 2[Sn. Cl 4] + 2 Zn = Zn+Mg. Cl 2+ 2 HCl выделение олова в виде губчатой массы на грануле цинка
2+ Sn • + Na 2 S+ 2 -3 капли HCL S 2 -+ Sn 2+=Sn. S шоколадно-коричневый осадок, нерастворимый в кислоте • + Zn H 2[Sn. Cl 4] + 2 Zn = Zn+Mg. Cl 2+ 2 HCl выделение олова в виде губчатой массы на грануле цинка
 3+ AI +Nа. ОН (недостаток) или раствор аммиака осадок белого цвета. Осадок растворяется в избытке раствора щелочи. При добавлении к полученному раствору хлорида аммония вновь выпадает осадок белого цвета. +Na 2 СОз белый осадок и газ +(NH 4)2 HP 04 белый осадок, нерастворимый в уксусной, но растворимый в НС 1
3+ AI +Nа. ОН (недостаток) или раствор аммиака осадок белого цвета. Осадок растворяется в избытке раствора щелочи. При добавлении к полученному раствору хлорида аммония вновь выпадает осадок белого цвета. +Na 2 СОз белый осадок и газ +(NH 4)2 HP 04 белый осадок, нерастворимый в уксусной, но растворимый в НС 1
 2+ Zn + Nа. ОН (недостаток) Выпадает осадок белого цвета. Осадок растворяется в избытке раствора щелочи. При действии на полученный раствор хлоридом аммония не наблюдается выпадение осадка (отличие от катиона А 13+)
2+ Zn + Nа. ОН (недостаток) Выпадает осадок белого цвета. Осадок растворяется в избытке раствора щелочи. При действии на полученный раствор хлоридом аммония не наблюдается выпадение осадка (отличие от катиона А 13+)
 3+ Cr • +Nа. ОН (недостаток) Выпадает осадок зеленого цвета. Осадок растворяется в избытке раствора щелочи, но нерастворим в аммиаке Cr 3+ +3 OH-=Cr(OH)3 • + Na. OH + Н 2 О 2, при нагревании желтый раствор 2 Cr. Br 3 + 3 H 2 O 2 + 10 Na. OH → 2 Na 2 Cr. O 4 + 6 Na. Br + 8 H 2 O
3+ Cr • +Nа. ОН (недостаток) Выпадает осадок зеленого цвета. Осадок растворяется в избытке раствора щелочи, но нерастворим в аммиаке Cr 3+ +3 OH-=Cr(OH)3 • + Na. OH + Н 2 О 2, при нагревании желтый раствор 2 Cr. Br 3 + 3 H 2 O 2 + 10 Na. OH → 2 Na 2 Cr. O 4 + 6 Na. Br + 8 H 2 O
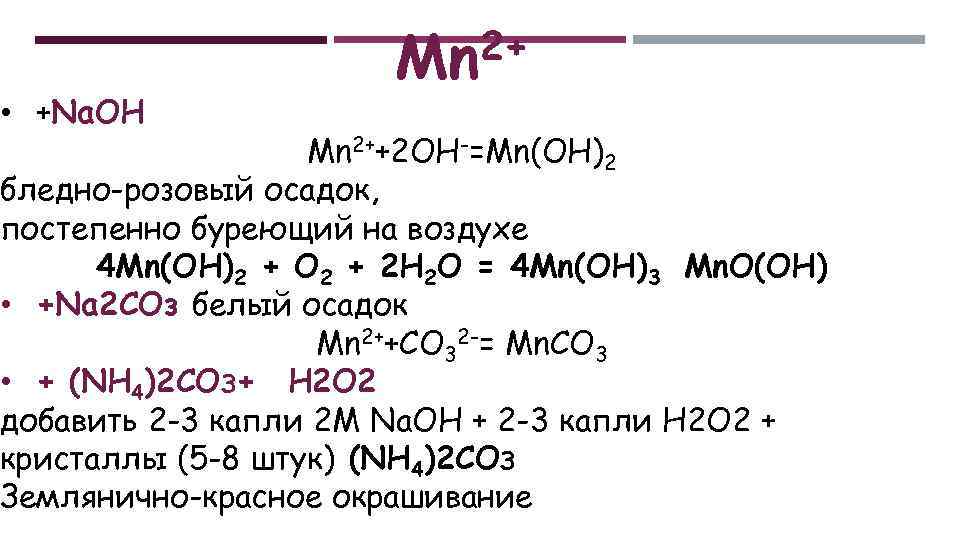 • +Na. OH 2+ Mn Mn 2++2 OH-=Mn(OH)2 бледно-розовый осадок, постепенно буреющий на воздухе 4 Mn(OH)2 + O 2 + 2 H 2 O = 4 Mn(OH)3 Mn. O(OH) • +Na 2 СОз белый осадок Mn 2++CO 32 -= Mn. CO 3 • + (NН 4)2 СОЗ+ Н 2 О 2 добавить 2 -3 капли 2 М Na. OH + 2 -3 капли Н 2 О 2 + кристаллы (5 -8 штук) (NН 4)2 СОЗ Землянично красное окрашивание
• +Na. OH 2+ Mn Mn 2++2 OH-=Mn(OH)2 бледно-розовый осадок, постепенно буреющий на воздухе 4 Mn(OH)2 + O 2 + 2 H 2 O = 4 Mn(OH)3 Mn. O(OH) • +Na 2 СОз белый осадок Mn 2++CO 32 -= Mn. CO 3 • + (NН 4)2 СОЗ+ Н 2 О 2 добавить 2 -3 капли 2 М Na. OH + 2 -3 капли Н 2 О 2 + кристаллы (5 -8 штук) (NН 4)2 СОЗ Землянично красное окрашивание
 2+ Mn • +В пробирку поместить 5 -6 капель+(NH 4)2 S 208 + 1 -2 капли конц Н 3 РО 4 + 1 -2 капли Аg. NОз, нагреть на водяной бане. Затем с помощью стеклянной палочки внести каплю исследуемого раствора и перемешать. Розовое окрашивание
2+ Mn • +В пробирку поместить 5 -6 капель+(NH 4)2 S 208 + 1 -2 капли конц Н 3 РО 4 + 1 -2 капли Аg. NОз, нагреть на водяной бане. Затем с помощью стеклянной палочки внести каплю исследуемого раствора и перемешать. Розовое окрашивание
![Mn 2+ • + K 4[Fe(CN)6] белый осадок • + K 3[Fe(CN)6] бурый осадок, Mn 2+ • + K 4[Fe(CN)6] белый осадок • + K 3[Fe(CN)6] бурый осадок,](https://present5.com/presentation/1/189824115_453065987.pdf-img/189824115_453065987.pdf-15.jpg) Mn 2+ • + K 4[Fe(CN)6] белый осадок • + K 3[Fe(CN)6] бурый осадок, нерастворимый в аммиаке + КВг. Оз • + KBr. O 3 фиолетовая окраска
Mn 2+ • + K 4[Fe(CN)6] белый осадок • + K 3[Fe(CN)6] бурый осадок, нерастворимый в аммиаке + КВг. Оз • + KBr. O 3 фиолетовая окраска
 2+ Co + НС 1 конц синий раствор + Na. OH синий осадок, в избытке реагента становится розовым, затем переходит в раствор Co 2++2 OH-=Co(OH)2 4 Co(OH)2 + O 2 + 2 H 2 O = 4 Co(OH)3 + NНз* н 2 о Co(OH)2 + 6 NH 3 = [Co(NH 3)6](OH)2 синий осадок, частично растворимый в избытке реагента с образованием грязно-желтого раствора, постепенно краснеющего на воздухе
2+ Co + НС 1 конц синий раствор + Na. OH синий осадок, в избытке реагента становится розовым, затем переходит в раствор Co 2++2 OH-=Co(OH)2 4 Co(OH)2 + O 2 + 2 H 2 O = 4 Co(OH)3 + NНз* н 2 о Co(OH)2 + 6 NH 3 = [Co(NH 3)6](OH)2 синий осадок, частично растворимый в избытке реагента с образованием грязно-желтого раствора, постепенно краснеющего на воздухе
 +Na 2 S черный осадок S 2 -+ Co 2+=Co. S 2+ Co +K 3[Fe(CN)6] буровато-красный осадок + NH 4 CNS (конц. раствор) синий раствор Co 2++2 CNS-=Co(CNS)2
+Na 2 S черный осадок S 2 -+ Co 2+=Co. S 2+ Co +K 3[Fe(CN)6] буровато-красный осадок + NH 4 CNS (конц. раствор) синий раствор Co 2++2 CNS-=Co(CNS)2
 Ni 2+ • + Na. OH зеленый осадок • +Na 2 S черный осадок • + NH 3 Н 2 О зеленый осадок, переходящий в васильково-синий раствор • + фосфат натрия яблочно-зеленый осадок, легко растворимый в кислотах • + K 4[Fe(CN)6] зеленоватый осадок • + K 3[Fe(CN)6] желтовато-бурый осадок
Ni 2+ • + Na. OH зеленый осадок • +Na 2 S черный осадок • + NH 3 Н 2 О зеленый осадок, переходящий в васильково-синий раствор • + фосфат натрия яблочно-зеленый осадок, легко растворимый в кислотах • + K 4[Fe(CN)6] зеленоватый осадок • + K 3[Fe(CN)6] желтовато-бурый осадок
 2+ Fe • + Na. OH Выпадает осадок белого цвета. Возможно образование зеленого осадка ( «зеленая ржавчина» ). Осадок буреет на воздухе. Fe 2++2 OH-=Fe(OH)2 4 Fe(OH)2 + O 2 + 2 H 2 O = 4 Fe(OH)3 • + K 3[Fe(CN)6] Fe. SO 4+ K 3[Fe(CN)6]= K Fe. Fe(CN)6 + K 2 SO 4 Выпадает осадок или образуется раствор синего цвета
2+ Fe • + Na. OH Выпадает осадок белого цвета. Возможно образование зеленого осадка ( «зеленая ржавчина» ). Осадок буреет на воздухе. Fe 2++2 OH-=Fe(OH)2 4 Fe(OH)2 + O 2 + 2 H 2 O = 4 Fe(OH)3 • + K 3[Fe(CN)6] Fe. SO 4+ K 3[Fe(CN)6]= K Fe. Fe(CN)6 + K 2 SO 4 Выпадает осадок или образуется раствор синего цвета
 2+ Fe • + NH 4 CNS нет изменений + карбонат аммония белый осадок, буреющий на воздухе Fe 2++CO 32 -= Fe. CO 3 • + Na 2 S • Fe 2++S 2 -= Fe. S черный осадок, растворимый в кислотах
2+ Fe • + NH 4 CNS нет изменений + карбонат аммония белый осадок, буреющий на воздухе Fe 2++CO 32 -= Fe. CO 3 • + Na 2 S • Fe 2++S 2 -= Fe. S черный осадок, растворимый в кислотах
 3+ Fe • + Na. OH Fe 3++3 OH-=Fe(OH)3 осадок бурого цвета, с трудом растворимый в избытке реагента • + NH 3 осадок бурого цвета, нерастворимый в избытке реагента • + K 4[Fe(CN)6] Fe. Cl 3+ K 4[Fe(CN)6]= K Fe. Fe(CN)6 + 3 KCl + NH 4 CNS Fe 3++3 CNS-=Fe(CNS)3 образуется раствор темно-красного цвета. Окраска исчезает в присутствии фторид-ионов
3+ Fe • + Na. OH Fe 3++3 OH-=Fe(OH)3 осадок бурого цвета, с трудом растворимый в избытке реагента • + NH 3 осадок бурого цвета, нерастворимый в избытке реагента • + K 4[Fe(CN)6] Fe. Cl 3+ K 4[Fe(CN)6]= K Fe. Fe(CN)6 + 3 KCl + NH 4 CNS Fe 3++3 CNS-=Fe(CNS)3 образуется раствор темно-красного цвета. Окраска исчезает в присутствии фторид-ионов
 3+ Fe + ацетат натрия CH 3 COONa темно-бурое окрашивание, при кипячении хлопья осадка основной соли. В присутствии лимонной кислоты, глицерина сахаров осадок не выпадает • + Zn. O (внести в раствор, перемешать, нагреть) бурый осадок • + Nа 2 Н РО 4 желтовато-белый осадок
3+ Fe + ацетат натрия CH 3 COONa темно-бурое окрашивание, при кипячении хлопья осадка основной соли. В присутствии лимонной кислоты, глицерина сахаров осадок не выпадает • + Zn. O (внести в раствор, перемешать, нагреть) бурый осадок • + Nа 2 Н РО 4 желтовато-белый осадок
 3+ Fe • сульфосалициловая кислота красно-фиолетовое окрашивание (p. H 3 - 5). При добавлении аммиака (p. H 9 - 11) окраска переходит в желтую. Контроль p. H по индикаторной бумаге! • Na 2 S 203 p. H близок к нейтральному красно-фиолетовая окраска, которая быстро исчезает из-за восстановления железа (+ образуется тетратионат!!!)
3+ Fe • сульфосалициловая кислота красно-фиолетовое окрашивание (p. H 3 - 5). При добавлении аммиака (p. H 9 - 11) окраска переходит в желтую. Контроль p. H по индикаторной бумаге! • Na 2 S 203 p. H близок к нейтральному красно-фиолетовая окраска, которая быстро исчезает из-за восстановления железа (+ образуется тетратионат!!!)
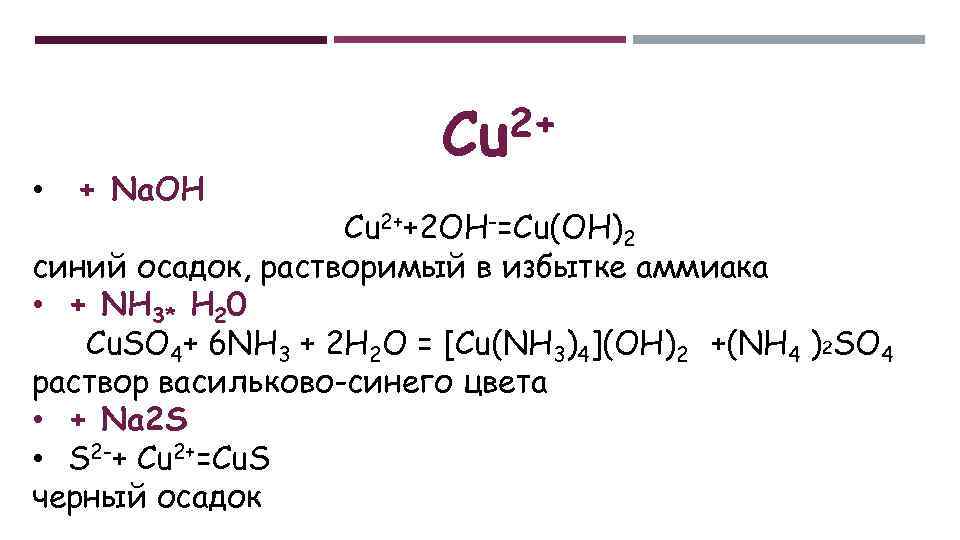 • + Na. OH 2+ Cu Cu 2++2 OH-=Cu(OH)2 синий осадок, растворимый в избытке аммиака • + NH 3* Н 20 Cu. SO 4+ 6 NH 3 + 2 H 2 O = [Cu(NH 3)4](OH)2 +(NH 4 )2 SO 4 раствор васильково-синего цвета • + Na 2 S • S 2 -+ Cu 2+=Cu. S черный осадок
• + Na. OH 2+ Cu Cu 2++2 OH-=Cu(OH)2 синий осадок, растворимый в избытке аммиака • + NH 3* Н 20 Cu. SO 4+ 6 NH 3 + 2 H 2 O = [Cu(NH 3)4](OH)2 +(NH 4 )2 SO 4 раствор васильково-синего цвета • + Na 2 S • S 2 -+ Cu 2+=Cu. S черный осадок
 +Na 2 СОз 2+ Cu Cu 2++CO 32 -=Cu. CO 3 зеленовато-голубой осадок, выделение газа + Na 2 S 203 бесцветный раствор, при кипячении красновато бурый осадок Cu 2 S) (
+Na 2 СОз 2+ Cu Cu 2++CO 32 -=Cu. CO 3 зеленовато-голубой осадок, выделение газа + Na 2 S 203 бесцветный раствор, при кипячении красновато бурый осадок Cu 2 S) (
 2+ Cu • + KI коричневый осадок, становящийся белым при обработке тиосульфатом 2 Cu. SO 4 + 4 KI = 2 Cu. I + I 2 + 2 K 2 SO 4 + K 4[Fe(CN)6] красно-бурый осадок K 4[Fe(CN)6] + 2 Cu. SO 4 =Си 2[Fe(CN)6] +2 K 2 SO 4 + Zn красный налет на грануле цинка Cu. SO 4 + Zn = Cu + I 2 + Zn. SO 4
2+ Cu • + KI коричневый осадок, становящийся белым при обработке тиосульфатом 2 Cu. SO 4 + 4 KI = 2 Cu. I + I 2 + 2 K 2 SO 4 + K 4[Fe(CN)6] красно-бурый осадок K 4[Fe(CN)6] + 2 Cu. SO 4 =Си 2[Fe(CN)6] +2 K 2 SO 4 + Zn красный налет на грануле цинка Cu. SO 4 + Zn = Cu + I 2 + Zn. SO 4
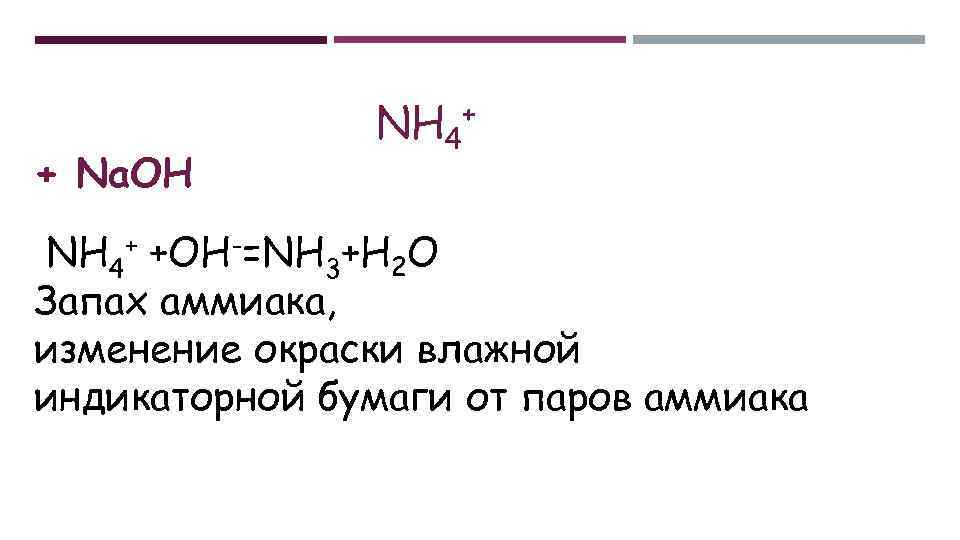 + Na. OH NH 4+ +OH-=NH 3+H 2 O Запах аммиака, изменение окраски влажной индикаторной бумаги от паров аммиака
+ Na. OH NH 4+ +OH-=NH 3+H 2 O Запах аммиака, изменение окраски влажной индикаторной бумаги от паров аммиака


