KR_po_SV_variant_1.pptx
- Количество слайдов: 21
 К/р «Строение вещества» 1. Расшифровать следующую схему ядерных превращений: ЭЗ 245 X Bk Y Укажите химические символы, массовые и зарядовые числа продуктов X и Y. а) -распад — испускание ядра гелия-4 245 Bk 97 4 Не 2 + 241 Х 95 Х = 241 Am 95 б) электронный захват — превращение протона в нейтрон 245 Bk ЭЗ 97 245 Y 96 Y = 245 Cm 96
К/р «Строение вещества» 1. Расшифровать следующую схему ядерных превращений: ЭЗ 245 X Bk Y Укажите химические символы, массовые и зарядовые числа продуктов X и Y. а) -распад — испускание ядра гелия-4 245 Bk 97 4 Не 2 + 241 Х 95 Х = 241 Am 95 б) электронный захват — превращение протона в нейтрон 245 Bk ЭЗ 97 245 Y 96 Y = 245 Cm 96
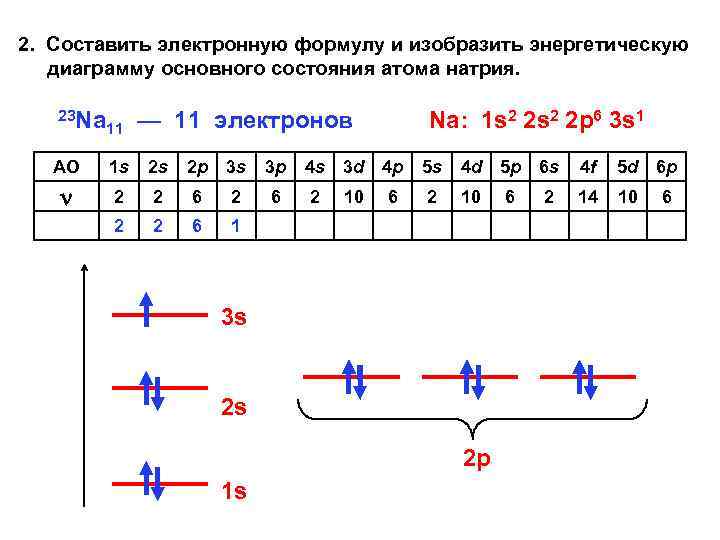 2. Составить электронную формулу и изобразить энергетическую диаграмму основного состояния атома натрия. 23 Na 11 — 11 электронов АО 1 s 2 s 2 p 3 s 3 p 4 s 3 d 4 p 5 s 4 d 5 p 6 s 4 f 5 d 6 p 2 2 6 2 10 6 2 14 10 6 2 2 6 1 Na: 1 s 2 2 p 6 3 s 1 3 s 2 s 2 p 1 s
2. Составить электронную формулу и изобразить энергетическую диаграмму основного состояния атома натрия. 23 Na 11 — 11 электронов АО 1 s 2 s 2 p 3 s 3 p 4 s 3 d 4 p 5 s 4 d 5 p 6 s 4 f 5 d 6 p 2 2 6 2 10 6 2 14 10 6 2 2 6 1 Na: 1 s 2 2 p 6 3 s 1 3 s 2 s 2 p 1 s
 3. В скольких стационарных состояниях может находиться атом с электронной конфигурацией. . . (3 p)4 ? k Сn n=6 k=4 n (n – 1) … (n – k + 1) = —————— 1 2 … k 4 С 6 6 5 4 3 = ————— = 15 1 2 3 4 N = 15 стационарных состояний
3. В скольких стационарных состояниях может находиться атом с электронной конфигурацией. . . (3 p)4 ? k Сn n=6 k=4 n (n – 1) … (n – k + 1) = —————— 1 2 … k 4 С 6 6 5 4 3 = ————— = 15 1 2 3 4 N = 15 стационарных состояний
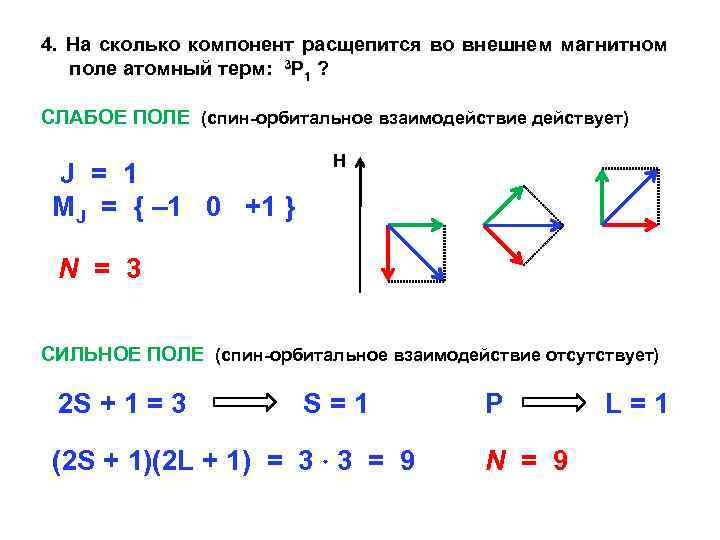 4. На сколько компонент расщепится во внешнем магнитном поле атомный терм: 3 Р 1 ? СЛАБОЕ ПОЛЕ (спин-орбитальное взаимодействие действует) J = 1 MJ = { – 1 0 +1 } H N = 3 СИЛЬНОЕ ПОЛЕ (спин-орбитальное взаимодействие отсутствует) 2 S + 1 = 3 S=1 (2 S + 1)(2 L + 1) = 3 3 = 9 P N = 9 L=1
4. На сколько компонент расщепится во внешнем магнитном поле атомный терм: 3 Р 1 ? СЛАБОЕ ПОЛЕ (спин-орбитальное взаимодействие действует) J = 1 MJ = { – 1 0 +1 } H N = 3 СИЛЬНОЕ ПОЛЕ (спин-орбитальное взаимодействие отсутствует) 2 S + 1 = 3 S=1 (2 S + 1)(2 L + 1) = 3 3 = 9 P N = 9 L=1
 5. Перечислите все возможные значения квантовых чисел J и MJ для атома с термом 3 D. 2 S + 1 = 3 S=1 D L=2 J = ( L + S ), ( L + S – 1 ), … , | L – S | MJ = +J, +J – 1, … , – J J = 3 MJ = { 3, 2, 1, 0, – 1, – 2, – 3 } J = 2 MJ = { 2, 1, 0, – 1, – 2 } J = 1 MJ = { 1, 0, – 1 }
5. Перечислите все возможные значения квантовых чисел J и MJ для атома с термом 3 D. 2 S + 1 = 3 S=1 D L=2 J = ( L + S ), ( L + S – 1 ), … , | L – S | MJ = +J, +J – 1, … , – J J = 3 MJ = { 3, 2, 1, 0, – 1, – 2, – 3 } J = 2 MJ = { 2, 1, 0, – 1, – 2 } J = 1 MJ = { 1, 0, – 1 }
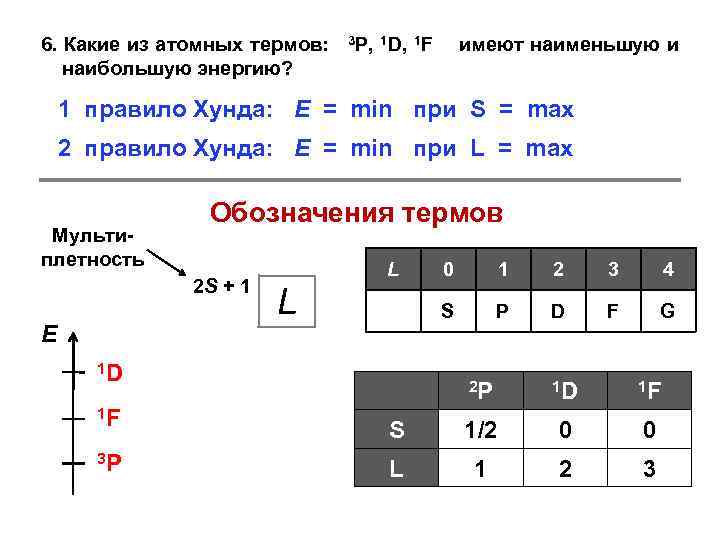 6. Какие из атомных термов: наибольшую энергию? 3 Р, 1 D, 1 F имеют наименьшую и 1 правило Хунда: E = min при S = max 2 правило Хунда: E = min при L = max Мультиплетность Обозначения термов 2 S + 1 E L 1 D 1 F 3 P 1 2 3 4 S L 0 P D F G 2 P 1 D 1 F S 1/2 0 0 L 1 2 3
6. Какие из атомных термов: наибольшую энергию? 3 Р, 1 D, 1 F имеют наименьшую и 1 правило Хунда: E = min при S = max 2 правило Хунда: E = min при L = max Мультиплетность Обозначения термов 2 S + 1 E L 1 D 1 F 3 P 1 2 3 4 S L 0 P D F G 2 P 1 D 1 F S 1/2 0 0 L 1 2 3
 7. Изобразить узловую структуру волновой функции 5 d для атома водорода. Nрадиальн. = n – ℓ – 1 = 5 – 2 – 1 = 2 Nуглов. = ℓ = 2 + – – + + – +
7. Изобразить узловую структуру волновой функции 5 d для атома водорода. Nрадиальн. = n – ℓ – 1 = 5 – 2 – 1 = 2 Nуглов. = ℓ = 2 + – – + + – +
 8. Изобразить энергетическую диаграмму для -МО линейного полиена с N = 12. 12 АО порождают 12 МО, из которых половина (6) — связывающие и половина (6) — разрыхляющие Е k Xk = – 2 cos ——— N+1 6 k — номер МО N — число атомов в цепи Х = ± 1, 942 ± 1, 136 ± 1, 771 ± 0, 709 ± 1, 497 ± 0, 241 6
8. Изобразить энергетическую диаграмму для -МО линейного полиена с N = 12. 12 АО порождают 12 МО, из которых половина (6) — связывающие и половина (6) — разрыхляющие Е k Xk = – 2 cos ——— N+1 6 k — номер МО N — число атомов в цепи Х = ± 1, 942 ± 1, 136 ± 1, 771 ± 0, 709 ± 1, 497 ± 0, 241 6
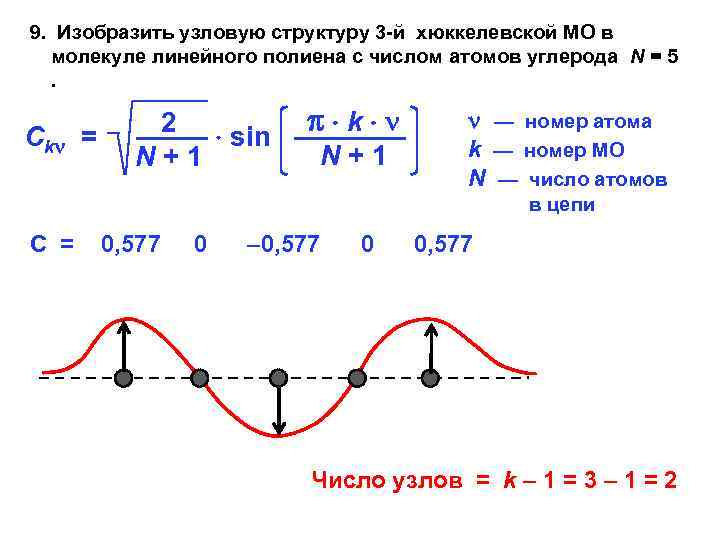 9. Изобразить узловую структуру 3 -й хюккелевской МО в молекуле линейного полиена с числом атомов углерода N = 5. С k = k 2 sin ———— ——– N+1 — номер атома k — номер МО N — число атомов в цепи С = 0, 577 0 – 0, 577 0 0, 577 Число узлов = k – 1 = 3 – 1 = 2
9. Изобразить узловую структуру 3 -й хюккелевской МО в молекуле линейного полиена с числом атомов углерода N = 5. С k = k 2 sin ———— ——– N+1 — номер атома k — номер МО N — число атомов в цепи С = 0, 577 0 – 0, 577 0 0, 577 Число узлов = k – 1 = 3 – 1 = 2
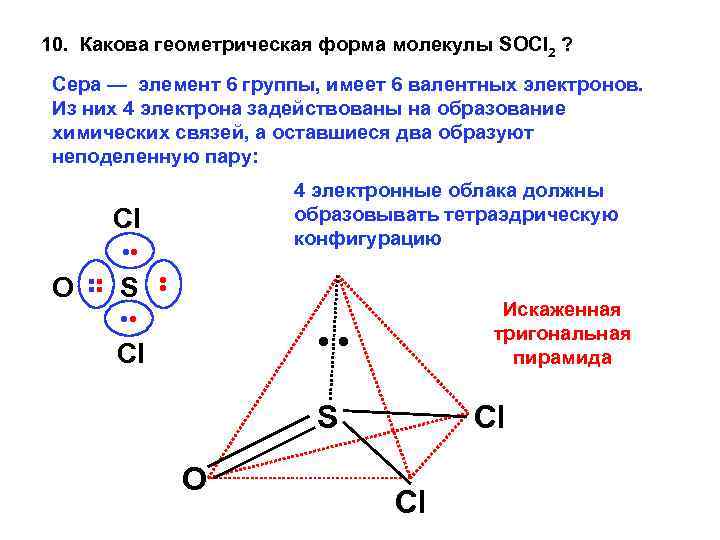 10. Какова геометрическая форма молекулы SOCl 2 ? Сера — элемент 6 группы, имеет 6 валентных электронов. Из них 4 электрона задействованы на образование химических связей, а оставшиеся два образуют неподеленную пару: 4 электронные облака должны образовывать тетраэдрическую конфигурацию Cl • • O : : S • • Искаженная тригональная пирамида • • Cl S O Cl Cl
10. Какова геометрическая форма молекулы SOCl 2 ? Сера — элемент 6 группы, имеет 6 валентных электронов. Из них 4 электрона задействованы на образование химических связей, а оставшиеся два образуют неподеленную пару: 4 электронные облака должны образовывать тетраэдрическую конфигурацию Cl • • O : : S • • Искаженная тригональная пирамида • • Cl S O Cl Cl
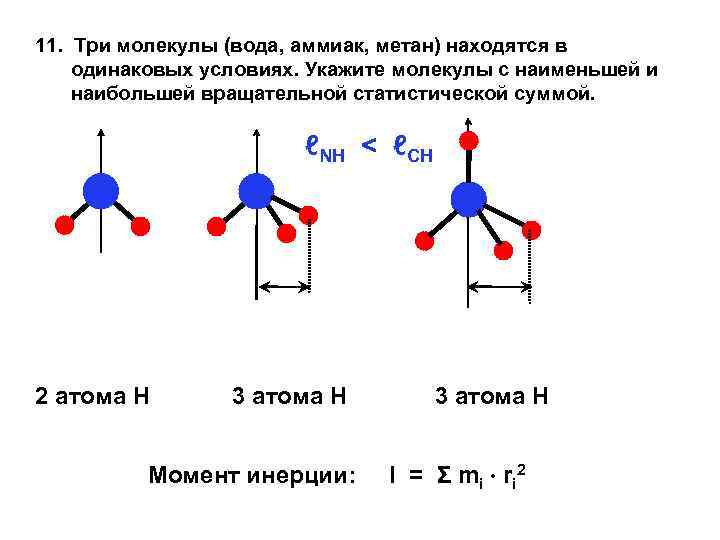 11. Три молекулы (вода, аммиак, метан) находятся в одинаковых условиях. Укажите молекулы с наименьшей и наибольшей вращательной статистической суммой. ℓNH < ℓCH 2 атома Н 3 атома Н Момент инерции: 3 атома Н I = Σ m i r i 2
11. Три молекулы (вода, аммиак, метан) находятся в одинаковых условиях. Укажите молекулы с наименьшей и наибольшей вращательной статистической суммой. ℓNH < ℓCH 2 атома Н 3 атома Н Момент инерции: 3 атома Н I = Σ m i r i 2
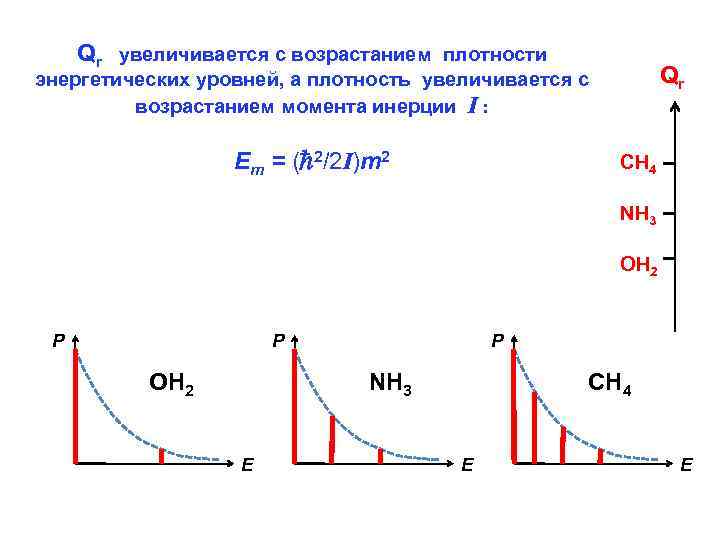 Qr увеличивается с возрастанием плотности Qr энергетических уровней, а плотность увеличивается с возрастанием момента инерции I : Еm = ( 2/2 I)m 2 CH 4 NH 3 OH 2 Р Р OН 2 Р NН 3 Е CН 4 Е Е
Qr увеличивается с возрастанием плотности Qr энергетических уровней, а плотность увеличивается с возрастанием момента инерции I : Еm = ( 2/2 I)m 2 CH 4 NH 3 OH 2 Р Р OН 2 Р NН 3 Е CН 4 Е Е
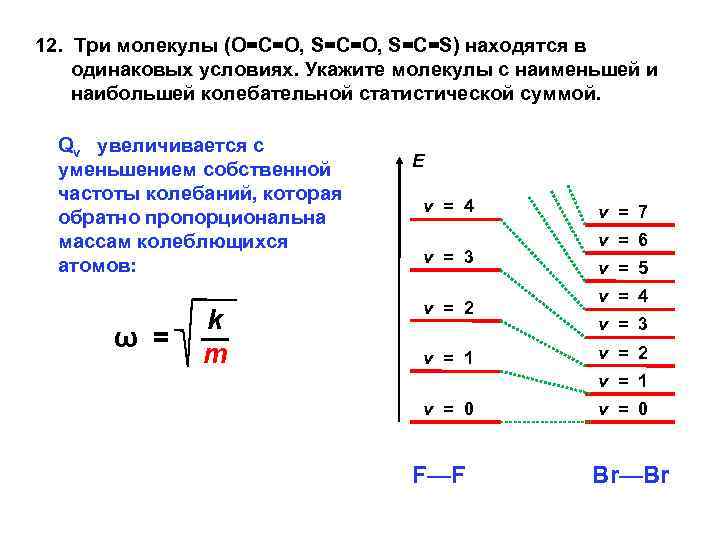 12. Три молекулы (O=C=O, S=C=S) находятся в одинаковых условиях. Укажите молекулы с наименьшей и наибольшей колебательной статистической суммой. Qv увеличивается с уменьшением собственной частоты колебаний, которая обратно пропорциональна массам колеблющихся атомов: ω = k — m E v = 4 v = 3 v = 2 v = 1 v = 7 v = 6 v = 5 v = 4 v = 3 v = 2 v = 1 v = 0 F—F v = 0 Br—Br
12. Три молекулы (O=C=O, S=C=S) находятся в одинаковых условиях. Укажите молекулы с наименьшей и наибольшей колебательной статистической суммой. Qv увеличивается с уменьшением собственной частоты колебаний, которая обратно пропорциональна массам колеблющихся атомов: ω = k — m E v = 4 v = 3 v = 2 v = 1 v = 7 v = 6 v = 5 v = 4 v = 3 v = 2 v = 1 v = 0 F—F v = 0 Br—Br
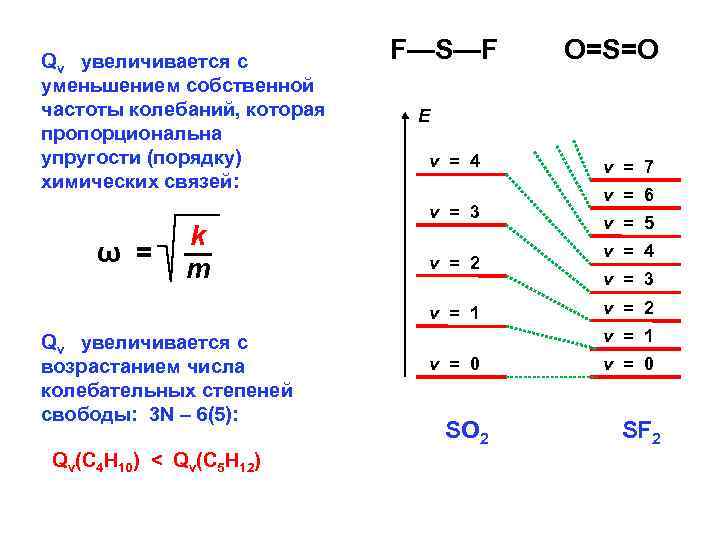 Qv увеличивается с уменьшением собственной частоты колебаний, которая пропорциональна упругости (порядку) химических связей: ω = k — m F—S—F E v = 4 v = 3 v = 2 v = 1 Qv увеличивается с возрастанием числа колебательных степеней свободы: 3 N – 6(5): Qv(С 4 Н 10) < Qv(С 5 Н 12) O=S=O v = 7 v = 6 v = 5 v = 4 v = 3 v = 2 v = 1 v = 0 SO 2 v = 0 SF 2
Qv увеличивается с уменьшением собственной частоты колебаний, которая пропорциональна упругости (порядку) химических связей: ω = k — m F—S—F E v = 4 v = 3 v = 2 v = 1 Qv увеличивается с возрастанием числа колебательных степеней свободы: 3 N – 6(5): Qv(С 4 Н 10) < Qv(С 5 Н 12) O=S=O v = 7 v = 6 v = 5 v = 4 v = 3 v = 2 v = 1 v = 0 SO 2 v = 0 SF 2
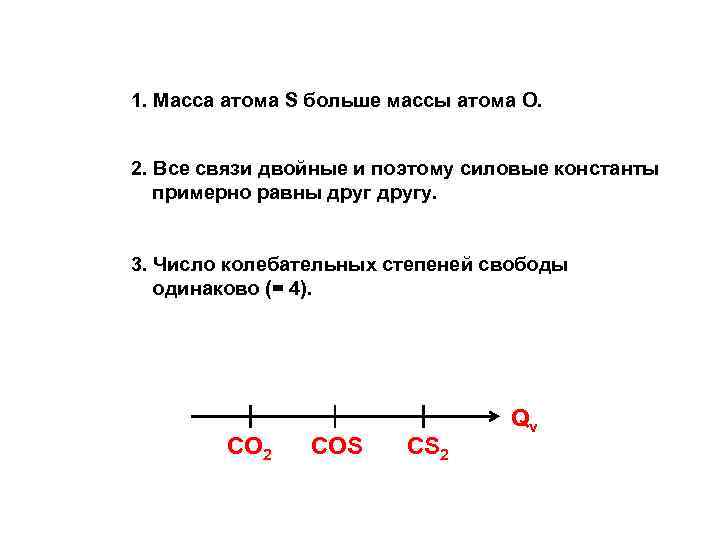 1. Масса атома S больше массы атома О. 2. Все связи двойные и поэтому силовые константы примерно равны другу. 3. Число колебательных степеней свободы одинаково (= 4). CO 2 COS CS 2 Qv
1. Масса атома S больше массы атома О. 2. Все связи двойные и поэтому силовые константы примерно равны другу. 3. Число колебательных степеней свободы одинаково (= 4). CO 2 COS CS 2 Qv
 13. Определить число ядерных спиновых состояний для трехядерной молекулы, если спиновые квантовые числа ядер равны 0, 7/2 и 3/2. ms = +s … –s 2 s + 1 N = (2 s 1 + 1)(2 s 2 + 1)(2 s 3 + 1) = 1 8 4 = 32
13. Определить число ядерных спиновых состояний для трехядерной молекулы, если спиновые квантовые числа ядер равны 0, 7/2 и 3/2. ms = +s … –s 2 s + 1 N = (2 s 1 + 1)(2 s 2 + 1)(2 s 3 + 1) = 1 8 4 = 32
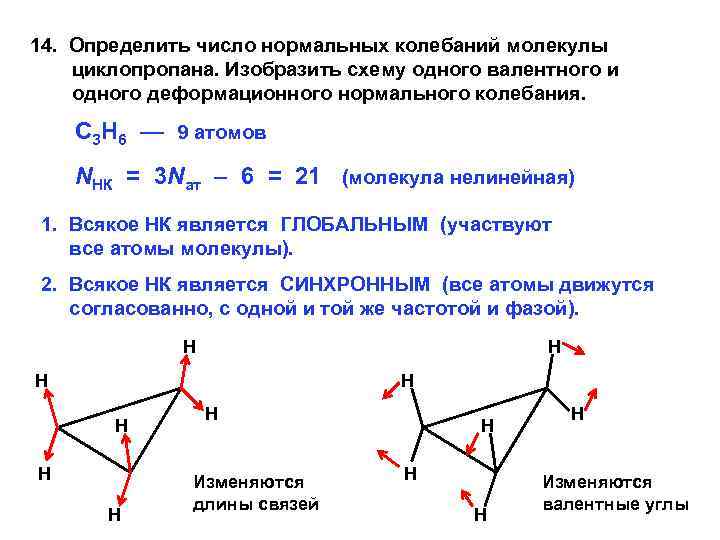 14. Определить число нормальных колебаний молекулы циклопропана. Изобразить схему одного валентного и одного деформационного нормального колебания. C 3 H 6 — 9 атомов NНК = 3 Nат – 6 = 21 (молекула нелинейная) 1. Всякое НК является ГЛОБАЛЬНЫМ (участвуют все атомы молекулы). 2. Всякое НК является СИНХРОННЫМ (все атомы движутся согласованно, с одной и той же частотой и фазой). Н Н Н Н Изменяются длины связей Н Н Изменяются валентные углы
14. Определить число нормальных колебаний молекулы циклопропана. Изобразить схему одного валентного и одного деформационного нормального колебания. C 3 H 6 — 9 атомов NНК = 3 Nат – 6 = 21 (молекула нелинейная) 1. Всякое НК является ГЛОБАЛЬНЫМ (участвуют все атомы молекулы). 2. Всякое НК является СИНХРОННЫМ (все атомы движутся согласованно, с одной и той же частотой и фазой). Н Н Н Н Изменяются длины связей Н Н Изменяются валентные углы
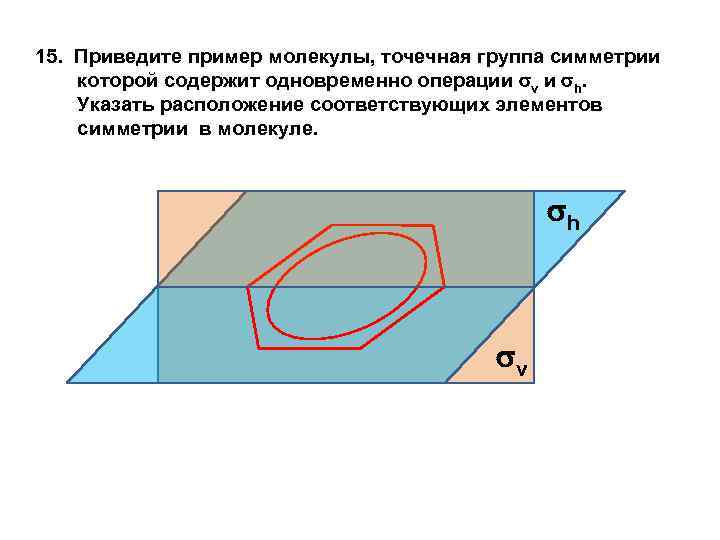 15. Приведите пример молекулы, точечная группа симметрии которой содержит одновременно операции v и h. Указать расположение соответствующих элементов симметрии в молекуле. h v
15. Приведите пример молекулы, точечная группа симметрии которой содержит одновременно операции v и h. Указать расположение соответствующих элементов симметрии в молекуле. h v
 16. Какой тип магнетизма (диа- или пара-) должен проявлять атом бериллия? = 0 ≠ 0 9 Be 4 диамагнетизм парамегнетизм 1 s 2 2 s 2 (4 электрона, образуют две пары, поэтому суммарный электронный спин равен нулю) Ядро содержит 9 нуклонов, из которых 1 неспаренный, поэтому ядерный спин не равен нулю Атом бериллия проявляет парамагнетизм (относительно слабый, так как ядерные магнитные моменты малы, по сравнению с электронными)
16. Какой тип магнетизма (диа- или пара-) должен проявлять атом бериллия? = 0 ≠ 0 9 Be 4 диамагнетизм парамегнетизм 1 s 2 2 s 2 (4 электрона, образуют две пары, поэтому суммарный электронный спин равен нулю) Ядро содержит 9 нуклонов, из которых 1 неспаренный, поэтому ядерный спин не равен нулю Атом бериллия проявляет парамагнетизм (относительно слабый, так как ядерные магнитные моменты малы, по сравнению с электронными)
 17. О каких особенностях строения молекулы можно получить информацию методом КР-спектроскопии? Спектроскопия комбинационного рассеяния — разновидность колебательной спектроскопии. Поэтому ее можно использовать для получения информации о: а) частотах нормальных колебаний; б) массах колеблющихся атомов (групп атомов); в) силовых константах (порядках) химических связей; г) пространственной симметрии и форме молекулы (правила отбора зависят от симметрии молекулы).
17. О каких особенностях строения молекулы можно получить информацию методом КР-спектроскопии? Спектроскопия комбинационного рассеяния — разновидность колебательной спектроскопии. Поэтому ее можно использовать для получения информации о: а) частотах нормальных колебаний; б) массах колеблющихся атомов (групп атомов); в) силовых константах (порядках) химических связей; г) пространственной симметрии и форме молекулы (правила отбора зависят от симметрии молекулы).


