параграф_18_Галогены.ppt
- Количество слайдов: 27

 • К элементам VII группы, главной подгруппы относятся фтор F, хлор Cl, бром Br, иод I, астат At • Общее название - галогены (греч. «солеобразующие» ) - большинство их соединений с металлами представляют собой типичные соли (KCl, Na. Cl и т. д. ).
• К элементам VII группы, главной подгруппы относятся фтор F, хлор Cl, бром Br, иод I, астат At • Общее название - галогены (греч. «солеобразующие» ) - большинство их соединений с металлами представляют собой типичные соли (KCl, Na. Cl и т. д. ).
 • В свободном виде не встречаются Флюорит Ca. F 2
• В свободном виде не встречаются Флюорит Ca. F 2
 Галит Na. Cl
Галит Na. Cl
 Cильвинит KCl Na. Cl
Cильвинит KCl Na. Cl
 • Иод — элемент редкий Иодиды в морской воде • 20 — 30 мг на тонну морской воды В живых организмах, больше всего в водорослях • 5 кг на тонну высушенной морской капусты (ламинарии)
• Иод — элемент редкий Иодиды в морской воде • 20 — 30 мг на тонну морской воды В живых организмах, больше всего в водорослях • 5 кг на тонну высушенной морской капусты (ламинарии)
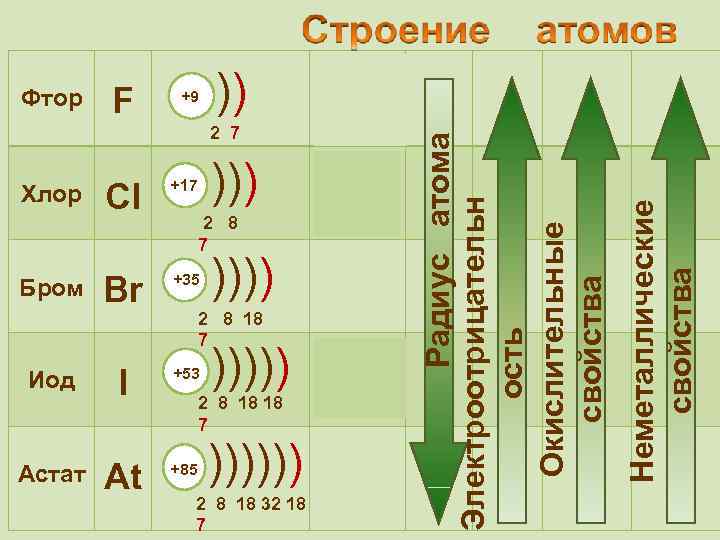 )) 2 s 22 р5 2 7 ))) Cl +17 Br +35 Иод I +53 Астат At +85 Хлор Бром 3 s 23 p 5 2 8 7 )))) 4 s 24 p 5 2 8 18 7 ))))) 5 s 25 p 5 2 8 18 18 7 )))))) 6 s 6 p 2 2 8 18 32 18 7 5 Неметаллические свойства F +9 Радиус атома Электроотрицательн ость Окислительные свойства Фтор
)) 2 s 22 р5 2 7 ))) Cl +17 Br +35 Иод I +53 Астат At +85 Хлор Бром 3 s 23 p 5 2 8 7 )))) 4 s 24 p 5 2 8 18 7 ))))) 5 s 25 p 5 2 8 18 18 7 )))))) 6 s 6 p 2 2 8 18 32 18 7 5 Неметаллические свойства F +9 Радиус атома Электроотрицательн ость Окислительные свойства Фтор
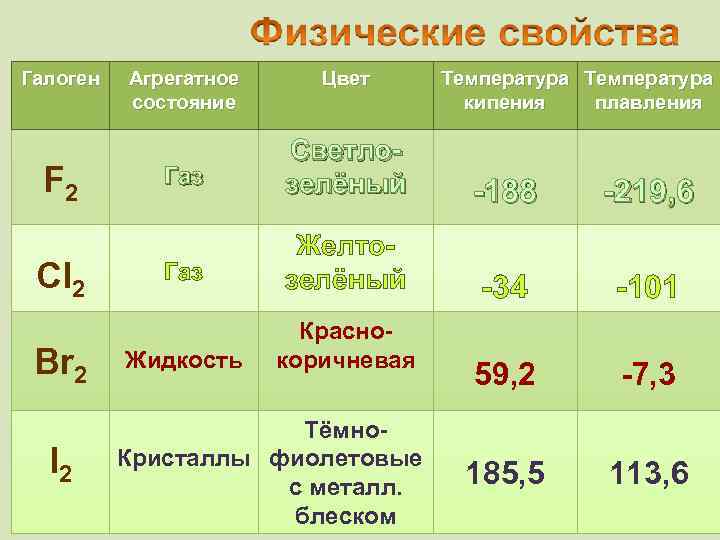 Галоген F 2 Cl 2 Br 2 I 2 Агрегатное состояние Цвет Tемпература Температура кипения плавления Газ Светлозелёный -188 -219, 6 Газ Желтозелёный -34 -101 Жидкость Краснокоричневая 59, 2 -7, 3 185, 5 113, 6 Тёмно. Кристаллы фиолетовые с металл. блеском
Галоген F 2 Cl 2 Br 2 I 2 Агрегатное состояние Цвет Tемпература Температура кипения плавления Газ Светлозелёный -188 -219, 6 Газ Желтозелёный -34 -101 Жидкость Краснокоричневая 59, 2 -7, 3 185, 5 113, 6 Тёмно. Кристаллы фиолетовые с металл. блеском
 9 18, 99 8 7 2 • Название "фтор" (от греческого phthoros - разрушение, гибель) • В свободном состоянии фтор был получен 26 июня 1886 г. французским химиком Муассаном. • Это зеленовато-желтый газ, немного тяжелее воздуха, с характерным запахом и необыкновенной химической активностью. • Ни один из химических элементов не принес химикам столько трагических
9 18, 99 8 7 2 • Название "фтор" (от греческого phthoros - разрушение, гибель) • В свободном состоянии фтор был получен 26 июня 1886 г. французским химиком Муассаном. • Это зеленовато-желтый газ, немного тяжелее воздуха, с характерным запахом и необыкновенной химической активностью. • Ни один из химических элементов не принес химикам столько трагических
 17 35, 45 3 7 8 2 • Хлор был открыт шведским химиком Карлом Шееле в 1774 г. • в 1810 году сэр Гемфри Дэви назвал газ "хлорином"(Chlorine), от греческого "зелёный". • Этот термин используется в английском языке, а в других языках закрепилось название "хлор". • Газ желто-зеленого цвета с резким запахом, ядовит • в 2, 5 раза тяжелее воздуха • в 1 объеме воды при 20 °С растворяется около 2 объемов хлора
17 35, 45 3 7 8 2 • Хлор был открыт шведским химиком Карлом Шееле в 1774 г. • в 1810 году сэр Гемфри Дэви назвал газ "хлорином"(Chlorine), от греческого "зелёный". • Этот термин используется в английском языке, а в других языках закрепилось название "хлор". • Газ желто-зеленого цвета с резким запахом, ядовит • в 2, 5 раза тяжелее воздуха • в 1 объеме воды при 20 °С растворяется около 2 объемов хлора
 35 79, 9 7 18 8 2 79 Вr (50, 56%) 81 Вr (49, 44%) • от греч. bromos – зловоние • единственный неметалл, жидкий при комнатной температуре • тяжелая красно-бурая жидкость с неприятным запахом • пары брома имеют желто-бурый цвет • при температуре – 7, 25° C бром затвердевает, превращаясь в краснокоричневые игольчатые кристаллы со слабым металлическим блеском
35 79, 9 7 18 8 2 79 Вr (50, 56%) 81 Вr (49, 44%) • от греч. bromos – зловоние • единственный неметалл, жидкий при комнатной температуре • тяжелая красно-бурая жидкость с неприятным запахом • пары брома имеют желто-бурый цвет • при температуре – 7, 25° C бром затвердевает, превращаясь в краснокоричневые игольчатые кристаллы со слабым металлическим блеском
 53 7 18 18 8 2 • от греч. iodes—имеющий фиалковый цвет • в парообразное состояние переходит при комнатной t°, не плавясь (сублимация); • пары -фиолетового цвета Иод был открыт в 1811 г. Куртуа в золе морских водорослей, а с 1815 г. Гей-Люссак стал рассматривать его как химический элемент Известны 37 изотопов иода с массовыми числами от 108 до 144. 126, 9
53 7 18 18 8 2 • от греч. iodes—имеющий фиалковый цвет • в парообразное состояние переходит при комнатной t°, не плавясь (сублимация); • пары -фиолетового цвета Иод был открыт в 1811 г. Куртуа в золе морских водорослей, а с 1815 г. Гей-Люссак стал рассматривать его как химический элемент Известны 37 изотопов иода с массовыми числами от 108 до 144. 126, 9
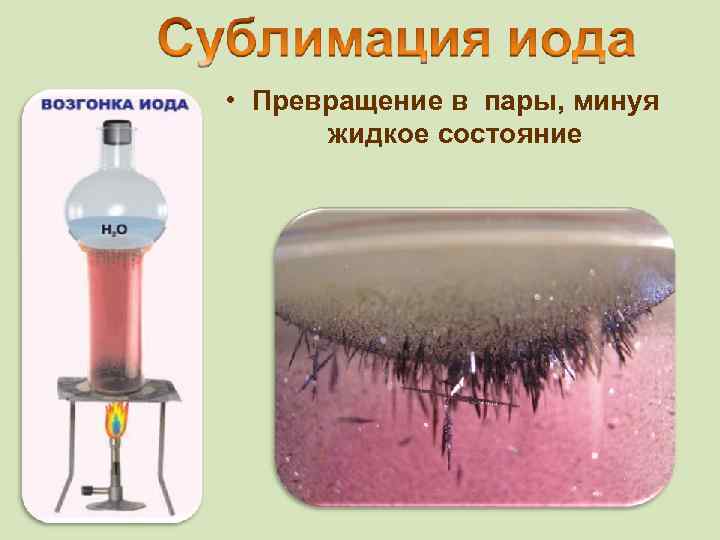 • Превращение в пары, минуя жидкое состояние
• Превращение в пары, минуя жидкое состояние
 • Молекулы галогенов состоят из двух атомов. Cl + Cl → Cl Cl • Связь – ковалентная неполярная
• Молекулы галогенов состоят из двух атомов. Cl + Cl → Cl Cl • Связь – ковалентная неполярная
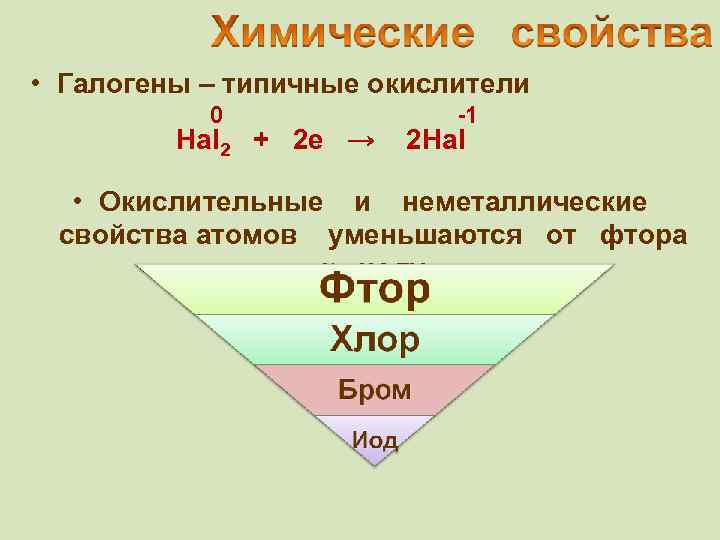 • Галогены – типичные окислители 0 -1 Hal 2 + 2 e → 2 Hal • Окислительные и неметаллические свойства атомов уменьшаются от фтора к иоду
• Галогены – типичные окислители 0 -1 Hal 2 + 2 e → 2 Hal • Окислительные и неметаллические свойства атомов уменьшаются от фтора к иоду
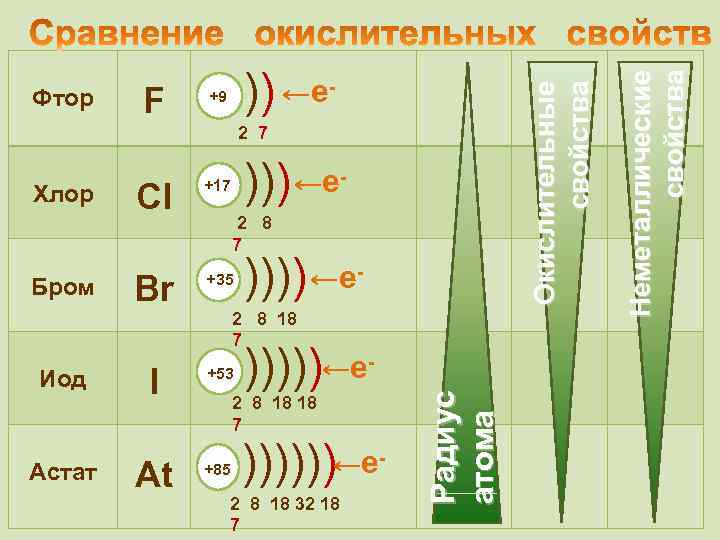 - 2 7 Бром Иод Астат ))) Cl Br +35 I +53 At +85 ←е- 2 8 7 )))) ←е- 2 8 18 7 ← - ))))) е 2 8 18 18 7 ))))))←е - 2 8 18 32 18 7 Радиус атома Хлор +17 Неметаллические свойства F )) ←е +9 Окислительные свойства Фтор
- 2 7 Бром Иод Астат ))) Cl Br +35 I +53 At +85 ←е- 2 8 7 )))) ←е- 2 8 18 7 ← - ))))) е 2 8 18 18 7 ))))))←е - 2 8 18 32 18 7 Радиус атома Хлор +17 Неметаллические свойства F )) ←е +9 Окислительные свойства Фтор
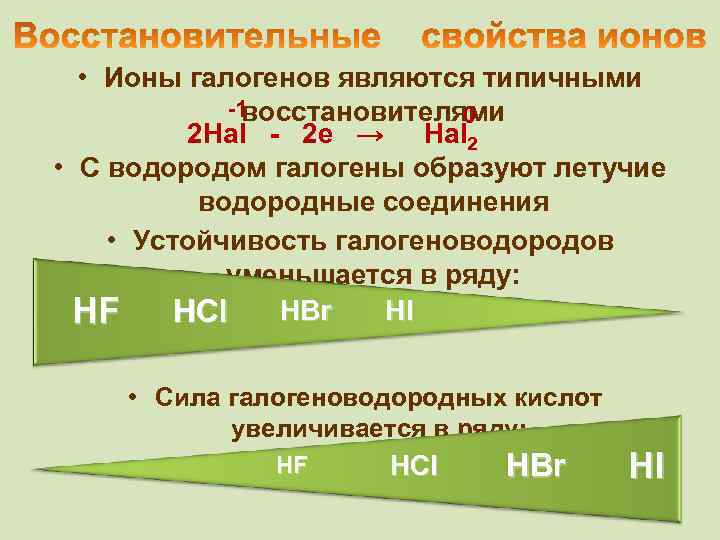 • Ионы галогенов являются типичными -1 восстановителями 0 2 Hal - 2 e → Hal 2 • С водородом галогены образуют летучие водородные соединения • Устойчивость галогеноводородов уменьшается в ряду: HI HF HCl HBr • Cила галогеноводородных кислот увеличивается в ряду: HF HCl HBr HI
• Ионы галогенов являются типичными -1 восстановителями 0 2 Hal - 2 e → Hal 2 • С водородом галогены образуют летучие водородные соединения • Устойчивость галогеноводородов уменьшается в ряду: HI HF HCl HBr • Cила галогеноводородных кислот увеличивается в ряду: HF HCl HBr HI
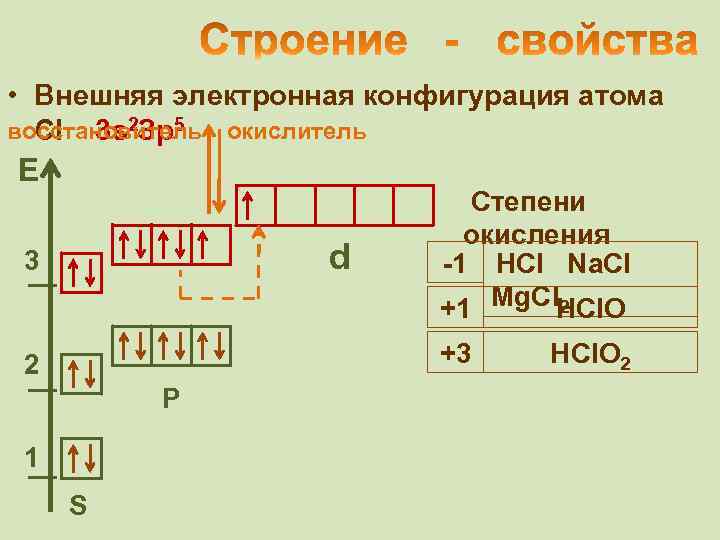 • Внешняя электронная конфигурация атома восстановитель окислитель Cl 3 s 2 Зр5 Е d 3 Степени окисления -1 HCl Na. Cl 2 +1 Mg. Cl. HCl. O +3 2 Р 1 S HCl. O 2
• Внешняя электронная конфигурация атома восстановитель окислитель Cl 3 s 2 Зр5 Е d 3 Степени окисления -1 HCl Na. Cl 2 +1 Mg. Cl. HCl. O +3 2 Р 1 S HCl. O 2
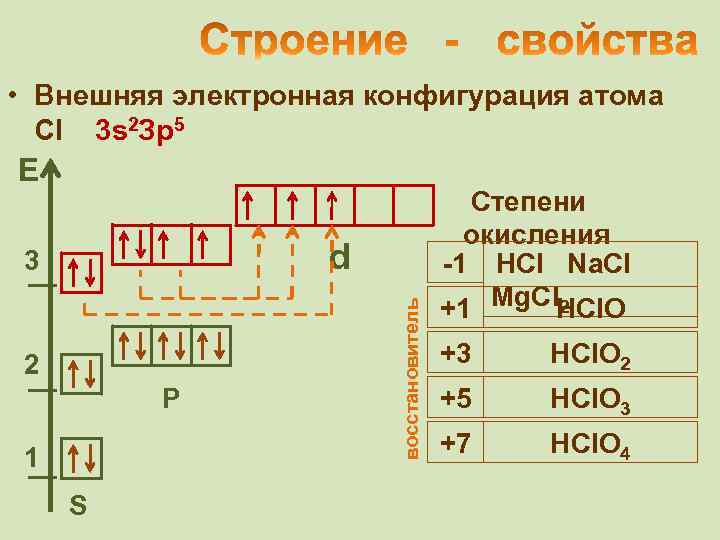 • Внешняя электронная конфигурация атома Cl 3 s 2 Зр5 Е 2 Р 1 S восстановитель d 3 Степени окисления -1 HCl Na. Cl 2 +1 Mg. Cl. HCl. O +3 HCl. O 2 +5 HCl. O 3 +7 HCl. O 4
• Внешняя электронная конфигурация атома Cl 3 s 2 Зр5 Е 2 Р 1 S восстановитель d 3 Степени окисления -1 HCl Na. Cl 2 +1 Mg. Cl. HCl. O +3 HCl. O 2 +5 HCl. O 3 +7 HCl. O 4
 1. Взаимодействие с металлами Хлор непосредственно реагирует почти со всеми металлами (с некоторыми только в присутствии -1 влаги или при нагревании): 2 Na + Cl 2 → 2 Na. Cl -1 2 Fe + 3 Cl 2 → 2 Fe. Cl 3 2. Взаимодействие с неметаллами C неметаллами (кроме углерода, азота, кислорода и инертных газов), образует соответствующие хлориды. -1 Cl 2 + H 2 → 2 HCl -1 5 Cl 2 + 2 P → 2 PCl 5
1. Взаимодействие с металлами Хлор непосредственно реагирует почти со всеми металлами (с некоторыми только в присутствии -1 влаги или при нагревании): 2 Na + Cl 2 → 2 Na. Cl -1 2 Fe + 3 Cl 2 → 2 Fe. Cl 3 2. Взаимодействие с неметаллами C неметаллами (кроме углерода, азота, кислорода и инертных газов), образует соответствующие хлориды. -1 Cl 2 + H 2 → 2 HCl -1 5 Cl 2 + 2 P → 2 PCl 5
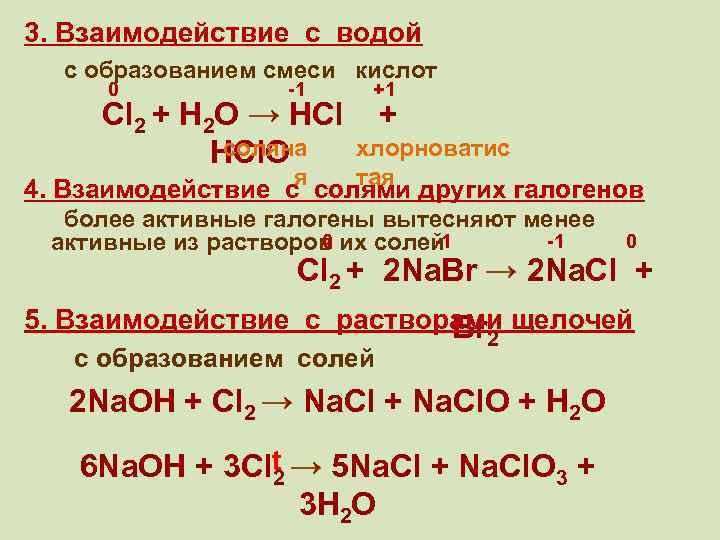 3. Взаимодействие с водой с образованием смеси кислот 0 -1 +1 я тая Cl 2 + H 2 О → HCl + соляна хлорноватис HCl. O 4. Взаимодействие с солями других галогенов более активные галогены вытесняют менее 0 -1 -1 активные из растворов их солей 0 Cl 2 + 2 Na. Br → 2 Na. Cl + 5. Взаимодействие с растворами щелочей Br с образованием солей 2 2 Na. OH + Cl 2 → Na. Cl + Na. Cl. O + H 2 O 6 Na. OH + 3 Clt → 5 Na. Cl + Na. Cl. O 3 + 2 3 H 2 O
3. Взаимодействие с водой с образованием смеси кислот 0 -1 +1 я тая Cl 2 + H 2 О → HCl + соляна хлорноватис HCl. O 4. Взаимодействие с солями других галогенов более активные галогены вытесняют менее 0 -1 -1 активные из растворов их солей 0 Cl 2 + 2 Na. Br → 2 Na. Cl + 5. Взаимодействие с растворами щелочей Br с образованием солей 2 2 Na. OH + Cl 2 → Na. Cl + Na. Cl. O + H 2 O 6 Na. OH + 3 Clt → 5 Na. Cl + Na. Cl. O 3 + 2 3 H 2 O
 1. В промышленности: электролиз расплава или раствора хлорида натрия 2 Na. Cl → 2 Na + Cl 2 2. В лаборатории: 4 HСl + Mn. O 2 → Mn. Cl 2 + Cl 2 ↑+ H 2 O HСl + Mn. O ↑+ 2 H 16 HСl + 2 KMn. O 4 → 2 KСl + 2 Mn. Cl 2 + 5 Cl 2 ↑+ 8 H 2 O
1. В промышленности: электролиз расплава или раствора хлорида натрия 2 Na. Cl → 2 Na + Cl 2 2. В лаборатории: 4 HСl + Mn. O 2 → Mn. Cl 2 + Cl 2 ↑+ H 2 O HСl + Mn. O ↑+ 2 H 16 HСl + 2 KMn. O 4 → 2 KСl + 2 Mn. Cl 2 + 5 Cl 2 ↑+ 8 H 2 O
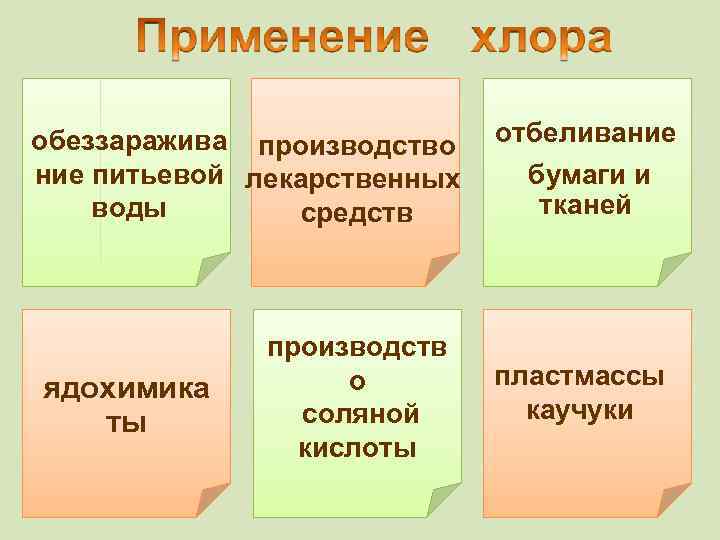 обеззаражива производство отбеливание бумаги и ние питьевой лекарственных тканей воды средств ядохимика ты производств о соляной кислоты пластмассы каучуки
обеззаражива производство отбеливание бумаги и ние питьевой лекарственных тканей воды средств ядохимика ты производств о соляной кислоты пластмассы каучуки
 В медицине - 5 % спиртовой раствор йода используется для дезинфекции кожи вокруг повреждения - В рентгенологических и томографических исследованиях применяются йодсодержащие В технике - Галоге нная ла мпа — лампа накаливания, контрастные препараты в баллон которой добавлены пары галогенов (брома или йода) - Лазерный термоядерный синтез - иодорганические соединения применяются для производства сверхмощных газовых лазеров на возбужденных атомах
В медицине - 5 % спиртовой раствор йода используется для дезинфекции кожи вокруг повреждения - В рентгенологических и томографических исследованиях применяются йодсодержащие В технике - Галоге нная ла мпа — лампа накаливания, контрастные препараты в баллон которой добавлены пары галогенов (брома или йода) - Лазерный термоядерный синтез - иодорганические соединения применяются для производства сверхмощных газовых лазеров на возбужденных атомах

 • Что значит название «Галогены» ? • В чём сходство электронного строения этих элементов? • Какие свойства в окислительновосстановительном плане проявляют галогены? • Какой галоген наиболее химически активен? • Как изменяется активность галогенов вниз по группе?
• Что значит название «Галогены» ? • В чём сходство электронного строения этих элементов? • Какие свойства в окислительновосстановительном плане проявляют галогены? • Какой галоген наиболее химически активен? • Как изменяется активность галогенов вниз по группе?



