prezentatsia_1_po_Nissen_NKA.pptx
- Количество слайдов: 10

+, K+-ATPазы Na Взаимодействие белками-партнерами По обзору “Na+, K+-ATPase as a docking station: protein–protein complexes of the Na+, K+-ATPase” Linda Reinhard • Henning Tidow • Michael J. Clausen • Poul Nissen Лопачев А. В. с
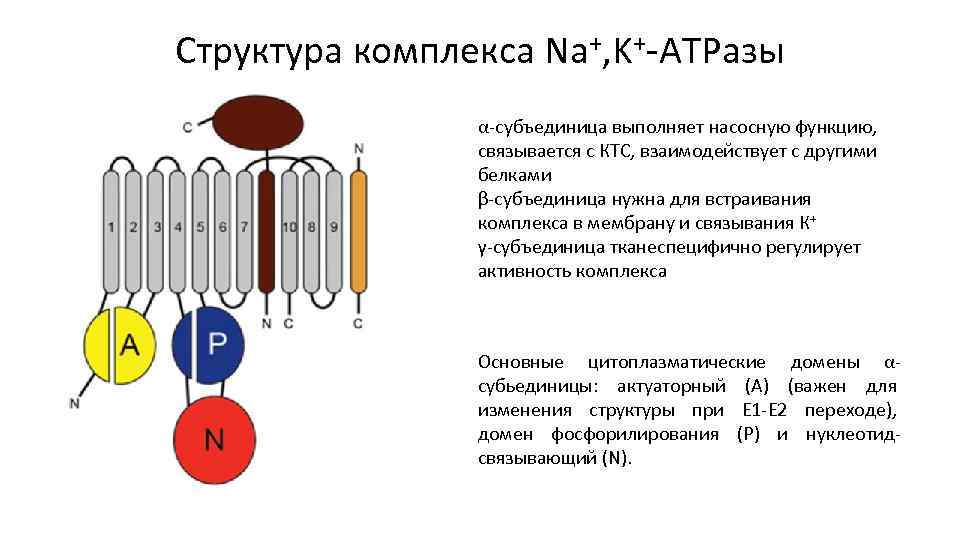
Структура комплекса Na+, K+-ATPазы α-субъединица выполняет насосную функцию, связывается с КТС, взаимодействует с другими белками β-субъединица нужна для встраивания комплекса в мембрану и связывания К+ γ-субъединица тканеспецифично регулирует активность комплекса Основные цитоплазматические домены αсубьединицы: актуаторный (А) (важен для изменения структуры при E 1 -E 2 переходе), домен фосфорилирования (P) и нуклеотидсвязывающий (N).
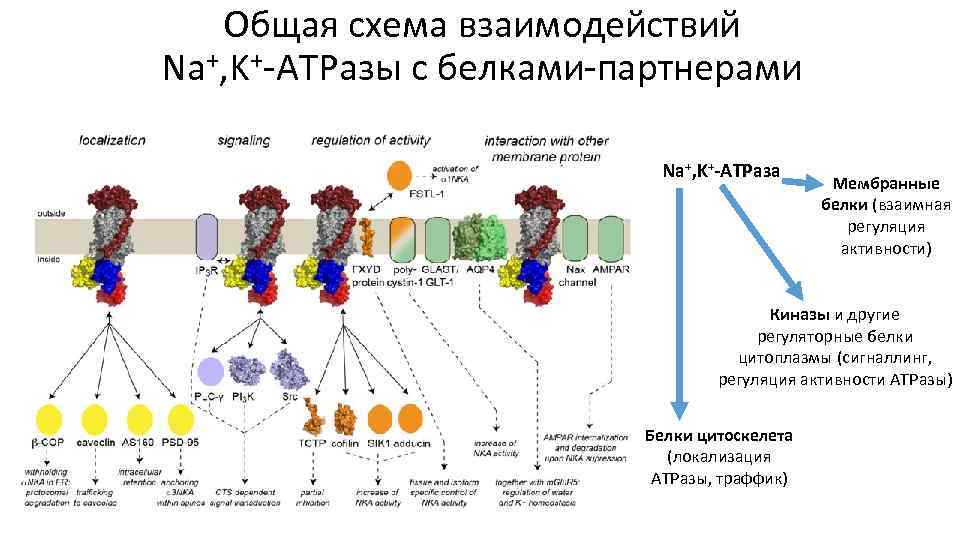
Общая схема взаимодействий Na+, K+-ATPазы с белками-партнерами Na+, K+-ATPаза Мембранные белки (взаимная регуляция активности) Киназы и другие регуляторные белки цитоплазмы (сигналлинг, регуляция активности ATPазы) Белки цитоскелета (локализация ATPазы, траффик)

Регуляция траффика Na+, K+-ATPазы 1. Шаперон Bi. P контролирует правильную сборку αβ комплекса. 2. β-COP на ЭПР не дает α-субъединице без β встраиваться в плазматическую мембрану. 3. Кавеолин (структурный белок 21 -24 к. Да) связывается с α 1 -субъединицей в двух сайтах: А-домене и M 10. Кавеолы – участки мембраны с холестерином, гликосфинголипидами и сфингомиелином. 4. AS 160 участвует в эндоцитозе Na+, K+-ATPазы. Регулируется Akt и AMPK (ингибирование AMPK вызывает интернализацию Na+, K+-ATPазы). 5. α 3 локализуется в шипиках дендритов, связываясь с PSD-95 при помощи N -конца.

Роль Na+, K+-ATPазы в клеточном сигналлинге Na+, K+-ATPаза взаимодействует с Src; предложенный механизм: • Взаимодействие с Src при помощи CD 2 участка (A-домен) • Src – семейство нерецепторных тирозиновых киназ. Активируются при дефосфорилировании Y 530 и фосфориилировании Y 419. Последовательность Na. Ktide в N-конце α 1 ингибирует активность Src. • Для связывания Src с Na+, K+-ATPазой нужно взаимодействие с SH 2 и SH 3 доменами Src. • При связывании уабаина с Na+, K+-ATPазой происходит высвобождение Src и ее активация. • При связывании уабаина с Na+, K+-ATPазой A-домен проворачивается на 10°, и смещается TM 1 -2 участок, который отвечает за белок-белковые взаимодействия. • Src частично высвобождается при каталитическом цикле Na+, K+-ATPазы, однако, связь с Src не влияет на каталитическую функцию. Однако, есть противоречия: • Y 255, с которым могла бы связываться Src, есть только в α 1 и только у млекопитающих. • Na. Ktide спрятан в N-домене в конформации, в которой он должен взаимодействовать с Src. • Изменение концентрации ATP и ADP не влияет на активность Src.
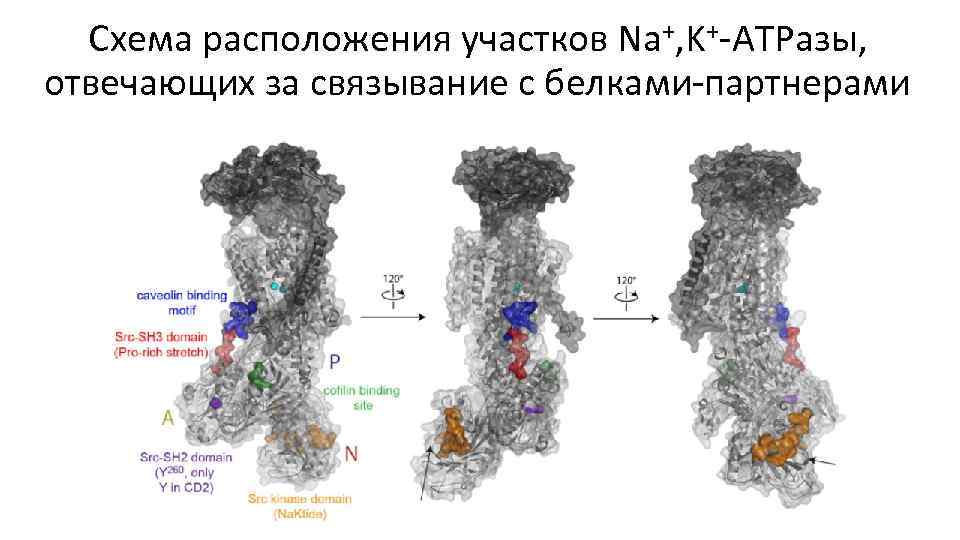
Схема расположения участков Na+, K+-ATPазы, отвечающих за связывание с белками-партнерами
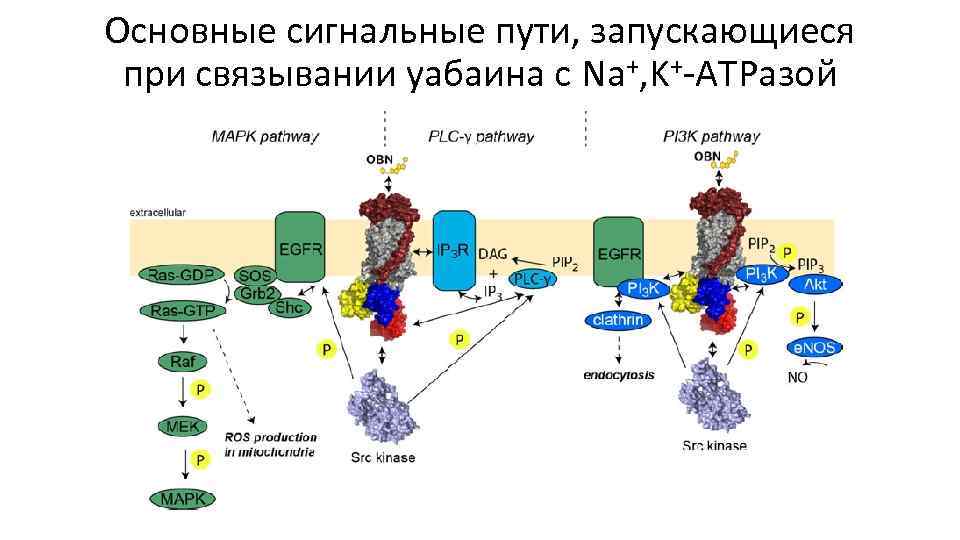
Основные сигнальные пути, запускающиеся при связывании уабаина с Na+, K+-ATPазой

Другие белки-партнеры Na+, K+-ATPазы • TCTP (translationally controlled tumor protein) связан с ответом на стресс, ростовые и цитотоксические факторы. При связывании с Na+, K+-ATPазой уменьшает ее активность, а также высвобождает Src, увеличивая ее активность. • Аддуцин – белок цитоскелета, связанный с клеточной адгезией, миграцией, межклеточными контактами. Мутантный аддуцин сильнее связывается с Na+, K+-ATPазой, активируя ее, чем вызывает гипертензию.

Регуляторы активности Na+, K+-ATPазы • SIK 1 (Salt-inducible kinase 1) активирует Na+, K+-ATPазу через комлекс с PP 2 A и PME-1, а также через увеличение экспрессии ATP 1 B 1. • Кофилин – белок, взаимодействующий с актином. Фосфорилированная форма связывается с Na+, K+-ATPазой, увеличивая ее активность. Есть связь с уабаин-зависимой активацией ERK 1/2 и дефосфорилированием кофилина. Дефосфорилированный кофилин связан с реорганизацией цитоскелета и регуляцией объема клетки. • FSTL-1 связывается с α 1 -субъединицей Na+, K+-ATPазы, увеличивая ее активность. Влияет на мембранный потенциал и возбудимость нейронов.

Мембранные белки, взаимодействующие с Na+, K+-ATPазой • GLAST взаимодействует с Na+, K+-ATPазой. Он использует градиент Na+. Увеличение количества GLAST приводит к увеличению активности Na+, K+-ATPазы. Возможен комплекс с Src, т. к. ингибирование Src уменьшает активность GLAST. • Nax - Na+ каналы, экспрессируемые в особых глиальных клетках, которые отвечают за определение концентрации Na+ в организме. α 1 и α 2 субъединицы Na+, K+-ATPазы напрямую взаимодействует с ними. Увеличение ее активности приводит к усилению метаболизма глюкозы и увеличению количества лактата. • D 1 и D 2 уменьшают активность Na+, K+-ATPазы как физическим взаимодействием через PSD 95, так и через PKC. • AQP 4 взаимодействует с α 1 и α 2 субъединицами Na+, K+-ATPазы. Предположительно, регулирует баланс K+ и нейрон-глиальные связи в мозге. • AMPAR непосредственно взаимодействует с Na+, K+-ATPазой. • Polycystin-1 взаимодействует с Na+, K+-ATPазой в эпителиальных клетках, увеличивая ее активность.
prezentatsia_1_po_Nissen_NKA.pptx