 Изучение термодинамики и кинетики химических реакций в школе
Изучение термодинамики и кинетики химических реакций в школе
 Цель изучения? Место изучения? Порядок изучения?
Цель изучения? Место изучения? Порядок изучения?
 Химическая кинетика - раздел химии, изучающий скорость и механизмы химических реакций Термодинамика - наука о макросистемах Химическая кинетика рассматривает механизм реакций на уровне отдельных частиц Кинетика и термодинамика дают целостное представление о закономерностях протекания реакций
Химическая кинетика - раздел химии, изучающий скорость и механизмы химических реакций Термодинамика - наука о макросистемах Химическая кинетика рассматривает механизм реакций на уровне отдельных частиц Кинетика и термодинамика дают целостное представление о закономерностях протекания реакций
 Термодинамика Тепловой эффект реакции Эндо- и экзотермические реакции Энтальпия ? Энтропия? ? Энергия Гиббса? Кинетика Скорость химической реакции Факторы влияющие на скорость ? Закон действующих масс? Температурный коэффициент Вант -Гоффа Катализ Обратимость реакций Равновесие и его смещение ? Константа равновесия?
Термодинамика Тепловой эффект реакции Эндо- и экзотермические реакции Энтальпия ? Энтропия? ? Энергия Гиббса? Кинетика Скорость химической реакции Факторы влияющие на скорость ? Закон действующих масс? Температурный коэффициент Вант -Гоффа Катализ Обратимость реакций Равновесие и его смещение ? Константа равновесия?
 ТЕМА 5. ИЗМЕНЕНИЯ, ПРОИСХОДЯЩИЕ С ВЕЩЕСТВАМИ – 10: ТЕМА 3. ХИМИЯ ПРОСТЫХ ВЕЩЕСТВ — 11: 34. Физические и химические явления. Понятие об экзо- и эндотермических реакциях. Реакции горения как частный случай экзотермических реакций. 34. Воздух. Строение пламени. Экология воздуха 38. Реакции разложения. Понятие о скорости химических реакций. Катализаторы. Ферменты. 36. Решение задач по теме «термохимия» 39. Реакции соединения. Каталитические и некаталитические реакции. Обратимые и необратимые реакции. 51. Кинетика. Скорость химических реакций ТЕМА 3. ХИМИЧЕСКИЕ РЕАКЦИИ – 10 -15: 19. Классификация химических реакций в органической и неорганической химии. 20. Скорость химических реакций. 21. Факторы, влияющие на скорость химической реакции. 22. Обратимость химических реакций. Химическое равновесие. 35. Термохимические расчеты ТЕМА 5 ХИМИЯ НЕМЕТАЛЛОВ — 15: 52. Кинетика. Обратимые химические реакции ТЕМА 6 ХИМИЧЕСКИЕ РЕАКЦИИ — 7: 38. Классификация химических реакций. Термохимические расчеты 40. Кинетика. Скорость химических реакций 41. Обратимые химические реакции. Принцип ле – шателье
ТЕМА 5. ИЗМЕНЕНИЯ, ПРОИСХОДЯЩИЕ С ВЕЩЕСТВАМИ – 10: ТЕМА 3. ХИМИЯ ПРОСТЫХ ВЕЩЕСТВ — 11: 34. Физические и химические явления. Понятие об экзо- и эндотермических реакциях. Реакции горения как частный случай экзотермических реакций. 34. Воздух. Строение пламени. Экология воздуха 38. Реакции разложения. Понятие о скорости химических реакций. Катализаторы. Ферменты. 36. Решение задач по теме «термохимия» 39. Реакции соединения. Каталитические и некаталитические реакции. Обратимые и необратимые реакции. 51. Кинетика. Скорость химических реакций ТЕМА 3. ХИМИЧЕСКИЕ РЕАКЦИИ – 10 -15: 19. Классификация химических реакций в органической и неорганической химии. 20. Скорость химических реакций. 21. Факторы, влияющие на скорость химической реакции. 22. Обратимость химических реакций. Химическое равновесие. 35. Термохимические расчеты ТЕМА 5 ХИМИЯ НЕМЕТАЛЛОВ — 15: 52. Кинетика. Обратимые химические реакции ТЕМА 6 ХИМИЧЕСКИЕ РЕАКЦИИ — 7: 38. Классификация химических реакций. Термохимические расчеты 40. Кинетика. Скорость химических реакций 41. Обратимые химические реакции. Принцип ле – шателье
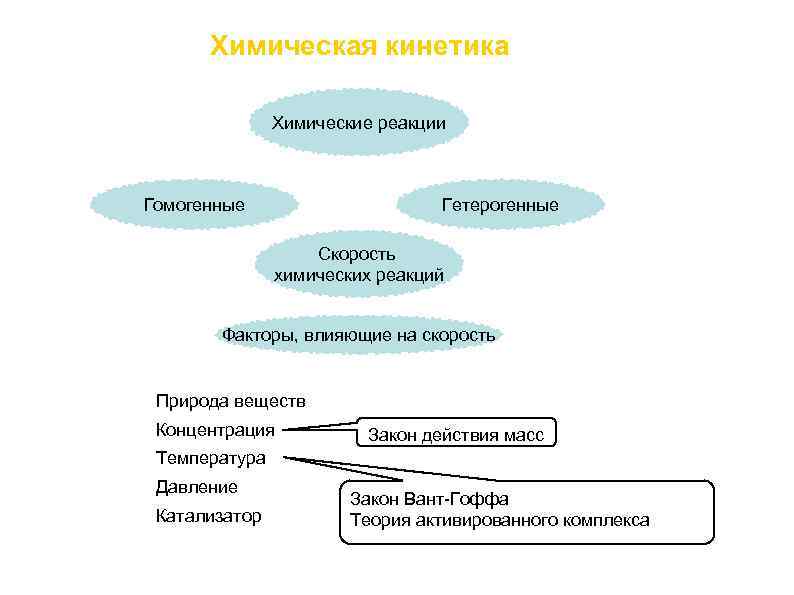 Химическая кинетика Химические реакции Гомогенные Гетерогенные Скорость химических реакций Факторы, влияющие на скорость • Природа веществ • Концентрация Закон действия масс • Температура • Давление • Катализатор Закон Вант-Гоффа Теория активированного комплекса
Химическая кинетика Химические реакции Гомогенные Гетерогенные Скорость химических реакций Факторы, влияющие на скорость • Природа веществ • Концентрация Закон действия масс • Температура • Давление • Катализатор Закон Вант-Гоффа Теория активированного комплекса
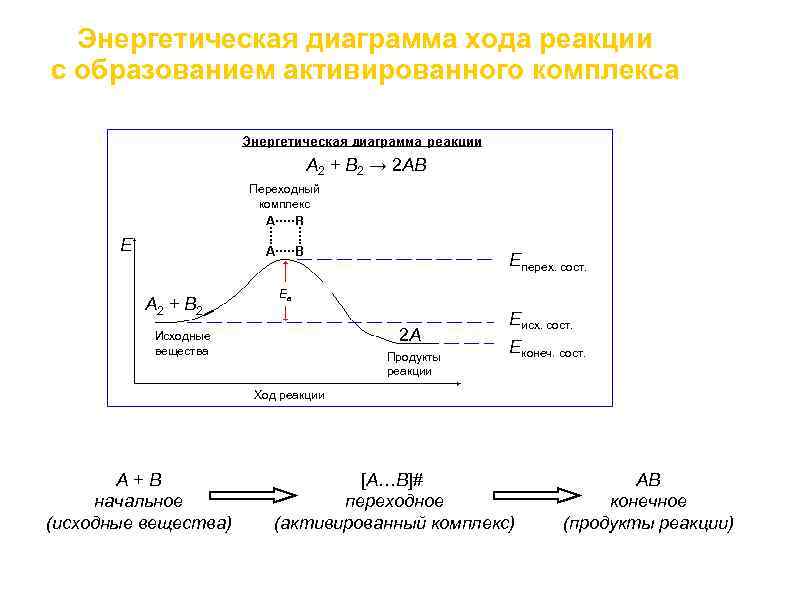 Энергетическая диаграмма хода реакции с образованием активированного комплекса A 2 + B 2 → 2 AB Переходный комплекс E Еперех. сост. A 2 + B 2 Ea 2 A Продукты B Исходные вещества Еисх. сост. Еконеч. сост. реакции Ход реакции А+В начальное (исходные вещества) [А…В]# переходное (активированный комплекс) АВ конечное (продукты реакции)
Энергетическая диаграмма хода реакции с образованием активированного комплекса A 2 + B 2 → 2 AB Переходный комплекс E Еперех. сост. A 2 + B 2 Ea 2 A Продукты B Исходные вещества Еисх. сост. Еконеч. сост. реакции Ход реакции А+В начальное (исходные вещества) [А…В]# переходное (активированный комплекс) АВ конечное (продукты реакции)
![Катализ Положительный Отрицательный [A…B]' G Каталитические яды – [B…AK]' ∆(∆G)' [A…K]' A+B Автокатализ Промоторы Катализ Положительный Отрицательный [A…B]' G Каталитические яды – [B…AK]' ∆(∆G)' [A…K]' A+B Автокатализ Промоторы](https://present5.com/presentation/3/-96954499_438542213.pdf-img/-96954499_438542213.pdf-8.jpg) Катализ Положительный Отрицательный [A…B]' G Каталитические яды – [B…AK]' ∆(∆G)' [A…K]' A+B Автокатализ Промоторы – вещества, +K Gисходное Путь реакции вещества, ухудшающие действие катализаторов. AB Gконечное усиливающие действие катализаторов. Ингибиторы – вещества, уменьшающие скорость реакции.
Катализ Положительный Отрицательный [A…B]' G Каталитические яды – [B…AK]' ∆(∆G)' [A…K]' A+B Автокатализ Промоторы – вещества, +K Gисходное Путь реакции вещества, ухудшающие действие катализаторов. AB Gконечное усиливающие действие катализаторов. Ингибиторы – вещества, уменьшающие скорость реакции.
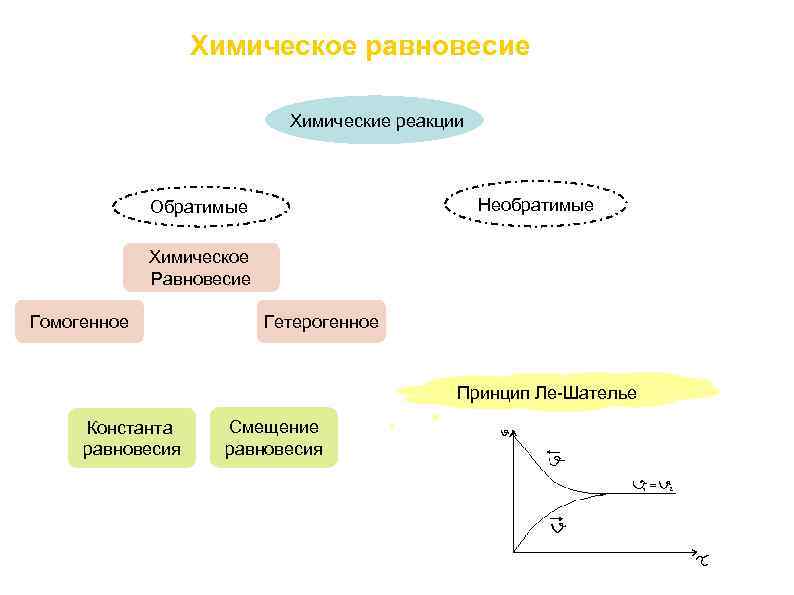 Химическое равновесие Химические реакции Необратимые Обратимые Химическое Равновесие Гомогенное Гетерогенное Принцип Ле-Шателье Константа равновесия Смещение равновесия
Химическое равновесие Химические реакции Необратимые Обратимые Химическое Равновесие Гомогенное Гетерогенное Принцип Ле-Шателье Константа равновесия Смещение равновесия