 Изопроцессы в газах 10 класс учитель: Курочкина Н. А.
Изопроцессы в газах 10 класс учитель: Курочкина Н. А.
 Цель: установить зависимость между двумя макроскопическими параметрами газа при неизменном третьем.
Цель: установить зависимость между двумя макроскопическими параметрами газа при неизменном третьем.
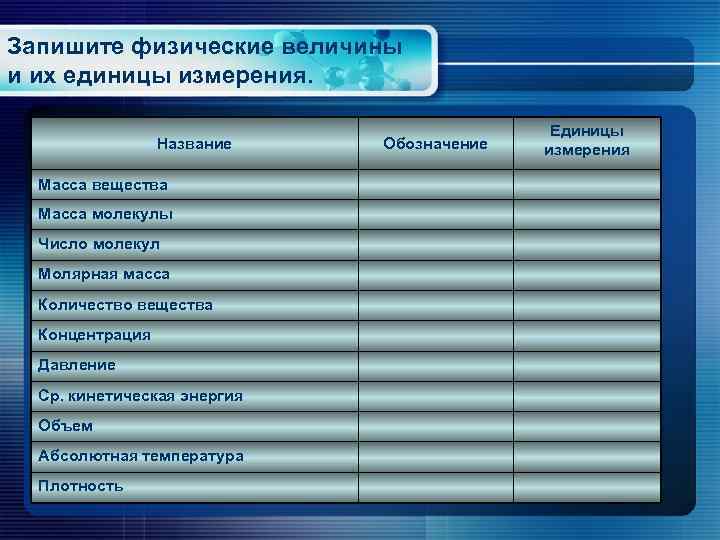 Запишите физические величины и их единицы измерения. Название Масса вещества Масса молекулы Число молекул Молярная масса Количество вещества Концентрация Давление Ср. кинетическая энергия Объем Абсолютная температура Плотность Обозначение Единицы измерения
Запишите физические величины и их единицы измерения. Название Масса вещества Масса молекулы Число молекул Молярная масса Количество вещества Концентрация Давление Ср. кинетическая энергия Объем Абсолютная температура Плотность Обозначение Единицы измерения
 Изопроцесс, при котором один из макроскопических параметров состояния данной массы газа остается постоянным. V, p, Т
Изопроцесс, при котором один из макроскопических параметров состояния данной массы газа остается постоянным. V, p, Т
 Изо – (постоянный) Изобарный изопроцессы Изохорный Изотермический
Изо – (постоянный) Изобарный изопроцессы Изохорный Изотермический
 Изотермический процесс ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ МАССЫ ГАЗА ПРИ ПОСТОЯННОЙ ТЕМПЕРАТУРЕ. Т = const m = const
Изотермический процесс ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ МАССЫ ГАЗА ПРИ ПОСТОЯННОЙ ТЕМПЕРАТУРЕ. Т = const m = const
 Изотермический процесс Из уравнения Клапейрона – Менделеева следует: p. V = const = m RT M
Изотермический процесс Из уравнения Клапейрона – Менделеева следует: p. V = const = m RT M
 Закон Бойля – Мариотта. Закон экспериментально получен в: • 1662 г. Р. Бойлем; • 1676 г. Э. Мариоттом. T - const Р. Бойль Для газа данной массы при постоянной температуре произведение давления газа на его объем постоянно: p 1 V 1 = p 2 V 2
Закон Бойля – Мариотта. Закон экспериментально получен в: • 1662 г. Р. Бойлем; • 1676 г. Э. Мариоттом. T - const Р. Бойль Для газа данной массы при постоянной температуре произведение давления газа на его объем постоянно: p 1 V 1 = p 2 V 2
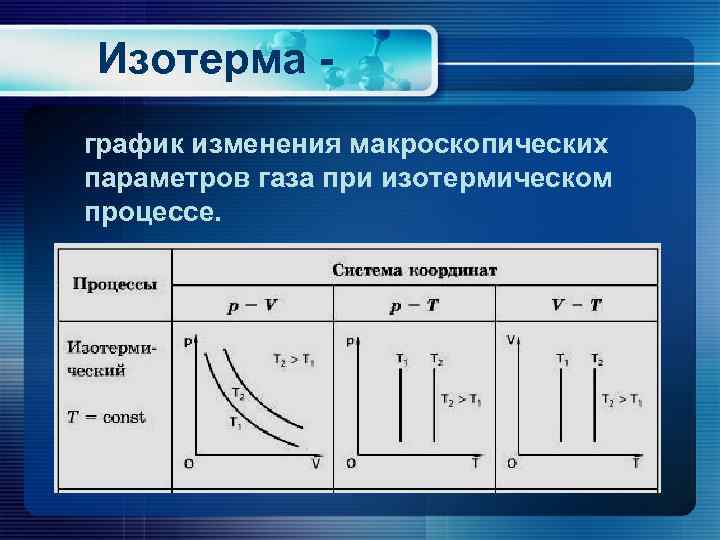 Изотерма график изменения макроскопических параметров газа при изотермическом процессе.
Изотерма график изменения макроскопических параметров газа при изотермическом процессе.
 Изобарный процесс ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ МАССЫ ГАЗА ПРИ ПОСТОЯННОМ ДАВЛЕНИИ. P = const m = const
Изобарный процесс ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ МАССЫ ГАЗА ПРИ ПОСТОЯННОМ ДАВЛЕНИИ. P = const m = const
 Изобарный процесс Из уравнения Клапейрона – Менделеева следует: V T = const = m. R Mp
Изобарный процесс Из уравнения Клапейрона – Менделеева следует: V T = const = m. R Mp
 Закон Гей-Люссака. Закон экспериментально получен в 1802 г. p - const Для газа данной массы при постоянном давлении отношение объема газа к его термодинамической температуре постоянно: V 1 / T 1 = V 2 / T 2 ГЕЙ-ЛЮССАК Жозеф Луи
Закон Гей-Люссака. Закон экспериментально получен в 1802 г. p - const Для газа данной массы при постоянном давлении отношение объема газа к его термодинамической температуре постоянно: V 1 / T 1 = V 2 / T 2 ГЕЙ-ЛЮССАК Жозеф Луи
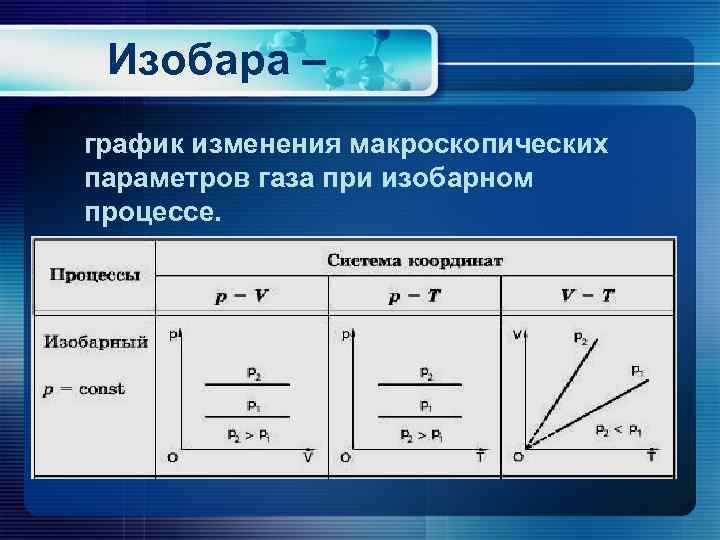 Изобара – график изменения макроскопических параметров газа при изобарном процессе.
Изобара – график изменения макроскопических параметров газа при изобарном процессе.
 Изохорный процесс ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ МАССЫ ГАЗА ПРИ ПОСТОЯННОМ ОБЪЕМЕ. V = const m = const
Изохорный процесс ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ МАССЫ ГАЗА ПРИ ПОСТОЯННОМ ОБЪЕМЕ. V = const m = const
 Изохорный процесс Из уравнения Клапейрона – Менделеева следует: p T = const = m. R MV
Изохорный процесс Из уравнения Клапейрона – Менделеева следует: p T = const = m. R MV
 Закон Шарля. Закон экспериментально получен в 1787 г. V - const Для газа данной массы при постоянном объеме отношение давления газа к его термодинамической температуре постоянно: p 1 / T 1 = p 2 / T 2
Закон Шарля. Закон экспериментально получен в 1787 г. V - const Для газа данной массы при постоянном объеме отношение давления газа к его термодинамической температуре постоянно: p 1 / T 1 = p 2 / T 2
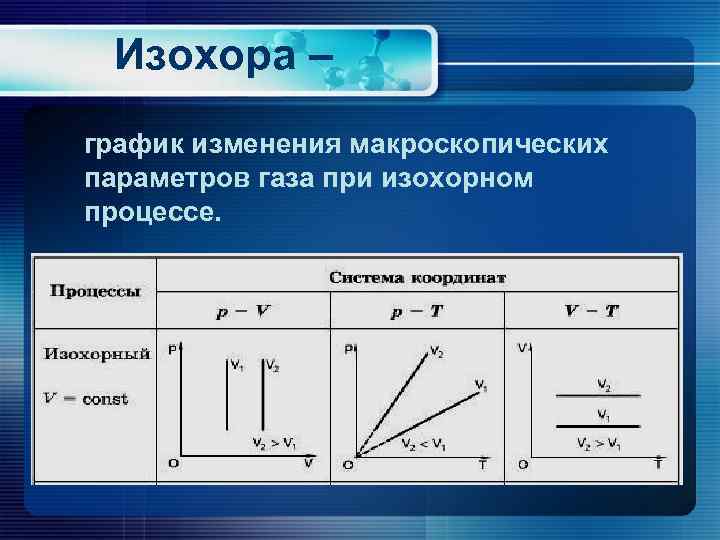 Изохора – график изменения макроскопических параметров газа при изохорном процессе.
Изохора – график изменения макроскопических параметров газа при изохорном процессе.
 Циклы.
Циклы.