 Изопроцессы в газах 10 класс
Изопроцессы в газах 10 класс
 Цель: установить зависимость между двумя макроскопическими параметрами газа при неизменном третьем.
Цель: установить зависимость между двумя макроскопическими параметрами газа при неизменном третьем.
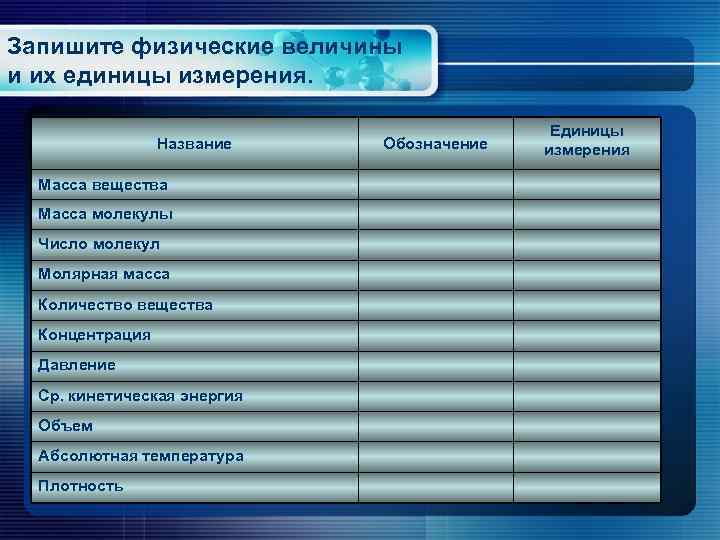 Запишите физические величины и их единицы измерения. Единицы Название Обозначение измерения Масса вещества Масса молекулы Число молекул Молярная масса Количество вещества Концентрация Давление Ср. кинетическая энергия Объем Абсолютная температура Плотность
Запишите физические величины и их единицы измерения. Единицы Название Обозначение измерения Масса вещества Масса молекулы Число молекул Молярная масса Количество вещества Концентрация Давление Ср. кинетическая энергия Объем Абсолютная температура Плотность
 Изопроцесс - процесс, при котором один из макроскопических параметров состояния данной массы газа остается постоянным. V, p, Т
Изопроцесс - процесс, при котором один из макроскопических параметров состояния данной массы газа остается постоянным. V, p, Т
 Изо – (постоянный) Изобарный изопроцессы Изохорный Изотермический
Изо – (постоянный) Изобарный изопроцессы Изохорный Изотермический
 Изотермический процесс - ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ МАССЫ ГАЗА ПРИ ПОСТОЯННОЙ ТЕМПЕРАТУРЕ. Т = const m = const
Изотермический процесс - ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ МАССЫ ГАЗА ПРИ ПОСТОЯННОЙ ТЕМПЕРАТУРЕ. Т = const m = const
 Изотермический процесс Из уравнения Клапейрона – Менделеева следует: m p. V = const = RT M
Изотермический процесс Из уравнения Клапейрона – Менделеева следует: m p. V = const = RT M
 Закон Бойля – Мариотта. Закон экспериментально получен в: • 1662 г. Р. Бойлем; • 1676 г. Э. Мариоттом. T - const Р. Бойль Для газа данной массы при постоянной температуре произведение давления газа на его объем постоянно: p 1 V 1 = p 2 V 2
Закон Бойля – Мариотта. Закон экспериментально получен в: • 1662 г. Р. Бойлем; • 1676 г. Э. Мариоттом. T - const Р. Бойль Для газа данной массы при постоянной температуре произведение давления газа на его объем постоянно: p 1 V 1 = p 2 V 2
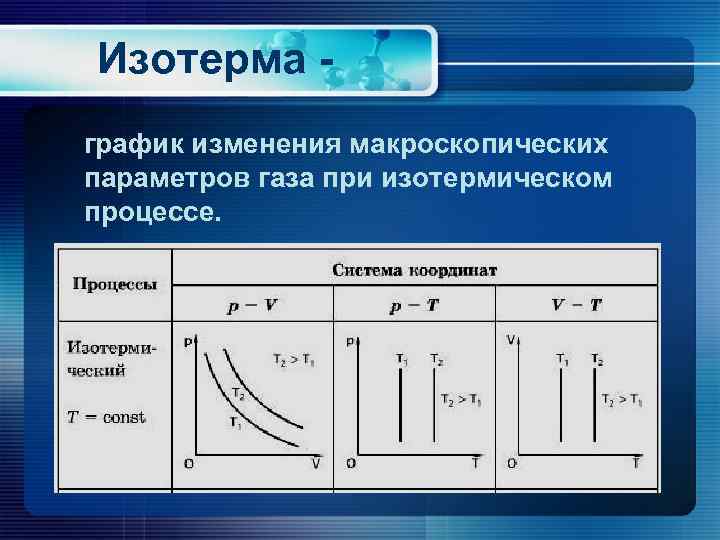 Изотерма - график изменения макроскопических параметров газа при изотермическом процессе.
Изотерма - график изменения макроскопических параметров газа при изотермическом процессе.
 Изобарный процесс - ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ МАССЫ ГАЗА ПРИ ПОСТОЯННОМ ДАВЛЕНИИ. P = const m = const
Изобарный процесс - ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ МАССЫ ГАЗА ПРИ ПОСТОЯННОМ ДАВЛЕНИИ. P = const m = const
 Изобарный процесс Из уравнения Клапейрона – Менделеева следует: V m. R = const = T Mp
Изобарный процесс Из уравнения Клапейрона – Менделеева следует: V m. R = const = T Mp
 Закон Гей-Люссака. Закон экспериментально получен в 1802 г. p - const ГЕЙ-ЛЮССАК Жозеф Луи Для газа данной массы при постоянном давлении отношение объема газа к его термодинамической температуре постоянно: V 1 / T 1 = V 2 / T 2
Закон Гей-Люссака. Закон экспериментально получен в 1802 г. p - const ГЕЙ-ЛЮССАК Жозеф Луи Для газа данной массы при постоянном давлении отношение объема газа к его термодинамической температуре постоянно: V 1 / T 1 = V 2 / T 2
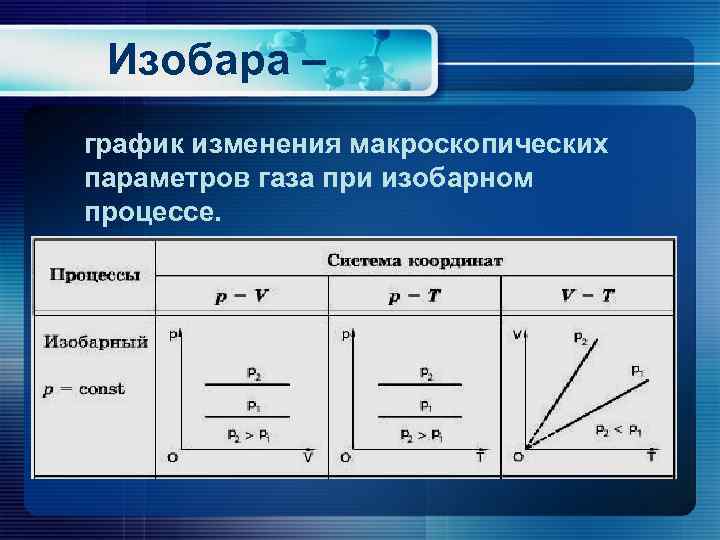 Изобара – график изменения макроскопических параметров газа при изобарном процессе.
Изобара – график изменения макроскопических параметров газа при изобарном процессе.
 Изохорный процесс - ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ МАССЫ ГАЗА ПРИ ПОСТОЯННОМ ОБЪЕМЕ. V = const m = const
Изохорный процесс - ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ МАССЫ ГАЗА ПРИ ПОСТОЯННОМ ОБЪЕМЕ. V = const m = const
 Изохорный процесс Из уравнения Клапейрона – Менделеева следует: p m. R = const = T MV
Изохорный процесс Из уравнения Клапейрона – Менделеева следует: p m. R = const = T MV
 Закон Шарля. Закон экспериментально получен в 1787 г. V - const Для газа данной массы при постоянном объеме отношение давления газа к его термодинамической температуре постоянно: p 1 / T 1 = p 2 / T 2
Закон Шарля. Закон экспериментально получен в 1787 г. V - const Для газа данной массы при постоянном объеме отношение давления газа к его термодинамической температуре постоянно: p 1 / T 1 = p 2 / T 2
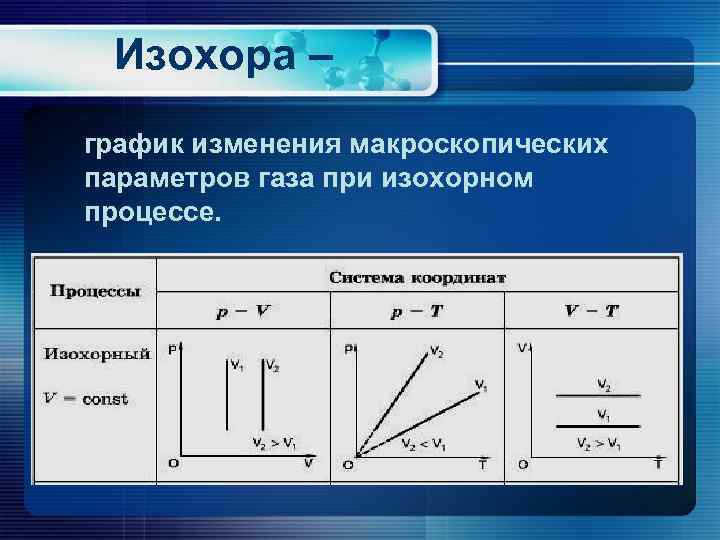 Изохора – график изменения макроскопических параметров газа при изохорном процессе.
Изохора – график изменения макроскопических параметров газа при изохорном процессе.
 Циклы.
Циклы.





































