Изомерия комплексных соединений Изомер (от греч. izos








![Координационная полимерия • [Pt(NH 3)2 Cl 2] –соль Пейроне • Координационная полимерия • [Pt(NH 3)2 Cl 2] –соль Пейроне •](https://present5.com/presentation/3/54806551_132247623.pdf-img/54806551_132247623.pdf-9.jpg)



![Тригидрат триоксалатокобальтата(III) аммония (NH 4)3[Co(ox)3]. 3 H 2 O Тригидрат триоксалатокобальтата(III) аммония (NH 4)3[Co(ox)3]. 3 H 2 O](https://present5.com/presentation/3/54806551_132247623.pdf-img/54806551_132247623.pdf-16.jpg)
![Оптическая изомерия • оптические изомеры комплекса [Ru(dipy)3]Cl 2 (dipy - Оптическая изомерия • оптические изомеры комплекса [Ru(dipy)3]Cl 2 (dipy -](https://present5.com/presentation/3/54806551_132247623.pdf-img/54806551_132247623.pdf-17.jpg)
Изомерия комплексных соединений.ppt
- Количество слайдов: 18
 Изомерия комплексных соединений
Изомерия комплексных соединений
 Изомер (от греч. izos - равный, meros - мера) • Под изомерией понимают способность веществ образовывать несколько соединений одинакового состава, отличающихся взаимным расположением атомов в молекуле, а следовательно, различных по свойствам.
Изомер (от греч. izos - равный, meros - мера) • Под изомерией понимают способность веществ образовывать несколько соединений одинакового состава, отличающихся взаимным расположением атомов в молекуле, а следовательно, различных по свойствам.
 Изомерия комплексных соединений обусловлена: • разным распределением частиц между внутренней и внешней сферой; • различиями в строении и координации лигандов; • различиями в строении внутренней координационной сферы.
Изомерия комплексных соединений обусловлена: • разным распределением частиц между внутренней и внешней сферой; • различиями в строении и координации лигандов; • различиями в строении внутренней координационной сферы.
 Ионизационная изомерия • связана с различным распределением заряженных лигандов между внешней и внутренней сферами комплексного соединения; • нитрат дихлоротетраамминкобальта(III) и хлорид нитратохлоротетраамминкобальта(III): [Co(NH 3)4 Cl 2]NO 3 и [Co(NH 3)4 Cl(NO 3)]Cl; • бромид дихлоротетраамминплатины(IV) и хлорид дибромотетраамминплатины(IV): • [Pt(NH 3)4 Cl 2]Br 2 и [Pt(NH 3)4 Br 2]Cl 2
Ионизационная изомерия • связана с различным распределением заряженных лигандов между внешней и внутренней сферами комплексного соединения; • нитрат дихлоротетраамминкобальта(III) и хлорид нитратохлоротетраамминкобальта(III): [Co(NH 3)4 Cl 2]NO 3 и [Co(NH 3)4 Cl(NO 3)]Cl; • бромид дихлоротетраамминплатины(IV) и хлорид дибромотетраамминплатины(IV): • [Pt(NH 3)4 Cl 2]Br 2 и [Pt(NH 3)4 Br 2]Cl 2
 Сольватная (гидратная) изомерия • заключается в различном распределении молекул растворителя между внутренней и внешней сферами комплексного соединения, в различном характере химической связи молекул воды с комплексообразователем. • [Cr(H 2 O)6]Cl 3 – хлорид гексааквахрома(III) – кристаллы серо-сиреневого цвета, которые при растворении в воде образуют фиолетовый раствор; • [Cr(H 2 O)5 Cl]Cl 2. H 2 O, моногидрат хлорида хлоропентааквахрома(III) – придает раствору голубовато-зеленый цвет; • [Cr(H 2 O)4 Cl 2]Cl. 2 H 2 O, дигидрат хлорида дихлоротетрааквахрома(III) – окрашивает раствор в темно-зеленый цвет.
Сольватная (гидратная) изомерия • заключается в различном распределении молекул растворителя между внутренней и внешней сферами комплексного соединения, в различном характере химической связи молекул воды с комплексообразователем. • [Cr(H 2 O)6]Cl 3 – хлорид гексааквахрома(III) – кристаллы серо-сиреневого цвета, которые при растворении в воде образуют фиолетовый раствор; • [Cr(H 2 O)5 Cl]Cl 2. H 2 O, моногидрат хлорида хлоропентааквахрома(III) – придает раствору голубовато-зеленый цвет; • [Cr(H 2 O)4 Cl 2]Cl. 2 H 2 O, дигидрат хлорида дихлоротетрааквахрома(III) – окрашивает раствор в темно-зеленый цвет.
 Связевая (солевая) изомерия • определяется разным типом координации одного и того же лиганда ( амбидентатные лиганды) • нитро- и нитрито-комплексы кобальта(III) K 3[Co(NO 2)6] и K 3[Co(ONO)6], в которых координация лиганда NO 2 - осуществляется, соответственно, через атом азота или атом кислорода; • координация тиоцианат-иона NCS- через атом азота или через атом серы, с образованием изотиоцианато- или тиоцианато-комплексов.
Связевая (солевая) изомерия • определяется разным типом координации одного и того же лиганда ( амбидентатные лиганды) • нитро- и нитрито-комплексы кобальта(III) K 3[Co(NO 2)6] и K 3[Co(ONO)6], в которых координация лиганда NO 2 - осуществляется, соответственно, через атом азота или атом кислорода; • координация тиоцианат-иона NCS- через атом азота или через атом серы, с образованием изотиоцианато- или тиоцианато-комплексов.
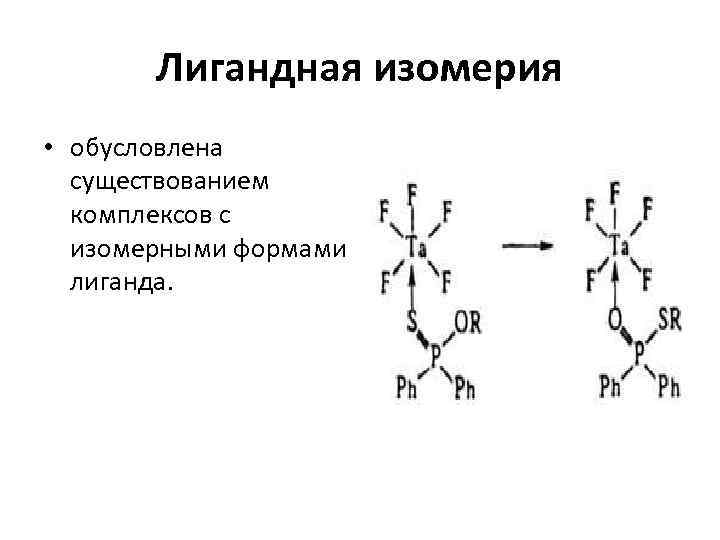
 Лигандная изомерия • обусловлена существованием комплексов с изомерными формами лиганда.
Лигандная изомерия • обусловлена существованием комплексов с изомерными формами лиганда.
 Координационная изомерия • возможна при наличии двух и более комплексообразователей, с которыми связаны разные лиганды. • Например, [Cr(NH 3)6][Co(CN)6] и [Co(NH 3)6][Cr(CN)6].
Координационная изомерия • возможна при наличии двух и более комплексообразователей, с которыми связаны разные лиганды. • Например, [Cr(NH 3)6][Co(CN)6] и [Co(NH 3)6][Cr(CN)6].
![> Координационная полимерия • [Pt(NH 3)2 Cl 2] –соль Пейроне • > Координационная полимерия • [Pt(NH 3)2 Cl 2] –соль Пейроне •](https://present5.com/presentation/3/54806551_132247623.pdf-img/54806551_132247623.pdf-9.jpg) Координационная полимерия • [Pt(NH 3)2 Cl 2] –соль Пейроне • [Pt(NH 3)4] [Pt. Cl 4] • [Pt(NH 3)4] [Pt. NH 3 Cl 2] 2 • [Pt(NH 3)3 Cl 2] 2 [Pt. Cl 4]
Координационная полимерия • [Pt(NH 3)2 Cl 2] –соль Пейроне • [Pt(NH 3)4] [Pt. Cl 4] • [Pt(NH 3)4] [Pt. NH 3 Cl 2] 2 • [Pt(NH 3)3 Cl 2] 2 [Pt. Cl 4]
 Геометрическая изомерия • вызвана неодинаковым размещением лигандов во внутренней сфере относительно друга; • необходимо наличие во внутренней координационной сфере не менее двух различных лигандов; • проявляется преимущественно у комплексных соединений, имеющих октаэдрическое строение, строение плоского квадрата или квадратной пирамиды.
Геометрическая изомерия • вызвана неодинаковым размещением лигандов во внутренней сфере относительно друга; • необходимо наличие во внутренней координационной сфере не менее двух различных лигандов; • проявляется преимущественно у комплексных соединений, имеющих октаэдрическое строение, строение плоского квадрата или квадратной пирамиды.
 Геометрическая изомерия • Цис-ихлородиамминплатина(II) [Pt(NH 3)2 Cl 2] оранжево-желтые кристаллы, хорошо растворимые в воде; обладает отчетливо выраженными противоопухолевыми свойствами. (цис-платин) • транс- дихлородиамминплатина(II) – Изомер, в котором одинаковые кристаллы бледно-желтого лиганды расположены по одному ребру цвета, растворимость которых квадрата, называется цис-формой, а в воде несколько ниже, чем у если по диагонали, это транс-изомер цис-изомера. (от лат. cis - вместе, trans - напротив).
Геометрическая изомерия • Цис-ихлородиамминплатина(II) [Pt(NH 3)2 Cl 2] оранжево-желтые кристаллы, хорошо растворимые в воде; обладает отчетливо выраженными противоопухолевыми свойствами. (цис-платин) • транс- дихлородиамминплатина(II) – Изомер, в котором одинаковые кристаллы бледно-желтого лиганды расположены по одному ребру цвета, растворимость которых квадрата, называется цис-формой, а в воде несколько ниже, чем у если по диагонали, это транс-изомер цис-изомера. (от лат. cis - вместе, trans - напротив).
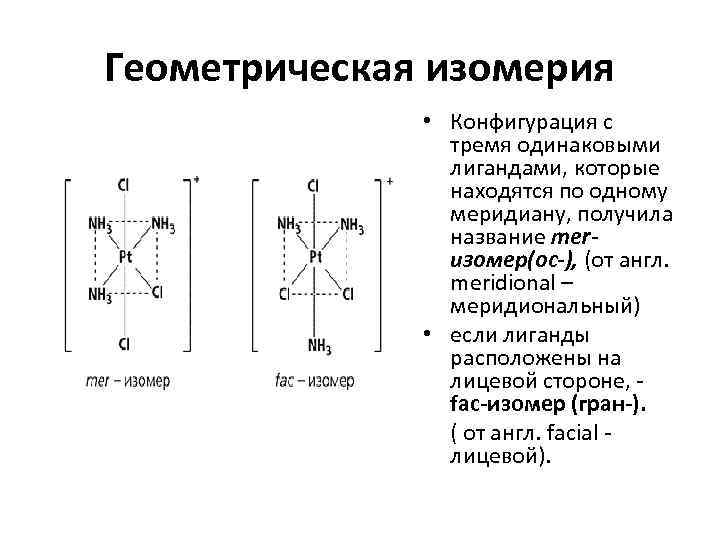
 Геометрическая изомерия • Конфигурация с тремя одинаковыми лигандами, которые находятся по одному меридиану, получила название mer- изомер(ос-), (от англ. meridional – меридиональный) • если лиганды расположены на лицевой стороне, - fac-изомер (гран-). ( от англ. facial - лицевой).
Геометрическая изомерия • Конфигурация с тремя одинаковыми лигандами, которые находятся по одному меридиану, получила название mer- изомер(ос-), (от англ. meridional – меридиональный) • если лиганды расположены на лицевой стороне, - fac-изомер (гран-). ( от англ. facial - лицевой).
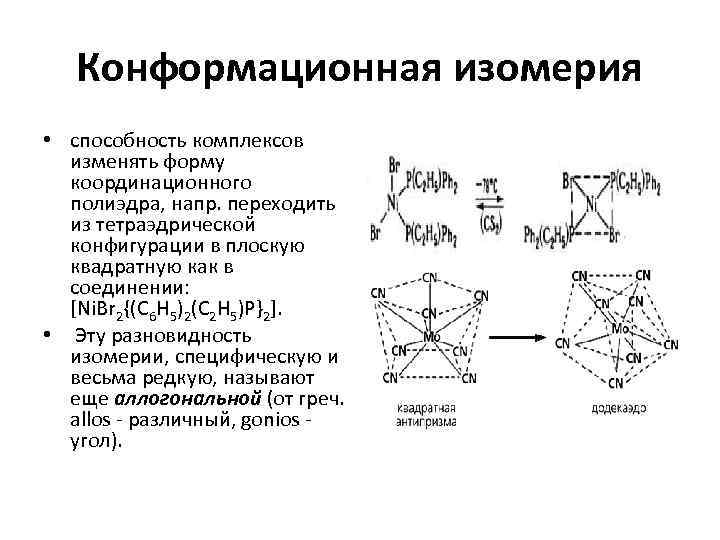
 Конформационная изомерия • способность комплексов изменять форму координационного полиэдра, напр. переходить из тетраэдрической конфигурации в плоскую квадратную как в соединении: [Ni. Br 2{(C 6 H 5)2(C 2 H 5)P}2]. • Эту разновидность изомерии, специфическую и весьма редкую, называют еще аллогональной (от греч. allos - различный, gonios - угол).
Конформационная изомерия • способность комплексов изменять форму координационного полиэдра, напр. переходить из тетраэдрической конфигурации в плоскую квадратную как в соединении: [Ni. Br 2{(C 6 H 5)2(C 2 H 5)P}2]. • Эту разновидность изомерии, специфическую и весьма редкую, называют еще аллогональной (от греч. allos - различный, gonios - угол).
 Оптическая (зеркальная) изомерия • Оптическая изомерия связана со способностью некоторых комплексных соединений существовать в виде двух форм, не совмещаемых в трехмерном пространстве и являющихся зеркальным отображением друга. • Оптические изомеры отличаются тем, что их растворы способны вращать плоскость поляризации светового луча. Один изомер вращает плоскость поляризации влево и поэтому называется L- изомером, другой – вправо и называется D- изомером.
Оптическая (зеркальная) изомерия • Оптическая изомерия связана со способностью некоторых комплексных соединений существовать в виде двух форм, не совмещаемых в трехмерном пространстве и являющихся зеркальным отображением друга. • Оптические изомеры отличаются тем, что их растворы способны вращать плоскость поляризации светового луча. Один изомер вращает плоскость поляризации влево и поэтому называется L- изомером, другой – вправо и называется D- изомером.
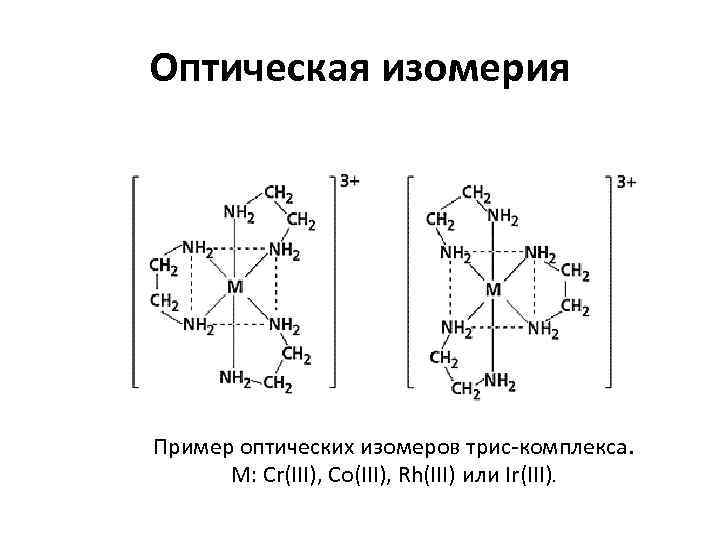
 Оптическая изомерия Пример оптических изомеров трис-комплекса. M: Cr(III), Co(III), Rh(III) или Ir(III).
Оптическая изомерия Пример оптических изомеров трис-комплекса. M: Cr(III), Co(III), Rh(III) или Ir(III).
![>Тригидрат триоксалатокобальтата(III) аммония (NH 4)3[Co(ox)3]. 3 H 2 O >Тригидрат триоксалатокобальтата(III) аммония (NH 4)3[Co(ox)3]. 3 H 2 O](https://present5.com/presentation/3/54806551_132247623.pdf-img/54806551_132247623.pdf-16.jpg) Тригидрат триоксалатокобальтата(III) аммония (NH 4)3[Co(ox)3]. 3 H 2 O
Тригидрат триоксалатокобальтата(III) аммония (NH 4)3[Co(ox)3]. 3 H 2 O
![> Оптическая изомерия • оптические изомеры комплекса [Ru(dipy)3]Cl 2 (dipy - > Оптическая изомерия • оптические изомеры комплекса [Ru(dipy)3]Cl 2 (dipy -](https://present5.com/presentation/3/54806551_132247623.pdf-img/54806551_132247623.pdf-17.jpg) Оптическая изомерия • оптические изомеры комплекса [Ru(dipy)3]Cl 2 (dipy - обозначение 2, 2'-дипиридила): один из них, правовращающий, - сильный мышиный яд, а другой, левовращающий, действует как противоядие.
Оптическая изомерия • оптические изомеры комплекса [Ru(dipy)3]Cl 2 (dipy - обозначение 2, 2'-дипиридила): один из них, правовращающий, - сильный мышиный яд, а другой, левовращающий, действует как противоядие.
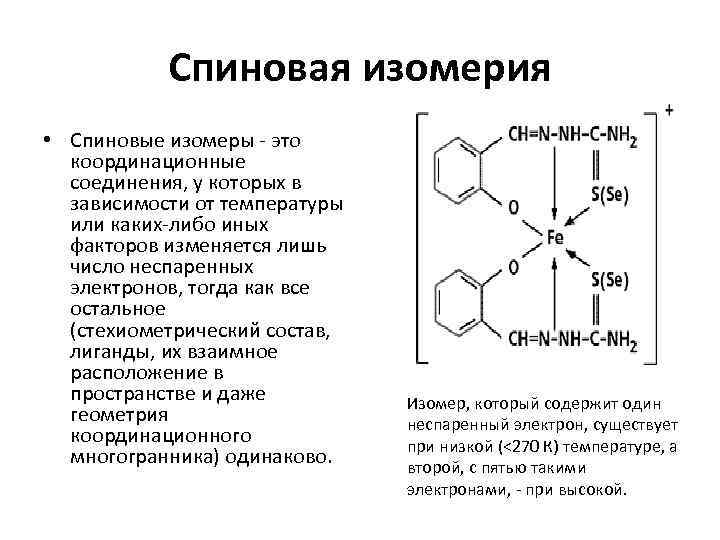
 Спиновая изомерия • Спиновые изомеры - это координационные соединения, у которых в зависимости от температуры или каких-либо иных факторов изменяется лишь число неспаренных электронов, тогда как все остальное (стехиометрический состав, лиганды, их взаимное расположение в пространстве и даже Изомер, который содержит один геометрия неспаренный электрон, существует координационного при низкой (<270 К) температуре, а многогранника) одинаково. второй, с пятью такими электронами, - при высокой.
Спиновая изомерия • Спиновые изомеры - это координационные соединения, у которых в зависимости от температуры или каких-либо иных факторов изменяется лишь число неспаренных электронов, тогда как все остальное (стехиометрический состав, лиганды, их взаимное расположение в пространстве и даже Изомер, который содержит один геометрия неспаренный электрон, существует координационного при низкой (<270 К) температуре, а многогранника) одинаково. второй, с пятью такими электронами, - при высокой.

