хим р-ции, их типы, энерг эффект 8 кл.ppt
- Количество слайдов: 25
 Изменения, происходящие с веществами.
Изменения, происходящие с веществами.
 Реакции с энергетическим эффектом. Любая химическая реакция сопровождается: b либо выделением энергии b либо поглощением энергии
Реакции с энергетическим эффектом. Любая химическая реакция сопровождается: b либо выделением энергии b либо поглощением энергии
 Энергия может выделяться или поглощаться в виде тепла или света (редко). Энергетический эффект- это то количество теплоты, которое выделяется или поглощается в ходе химической реакции Q - тепловой эффект [ Q ] =к. Дж
Энергия может выделяться или поглощаться в виде тепла или света (редко). Энергетический эффект- это то количество теплоты, которое выделяется или поглощается в ходе химической реакции Q - тепловой эффект [ Q ] =к. Дж
 Экзотермические реакции - это реакции, идущие с выделением энергии (+Q) экзо - наружу К экзотермическим реакциям относятся: b горение b реакции, идущие сами по себе
Экзотермические реакции - это реакции, идущие с выделением энергии (+Q) экзо - наружу К экзотермическим реакциям относятся: b горение b реакции, идущие сами по себе
![Эндотермические реакции - это реакции, идущие с поглощением энергии [-Q ] эндо - вовнутрь Эндотермические реакции - это реакции, идущие с поглощением энергии [-Q ] эндо - вовнутрь](https://present5.com/presentation/3/62121424_52176076.pdf-img/62121424_52176076.pdf-5.jpg) Эндотермические реакции - это реакции, идущие с поглощением энергии [-Q ] эндо - вовнутрь К эндотермическим реакциям относятся большинство реакций разложения.
Эндотермические реакции - это реакции, идущие с поглощением энергии [-Q ] эндо - вовнутрь К эндотермическим реакциям относятся большинство реакций разложения.
 Химические уравнения. Химическое уравнение - это условная запись химической реакции с помощью химических формул и математических знаков.
Химические уравнения. Химическое уравнение - это условная запись химической реакции с помощью химических формул и математических знаков.
 Классификация химических реакций по числу и составу исходных веществ и продуктов реакции: b. А + В АВ (соединение ) b АВ А+В (разложение) b А + ВС АС + В (замещение) реже А + BC BA + C (замещение) b АВ + СD АD + CB (обмен)
Классификация химических реакций по числу и составу исходных веществ и продуктов реакции: b. А + В АВ (соединение ) b АВ А+В (разложение) b А + ВС АС + В (замещение) реже А + BC BA + C (замещение) b АВ + СD АD + CB (обмен)
 Реакции разложения. АВ А+В В ходе этих реакций из одного более сложного вещества образуется несколько более простых.
Реакции разложения. АВ А+В В ходе этих реакций из одного более сложного вещества образуется несколько более простых.
 Н 2 О Н 2 + О 2 Избавься от нечетности по кислороду, поставь коэффициент « 2» перед формулой вещества, где он нечетен. 2 Н 2 О 2 Н 2 + О 2
Н 2 О Н 2 + О 2 Избавься от нечетности по кислороду, поставь коэффициент « 2» перед формулой вещества, где он нечетен. 2 Н 2 О 2 Н 2 + О 2
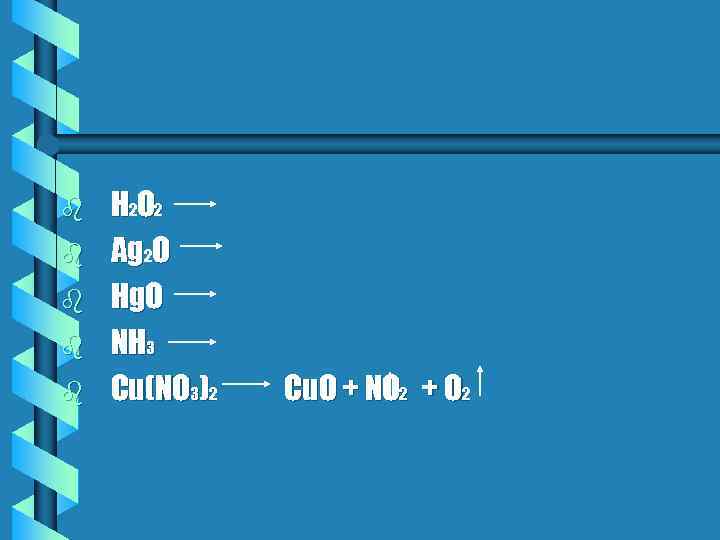 b b b H 2 O 2 Ag 2 O Hg. O NH 3 Cu(NO 3)2 Cu. O + NO 2 + O 2
b b b H 2 O 2 Ag 2 O Hg. O NH 3 Cu(NO 3)2 Cu. O + NO 2 + O 2
 Закон сохранения массы веществ. « Масса веществ, вступивших в реакцию, равна массе образующихся веществ » 1756 г. М. В Ломоносов
Закон сохранения массы веществ. « Масса веществ, вступивших в реакцию, равна массе образующихся веществ » 1756 г. М. В Ломоносов
 Реакции соединения. А+В АВ В ходе этих реакций из нескольких более простых веществ образуется одно более сложное.
Реакции соединения. А+В АВ В ходе этих реакций из нескольких более простых веществ образуется одно более сложное.
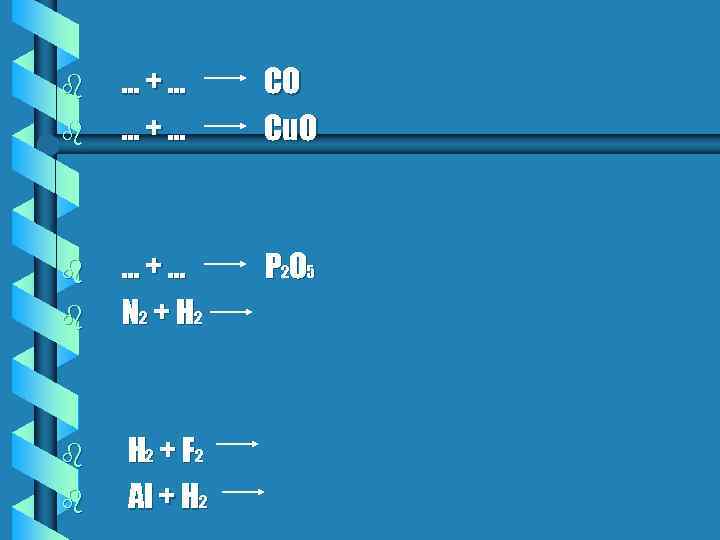 b b b …+… СО Сu. O …+… N 2 + H 2 P 2 O 5 H 2 + F 2 Al + H 2
b b b …+… СО Сu. O …+… N 2 + H 2 P 2 O 5 H 2 + F 2 Al + H 2
 Домашнее задание: Осуществить превращение, назвать все сложные вещества, определить тип реакции: Р Р 2 О 5 Н 3 РО 4 Са Са. О Са(ОН)2 S SO 2 SO 3
Домашнее задание: Осуществить превращение, назвать все сложные вещества, определить тип реакции: Р Р 2 О 5 Н 3 РО 4 Са Са. О Са(ОН)2 S SO 2 SO 3
 Реакции замещения. А + ВС Zn + H 2 SO 4 серная кислота Al + HCl Al + Cu Cl 2 АВ + С Zn. SO 4 + H 2 сульфат цинка
Реакции замещения. А + ВС Zn + H 2 SO 4 серная кислота Al + HCl Al + Cu Cl 2 АВ + С Zn. SO 4 + H 2 сульфат цинка
 Электрохимический ряд напряжений металлов (ряд активности) , ряд Бекетова. Металлы по активности делятся на 3 группы: 1) очень активные от H до Mg, они бурно реагируют с водой с образованием основания и газообразного водорода Na + HOH Na. OH + H 2 Ca + HOH Ca (OH)2 + H 2
Электрохимический ряд напряжений металлов (ряд активности) , ряд Бекетова. Металлы по активности делятся на 3 группы: 1) очень активные от H до Mg, они бурно реагируют с водой с образованием основания и газообразного водорода Na + HOH Na. OH + H 2 Ca + HOH Ca (OH)2 + H 2
 Оксиды этих металлов бурно реагируют с водой с образованием основания K 2 O + H 2 O Ba. O + H 2 O KOH Ba(OH)2
Оксиды этих металлов бурно реагируют с водой с образованием основания K 2 O + H 2 O Ba. O + H 2 O KOH Ba(OH)2
 2) Металлы средней активности от Al до Н. Они менее бурно реагируют с водой с образованием оксида и газообразного водорода Al + H 2 O Al 2 O 3 + H 2 Zn + H 2 O Zn. O + H 2 Оксиды этих металлов с водой не реагируют.
2) Металлы средней активности от Al до Н. Они менее бурно реагируют с водой с образованием оксида и газообразного водорода Al + H 2 O Al 2 O 3 + H 2 Zn + H 2 O Zn. O + H 2 Оксиды этих металлов с водой не реагируют.
 3) Неактивные металлы (после Н) не реагируют с водой Ag + H 2 O Их оксиды не реагируют с водой Cu. O + H 2 O
3) Неактивные металлы (после Н) не реагируют с водой Ag + H 2 O Их оксиды не реагируют с водой Cu. O + H 2 O
 Me + H 2 O Li Me. O + H 2 O Me. OH + H 2 Mg Me. OH Me + H 2 O Al Me. O + H 2 O Me O + H 2 H Me + H 2 O Cu Me. O + H 2 O
Me + H 2 O Li Me. O + H 2 O Me. OH + H 2 Mg Me. OH Me + H 2 O Al Me. O + H 2 O Me O + H 2 H Me + H 2 O Cu Me. O + H 2 O
 Активность металлов слева на право уменьшается. Любой левее стоящий металл может вытеснить правее стоящий металл из раствора его соли из оксида. Al + Cu( NO 3)2 Al( NO 3)3 Zn + Na 2 SO 4 Zn + Ag 2 O Mg + Fe 3 O 4 Fe + Al 2 O 3 Zn. O + Ag Mg. O + Fe
Активность металлов слева на право уменьшается. Любой левее стоящий металл может вытеснить правее стоящий металл из раствора его соли из оксида. Al + Cu( NO 3)2 Al( NO 3)3 Zn + Na 2 SO 4 Zn + Ag 2 O Mg + Fe 3 O 4 Fe + Al 2 O 3 Zn. O + Ag Mg. O + Fe
 Реакции обмена AB + CD AD + CB Это реакции, в ходе которых два сложных вещества обмениваются своими составными частями с образованием двух новых сложных веществ. HCl + Na. OH Na. Cl + H 2 O соляная кислота гидроксид натрия хлорид натрия
Реакции обмена AB + CD AD + CB Это реакции, в ходе которых два сложных вещества обмениваются своими составными частями с образованием двух новых сложных веществ. HCl + Na. OH Na. Cl + H 2 O соляная кислота гидроксид натрия хлорид натрия
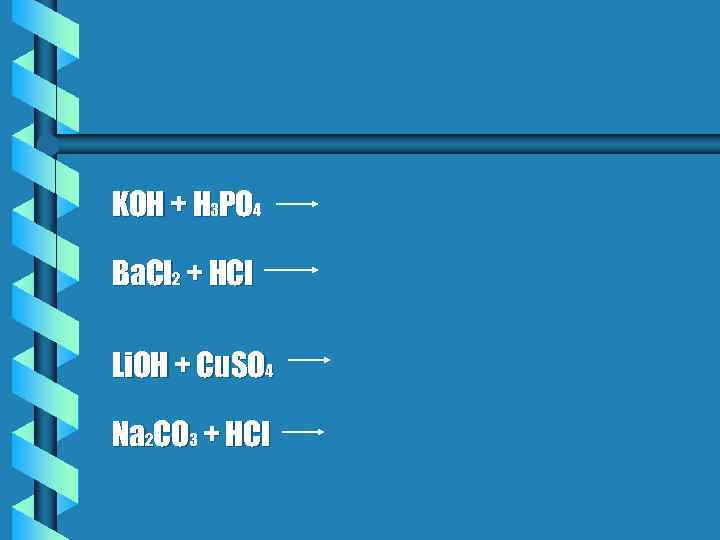 KOH + H 3 PO 4 Ba. Cl 2 + HCl Li. OH + Cu. SO 4 Na 2 CO 3 + HCl
KOH + H 3 PO 4 Ba. Cl 2 + HCl Li. OH + Cu. SO 4 Na 2 CO 3 + HCl
 Домашнее задание: Осуществить цепочку превращений, назвать все вещества и типы реакций: Ba. SO 4 SO 3 H 2 SO 4 Ba. SO 4
Домашнее задание: Осуществить цепочку превращений, назвать все вещества и типы реакций: Ba. SO 4 SO 3 H 2 SO 4 Ba. SO 4
 Реакции обмена, происходящие между кислотой (или кислотным оксидом) и основанием, называется реакциями нейтрализации.
Реакции обмена, происходящие между кислотой (или кислотным оксидом) и основанием, называется реакциями нейтрализации.


