48-Цивилёва .pptx
- Количество слайдов: 16
 Ивановский Государственный Химико-Технологический университет Кадмий Выполнила: студентка 2/11 Цивилёва Е. Н Иваново, 2017. .
Ивановский Государственный Химико-Технологический университет Кадмий Выполнила: студентка 2/11 Цивилёва Е. Н Иваново, 2017. .
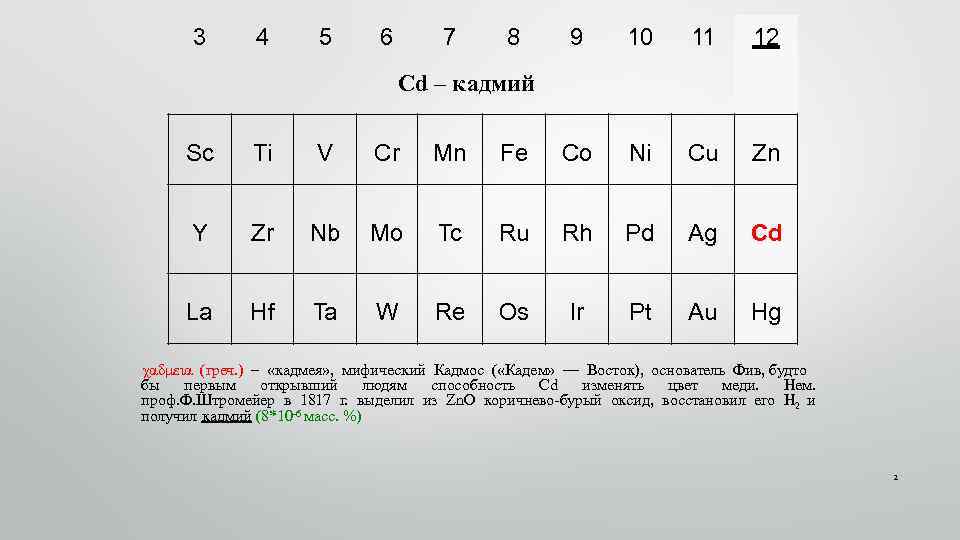 3 4 5 6 7 8 9 10 11 12 Cd – кадмий Sc Ti V Cr Mn Fe Co Ni Cu Zn Y Zr Nb Mo Tc Ru Rh Pd Ag Cd La Hf Ta W Re Os Ir Pt Au Hg χαδμεια (греч. ) – «кадмея» , мифический Кадмос ( «Кадем» — Восток), основатель Фив, будто бы первым открывший людям способность Cd изменять цвет меди. Нем. проф. Ф. Штромейер в 1817 г. выделил из Zn. O коричнево-бурый оксид, восстановил его H 2 и получил кадмий (8*10 -6 масс. %) 2
3 4 5 6 7 8 9 10 11 12 Cd – кадмий Sc Ti V Cr Mn Fe Co Ni Cu Zn Y Zr Nb Mo Tc Ru Rh Pd Ag Cd La Hf Ta W Re Os Ir Pt Au Hg χαδμεια (греч. ) – «кадмея» , мифический Кадмос ( «Кадем» — Восток), основатель Фив, будто бы первым открывший людям способность Cd изменять цвет меди. Нем. проф. Ф. Штромейер в 1817 г. выделил из Zn. O коричнево-бурый оксид, восстановил его H 2 и получил кадмий (8*10 -6 масс. %) 2
 Свойства атома Название, символ, номер Ка дмий / Cadmium (Cd), 48 Атомная масса (молярная масса) 112, 411(8)[1] а. е. м. (г/моль) Электронная конфигурация [Kr] 4 d 10 5 s 2 Радиус атома 154 пм Химические свойства Ковалентный радиус 148 пм Радиус иона (+2 e) 97 пм Электроотрицательность 1, 69 (шкала Полинга) Электродный потенциал − 0, 403[2] Степени окисления 2 Энергия ионизации (первый электрон) 867, 2 (8, 99) к. Дж/моль (э. В) Термодинамические свойства простого вещества Плотность (при н. у. ) 8, 65 г/см³ Температура плавления 594, 1 K Температура кипения 1 038 K Уд. теплота плавления 6, 11 к. Дж/моль Уд. теплота испарения 59, 1 к. Дж/моль Молярная теплоёмкость 26, 0[2] Дж/(K·моль) Молярный объём 13, 1 см³/моль 3
Свойства атома Название, символ, номер Ка дмий / Cadmium (Cd), 48 Атомная масса (молярная масса) 112, 411(8)[1] а. е. м. (г/моль) Электронная конфигурация [Kr] 4 d 10 5 s 2 Радиус атома 154 пм Химические свойства Ковалентный радиус 148 пм Радиус иона (+2 e) 97 пм Электроотрицательность 1, 69 (шкала Полинга) Электродный потенциал − 0, 403[2] Степени окисления 2 Энергия ионизации (первый электрон) 867, 2 (8, 99) к. Дж/моль (э. В) Термодинамические свойства простого вещества Плотность (при н. у. ) 8, 65 г/см³ Температура плавления 594, 1 K Температура кипения 1 038 K Уд. теплота плавления 6, 11 к. Дж/моль Уд. теплота испарения 59, 1 к. Дж/моль Молярная теплоёмкость 26, 0[2] Дж/(K·моль) Молярный объём 13, 1 см³/моль 3
 История 48 Cd Кадмий 112, 414 4 d 105 s 2 Открыт немецким профессором Ф. Штромейером в 1817. Провизоры Магдебурга при изучении оксида цинка Zn. O заподозрили в нём примесь мышьяка. Штромейер выделил из Zn. O коричнево-бурый оксид, восстановил его водородом и получил серебристо-белый металл, который получил название кадмий. 4
История 48 Cd Кадмий 112, 414 4 d 105 s 2 Открыт немецким профессором Ф. Штромейером в 1817. Провизоры Магдебурга при изучении оксида цинка Zn. O заподозрили в нём примесь мышьяка. Штромейер выделил из Zn. O коричнево-бурый оксид, восстановил его водородом и получил серебристо-белый металл, который получил название кадмий. 4
 Местонахождение в природе 1. Среднее содержание кадмия в земной коре — 130 мг/т, в морской воде — 0, 11 мкг/л. 2. Известно всего лишь 6 кадмиевых минералов. Весьма редкими минералами кадмия являются гринокит Cd. S (77, 8 % Cd), хоулиит (то же), отавит Cd. CO 3, монтепонит Cd. O (87, 5 % Cd), кадмоселит Cd. Se (47 % Cd), ксантохроит Cd. S(H 2 O)х (77, 2 % Cd). 3. Кадмий не образует самостоятельных месторождений, а входит в состав руд месторождений других металлов. 5
Местонахождение в природе 1. Среднее содержание кадмия в земной коре — 130 мг/т, в морской воде — 0, 11 мкг/л. 2. Известно всего лишь 6 кадмиевых минералов. Весьма редкими минералами кадмия являются гринокит Cd. S (77, 8 % Cd), хоулиит (то же), отавит Cd. CO 3, монтепонит Cd. O (87, 5 % Cd), кадмоселит Cd. Se (47 % Cd), ксантохроит Cd. S(H 2 O)х (77, 2 % Cd). 3. Кадмий не образует самостоятельных месторождений, а входит в состав руд месторождений других металлов. 5
 Реакционная способность Сd 1. Cd реагируют с O 2 Cd + ½O 2 = Cd. O (350 o. C) 2. Cd растворяются в кислотах Cd + 2 HCl = Cd. Cl 2 + H 2 3. Cd окисляется в кислой среде Cd + 2 H 2 SO 4 (конц) = Cd. SO 4 + SO 2 + 2 H 2 O 4. Cd реагирует с галогенами, халькогенами, не реагирует с азотом, углеродом и водородом. Cd (тв) + S (ж) = Cd. S (тв) 5. Cd реагируют с фосфором Cd + P = Cd. P 2 6. Cd образует аналоги амальгам: Ba. Cd 11, Mg. Cd 3 6
Реакционная способность Сd 1. Cd реагируют с O 2 Cd + ½O 2 = Cd. O (350 o. C) 2. Cd растворяются в кислотах Cd + 2 HCl = Cd. Cl 2 + H 2 3. Cd окисляется в кислой среде Cd + 2 H 2 SO 4 (конц) = Cd. SO 4 + SO 2 + 2 H 2 O 4. Cd реагирует с галогенами, халькогенами, не реагирует с азотом, углеродом и водородом. Cd (тв) + S (ж) = Cd. S (тв) 5. Cd реагируют с фосфором Cd + P = Cd. P 2 6. Cd образует аналоги амальгам: Ba. Cd 11, Mg. Cd 3 6
 Получение Cd 1. Cd не образует значимых собственных минералов Cd. S – гринокит, Ca. CO 3 – отавит Cd получают из отходов производства Zn, если содержание Cd > 5 % Cd. SO 4 + Zn = Zn. SO 4 + Cd 2. Металлический кадмий очищают от примеси цинка переплавкой под слоем расплавленной щелочи, которая с цинком образует цинкат. Кадмий высокой чистоты получают вакуумной дистилляцией. 7
Получение Cd 1. Cd не образует значимых собственных минералов Cd. S – гринокит, Ca. CO 3 – отавит Cd получают из отходов производства Zn, если содержание Cd > 5 % Cd. SO 4 + Zn = Zn. SO 4 + Cd 2. Металлический кадмий очищают от примеси цинка переплавкой под слоем расплавленной щелочи, которая с цинком образует цинкат. Кадмий высокой чистоты получают вакуумной дистилляцией. 7
 Применение Cd 1. в парфюмерии, в пластиках 2. в электронике гальванические элементы, лампы, электроды 3. припои, легкоплавкие сплавы 4. антикоррозийные покрытия 5. компонент полупроводниковых материалов и люминофоров 6. применяется для криогенной техники 8
Применение Cd 1. в парфюмерии, в пластиках 2. в электронике гальванические элементы, лампы, электроды 3. припои, легкоплавкие сплавы 4. антикоррозийные покрытия 5. компонент полупроводниковых материалов и люминофоров 6. применяется для криогенной техники 8
 Элемент Вестона Cd + Hg 22+ = Cd 2+ + 2 Hg 1 — отрицательный электрод (амальгама кадмия — 10% Cd, 90% Hg); 2 — кристаллы 3 Cd. SO 4*8 H 2 O; 3— электролит — насыщенный водный раствор Cd. SO 4; 4 — положительный электрод (Hg); 5— паста из Hg 2 SO 4 (деполяризатор), растёртого с Hg и кристаллами 3 Cd. SO 4· 8 H 2 O; 6 — корковая пробка; 7 — синтетическая смола; выводы от электродов изготовлены из платиновой проволоки Аккумуляторы 2 Ni. OOH + Cd = 2 Ni(OH)2 + Cd(OH)2 (никелькадмиевый) 9
Элемент Вестона Cd + Hg 22+ = Cd 2+ + 2 Hg 1 — отрицательный электрод (амальгама кадмия — 10% Cd, 90% Hg); 2 — кристаллы 3 Cd. SO 4*8 H 2 O; 3— электролит — насыщенный водный раствор Cd. SO 4; 4 — положительный электрод (Hg); 5— паста из Hg 2 SO 4 (деполяризатор), растёртого с Hg и кристаллами 3 Cd. SO 4· 8 H 2 O; 6 — корковая пробка; 7 — синтетическая смола; выводы от электродов изготовлены из платиновой проволоки Аккумуляторы 2 Ni. OOH + Cd = 2 Ni(OH)2 + Cd(OH)2 (никелькадмиевый) 9
 Оксиды и гидроксиды Cd(II) 1. Кислотно-основные свойства p. Kb Cd(OH)2 3. 0 2. Растворение в аммиаке Cd(OH)2 + 6 NH 3 (р-р) = [Cd(NH 3)6](OH)2 к. ч. = 6 10
Оксиды и гидроксиды Cd(II) 1. Кислотно-основные свойства p. Kb Cd(OH)2 3. 0 2. Растворение в аммиаке Cd(OH)2 + 6 NH 3 (р-р) = [Cd(NH 3)6](OH)2 к. ч. = 6 10
 Галогениды Cd(II) Сульфиды Cd(II) Cd. F 2 Т. пл. 1072 0 С К. ч. = 8 Cd. Cl 2 Т. пл. 568 0 С К. ч. = 6 Cd. Br 2 Т. пл. 567 0 С К. ч. = 6 Cd. I 2 Т. пл. 388 0 С К. ч. = 6 Cd. S желтый ПР = 10– 28 т. возг. = 1380 о. С к. ч. = 6 Cd. SO 4 + H 2 S = Cd. S + H 2 SO 4 11
Галогениды Cd(II) Сульфиды Cd(II) Cd. F 2 Т. пл. 1072 0 С К. ч. = 8 Cd. Cl 2 Т. пл. 568 0 С К. ч. = 6 Cd. Br 2 Т. пл. 567 0 С К. ч. = 6 Cd. I 2 Т. пл. 388 0 С К. ч. = 6 Cd. S желтый ПР = 10– 28 т. возг. = 1380 о. С к. ч. = 6 Cd. SO 4 + H 2 S = Cd. S + H 2 SO 4 11
 Соединения Cd(II) 1. Получение галогенидов Cd(NO 3)2 + 2 KF = Cd. F 2 + 2 KNO 3 2. Cd. F 2 нерастворим 3. Комплексные галогениды Cd. Cl 2 + 4 NH 4 Cl = (NH 4)4[Cd. Cl 6] октаэдр Cd. Br 2 + 2 Na. Br = Na 2[Cd. Br 4] тетраэдр 4. Растворение сульфидов Cd. S + 2 HCl (конц) = Cd. Cl 2+H 2 S Cd. S + 8 HNO 3 (конц) = Cd. SO 4 + 8 NO 2 + 4 H 2 O 12
Соединения Cd(II) 1. Получение галогенидов Cd(NO 3)2 + 2 KF = Cd. F 2 + 2 KNO 3 2. Cd. F 2 нерастворим 3. Комплексные галогениды Cd. Cl 2 + 4 NH 4 Cl = (NH 4)4[Cd. Cl 6] октаэдр Cd. Br 2 + 2 Na. Br = Na 2[Cd. Br 4] тетраэдр 4. Растворение сульфидов Cd. S + 2 HCl (конц) = Cd. Cl 2+H 2 S Cd. S + 8 HNO 3 (конц) = Cd. SO 4 + 8 NO 2 + 4 H 2 O 12
 Важнейшие соединения кадмия 1. Гидрид кадмия (Cd. H 2)n. Получают при температуре -70 о. С действием раствора Cd. I 2 или Cd(CH 3)2 в тетрагидрофуране на эфирный раствор Li. Al. H 4. 2. Оксид кадмия Cd. O. tпл=1426 о. С. Применяют в качестве катализатора. 3. Гидроксид кадмия Cd(OH)2. Токсичен. Применяют для получения солей кадмия. 4. Фторид кадмия Cd. F 2. tпл=1100°С, tкип=1758 о. С. Применяют как оптический материал, компонент оптических стекол, люминофоров, лазерных материалов; для изготовления катодов и как компонент твердых электролитов в химических источниках тока. 5. Сульфид кадмия Cd. S. Применяется в качестве желтого пигмента при изготовлении масляных красок. 6. Сульфат кадмия Cd. SO 4. tпл=1000°С. Применяется для получения соединений кадмия и в фармацевтической промышленности. 7. Нитрат кадмия Cd(NO 3)2. tпл=350°С. Применяют как пигмент для стекла и фарфора и как компонент вирирующих составов в фотографии. 8. Карбонат кадмия Cd. CO 3. В природе встречается в виде минерала отавита. 13
Важнейшие соединения кадмия 1. Гидрид кадмия (Cd. H 2)n. Получают при температуре -70 о. С действием раствора Cd. I 2 или Cd(CH 3)2 в тетрагидрофуране на эфирный раствор Li. Al. H 4. 2. Оксид кадмия Cd. O. tпл=1426 о. С. Применяют в качестве катализатора. 3. Гидроксид кадмия Cd(OH)2. Токсичен. Применяют для получения солей кадмия. 4. Фторид кадмия Cd. F 2. tпл=1100°С, tкип=1758 о. С. Применяют как оптический материал, компонент оптических стекол, люминофоров, лазерных материалов; для изготовления катодов и как компонент твердых электролитов в химических источниках тока. 5. Сульфид кадмия Cd. S. Применяется в качестве желтого пигмента при изготовлении масляных красок. 6. Сульфат кадмия Cd. SO 4. tпл=1000°С. Применяется для получения соединений кадмия и в фармацевтической промышленности. 7. Нитрат кадмия Cd(NO 3)2. tпл=350°С. Применяют как пигмент для стекла и фарфора и как компонент вирирующих составов в фотографии. 8. Карбонат кадмия Cd. CO 3. В природе встречается в виде минерала отавита. 13
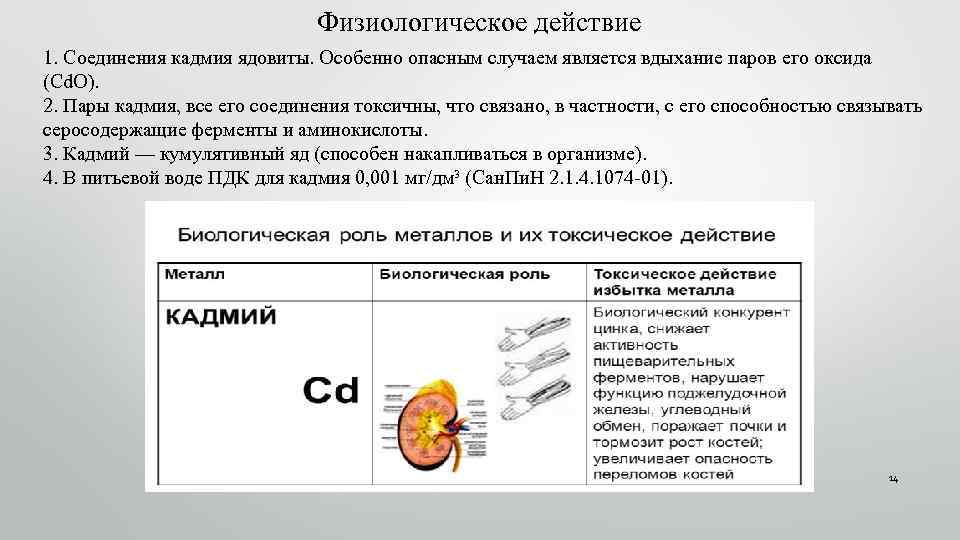 Физиологическое действие 1. Соединения кадмия ядовиты. Особенно опасным случаем является вдыхание паров его оксида (Cd. O). 2. Пары кадмия, все его соединения токсичны, что связано, в частности, с его способностью связывать серосодержащие ферменты и аминокислоты. 3. Кадмий — кумулятивный яд (способен накапливаться в организме). 4. В питьевой воде ПДК для кадмия 0, 001 мг/дм³ (Сан. Пи. Н 2. 1. 4. 1074 -01). 14
Физиологическое действие 1. Соединения кадмия ядовиты. Особенно опасным случаем является вдыхание паров его оксида (Cd. O). 2. Пары кадмия, все его соединения токсичны, что связано, в частности, с его способностью связывать серосодержащие ферменты и аминокислоты. 3. Кадмий — кумулятивный яд (способен накапливаться в организме). 4. В питьевой воде ПДК для кадмия 0, 001 мг/дм³ (Сан. Пи. Н 2. 1. 4. 1074 -01). 14
 Интересные факты о кадмии 1. Во влажной среде на поверхности кадмия образуется плёнка оксида, препятствующая дальнейшему окислению металла. 2. Ежегодно производится около 20000 тонн кадмия. 3. При нагревании выше 80 °C кадмий теряет упругость до такой степени, что его можно истолочь в порошок. 4. Если кадмиевую палочку изгибать, то будет услышан слабый треск (это признак того что трутся друг о друга микрокристаллы металла). 5. Кадмий можно резать ножом (он твёрже олова, но мягче цинка). 6. Кадмий применяется как компонент твёрдых припоев для снижения их температуры плавления. 7. Сплав кадмия с золотом имеет зеленоватый цвет. 8. Соединения кадмия после всасывания в кровь поражают центральную нервную систему, печень и почки, нарушают фосфорно-кальциевый обмен (хроническое отравление кадмием приводит к анемии и разрушению костей). 15
Интересные факты о кадмии 1. Во влажной среде на поверхности кадмия образуется плёнка оксида, препятствующая дальнейшему окислению металла. 2. Ежегодно производится около 20000 тонн кадмия. 3. При нагревании выше 80 °C кадмий теряет упругость до такой степени, что его можно истолочь в порошок. 4. Если кадмиевую палочку изгибать, то будет услышан слабый треск (это признак того что трутся друг о друга микрокристаллы металла). 5. Кадмий можно резать ножом (он твёрже олова, но мягче цинка). 6. Кадмий применяется как компонент твёрдых припоев для снижения их температуры плавления. 7. Сплав кадмия с золотом имеет зеленоватый цвет. 8. Соединения кадмия после всасывания в кровь поражают центральную нервную систему, печень и почки, нарушают фосфорно-кальциевый обмен (хроническое отравление кадмием приводит к анемии и разрушению костей). 15
 Источники информации 1. Неорганическая химия. Я. А. Угай 2. Материал из Википедии – Кадмий. 3. Общая и неорганическая химия. Учебник для вузов. – 3 -е изд. , стер. – М. : Химия, 1994, С. 561. 16
Источники информации 1. Неорганическая химия. Я. А. Угай 2. Материал из Википедии – Кадмий. 3. Общая и неорганическая химия. Учебник для вузов. – 3 -е изд. , стер. – М. : Химия, 1994, С. 561. 16


