 IV-1 Распространение углерода в природе Нахождение углерода Количество углерода, тонны 12 Атмосфера 2*10 12 Живое вещество 10*10 Каменные угли 20*1012 Океаны 100*1012 12 Известняки 30 000* 10
IV-1 Распространение углерода в природе Нахождение углерода Количество углерода, тонны 12 Атмосфера 2*10 12 Живое вещество 10*10 Каменные угли 20*1012 Океаны 100*1012 12 Известняки 30 000* 10
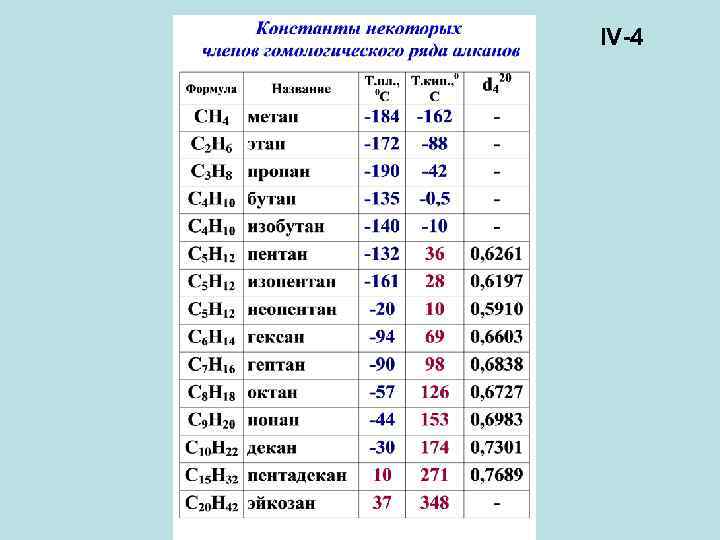 IV-4
IV-4
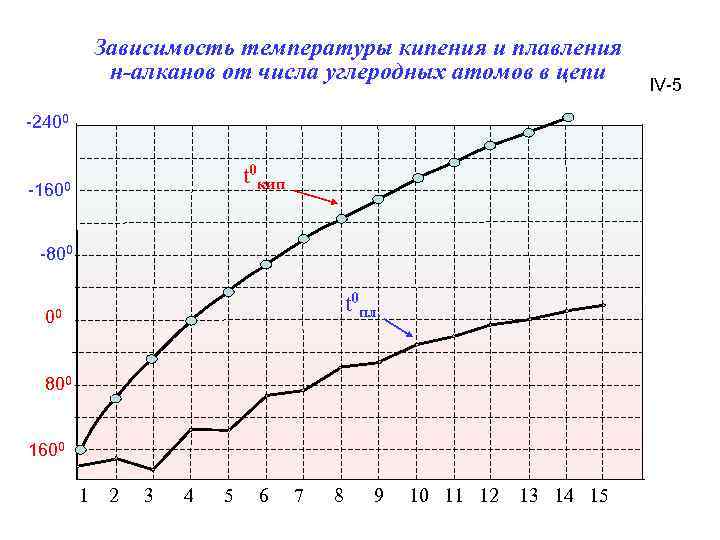 Зависимость температуры кипения и плавления н-алканов от числа углеродных атомов в цепи -2400 t 0 кип -1600 -800 t 0 пл. 00 800 1600 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 IV-5
Зависимость температуры кипения и плавления н-алканов от числа углеродных атомов в цепи -2400 t 0 кип -1600 -800 t 0 пл. 00 800 1600 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 IV-5
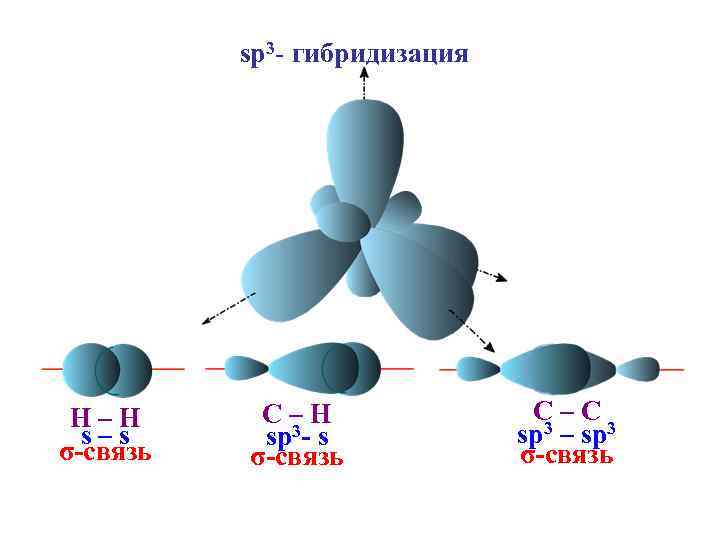 sp 3 - гибридизация H–H s–s σ-связь C–H sp 3 - s σ-связь С–C sp 3 – sp 3 σ-связь
sp 3 - гибридизация H–H s–s σ-связь C–H sp 3 - s σ-связь С–C sp 3 – sp 3 σ-связь
 Предельные углеводороды алканы Методы получения 1. Действие металлического натрия на моногалогенопроизводные – реакция Вюрца +2 Na CH 3 -CH 2 -Br + Br-CH 2 -CH 3 Br +CH 3 CH 2 Br +6 Na CH 3 -CH 2 -CH 3 + 2 Na. Br CH 3+CH 3 CH 2 CH 3+ + 6 Na. Br 2. Восстановление алкенов и алкинов водородом. H 2/Pt, Pd, Ni CH 3 CH 2 CH 3 -CH=CH 2 3. Восстановление иодистоводородной кислотой. CH 3 to CH 3 CHBr +2 HI CH 2 + HBr + I 2 CH 3 4. Сплавление щелочных солей карбоновых кислот со щелочами O сплавление CH 3 -C CH 4 + Na 2 CO 3 ONa +Na. OH
Предельные углеводороды алканы Методы получения 1. Действие металлического натрия на моногалогенопроизводные – реакция Вюрца +2 Na CH 3 -CH 2 -Br + Br-CH 2 -CH 3 Br +CH 3 CH 2 Br +6 Na CH 3 -CH 2 -CH 3 + 2 Na. Br CH 3+CH 3 CH 2 CH 3+ + 6 Na. Br 2. Восстановление алкенов и алкинов водородом. H 2/Pt, Pd, Ni CH 3 CH 2 CH 3 -CH=CH 2 3. Восстановление иодистоводородной кислотой. CH 3 to CH 3 CHBr +2 HI CH 2 + HBr + I 2 CH 3 4. Сплавление щелочных солей карбоновых кислот со щелочами O сплавление CH 3 -C CH 4 + Na 2 CO 3 ONa +Na. OH
 Предельные углеводороды алканы Химические свойства Алканы обладают большой химической инертностью. Все -связи С-С, С-Н очень прочны. Энергия этих связей ~ 376 к. Дж/мол. С 5 Н 12 + 8 О 2 5 СО 2 + 6 Н 2 О 1. Окисление: 2. Нитрование: (1889 г. М. И. Коновалов) СН 3 - H 2 O СН 3 -СН 2 -С-NO 2 СН 3 -СН 2 -С-Н + НО-NO 2 СН 3 Реакция идёт при нагревании (~ 1400 С) с разбавленной азотной кислотой в запаянной ампуле.
Предельные углеводороды алканы Химические свойства Алканы обладают большой химической инертностью. Все -связи С-С, С-Н очень прочны. Энергия этих связей ~ 376 к. Дж/мол. С 5 Н 12 + 8 О 2 5 СО 2 + 6 Н 2 О 1. Окисление: 2. Нитрование: (1889 г. М. И. Коновалов) СН 3 - H 2 O СН 3 -СН 2 -С-NO 2 СН 3 -СН 2 -С-Н + НО-NO 2 СН 3 Реакция идёт при нагревании (~ 1400 С) с разбавленной азотной кислотой в запаянной ампуле.
 Предельные углеводороды алканы Химические свойства 3. Радикальное галогенирование: CH 4 + Br 2 1) Br h CH 3 Br + HBr Br h 2 Br 2) CH 3 H + Br CH 3 + H Br 3) CH 3 + Br Br CH 3 Br + Br Реакции обрыва цепи CH 3 + СН 3 Br + Br СН 3 -СН 3 Br-Br
Предельные углеводороды алканы Химические свойства 3. Радикальное галогенирование: CH 4 + Br 2 1) Br h CH 3 Br + HBr Br h 2 Br 2) CH 3 H + Br CH 3 + H Br 3) CH 3 + Br Br CH 3 Br + Br Реакции обрыва цепи CH 3 + СН 3 Br + Br СН 3 -СН 3 Br-Br
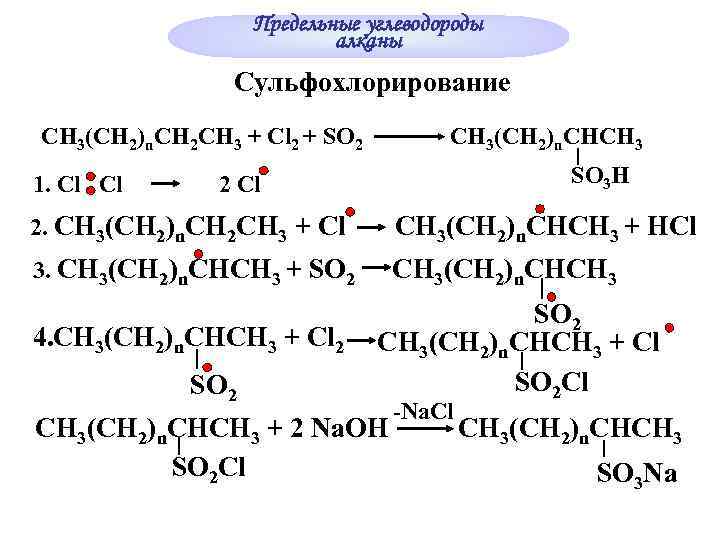 Предельные углеводороды алканы Сульфохлорирование CH 3(CH 2)n. CH 2 CH 3 + Cl 2 + SO 2 1. Cl Cl CH 3(CH 2)n. CHCH 3 SO 3 H 2 Cl 2. CH 3(CH 2)n. CH 2 CH 3 + Cl CH 3(CH 2)n. CHCH 3 + HCl 3. CH 3(CH 2)n. CHCH 3 + SO 2 CH 3(CH 2)n. CHCH 3 4. CH 3(CH 2)n. CHCH 3 + Cl 2 SO 2 CH 3(CH 2)n. CHCH 3 + Cl SO 2 Cl CH 3(CH 2)n. CHCH 3 + 2 Na. OH SO 2 Cl -Na. Cl CH 3(CH 2)n. CHCH 3 SO 3 Na
Предельные углеводороды алканы Сульфохлорирование CH 3(CH 2)n. CH 2 CH 3 + Cl 2 + SO 2 1. Cl Cl CH 3(CH 2)n. CHCH 3 SO 3 H 2 Cl 2. CH 3(CH 2)n. CH 2 CH 3 + Cl CH 3(CH 2)n. CHCH 3 + HCl 3. CH 3(CH 2)n. CHCH 3 + SO 2 CH 3(CH 2)n. CHCH 3 4. CH 3(CH 2)n. CHCH 3 + Cl 2 SO 2 CH 3(CH 2)n. CHCH 3 + Cl SO 2 Cl CH 3(CH 2)n. CHCH 3 + 2 Na. OH SO 2 Cl -Na. Cl CH 3(CH 2)n. CHCH 3 SO 3 Na