 Исходное уравнение Оператор Гамильтона Уравнение Шредингера Переходя от декартовым к полярным координатам, получим: Для решения этого уравнения разделим переменные с помощью подстановки Радиальная часть Атом водорода Угловая часть или сферическая гармоника 1 Лекции по квантовой химии
Исходное уравнение Оператор Гамильтона Уравнение Шредингера Переходя от декартовым к полярным координатам, получим: Для решения этого уравнения разделим переменные с помощью подстановки Радиальная часть Атом водорода Угловая часть или сферическая гармоника 1 Лекции по квантовой химии
 Угловая часть m = 0, 1, 2, … C = l(l + 1), l = 0, 1, 2, …, -l m l Присоединенный полином Лежандра Сферическая гармоника Ylm( , ) = lm( ) Атом водорода 2 Лекции по квантовой химии
Угловая часть m = 0, 1, 2, … C = l(l + 1), l = 0, 1, 2, …, -l m l Присоединенный полином Лежандра Сферическая гармоника Ylm( , ) = lm( ) Атом водорода 2 Лекции по квантовой химии
 Радиальная часть Сделаем подстановку C = l(l + 1), a 0 = ħ 2/(mee 2), раскроем скобки и упростим Решение n = 1, 2, 3, …; n l + 1, где l = 0, 1, 2, …, n – 1 Присоединенный полином Лягерра Атом водорода 3 Лекции по квантовой химии
Радиальная часть Сделаем подстановку C = l(l + 1), a 0 = ħ 2/(mee 2), раскроем скобки и упростим Решение n = 1, 2, 3, …; n l + 1, где l = 0, 1, 2, …, n – 1 Присоединенный полином Лягерра Атом водорода 3 Лекции по квантовой химии
 Решения: n l m Орбиталь 1 0 0 1 S 2 0 0 2 S 2 1 1 2 Px 3 0 0 3 S 3 2 1 3 Dxz Атом водорода 4 Лекции по квантовой химии
Решения: n l m Орбиталь 1 0 0 1 S 2 0 0 2 S 2 1 1 2 Px 3 0 0 3 S 3 2 1 3 Dxz Атом водорода 4 Лекции по квантовой химии
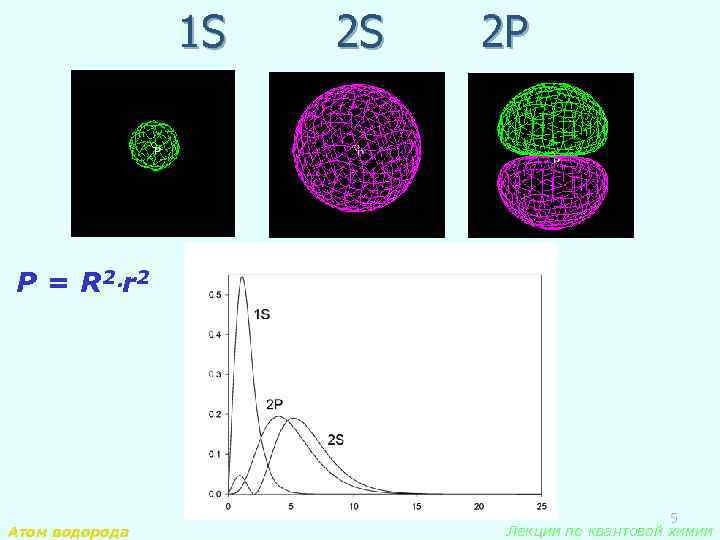 1 S 2 S 2 P P = R 2 r 2 Атом водорода 5 Лекции по квантовой химии
1 S 2 S 2 P P = R 2 r 2 Атом водорода 5 Лекции по квантовой химии
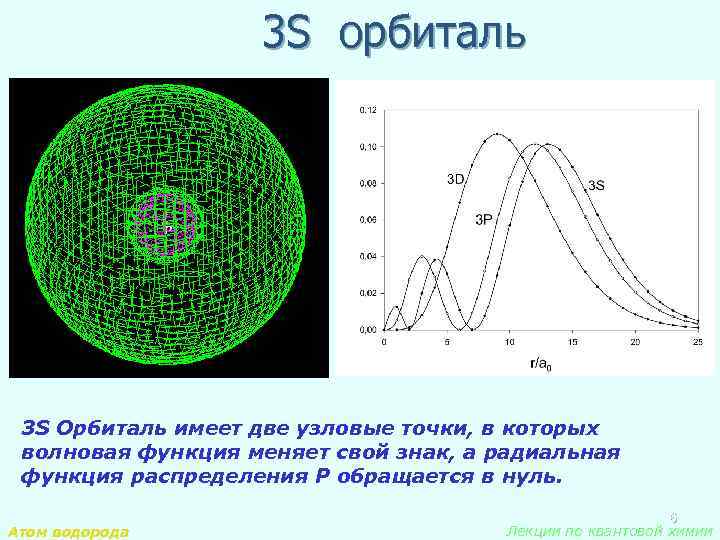 3 S орбиталь 3 S Орбиталь имеет две узловые точки, в которых волновая функция меняет свой знак, а радиальная функция распределения Р обращается в нуль. Атом водорода 6 Лекции по квантовой химии
3 S орбиталь 3 S Орбиталь имеет две узловые точки, в которых волновая функция меняет свой знак, а радиальная функция распределения Р обращается в нуль. Атом водорода 6 Лекции по квантовой химии
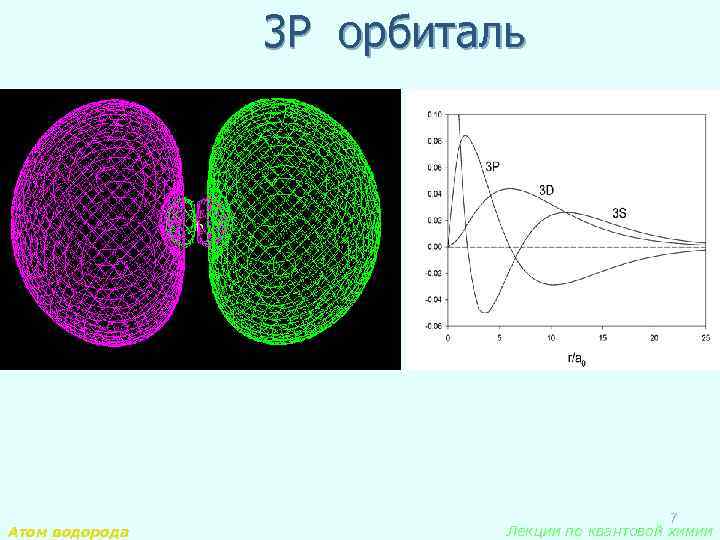 3 P орбиталь Атом водорода 7 Лекции по квантовой химии
3 P орбиталь Атом водорода 7 Лекции по квантовой химии
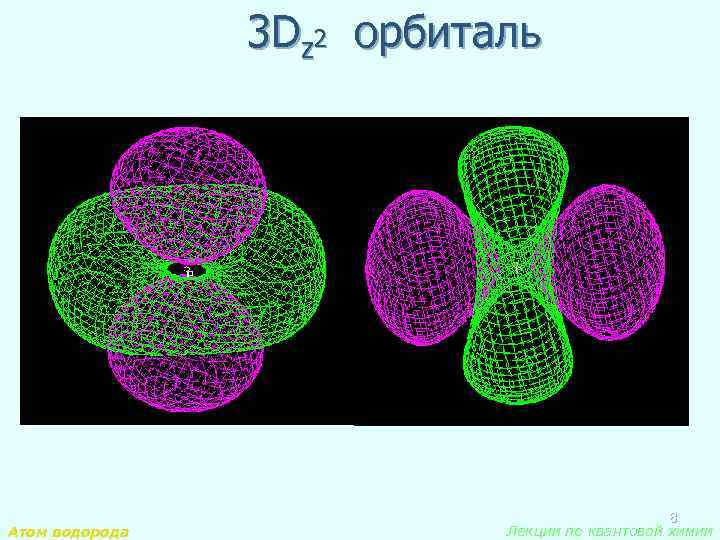 3 Dz 2 орбиталь Атом водорода 8 Лекции по квантовой химии
3 Dz 2 орбиталь Атом водорода 8 Лекции по квантовой химии
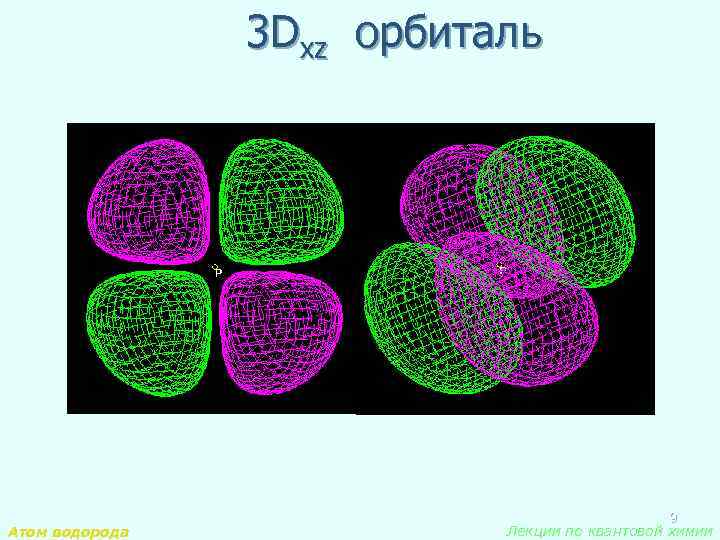 3 Dxz орбиталь Атом водорода 9 Лекции по квантовой химии
3 Dxz орбиталь Атом водорода 9 Лекции по квантовой химии
 4 S орбиталь Вопрос: Сколько узловых точек имеет радиальная функция этой орбитали? Ответ: Правильно, три!!! Атом водорода 10 Лекции по квантовой химии
4 S орбиталь Вопрос: Сколько узловых точек имеет радиальная функция этой орбитали? Ответ: Правильно, три!!! Атом водорода 10 Лекции по квантовой химии
 4 P орбиталь Вопрос: А сколько узловых точек имеет радиальная функция этой орбитали? Ответ: Две, конечно!!! Вот посмотрите… Атом водорода 11 Лекции по квантовой химии
4 P орбиталь Вопрос: А сколько узловых точек имеет радиальная функция этой орбитали? Ответ: Две, конечно!!! Вот посмотрите… Атом водорода 11 Лекции по квантовой химии
 Энергии состояний Частица расчет Энергия 1 S состояния, э. В эксперимент He+ -54. 416 -0. 007 Li 2+ -122. 452 -122. 451 -0. 001 Be 3+ -217. 693 -217. 713 +0. 020 B 4+ Атом водорода -54. 423 -340. 145 -340. 217 +0. 072 12 Лекции по квантовой химии
Энергии состояний Частица расчет Энергия 1 S состояния, э. В эксперимент He+ -54. 416 -0. 007 Li 2+ -122. 452 -122. 451 -0. 001 Be 3+ -217. 693 -217. 713 +0. 020 B 4+ Атом водорода -54. 423 -340. 145 -340. 217 +0. 072 12 Лекции по квантовой химии
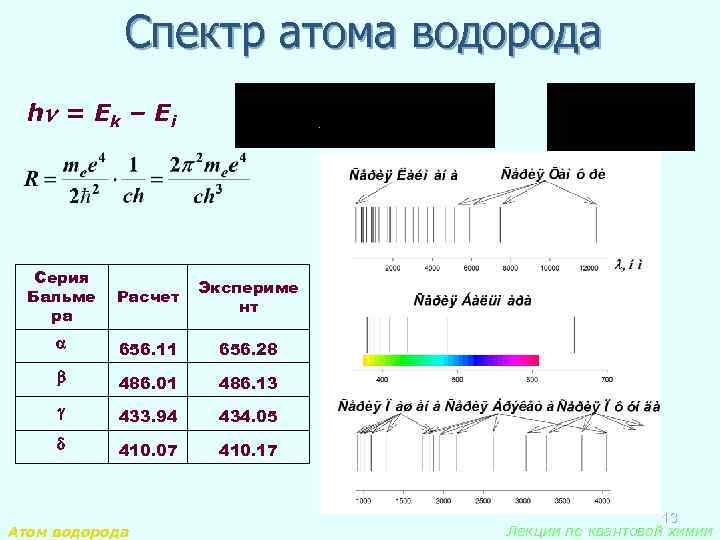 Спектр атома водорода h = Ek – Ei Серия Бальме ра Расчет Экспериме нт 656. 11 656. 28 486. 01 486. 13 433. 94 434. 05 410. 07 410. 17 Атом водорода 13 Лекции по квантовой химии
Спектр атома водорода h = Ek – Ei Серия Бальме ра Расчет Экспериме нт 656. 11 656. 28 486. 01 486. 13 433. 94 434. 05 410. 07 410. 17 Атом водорода 13 Лекции по квантовой химии
 ВЫВОД Квантовомеханическое описание объективно отражает свойства микрообъектов. Это позволяет заключить, что квантовомеханический подход является исключительно полезным и точным методом описания свойств химических соединений. Таким образом, квантовая химия является теоретическим фундаментом химии как науки. Атом водорода 14 Лекции по квантовой химии
ВЫВОД Квантовомеханическое описание объективно отражает свойства микрообъектов. Это позволяет заключить, что квантовомеханический подход является исключительно полезным и точным методом описания свойств химических соединений. Таким образом, квантовая химия является теоретическим фундаментом химии как науки. Атом водорода 14 Лекции по квантовой химии