Источники_связь.ppt
- Количество слайдов: 56
 Источники информирования и методы получения информации о ПР ЛС. Подходы к определению причинно-следственной связи между побочной реакцией и лекарственным средством. Е. В. Матвеева Директор Депаратмента послерегистрационного надзора ГП «Государственный экспертный центр МЗ Украины»
Источники информирования и методы получения информации о ПР ЛС. Подходы к определению причинно-следственной связи между побочной реакцией и лекарственным средством. Е. В. Матвеева Директор Депаратмента послерегистрационного надзора ГП «Государственный экспертный центр МЗ Украины»
 Источники получения сообщений о ПР ЛС 1. Системы с не исчерпывающей, необязательной фиксацией данных. 2. Системы с обязательной фиксацией данных.
Источники получения сообщений о ПР ЛС 1. Системы с не исчерпывающей, необязательной фиксацией данных. 2. Системы с обязательной фиксацией данных.
 Источники о ПР ЛС с обязательной фиксацией данных: Клинические испытания 2. Регистры 3. Программы работы с пациентами 4. Программы управления рисками 1.
Источники о ПР ЛС с обязательной фиксацией данных: Клинические испытания 2. Регистры 3. Программы работы с пациентами 4. Программы управления рисками 1.
 Источники о ПР ЛС с не исчерпывающей, необязательной фиксацией данных o Спонтанные сообщения – добровольная передача информации об одной или более ПР при медицинском применении ЛС от: специалиста здравоохранения потребителя продукции компании (пациента, его близких, адвоката) (эта информация не должна быть получена в ходе исследований или любой другой организованной схемы сбора данных). o Литературные данные (регулярный просмотр мировой научной литературы (обзоры, реферативная информация)). o Интернет (просмотр внешних веб-сайтов). o Другие источники (средства массовой информации).
Источники о ПР ЛС с не исчерпывающей, необязательной фиксацией данных o Спонтанные сообщения – добровольная передача информации об одной или более ПР при медицинском применении ЛС от: специалиста здравоохранения потребителя продукции компании (пациента, его близких, адвоката) (эта информация не должна быть получена в ходе исследований или любой другой организованной схемы сбора данных). o Литературные данные (регулярный просмотр мировой научной литературы (обзоры, реферативная информация)). o Интернет (просмотр внешних веб-сайтов). o Другие источники (средства массовой информации).
 Источники информации о ПР ЛС o Сообщения спонтанного характера, полученные от : - медицинских работников, пациентов, родственников пациентов, из обзоров медицинской литературы.
Источники информации о ПР ЛС o Сообщения спонтанного характера, полученные от : - медицинских работников, пациентов, родственников пациентов, из обзоров медицинской литературы.
 Рекомендации ВООЗ в отношении развития пострегистрационного надзора (ICDRA, 14 -15 сентября 2008 г. , Берн, Швейцария) o Стимулирование разработки регионального, объединенного пострегистрационного надзора и системы фармнадзора для контроля качества, безопасности и эффективности лекарственных средств o Привлечение потребителей к информированию о побочных реакциях лекарственных средств
Рекомендации ВООЗ в отношении развития пострегистрационного надзора (ICDRA, 14 -15 сентября 2008 г. , Берн, Швейцария) o Стимулирование разработки регионального, объединенного пострегистрационного надзора и системы фармнадзора для контроля качества, безопасности и эффективности лекарственных средств o Привлечение потребителей к информированию о побочных реакциях лекарственных средств
 Возможные пути привлечения потребителей к информированию о побочных реакциях лекарственных средств o Создание страницы на официальном сайте компании по безопасности, которая даст возможность пациенту информировать компанию в режиме on-line о возникших осложнениях или отсутствии эффективности применении ЛС компании. o Разработка и внедрение активных программ по работе с пациенами o Внесение в Инструкцию для медицинского применения ЛС информации о контактах, которые дадут возможность пациенту информировать компанию (по телефону, факсом, почтой) о возникших осложнениях или отсутствии эффективности применении ЛС компании.
Возможные пути привлечения потребителей к информированию о побочных реакциях лекарственных средств o Создание страницы на официальном сайте компании по безопасности, которая даст возможность пациенту информировать компанию в режиме on-line о возникших осложнениях или отсутствии эффективности применении ЛС компании. o Разработка и внедрение активных программ по работе с пациенами o Внесение в Инструкцию для медицинского применения ЛС информации о контактах, которые дадут возможность пациенту информировать компанию (по телефону, факсом, почтой) о возникших осложнениях или отсутствии эффективности применении ЛС компании.
 Основные методы получения информации о безопасности ЛС в пострегистрационном периоде o спонтанные сообщения о подозреваемых ПР ЛС, o фармакоэпидемиологические исследования (по типу случай-контроль и когортные), o мониторинг ПР ЛС
Основные методы получения информации о безопасности ЛС в пострегистрационном периоде o спонтанные сообщения о подозреваемых ПР ЛС, o фармакоэпидемиологические исследования (по типу случай-контроль и когортные), o мониторинг ПР ЛС
 Преимущества метода спонтанных сообщений 1. Позволяет: o учитывать все ПР ЛС у всех групп больных, o получать информацию о безопасности всех ЛС, находящихся на фармацевтическом рынке страны; o учитывать ПР, развивающиеся у госпитализированных и амбулаторных больных как на рецептурные, так и безрецептурные средства, как на «новые» , так и на «старые» ЛС; o получать предварительные данные о частоте ПР и степени риска; o выявлять редкие и неожиданные ПР; o выявлять механизм некоторых ПР и группы риска применении ЛС. 2. Прост. 3. Недорог
Преимущества метода спонтанных сообщений 1. Позволяет: o учитывать все ПР ЛС у всех групп больных, o получать информацию о безопасности всех ЛС, находящихся на фармацевтическом рынке страны; o учитывать ПР, развивающиеся у госпитализированных и амбулаторных больных как на рецептурные, так и безрецептурные средства, как на «новые» , так и на «старые» ЛС; o получать предварительные данные о частоте ПР и степени риска; o выявлять редкие и неожиданные ПР; o выявлять механизм некоторых ПР и группы риска применении ЛС. 2. Прост. 3. Недорог
 Недостатки метода спонтанных сообщений o Недосообщения o Не всегда качественные o Неизвестна экспозиция пациентов (т. е. не известен знаменатель) o Частота подачи сообщений зависит от серьезности реакции, длительности пребывания препарата на рынке, промоции препарата и внимания (настороженности) к подозреваемой реакции.
Недостатки метода спонтанных сообщений o Недосообщения o Не всегда качественные o Неизвестна экспозиция пациентов (т. е. не известен знаменатель) o Частота подачи сообщений зависит от серьезности реакции, длительности пребывания препарата на рынке, промоции препарата и внимания (настороженности) к подозреваемой реакции.
 Недостатки метода спонтанных сообщений o не позволяет выявлять весь спектр ПР ЛС из-за o o o низкой сообщаемости о ПР врачами; не позволяет определить частоту встречаемости конкретной ПР; для принятия решения, является ли ПР недопустимо частой, требуется длительный период; не может дать качественную оценку препарату; личное предубеждение врача; наиболее информативен в отношении тяжелых и серьезных ПР, реакций типа А и В.
Недостатки метода спонтанных сообщений o не позволяет выявлять весь спектр ПР ЛС из-за o o o низкой сообщаемости о ПР врачами; не позволяет определить частоту встречаемости конкретной ПР; для принятия решения, является ли ПР недопустимо частой, требуется длительный период; не может дать качественную оценку препарату; личное предубеждение врача; наиболее информативен в отношении тяжелых и серьезных ПР, реакций типа А и В.
 Определение распространенности и частоты побочных реакций лекарственных средств по данным спонтанных сообщений (по Puijnbroek E. P. )
Определение распространенности и частоты побочных реакций лекарственных средств по данным спонтанных сообщений (по Puijnbroek E. P. )
 Примеры побочных реакций лекарственных средств, выявленных методом спонтанных сообщений Лекарственное средство Побочная реакция Левомицетин «Серый синдром» у новорожденных Диэтилстилбестрол Рак влагалища у девочек подростков -адреноблокаторы Диплопия Азапропазон Фотосенсибилизация Флюнарезин, цинаризин Экстрапирамидные расстройства Триазолам Нарушения ЦНС Оральные контрацептивы Тромбоэмболии, взаимодействие с другими ЛС Фенфлюрамин, дексфенфлюрамин Поражение клапанов сердца Эналаприл Ангиоотек Каптоприл Гинекомастия Индалпин Агранолоцитоз Клозапин Агранулоцитоз Фенилбутазон, оксифенилбутазон Агранулоцитоз Астемизол Нарушения сердечного ритма
Примеры побочных реакций лекарственных средств, выявленных методом спонтанных сообщений Лекарственное средство Побочная реакция Левомицетин «Серый синдром» у новорожденных Диэтилстилбестрол Рак влагалища у девочек подростков -адреноблокаторы Диплопия Азапропазон Фотосенсибилизация Флюнарезин, цинаризин Экстрапирамидные расстройства Триазолам Нарушения ЦНС Оральные контрацептивы Тромбоэмболии, взаимодействие с другими ЛС Фенфлюрамин, дексфенфлюрамин Поражение клапанов сердца Эналаприл Ангиоотек Каптоприл Гинекомастия Индалпин Агранолоцитоз Клозапин Агранулоцитоз Фенилбутазон, оксифенилбутазон Агранулоцитоз Астемизол Нарушения сердечного ритма
 Активный мониторинг стационара вид ретроспективного и проспективного исследования и предполагающий сбор демографических, социальных и медицинских данных на всех поступающих в стационар пациентов с целью активного выявления возникающих у них ПР.
Активный мониторинг стационара вид ретроспективного и проспективного исследования и предполагающий сбор демографических, социальных и медицинских данных на всех поступающих в стационар пациентов с целью активного выявления возникающих у них ПР.
 Преимущества метода активного мониторинга стационара 1. 2. 3. Позволяет определить частоту развития ПР Позволяет выявить результаты взаимодействия ЛС Позволяет получить информацию о группах риска развития ПР Недостатки метода активного мониторинга стационара 1. 2. 3. Трудоемкость Ограниченность в применении Дополнительные затраты на осуществление.
Преимущества метода активного мониторинга стационара 1. 2. 3. Позволяет определить частоту развития ПР Позволяет выявить результаты взаимодействия ЛС Позволяет получить информацию о группах риска развития ПР Недостатки метода активного мониторинга стационара 1. 2. 3. Трудоемкость Ограниченность в применении Дополнительные затраты на осуществление.
 Рецептурный мониторинг вид когортных наблюдательных исследований в процессе проведения которого сопоставляется число и качественная характеристика развившехся ПР с количеством назначений исследуемого ЛС по выписанным рецептам в течение периода наблюдения.
Рецептурный мониторинг вид когортных наблюдательных исследований в процессе проведения которого сопоставляется число и качественная характеристика развившехся ПР с количеством назначений исследуемого ЛС по выписанным рецептам в течение периода наблюдения.
 Преимущества метода рецептурного мониторинга 1. 2. 3. 4. 5. 6. Позволяет выявлять ожидаемые и неожиданные ПР. Позволяет выявлять ПР на новые ЛС. Позволяет выявлять ПР с латентным периодом. Позволяет выявлять новые эффекты ЛС. Позволяет выявлять и определять частоту ПР. Такие исследования относительно недорогие. Недостатки метода рецептурного мониторинга 1. 2. 3. 4. Ограничено число больных. Отсутствует группа сравнения. В исследовании не принимают участие пациенты стационаров. Нет возможности проконтролировать соблюдение пациентом рекомендаций врача по применению данного ЛС.
Преимущества метода рецептурного мониторинга 1. 2. 3. 4. 5. 6. Позволяет выявлять ожидаемые и неожиданные ПР. Позволяет выявлять ПР на новые ЛС. Позволяет выявлять ПР с латентным периодом. Позволяет выявлять новые эффекты ЛС. Позволяет выявлять и определять частоту ПР. Такие исследования относительно недорогие. Недостатки метода рецептурного мониторинга 1. 2. 3. 4. Ограничено число больных. Отсутствует группа сравнения. В исследовании не принимают участие пациенты стационаров. Нет возможности проконтролировать соблюдение пациентом рекомендаций врача по применению данного ЛС.
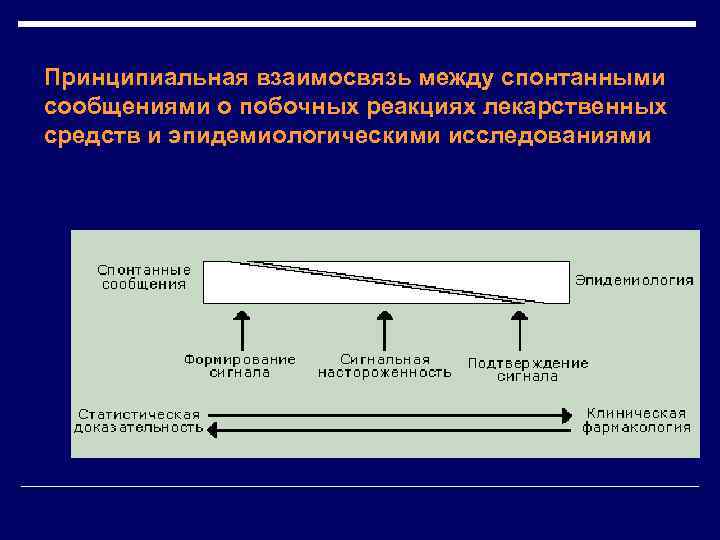 Принципиальная взаимосвязь между спонтанными сообщениями о побочных реакциях лекарственных средств и эпидемиологическими исследованиями
Принципиальная взаимосвязь между спонтанными сообщениями о побочных реакциях лекарственных средств и эпидемиологическими исследованиями
 Значение проведения фармакоэпидемиологических исследований Позволяют уточнить данные о ЛС, полученные в ходе клинических испытаний. 2. Дополнить имеющиеся данные о ЛС новыми сведениями об эффективности и безопасности. 3. Изучить другие аспекты применения препарата. 1.
Значение проведения фармакоэпидемиологических исследований Позволяют уточнить данные о ЛС, полученные в ходе клинических испытаний. 2. Дополнить имеющиеся данные о ЛС новыми сведениями об эффективности и безопасности. 3. Изучить другие аспекты применения препарата. 1.
 Виды дизайна фармакоэпидемиологических исследований 1. 2. 3. 4. 5. Описания отдельных случаев Исследование серий случаев Изучение долговременных тенденций Исследование типа «случайконтроль» Когортные исследования
Виды дизайна фармакоэпидемиологических исследований 1. 2. 3. 4. 5. Описания отдельных случаев Исследование серий случаев Изучение долговременных тенденций Исследование типа «случайконтроль» Когортные исследования
 Информация, которая должна принематься во внимание при проведении оценки безопасности ЛС o o o o o Данные, представленные на официальных сайтах, так называемых, “строгих” регуляторных агентств (США (FDA), ЕС (EMA), Великобритании (MHRA), Канады (НС), Австралии (TGA), Швейцарии (Swissmedic), Японии (PMDA) Результаты переписки по системе Vigimed со странами-участницами международной программы Мониторинга безопасности ЛС ВОЗ Данные, представленные на официальных сайтах компаний Данные международного справочника Martindale Данные общедоступных источников доказательной медицины, а именно: третичных (Модельный формуляр ВОЗ, Национальный Британский формуляр), вторичных (Medline, The Cochrane Library) и первичных* Данные базы данных ВООЗ, Eudravigilance про ПР ЛС Данные базы данных про ПР ЛС ГЭЦ МЗ Украины Приказы МЗ, Постановления КМ Украины Решения НЭС Центру, рабочих групп Центра, специалистов МЗ * Хотя не существует формальных критериев отбора, тем не менее, любой источник информации (сайт), особенно первичный, должен отбираться согласно определенным критериям, что позволяет выбирать лишь высококачественные источники (Dennett L. Health Technology Assessment on the Net: A. Guide to Internet Sources of Information/ L. Dennett, T. Chatterley [Электоронный ресурс]. - [10 -th Edition]. -June 2008. - 36 p. - Access mode: - URL: http: //www. ihe. ca/documents/HTA_10 thedition_0. pdf/ Title from the screen; Topfer L. A. Etext on Health Technology Assessment (HTA)/ L. A. Topfer, L. Auston [Электоронный ресурс]. - Access mode: - URL: http: //www. nlm. nih. gov/archive//2060905/nichsr/ehta. html. - Title from the screen).
Информация, которая должна принематься во внимание при проведении оценки безопасности ЛС o o o o o Данные, представленные на официальных сайтах, так называемых, “строгих” регуляторных агентств (США (FDA), ЕС (EMA), Великобритании (MHRA), Канады (НС), Австралии (TGA), Швейцарии (Swissmedic), Японии (PMDA) Результаты переписки по системе Vigimed со странами-участницами международной программы Мониторинга безопасности ЛС ВОЗ Данные, представленные на официальных сайтах компаний Данные международного справочника Martindale Данные общедоступных источников доказательной медицины, а именно: третичных (Модельный формуляр ВОЗ, Национальный Британский формуляр), вторичных (Medline, The Cochrane Library) и первичных* Данные базы данных ВООЗ, Eudravigilance про ПР ЛС Данные базы данных про ПР ЛС ГЭЦ МЗ Украины Приказы МЗ, Постановления КМ Украины Решения НЭС Центру, рабочих групп Центра, специалистов МЗ * Хотя не существует формальных критериев отбора, тем не менее, любой источник информации (сайт), особенно первичный, должен отбираться согласно определенным критериям, что позволяет выбирать лишь высококачественные источники (Dennett L. Health Technology Assessment on the Net: A. Guide to Internet Sources of Information/ L. Dennett, T. Chatterley [Электоронный ресурс]. - [10 -th Edition]. -June 2008. - 36 p. - Access mode: - URL: http: //www. ihe. ca/documents/HTA_10 thedition_0. pdf/ Title from the screen; Topfer L. A. Etext on Health Technology Assessment (HTA)/ L. A. Topfer, L. Auston [Электоронный ресурс]. - Access mode: - URL: http: //www. nlm. nih. gov/archive//2060905/nichsr/ehta. html. - Title from the screen).
 Критерии отбора источника/сайта информации o Авторитетность и надежность (authority and reliability) – o o разработан некоммерческими организациями (организации и университеты, которые финансируются правительством) Используемость (currency) – регулярно обновляется (за исключением некоторых сайтов, которые были включены по историческим причинам) Применимость (applicability) – содержит ценную информацию для оценки технологий здравоохранения Достоверность (validity) – библиографические базы данных, которые, как правило, содержат рецензированные исследования, оценку технологий здравоохранения и источники здравоохранения на основе доказательной медицины, которые в целом придерживаются допустимых методов для обеспечения полноты, прозрачности и надежности методов, которые используются в их систематических обзорах Простота в использовании (usability) – структура этих сайтов позволяет легко ориентироваться и производить поиск
Критерии отбора источника/сайта информации o Авторитетность и надежность (authority and reliability) – o o разработан некоммерческими организациями (организации и университеты, которые финансируются правительством) Используемость (currency) – регулярно обновляется (за исключением некоторых сайтов, которые были включены по историческим причинам) Применимость (applicability) – содержит ценную информацию для оценки технологий здравоохранения Достоверность (validity) – библиографические базы данных, которые, как правило, содержат рецензированные исследования, оценку технологий здравоохранения и источники здравоохранения на основе доказательной медицины, которые в целом придерживаются допустимых методов для обеспечения полноты, прозрачности и надежности методов, которые используются в их систематических обзорах Простота в использовании (usability) – структура этих сайтов позволяет легко ориентироваться и производить поиск
 Для чего нужно определять причинно-следственную связь между побочной реакцией (ПР) и подозреваемым лекарственным средством (ЛС)? o Чтобы определить степень причастности ЛС к возникновению ПР o В качестве помощи при обнаружении сигнала o Для оценки и принятия мер по обеспечению безопасности ЛС: Изменения в регистрационном свидетельстве ЛС или изменения в медицинской/фармацевтической практике должны основываться на доказательствах p Возможно ли что ЛС А может вызвать ПР В? p Возможно ли что ЛС А привело к возникновению ПР В у конкретного пациента? Pia Caduff-Janosa; 2011 23
Для чего нужно определять причинно-следственную связь между побочной реакцией (ПР) и подозреваемым лекарственным средством (ЛС)? o Чтобы определить степень причастности ЛС к возникновению ПР o В качестве помощи при обнаружении сигнала o Для оценки и принятия мер по обеспечению безопасности ЛС: Изменения в регистрационном свидетельстве ЛС или изменения в медицинской/фармацевтической практике должны основываться на доказательствах p Возможно ли что ЛС А может вызвать ПР В? p Возможно ли что ЛС А привело к возникновению ПР В у конкретного пациента? Pia Caduff-Janosa; 2011 23
 Критерии Бредфорда Хилла o o o o o Сила Логичность Специфичность Временна связь я Биологический градиент (кривая доза-ответ) Биологическое правдоподобие Согласованность событий Эксперимент Аналогия » Sir Austin Bradford Hill, January 14 th 1965 24
Критерии Бредфорда Хилла o o o o o Сила Логичность Специфичность Временна связь я Биологический градиент (кривая доза-ответ) Биологическое правдоподобие Согласованность событий Эксперимент Аналогия » Sir Austin Bradford Hill, January 14 th 1965 24
 Методы o Стандартизованная оценка (алгоритмы) o Вычисление вероятности o Глобальная интроспекция (критерии оценки причинно-следственной связи ВОЗ) Pia Caduff-Janosa; 2011
Методы o Стандартизованная оценка (алгоритмы) o Вычисление вероятности o Глобальная интроспекция (критерии оценки причинно-следственной связи ВОЗ) Pia Caduff-Janosa; 2011
 Основные проблемы o Общие сложности в медицинской диагностике o Отсутствие диагностических индикаторов или лабораторных тестов, доказывающих степень причастности ЛС к возникшей ПР за исключением передозирования или использования ЛС в нетерапевтических дозах, если ПР можно связать с фармакокинетическими параметрами ЛС o Клинические проявления ПР, спровоцированные ЛС, зачастую сложно отличить от симптоматики основного заболевания n Pia Caduff-Janosa; 2011 26
Основные проблемы o Общие сложности в медицинской диагностике o Отсутствие диагностических индикаторов или лабораторных тестов, доказывающих степень причастности ЛС к возникшей ПР за исключением передозирования или использования ЛС в нетерапевтических дозах, если ПР можно связать с фармакокинетическими параметрами ЛС o Клинические проявления ПР, спровоцированные ЛС, зачастую сложно отличить от симптоматики основного заболевания n Pia Caduff-Janosa; 2011 26
 Алгоритмы o Стандартизованный набор вопросов с подсчетом результата, что позволяет: n Снизить вариабельность результатов у разных экспертов n Снизить вариабельности результатов у одного эксперта Pia Caduff-Janosa; 2011 27
Алгоритмы o Стандартизованный набор вопросов с подсчетом результата, что позволяет: n Снизить вариабельность результатов у разных экспертов n Снизить вариабельности результатов у одного эксперта Pia Caduff-Janosa; 2011 27
 Алгоритмы (продолжение) o Время возникновения ПР? o Реакция на месте введения? o ПР возникла сразу после введения ЛС и было острое начало? o ПР прошла после отмены ЛС/ПР появилась после повторного назначения ЛС? o Сопутствующие ЛС отменили в то же время, что и подозреваемое ЛС? o Такая же ПР возникала раньше на это же подозреваемое ЛС? o ПР известна для этого ЛС? o Morges International Meeting 1981 28
Алгоритмы (продолжение) o Время возникновения ПР? o Реакция на месте введения? o ПР возникла сразу после введения ЛС и было острое начало? o ПР прошла после отмены ЛС/ПР появилась после повторного назначения ЛС? o Сопутствующие ЛС отменили в то же время, что и подозреваемое ЛС? o Такая же ПР возникала раньше на это же подозреваемое ЛС? o ПР известна для этого ЛС? o Morges International Meeting 1981 28
 Алгоритмы (продолжение) o Нет согласованности между различными алгоритмами o Вариабельность результатов у одного/разных экспертов снижена, однако все же присутствует o Нет проверки o Отсутствующие данные? o Вопросы „вводящие в заблуждение“? (Наранжо 10) Pia Caduff-Janosa; 2011 29
Алгоритмы (продолжение) o Нет согласованности между различными алгоритмами o Вариабельность результатов у одного/разных экспертов снижена, однако все же присутствует o Нет проверки o Отсутствующие данные? o Вопросы „вводящие в заблуждение“? (Наранжо 10) Pia Caduff-Janosa; 2011 29
 Алгоритм Наранжо Вопрос Да Нет Не знаю 1. Имеются ли достоверные сообщения о такой же реакции, выявленные ранее? +1 0 0 2. Побочная реакция (ПР) возникла после введения подозреваемого лекарственного средства (ЛС)? +2 -1 0 3. ПР уменьшилась после отмены ЛС или после введения специфического антагониста? +1 0 0 4. ПР повторилась после повторного использования ЛС? +2 -1 0 5. Существуют ли альтернативные причины (кроме подозреваемого ЛС), которые могли бы вызвать эту ПР? -1 +2 0 6. Возникала ли ПР при использовании плацебо? -1 +1 0 7. Был ли выявлен препарат в крови (или другой биологической жидкости организма) в токсической концентрации? +1 0 0 8. Интенсивность проявления ПР усилилась после повышения дозы ЛС, или снизилась после снижения дозы ЛС? +1 0 0 9. Возникали у пациента аналогичные реакции применении того же самого ЛС или ему подобного ЛС в прошлом? +1 0 0 10. ПР была подтверждена объективными данными? +1 0 0 Общий балл Балл
Алгоритм Наранжо Вопрос Да Нет Не знаю 1. Имеются ли достоверные сообщения о такой же реакции, выявленные ранее? +1 0 0 2. Побочная реакция (ПР) возникла после введения подозреваемого лекарственного средства (ЛС)? +2 -1 0 3. ПР уменьшилась после отмены ЛС или после введения специфического антагониста? +1 0 0 4. ПР повторилась после повторного использования ЛС? +2 -1 0 5. Существуют ли альтернативные причины (кроме подозреваемого ЛС), которые могли бы вызвать эту ПР? -1 +2 0 6. Возникала ли ПР при использовании плацебо? -1 +1 0 7. Был ли выявлен препарат в крови (или другой биологической жидкости организма) в токсической концентрации? +1 0 0 8. Интенсивность проявления ПР усилилась после повышения дозы ЛС, или снизилась после снижения дозы ЛС? +1 0 0 9. Возникали у пациента аналогичные реакции применении того же самого ЛС или ему подобного ЛС в прошлом? +1 0 0 10. ПР была подтверждена объективными данными? +1 0 0 Общий балл Балл
 Расчет вероятности o Теорема Байеса p апостериорные шансы = коэффициент вероятности x априорные шансы o Сложные расчеты o Данные, необходимые для подсчета коэффициента вероятности, часто недоступны и/или непостоянны для разных популяций o Можно успешно применять только для большого набора данных Pia Caduff-Janosa; 2011 31
Расчет вероятности o Теорема Байеса p апостериорные шансы = коэффициент вероятности x априорные шансы o Сложные расчеты o Данные, необходимые для подсчета коэффициента вероятности, часто недоступны и/или непостоянны для разных популяций o Можно успешно применять только для большого набора данных Pia Caduff-Janosa; 2011 31
 Глобальная интроспекция o Хронология (согласование во времени) o Идентификация проявлений/симптомов o Ретроспективная оценка частоты события o Исследования o Отмена/повторное назначение Pia Caduff-Janosa; 2011 32
Глобальная интроспекция o Хронология (согласование во времени) o Идентификация проявлений/симптомов o Ретроспективная оценка частоты события o Исследования o Отмена/повторное назначение Pia Caduff-Janosa; 2011 32
 Оцениваемые элементы o Пациент o ЛС o Событие/явление o Хронология o Отмена/повторное назначение o Лечение Pia Caduff-Janosa; 2011
Оцениваемые элементы o Пациент o ЛС o Событие/явление o Хронология o Отмена/повторное назначение o Лечение Pia Caduff-Janosa; 2011
 Категории причинно-следственной связи между подозреваемым ЛС и ПР (согласно качественной методике ее определения ВОЗ) o Определенная причинно-следственная связь (І) o Вероятная причинно-следственная связь (ІІ) o Возможная причинно-следственная связь (ІІІ) o Сомнительная причинно-следственная связь (IV) o Условная причинно-следственная связь (V) o Отсутствующая причинно-следственная связь (не подлежит идентификации) (VI)
Категории причинно-следственной связи между подозреваемым ЛС и ПР (согласно качественной методике ее определения ВОЗ) o Определенная причинно-следственная связь (І) o Вероятная причинно-следственная связь (ІІ) o Возможная причинно-следственная связь (ІІІ) o Сомнительная причинно-следственная связь (IV) o Условная причинно-следственная связь (V) o Отсутствующая причинно-следственная связь (не подлежит идентификации) (VI)
 Критерии определения причинно-следственной связи между подозреваемым ЛС и ПР (согласно качественной методике ее определения ВОЗ) - Наличие связи во времени между ПР и подозреваемым ЛС / или отсутствие такового; - Возможность объяснения ПР наличием существующих заболеваний, влиянием других факторов или химических соединений / или невозможность такового; - Регресс ПР после отмены подозреваемого ЛС / или отсутствие такового; - Возникновение ПР вновь при повторном назначении ЛС / или отсутствие таковой.
Критерии определения причинно-следственной связи между подозреваемым ЛС и ПР (согласно качественной методике ее определения ВОЗ) - Наличие связи во времени между ПР и подозреваемым ЛС / или отсутствие такового; - Возможность объяснения ПР наличием существующих заболеваний, влиянием других факторов или химических соединений / или невозможность такового; - Регресс ПР после отмены подозреваемого ЛС / или отсутствие такового; - Возникновение ПР вновь при повторном назначении ЛС / или отсутствие таковой.
 Степень достоверности причинно-следственной связи между ПР и подозреваемым ЛС Достоверная, определенная (Certain) - клинические проявления ПР, включая нарушения лабораторных показателей: o связаны по времени с приемом ЛС; o не могут быть объяснены сопутствующими заболеваниями, приемом других ЛС или воздействием химических веществ; o уменьшаются или исчезают в ответ на отмену ЛС; o вновь возникают при повторном назначении ЛС по клиническим показаниям. Ключевой признак: реакция повторилась после повторного назначения ЛС
Степень достоверности причинно-следственной связи между ПР и подозреваемым ЛС Достоверная, определенная (Certain) - клинические проявления ПР, включая нарушения лабораторных показателей: o связаны по времени с приемом ЛС; o не могут быть объяснены сопутствующими заболеваниями, приемом других ЛС или воздействием химических веществ; o уменьшаются или исчезают в ответ на отмену ЛС; o вновь возникают при повторном назначении ЛС по клиническим показаниям. Ключевой признак: реакция повторилась после повторного назначения ЛС
 Процесс оценки связи Проверочная логика. . . Связь является. . . определенной если: § было повторное назначение ЛС и известен его результат (повторное возникновение ПР, клинические проявления которой аналогичны тем, что возникали при назначении этого ЛС ранее) Исключение o Анафилаксия Очевидная прямая связь (без повторного назначения ЛС!!!) Определенная Geraldine Hill; 2011 37
Процесс оценки связи Проверочная логика. . . Связь является. . . определенной если: § было повторное назначение ЛС и известен его результат (повторное возникновение ПР, клинические проявления которой аналогичны тем, что возникали при назначении этого ЛС ранее) Исключение o Анафилаксия Очевидная прямая связь (без повторного назначения ЛС!!!) Определенная Geraldine Hill; 2011 37
 Пример 1 Пациент: К. С. П. , мужчина, 31 год, №и/б 2014. Диагноз: ВИЧ-инфекция. Клиническая стадия ІІІ. Кандидоз слизистой полости рта. Лечение: начато 18. 04. 2010 г. препаратами: ламивудин/зидовудин (таб. 150/300 мг 2 раза в сутки), эфавиренз (таб. 600 мг 1 раз в сутки). Описание клинической ситуации: через сутки от начала лечения (19. 04. 2010 г. ) возникла сильная тошнота, однократная рвота. В связи с возникшей симптоматикой 20. 04. 2010 пациент обратился к врачу, пациенту был назначен метоклопрамид (10 мг 3 раза в сутки), АРТ не отменялась. В течение трех дней симптомы не прекратились. 23. 04. 2010 врач отменил АРТ. Указанные симптомы прошли 25. 04. 2010. После обращения к врачу 26. 04. 10 г. , повторно были назначены ламивудин/зидовудин и эфавиренз в том же дозовом режиме. Тошнота возобновилась, многократная рвота. После повторного обращения 28. 04. 2010 г. препарат ламивудин/зидовудин был заменен на тенофовир (300 мг 1 раз в сутки) и ламивудин (150 мг 2 раза в сутки), эфавиренз не отменялся. Тошнота и рвота больше не повторялись.
Пример 1 Пациент: К. С. П. , мужчина, 31 год, №и/б 2014. Диагноз: ВИЧ-инфекция. Клиническая стадия ІІІ. Кандидоз слизистой полости рта. Лечение: начато 18. 04. 2010 г. препаратами: ламивудин/зидовудин (таб. 150/300 мг 2 раза в сутки), эфавиренз (таб. 600 мг 1 раз в сутки). Описание клинической ситуации: через сутки от начала лечения (19. 04. 2010 г. ) возникла сильная тошнота, однократная рвота. В связи с возникшей симптоматикой 20. 04. 2010 пациент обратился к врачу, пациенту был назначен метоклопрамид (10 мг 3 раза в сутки), АРТ не отменялась. В течение трех дней симптомы не прекратились. 23. 04. 2010 врач отменил АРТ. Указанные симптомы прошли 25. 04. 2010. После обращения к врачу 26. 04. 10 г. , повторно были назначены ламивудин/зидовудин и эфавиренз в том же дозовом режиме. Тошнота возобновилась, многократная рвота. После повторного обращения 28. 04. 2010 г. препарат ламивудин/зидовудин был заменен на тенофовир (300 мг 1 раз в сутки) и ламивудин (150 мг 2 раза в сутки), эфавиренз не отменялся. Тошнота и рвота больше не повторялись.
 Пример 1 Категория побочной реакции: ничего (несерьезная ожидаемая побочная реакция), ПЛС – зидовудин. Причинно-следственная связь: достоверная.
Пример 1 Категория побочной реакции: ничего (несерьезная ожидаемая побочная реакция), ПЛС – зидовудин. Причинно-следственная связь: достоверная.
 Вероятная (Probable) - клинические проявления ПР, включая нарушения лабораторных показателей: o связаны по времени с приемом ЛС; o не могут быть объяснены сопутствующими заболеваниями, приемом других ЛС или воздействием химических веществ; o уменьшаются или исчезают в ответ на отмену ЛС; o повторно ЛС не назначался Ключевой признак: позитивный результат отмены ЛС (проявления ПР исчезли или регрессируют)
Вероятная (Probable) - клинические проявления ПР, включая нарушения лабораторных показателей: o связаны по времени с приемом ЛС; o не могут быть объяснены сопутствующими заболеваниями, приемом других ЛС или воздействием химических веществ; o уменьшаются или исчезают в ответ на отмену ЛС; o повторно ЛС не назначался Ключевой признак: позитивный результат отмены ЛС (проявления ПР исчезли или регрессируют)
 Процесс оценки связи Проверочная логика. . . Связь не является. . . определенной если: § не было повторного назначения ЛС или его результат неизвестен Связь вероятная если: § была отмена ЛС и результат отмены известен § известен результат события Geraldine Hill; 2011 41
Процесс оценки связи Проверочная логика. . . Связь не является. . . определенной если: § не было повторного назначения ЛС или его результат неизвестен Связь вероятная если: § была отмена ЛС и результат отмены известен § известен результат события Geraldine Hill; 2011 41
 Исключения: o Смерть Не может быть закодирована как вероятная, так как нет возможности оценить эффект отмены ЛС Возможная o Инфаркт миокарда Многие пациенты выздоравливают в силу естественного течения болезни; выздоровление не является ответом на отмену ЛС, поэтому результат отмены ЛС не имеет смысла Возможная o Инсульт Вариабельность естественных выздоровлений; повторное назначение не имеет смысла Возможная Geraldine Hill; 2011 42
Исключения: o Смерть Не может быть закодирована как вероятная, так как нет возможности оценить эффект отмены ЛС Возможная o Инфаркт миокарда Многие пациенты выздоравливают в силу естественного течения болезни; выздоровление не является ответом на отмену ЛС, поэтому результат отмены ЛС не имеет смысла Возможная o Инсульт Вариабельность естественных выздоровлений; повторное назначение не имеет смысла Возможная Geraldine Hill; 2011 42
 Пример 2 Пациент: В. П. Н. , мужчина, 34 года, № и/б 6132. Диагноз: ВИЧ-инфекция. IІІ клиническая стадия. Кандидоз слизистой полости рта, Хронический вирусный гепатит С, репликативная фаза, генотип 3 а. Лечение: Зидовудин/ламивудин по 300/150 мг 2 раза в сутки длительно (с 25. 03. 2008 г. ), эфавиренц по 600 мг 1 раз в сутки длительно (с 25. 03. 2008 г. ). В связи с началом лечения ХГС, 02. 2010 г. зидовудин/ламивудин заменен на ламивудин по 150 мг 2 раза в сутки длительно и тенофовир по 300 мг 1 раз в сутки длительно. Пегинтрон-120 по 120 мкг 1 раз в неделю п/к в течение 48 недель (с 03. 02. 2010 г. ), ребетол по 200 мг, 2 таблетки 2 раза в сутки в течение 48 недель (с 03. 02. 2010 г. ). Описание клинической ситуации: 03. 2010 г. при плановом обращении к врачу по данным контрольных лабораторных исследований (через 30 дней после начала приема TDF) выявлено повышение уровня креатинина и снижение клиренса креатинина. Данные лабораторных исследований: 02. 03. 2010 г. : креатинин - 155, 4 мкмоль/л, клиренс креатинина – 62, 7 мл/мин. ; 02. 03. 2010 г. : лейкоциты - 2, 5 х10 х9/л; эритроциты – 3, 1 х10 х12/л, гемоглобин - 110 г/л, мочевина - 9, 4 ммоль/л; 09. 03. 2010 г. : креатинин - 340, 6 мкмоль/л, клиренс креатинина – 28, 68 мл/мин. ; 18. 03. 2010 г. : креатинин - 120 мкмоль/л, клиренс креатинина - 81 мл/мин. (после коррекции и отмены препаратов). Коррекция клинической ситуации: 09. 03. 2010 г. - отмена тенофовира, замена тенофовира на зидовудин по 300 мг 2 раза в сутки длительно. Контроль гемоглобина! Контроль креатинина!
Пример 2 Пациент: В. П. Н. , мужчина, 34 года, № и/б 6132. Диагноз: ВИЧ-инфекция. IІІ клиническая стадия. Кандидоз слизистой полости рта, Хронический вирусный гепатит С, репликативная фаза, генотип 3 а. Лечение: Зидовудин/ламивудин по 300/150 мг 2 раза в сутки длительно (с 25. 03. 2008 г. ), эфавиренц по 600 мг 1 раз в сутки длительно (с 25. 03. 2008 г. ). В связи с началом лечения ХГС, 02. 2010 г. зидовудин/ламивудин заменен на ламивудин по 150 мг 2 раза в сутки длительно и тенофовир по 300 мг 1 раз в сутки длительно. Пегинтрон-120 по 120 мкг 1 раз в неделю п/к в течение 48 недель (с 03. 02. 2010 г. ), ребетол по 200 мг, 2 таблетки 2 раза в сутки в течение 48 недель (с 03. 02. 2010 г. ). Описание клинической ситуации: 03. 2010 г. при плановом обращении к врачу по данным контрольных лабораторных исследований (через 30 дней после начала приема TDF) выявлено повышение уровня креатинина и снижение клиренса креатинина. Данные лабораторных исследований: 02. 03. 2010 г. : креатинин - 155, 4 мкмоль/л, клиренс креатинина – 62, 7 мл/мин. ; 02. 03. 2010 г. : лейкоциты - 2, 5 х10 х9/л; эритроциты – 3, 1 х10 х12/л, гемоглобин - 110 г/л, мочевина - 9, 4 ммоль/л; 09. 03. 2010 г. : креатинин - 340, 6 мкмоль/л, клиренс креатинина – 28, 68 мл/мин. ; 18. 03. 2010 г. : креатинин - 120 мкмоль/л, клиренс креатинина - 81 мл/мин. (после коррекции и отмены препаратов). Коррекция клинической ситуации: 09. 03. 2010 г. - отмена тенофовира, замена тенофовира на зидовудин по 300 мг 2 раза в сутки длительно. Контроль гемоглобина! Контроль креатинина!
 Пример 2 Категория побочной реакции: госпитализация (серьезная ожидаемая побочная реакция), ПЛС – тенофовир. Причинно-следственная связь: вероятная.
Пример 2 Категория побочной реакции: госпитализация (серьезная ожидаемая побочная реакция), ПЛС – тенофовир. Причинно-следственная связь: вероятная.
 Возможная (Possible) - клинические проявления ПР, включая нарушения лабораторных показателей: • связаны по времени с приемом ЛС; • могут быть объяснены сопутствующими заболеваниями или приемом других ЛС или воздействием химических веществ; • информация о реакции на отмену ЛС недостаточна или неясна Ключевой признак: клинические проявления ПР могут быть объяснены не только применением подозреваемого ЛС, но и другими причинами
Возможная (Possible) - клинические проявления ПР, включая нарушения лабораторных показателей: • связаны по времени с приемом ЛС; • могут быть объяснены сопутствующими заболеваниями или приемом других ЛС или воздействием химических веществ; • информация о реакции на отмену ЛС недостаточна или неясна Ключевой признак: клинические проявления ПР могут быть объяснены не только применением подозреваемого ЛС, но и другими причинами
 Пример 3 Пациент: А. Р. К. , женщина, 25 лет, беременность 27 недель, № и/б 2867 Диагноз: ВИЧ-инфекция. Клиническая стадия ІІI (CD 4 230 кл/мкл). Волосатая лейкоплакия языка. Острый пиелонефрит. Лечение: зидовудин по 300 мг 2 раза в сутки (с 27. 01. 2011 г. постоянно), ламивудин по 150 мг 2 раза в сутки(с 27. 01. 2011 г. постоянно), невирапин по 200 мг 1 раз в сутки (с 27. 01. 2011 г. постоянно), ампициллин по 0, 5 г 4 раза в сутки в/м (03. 02. 2011 г. - 12. 02. 2011 г. ). Описание клинической ситуации: 05. 02. 2011 г. возникла острая крапивница. Коррекция клинической ситуации: отмена АРТ, ампициллина. Медикаментозная коррекция: супрастин 2 мл в/м однократно, дексаметазон 4 мг однократно. ПР прошла в тот же день (05. 02. 2011 г. ) после медикаментозной коррекции без последствий. С целью лечения пиелонефрита назначен цефипим 1 г 2 раза в сутки в/м (06. 02. 2011 г. -15. 02. 2011 г. ). С 16. 02. 2011 г. возобновлен прием АРВ-препаратов: зидовудин, ламивудин, - в прежнем дозовом режиме. Начат прием АРВ-препарата лопинавир/ритонавир 400/100 мг 2 раза в сутки. Препарат невирапин повторно не назначался.
Пример 3 Пациент: А. Р. К. , женщина, 25 лет, беременность 27 недель, № и/б 2867 Диагноз: ВИЧ-инфекция. Клиническая стадия ІІI (CD 4 230 кл/мкл). Волосатая лейкоплакия языка. Острый пиелонефрит. Лечение: зидовудин по 300 мг 2 раза в сутки (с 27. 01. 2011 г. постоянно), ламивудин по 150 мг 2 раза в сутки(с 27. 01. 2011 г. постоянно), невирапин по 200 мг 1 раз в сутки (с 27. 01. 2011 г. постоянно), ампициллин по 0, 5 г 4 раза в сутки в/м (03. 02. 2011 г. - 12. 02. 2011 г. ). Описание клинической ситуации: 05. 02. 2011 г. возникла острая крапивница. Коррекция клинической ситуации: отмена АРТ, ампициллина. Медикаментозная коррекция: супрастин 2 мл в/м однократно, дексаметазон 4 мг однократно. ПР прошла в тот же день (05. 02. 2011 г. ) после медикаментозной коррекции без последствий. С целью лечения пиелонефрита назначен цефипим 1 г 2 раза в сутки в/м (06. 02. 2011 г. -15. 02. 2011 г. ). С 16. 02. 2011 г. возобновлен прием АРВ-препаратов: зидовудин, ламивудин, - в прежнем дозовом режиме. Начат прием АРВ-препарата лопинавир/ритонавир 400/100 мг 2 раза в сутки. Препарат невирапин повторно не назначался.
 Пример 3 Категория побочной реакции: ничего (несерьезная ожидаемая побочная реакция), ПЛС – ампициллин. Причинно-следственная связь: возможная
Пример 3 Категория побочной реакции: ничего (несерьезная ожидаемая побочная реакция), ПЛС – ампициллин. Причинно-следственная связь: возможная
 Сомнительная (Unlikely) – клинические проявления (ПР), включая нарушения лабораторных показателей: o когда нет четкой временной связи с приемом ЛС; o могут быть объяснены сопутствующими заболеваниями, использованием других ЛС или воздействием химических веществ Ключевой признак: несколько факторов могут быть причиной возникновения клинической ситуации
Сомнительная (Unlikely) – клинические проявления (ПР), включая нарушения лабораторных показателей: o когда нет четкой временной связи с приемом ЛС; o могут быть объяснены сопутствующими заболеваниями, использованием других ЛС или воздействием химических веществ Ключевой признак: несколько факторов могут быть причиной возникновения клинической ситуации
 Пример 4 Пациент: Л. А. М. , женщина, 55 лет, № и/б 132 Диагноз: ВИЧ-инфекция. Клиническая стадия II. Ангулярный хейлит. Гипертоническая болезнь I стадии. Лечение: начато 10. 06. 2011 АРВ-препаратами: трувада (таб, комбинированный препарат, содержащий эмтрицитабин 200 мг/тенофовир 300 мг 1 раз в сутки), эфавиренз (табл. 600 мг 1 раз в сутки). Сопутствующего лечения по поводу ГБ регулярно не принимала. Описание клинической ситуации: С 11. 06. 2011 г. появилась сильная головная боль, головокружение. Коррекция клинической ситуации: 15. 06. 2011 г. при визите к врачу АД 140/100 мм рт. ст. Для коррекции проявлений побочной реакции был назначен эналаприл 10 мг 1 раз в сутки длительно. Эфавиренз был отменен и назначен лопинавир/ритонавир по 400/100 мг 2 раза в сутки. Прием трувады продолжался в прежнем дозовом режиме. Проявления побочной реакции прошли 16. 06. 2011 г. без последствий. .
Пример 4 Пациент: Л. А. М. , женщина, 55 лет, № и/б 132 Диагноз: ВИЧ-инфекция. Клиническая стадия II. Ангулярный хейлит. Гипертоническая болезнь I стадии. Лечение: начато 10. 06. 2011 АРВ-препаратами: трувада (таб, комбинированный препарат, содержащий эмтрицитабин 200 мг/тенофовир 300 мг 1 раз в сутки), эфавиренз (табл. 600 мг 1 раз в сутки). Сопутствующего лечения по поводу ГБ регулярно не принимала. Описание клинической ситуации: С 11. 06. 2011 г. появилась сильная головная боль, головокружение. Коррекция клинической ситуации: 15. 06. 2011 г. при визите к врачу АД 140/100 мм рт. ст. Для коррекции проявлений побочной реакции был назначен эналаприл 10 мг 1 раз в сутки длительно. Эфавиренз был отменен и назначен лопинавир/ритонавир по 400/100 мг 2 раза в сутки. Прием трувады продолжался в прежнем дозовом режиме. Проявления побочной реакции прошли 16. 06. 2011 г. без последствий. .
 Пример 4 Категория побочной реакции: ничего (несерьезная ожидаемая побочная реакция), ПЛС – эфавиренз. Причинно-следственная связь: сомнительная. .
Пример 4 Категория побочной реакции: ничего (несерьезная ожидаемая побочная реакция), ПЛС – эфавиренз. Причинно-следственная связь: сомнительная. .
 Отсутствие причинной связи (Unrelated) – клинические проявления, включая лабораторные показатели: · когда отсутствует временная связь с приемом ЛС; · имеются четкие доказательства отсутствия причинной связи данной нежелательной реакцией с приемом препарата Ключевой признак: не возможно оценить по имеющейся информации Pia Caduff-Janosa; 2011
Отсутствие причинной связи (Unrelated) – клинические проявления, включая лабораторные показатели: · когда отсутствует временная связь с приемом ЛС; · имеются четкие доказательства отсутствия причинной связи данной нежелательной реакцией с приемом препарата Ключевой признак: не возможно оценить по имеющейся информации Pia Caduff-Janosa; 2011
 Пример 5 Пациентка: Б. Г. Д. , женщина, 39 лет, медицинская сестра, номер истории болезни 2745. Диагноз: постконтактная профилактика ВИЧ Клиническая ситуация: в течение 28 дней (01. 02. 10 по 28. 02. 10) пациентка принимала препарат «комбивудин» (зидовудин 300 мг/ламивудин 150 мг) 1 табл. 2 раза в сутки и «алувия» (лопинавир 400 мг/ритонавир 100 мг) 2 табл. 2 раза в сутки в качестве постконтактной профилактики. В январе 2011 года у пациентки развилась гипохромная анемия. Гемогобин 86 г/л, Эр – 3, 5 Х 1012/л. Пациентка обратилась к терапевту 10. 01. 2011 г. , назначен глобирон 1 капс. в сутки в течение 30 дней, открыт больничный лист. При повторном обращении к врачу 24. 01. 2011 г. , гемоглобин 105 г/л, Эр – 3, 8 Х 1012/л. , Б/Л закрыт. В феврале пациентка обратилась в страховую компанию за компенсацией, т. к она связала развитие анемии с приемом комбивудина в прошлом.
Пример 5 Пациентка: Б. Г. Д. , женщина, 39 лет, медицинская сестра, номер истории болезни 2745. Диагноз: постконтактная профилактика ВИЧ Клиническая ситуация: в течение 28 дней (01. 02. 10 по 28. 02. 10) пациентка принимала препарат «комбивудин» (зидовудин 300 мг/ламивудин 150 мг) 1 табл. 2 раза в сутки и «алувия» (лопинавир 400 мг/ритонавир 100 мг) 2 табл. 2 раза в сутки в качестве постконтактной профилактики. В январе 2011 года у пациентки развилась гипохромная анемия. Гемогобин 86 г/л, Эр – 3, 5 Х 1012/л. Пациентка обратилась к терапевту 10. 01. 2011 г. , назначен глобирон 1 капс. в сутки в течение 30 дней, открыт больничный лист. При повторном обращении к врачу 24. 01. 2011 г. , гемоглобин 105 г/л, Эр – 3, 8 Х 1012/л. , Б/Л закрыт. В феврале пациентка обратилась в страховую компанию за компенсацией, т. к она связала развитие анемии с приемом комбивудина в прошлом.
 Пример 5 Категория побочной реакции: временная нетрудоспособность (серьезная ожидаемая побочная реакция), ПЛС – комбивудин. Причинно-следственная связь: отсутствует.
Пример 5 Категория побочной реакции: временная нетрудоспособность (серьезная ожидаемая побочная реакция), ПЛС – комбивудин. Причинно-следственная связь: отсутствует.
 Преимущества оценки причинно-следственной связи o Снижает (однако не исключает) разногласия между экспертами o Оценивание каждого индивидуального случая ПР o Классификация степени определенности Pia Caduff-Janosa; 2011
Преимущества оценки причинно-следственной связи o Снижает (однако не исключает) разногласия между экспертами o Оценивание каждого индивидуального случая ПР o Классификация степени определенности Pia Caduff-Janosa; 2011
 Недостатки оценки причинно-следственной связи o Нет количественного измерения вероятности ассоциации o Нет доказательств причинно-следственной связи o Оценка всегда временная Pia Caduff-Janosa; 2011
Недостатки оценки причинно-следственной связи o Нет количественного измерения вероятности ассоциации o Нет доказательств причинно-следственной связи o Оценка всегда временная Pia Caduff-Janosa; 2011
 Спасибо за внимание!
Спасибо за внимание!


