Источники тока из овощей и фруктов.ppt
- Количество слайдов: 18

Исследовательскую работу выполнили: Коскин Игорь Прохорова Дарья Третьяков Борис Научный руководители: Мостович Е. А. научный сотрудник НИОХ СО РАН, преподаватель кафедры органической химии НГУ. Дубцова Ю. Ю. преподаватель высшей квалификационной категории, кандидат биологических наук.

Цель: Создание наиболее эффективного источника тока из доступных овощей или фруктов и исследование его работы. Задачами нашей работы являются: 1)Изучение основных свойств гальванических элементов и их экспериментальное доказательство. 2)Изучение различных овощей и фруктов и выбор из них наиболее эффективного источника тока. 3)Сборка различных источников тока.

Это источник тока, в котором энергия протекающих в нём химических реакций непосредственно превращается в электрическую энергию. Аккумулятор Гальванический элемент Топливный элемент Используются обратимые Реагенты электрохимиреакции, перезарядка ческой реакции подают. Реакции необратимы, возможна ся извне а продукты значит перезарядка удаляются. Функциониневозможна рует непрерывно.
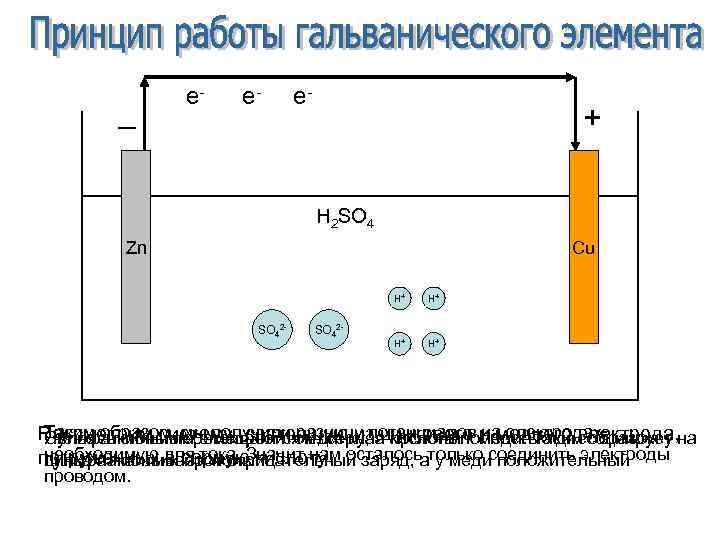
_ e- e- e- + H 2 SO 4 Zn Cu H+ SO 42 - H+ H+ H+ Таким образом, мы получили разницу потенциалов на электродах, Рассмотрим систему, состоящую из цинкового и медного электрода, Сульфат-ионы перемещаются к цинку, а протоны к меди. Таким образом у Являясь сильным электролитом, серная кислота полностью диссоциирует на необходимую для тока. Значит нам осталось только соединить электроды погруженных в серную кислоту цинка накапливается отрицательный заряд, а у меди положительный сульфат-ионы и протоны проводом.

1)Электрохимическое напряжение металлов (стандартный потенциал) 2)Концентрация электролита 3)Температура 4)Время работы гальванического элемента

Пара U Железо - Медь 405 м. В Железо - Свинец 210 м. В Алюминий – Медь 555 м. В Алюминий – Свинец 450 м. В Алюминий – Железо 310 м. В Свинец - Медь 385 м. В Эл ряд
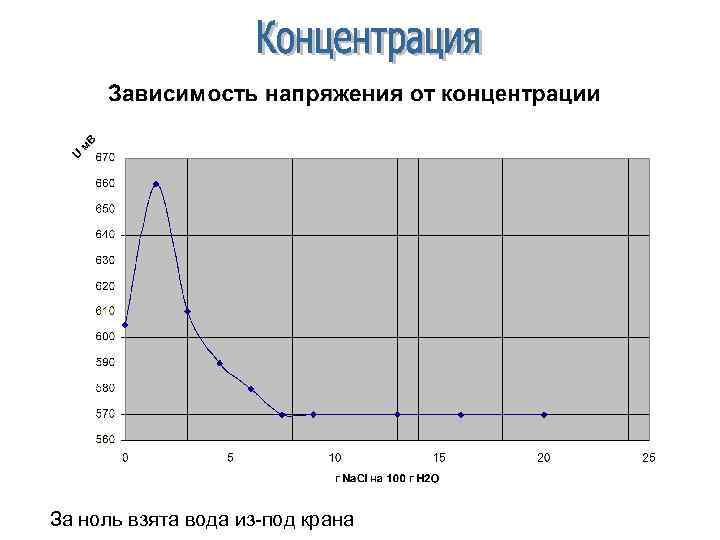
За ноль взята вода из-под крана


Na. Cl Cl- Zn Na+ Na+ Cl- Na+ H+ H+ Cl- Cu Na+ OH-OH-- Но когда мы добавим еще соли, то концентрация ионов вырастет, а В начальный момент времени, в воде присутствуют только гидроксид Когда мы растворяем в воде соль или кислоту, то концентрация ионов расстояние между ними уменьшится, и заряды начнут компенсировать ионы и протоны от самодиссоциации воды, но их концентрация растет, из-за чего электрохимическая реакция идет активнее друга очень мала

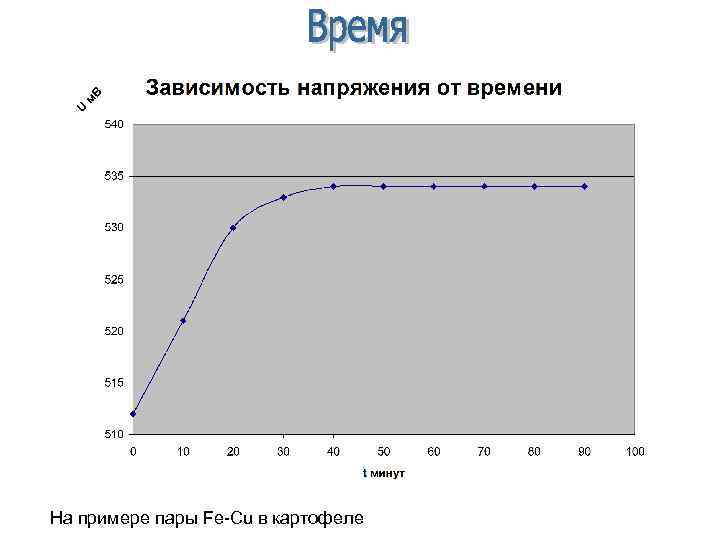
На примере пары Fe-Cu в картофеле

Уравнения Нернста является основным уравнением для системы гальванического элемента. R — универсальная газовая постоянная T — абсолютная температура F — число Фарадея n — число молей электронов, участвующих в процессе aoxи ared — активности соответственно окисленной и восстановленной форм вещества, участвующего в полуреакции.

Одной из возможных схем сборки является так называемый вольтов столб. В нем гальванические элементы соединены последовательно, а значит напряжение будет расти. Вольтов столб был назван в честь своего изобретателя – А. Вольта.

Измерения с парой Fe-Cu Фрукт/Овощ U Апельсин 600 м. В Лимон 570 м. В Груша 550 м. В Яблоко 565 м. В Картофель 530 м. В Свекла 520 м. В Морковь 510 м. В Огурец 530 м. В

Картофель Кожура картофеля 510 м. В Очищенный картофель 525 м. В Неочищенный картофель 535 м. В Лимон Кожура лимона 530 м. В Сок лимона 495 м. В Долька лимона 520 м. В В кожуре и в дольке лимона (медь в дольку, железо в кожуру) 555 м. В В кожуре и в дольке лимона (медь в кожуру, железо в дольку) 450 м. В Яблоко Кожура яблока 530 м. В Очищенное от кожуры, целое 560 м. В Неочищенное от кожуры, целое 580 м. В Долька, неочищенная 555 м. В Долька, очищенная 525 м. В



1)Экспериментально было доказана правильность уравнение Нернста: напряжение зависит от концентрации, температуры и активности металлов. 2)Наиболее эффективным и экономически выгодным источником тока является лимон 3)Собран источник тока из лимонов по типу вольтового столба. 4)С помощью источника тока из лимонов был зажжен светодиод.
Источники тока из овощей и фруктов.ppt