Research.pptx
- Количество слайдов: 27
 Исследовательская деятельность № 3 стол
Исследовательская деятельность № 3 стол
 Теория Свойства идеального газа: 1. Собственный объем молекул газа мал по сравнению с объемом сосуда 2. Между молекулами идеального газа отсутствует взаимодействие (кроме столкновений) 3. Упругое столкновение между молекулами газа и со стенками сосуда
Теория Свойства идеального газа: 1. Собственный объем молекул газа мал по сравнению с объемом сосуда 2. Между молекулами идеального газа отсутствует взаимодействие (кроме столкновений) 3. Упругое столкновение между молекулами газа и со стенками сосуда
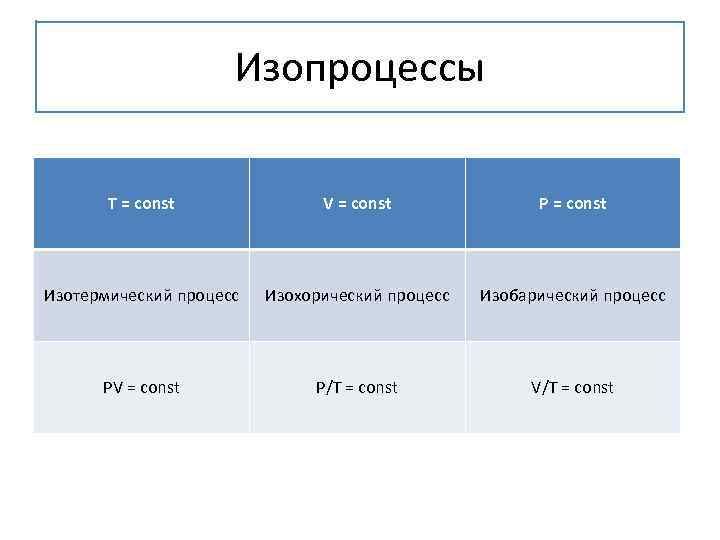 Изопроцессы T = const V = const P = const Изотермический процесс Изохорический процесс Изобарический процесс PV = const P/T = const V/T = const
Изопроцессы T = const V = const P = const Изотермический процесс Изохорический процесс Изобарический процесс PV = const P/T = const V/T = const
 Уравнение состояния идеального газа Уравнение, которое связывает параметры термодинамической системы, находящейся в состоянии равновесия
Уравнение состояния идеального газа Уравнение, которое связывает параметры термодинамической системы, находящейся в состоянии равновесия
 Формула Клапейрона - Менделеева P=nk. T Универсальная газовая постоянная R = 8, 31 Дж/(моль·К) = const Постоянная Больцмана k = R/Na = 1, 38· 10 -23 Дж/К = const
Формула Клапейрона - Менделеева P=nk. T Универсальная газовая постоянная R = 8, 31 Дж/(моль·К) = const Постоянная Больцмана k = R/Na = 1, 38· 10 -23 Дж/К = const
 Связь давления с импульсом Известно, что давление определяется, как где F – сила, S – площадь поверхности. В свою очередь сила – это производная от импульса. Поэтому, давление прямо пропорционально импульсу, которым обладают хаотически движущиеся молекулы Также известно, что давление
Связь давления с импульсом Известно, что давление определяется, как где F – сила, S – площадь поверхности. В свою очередь сила – это производная от импульса. Поэтому, давление прямо пропорционально импульсу, которым обладают хаотически движущиеся молекулы Также известно, что давление
 Средняя квадратичная скорость молекул идеального газа V 2 = 3 k. T/m=3 RT/M Средняя кинетическая энергия
Средняя квадратичная скорость молекул идеального газа V 2 = 3 k. T/m=3 RT/M Средняя кинетическая энергия
 Эксперимент № 1 Цель: Провести опыт. Надуть шар в бутылке и вне бутылки Оборудование: • воздушный шар • стеклянная бутылка • горячая вода • холодная вода
Эксперимент № 1 Цель: Провести опыт. Надуть шар в бутылке и вне бутылки Оборудование: • воздушный шар • стеклянная бутылка • горячая вода • холодная вода
 Шаги 1. Нагреть бутылку кипятком 2. Надеть на бутылку шарик 3. Быстро опустить бутылку в холодную воду Результат после 3 шага
Шаги 1. Нагреть бутылку кипятком 2. Надеть на бутылку шарик 3. Быстро опустить бутылку в холодную воду Результат после 3 шага
 Шаги 4. Вытащить и нагреть, используя горячую воду Результат после 4 шага
Шаги 4. Вытащить и нагреть, используя горячую воду Результат после 4 шага
 Объяснение 1. После нагревания бутылки часть воздуха покинуло бутылку. Сразу после одевания шарика давление внутри бутылки равно атмосферному. При охлаждении бутылки уменьшается давление воздуха внутри бутылки. За счет этого шарик втягивается во внутрь бутылки. 2. При нагревании бутылки увеличивается давление воздуха в ней, и шарик постепенно выходит из бутылки. Формула Клапейрона- Менделеева
Объяснение 1. После нагревания бутылки часть воздуха покинуло бутылку. Сразу после одевания шарика давление внутри бутылки равно атмосферному. При охлаждении бутылки уменьшается давление воздуха внутри бутылки. За счет этого шарик втягивается во внутрь бутылки. 2. При нагревании бутылки увеличивается давление воздуха в ней, и шарик постепенно выходит из бутылки. Формула Клапейрона- Менделеева
 Теория термодинамики Первый закон термодинамики: Теплота, сообщаемая системе, расходуется на изменение ее внутренней энергии и совершение работы против внешних сил
Теория термодинамики Первый закон термодинамики: Теплота, сообщаемая системе, расходуется на изменение ее внутренней энергии и совершение работы против внешних сил
 Второй закон термодинамики: Тепло передается от более горячему телу к более холодному – направление передачи тепла
Второй закон термодинамики: Тепло передается от более горячему телу к более холодному – направление передачи тепла
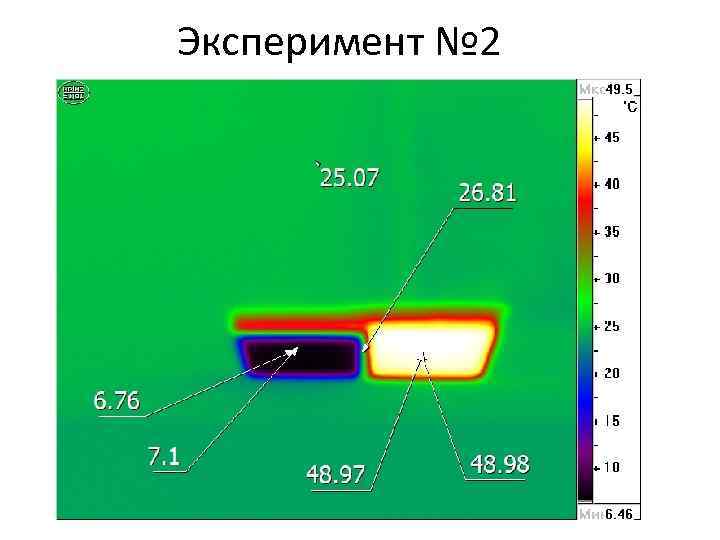 Эксперимент № 2
Эксперимент № 2
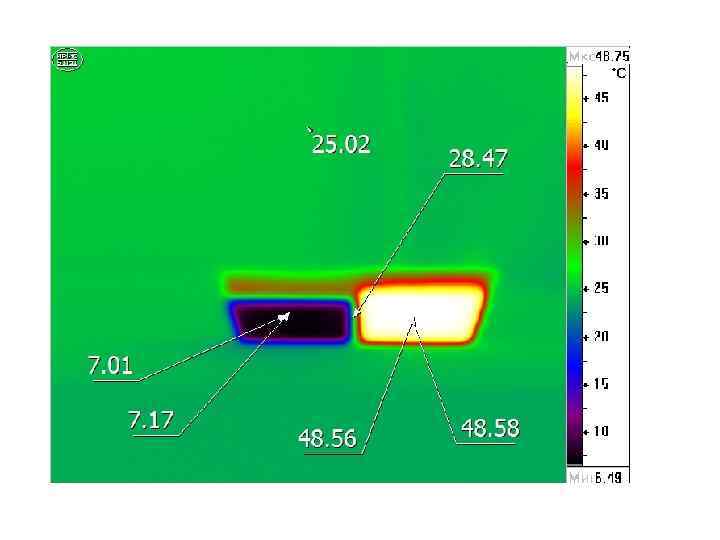
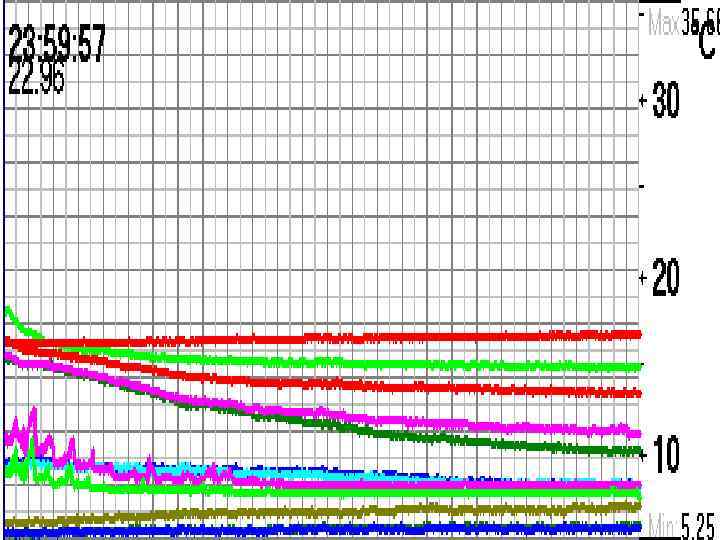
 Не увидели такой график, т. к. температура меняется плавно из-за инерции в системе источник тепла – приемник тепла T, С Q, Дж
Не увидели такой график, т. к. температура меняется плавно из-за инерции в системе источник тепла – приемник тепла T, С Q, Дж
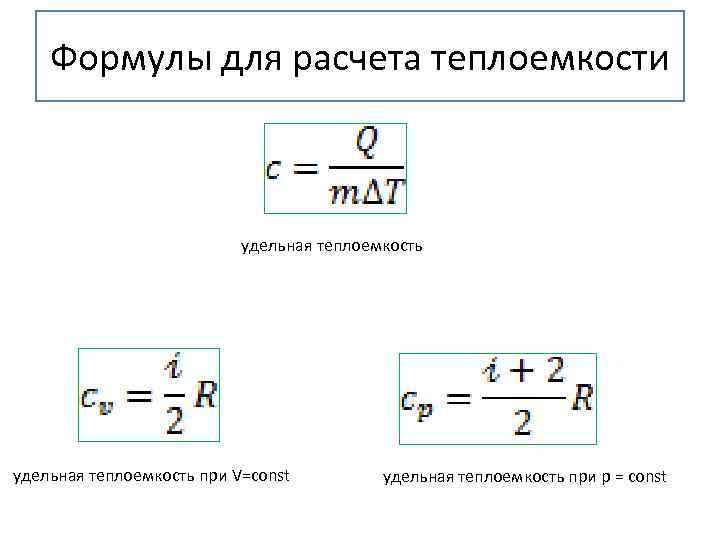 Формулы для расчета теплоемкости удельная теплоемкость при V=const удельная теплоемкость при p = const
Формулы для расчета теплоемкости удельная теплоемкость при V=const удельная теплоемкость при p = const
 Эксперимент № 3 Цель: Поиск удельной теплоемкости воды Оборудование: • Электрический чайник мощностью 2000 Вт, • термометр, • 1 л воды, • термограф, • секундомер
Эксперимент № 3 Цель: Поиск удельной теплоемкости воды Оборудование: • Электрический чайник мощностью 2000 Вт, • термометр, • 1 л воды, • термограф, • секундомер
 Ход работы: 1. Наливаем в чайник воду и измеряем ее температуру. 2. Начинаем нагревать воду приблизительно в течение минуты. 3. После нагревания измеряем температуру воды. 4. Находим общую теплоемкость
Ход работы: 1. Наливаем в чайник воду и измеряем ее температуру. 2. Начинаем нагревать воду приблизительно в течение минуты. 3. После нагревания измеряем температуру воды. 4. Находим общую теплоемкость
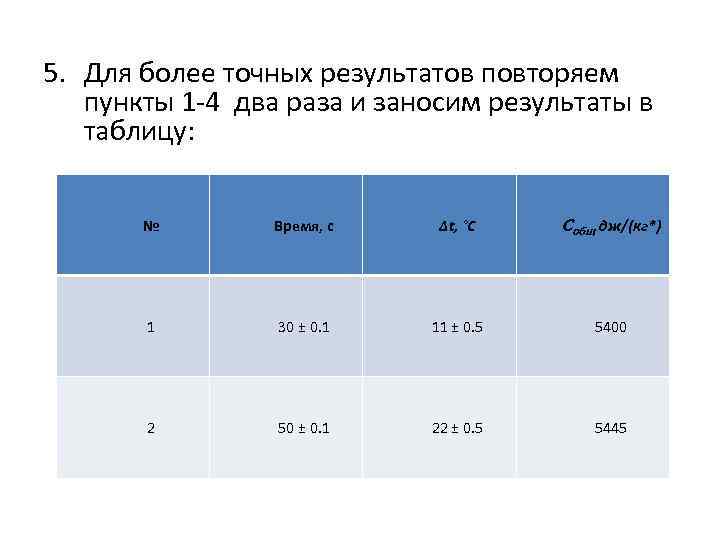 5. Для более точных результатов повторяем пункты 1 -4 два раза и заносим результаты в таблицу: № Время, с Δt, °C Cобщ дж/(кг*) 1 30 ± 0. 1 11 ± 0. 5 5400 2 50 ± 0. 1 22 ± 0. 5 5445
5. Для более точных результатов повторяем пункты 1 -4 два раза и заносим результаты в таблицу: № Время, с Δt, °C Cобщ дж/(кг*) 1 30 ± 0. 1 11 ± 0. 5 5400 2 50 ± 0. 1 22 ± 0. 5 5445
 6. Зная, что общая теплоемкость рассчитывается , вычитаем из нее теплоемкость чайника, которая примерно равна 1200 Дж/(кг∙°С), получаем, что удельная теплоемкость равна
6. Зная, что общая теплоемкость рассчитывается , вычитаем из нее теплоемкость чайника, которая примерно равна 1200 Дж/(кг∙°С), получаем, что удельная теплоемкость равна
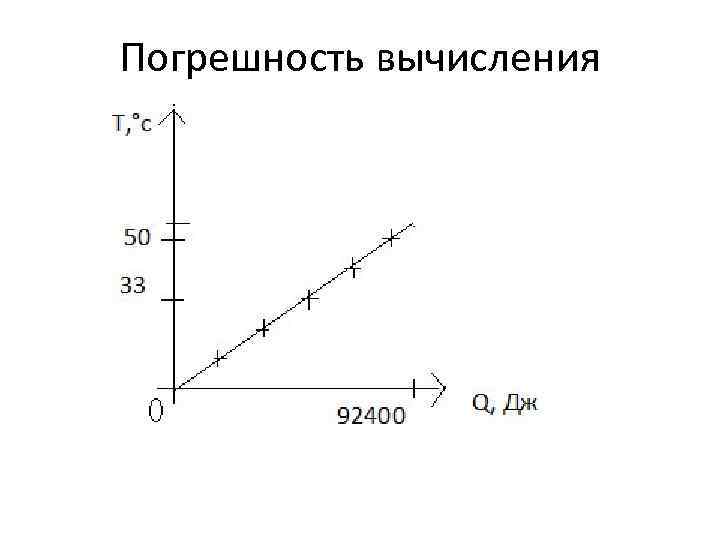 Погрешность вычисления
Погрешность вычисления
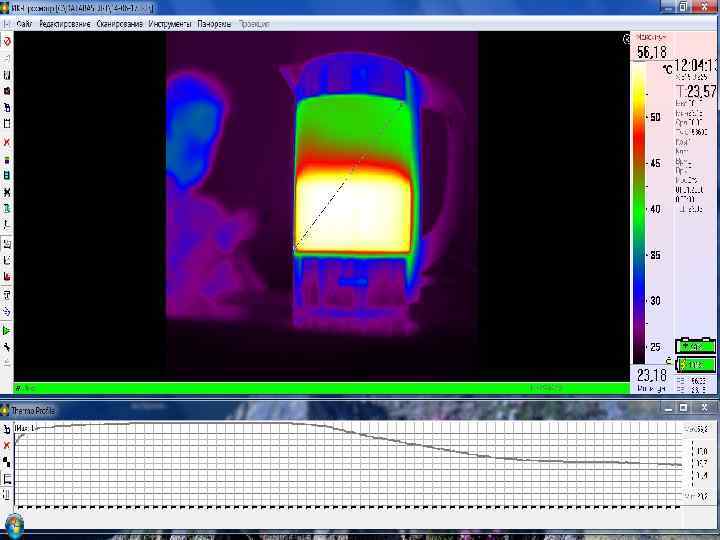
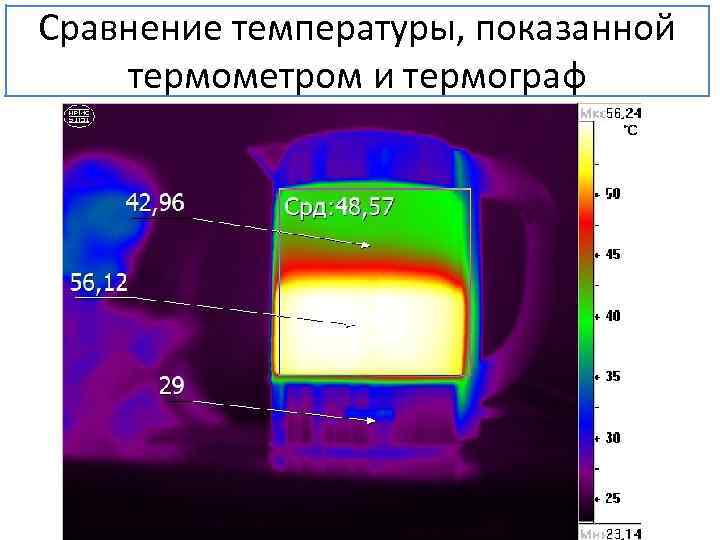 Сравнение температуры, показанной термометром и термограф
Сравнение температуры, показанной термометром и термограф
 Вывод Все наблюдаемые тепловые явления объясняются динамикой молекул, из которых состоит вещество
Вывод Все наблюдаемые тепловые явления объясняются динамикой молекул, из которых состоит вещество



