Лекция 9_Исследования с участием человека.ppt
- Количество слайдов: 27
 Исследования с участием человека. Часть 2 Лекция 9 Вишневская Юлия Андреевна
Исследования с участием человека. Часть 2 Лекция 9 Вишневская Юлия Андреевна
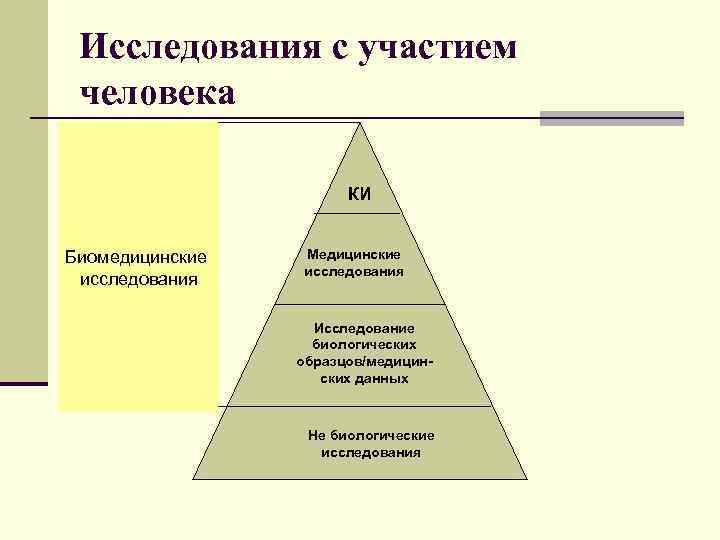 Исследования с участием человека КИ Биомедицинские исследования Медицинские исследования Исследование биологических образцов/медицинских данных Не биологические исследования
Исследования с участием человека КИ Биомедицинские исследования Медицинские исследования Исследование биологических образцов/медицинских данных Не биологические исследования
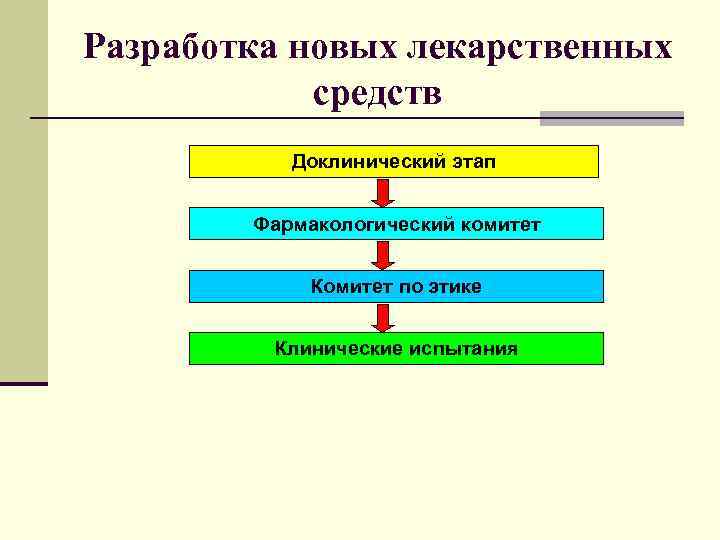 Разработка новых лекарственных средств Доклинический этап Фармакологический комитет Комитет по этике Клинические испытания
Разработка новых лекарственных средств Доклинический этап Фармакологический комитет Комитет по этике Клинические испытания
 Клинические испытания n Клинические испытания являются видом научной деятельности, без которого невозможны получение и отбор новых более эффективных и безопасных лекарств. В последнее время роль клинических исследований возросла в связи с внедрением в практическое здравоохранение принципов доказательной медицины. Главным среди них является принятие конкретных клинических решений для лечения пациента не столько на основе личного опыта или мнения экспертов, сколько исходя из строго доказанных научных данных, которые могут быть получены в ходе хорошо спланированных, контролируемых клинических исследований.
Клинические испытания n Клинические испытания являются видом научной деятельности, без которого невозможны получение и отбор новых более эффективных и безопасных лекарств. В последнее время роль клинических исследований возросла в связи с внедрением в практическое здравоохранение принципов доказательной медицины. Главным среди них является принятие конкретных клинических решений для лечения пациента не столько на основе личного опыта или мнения экспертов, сколько исходя из строго доказанных научных данных, которые могут быть получены в ходе хорошо спланированных, контролируемых клинических исследований.
 Уровни доказательности КИ n Класс (уровень) I (A) большие двойные слепые плацебоконтролируемые исследования, а также данные, полученные при мета-анализе нескольких рандомизированных контролируемых исследований. n Класс (уровень) II (B) небольшие рандомизированные и контролируемые исследования, при которых статистические данные построены на небольшом числе больных. n Класс (уровень) III (C) нерандомизированные клинические исследования на ограниченном количестве пациентов. n Класс (уровень) IV (D) выработка группой экспертов консенсуса по определённой проблеме
Уровни доказательности КИ n Класс (уровень) I (A) большие двойные слепые плацебоконтролируемые исследования, а также данные, полученные при мета-анализе нескольких рандомизированных контролируемых исследований. n Класс (уровень) II (B) небольшие рандомизированные и контролируемые исследования, при которых статистические данные построены на небольшом числе больных. n Класс (уровень) III (C) нерандомизированные клинические исследования на ограниченном количестве пациентов. n Класс (уровень) IV (D) выработка группой экспертов консенсуса по определённой проблеме
 Фазы клинических испытаний n Фаза 1 включает тщательное исследование зависимости «доза-эффект» на небольшой группе здоровых добровольцев (20 -30 человек). Исключение составляют противоопухолевые препараты и средства для лечения ВИЧ, которые проводятся на уже больных пациентах. На этой фазе проводят исследование острых эффектов лекарственных препаратов в широком диапазоне доз, начиная с доз, не вызывающих ожидаемого эффекта, и заканчивая дозами, вызывающими главный терапевтический эффект или минимальный токсический. Цель: определение оптимальной дозировки, которые вызывают желаемый эффект, а также особенности фармакокинетики препарата. n Фаза 2 включает оценку терапевтического эффекта препарата на ограниченной группе пациентов (100 -300 человек), страдающих заболеванием, являющимся главной целью данного вида терапии. Целью данного этапа является установить наличие терапевтического действия исследуемого препарата в дозах, переносимых больными пациентами.
Фазы клинических испытаний n Фаза 1 включает тщательное исследование зависимости «доза-эффект» на небольшой группе здоровых добровольцев (20 -30 человек). Исключение составляют противоопухолевые препараты и средства для лечения ВИЧ, которые проводятся на уже больных пациентах. На этой фазе проводят исследование острых эффектов лекарственных препаратов в широком диапазоне доз, начиная с доз, не вызывающих ожидаемого эффекта, и заканчивая дозами, вызывающими главный терапевтический эффект или минимальный токсический. Цель: определение оптимальной дозировки, которые вызывают желаемый эффект, а также особенности фармакокинетики препарата. n Фаза 2 включает оценку терапевтического эффекта препарата на ограниченной группе пациентов (100 -300 человек), страдающих заболеванием, являющимся главной целью данного вида терапии. Целью данного этапа является установить наличие терапевтического действия исследуемого препарата в дозах, переносимых больными пациентами.
 Фазы клинических испытаний n Фаза 3 представляет собой широкую исследовательскую программу обследования от 1 до 5 тысяч пациентов – многоцентровое исследование. Препарат исследуется в том виде, в котором он предложен для окончательного использования. Цель: дальнейшее исследование желаемого терапевтического эффекта, сравнение его с другими терапевтическими эффектами, установления редких токсических явлений, которые не могут быть выявлены в ходе фазы 2. Результаты передаются в Фармакологический комитет. После получения одобрения препарат поступает в продажу. n Фаза 4 служит для выявления всех видов крайне редко встречающейся токсичности, о которой будет сообщено достаточно рано, чтобы предотвратить терапевтическую катастрофу. Оцениваются отдаленные последствия лечения.
Фазы клинических испытаний n Фаза 3 представляет собой широкую исследовательскую программу обследования от 1 до 5 тысяч пациентов – многоцентровое исследование. Препарат исследуется в том виде, в котором он предложен для окончательного использования. Цель: дальнейшее исследование желаемого терапевтического эффекта, сравнение его с другими терапевтическими эффектами, установления редких токсических явлений, которые не могут быть выявлены в ходе фазы 2. Результаты передаются в Фармакологический комитет. После получения одобрения препарат поступает в продажу. n Фаза 4 служит для выявления всех видов крайне редко встречающейся токсичности, о которой будет сообщено достаточно рано, чтобы предотвратить терапевтическую катастрофу. Оцениваются отдаленные последствия лечения.
 Методы клинических испытаний n n n Исследование является контролируемым, когда исследуемый препарат сравнивают с группой сравнения (контрольной группой). Группой сравнения может быть: другое активное лечение – имеющее уже известную эффективность и переносимость; другая доза или лекарственная форма того же препарата; плацебо; отсутствие лечения; рутинная терапия (лечение, не оговорённое протоколом исследования) или исторический контроль. Кроме того, при проведении каждого клинического исследования используется контроль исходного состояния.
Методы клинических испытаний n n n Исследование является контролируемым, когда исследуемый препарат сравнивают с группой сравнения (контрольной группой). Группой сравнения может быть: другое активное лечение – имеющее уже известную эффективность и переносимость; другая доза или лекарственная форма того же препарата; плацебо; отсутствие лечения; рутинная терапия (лечение, не оговорённое протоколом исследования) или исторический контроль. Кроме того, при проведении каждого клинического исследования используется контроль исходного состояния.
 Методы клинических испытаний Важно объективно оценивать эффект, поэтому применяют слепой и двойной слепой метод. При этом двойной слепой метод является «золотым стандартом» .
Методы клинических испытаний Важно объективно оценивать эффект, поэтому применяют слепой и двойной слепой метод. При этом двойной слепой метод является «золотым стандартом» .
 Методы клинических испытаний n Рандомизированные контролируемые исследования – в которых распределение участников в группы происходит в случайном порядке, являются чрезвычайно важным инструментом научных исследований. Они способны представить убедительные доказательства эффективности (или неэффективности), безопасности и целесообразности различных вмешательств, а также соотношения польза/вред в сравнении с другими вмешательствами.
Методы клинических испытаний n Рандомизированные контролируемые исследования – в которых распределение участников в группы происходит в случайном порядке, являются чрезвычайно важным инструментом научных исследований. Они способны представить убедительные доказательства эффективности (или неэффективности), безопасности и целесообразности различных вмешательств, а также соотношения польза/вред в сравнении с другими вмешательствами.
 Регулирование клинических испытаний Главным документом, регламентирующим проведение клинических испытаний, является стандарт GCP – надлежащей клинической практики. В РБ – Технический кодекс установившейся практики “Надлежащая клиническая практика” (2009).
Регулирование клинических испытаний Главным документом, регламентирующим проведение клинических испытаний, является стандарт GCP – надлежащей клинической практики. В РБ – Технический кодекс установившейся практики “Надлежащая клиническая практика” (2009).
 Этические проблемы, связанные с проведением клинических испытаний Набор участников: После одобрения программы исследований комитетом по этике проводят подбор добровольцев для участия в испытаниях. При этом существует 2 ключевые этические проблемы: 1. Получение добровольного информированного согласия n «терапевтическое заблуждение» - стойкая уверенность в том, что их участие в исследовании отвечает удовлетворению их индивидуальных потребностей в лечении. n «чрезмерное вознаграждение»
Этические проблемы, связанные с проведением клинических испытаний Набор участников: После одобрения программы исследований комитетом по этике проводят подбор добровольцев для участия в испытаниях. При этом существует 2 ключевые этические проблемы: 1. Получение добровольного информированного согласия n «терапевтическое заблуждение» - стойкая уверенность в том, что их участие в исследовании отвечает удовлетворению их индивидуальных потребностей в лечении. n «чрезмерное вознаграждение»
 Пример 1 n n n Доктора Эбботт, онколога, попросили предложить некоторым из ее пациентов участие в клинических испытаниях нового средства для лечения рака. Мистер Дэй – пациент с терминальной стадией рака подходящего типа для включения его в программу клинических испытаний. Мистер Дэй жаждет участвовать и поэтому вызывается при первой возможности. На просьбу объяснить его рвение во время проведения интервью, он ответил, что Бог послал ему эту возможность, и что это новое средство (о котором он «уже все прочитал в Интернете» ) является чудодейственным и сможет спасти ему жизнь, и что (при условии, что он будет включен в исследования), он ожидает полного выздоровления уже к Рождеству (до которого осталось меньше 6 месяцев). Все специалисты, наблюдающие Мистера Дэя, считают его точку зрения сверхоптимистичной. Более того, его точка зрения не меняется, несмотря на то, что ему было рассказано о ряде важных обстоятельств: нет оснований полагать, что испытываемое экспериментальное средство продлит его жизнь более чем на несколько месяцев (хотя оно может улучшить качество его жизни); ожидаемые улучшения не могут быть предсказаны с уверенностью; его шансы полностью излечиться с помощью этого препарата, как и любого другого, практически равны нулю. Сталкиваясь с такой информацией, Мистер Дэй ограничивается отговорками типа «Вы просторожничаете и перестраховываетесь» или «Ваша вера слаба» . Доктор Эббот считает, что участие в испытаниях пойдет Мистеру Дэю на пользу с психологической точки зрения, наряду с непосредственными клиническими эффектами, благодаря поддержке его надежд и ожиданий, а запрещение участвовать в испытаниях, наоборот, подорвет его психологически. Она также полагает, что его стремление участвовать следует воспринимать очень серьезно, и что игнорирование этого стремления будет противоречить принципу уважительного отношения к его автономии. Но с другой стороны, доктор Эббот не уверена, способен ли Мистер Дэй дать действительное, имеющее силу, согласие в связи с тем, что он не может или не хочет понять истинную сущность исследования и объективно оценить свое состояние.
Пример 1 n n n Доктора Эбботт, онколога, попросили предложить некоторым из ее пациентов участие в клинических испытаниях нового средства для лечения рака. Мистер Дэй – пациент с терминальной стадией рака подходящего типа для включения его в программу клинических испытаний. Мистер Дэй жаждет участвовать и поэтому вызывается при первой возможности. На просьбу объяснить его рвение во время проведения интервью, он ответил, что Бог послал ему эту возможность, и что это новое средство (о котором он «уже все прочитал в Интернете» ) является чудодейственным и сможет спасти ему жизнь, и что (при условии, что он будет включен в исследования), он ожидает полного выздоровления уже к Рождеству (до которого осталось меньше 6 месяцев). Все специалисты, наблюдающие Мистера Дэя, считают его точку зрения сверхоптимистичной. Более того, его точка зрения не меняется, несмотря на то, что ему было рассказано о ряде важных обстоятельств: нет оснований полагать, что испытываемое экспериментальное средство продлит его жизнь более чем на несколько месяцев (хотя оно может улучшить качество его жизни); ожидаемые улучшения не могут быть предсказаны с уверенностью; его шансы полностью излечиться с помощью этого препарата, как и любого другого, практически равны нулю. Сталкиваясь с такой информацией, Мистер Дэй ограничивается отговорками типа «Вы просторожничаете и перестраховываетесь» или «Ваша вера слаба» . Доктор Эббот считает, что участие в испытаниях пойдет Мистеру Дэю на пользу с психологической точки зрения, наряду с непосредственными клиническими эффектами, благодаря поддержке его надежд и ожиданий, а запрещение участвовать в испытаниях, наоборот, подорвет его психологически. Она также полагает, что его стремление участвовать следует воспринимать очень серьезно, и что игнорирование этого стремления будет противоречить принципу уважительного отношения к его автономии. Но с другой стороны, доктор Эббот не уверена, способен ли Мистер Дэй дать действительное, имеющее силу, согласие в связи с тем, что он не может или не хочет понять истинную сущность исследования и объективно оценить свое состояние.
 Пример 1 Вопросы n Находится ли Мистер Дэй в ситуации, позволяющей дать полноценное согласие на участие в испытаниях? n Будет ли лишение Мистера Дэя шанса на участие в испытаниях противоречить принципу уважительного отношения к его автономии? Как соотносятся иррациональные убеждения и независимо принимаемые решения? n Должен ли факт того, что иррациональные убеждения Мистера Дэя по-видимому имеют под собой религиозную природу, быть причиной особого внимания при оценки его уязвимости? n Существуют ли какие-либо альтернативы предложению дать свое согласие и необходимы ли дополнительные меры для защиты интересов Мистера Дэя?
Пример 1 Вопросы n Находится ли Мистер Дэй в ситуации, позволяющей дать полноценное согласие на участие в испытаниях? n Будет ли лишение Мистера Дэя шанса на участие в испытаниях противоречить принципу уважительного отношения к его автономии? Как соотносятся иррациональные убеждения и независимо принимаемые решения? n Должен ли факт того, что иррациональные убеждения Мистера Дэя по-видимому имеют под собой религиозную природу, быть причиной особого внимания при оценки его уязвимости? n Существуют ли какие-либо альтернативы предложению дать свое согласие и необходимы ли дополнительные меры для защиты интересов Мистера Дэя?
 Этические проблемы, связанные с проведением клинических испытаний Набор участников: 2. Критерии отбора: n максимального исключения из исследований уязвимых групп (детей, людей с психическими нарушениями или ограниченными умственными способностями, беременных и кормящих матерей, и людей с ограниченной свободой – военных и заключенных); n минимизации риска и неудобств (предполагает полное предварительное испытаниям обследование пациентов, напрімер нельзя включать пациентов перенесших инфаркт в программу испытаний салицилатов (например аспирина), т. к. для таких пациентов показана идиопатическая гиперчувствительность к препаратам этой группы; или набирать в испытания бэтаблокаторов пациентов с сердечными нарушениями и одновременной астмой) для испытуемого; n выгодности для испытуемого (участие должно быть оплачено, предоставлено соответствующее медицинское обслуживание); n справедливости и равенства при предоставлении доступа к новым средствам терапии. n Исключение эксплуатации.
Этические проблемы, связанные с проведением клинических испытаний Набор участников: 2. Критерии отбора: n максимального исключения из исследований уязвимых групп (детей, людей с психическими нарушениями или ограниченными умственными способностями, беременных и кормящих матерей, и людей с ограниченной свободой – военных и заключенных); n минимизации риска и неудобств (предполагает полное предварительное испытаниям обследование пациентов, напрімер нельзя включать пациентов перенесших инфаркт в программу испытаний салицилатов (например аспирина), т. к. для таких пациентов показана идиопатическая гиперчувствительность к препаратам этой группы; или набирать в испытания бэтаблокаторов пациентов с сердечными нарушениями и одновременной астмой) для испытуемого; n выгодности для испытуемого (участие должно быть оплачено, предоставлено соответствующее медицинское обслуживание); n справедливости и равенства при предоставлении доступа к новым средствам терапии. n Исключение эксплуатации.
 Пример 2 n n Крупная фармацевтическая компания проводит первую фазу клинических испытаний своих продуктов в специализированной клинике в одном крупном городе. Добровольцы обычно находятся в клинике от нескольких дней до нескольких недель. После заполнения анкеты и прохождения первичного медицинского осмотра и базовых обследований, они получают одну или более доз исследуемого препарата, становясь при этом объектом регулярного наблюдения и анализа. От добровольцев требуется сообщать о любых неблагоприятных эффектах, а соответствующий персонал всегда находится на связи в случае необходимости оказания медицинской помощи. Поскольку участники первой фазы клинических испытаний не получают терапевтического эффекта, их участие в испытаниях обычно оплачивается. В материалах, используемых для приглашения новых участников (листовках и постерах, которые предлагается взять с собой добровольцам для последующего распространения), сказано, что «компенсация времени и неудобств» будет оплачена «в соответствии с продолжительностью и видом исследований» . Кроме того, листовки подчеркивают тот факт, что участникам бесплатно предоставляется питание и проживание на протяжении всего периода испытаний, а также то, что им будут предоставлены возможности для отдыха и развлечения. Ранее компания без особых затруднений получала разрешения на проведения клинических испытаний от комитета по этике, и имеет хорошие показатели безопасности. Однако новый член регионального комитета поставил под сомнение уровень выплат, предлагаемых добровольцам, и обнаружил, что они намного ниже, чем обычно предлагается другими фармацевтическими компаниями. При дальнейшем изучении вопроса оказалось, что большая часть добровольцев – это безработные и бездомные (большинство адресов указанных в анкете соответствует местным общежитиям для бездомных или иным местам временного проживания). Есть основания полагать, что значительная часть добровольцев является алкоголиками или наркоманами, хотя во время процедуры регистрации участники должны подтвердить, что не имеют зависимостей, а также не будут употреблять алкоголь или другие препараты (кроме исследуемого), в процессе эксперимента. Также есть сведения, что, несмотря на отсутствие громкой рекламы, информация об исследованиях широко распространена, и часто добровольцы приезжают издалека, чтобы принять в них участие. Многие ранее неоднократно участвовали в клинических испытаниях, проводимых этой, или другими компаниями, и, несмотря на то, что критерии пригодности устанавливают срок не менее трех месяцев между испытаниями, есть определенные свидетельства фальсификации личностей добровольцев с целью преодолеть это ограничение. Компания не видит проблемы в низком уровне оплаты или подборе субъектов для испытаний из неблагополучных социально-экономических групп. Утверждается, что легкость, с которой находятся добровольцы, показывает, что выгоды для них существенны, и что более высокие выплаты могут стать чрезмерным стимулом. Отмечается также, что количество участников прекращающих участие в испытаниях является очень низким, как и число получаемых жалоб.
Пример 2 n n Крупная фармацевтическая компания проводит первую фазу клинических испытаний своих продуктов в специализированной клинике в одном крупном городе. Добровольцы обычно находятся в клинике от нескольких дней до нескольких недель. После заполнения анкеты и прохождения первичного медицинского осмотра и базовых обследований, они получают одну или более доз исследуемого препарата, становясь при этом объектом регулярного наблюдения и анализа. От добровольцев требуется сообщать о любых неблагоприятных эффектах, а соответствующий персонал всегда находится на связи в случае необходимости оказания медицинской помощи. Поскольку участники первой фазы клинических испытаний не получают терапевтического эффекта, их участие в испытаниях обычно оплачивается. В материалах, используемых для приглашения новых участников (листовках и постерах, которые предлагается взять с собой добровольцам для последующего распространения), сказано, что «компенсация времени и неудобств» будет оплачена «в соответствии с продолжительностью и видом исследований» . Кроме того, листовки подчеркивают тот факт, что участникам бесплатно предоставляется питание и проживание на протяжении всего периода испытаний, а также то, что им будут предоставлены возможности для отдыха и развлечения. Ранее компания без особых затруднений получала разрешения на проведения клинических испытаний от комитета по этике, и имеет хорошие показатели безопасности. Однако новый член регионального комитета поставил под сомнение уровень выплат, предлагаемых добровольцам, и обнаружил, что они намного ниже, чем обычно предлагается другими фармацевтическими компаниями. При дальнейшем изучении вопроса оказалось, что большая часть добровольцев – это безработные и бездомные (большинство адресов указанных в анкете соответствует местным общежитиям для бездомных или иным местам временного проживания). Есть основания полагать, что значительная часть добровольцев является алкоголиками или наркоманами, хотя во время процедуры регистрации участники должны подтвердить, что не имеют зависимостей, а также не будут употреблять алкоголь или другие препараты (кроме исследуемого), в процессе эксперимента. Также есть сведения, что, несмотря на отсутствие громкой рекламы, информация об исследованиях широко распространена, и часто добровольцы приезжают издалека, чтобы принять в них участие. Многие ранее неоднократно участвовали в клинических испытаниях, проводимых этой, или другими компаниями, и, несмотря на то, что критерии пригодности устанавливают срок не менее трех месяцев между испытаниями, есть определенные свидетельства фальсификации личностей добровольцев с целью преодолеть это ограничение. Компания не видит проблемы в низком уровне оплаты или подборе субъектов для испытаний из неблагополучных социально-экономических групп. Утверждается, что легкость, с которой находятся добровольцы, показывает, что выгоды для них существенны, и что более высокие выплаты могут стать чрезмерным стимулом. Отмечается также, что количество участников прекращающих участие в испытаниях является очень низким, как и число получаемых жалоб.
 Пример 2 Вопросы n Какие преимущества получает фармацевтическая компания в результате найма добровольцев из неблагополучных слоев общества, и в чем преимущества для добровольцев от участия в испытаниях? n В чем состоят недостатки и риски такого метода найма для компании и для добровольцев? n Есть ли основания считать способ найма, практикуемый этой компанией, эксплуататорским? Если да, то каковы эти основания, и согласны ли вы, что описанный способ найма действительно является эксплуататорским? n Какие изменения, если таковые будут, нужно внести компании для того, чтобы убедить вас, что практика набора добровольцев морально приемлема?
Пример 2 Вопросы n Какие преимущества получает фармацевтическая компания в результате найма добровольцев из неблагополучных слоев общества, и в чем преимущества для добровольцев от участия в испытаниях? n В чем состоят недостатки и риски такого метода найма для компании и для добровольцев? n Есть ли основания считать способ найма, практикуемый этой компанией, эксплуататорским? Если да, то каковы эти основания, и согласны ли вы, что описанный способ найма действительно является эксплуататорским? n Какие изменения, если таковые будут, нужно внести компании для того, чтобы убедить вас, что практика набора добровольцев морально приемлема?
 Этические проблемы, связанные с проведением клинических испытаний Фаза 1 n Как сбалансировать соотношения риска и пользы? n Как мотивировать здоровых добровольцев к участию в испытаниях?
Этические проблемы, связанные с проведением клинических испытаний Фаза 1 n Как сбалансировать соотношения риска и пользы? n Как мотивировать здоровых добровольцев к участию в испытаниях?
 Этические проблемы, связанные с проведением клинических испытаний Фаза 2 n Случайное распределение пациентов в контрольную и экспериментальную группы. Т. е. часть пациентов остается без необходимого им лечения. Таким образом, возникает конфликт между интересами пациента и необходимостью получения нового медицинского знания.
Этические проблемы, связанные с проведением клинических испытаний Фаза 2 n Случайное распределение пациентов в контрольную и экспериментальную группы. Т. е. часть пациентов остается без необходимого им лечения. Таким образом, возникает конфликт между интересами пациента и необходимостью получения нового медицинского знания.
 Этические проблемы, связанные с проведением клинических испытаний Фаза 3 n Аналогично фазе 2. Однако соотношение риска и пользы более благоприятно, ввиду существования предварительных результатов, полученных во время предыдущей фазы.
Этические проблемы, связанные с проведением клинических испытаний Фаза 3 n Аналогично фазе 2. Однако соотношение риска и пользы более благоприятно, ввиду существования предварительных результатов, полученных во время предыдущей фазы.
 Этические проблемы, связанные с проведением клинических испытаний Фаза 4 n Несмотря на то, что методы этой фазы уже совершенно другие, к ней применяются теже этические стандарты.
Этические проблемы, связанные с проведением клинических испытаний Фаза 4 n Несмотря на то, что методы этой фазы уже совершенно другие, к ней применяются теже этические стандарты.
 Проблема исполнения профессионального долга врача Любое клиническое испытание включает в себя элементы клинической медицины и научного исследования. Это и стало основой для возникновения 2 различных этических позиций – «позиции сходства» и «позиции различий» .
Проблема исполнения профессионального долга врача Любое клиническое испытание включает в себя элементы клинической медицины и научного исследования. Это и стало основой для возникновения 2 различных этических позиций – «позиции сходства» и «позиции различий» .
 Проблема исполнения профессионального долга врача Аргументы в пользу сходства клинических испытаний с клинической медициной: n включение в испытания людей с заболеваниями, n проведение испытаний медицинскими работниками n и применение аналогичных методов диагностики и лечения.
Проблема исполнения профессионального долга врача Аргументы в пользу сходства клинических испытаний с клинической медициной: n включение в испытания людей с заболеваниями, n проведение испытаний медицинскими работниками n и применение аналогичных методов диагностики и лечения.
 Проблема исполнения профессионального долга врача Позиция сходства требует: Благополучие пациента является первостепенной обязанностью врача-исследователя. И врач имеет перед участниками клинического испытания терапевтические обязательства. В таком случае врач, выбирая схему лечения, не может назначать средства «второго сорта» или оставить страдающего человека без лечения. Такая система взаимоотношений врача и пациента предполагает необходимость соблюдения требования клинического равновесия.
Проблема исполнения профессионального долга врача Позиция сходства требует: Благополучие пациента является первостепенной обязанностью врача-исследователя. И врач имеет перед участниками клинического испытания терапевтические обязательства. В таком случае врач, выбирая схему лечения, не может назначать средства «второго сорта» или оставить страдающего человека без лечения. Такая система взаимоотношений врача и пациента предполагает необходимость соблюдения требования клинического равновесия.
 Проблема исполнения профессионального долга врача n Концепция клинического равновесия - экспериментальное средство и наилучшее из уже существующих доказанных средств лечения должны быть предположительно одинаково эффективны, либо должны существовать профессиональные сомнения, касающиеся относительных преимуществ экспериментального и лучшего из существующих способов лечения.
Проблема исполнения профессионального долга врача n Концепция клинического равновесия - экспериментальное средство и наилучшее из уже существующих доказанных средств лечения должны быть предположительно одинаково эффективны, либо должны существовать профессиональные сомнения, касающиеся относительных преимуществ экспериментального и лучшего из существующих способов лечения.
 Проблема исполнения профессионального долга врача Различия между клиническими испытаниями и клинической медициной: n нацеленность не на терапию отдельного человека, а группы пациентов, n существование принципиальной вероятности эксплуатации объектов исследования, n методы исследования, обеспечивающие его научную достоверность, могут представлять риск для участников испытаний.
Проблема исполнения профессионального долга врача Различия между клиническими испытаниями и клинической медициной: n нацеленность не на терапию отдельного человека, а группы пациентов, n существование принципиальной вероятности эксплуатации объектов исследования, n методы исследования, обеспечивающие его научную достоверность, могут представлять риск для участников испытаний.
 Проблема исполнения профессионального долга врача Позиция различий предполагает: У врача-исследователя нет терапевтических обязательств. А его главной задачей становится соответствие требованиям научной значимости и достоверности при получении новых научных данных. Такие взаимоотношения уже не могут регулироваться с позиций клинического равновесия и требуют использования альтернативных систем этических требований.
Проблема исполнения профессионального долга врача Позиция различий предполагает: У врача-исследователя нет терапевтических обязательств. А его главной задачей становится соответствие требованиям научной значимости и достоверности при получении новых научных данных. Такие взаимоотношения уже не могут регулироваться с позиций клинического равновесия и требуют использования альтернативных систем этических требований.


