Исследование белков и пептидов методами масс-спектрометрии.pptx
- Количество слайдов: 49

Исследование белков и пептидов методами массспектрометрии MALDI Д. А. Фармаковский, Shimadzu Europa Gmb. H

Масс-спектрометрия MALDI: история Matrix Assisted Laser Desorption/Ionization Time-Of-Flight Mass Spectrometry - Лазерная десорбция/ионизация при содействии матрицы + времяпролетная масс-спектрометрия разработано в 1980 -х Karas & Hillenkamp и К. Tanaka с соавторами Нобелевская премия по химии K. Tanaka, 2002
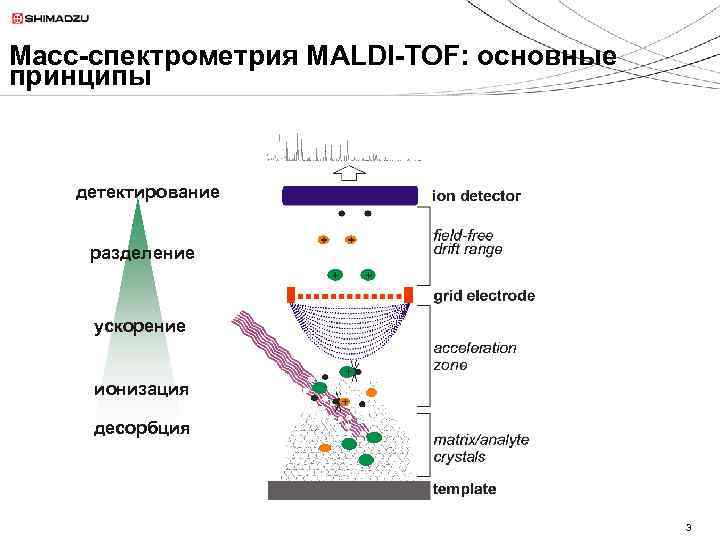
Масс-спектрометрия MALDI-TOF: основные принципы детектирование разделение ускорение ионизация десорбция 3
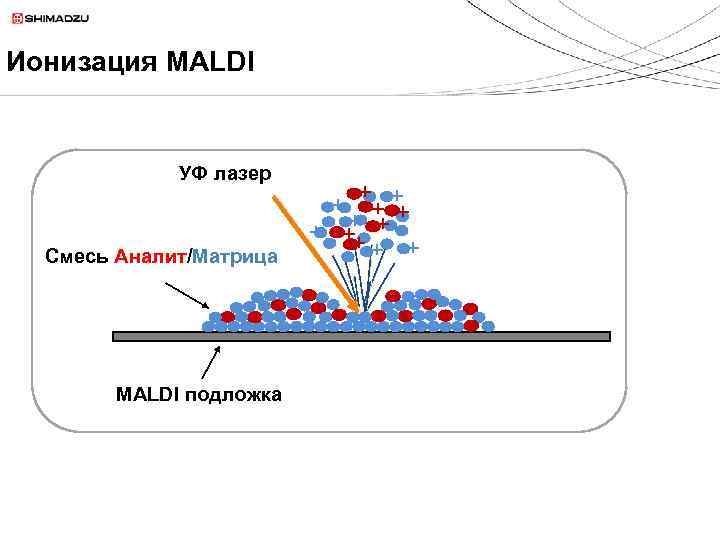
Ионизация MALDI УФ лазер Смесь Аналит/Матрица MALDI подложка + + ++ + +
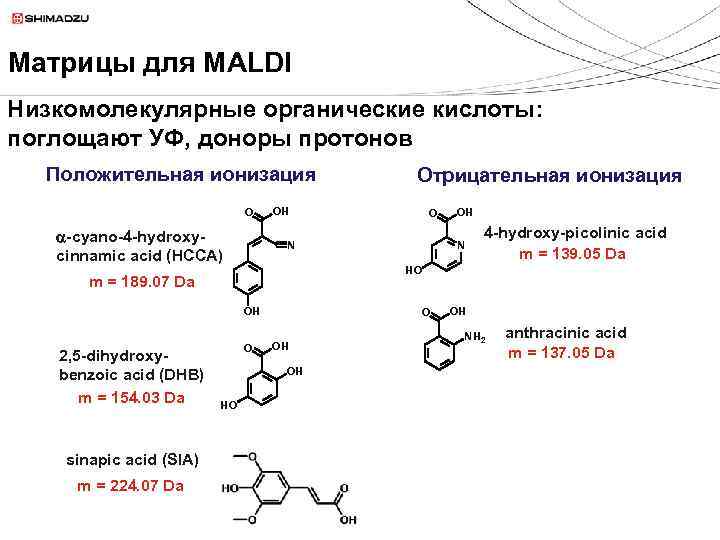
Матрицы для MALDI Низкомолекулярные органические кислоты: поглощают УФ, доноры протонов Положительная ионизация O a-cyano-4 -hydroxy- cinnamic acid (HCCA) OH sinapic acid (SIA) m = 224. 07 Da OH N 4 -hydroxy-picolinic acid m = 139. 05 Da HO OH OH HO O N m = 189. 07 Da 2, 5 -dihydroxybenzoic acid (DHB) m = 154. 03 Da Отрицательная ионизация OH NH 2 anthracinic acid m = 137. 05 Da
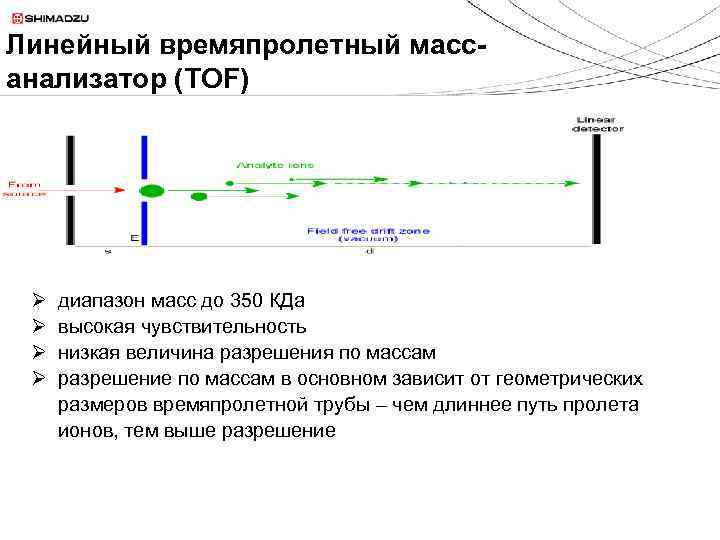
Линейный времяпролетный массанализатор (TOF) Ø Ø диапазон масс до 350 КДa высокая чувствительность низкая величина разрешения по массам разрешение по массам в основном зависит от геометрических размеров времяпролетной трубы – чем длиннее путь пролета ионов, тем выше разрешение
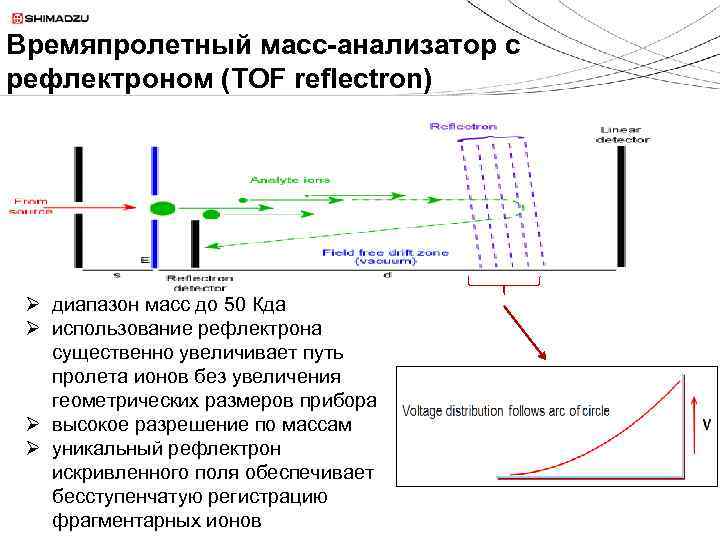
Времяпролетный масс-анализатор с рефлектроном (TOF reflectron) Ø диапазон масс до 50 Кдa Ø использование рефлектрона существенно увеличивает путь пролета ионов без увеличения геометрических размеров прибора Ø высокое разрешение по массам Ø уникальный рефлектрон искривленного поля обеспечивает бесступенчатую регистрацию фрагментарных ионов
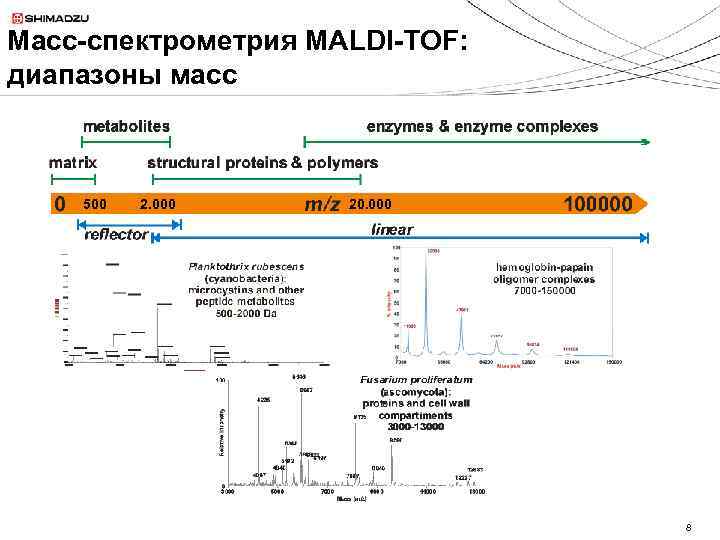
Масс-спектрометрия MALDI-TOF: диапазоны масс 500 2. 000 20. 000 8

Масс-спектрометрия MALDI-TOF: преимущества метода Ø Широчайший диапазон масс анализируемых соединений: от сотен Да до 500 КДа Ø Возможность анализа высокомолекулярных соединений без разрушения молекулы. Ø Высочайшая чувствительность: от 10 -12 до 10 -21 моль исследуемого вещества Ø Высокая толерантность к солям Ø В ходе ионизации образуются в основном однозарядные ионы, что значительно облегчает интерпретацию массспектров Ø Возможность работы с многокомпонентными смесями Ø Возможность получения информации о структуре анализируемых соединений при использовании MС/MСанализа
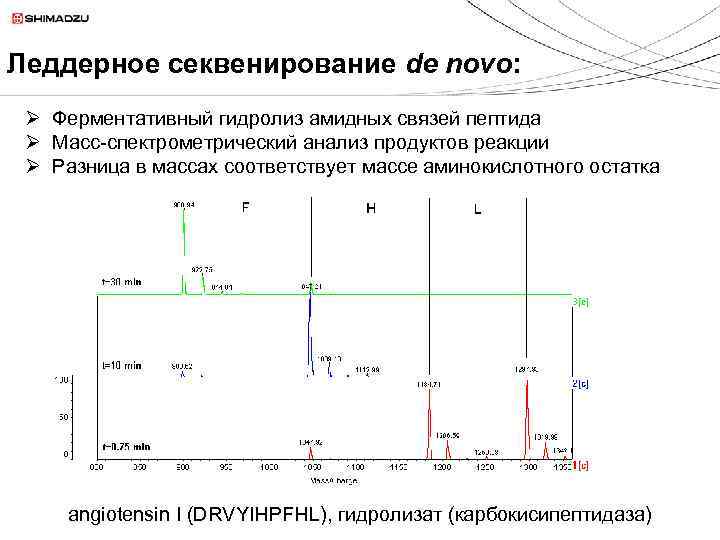
Леддерное секвенирование de novo: Ø Ферментативный гидролиз амидных связей пептида Ø Масс-спектрометрический анализ продуктов реакции Ø Разница в массах соответствует массе аминокислотного остатка angiotensin I (DRVYIHPFHL), гидролизат (карбокисипептидаза)
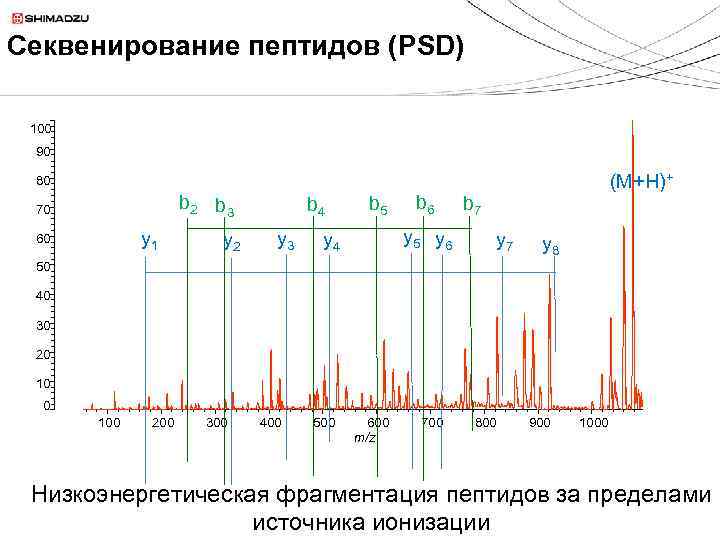
Секвенирование пептидов (PSD) 100 90 (M+H)+ 80 b 2 b 3 70 y 1 60 y 2 b 4 y 3 b 5 b 6 y 5 y 6 y 4 b 7 y 8 50 40 30 20 100 200 300 400 500 600 m/z 700 800 900 1000 Низкоэнергетическая фрагментация пептидов за пределами источника ионизации
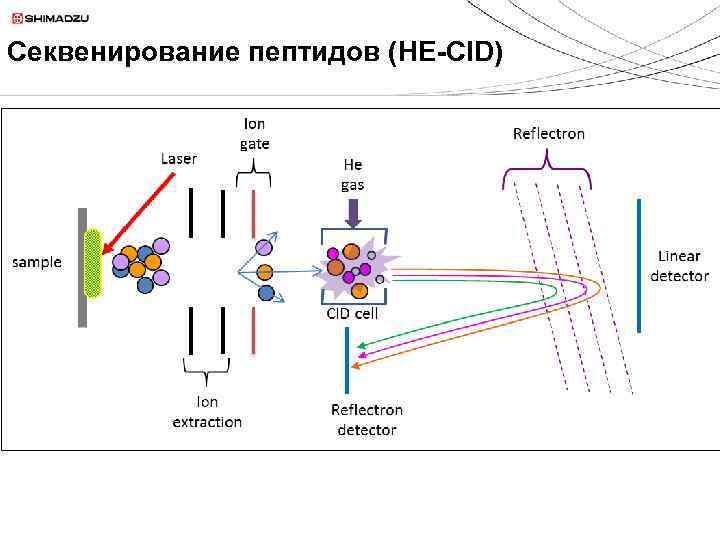
Секвенирование пептидов (HE-CID)
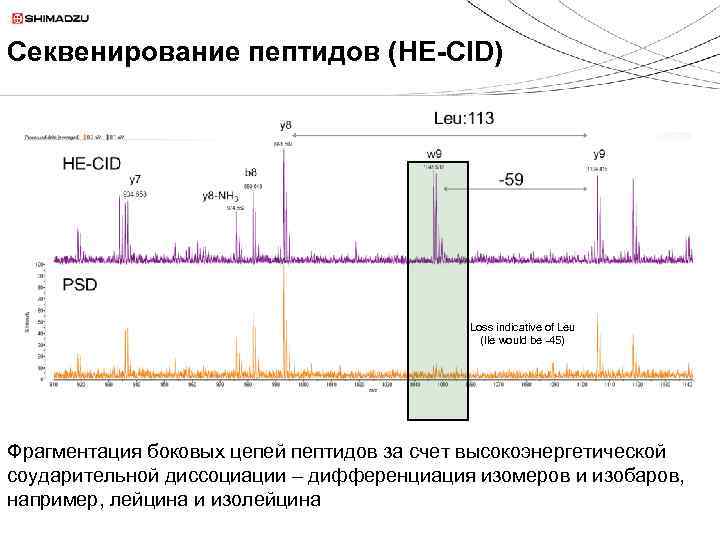
Секвенирование пептидов (HE-CID) Loss indicative of Leu (Ile would be -45) Фрагментация боковых цепей пептидов за счет высокоэнергетической соударительной диссоциации – дифференциация изомеров и изобаров, например, лейцина и изолейцина

Дифференциация лейцина и изолейцина Фрагментация боковых цепей пептидов за счет высокоэнергетической соударительной диссоциации (HE CID) – дифференциация изомеров и изобаров, например, лейцина и изолейцина
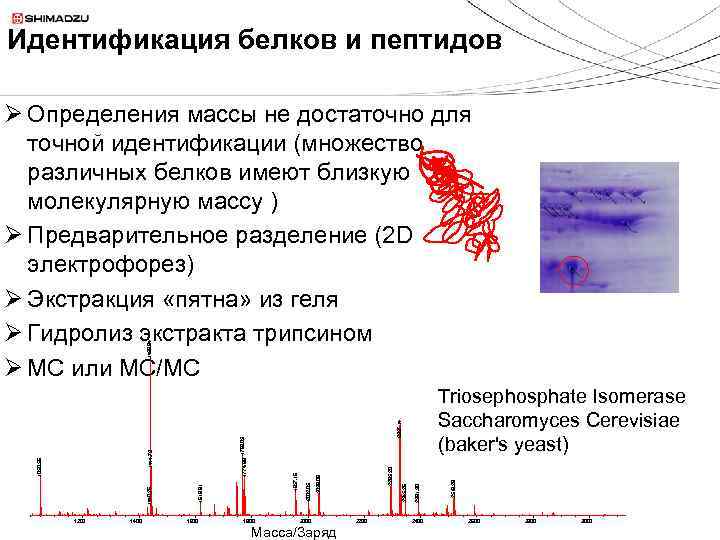
Идентификация белков и пептидов 1439. 84 Ø Определения массы не достаточно для точной идентификации (множество различных белков имеют близкую молекулярную массу ) Ø Предварительное разделение (2 D электрофорез) Ø Экстракция «пятна» из геля Ø Гидролиз экстракта трипсином Ø МС или МС/МС 1400 1600 Масса/Заряд 2400 2519. 28 2391. 30 2295. 20 2200 2345. 26 2327. 14 2000 2039. 08 1957. 16 1800 2002. 05 1774. 88 1768. 03 1618. 91 1444. 72 1440. 26 1050. 56 1200 Triosephosphate Isomerase Saccharomyces Cerevisiae (baker's yeast) 2600 2800 3000
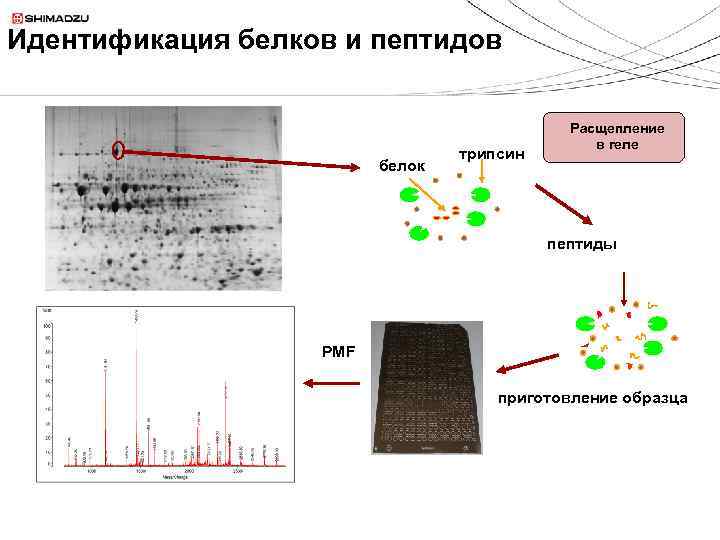
Идентификация белков и пептидов белок трипсин Расщепление в геле пептиды PMF приготовление образца
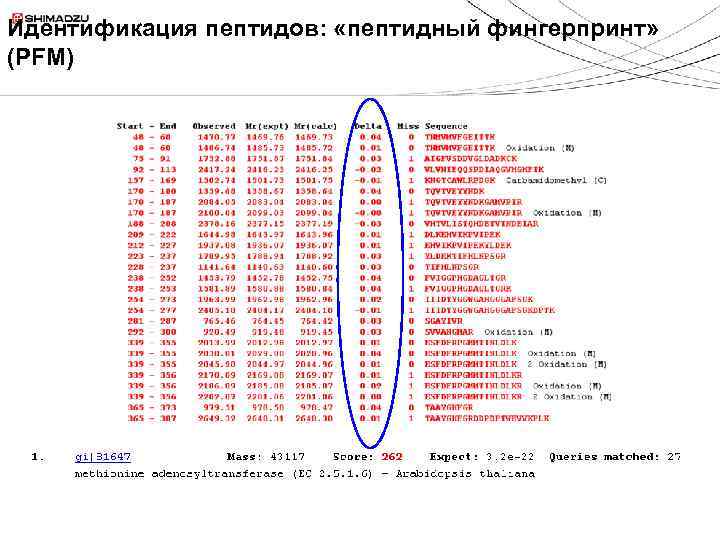
Идентификация пептидов: «пептидный фингерпринт» (PFM)

«Perfinity i. DP» – автоматизированная подготовка белковых образцов для анализа Ø Ø Ø Обычно подготовка проб для протеомного анализа требует 18 -часового гидролиза трипсином Perfinity i. DP cнижает время пробоподготоки до 30 мин! Система обеспечивает автоматическую замену буфера, ферментное разложение, обессоливание и ОФ разделение Уменьшение вспомогательного оборудования, минимизация ошибки, увеличение продуктивности лаборатории Применение: очистка белков, разработка лекарственных препаратов, исследование биомаркеров Колонка с иммобилизованным трипсином
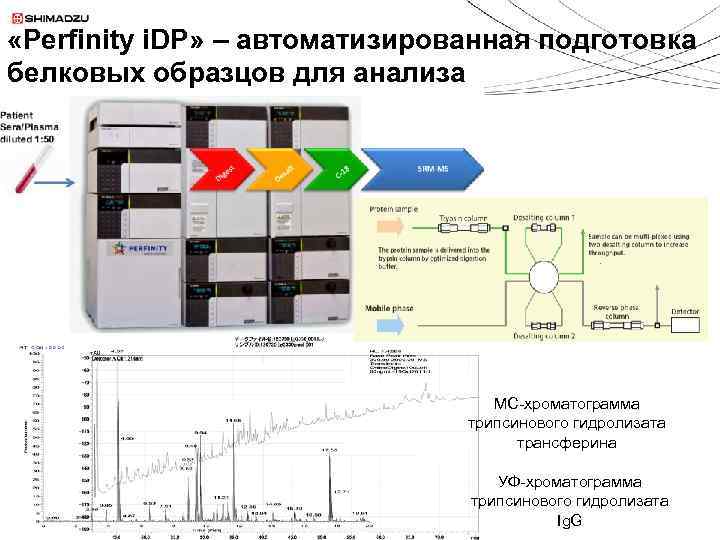
«Perfinity i. DP» – автоматизированная подготовка белковых образцов для анализа МС-хроматограмма трипсинового гидролизата трансферина УФ-хроматограмма трипсинового гидролизата Ig. G
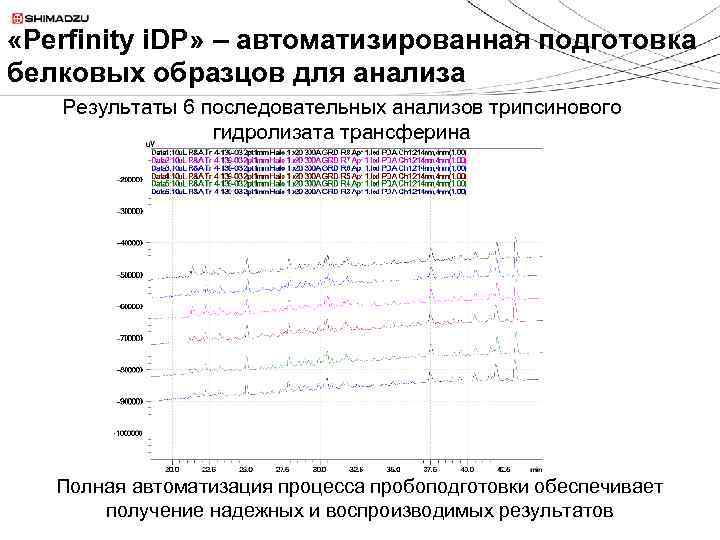
«Perfinity i. DP» – автоматизированная подготовка белковых образцов для анализа Результаты 6 последовательных анализов трипсинового гидролизата трансферина Полная автоматизация процесса пробоподготовки обеспечивает получение надежных и воспроизводимых результатов
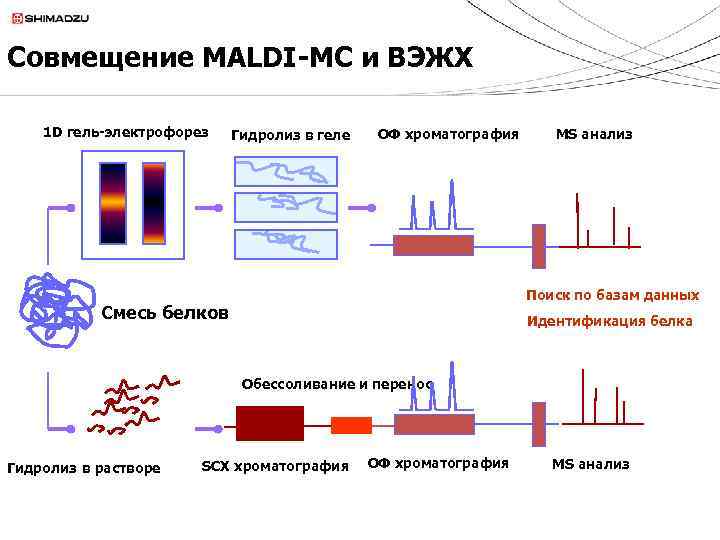
Совмещение MALDI-МС и ВЭЖХ 1 D гель-электрофорез Гидролиз в геле ОФ хроматография MS анализ Поиск по базам данных Смесь белков Идентификация белка Обессоливание и перенос Гидролиз в растворе SCX хроматография ОФ хроматография MS анализ

Accu. Spot – нано-споттер для MALDI-MС
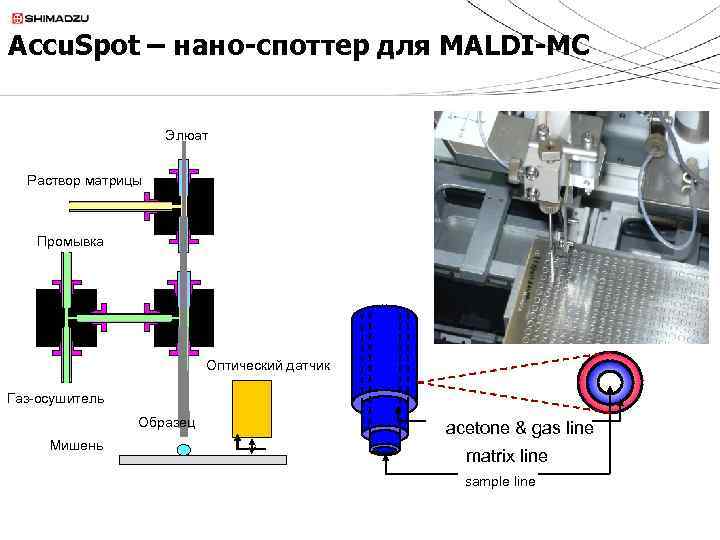
Accu. Spot – нано-споттер для MALDI-MС Элюат Раствор матрицы Промывка Оптический датчик Газ-осушитель Образец Мишень acetone & gas line matrix line sample line
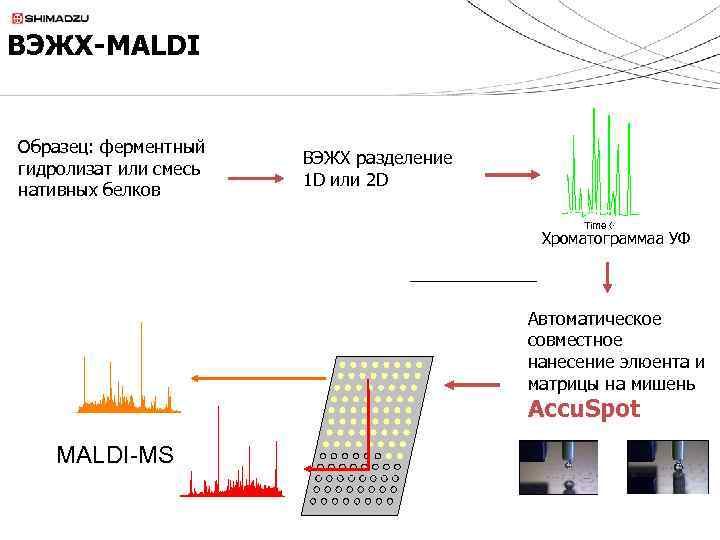
ВЭЖХ-MALDI Образец: ферментный гидролизат или смесь нативных белков ВЭЖХ разделение 1 D или 2 D Time Хроматограммаа УФ Автоматическое совместное нанесение элюента и матрицы на мишень Accu. Spot MALDI-MS
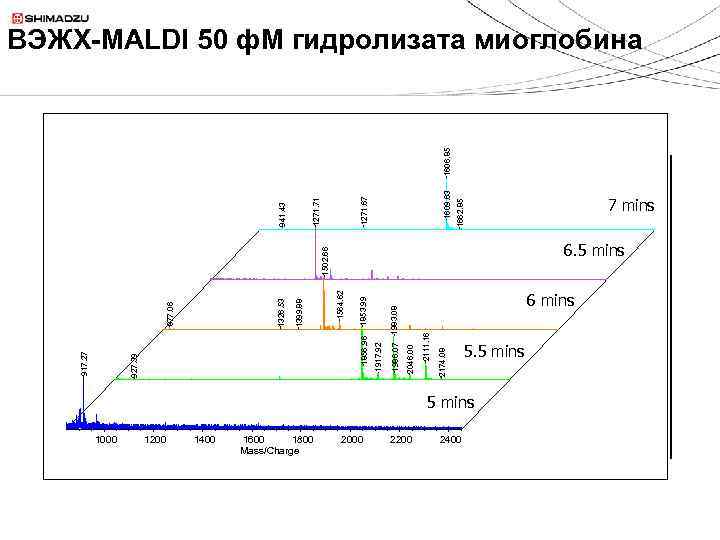
1000 1200 1400 1600 1800 Mass/Charge 2000 2200 2174. 08 1853. 99 1564. 62 1399. 88 1326. 53 877. 06 1983. 08 2111. 16 2046. 00 1986. 07 1917. 92 1856. 96 927. 39 917. 27 1502. 66 1662. 85 1609. 63 1271. 67 1271. 71 941. 43 1606. 85 ВЭЖХ-MALDI 50 ф. М гидролизата миоглобина 2400 5. 5 mins 7 mins 6. 5 mins 6 mins

Новое интесивно развивающееся направление: идентификация микроорганизмов методом массспектрометрии MALDI Ø Идентификация микроорганизмов: ü Быстрый и надежный скрининг широкого спектра микроорганизмов ü Идентификация грам-положительных и грам-отрицательных бактерий, водорослей, грибов и дрожжей ü Надежная идентификация возможна благодаря тому, что MALDI является таксономически-специфичным ü Для идентификации используются масс-спектры из базы данных SARAMIS ü SARAMIS: Spectral ARchive And Microbial Identification System Неизвестный микроорганизм Идентификация
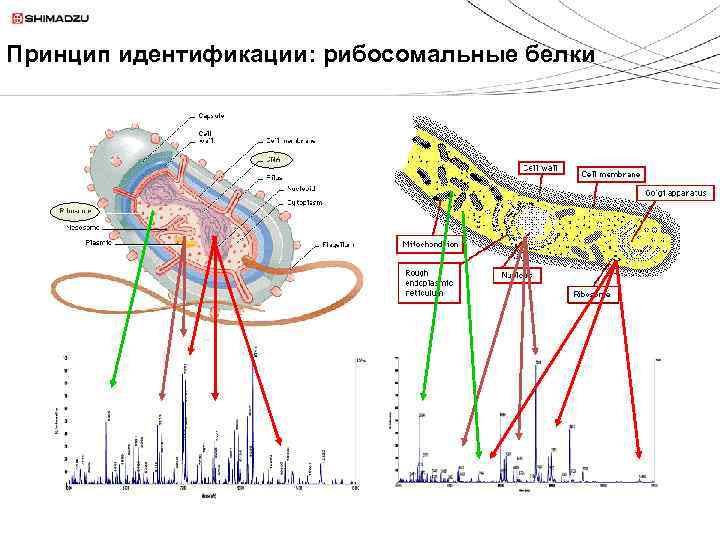
Принцип идентификации: рибосомальные белки
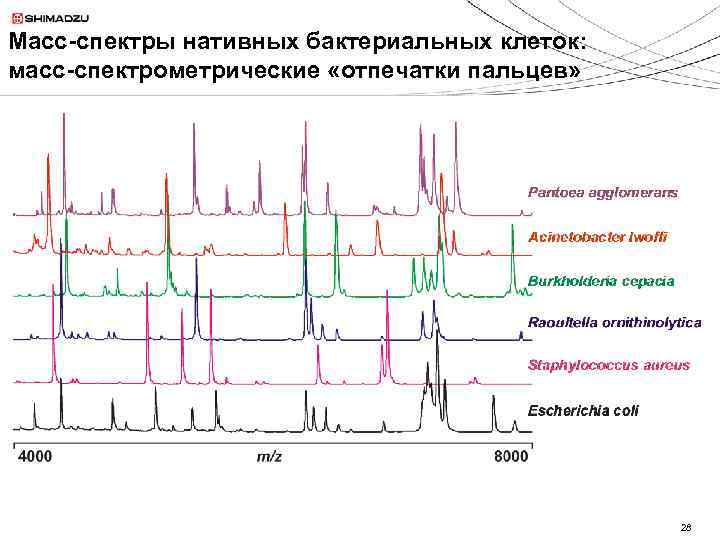
Масс-спектры нативных бактериальных клеток: масс-спектрометрические «отпечатки пальцев» 28
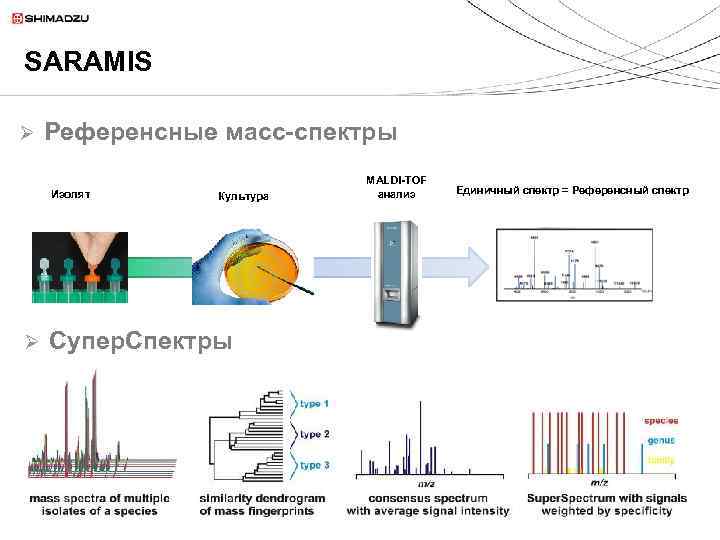
SARAMIS Ø Референсные масс-спектры Изолят Ø Культура Супер. Спектры MALDI-TOF анализ Единичный спектр = Референсный спектр
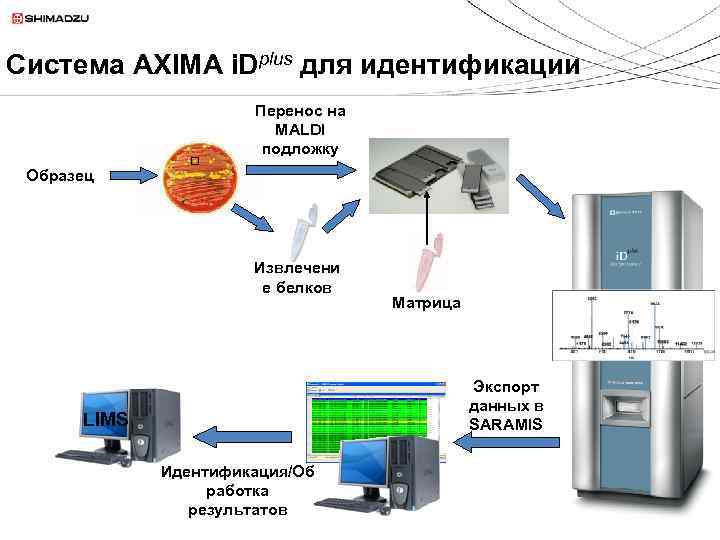
Система AXIMA i. Dplus для идентификации Перенос на MALDI подложку Образец Извлечени е белков Матрица Экспорт данных в SARAMIS LIMS Идентификация/Об работка результатов
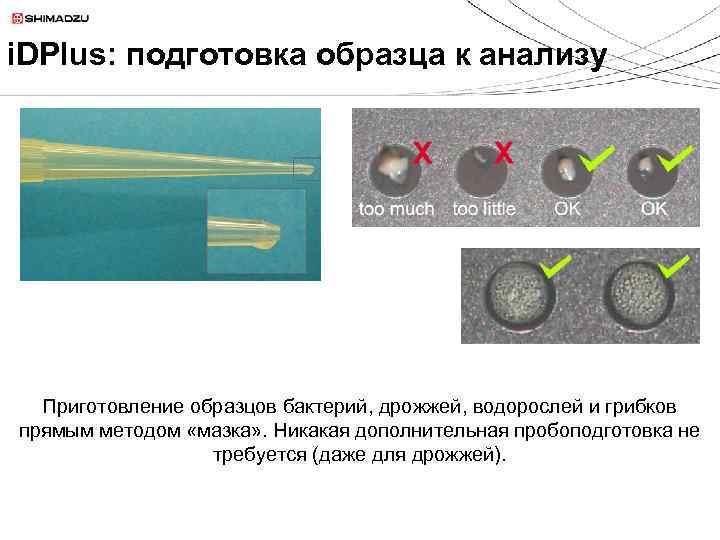
i. DPlus: подготовка образца к анализу Приготовление образцов бактерий, дрожжей, водорослей и грибков прямым методом «мазка» . Никакая дополнительная пробоподготовка не требуется (даже для дрожжей).
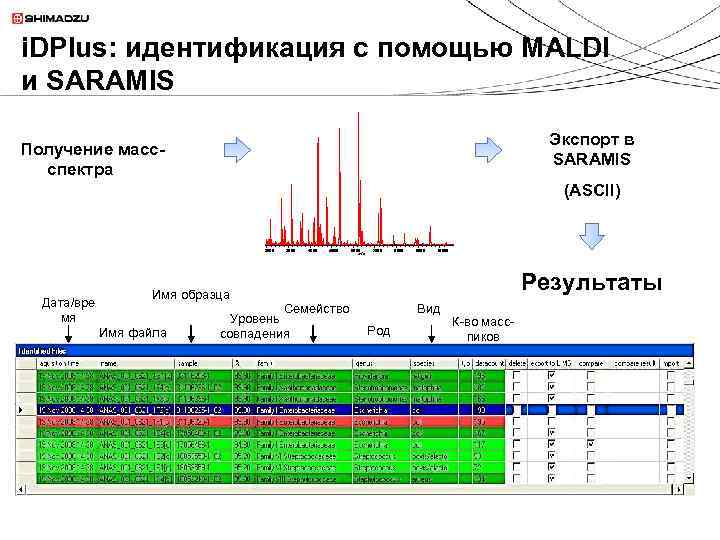
i. DPlus: идентификация с помощью MALDI и SARAMIS Экспорт в SARAMIS Получение массспектра (ASCII) 2000 Дата/вре мя 3000 4000 5000 6000 m/z 7000 Имя файла 9000 10000 Результаты Имя образца Семейство Уровень совпадения 8000 Вид Род К-во масспиков
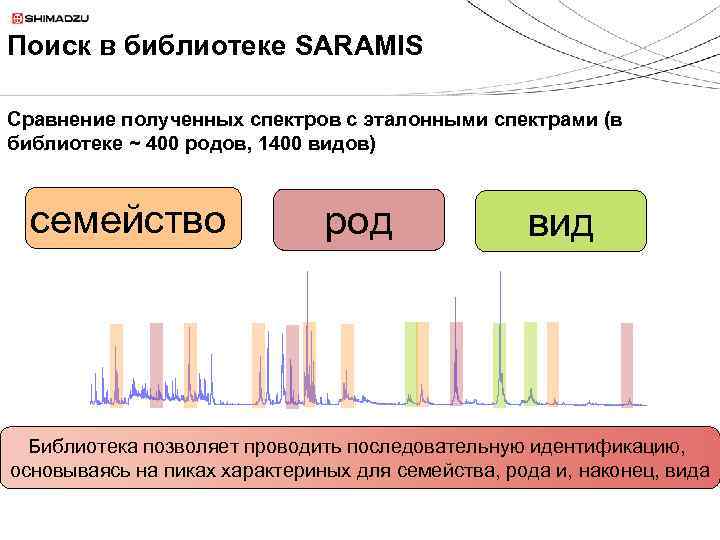
Поиск в библиотеке SARAMIS Сравнение полученных спектров с эталонными спектрами (в библиотеке ~ 400 родов, 1400 видов) семейство род вид Библиотека позволяет проводить последовательную идентификацию, основываясь на пиках характериных для семейства, рода и, наконец, вида
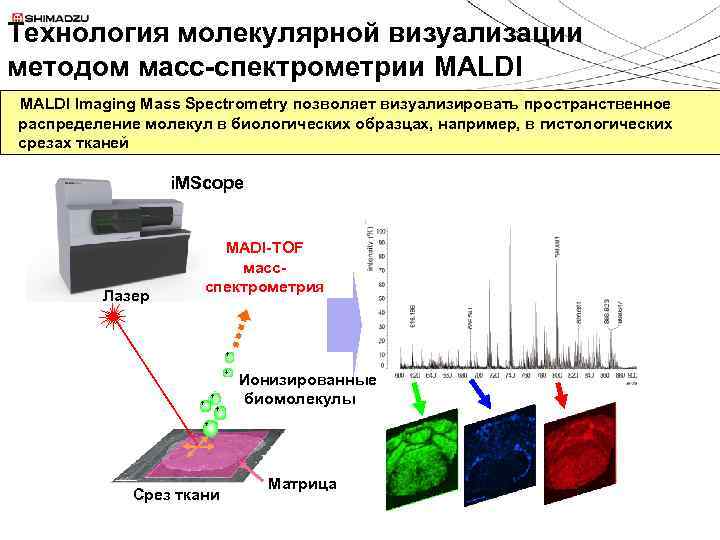
Технология молекулярной визуализации методом масс-спектрометрии MALDI Imaging Mass Spectrometry позволяет визуализировать пространственное распределение молекул в биологических образцах, например, в гистологических срезах тканей i. MScope Лазер MADI-TOF массспектрометрия + + + Ионизированные биомолекулы + Срез ткани Матрица

Визуализирующая масс-спектрометрия – мощная технология для молекулярной визуализации Ø Визуализация распределения биомолекул в различных гистологических образцах ü Свежевыделенные, замороженные, зафиксированные в формалине и залитые парафином (FFPE), клеточные культуры Ø Идентификация широкого спектра высоко- и низкомолекулярных соединений ü Липиды (фосфолипиды: PC, PE, SM, SE и др. ), белки/пептиды, низкомолекулярные метаболиты (АТФ/АДФ/АМФ и др), лекарства и их метаболиты и т. д. ü Высокоточная идентификация за счет МС/МС анализа Ø Одновременная визуализация многих молекул ü Нет необходимости в предварительном выборе соединения ü Непрерывный анализ: скрининг и идентификация Ø Детектирование без меток или мишеней ü Не нужны изотопные или флуоресцентные метки (соответственно сигнал не «размывается» в пространстве) ü Нет необходимости использовать антитела

Приборы для молекулярной визуализации Инструмент i. MScope TRIO MALDI-7090 Назначение Молекулярная визуализация Мол. визуализация и другие применения Оптический микроскоп Встроен Нет MALDI при атм. давлении MALDI в вакууме 5 мкм 10 мкм Частота лазера ~ 1000 Гц ~ 2000 Гц Диапазон масс, m/z 50 ~ 3, 000 ~ 500, 000 ≦ 10 ≦ 2 Ионизация Разрешение простр. MСn
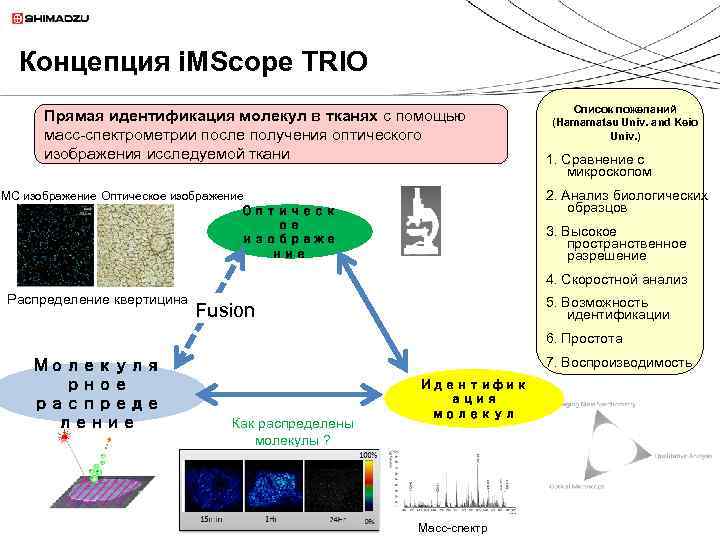
Концепция i. MScope TRIO Прямая идентификация молекул в тканях с помощью масс-спектрометрии после получения оптического изображения исследуемой ткани Список пожеланий (Hamamatsu Univ. and Keio Univ. ) 1. Сравнение с микроскопом 2. Анализ биологических образцов MС изображение Оптическое изображение Оптическ ое изображе ние 3. Высокое пространственное разрешение 4. Скоростной анализ Распределение квертицина 5. Возможность идентификации Fusion 6. Простота Молекуля рное распреде ление 7. Воспроизводимость Как распределены молекулы ? Идентифик ация молекул Масс-спектр
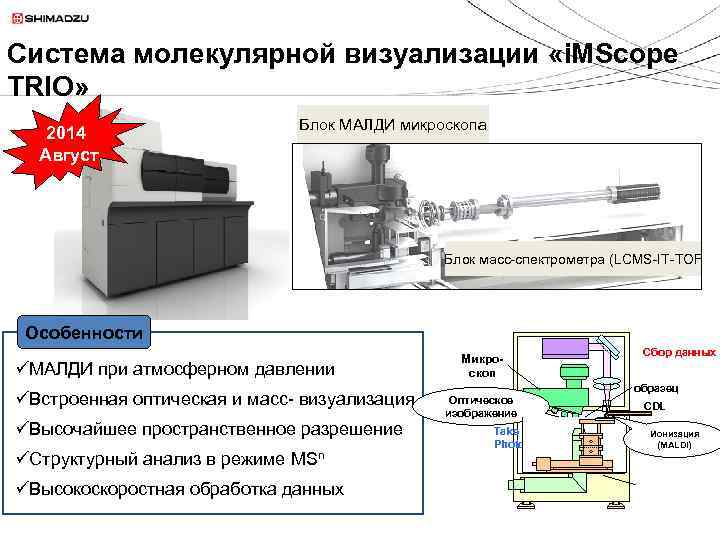
Система молекулярной визуализации «i. MScope TRIO» 2014 Август Блок МАЛДИ микроскопа Блок масс-спектрометра (LCMS-IT-TOF Особенности üМАЛДИ при атмосферном давлении üВстроенная оптическая и масс- визуализация üВысочайшее пространственное разрешение üСтруктурный анализ в режиме MSn üВысокоскоростная обработка данных Микроскоп Оптическое изображение Take Photo Сбор данных образец CDL Ионизация (MALDI)
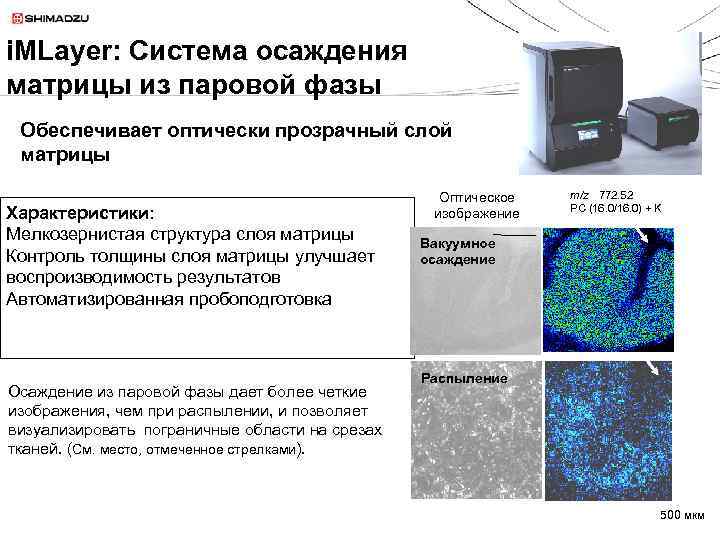
i. MLayer: Система осаждения матрицы из паровой фазы Обеспечивает оптически прозрачный слой матрицы Характеристики: Мелкозернистая структура слоя матрицы Контроль толщины слоя матрицы улучшает воспроизводимость результатов Автоматизированная пробоподготовка Осаждение из паровой фазы дает более четкие изображения, чем при распылении, и позволяет визуализировать пограничные области на срезах тканей. (См. место, отмеченное стрелками). Оптическое изображение m/z 772. 52 PC (16. 0/16. 0) + K Вакуумное осаждение Распыление 500 мкм
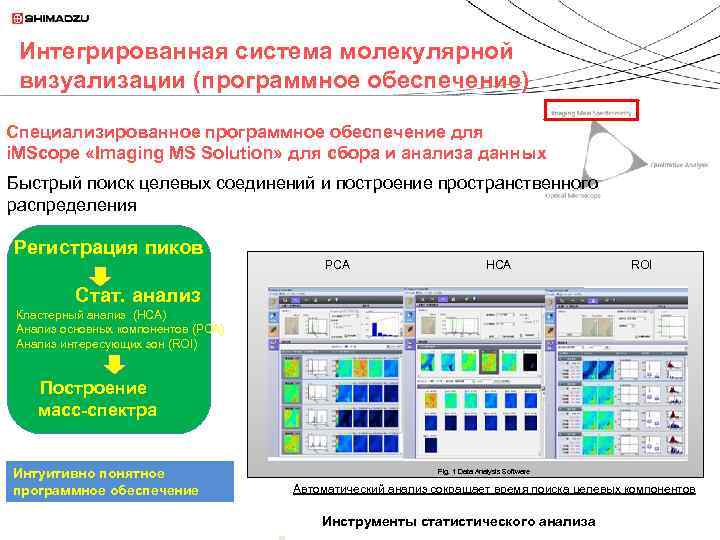
Интегрированная система молекулярной визуализации (программное обеспечение) Специализированное программное обеспечение для i. MScope «Imaging MS Solution» для сбора и анализа данных Быстрый поиск целевых соединений и построение пространственного распределения Регистрация пиков PCA HCA ROI Стат. анализ Кластерный анализ (HCA) Анализ основных компонентов (PCA) Анализ интересующих зон (ROI) Построение масс-спектра Интуитивно понятное программное обеспечение Fig. 1 Data Analysis Software Автоматический анализ сокращает время поиска целевых компонентов Инструменты статистического анализа
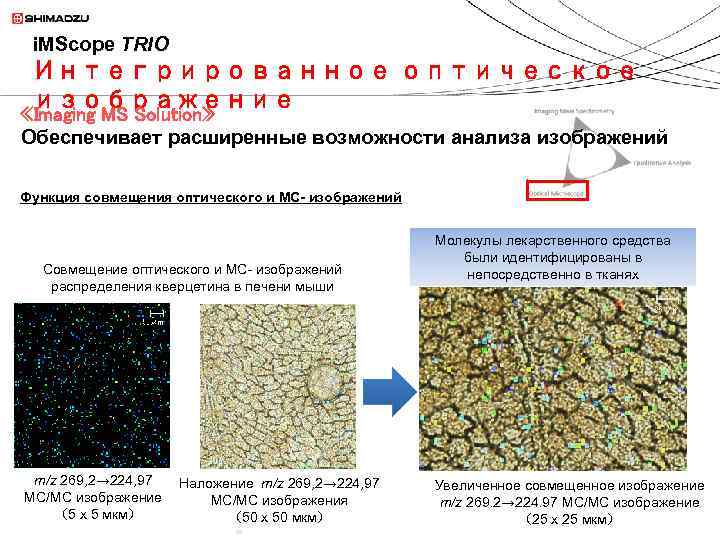
i. MScope TRIO Интегрированное оптическое изображение «Imaging MS Solution» Обеспечивает расширенные возможности анализа изображений Функция совмещения оптического и МС- изображений Совмещение оптического и МС- изображений распределения кверцетина в печени мыши m/z 269, 2→ 224, 97 MС/MС изображение (5 х 5 мкм) Наложение m/z 269, 2→ 224, 97 MС/MС изображения (50 х 50 мкм) Молекулы лекарственного средства были идентифицированы в непосредственно в тканях Увеличенное совмещенное изображение m/z 269. 2→ 224. 97 MС/MС изображение 41 (25 х 25 мкм)

i. MScope TRIO Возможности визуализации с использованием флуоресцентной микроскопии МС визуализация рака толстой кишки человека, пересаженного в печень мыши a b c Раковые ткани с флуоресцентными метками можно визуализировать с помощью флуоресцентного микроскопа. a, b: Изображения со встроенного оптического микроскопа Клеточные линии пересаженного рака толстой кишки имеют зеленую флуоресценцию. Изображение светового микроскопа d Изображение флуоресцентного 0 1. 0 микроскопа [UDP-Hex. NAc] app mol/ g tissue c: UDP-Glc. NAc накапливается в Зеленое: Опухоль e f опухолевой ткани. Принцип: Предыдущий метод: Иммуноокрашивание не позволяет отличить восстановленную и окисленную форму глутатиона. i. MScope: Распределение восстановленной и окисленной форм глутатиона можно визуализировать. 0 15 [GSH] app mol/ g tissue d: Пониженное содержание глутатиона Больше в области толстой кишки и меньше внутри опухоли. 0 10 [GSSG] app mol/ g tissue e: Окисленный глутатион 0 5 [GSH] app/[GSSG] app f: Мольное соотношение окисленной и восстановленной форм глутатиона. Отношение восстановленной формы глутатиона выше в опухолевой ткани. Масштаб: 0, 5 мм Пригоден для исследований рака (в том числе патологических) или при разработке и оценке противоопухолевых препаратов Kubo et al. , Anal. And Bioanal. Chem 2011 42

i. MScope TRIO Качественный и количественный анализ Новая функция i. MScope TRIO: Возможность ионизации электроспреем (ESI) в режиме работы ВЭЖХ-МС Подключение блока ESI Working: Door close DL ESI Visualizing ESI condition on PC ■ Переключение между режимами ESI и MALDI Увеличение чувствительности и точности структурного анализа за счет MСn (n≦ 10 ) и предварительной сепарации при помощи ВЭЖХ 43
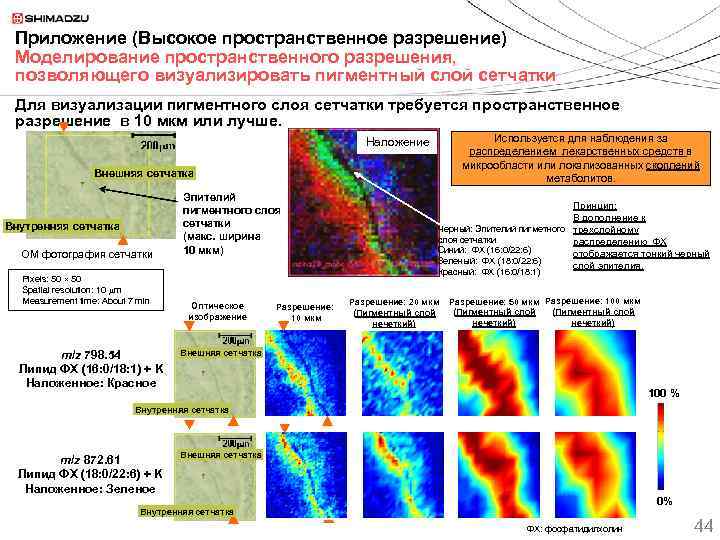
Приложение (Высокое пространственное разрешение) Моделирование пространственного разрешения, позволяющего визуализировать пигментный слой сетчатки Для визуализации пигментного слоя сетчатки требуется пространственное разрешение в 10 мкм или лучше. Используется для наблюдения за распределением лекарственных средств в микрообласти или локализованных скоплений метаболитов. Наложение Внешняя сетчатка Внутренняя сетчатка ОМ фотография сетчатки Pixels: 50 Spatial resolution: 10 m Measurement time: About 7 min m/z 798. 54 Липид ФХ (16: 0/18: 1) + K Наложенное: Красное Эпителий пигментного слоя сетчатки (макс. ширина 10 мкм) Принцип: В дополнение к Черный: Эпителий пигметного трехслойному слоя сетчатки распределению ФХ Синий: ФХ (16: 0/22: 6) отображается тонкий черный Зеленый: ФХ (18: 0/22: 6) слой эпителия. Красный: ФХ (16: 0/18: 1) Оптическое изображение Разрешение: 10 мкм Разрешение: 20 мкм (Пигментный слой нечеткий) Разрешение: 50 мкм Разрешение: 100 мкм (Пигментный слой нечеткий) Внешняя сетчатка 100 % Внутренняя сетчатка m/z 872. 61 Липид ФХ (18: 0/22: 6) + K Наложенное: Зеленое Внешняя сетчатка 0% Внутренняя сетчатка ФХ: фосфатидилхолин 44
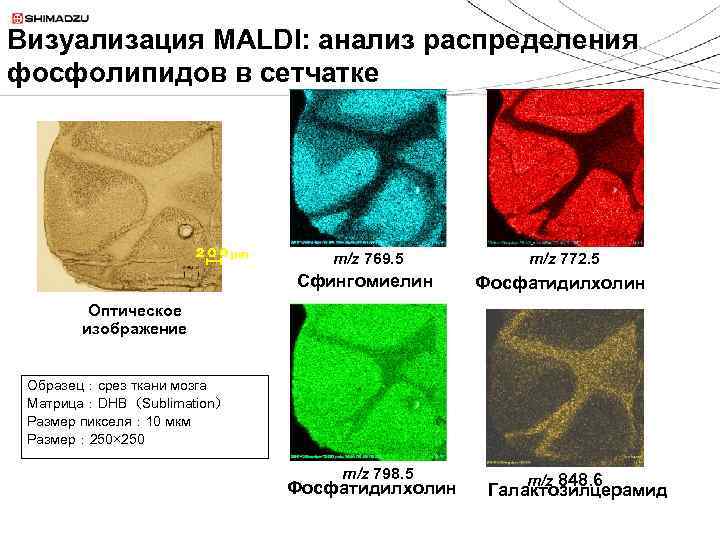
Визуализация MALDI: анализ распределения фосфолипидов в сетчатке 200μm m/z 769. 5 Сфингомиелин m/z 772. 5 Фосфатидилхолин Оптическое изображение Образец:срез ткани мозга Матрица:DHB(Sublimation) Размер пикселя: 10 мкм Размер: 250× 250 m/z 798. 5 Фосфатидилхолин m/z 848. 6 Галактозилцерамид
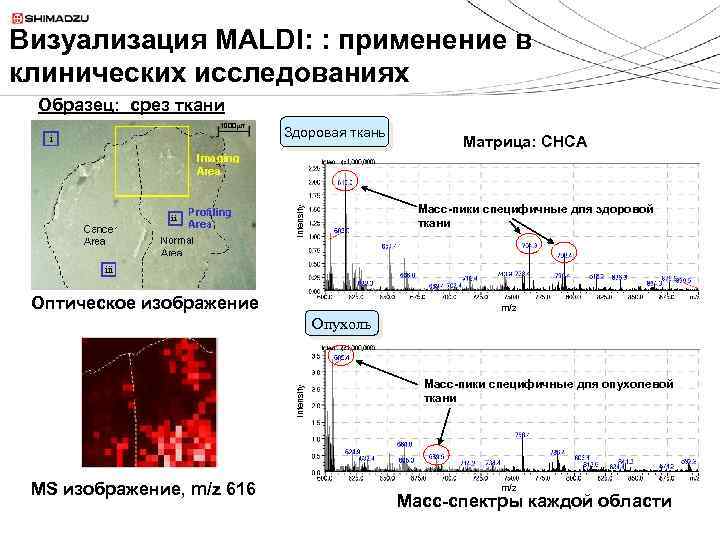
Визуализация MALDI: : применение в клинических исследованиях Образец: срез ткани Здоровая ткань Матрица: CHCA intensity Масс-пики специфичные для здоровой ткани Оптическое изображение m/z intensity Опухоль МS изображение, m/z 616 Масс-пики специфичные для опухолевой ткани m/z Масс-спектры каждой области
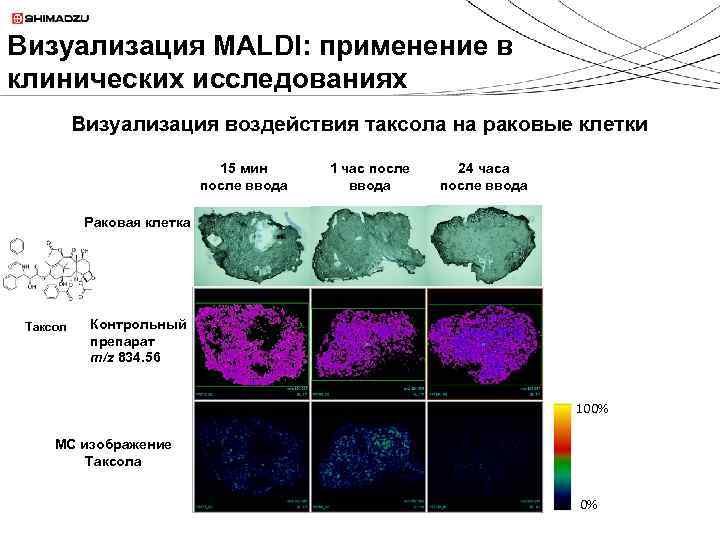
Визуализация MALDI: применение в клинических исследованиях Визуализация воздействия таксола на раковые клетки 15 мин после ввода 1 час после ввода 24 часа после ввода Раковая клетка Таксол Контрольный препарат m/z 834. 56 100% МС изображение Таксола 0%
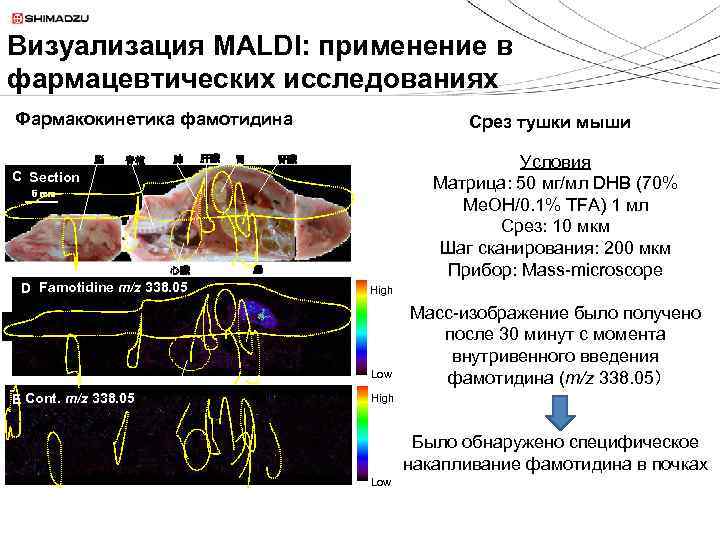
Визуализация MALDI: применение в фармацевтических исследованиях Фармакокинетика фамотидина 脳 脊椎 肺 肝臓 Срез тушки мыши Условия Матрица: 50 мг/мл DHB (70% Me. OH/0. 1% TFA) 1 мл Срез: 10 мкм Шаг сканирования: 200 мкм Прибор: Mass-microscope 腎臓 胃 C Section 5 mm 心臓 D Famotidine m/z 338. 05 腸 High Low E Cont. m/z 338. 05 Масс-изображение было получено после 30 минут с момента внутривенного введения фамотидина (m/z 338. 05) High Было обнаружено специфическое накапливание фамотидина в почках Low

Большое спасибо!
Исследование белков и пептидов методами масс-спектрометрии.pptx