06_Khemilyuminestsentsia_2-2011.ppt
- Количество слайдов: 40

Использование хемилюминесценции для решения медикобиологических задач Ю. А. Владимиров, А. Н. Осипов 2011
Методы изучения реакций с участием свободных радикалов Электронный парамагнитный резонанс (ЭПР) Прямое обнаружение радикалов Метод спиновых ловушек Хемилюминесценция Собственная Активированная

Свободные радикалы. Образование и метаболизм
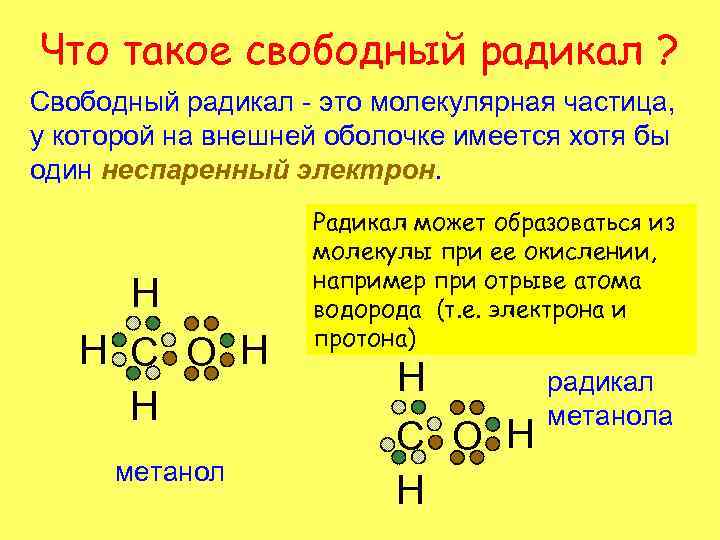
Что такое свободный радикал ? Свободный радикал - это молекулярная частица, у которой на внешней оболочке имеется хотя бы один неспаренный электрон. H H C O H H метанол Радикал может образоваться из молекулы при ее окислении, например при отрыве атома водорода (т. е. электрона и протона) H C O H H радикал метанола
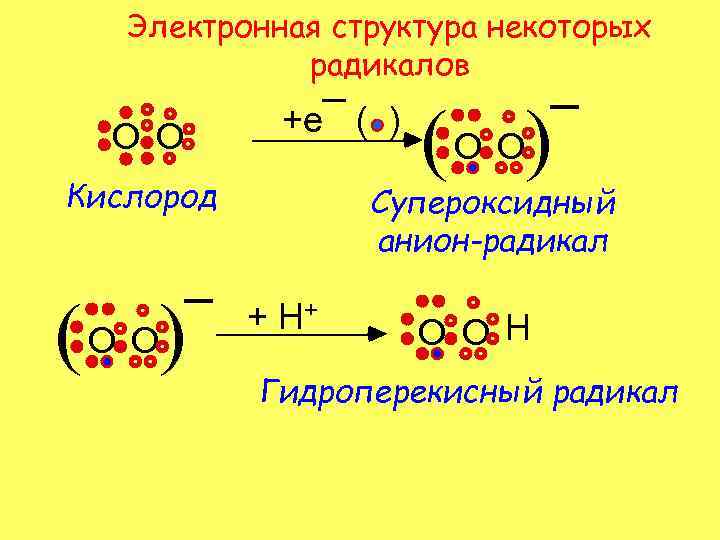
Электронная структура некоторых радикалов O O +e¯ ( ) Кислород ( ) ¯ O O ( ) O O ¯ Супероксидный анион-радикал + H+ O O H Гидроперекисный радикал

Химические реакции, ответственные за сверхслабое свечение животных тканей Реакции активных форм кислорода HOOH ·OO¯ ·OH 1 O 2 Пероксид водорода Супероксид-радикал Радикал гидроксила Синглетный кислород Активные формы кислорода (АФК) Свободнорадикальное окисление липидов LOOH Гидропероксид LOO· Диоксил-радикал LO· Алкоксил радикал Реакции активных фором азота. ·NO Нитроксид ONOO¯ Пероксинитрит Активные формы липидов АФ азота

Хемилюминесценция при образовании активных форм кислорода

Супероксидный радикал Основной источник супероксидных радикалов в нашем организме - клетки-фагоциты, к которым относятся гранулоциты и моноциты крови, и тканевые макрофаги. Фагоцит Встретив чужеродную частицу, например, бактерию, фагоцит прикрепляется к ней и начинает выделять активные формы кислорода, первая из которых супероксидный радикал. НАДФН + 2 О 2 НАДФ+ + 2( • О 2¯) Реакция катализируется ферментным комплексом —НАДФН оксидазой, который встроен в цитоплазматическую мембрану.

Метаболизм супероксидного радикала 1) 2 ·OO¯ H 2 O 2 + 3 O 2 (Супероксиддисмутаза) 2) 2 ·OO¯ H 2 O 2 + 1 O 2 (Спонтанно) 3) 1 O 3 O + фотон (1268 нм) 2 2 4) H 2 O 2 H 2 O + ½O 2 (Каталаза) 5) H 2 O 2 + Cl¯ H 2 O + Cl. O¯ (Миелопероксидаза) 6) H 2 O 2 + ·OO¯ + H+ H 2 O + ·OH + 1 O 2 (Реакция Габер-Вейса) 7) H 2 O 2 + Fe 2+ HO¯ + Fe 3+ + ·OH (Реакция Фентона) 8) Cl. O¯ + Fe 2+ Cl¯ + Fe 3+ + ·OH

Хемилюмнесценция при реакциях АФК H 2 O 2 + Cl. O¯ H 2 O + Cl¯ + 1 O 2 1 O 3 O + фотон (1268 нм) 2 2 A. U. Khan. Science 168, 476, 1970. M. Kasha and U. Khan. Ann. NY Acad, Sci. 171, 5, 1970. H 2 O 2 + ·OO¯ H 2 O + ·OH + 1 O 2 1 O 3 O + фотон (1268 нм) 2 2 A. U. Khan and M. Kasha. Singlet molecular oxygen in the Haber. Weiss reaction. Proc. Natl. Acad. Sci. U. S. A 91 (26): 12365 -12367, 1994. ·NO + ·OO¯ ONOO¯ (пероксинитрит) ONOO¯ NO¯ + 1 O 2 1 O 3 O + фотон (1268 нм) 2 2 A. U. Khan. J. Biolumin. Chemilumin. 10 (6): 329 -333, 1995.

Хемилюминесценция при образовании эксимеров кислорода H 2 O 2 + ·OO¯ H 2 O + ·OH + 1 O 2 1 O 3 O + фотон (1268 нм); 2 2 O 21 + 3 O 2 (O 2)2* 2 O 2 + фотон (480, 535 или 580 нм) J. Stauff et al. in Chemiluminescence and Bioluminescence (M. Cormier et al. , eds), 131 -140 Plenum, NY, 1973. HO ¯O C O + ·OH ·O C O + HOH ¯O 2(·CO 3¯) 2 CO 2 + 1 O 2 свечение Гипотетическая схема

Хемилюминесценция при перекисном окислении липидов
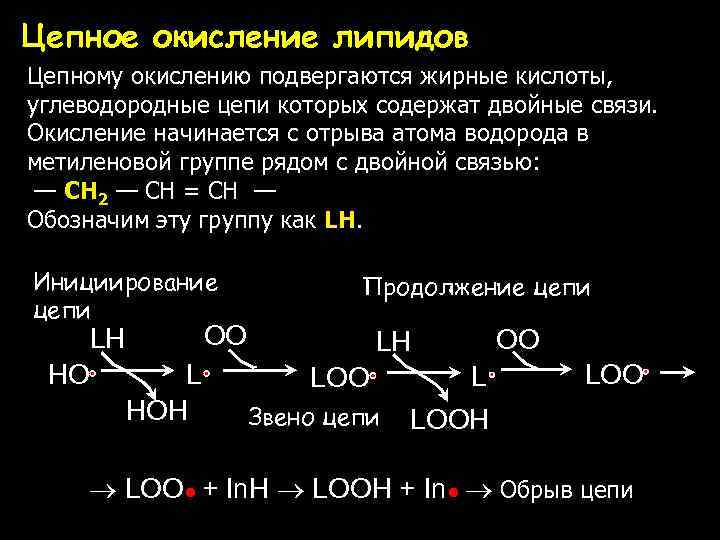
Цепное окисление липидов Цепному окислению подвергаются жирные кислоты, углеводородные цепи которых содержат двойные связи. Окисление начинается с отрыва атома водорода в метиленовой группе рядом с двойной связью: — CH 2 — CH = CH — Обозначим эту группу как LH. Инициирование цепи OO LH HO Продолжение цепи L HOH OO LH LOO Звено цепи L LOOH LOO● + In. H LOOH + In● Обрыв цепи
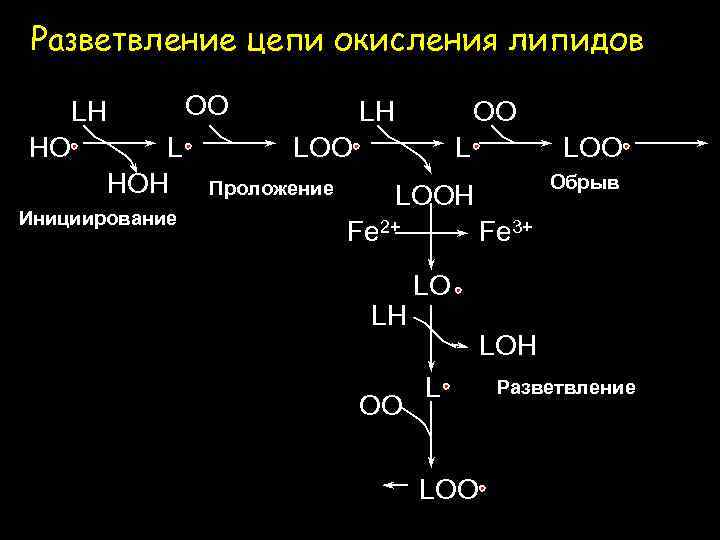
Разветвление цепи окисления липидов OO LH HO L HOH Инициирование LH OO LOO Проложение L LOOH Обрыв Fe 2+ LH OO Fe 3+ LO LOH L LOO Разветвление
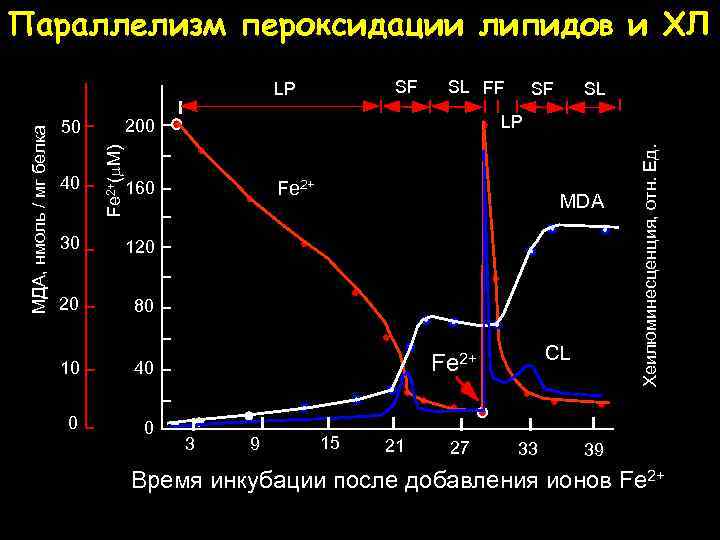
Параллелизм пероксидации липидов и ХЛ SF Fe 2+ MDA 120 20 SL LP 160 30 SF 80 10 40 0 0 CL Fe 2+ 3 9 15 21 27 33 Хеилюминесценция, отн. Ед. 40 SL FF 200 50 Fe 2+(m. M) МДА, нмоль / мг белка LP 39 Время инкубации после добавления ионов Fe 2+
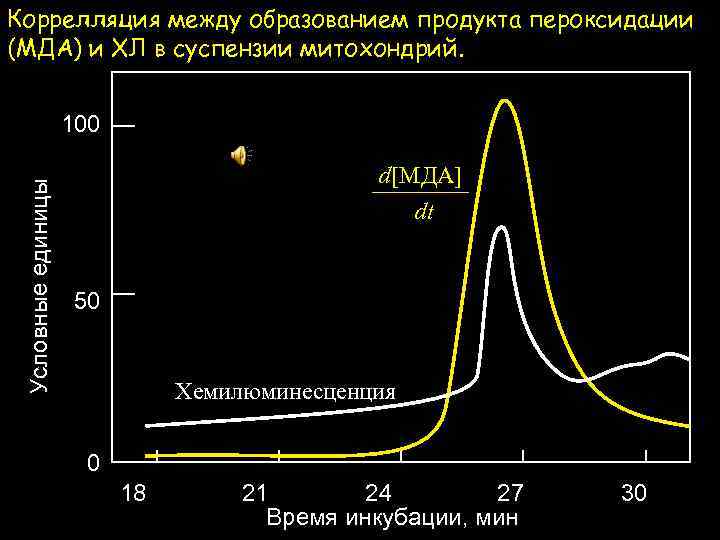
Коррелляция между образованием продукта пероксидации (МДА) и ХЛ в суспензии митохондрий. Условные единицы 100 d[МДА] dt 50 Хемилюминесценция 0 18 21 24 27 Время инкубации, мин 30
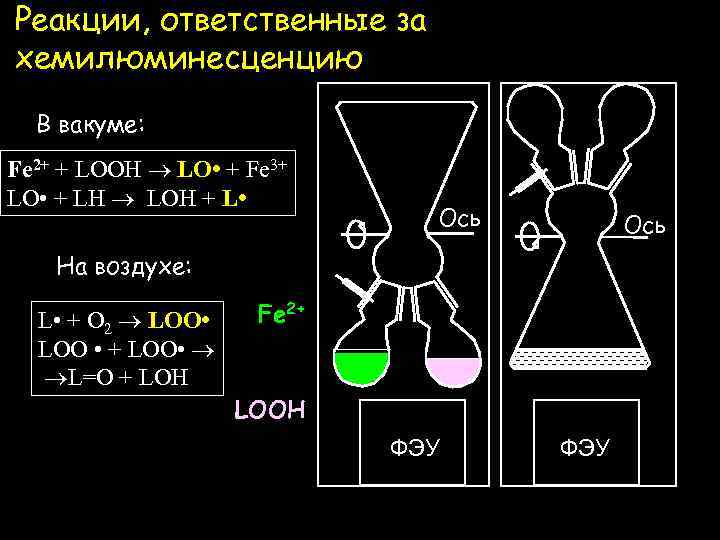
Реакции, ответственные за хемилюминесценцию В вакуме: Fe 2+ + LOOH LO • + Fe 3+ LO • + LH LOH + L • Ось На воздухе: L • + O 2 LOO • + LOO • L=O + LOH Fe 2+ LOOH PM ФЭУ
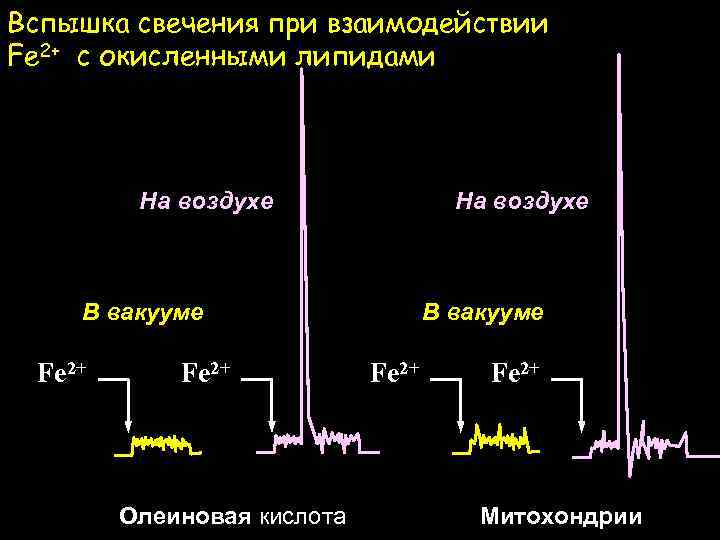
Вспышка свечения при взаимодействии Fe 2+ с окисленными липидами На воздухе В вакууме Fe 2+ Олеиновая кислота В вакууме Fe 2+ Митохондрии

Измерение ХЛ – прямой метод определения радикалов LOO· в биохимических системах LOO· + LOO· LOH + L=O* + 1 O 2 L=O* L=O + фотон 1 O 3 O + фотон 2 2 Недостатки ХЛ метода: 1. Свечение очень слабое. 2. Свечение неспецифическое. В результате: Неизвестно, измеряем ли мы нужные нам процессы или же побочные реакции.

Активированная ХЛ (CL enhancers)

Два типа активаторов ХЛ Химические активаторы Вступают в химическую реакцию с образованием продуктов в эектронно-возбужденном состоянии. Физические активаторы Не вступают в химические реакции, но увеличивают квантовый выход испускания фотона.

1. Химические активаторы (Probes)
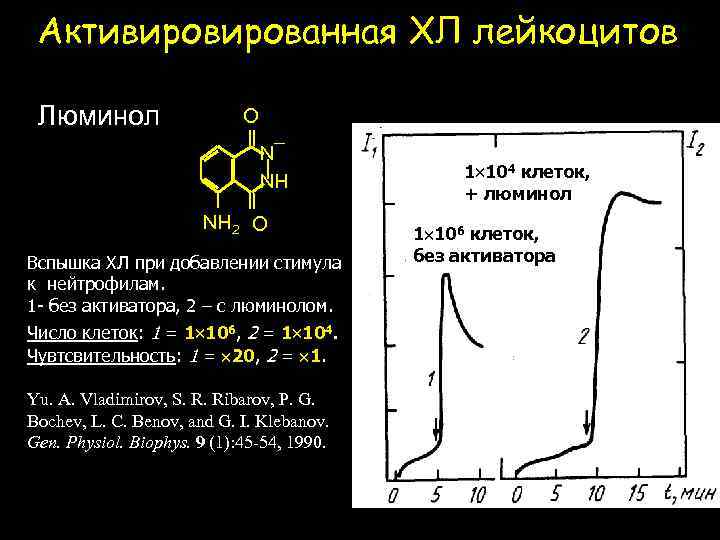
Активированная ХЛ лейкоцитов Люминол O N¯ NH NH 2 O Вспышка ХЛ при добавлении стимула к нейтрофилам. 1 - без активатора, 2 – с люминолом. Число клеток: 1 = 1 106, 2 = 1 104. Чувтсвительность: 1 = 20, 2 = 1. Yu. A. Vladimirov, S. R. Ribarov, P. G. Bochev, L. C. Benov, and G. I. Klebanov. Gen. Physiol. Biophys. 9 (1): 45 -54, 1990. 1 104 клеток, + люминол 1 106 клеток, без активатора
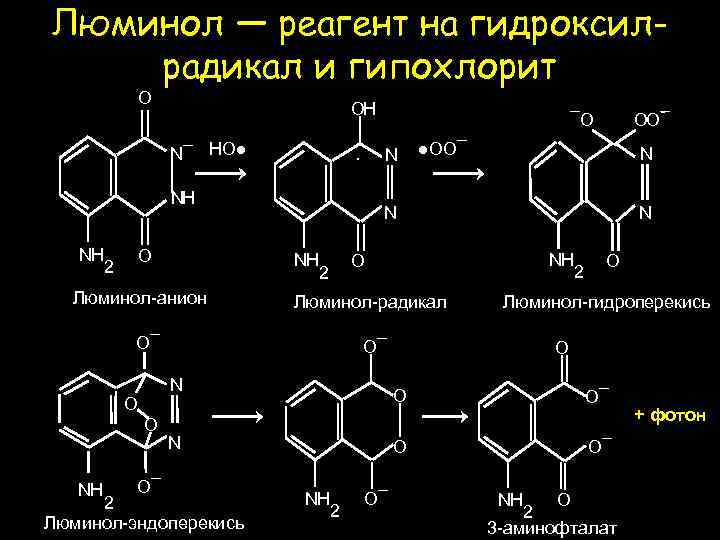
Люминол — реагент на гидроксилрадикал и гипохлорит O OH N¯ HO● N · NH NH O 2 NH O¯ N NH Люминол-радикал O O O NH 2 O¯ O¯ O N 2 Люминол-эндоперекись 2 Люминол-гидроперекись O¯ N O 2 O¯ O ●OO¯ N NH Люминол-анион OO¯ ¯O O¯ NH O 2 3 -аминофталат + фотон
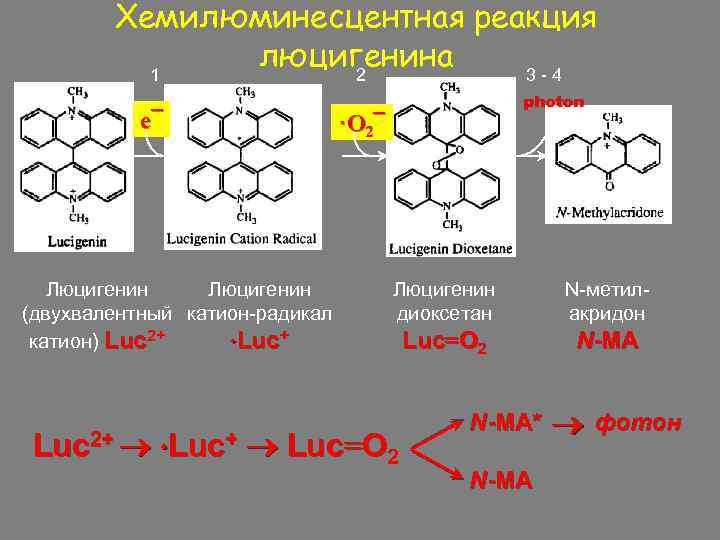
Хемилюминесцентная реакция люцигенина 1 2 3 -4 e¯ eЇ 1 Люцигенин (двухвалентный катион-радикал катион) Luc 2+ Luc+ photon ·O 2¯ Люцигенин диоксетан N-метилакридон Luc=O 2 N-MA Luc 2+ Luc=O 2 N-MA* N-MA фотон

Механизм люцигенин-зависимой ХЛ (Люц-ХЛ) Катион-радикал люцигенина ∙Luc¯ дает свечение в результате взаимодействия с супероксидом ∙O 2¯ Luc 2+ + e¯ ∙Luc¯ O 2 + e¯ ∙O 2¯ ∙Luc¯ + ∙O 2¯ Luc-O 2 (диоксетан) Luc-O 2 2 MA (метилакридон) + hn (1) (2) (3) (4)
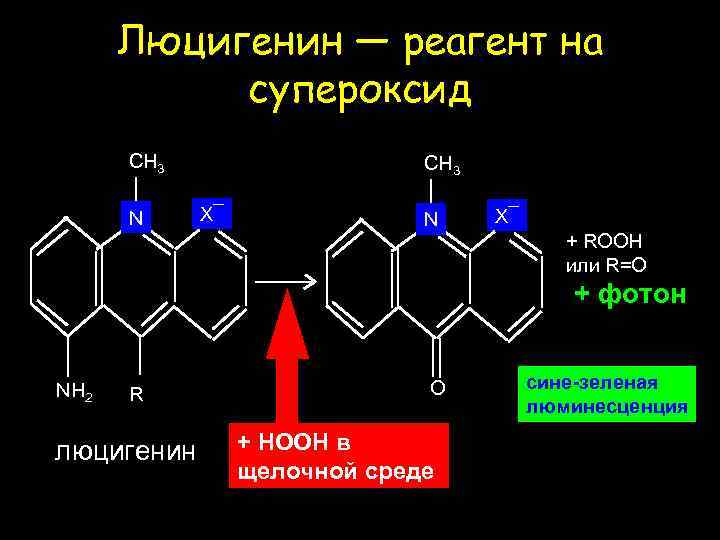
Люцигенин — реагент на супероксид CH 3 N CH 3 X¯ N X¯ + ROOH или R=O + фотон NH 2 R люцигенин O + HOOH в щелочной среде сине-зеленая люминесценция
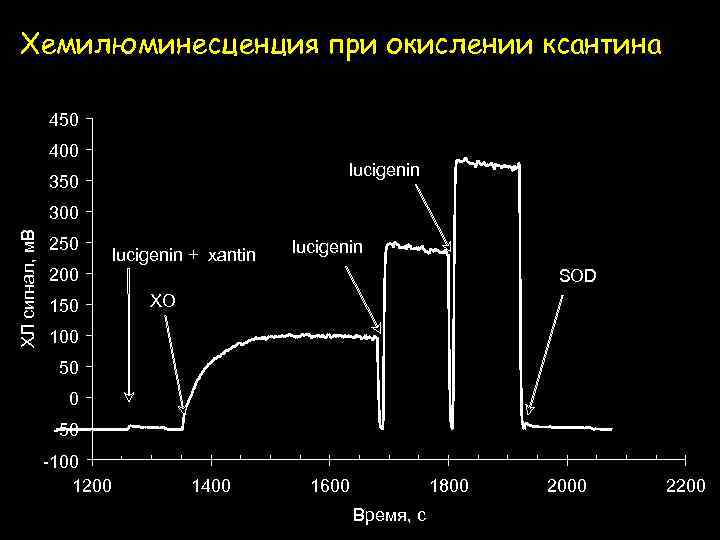
Хемилюминесценция при окислении ксантина 450 400 lucigenin 350 ХЛ сигнал, м. В 300 250 200 lucigenin + xantin 150 lucigenin SOD XO 100 50 0 -50 -100 1200 1400 1600 1800 Время, с 2000 2200
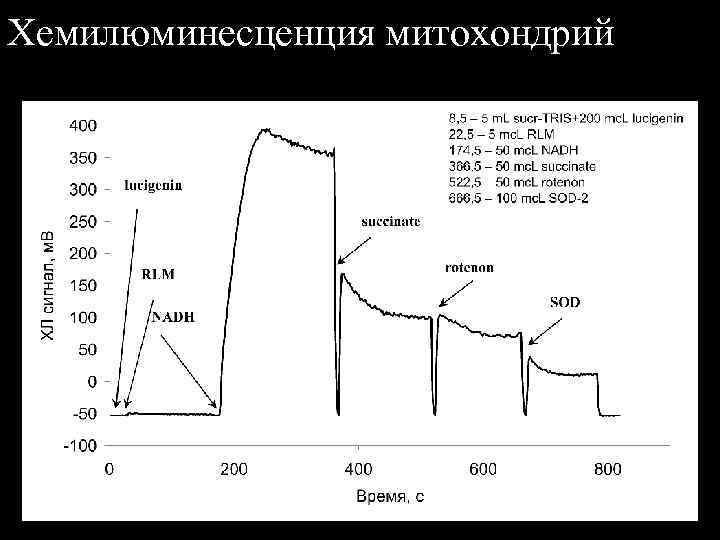
Хемилюминесценция митохондрий

2. Физические активаторы (Sensitizers)
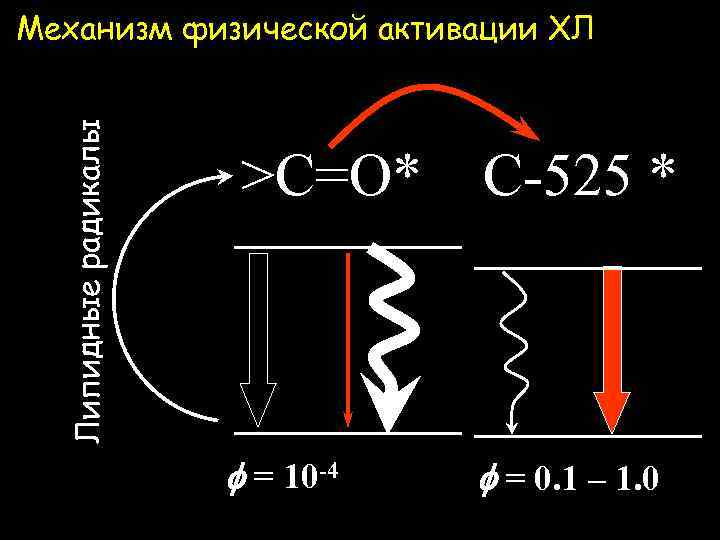
Липидные радикалы Механизм физической активации ХЛ >C=O* f = 10 -4 C-525 * f = 0. 1 – 1. 0

Квантовый выход ХЛ ( ХЛ): Многие химические реакции сопровождаются очень слабым свечением. Почему оно слабое? 10– 8 10– 4
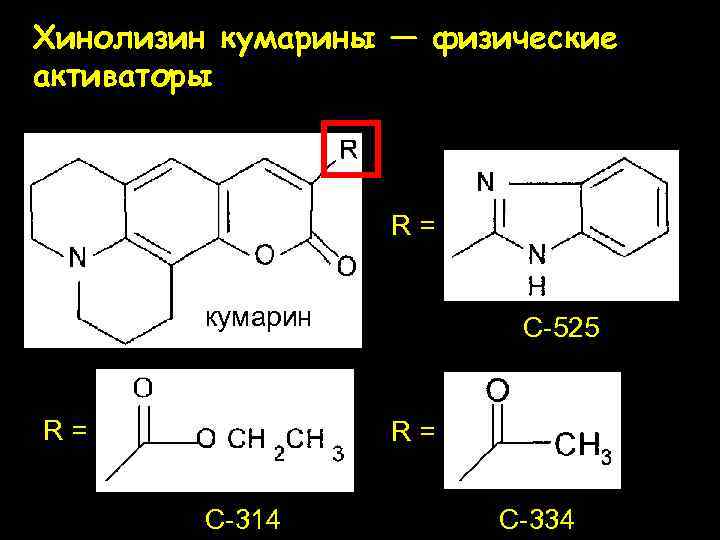
Хинолизин кумарины — физические активаторы R= кумарин R= C-525 R= C-314 C-334
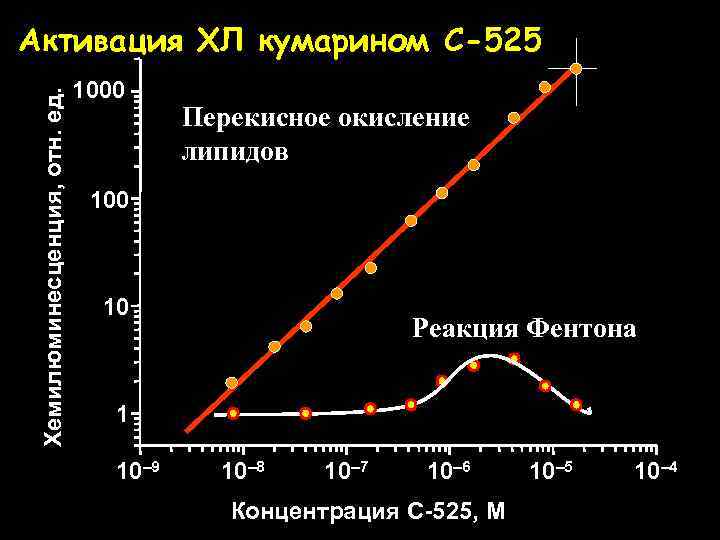
Хемилюминесценция, отн. ед. Активация ХЛ кумарином C-525 1000 Перекисное окисление липидов 100 10 Реакция Фентона 1 10– 9 10– 8 10– 7 10– 6 Концентрация C-525, M 10– 5 10– 4
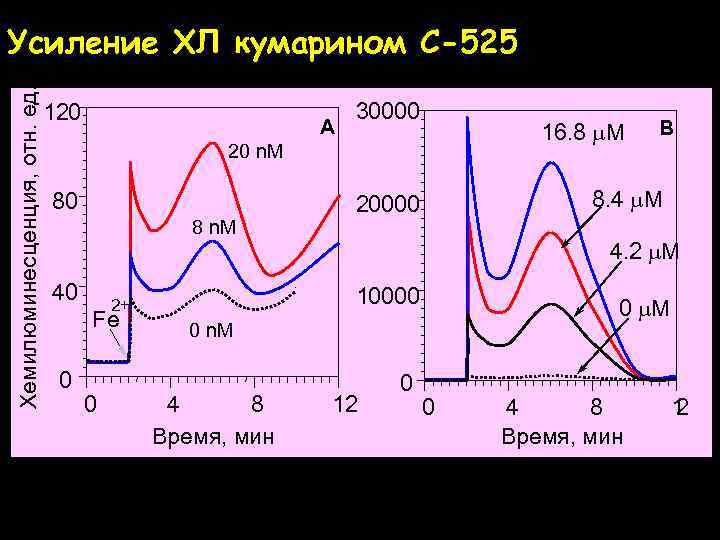
Хемилюминесценция, отн. ед. Усиление ХЛ кумарином C-525 120 A 30000 16. 8 m. M 20 n. M 80 8 n. M 40 Fe 0 0 8. 4 m. M 20000 4. 2 m. M 10000 2+ 0 m. M 0 n. M 4 8 Время, мин B 12 0 0 4 8 Время, мин 1 2

Антиоксидантная активность
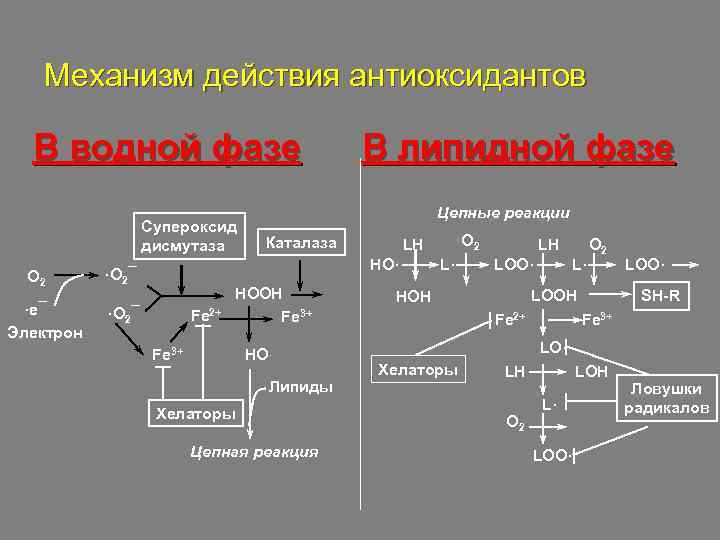
Механизм действия антиоксидантов В водной фазе Супероксид дисмутаза O 2 ·e¯ Электрон В липидной фазе Цепные реакции Каталаза HO· ·O 2¯ Fe 2+ HOOH Fe 3+ HO. Липиды Хелаторы Цепная реакция O 2 LH L· LH LOO· L· O 2 SH-R LOOH HOH Fe 2+ LOO· Fe 3+ LO· Хелаторы LOH LH O 2 L· LOO· Ловушки радикалов

Определение АОА по кинетике Fe 2+- ХЛ мотор А мешалка кювета Интенсивность ХЛ термостат светозащитный кожух шторка ФЭУ 4 Б 0 3 t 5 Fe 2+ 2 a A 1 0 2 4 6 8 10 Время (мин) 10 12 14
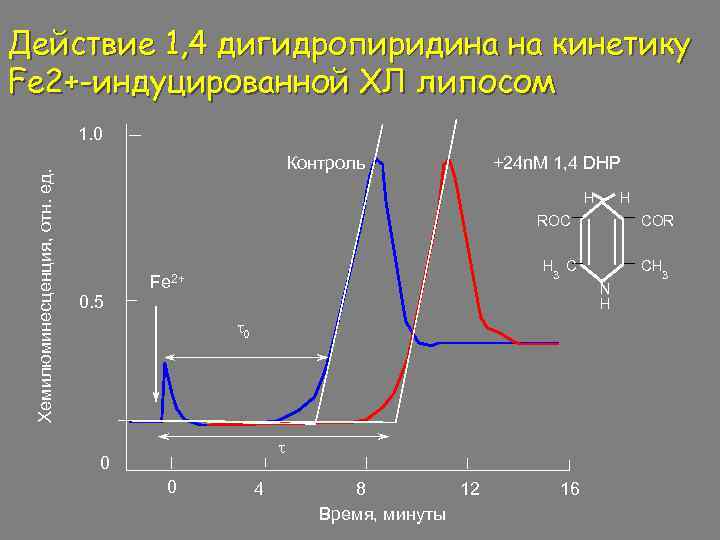
Действие 1, 4 дигидропиридина на кинетику Fe 2+-индуцированной ХЛ липосом Хемилюминесценция, отн. ед. 1. 0 Контроль +24 n. M 1, 4 DHP H H ROC 0. 5 H 3 C Fe 2+ t 0 0 4 8 12 Время, минуты 16 COR N H CH 3
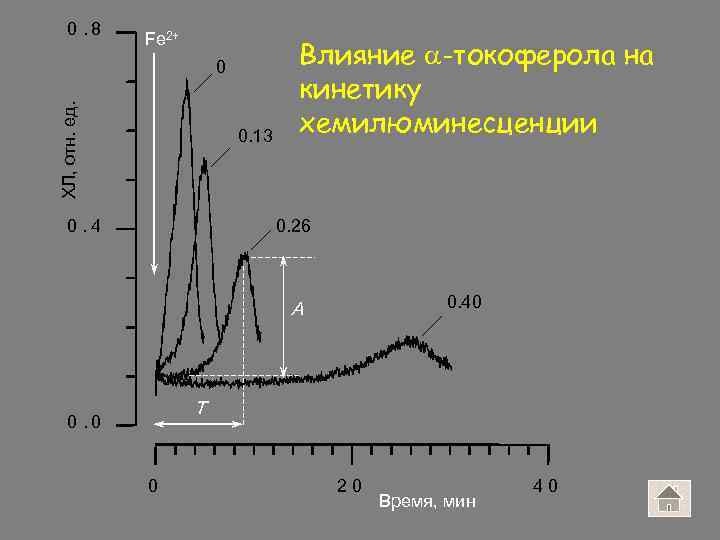
0. 8 Fe 2+ ХЛ, отн. ед. 0 0. 13 0. 4 Влияние -токоферола на кинетику хемилюминесценции 0. 26 0. 40 A T 0. 0 0 20 Время, мин 40
06_Khemilyuminestsentsia_2-2011.ppt