Методы микр. набл.почв.ppt
- Количество слайдов: 14
 Использование различных видов микроскопов в исследовании почвенных микроорганизмов Электронные микроскопы Трансмиссионный Сканирующий (просвечивающий) (растровый)
Использование различных видов микроскопов в исследовании почвенных микроорганизмов Электронные микроскопы Трансмиссионный Сканирующий (просвечивающий) (растровый)
 В трансмиссионном (ТЭМ) микроскопе исследуемый объект просвечивается пучком электронов, создающим затем на экране или фотопластинке соответствующее изображение В сканирующием (СЭМ)микроскопе изображение создается вторичными электронами, испускаемыми исследуемой поверхностью при облучении ее пучком первичных электронов. Электронные микроскопы просвечивающего типа (трансмиссионные) отличаются более высокой разрешающей способностью, однако они пригодны только для изучения очень тонких образцов (с толщиной, не превышающей 5 Х 10 -2 мкм). Поэтому в микробиологии и почвоведении все более широкое применение находит растровая (сканирующая) электронная микроскопия, позволяющая исследовать массивные непрозрачные объекты произвольной геометрии.
В трансмиссионном (ТЭМ) микроскопе исследуемый объект просвечивается пучком электронов, создающим затем на экране или фотопластинке соответствующее изображение В сканирующием (СЭМ)микроскопе изображение создается вторичными электронами, испускаемыми исследуемой поверхностью при облучении ее пучком первичных электронов. Электронные микроскопы просвечивающего типа (трансмиссионные) отличаются более высокой разрешающей способностью, однако они пригодны только для изучения очень тонких образцов (с толщиной, не превышающей 5 Х 10 -2 мкм). Поэтому в микробиологии и почвоведении все более широкое применение находит растровая (сканирующая) электронная микроскопия, позволяющая исследовать массивные непрозрачные объекты произвольной геометрии.
 Подготовка препаратов для электронной микроскопии 1. Для микроскопов просвечивающего типа (трансмиссионных) Подложка препаратов должна быть очень тонкой (10— 15 мкм) и проницаемой для электронов. Такие пленки изготовляют из коллодия, формвара, угля и кварца и помещают на металлические сетки, диаметр предметных сеток равен 2—З мм. На пленки наносят суспензию микроорганизмов и после испарения воды препарат просматривают. Часто препарат подвергают дополнительной обработке — оттенению металлом (золотом, платиной, палладием, хромом или ураном). Напыление металлом производят под вакуумом на специальном приборе — напылителе. Такая дополнительная обработка повышает контрастность изображения. При микроскопировании почвенной суспензии ее очищают от растворимых веществ путем диализа.
Подготовка препаратов для электронной микроскопии 1. Для микроскопов просвечивающего типа (трансмиссионных) Подложка препаратов должна быть очень тонкой (10— 15 мкм) и проницаемой для электронов. Такие пленки изготовляют из коллодия, формвара, угля и кварца и помещают на металлические сетки, диаметр предметных сеток равен 2—З мм. На пленки наносят суспензию микроорганизмов и после испарения воды препарат просматривают. Часто препарат подвергают дополнительной обработке — оттенению металлом (золотом, платиной, палладием, хромом или ураном). Напыление металлом производят под вакуумом на специальном приборе — напылителе. Такая дополнительная обработка повышает контрастность изображения. При микроскопировании почвенной суспензии ее очищают от растворимых веществ путем диализа.
 2. Для микроскопов растрового типа (сканирующего) Препарирование образцов для растрового электронного микроскопа включает ряд операций, в том числе дегидратацию и высушивание образцов без нарушения их морфологической структуры и напыление их поверхности тяжелыми металлами. Исследуют образцы, не превышающие 10 мм в диаметре, поверхность образца не должна иметь больших неровностей, так как наличие неровностей сказывается на фокусе изображения и препятствует равномерному напылению образца металлом. Высушенные образцы наклеиваются на металлические столбики и после напыления металлом просматриваются под микроскопом.
2. Для микроскопов растрового типа (сканирующего) Препарирование образцов для растрового электронного микроскопа включает ряд операций, в том числе дегидратацию и высушивание образцов без нарушения их морфологической структуры и напыление их поверхности тяжелыми металлами. Исследуют образцы, не превышающие 10 мм в диаметре, поверхность образца не должна иметь больших неровностей, так как наличие неровностей сказывается на фокусе изображения и препятствует равномерному напылению образца металлом. Высушенные образцы наклеиваются на металлические столбики и после напыления металлом просматриваются под микроскопом.
 Люминесцентный микроскоп
Люминесцентный микроскоп
 Особенности люминесцентной микроскопии Люминесцентная микроскопия основана на способности многих веществ биологического происхождения и красителей светиться под воздействием попадающего на них света. Молекулы веществ, способных к люминесценции, поглощают энергию попадающего на них света и переходят в возбужденное состояние, которое характеризуется более высоким энергетическим уровнем. При переходе к исходному энергетическому уровню происходит отдача молекулами избытка энергии в виде света – люминесценции. Для возбуждения люминесценции объект освещают ультрафиолетовыми лучами с длиной волны 300 -400 нм или синефиолетовыми лучами с длиной волны 400 -460 нм. Клетки большинства микроорганизмов флюоресцируют очень слабо, поэтому их обрабатывают специальными красителями – флюорохромами, обладающими люминесценцией.
Особенности люминесцентной микроскопии Люминесцентная микроскопия основана на способности многих веществ биологического происхождения и красителей светиться под воздействием попадающего на них света. Молекулы веществ, способных к люминесценции, поглощают энергию попадающего на них света и переходят в возбужденное состояние, которое характеризуется более высоким энергетическим уровнем. При переходе к исходному энергетическому уровню происходит отдача молекулами избытка энергии в виде света – люминесценции. Для возбуждения люминесценции объект освещают ультрафиолетовыми лучами с длиной волны 300 -400 нм или синефиолетовыми лучами с длиной волны 400 -460 нм. Клетки большинства микроорганизмов флюоресцируют очень слабо, поэтому их обрабатывают специальными красителями – флюорохромами, обладающими люминесценцией.
 Люминесцентная микроскопия увеличивает контрастность изображения, дает возможность различать отдельные клеточные структуры и даже отметить их изменения при различных функциональных состояниях клетки. Применяется для цитологических исследований, выявления живых и мертвых клеток, для изучения микроорганизмов в почве, илах, ризосфере растений.
Люминесцентная микроскопия увеличивает контрастность изображения, дает возможность различать отдельные клеточные структуры и даже отметить их изменения при различных функциональных состояниях клетки. Применяется для цитологических исследований, выявления живых и мертвых клеток, для изучения микроорганизмов в почве, илах, ризосфере растений.
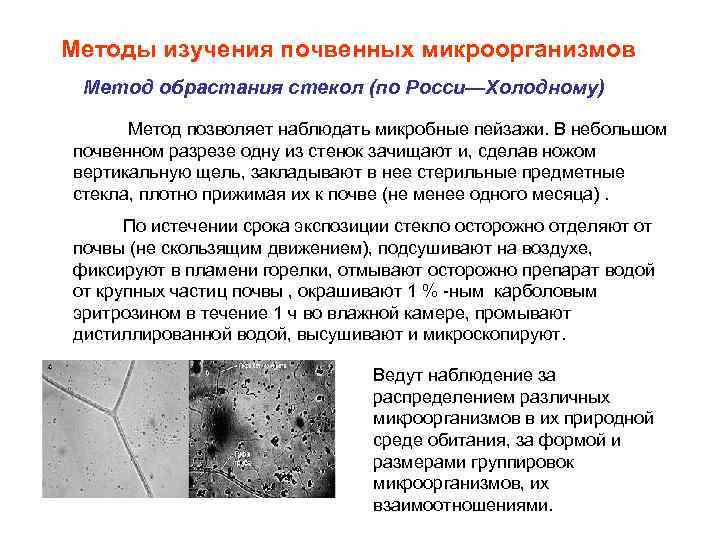 Методы изучения почвенных микроорганизмов Метод обрастания стекол (по Росси—Холодному) Метод позволяет наблюдать микробные пейзажи. В небольшом почвенном разрезе одну из стенок зачищают и, сделав ножом вертикальную щель, закладывают в нее стерильные предметные стекла, плотно прижимая их к почве (не менее одного месяца). По истечении срока экспозиции стекло осторожно отделяют от почвы (не скользящим движением), подсушивают на воздухе, фиксируют в пламени горелки, отмывают осторожно препарат водой от крупных частиц почвы , окрашивают 1 % -ным карболовым эритрозином в течение 1 ч во влажной камере, промывают дистиллированной водой, высушивают и микроскопируют. Ведут наблюдение за распределением различных микроорганизмов в их природной среде обитания, за формой и размерами группировок микроорганизмов, их взаимоотношениями.
Методы изучения почвенных микроорганизмов Метод обрастания стекол (по Росси—Холодному) Метод позволяет наблюдать микробные пейзажи. В небольшом почвенном разрезе одну из стенок зачищают и, сделав ножом вертикальную щель, закладывают в нее стерильные предметные стекла, плотно прижимая их к почве (не менее одного месяца). По истечении срока экспозиции стекло осторожно отделяют от почвы (не скользящим движением), подсушивают на воздухе, фиксируют в пламени горелки, отмывают осторожно препарат водой от крупных частиц почвы , окрашивают 1 % -ным карболовым эритрозином в течение 1 ч во влажной камере, промывают дистиллированной водой, высушивают и микроскопируют. Ведут наблюдение за распределением различных микроорганизмов в их природной среде обитания, за формой и размерами группировок микроорганизмов, их взаимоотношениями.
 Метод капиллярных педоскопов Б. В. Перфильев и Д. Р. Габе предложили использовать для наблюдения за жизнью микроорганизмов плоские капилляры с плоскопараллельными стенками. Был сконструирован специальный прибор — педоскоп, состоящий из набора таких капилляров. Стерильные педоскопы вставляют в почву с помощью специального пробойника так, чтобы каналы ячеек приняли вертикальное положение (направление движения почвенного раствора). Экспозиция педоскопов в почве – 1 месяц. Педоскопы вынимают из почвы, очищают снаружи от почвенных частичек, рассматривают под микроскопом с иммерсионным объективом. Микробные клетки в педоскопах могут быть зафиксированы (в парах осмиевой кислоты или в парах 40%-ного раствора формалина) и окрашены (1%-ным раствором карболового эритрозина).
Метод капиллярных педоскопов Б. В. Перфильев и Д. Р. Габе предложили использовать для наблюдения за жизнью микроорганизмов плоские капилляры с плоскопараллельными стенками. Был сконструирован специальный прибор — педоскоп, состоящий из набора таких капилляров. Стерильные педоскопы вставляют в почву с помощью специального пробойника так, чтобы каналы ячеек приняли вертикальное положение (направление движения почвенного раствора). Экспозиция педоскопов в почве – 1 месяц. Педоскопы вынимают из почвы, очищают снаружи от почвенных частичек, рассматривают под микроскопом с иммерсионным объективом. Микробные клетки в педоскопах могут быть зафиксированы (в парах осмиевой кислоты или в парах 40%-ного раствора формалина) и окрашены (1%-ным раствором карболового эритрозина).
 Метод люминесцентно-микроскопического наблюдения микроорганизмов в почвенных монолитах по Звягинцеву Цилиндрическую формочку (диаметр и высота по 1 см) из нержавеющей стали, пластмассы или стекла, имеющую острые края, вдавливают в почву исследуемого горизонта и осторожно вынимают ее так, чтобы над краями формочки возвышался слой почвы. Острой бритвой срезают почву, чтобы верхняя грань монолита была на уровне краев формочки. На поверхность почвы капают водный раствор акридинового оранжевого (1: 1000) и накрывают ее очень тонким покровным стеклом (0, 10— 0, 12 мм). Через 10— 20 мин исследуют в люминесцентном микроскопе с иммерсионным объективом (90 х) в отраженном свете. Основные трудности метода заключаются в подборе подходящей концентрации красителя; для каждой почвы она подбирается опытным путем.
Метод люминесцентно-микроскопического наблюдения микроорганизмов в почвенных монолитах по Звягинцеву Цилиндрическую формочку (диаметр и высота по 1 см) из нержавеющей стали, пластмассы или стекла, имеющую острые края, вдавливают в почву исследуемого горизонта и осторожно вынимают ее так, чтобы над краями формочки возвышался слой почвы. Острой бритвой срезают почву, чтобы верхняя грань монолита была на уровне краев формочки. На поверхность почвы капают водный раствор акридинового оранжевого (1: 1000) и накрывают ее очень тонким покровным стеклом (0, 10— 0, 12 мм). Через 10— 20 мин исследуют в люминесцентном микроскопе с иммерсионным объективом (90 х) в отраженном свете. Основные трудности метода заключаются в подборе подходящей концентрации красителя; для каждой почвы она подбирается опытным путем.
 Методы изучения микробных сукцессий в почве Для характеристики сукцессии применяют в совокупности метод посева и прямой метод и вычисляют коэффициент К (Звягинцев, 1987). Коэффициент К рассчитывают по формуле: К=М/П где М — численность бактерий, учитываемых прямым методом, П — бактерии, учтенные на определенной питательной среде, например МПА. Анализ соотношения данных микроскопии и посева на МПА (коэффициент К) позволяет предположить, что для сукцессии микроорганизмов в почве, инициируемой внесением одного легкодоступного субстрата (например, глюкозы), посев на МПА дает сведения о большей части микроорганизмов, способных к быстрому росту, так называемых r-стратегов. Для зрелых сообществ коэффициент К будет возрастать, а для молодых — уменьшаться.
Методы изучения микробных сукцессий в почве Для характеристики сукцессии применяют в совокупности метод посева и прямой метод и вычисляют коэффициент К (Звягинцев, 1987). Коэффициент К рассчитывают по формуле: К=М/П где М — численность бактерий, учитываемых прямым методом, П — бактерии, учтенные на определенной питательной среде, например МПА. Анализ соотношения данных микроскопии и посева на МПА (коэффициент К) позволяет предположить, что для сукцессии микроорганизмов в почве, инициируемой внесением одного легкодоступного субстрата (например, глюкозы), посев на МПА дает сведения о большей части микроорганизмов, способных к быстрому росту, так называемых r-стратегов. Для зрелых сообществ коэффициент К будет возрастать, а для молодых — уменьшаться.
 Методы исследования микроорганизмов в ризосфере Микроорганизмы в ризосфере исследуют методом последовательных отмываний корней по Теппер. Из почвенных монолитов с растениями стерильным пинцетом отбирают 1 г молодых корней (примерно одного диаметра) с приставшими к ним частицами почвы. Корни помещают в колбу со 100 мл стерильной водопроводной воды и взбалтывают в течение 2 мин. Стерильным пинцетом корни извлекают из колбы и переносят последовательно во вторую, третью, четвертую, пятую, шестую и седьмую колбы, также содержащие по 100 мл стерильной водопроводной воды. В каждой колбе корни отмывают по 2 мин. Из каждой колбы берут по капле отмывной воды и высевают на поверхность питательной среды (МПА или др. ) на чашки Петри. Чашки инкубируют в термостате при 28— 30°С. Учет посевов производится на 3— 7 -е сутки роста микроорганизмов.
Методы исследования микроорганизмов в ризосфере Микроорганизмы в ризосфере исследуют методом последовательных отмываний корней по Теппер. Из почвенных монолитов с растениями стерильным пинцетом отбирают 1 г молодых корней (примерно одного диаметра) с приставшими к ним частицами почвы. Корни помещают в колбу со 100 мл стерильной водопроводной воды и взбалтывают в течение 2 мин. Стерильным пинцетом корни извлекают из колбы и переносят последовательно во вторую, третью, четвертую, пятую, шестую и седьмую колбы, также содержащие по 100 мл стерильной водопроводной воды. В каждой колбе корни отмывают по 2 мин. Из каждой колбы берут по капле отмывной воды и высевают на поверхность питательной среды (МПА или др. ) на чашки Петри. Чашки инкубируют в термостате при 28— 30°С. Учет посевов производится на 3— 7 -е сутки роста микроорганизмов.
 Методы исследования биологической активности почв К методам изучения биологической активности почв относят: - микробиологические (прямой микробиологический подсчет микроорганизмов разных групп — бактерий, актиномицетов, грибов — и определение количества микроорганизмов на разных питательных средах), - биохимические (определение ферментативной активности почв, АТФ, ДНК), - физиологические (физиологический метод определения биомассы микроорганизмов, определение дыхания почв) - химические (определение нитратов, аммиака).
Методы исследования биологической активности почв К методам изучения биологической активности почв относят: - микробиологические (прямой микробиологический подсчет микроорганизмов разных групп — бактерий, актиномицетов, грибов — и определение количества микроорганизмов на разных питательных средах), - биохимические (определение ферментативной активности почв, АТФ, ДНК), - физиологические (физиологический метод определения биомассы микроорганизмов, определение дыхания почв) - химические (определение нитратов, аммиака).
 Методы делят на две группы: - методы определения действительной, актуальной природной биологической активности почвы (полевые методы определения дыхания, азотфиксации, денитрификации, некоторые изотопные методы); - методы определения потенциальной биологической активности почв, т. е. той активности, которая обнаруживается в лаборатории при оптимальных условиях для протекания данного процесса (определение ферментативной активности почв, лабораторные методы определения нитрификации, азотфиксации, денитрификации, дыхания). Ко второй группе методов относятся и определение численности микроорганизмов прямыми методами или посевом на питательные среды.
Методы делят на две группы: - методы определения действительной, актуальной природной биологической активности почвы (полевые методы определения дыхания, азотфиксации, денитрификации, некоторые изотопные методы); - методы определения потенциальной биологической активности почв, т. е. той активности, которая обнаруживается в лаборатории при оптимальных условиях для протекания данного процесса (определение ферментативной активности почв, лабораторные методы определения нитрификации, азотфиксации, денитрификации, дыхания). Ко второй группе методов относятся и определение численности микроорганизмов прямыми методами или посевом на питательные среды.


